第一章第一节原子结构(用)
第1章第1节 原子结构(第2课时 电子云与原子轨道 泡利原理 洪特规则 能量最低原理)(学生版)

《2021-2022学年高二化学同步精品学案(新人教版选择性必修2)》第一章原子结构与性质第一节原子结构第2课时电子云与原子轨道泡利原理、洪特规则、能量最低原理四.电子云与原子轨道由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称为电子云。
,注:(1)同一能层中,p能级的原子轨道空间伸展方向不同但原子轨道的能量相同;(2)人们把同一能级的几个能量相同的原子轨道称为简并轨道。
【思考讨论】分析同一原子的s电子的电子云轮廓图,请解释为什么同一原子的能层越高,s电子云半径越大?同一原子的s电子的电子云轮廓图【回顾与展望】各能级所含有原子轨道数目能级符号 n s n p n d n f 最多电子数 能级轨道数目能层轨道数目电子层为n 的状态含有 个原子轨道。
五、泡利原理、洪特规则、能量最低原理:基态电子排布遵循的三个原理1、电子的运动状态⎩⎪⎨⎪⎧空间运动状态:一个空间运动状态即一个原子轨道自旋状态:一个原子轨道内的两个电子有顺时针和逆时针两种取向【深刻理解】电子自旋(1)内在属性:自旋是微观粒子普遍存在的一种如同电荷、质量一样的内在属性; (2)两种取向:电子自旋在空间有顺时针和逆时针两种取向,简称 ; (3)表示方法:常用上下箭头(↑和↓)表示自旋相反的电子。
2、轨道表示式(电子排布图)(1)用方框(或圆圈)表示原子轨道,能量相同的原子轨道(简并轨道)的方框相连;(2)箭头表示一种自旋状态的电子,“↑↓”称 ,“↑”或“↓”称 (或称未成对电子); (3)能直观反映出电子的排布情况及电子的自旋状态。
【资料卡片】常见原子的电子排布图原子类别 电子排布式电子排布图 氢原子 1s 1 1s↑ 氦原子1s 21s ↑↓ 氮原子 1s 22s 22p 31s ↑↓ 2s ↑↓ 2p ↑ ↑ ↑ 氧原子 1s 22s 22p 41s ↑↓ 2s ↑↓ 2p ↑↓ ↑ ↑ 钠原子1s 22s 22p 63s 11s ↑↓ 2s ↑↓ 2p ↑↓ ↑↓ ↑↓ 3s ↑〔思考讨论〕(1)在钠原子中,有 种空间运动状态,有 种运动状态不同的电子。
第一章原子的结构与键合ppt课件

(1)共价键的定义 ➢ 有些同类原子,例如周期表IVA,VA,VIA族中大多数元
素或电负性相差不大的原子互相接近时,原子之间不产生 电子的转移,此时借共用电子对所产生的力结合。
(2)共价键的特点 ➢ 共价键键合的基本特点是核外电子云达到最大的重叠,形
成“共用电子对”,有确定的方位,且配位数较小。
由于金属键即无饱和性又无方向 性,因而每个原子有可能同更多 的原子结合,并趋于形成低能量 的密堆结构,当金属受力变形而 改变原子之间的相互位置时不至 于破坏金属键,这就使金属具有 良好的延展性。
金属变形时,由金属键结 合的原子可变换相对位置
(3)金属键型晶体的特征 良好的导电、导热性:
自由电子定向运动(在电场作用下)导电、(在热场作 用下)导热。
金属键模型
电子气 金属离子
图 金属键与金属晶体
© 2003 Brooks/Cole Publishing / Thomson Learning™
图 金属键与金属晶体
图 金属键、金属的导电性和金属的变形
问题1:金属具有良好导电、导热性能的原因? (自由电子的存在)
问题2:金属具有良好延展性的原因?
Pauli不相容原理(Pauli principle) 在一个原子中,不可能存在四个量子数 完全相同的两个电子。
Hund规则(Hund ’s rule) 在同一亚层中的各个能级中, 电子的排布尽可能分占不同 的能级,而且自旋方向相同
IA
1 H IIA 2 Li Be
碱金属
碱土金属 过渡元素
主族金属
第一节 原子结构
1.1.1 物质的组成
一切物质都是由无数微粒按一定 的方式聚集而成的。这些微粒可能 是分子、原子或离子。
人教版选修三第一章 第一节 原子结构

第一章 第一节 原子结构可能用到的原子量:一、选择题(只有1个正确答案;共15小题,每小题2分,共30分。
)1.道尔顿的原子学说曾经起了很大的作用。
他的学说中主要有下列三个论点:①原子是不能再分的微粒;②同种元素的原子的各种性质和质量都相同;③原子是微小的实心球体。
从现代原子——分子学说的观点看,你认为不正确的是( )A 只有①B 只有②C 只有③D ①②③2.下列能级中轨道数为5的是( )A S 能级B P 能级C d 能级D f 能级3.在第n 能层中,当它作为原子的最外层时容纳电子数最多与第(n -1)层相同; 当它作为原子的次外层时,其电子数比(n -1)层多10个,则对此电子层的判断正确的是( )A 必为K 层B 只能是L 层C 只能是M 层D 可以是任意层4.若n =3,以下能级符号错误的是( )A n pB n fC n dD n s5.目前普遍认为,质子和中子都是由被称为u 夸克和d 夸克的两类夸克组成。
u 夸克带电量为32e ,d 夸克带电量为31 e ,,e 为基元电荷。
下列结论中可能正确的是( ) A 质子由1个u 夸克和2个d 夸克组成,中子由1个u 夸克和2个d 夸克组成B 质子由2个u 夸克和1个d 夸克组成,中子由1个u 夸克和2个d 夸克组成C 质子由1个u 夸克和2个d 夸克组成,中子由2个u 夸克和1个d 夸克组成D 质子由2个u 夸克和1个d 夸克组成,中子由1个u 夸克和1个d 夸克组成6.一个电子排布为1s 22s 22p 63s 23p 1的元素最可能的价态是( )A +1B +2C +3D -17.下列各原子或离子的电子排布式错误的是( )A Al 1s 22s 22p 63s 23p 1B O 2- 1s 22s 22p6 C Na + 1s 22s 22p 6 D Si 1s 22s 22p 2 8.下列表达方式错误的是( )A 甲烷的电子式B 氟化钠的电子式C 硫离子的核外电子排布式 1s 22s 22p 63s 23p 4D 碳-12原子 126C9.(选作)列离子中外层d 轨道达半充满状态的是 ( )A Cr 3+B Fe 3+C Co 3+D Cu+ 10.在多电子原子中,轨道能量是由( )决定的。
第一章第一节原子结构练习题(带答案)

一、原子的诞生1.在物质结构研究的历史上,首先提出原子内有原子核的科学家是( )解析:汤姆生最早提出了电子学说,道尔顿最早提出了原子学说,卢瑟福最早提出了原子核,玻尔最早提出了原子的行星模型。
答案:C2.下列说法中,不符合现代大爆炸宇宙学理论的是( )A.我们所在的宇宙诞生于一次大爆炸B.恒星正在不断地合成自然界中没有的新元素C.氢、氦等轻核元素是宇宙中天然元素之母D.宇宙的所有原子中,最多的是氢元素的原子答案:B3.据报道,月球上有大量3He存在。
下列关于3He的说法正确的是( )A.是4He的同分异构体B.比4He多一个中子C.是4He的同位素D.比4He少一个质子答案:C二、能层与能级1..M能层对应的电子层是( )A.第一能层B.第二能层C.第三能层D.第四能层答案:C2.下列各能层中不包含p能级的是( )答案:D3.下列各电子能层中含有3p能级的是( )能层能层能层能层答案:C能层具有的能级数为( )解析:每一个能层所具有的能级数等于能层序数,N能层为第四能层,故能级数为4。
答案:B5.下列各能层中不包含d能级的是( )能层能层能层能层答案:C6.下列能级中,不属于M能层的是( )答案:B7.在N能层中,最多能容纳的电子数为( )答案:D9.下列能级中可容纳电子数最多的是( )答案:D10.下列说法正确的是( )A.同一原子中,1s、2s、3s电子的能量逐渐减小B.同一原子中,2p、3p、4p电子的能量相等C.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动D.各能层含有的能级数为n(n为能层序数)答案:D11.下列是关于多电子原子核外电子运动规律的叙述,其中叙述正确的是( )A.核外电子是分层运动的B.所有电子在同一区域里运动C.能量高的电子在离核近的区域运动D.同一能层的电子能量相同答案:A12.画出Be、N、Ne、Na、Mg这些元素的基态原子结构示意图,并回答下列问题:((1)只有K层与L层的元素有(2)含有M层的有(3)最外层电子数相同的有。
第一章 第一节 原子结构练习题(带答案)

一、原子的诞生1。
在物质结构研究的历史上,首先提出原子内有原子核的科学家是()解析:汤姆生最早提出了电子学说,道尔顿最早提出了原子学说,卢瑟福最早提出了原子核,玻尔最早提出了原子的行星模型。
答案:C2。
下列说法中,不符合现代大爆炸宇宙学理论的是()A。
我们所在的宇宙诞生于一次大爆炸B.恒星正在不断地合成自然界中没有的新元素C。
氢、氦等轻核元素是宇宙中天然元素之母D.宇宙的所有原子中,最多的是氢元素的原子答案:B3.据报道,月球上有大量3He存在。
下列关于3He的说法正确的是()A。
是4He的同分异构体B。
比4He多一个中子 C.是4He的同位素 D.比4He少一个质子答案:C二、能层与能级1.。
M能层对应的电子层是()A。
第一能层 B.第二能层 C.第三能层 D.第四能层答案:C2.下列各能层中不包含p能级的是()A.N B。
M C.L D.K答案:D3.下列各电子能层中含有3p能级的是()A.K能层B。
L能层C。
M能层 D。
N能层答案:C4.N能层具有的能级数为()A。
5 B。
4 C。
3 D.2解析:每一个能层所具有的能级数等于能层序数,N能层为第四能层,故能级数为4。
答案:B5。
下列各能层中不包含d能级的是()A.N能层B。
M能层 C.L能层D。
O能层答案:C6.下列能级中,不属于M能层的是()A.3sB.4sC.3pD.3d答案:B7。
在N能层中,最多能容纳的电子数为()A.2B.8C.18 D。
32答案:D9。
下列能级中可容纳电子数最多的是()A。
6s B。
4p C.3d D。
4f答案:D10。
下列说法正确的是()A.同一原子中,1s、2s、3s电子的能量逐渐减小B。
同一原子中,2p、3p、4p电子的能量相等C。
能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动D。
各能层含有的能级数为n(n为能层序数)答案:D11.下列是关于多电子原子核外电子运动规律的叙述,其中叙述正确的是()A。
人教版高中化学选择性必修第2册 第一章 原子结构与性质 第一节 原子结构(第1课时)

最多电
子数
2
8
18
32
50
72
98
M L
K
+
hv’
hv
能层越高,电子的能量 越高,能量的高低顺序为
E(K) < E(L) < E(M) < E(N) < E(O) < E(P) < E(Q)
核外电子在能层中的排布规律
(1)各能层最多能容纳2n2个电子。
(2)最外层电子数目不超过8个(K层为最外层时不超过2个);
(1)各电子层最多能容纳2n2个电子。
(2)最外层电子数目不超过8个(K层为最外层时不超过2个);
次外层电子数最多不超过18个;
倒数第三层不超过32个。
(3)核外电子总是尽量先排满能量最低、离核最近的电子层,
然后才由里往外,依次排在能量较高电子层。
而失电子总是先失最外层电子。
人类对原子结构的认识过程
能层
K
能级
1s
L
2s
M
2p
3s
3p 3d
N
4s
4p 4d
O
4f
5s
5p …
能层中填充电子表示方法——原子结构示意图
谢谢观看
高二—人教版—化学—选择性必修2—第一章
第一节 原子结构
(第一课时答疑)
1.在同一个原子中,M能层上的电子与Q能层上的电子的能量
A.前者大于后者
B.后者大于前者
√
C.前者等于后者
不同能层相同能级的能量顺序 E(1s)<E(2s)<E(3s)<E(4s)
【巩固・练习】
1.判断正误(正确的打“√”,错误的打“×”)
(1)能层就是电子层,包含不同的能级( √ )
第一节 原子结构(第一课时)

n37
பைடு நூலகம்
2、核素 思考: 1、元素的种类是由什么决定的? 2、同种元素的原子中的中子数也相同吗? 交流:
三种不同的氢原子
核素: 具有一定数目质子和一定数目中子 的一种原子 如:氢元素的三种核素 氕
A
14 N、14 C 7 6
),属于
B
40
Ar、4020Ca 18
35 Cl、37 Cl 17 17
C O2、O3
D
E、Fe、Fe2+、Fe3+ 5、3919K的中子数为 。 6、某元素原子的质量数为A,它的离子Xn+的 和外有y个电子,Wg这种种元素的原子核内的 中子数为 。
试一试
1. 下列各组物质中,互为同位素的是( D )
第一章 第一节 原子结构
第一讲 原子结构
help!
两千多年以来,科学家 一直在思考一个问题:如果 把一个物体一直分割下去, 将会怎样?能不能找到一种 组成物质的最基本粒子?
原子结构模型的演变
公元前5世纪,希腊哲学家 德谟克利特等人认为 :万物 是由大量的不可分割的微粒 构成的,即原子。
1897年,英国科学家汤姆生发现了电子。
“葡萄干布丁”模型
卢瑟福α粒子散射实验
ks5u精品课件
第一节 原子结构
交流与质疑: 1、构成物质的基本微粒有哪些? 2、三种微粒的组成和结构如何? 3、物质的性质与哪种微粒的结构有密切 的关系? 4、原子的结构如何?
一
原子核 核素
1.原子的构成
阅读P3 交流·研讨
名词解释:相对质量 相对原子质量= 一个原子的质量
高中化学选择性必修二 第1章第1节原子结构

新课讲解
2.电子排布式 (1)含义:电子排布式是用核外电子分布的能级及各能级上的电子数来表示电子排布 的式子。 (2)表示方法:
新课讲解
(3)书写方法: 第一步:按照构造原理写出电子填入能级的顺序, 1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s 第二步:根据各能级容纳的电子数填充电子。 第三步:去掉空能级,并按照能层顺序排列即可得到电子排布式。
元素周期律
提出构造原理
“能层、能级”
完整的构造原理
1936年马德隆
发表了以原子光 谱事实为依据的 完整的构造原理
1869年俄国化学家门捷
列夫发现了元素周期律
1920年丹麦科学家波尔提出了构造原理,即从氢开始,随 核电荷数递增,新增电子填入原子核外“壳层”的顺序, 1925年,波尔 的“壳层”落实为“能层”与“能级”,厘 清了核外电子的可能状态,复杂的原子光谱得以诠释。
新课讲解 复习回顾:1.原子的结构
质子 Z个
原子
A Z
X
原子核
中子(A—Z)个
(几乎集中原子的全部质量)
核外电子 Z个
(其运动空间几乎占据了原子的整个体积)
质量数:对质子和中子的相 对质量取整数相加的数值, 即近似原子量。
①数量关系:
②质量关系:
核电荷数(Z) = 核内质子数 = 核外电子数 质量数(A)= 质子数(Z)+ 中子数(N)
吸收光谱 明亮背景的暗色谱线
基态原子
吸收 能量
释放 能量
激发态原子
发射光谱 暗色背景的明亮谱线
新课讲解
(3)光谱分析: 在现代化学中,常利用原子光谱上的特征谱线来鉴定元素, 称为光谱分析 。
例如:铯(1860年)和铷(1861年),其光谱图中有特征的蓝光和红光,它们的 拉丁文名称由此得名。又如,稀有气体氦的原意是“太阳元素”,是1868年 分析太阳光谱发现的,最初人们以为它只存在于太阳,后来才在地球上发现。
人教版高中化学选修3 物质结构与性质 第一章 第一节 原子结构(第1课时)精品PPT课件

开天辟地—原子的诞生
质子(正电) 原子核 原子 (正电) 中子(不带电) 不显 电性 核外电子 分层排布 (负电) 与物质化学性质密切相关
2020/10/26
18
能层与能级
二、能层与能级
(1)能层
在多电子的原子核外电子的能量是不同的, 按电子的能量差异,可以将核外电子分成不 同的能层。
2020/10/26
开天辟地—原子的诞生
问题:宇宙大爆炸是怎么回事?物质是由原子构成的,那 么原子是怎样诞生的呢? P4
1932年勒梅特首次提出了现代大爆炸宇宙理论
宇宙大爆炸
2h后 诞生
大量的氢 大量的氦 极少量的锂
原子核的 熔合反应
合成
其他元素
2020/10/26
4
开天辟地—原子的诞生
一、开天辟地—原子的诞生
思考与交流 阅读课本P4
2020/10/26
5
开天辟地—原子的诞生
人类认识原子的过程
人类在认识自然的过 程中,经历了无数的艰 辛,正是因为有了无数 的探索者,才使人类对 事物的认识一步步地走 向深入,也越来越接近 事物的本质。随着现代 科学技术的发展,我们 现在所学习的科学理论, 还会随着人类对客观事 物的认识而不断地深入 和发展。
19
能层与能级
核外电子分层排布
依据核外电子的能量不同:
离核远近:近
远
能量高低:低
高
1
2
3
4
5
6
7
K
L
M
N
O
P
Q
2020/10/26
20
能层与能级
原子核外电子分层排布规律:
(1)各能层最多能容纳2n2个电子。
第一章:原子结构

n 光谱符号
1 K
2 L
3 M
4 N
5 O
· · · · · ·
对氢原子来说,电子能量完全由n决定:
2.181018 Z 2 E J 2 n
四 个 量 子 数
B:角量子数:l 取值:0、1,2,3,. n-1
它表示原子轨道和电子云的形状 ,l与能级或称电子亚层对应。
(也是决定能量高低的因素)
自然界的物质种类繁多,性质各异,但它们都是由种类不同的原子组成,
原子以不同的种类.数目和方式结合,形成了无数的物种,因此,原子结构的
知识是了解物质结构和性质的基础。 化学变化包含着旧的化学键断裂和新的化学键的形成,化学变化一般 只涉及核外电子运动状态的变化,所以研究原子结构时,主要研究核外电子
的运动状态。
∴|ψ|2 ∝电子的几率密度
电子云角度分布图表示出电子在空间不同角度所出现的几率密度大小。
三、波函数的空间图象
B:电子云角度分布图 ︱Y(θ.φ) ︱2
z
+
→ θ.φ 作图,就得到电子云角度分布图
z y
+
z
+
x
-
x
+ -
x
pz z
x
s px z z x s px x x pz x py y
py
三、波函数的空间图象
E 光子 E E 2 E1 h 2.18 10
18
Z n 2n 2 2 1
2
1
←波长
青
氢原子光谱的一部分
课堂小结
玻尔理论最大贡献:建立微观粒子量子化特性,成功地解释了氢
原子光谱是线状光谱,为化学键理论奠定了基础。
《第一章 第一节 原子结构》教学设计

《原子结构》教学设计方案(第一课时)一、教学目标1. 知识目标:学生能够了解原子的构成,理解电子在原子核外排布的规律,掌握原子结构示意图的画法。
2. 能力目标:学生能够通过观察、思考、讨论等活动,提高观察能力、思维能力和表达能力。
3. 情感目标:通过本节课的学习,增强学生对化学学科的学习兴趣,培养学生的科学态度和科学精神。
二、教学重难点1. 教学重点:电子在原子核外排布的规律。
2. 教学难点:如何通过观察原子结构示意图,判断原子的种类和元素的化学性质。
三、教学准备1. 准备教学用具:黑板、白板、投影仪、原子结构示意图。
2. 准备化学实验用品:实验器械、实验药品。
3. 准备相关视频、图片等多媒体素材。
4. 设计教室讨论问题及学生活动方案。
四、教学过程:1. 导入新课教师可以通过展示一些原子结构的图片或动画,引导学生思考原子结构的特点和构成,引出本节课的主题。
2. 原子模型的发展历程通过介绍原子模型的发展历程,让学生了解科学家们对原子结构认识的不息深化过程,激发学生对科学探索的兴趣。
3. 原子核外电子排布教师可以通过一些实验或事实,让学生了解原子核外电子的运动特点和排布规律,并介绍电子云的观点和意义。
4. 探究实验教师可以设计一些探究实验,让学生通过观察实验现象,进一步理解原子核外电子的运动特点和排布规律。
例如,利用激光照射锌板,观察荧光粉的发光现象等。
5. 教室互动教师可以提出一些问题,引导学生进行思考和讨论,增强师生之间的互动和交流。
例如,为什么原子核外电子排布有一定的规律?不同元素的原子核外电子排布有何不同?6. 总结与作业在课程结束时,教师对本节课的内容进行总结,强调重点和难点,并安置一些与原子结构相关的作业,让学生进一步稳固所学知识。
7. 拓展阅读教师可以推荐一些与原子结构相关的书籍、文章或网站,让学生进一步了解原子结构的相关知识,拓宽学生的视野。
8. 德育渗透在课程中,教师可以渗透一些德育思想,如科学探索的精神、团队协作的重要性等,帮助学生树立正确的人生观和价值观。
化学选修3第一章第一节

1.原子核外电子的排布是分层的 (以原子核为中心能量不同的电子在离核不同 距离的区域内运动)
离核近(内层)—能量低; 离核远(外层)—能量高
与核的距离 由近到远 电子层(n) 1 2 3 4 5 6 7 …
电子层符号 K L M N O P Q….
• 2、核外电子排布遵守能量最低原理
即先排满能量低的电子层,再排能量高的电子层。
近代科学原子论(1803年)
道• 尔
一切物质都是由最小的 不能再分的粒子——原 子构成。
顿• 原子模型:原子是坚实 原 的、不可再分的实心球。
子
模
型
英国化学家道尔顿 (J.Dalton , 1766~1844)
原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)
汤
• 电子是种带负电、有一 定质量的微粒,普遍存
电 子 云
模 型
构 模
模 型
型
复习: 化学必修已经学过的内容
质子(正电) 原子核 原子 (正电) 中子(不带电)
不显 电性 核外电子 分层排布
(负电) 与物质化学性质密切相关
两个关系式:
• 核电荷数 == 质子数 == 核外电子数
即 A == P + N]
做高速运动。
英国科学家卢瑟福 (E.Rutherford,1871~1937)
α粒子散射实验
Au
卢瑟福原子模型
玻尔原子模型(1913年)
玻 尔 原
• •
玻尔借助诞生不久的量子 理论改进了卢瑟福的模型。
玻尔原子模型(又称分层 模型):当原子只有一个
子 电子时,电子沿特定球形
模 型
轨道运转;当原子有多个
能级: 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
第一章第一节《原子结构》同步测试题
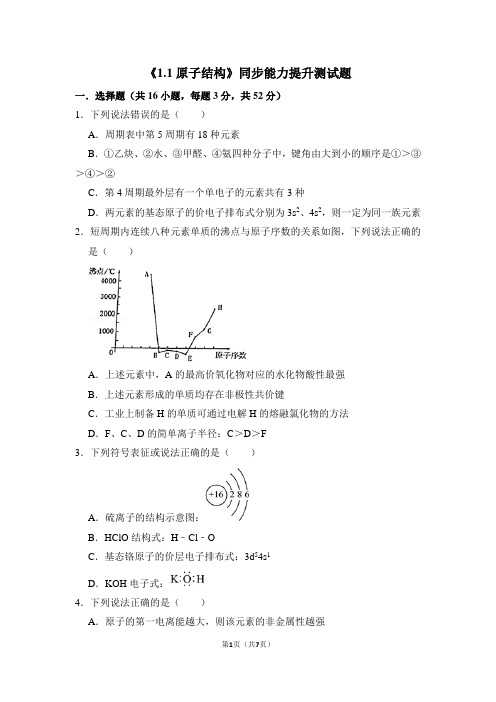
《1.1原子结构》同步能力提升测试题一.选择题(共16小题,每题3分,共52分)1.下列说法错误的是()A.周期表中第5周期有18种元素B.①乙炔、②水、③甲醛、④氨四种分子中,键角由大到小的顺序是①>③>④>②C.第4周期最外层有一个单电子的元素共有3种D.两元素的基态原子的价电子排布式分别为3s2、4s2,则一定为同一族元素2.短周期内连续八种元素单质的沸点与原子序数的关系如图,下列说法正确的是()A.上述元素中,A的最高价氧化物对应的水化物酸性最强B.上述元素形成的单质均存在非极性共价键C.工业上制备H的单质可通过电解H的熔融氯化物的方法D.F、C、D的简单离子半径:C>D>F3.下列符号表征或说法正确的是()A.硫离子的结构示意图:B.HClO结构式:H﹣Cl﹣OC.基态铬原子的价层电子排布式:3d54s1D.KOH电子式:4.下列说法正确的是()A.原子的第一电离能越大,则该元素的非金属性越强B.基态S原子的核外电子排布式写成1s22s22p63s23p23d2违背了泡利原理C.同一原子中,1s、2s、3s能级上的电子能量逐渐减小D.随着核电荷数递增,电子并不总是填满一个能层后再开始填入下一个能层的5.下列化学用语或图示表达不正确的是()A.Cl﹣的结构示意图:B.2﹣甲基丁烷的结构模型:C.乙醇的核磁共振氢谱:D.NaCl的电子式:6.下列说法正确的是()A.液晶的光学性质随外加电场的变化而变化B.超分子是由两个或多个分子通过共价键形成的分子聚集体C.按照现有构造原理,理论上元素周期表第八周期应有32种元素D.玻尔理论不仅成功解释了氢原子光谱,而且还推广到其他原子光谱7.下列轨道表示式正确且所表示的元素原子的能量处于最低状态的是()A.B.C.D.8.下列有关光谱的说法中不正确的是()A.原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原因B.原子光谱只有发射光谱C.通过原子光谱可以发现新的元素D.通过光谱分析可以鉴定某些元素9.下列说法正确的是()A.2p能级有3个轨道B.1s、2s、3s的电子云轮廓图形状不同C.p轨道呈哑铃形,因此p轨道上电子的运动轨迹呈哑铃形D.同一能层的p轨道电子能量不一定高于s轨道电子能量10.下列说法不正确的是()A.多电子原子中,原子轨道能量:3s<3p<3dB.基态原子的最外层电子排布为ns2的元素,在元素周期表中均位于第IIA 族C.基态Cl原子中,存在17个运动状态不同的电子D.基态O原子中能量最高的电子的电子云的形状为哑铃形11.下列轨道按能量由高到低排列正确的是()A.3d>3p>3s B.2p x>2p y>2p zC.1s>2s>3s D.5s>4f>4d12.下列表示正确的是()A.中子数为176的某核素:TsB.基态锌原子的价层电子排布式:3d104s2C.26Fe3+的结构示意图:D.基态氮原子的轨道表示式:13.三氯蔗糖(W)的结构简式如图所示,下列有关W的说法错误的是()A.基态氯原子的简化电子排布式为[Ne]3s23p5B.电负性最大的元素为氧元素C.碳原子的杂化方式均为sp3杂化D.所涉及的化学键类型有极性键和氢键14.通常状况下,NCl3是一种油状液体,容易水解,含氯生成物有漂白性,NCl3分子立体构型与氨分子相似,下列对NCl3的有关叙述正确的是()A.NCl3水解方程式:NCl3+2H2O=3HCl+HNO2B.NCl3中所有原子均达到8电子稳定结构C.NCl3分子是非极性分子D.NCl3比NF3键角小15.下列说法正确的是()A.甲醇分子和双氧水分子有相同的电子数;He和Be2+有相同的质子数B.乙醇和乙二醇互为同系物;正丁烷和异丁烷互为同分异构体C.NaHCO3晶体中阴阳离子数相等;BaO2固体中阴阳离子数也相等D.H2O分子间存在氢键,故H2O比H2S分解时需要的温度高16.有A、B两种原子,A原子的第三电子层比B原子的第三电子层少3个电子,B原子的第二电子层电子数恰好为A原子第二电子层电子数的2倍.A和B 分别是()A.硅原子和钠原子B.硼原子和氦原子C.氯原子和碳原子D.碳原子和铝原子二.非选择题(共4小题,共48分)17.(12分)推断下列化合物的化学式:(1)X、Y两元素能形成XY2型化合物,XY2中共有38个电子,若XY2是离子化合物,其化学式是;若XY2是共价化合物其化学式是.(2)第三周期内,X、Y两元素的原子序数之差为4,它们组成的XY型化合物,其化学式为.(3)1mol某物质含有不同周期三种元素的原子各1mol,其质子总数为20mol,该物质的化学式为.(4)某非金属X的最高正价为+m,它的最高价氧化物对应的水化物中有b 个氧原子,则这种酸的化学式是.(5)X元素的最高正价和负价绝对值之差为6,Y元素和X元素原子的次外电子层上都有8个电子,X和Y形成的化合物在水溶液中能电离出电子层结构相同的离子,则该化合物是.18.(10分)按要求填空:(1)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的,乙元素原子核内无中子,丙元素原子核内有8个质子。
人教版高中化学选修三第一章第一节 原子结构 课件(共54张PPT)
二、10电子微粒和18电子微粒 1.10电子微粒
【典例3】 已知A、B、C、D四种物质分别是由短周 期元素组成的微粒,它们之间有如图所示的转化关系,且A 是一种含有18电子的微粒,C是一种含有10电子的微粒。请 完成下列各题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的 化学方程式:________________;
是O2置换H2S中的S。问题(4)中H、O形成的原子个数为1:1 的化合物是H2O2,N、H形成的化合物分子中电子数也为18 的分子只能是N2H4。
[答案] (1) (2)X(或氧) 2H2S+O2===2H2O+2S↓ (3)NH4HSO4
点燃 (4)N2H4+2H2O2=====N2+4H2O
2.(2012·长沙模考)下列有关化学用语使用正确的是 ()
A.硫原子的结构示意图: B.11H2、12H2、31H2是氢的三种同位素 C.原子核内有10个中子的氧原子:188O D.金刚石和石墨、甲烷和乙烷都属于同素异形体
解析 硫原子的结构示意图应为
A项错误。同位
素的研究对象是原子,但B选项中三种粒子是氢的单质,故
(4)若D是一种含有22个电子的分子,则符合如图关系的 A的物质有________(写化学式,如果是有机物则写相应的结 构简式)。
[解析] 本题把指定电子数目的有关微粒作为命题素 材,着重考查考生的有序思维能力。寻找10电子、18电子、 22电子微粒,必须从元素周期表出发,遵循由原子到分子, 再到离子的思考途径,列出相应的微粒。关于18电子微粒的 推断,对有序思维的要求更高,技巧性更强,我们可以以推 断10电子微粒的思路来进行分析,对数字18作一拆分,把18 拆成9+9,找出F2后会使18电子微粒的推断打开一个大“空
化学选修三第一章第一节

5d
6d
6p
7p
通式:ns··(n-2)f、(n-1)d、np ·· ··
三、构造原理与电子排布式
2.构造原理中排布顺序的实质 -----各能级的能量高低顺序
(1)相同能层的不同能级的能量高低顺序 : ns<np<nd<nf (2)英文字母相同的不同能级的能量高低顺序: 1s<2s<3s<4s;2p<3p<4p; 3d<4d (3) 不同层不同能级可由下面的公式得出: ns < (n-2)f < (n-1)d < np (n为能层序数)
5. 各能级包含的原子轨道数:
三、构造原理与电子排布式
问题解释:
1s22s22p63s23p63d1 1s22s22p63s23p64s1 正确书写方法:
想一想
第3层 第4层 第2层 第1层
钙Ca
+20
K层
2
L层
8
8
2
钙Ca 1s22s22p63s23p64s2
M层 N层
三、构造原理与电子排布式
3、电子排布式:
用数字在能级符号右上角表明该能级上的 排布的电子数。 该能级上排布 能层序数 能级符号 的电子数
小黑点不表示电 子,只表示电子在 这里出现过一次。 小黑点的疏密表示 电子在核外空间内 出现的机会的多少。
电子云只是形象地表示 电子出现在各点的概率高低, 而实际上并不存在。
五、电子云与原子轨道
课堂练习 1.下列有关说法正确的是 ( C ) A、通常用小黑点来表示电子的多少 B、小黑点密表示在该核外空间的电子数多 C、小黑点密表示在该核外空间的单位体积内 电子出 现的概率大 D、通常用小黑点来表示绕核作高速圆周运动
选修3《物质结构与性质》
.
第一节《原子结构》第一课时教案

教案
多
电
2 8 18 32 ……2n2
子
数
【巩固练习】
1.下列对不同时期原子结构模型提出的时间排列正确的是( )。
①电子分层排布模型②“葡萄干布丁”模型③量子力学模型
④道尔顿原子学说⑤核式模型
A.①③②⑤④
B.④②③①⑤
C.④②⑤①③
D.④⑤②①③
2.下列叙述正确的是( )。
A.能级就是电子层
B.每个能层最多可容纳的电子数是2n2
C.同一能层中的不同能级的能量高低相同
D.不同能层中的s能级的能量高低相同
3、下列能级表示正确(实际存在的)且最多容纳的电子数按由少到多的顺序排列的是( )。
A.1s、2p、3d
B.1s、2s、3s
C.2s、2p、2d
D.3p、3d、3f
4.钙原子的结构示意图为
请回答下列问题:(1)钙原子核外有个能层填充电子。
(2)钙原子M层有个能级填充电子。
(3)钙原子能层上的电子能量最高。
【能力提升】
1.下列说法不正确
...的是(n表示能层序数)()。
A.各能层含有的能级数与能层序数相同
B.各能层的能级都是从s能级开始至f能级结束
C.1s、2s、3s的能量不同
D.s、p、d、f 4个能级最多容纳的电子数分别是2、6、10、14
2.氯原子核外能量最高的电子填充在()。
A.4s能级
B.3p能级
C.3d能级
D.3s能级。
第一节原子结构与性质

第一章原子結構與性質第一節原子結構一. 物質結的本質“原子”一詞源自古希臘,希臘語中ATOM是不可再分的意思,古希臘哲學家認為原子是世間萬物最小的粒子◦直到1808年,英國人道爾頓把物質由原組成的概念作出重大修訂,他認為物質是由不同的微細粒子所組成,而在化學反應中,反應物的粒子並沒有改變,它們只是重新排列形成生成物,這個想法在當時己透過實驗得以証實◦道爾頓原子學說道爾頓原子學說的要點如下:1.所有元素都是由微細和不能再被分割的粒子組成,這些粒子稱為原子◦2.原子既不能被製造,也不能被毀滅◦3.同一種元素的原子,它們的質量和化學性質完全相同◦4.不同元素的原子,它們的質量和化學性質都完全不同◦5.當不同元素的原子結合時,便形成化合物,化合物中,各種原子的數目成一個簡單的整數比◦到了十九世紀末,實驗証據顯示,原子的結構遠較道爾頓所想的複雜,當時的科學家透過很多實驗証明,原子並非僅僅是一個堅硬而均勻的粒子,而是由幾種次原子粒子所構成◦1.質子:原子核的組成部分,帶正電的小微粒,一個質子帶個單位的電荷。
2.中子:原子核的組成部分,不帶電的小微粒。
3.電子:原子的組成部分,位於原子的週邊,帶負電的小微粒。
4.質量數:將原子核內所有的質子和中子的相對質量取近似整數值加起來,所得的值。
質量數(A)=(Z)+(N)5.同位素在同一種元素的原子中,當中有一些質子數目相同(即相同的原子序),但其中子數目並不相同(即不同質量數),這些原子稱為同位素。
例如:氯(Cl)的兩種同位素可寫成:豐度(自然界中的原子含量)的計算:一種元素的相對子原子質量是指該元素的各種同位素在碳-12標度上的相對同位素質量的平均值。
由於35Cl 和37Cl 的相對豐度分別是75.77和24.23,因此氯的相對原子質量可由以下的簡單計算中求得:則銅的相對原子質量為:.例1 已知自然界氧的同位素有16O ,17O ,18O ,氫的同位素有H ,D 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
………………
2、能级
规定,任一能层的能级总是从 s 能级 开始,依次称p、d、f、g能级……
能层 K L M N O
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s … 最多 2 2 6 2 6 10 2 6 10 14 电子 数
学与问
1、原子核外电子的每一个能层最 多可容纳的电子数与能层的序数 (n)间存在什么关系? 2、不同能层分别有多少个能级, 与能层的序数间存在什么关系? 3、英文字母相同的不同能级中所 能容纳的最多电子数是否相同
S Fe Sc V Se Ga Br
22s12p1 1s
3.下列各原子或离子的电子 排布式错误的是( D ) A Al 1s22s22p63s23p1 222s22p6 B O 1s C Na+ 1s22s22p6 22s22p2 D Si 1s
思考与交流
•电子排布式可以简化,如可以 把钠的电子排布式写成【Ne】 3s1。试问:上式方括号中的 符号的意义是什么?你能仿照 钠原子的简化电子排布式写出 O、Si、Fe的简化电子排布式 吗?
小黑点的疏密表示电子在核外空间 单位体积内出现的概率的大小。
1s电子在原子核外 出现的概率分布图
★量子力学中将
这种电子云轮廓 图称为
“原子轨道”
2、原子轨道 a.s电子的原子轨道(电子云)形 状 是以原子核为中心的球体,只有 一个伸展方向
2.p电子云/原子轨道的形状是纺锤形 (或称为哑铃形),其伸展方向是互向 垂直的三个方向(Px、Py、Pz)。
大爆炸后约2小时,诞生了大量的H, 少量的He和极少量的Li
我们今天熟悉的各种元素(原子), 都是从那时起经历了漫长复杂的物理化学 变化,分批分期合成而来的
能层:在多电子原子的核外电子的
能量是不同的,按电子能量的差异, 可以将核外电子分为不同的能层.
能级:在多电子原子中,同一能层
的电子的能量也可能不同,可以将它 们分为不同的能级.
一、人类探索物质结构的历史
原子结构的衍变过程 德谟克利特的古代原子学说
道尔顿的近代原子学说(模型)
汤姆生原子模型 卢瑟福原子模型
玻尔原 子模型
电子云模型
近 代 原 子 论
发 现 电 子
带 核 原 子 结 构 模 型
轨 道 原 子 结 构 模 型
电 子 云 模 型
二、物质决定性质
原性论 物质结构理论
P电子原子轨道半径同样随着n增大而增大
科学探究
观察图1-14,这些图称为原子的
电子轨道表示式
1.每个原子轨道最多只能容纳几 个电子?
2.当电子排在同一个能级内时, 有什么规律?
★核外电子排布规则:
1.能量最低原理 2.泡利不相容原理
3.洪特规则
4.补充规则
全充满(p6,d10,f14)
相对稳定的状态 全空时(p0,d0,f0)
★所含能级个数=能层序数 n ★不同能层中的s、p、d、f、g能 级最多能容纳的电子数是相同的, 各为:
s
d g
1×2=2
5×2=10
p
3×2=6
f
7×2=14
9×2=18
三、构造原理
原子核外电子排布必须遵循 一定的排布顺序 —构造原理
核 构外 造电 原子 理排 图布 的
1s----2s----2p----3s----3p--4s----3d--4p----5s----4d----存在着能级交错
半充满(p3,d5,f7)
例:
24
Cr原子的电子排布图:
22s22p63s23p63d54s1 1s 44s2 不是3d
注意
小结:
1.各原子轨道的能量高低比较
(1)ns<np<nd<nf
(2)1s<2s<3s<4s (3)同一能层同一能级的各原子 轨道能量相等: 2Px=2Py=2Pz
电子层 1 2
★原子的电子排布遵循构造原理使
整个原子的能量处于最低状态,简 称能量最低原理
ns<(n-2)f<(n-1)d<np
试书写N、Cl、K、26Fe原子 的 核外电子排布式
1.下列各原子的电子排布正确的 是( BD ) A.Be B.C 1s22s22p2 C.He 1s12s1 D.Cl 1s22s22p63s23p5 2.书写下列原子的电子排布式
物质的元素组成决定了性质
同分异构体的存在说明物 质的结构决定物质的性质
晶体结构决定物质的性质
第一章
原 子 结 构
第 一 节
原子的结构
原子核
质子
原子
中子 核外电子
核电荷数=核内质子数=核外电子数
质量数=质子数+中子数
一 、开天辟地—原子的诞生
现代大爆炸宇宙学理论——
宇宙诞生于约140亿年前的一次大爆炸
四、基态与激发态、原子光谱
1.基态原子与激发态原子
处于最低能量的原子叫做基态原子
当基态原子的电子吸收能量后, 电子会跃迁到较高能级,变成 激发态原子
不同元素的原子发生跃迁时会吸收 或释放不同的能量 表现为光的形式
用光谱仪摄取 得到各种元素的电子的 吸收光谱或发射光谱
可利用原子光谱上的特征谱线来鉴 定元素,称为光谱分析
3 4 n
原子轨 原子轨 道类型 道数目
宏观物体的运动特征:
•可以准确地测出它们在某一时刻 所处的位置及运行的速度
电子的质量很小,只有9.11×10-31 千克; 核外电子的运动范围很小(相对于 宏观物体而言); 测不准 电子的运动速度很大;
1、电子云
图中
表示原子核,一个小黑点代表 电子在这里出现过一次
二、能层与能级
1、能层
能层 符号 1 K 2 L 3 M 4 N 5 O … … n
2×12 2×22 2×32 2×42 2×52 最多
电子 数
2 2n
核外电子的排布规律:
(1)先排能量低的电子层,再排能量高 的电子层,由里往外。 (2)每一层最多容纳电子数:2n2个。 (3)最外层电子数不超过8个(K层为 最外层时不超过2个)。 (4)次外层电子数不超过18个,倒数第 三层不超过32个。
课堂练习
1、判断下列表达是正确还是错误 1)1s22p1属于基态;
2)1s22s2 2p63s2 3p63d54s1属于激发态;
3)1s22s2 2p63d1属于激发态; 4)1s22s2 2p63p1属于基态;
答案: (1) x(2) x(3)√(4) x
五、电子云与原子轨道
思考: 宏观物体与微观物体(电 子)的运动有什么区别?
