青蒿素的工业生产流程
天然化学品(青蒿素)

青蒿素研究进展及合成方法摘要青蒿素(artemisinin)是我国自主开发的强效、低毒、无抗性抗疟特效药,尤其是治疗脑型疟疾和抗氯喹恶性疟疾的特效药。
青蒿中的青蒿素含量在0.4%~1.0%之间,从天然青蒿中提取青蒿素难以满足市场需求,而青蒿素化学合成的工艺复杂、成本高、毒性大、产率低,至今未能实现工业化生产。
目前。
本文对自青蒿素发现以来的最新研究进展进行了比较详尽的综述。
内容包括:中药青蒿和青蒿素的发现,青蒿素的来源,青蒿素的药理作用,青蒿素的全合成,青蒿素的生物合成,青蒿素衍生物以及植物组织培养生产青蒿素。
关键词青蒿素;青蒿素衍生物;合成青蒿素(artemisinin)是继氯喹、乙氨嘧啶、伯喹和磺胺后最热的抗疟特效药,尤其对脑型疟疾和抗氯喹疟疾具有速效和低毒的特点,已成为世界卫生组织推荐的药品。
青蒿素的抗疟机理与其它抗疟药不同,它的主要作用是通过干扰疟原虫的表膜-线粒体功能,而非干扰叶酸代谢,从而导致虫体结构全部瓦解。
目前药用青蒿素是从中药青蒿即菊科植物黄花蒿的叶和花蕾(Artemisia annua L.)中分离获得的。
由于青蒿的采购、收获,直至工厂加工提取,环节较多,费时费力,且不同采集地和不同采集期青蒿品质有很大的差别,同时,大量采集自然资源,必然会破坏环境和生态平衡,导致资源枯竭。
因此,为增加青蒿素的资源,世界各国都在加紧开展青蒿素及其衍生物的开发研究,长期稳定地和大量地供应青蒿素成为各国科学家面临的严峻考验。
本文将对目前国际上青蒿素研究的现状从以下几个方面进行论述。
1.中药青蒿和青蒿素的发现奎宁和氯喹这类药物对疟疾治疗的成功没有延续太久, 20世纪60年代开始出现了抗药性的疟原虫, 尤其是在东南亚和非洲地区, 甚至已到了无有效药物可用的地步。
而当时的越南战争则更凸显这一问题的严重性, 热带丛林地区疟疾肆虐, 成为部队大量减员的主要原因。
越南方面向中国提出了协助解决疟疾困扰的要求, 中国领导人接受了这一要求, 确立了由全国多部门参加, 以疟疾防治药物研究为主要任务, 代号为“523”的紧急军工项目。
青蒿素的性质及合成

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载青蒿素的性质及合成地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容青蒿素性质及合成方法院系:化工学院专业:应用化学学号:姓名:指导老师:2016/1/12摘要:青蒿素是目前治疗疟疾的特效药。
本文对自青蒿素发现以来的最新研究进展进行了比较详尽的综述。
内容包括:青蒿素的特性,青蒿素的合成,青蒿素的生物合成,青蒿素衍生物。
关键词:青蒿素;合成方法;青蒿素衍生物Abstract:The recent research advances in artemisinin, the most effective weapons against malarial parasites have been reviewed. An overview is given on artemisinin research from the following aspects: sources of artemisinin,synthesisof artemisinin, biosynthesis of artemisinin, analogs of artemisinin and artemisinin production from plant tissue cultures。
Key words:artemisinin,synthesis,artemisinin derivatives目录1、前言………………………………………………………………2、青蒿素的基本性质………………………………………………(1)分子结构…………………………………………………………(2)理化性质…………………………………………………………(3)药动力……………………………………………………………(4)提取工艺…………………………………………………………3、合成方法…………………………………………………………(1)全合成…………………………………………………………(2)半合成…………………………………………………………(3)生物合成………………………………………………………4、衍生物…………………………………………………………5、抗癌功能…………………………………………………………6.结论………………………………………………………………1前言:青蒿素是中国学者在20世纪70年代初从中药黄花蒿( Artem isia annua L1 )中分离得到的抗疟有效单体化合物,是目前世界上最有效的治疗脑型疟疾和抗氯喹恶性疟疾的药物, 对恶性疟、间日疟都有效, 可用于凶险型疟疾的抢救和抗氯喹病例的治疗。
青蒿素提取工艺流程

青蒿素提取工艺流程
青蒿素是一种从青蒿植物中提取的药物,被广泛用于治疗疟疾。
以下是青蒿素提取的一般工艺流程:
1.采集青蒿植物:青蒿素主要来源于青蒿植物,因此首先需要采集新鲜的青蒿植物。
最佳的收割时间通常是在植物的花朵开始开放但尚未完全开放的阶段。
2.晾晒:采集的青蒿植物需要在阴凉、通风的地方进行晾晒,以降低植物的水分含量。
3.粉碎:干燥后的青蒿植物需要被粉碎成细小的颗粒,以便后续的提取过程。
4.溶剂提取:将青蒿植物颗粒与适当的溶剂(通常是乙醚或丙酮)混合,并进行提取。
这一步骤有助于将青蒿素从植物中分离出来。
5.过滤:提取后的混合物需要经过过滤,以去除植物残渣和其他杂质。
6.溶剂蒸发:过滤后的溶液需要进行溶剂蒸发,使得青蒿素在残留物中沉淀。
这通常通过加热溶液并使溶剂挥发来完成。
7.结晶:蒸发后,青蒿素开始结晶。
这些结晶可以通过进一步处理和提纯来得到更纯净的青蒿素。
8.干燥:提取和结晶后的青蒿素需要经过干燥过程,以去除残留的水分。
9.提纯:最终的产品可能需要进行进一步的提纯步骤,以确保
青蒿素的纯度达到药品标准。
10.包装:最终提纯的青蒿素可以根据需要进行包装,以便在制药、医疗或其他应用中使用。
需要注意的是,青蒿素的提取工艺可能会因生产厂家和提取规模而有所不同。
在工业生产中,可能采用更复杂的提取和纯化工艺,以确保产品的质量和符合药品标准。
青蒿素的工业提取原理

青蒿素的工业提取原理
青蒿素的工业提取原理主要包括以下几个步骤:
1. 采集青蒿:选择品质良好的青蒿植株,进行采集。
通常采集花期较长的植株以获取较多的青蒿素。
2. 破碎:将采集到的青蒿进行破碎处理,通常采用粉碎机将青蒿破碎成适当大小的颗粒。
3. 浸提:将破碎后的青蒿颗粒与适量的溶剂(如乙醇、醚等)混合,进行浸提。
浸提的目的是将青蒿中的有机物溶解到溶剂中,其中包括青蒿素。
4. 滤液分离:将浸提液进行滤液分离,分离出提取溶剂和青蒿中的有机物。
通常使用过滤设备或离心机进行分离。
5. 浓缩:将滤液中的溶剂进行浓缩,通常采用蒸馏或加热蒸发的方式,使溶剂蒸发,留下溶剂中的有机物。
6. 结晶:将浓缩后的溶液进行冷却结晶,使青蒿素从溶液中析出。
结晶过程中,可以通过调节温度和冷却速度来控制青蒿素的结晶质量和纯度。
7. 分离和干燥:将青蒿素与溶剂分离,并进行干燥处理,去除残留的溶剂,得
到纯化的青蒿素。
整个工业提取过程中,通过合理选择溶剂、控制溶剂的比例、温度和压力等参数,可以提高青蒿素的提取效率和纯度。
此外,还可以通过进一步的纯化和结晶来提高青蒿素的纯度。
青蒿素提取方法

青蒿素提取方法青蒿素是一种有效的抗疟药物,广泛应用于全球疟疾的治疗。
青蒿素的提取方法一直是研究的热点,本文将介绍青蒿素提取的方法及其优缺点。
1.1 现代化半制备法现代化半制备法是通过青蒿素的快速提取和改进萃取技术来实现的。
该方法的主要步骤为草杆蒸后剪碎,浸泡于乙醇中,提取和蒸馏。
1.1.1 草杆的蒸馏将青蒿的草杆去除杂质,洗净并切碎。
将草杆放入蒸馏桶中进行蒸馏,蒸馏时需要加水。
蒸馏后的草杆取出,用水洗净。
1.1.2 乙醇浸泡将草杆放入含40%乙醇的容器中,充分浸泡12-24小时,振动抽取浸液使之均匀分布。
1.1.3 静置将乙醇提取液置于室温下2-3天静置,使青蒿素充分沉淀。
对浸液进行过滤,滤液将乙醇挥发殆尽。
将残渣加入水中,然后进行蒸馏。
收集和凝结的蒸馏液体即为青蒿素。
1.2 石油醚提取法将青蒿的草杆快速提取,将提取液过滤。
1.2.2 沉淀将过滤后的提取液加入20%氢氧化钠(NaOH)溶液中,反应后沉淀出青蒿素。
将青蒿素加入蒸馏瓶中,进行蒸馏操作,蒸馏后的液体即为纯青蒿素。
1.3 液液萃取法液液萃取法是利用具有选择性的溶剂和青蒿素的分配系数来提取青蒿素的方法。
该方法的主要步骤为制备草杆醚提取物,草杆醚提取物和苦苣酮的混合萃取,分离青蒿素并回收溶剂。
1.3.2 溶剂的配制以苦苣酮作为溶剂,配制出来的苦苣酮溶液用于提取青蒿素。
将草杆醚提取物和苦苣酮混合,加入适量的NaOH,通过搅拌,分离出青蒿素。
利用蒸馏方法,回收苦苣酮溶液。
优点:(1)提取效率高,可以快速提取出青蒿素。
(2)生产效率高,生产效率可达到500克/小时。
(3)不受天气和季节的影响,可以全年不断地进行青蒿素的提取。
(1)使用乙醇会导致环境污染,对环境造成影响。
(2)提取成本难以控制,与乙醇价格的波动有关。
(3)存在挥发后青蒿素含量较低的问题,影响提取效率。
(2)操作简单,不需要复杂的设备和复杂的操作过程。
(3)石油醚是易于挥发的,能够完全挥发掉提取液中残留的石油醚,减少环境污染的影响。
黄花蒿青蒿素提取分离工艺

青蒿素旳主要功能是抗疟,对鼠疟、猴疟、人疟都 有抗疟作用,对疟原虫红细胞内期滋养体有直接杀 灭作用,对红细胞外期无效。青蒿素可透过血脑屏 障,对凶险旳脑型疟疾有良好急救效果。
青篙素旳抗疟机理与其他抗疟药不同,它旳主要作 用是经过干扰疟原虫旳表膜一线粒体功能,而非干 扰叶酸代谢,从而造成虫体构造全部崩溃。在青篙 素分子构造与其抗疟活性旳关系研究中,最为肯定 旳成果是分子中必须有过氧基团,无过氧基团将失 去活性。过氧基是青篙素分子中关键构造,是抗疟 活性旳决定性原因。
青蒿素旳起源
青蒿素制备大致分为四个途径: (1)青蒿素旳化学合成 以R(+)-香草醛为原料,经十几步合成青蒿素
青蒿素旳起源
(2)青蒿素旳生物合成 涉及经过添加生物合成旳前体来增长青蒿素旳
含量,经过对控制青蒿素合成旳关键酶进行调 控,或者对关键酶控制旳基因进行激活来大幅 度增长青蒿素旳含量;利用基因工程手段 来变 化关键基因以增长它们所控制酶旳效率。
黄花蒿中青蒿素旳提取
目旳和意义
1、了解青蒿素是植物黄花蒿旳提取物, 是治疗疟疾旳一种特效药物。 2、掌握用石油醚提取黄花蒿旳措施。
青蒿素理化性质及药用价值简介
青蒿素(artemisinin)是从黄花蒿(Artemisia annua L.)及其变种大头黄花蒿中提取 旳一种倍半萜内酯过氧化物。
青蒿素旳物理性质
迟发型子孢子经过休眠后,在肝细胞内增殖,释 放裂殖子入血,即造成疟疾旳复发。
恶性疟疾无复发,是因为恶性疟疾子孢子无休眠 期。
红细胞内期:裂殖子侵入红细胞内,早期似戒指 状,红色旳核点,兰色环状旳胞浆。称为环状体 即小滋养体。
环状体发育长大,胞浆可伸出不规则旳伪足,以 摄噬血红蛋白,此为阿米巴滋养体或大滋养体。
青蒿素的提取

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载青蒿素的提取地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容青蒿素的提取工艺比较班级:制药工程111班姓名:黎健玲【摘要】青蒿素是从青蒿中提取的一种抗疟疾的有效成分,本文从青蒿中提取青蒿素的一些提取工艺,通过比较的方法,对青蒿中青蒿素的提取工艺进行了综述,讨论了青蒿素提取工艺的研究方向。
关键词:青蒿素;工艺提取;方法比较青蒿素( artemisinin) 又名黄蒿素,是从一年生菊科( As-teraceae) 艾属草本植物黄花蒿( Artemisia annua L. ) 中提取分离得到的一种化合物,于20 世纪 70 年代初首次由中国学者从黄花蒿中分离得到,是目前世界上公认的最有效治疗脑型疟疾和抗氯喹恶性疟疾的药物,且青蒿素联合治疗已成为世界卫生组织( World Health Organization WHO) 推荐的治疗疟疾的首选方法。
药理研究证实,青蒿素除具有抗疟作用外,还具有抗孕、抗纤维化、抗血吸虫、抗弓形虫、抗心律失常和肿瘤细胞毒性抑制瘢痕成纤维细胞、抗单纯疱疹病毒等作用,在现代临床上用于对恶性疟疾、发热、血吸虫病、口腔黏膜扁平苔藓、红斑狼疮、心律失常的治疗,并且对类风湿性关节炎的免疫有显著疗效,青蒿素及其衍生物是新型抗疟药,具有高效、快速、低毒、安全等特点。
1 青蒿素理化性质及来源青蒿素为无色针状结晶,溶点为 156 ~157 ℃,易溶于氯仿、丙酮、乙酸乙酯和苯,可溶于乙醇、乙醚,微溶于冷石油醚,几乎不溶于水,因其具有特殊的过氧基团,所以对热不稳定,易受湿、热和还原性物质的影响而分解。
青蒿素的分子式为 C15H22O5相对分子质量为 282.33,是一种含有过氧桥结构的新型倍半萜内酯,有一个包括过氧化物在内的 1,2,4-三噁烷结构单元,其中包括 7个手性中心。
青蒿素的合成路线

课题名称青蒿素的合成学生姓名学号一、前言 (3)二、路线设计(逆合成分析) (4)1、逆合成分析一: (4)2、逆合成分析二: (4)3、逆合成分析三: (4)4、逆合成分析四: (5)三、合成路线分析选择 (6)1、路线一 (6)2、路线二 (6)3、路线三 (7)4、路线四 (8)四、合成步骤 (9)五、总结 (11)六、参考文献 (12)青蒿素是我国学者在20世纪70年代初从药用植物黄花蒿中分离得到的抗疟有效成分,是含内过氧基团的倍半萜内酯化合物,是目前世界上最有效的治疗脑型疟疾和抗氯喹恶性疟疾的药物,由于具有速效和低毒的特点,已成为世界卫生组织推荐的治疗疟疾的首选药物。
近年来发现青蒿素除具有抗疟作用外,还有多种其他的药理作用,包括抗细菌脓毒症、放疗增敏、抗菌增敏、抗肿瘤等作用。
青蒿素的化学结构:目前药用青蒿素是从中药青蒿即植物黄花蒿的叶和花蕾中分离获得的,由于青蒿的采购、收获,直至工厂加工提取,环节较多,费时费力,而且不同采集地和不同采集期青蒿品质有很大差别。
同时,大量采集自然资源,必然会破坏环境和生态平衡,导致资源枯竭。
因此对青蒿素进行化学全合成研究,具有重要的经济和社会意义。
目前,青蒿素化学合成有全合成和半合成2种,全合成的原料主要是廉价易得的香茅醛(citronellal)、柠檬烯(isolimonene)、薄荷酮( pulegone)、β-蒎烯(β-pinene)、异胡薄荷醇(isopulegol)等,半合成原料主要是青蒿酸。
全合成原料:半合成原料:二、路线设计(逆合成分析)1、逆合成分析一:此路线是以香茅醛为原料进行合成青蒿素。
2、逆合成分析二:此路线是以异胡薄荷醇为原料进行合成青蒿素。
3、逆合成分析三:此路线是以环己烯酮为原料进行合成青蒿素。
4、逆合成分析四:此路线是以青蒿酸为原料半合成法来合成青蒿素。
三、合成路线分析选择1、路线一此方法是2010年Yadav等以香茅醛为原料的全合成路线,该路线通过脯氨酸衍生物和3,4-二羟基苯甲酸乙酯共催化的香茅醛和甲基乙烯基甲酮( MVK)的1,4 -不对称加成合成中间体2,随后经分子内羟醛缩合可得到不饱和醛酮中间体3。
青蒿素提取工艺

青蒿素提取工艺一、基本释义青蒿素英文别名Arteannuin、Artemisinine、Qinghaosu;熔点156-157℃ ( 水煎后分解);MDL号MFCD00081057;青蒿素分子式为C15H22O5,分子量282.33,组分含量:C 63.81%,H 7.85%,O 28.33%。
青蒿素是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物。
其对鼠疟原虫红内期超微结构的影响,主要是疟原虫膜系结构的改变,该药首先作用于食物泡膜、表膜、线粒体,内质网,此外对核内染色质也有一定的影响。
提示青蒿素的作用方式主要是干扰表膜-线粒体的功能。
可能是青蒿素作用于食物泡膜,从而阻断了营养摄取的最早阶段,使疟原虫较快出现氨基酸饥饿,迅速形成自噬泡,并不断排出虫体外,使疟原虫损失大量胞浆而死亡。
体外培养的恶性疟原虫对氚标记的异亮氨酸的摄入情况也显示其起始作用方式可能是抑制原虫蛋白合成。
二、提取工艺从青蒿中提取青蒿素的方法是以萃取原理为基础,主要有乙醚浸提法和溶剂汽油浸提法。
挥发油主要采用水蒸汽蒸馏提取,减压蒸馏分离,其工艺为:投料-加水-蒸馏-冷却-油水分离-精油;非挥发性成分主要采用有机溶剂提取,柱层析及重结晶分离,基本工艺为:干燥-破碎-浸泡、萃取(反复进行)-浓缩提取液-粗品-精制。
1、化学合成半合成路线:从青蒿酸为原料出发,经过五步反应得到青蒿素,总得率约为35~50%。
第一步:青蒿酸在重氮甲烷/碘甲烷/酸催化下与甲醇反应,再在氯化镍存在的条件下,被硼氢化钠选择性还原得到二氢青蒿酸甲酯;第二步:二氢青蒿酸甲酯在四氢呋喃或乙醚溶液中用氢化铝锂还原成青蒿醇;第三步:青蒿醇在甲醇/二氯甲烷/氯仿/四氯化碳溶液中被臭氧氧化后得到过氧化物,抽干后再在二甲苯中用对甲苯磺酸处理得到环状烯醚;第四步:环状烯醚溶解于溶剂中,在光敏剂玫瑰红/亚甲基蓝/竹红菌素等存在下进行光氧化合生成二氧四环中间体,再用酸处理得到脱羧青蒿素;第五步:脱羧青蒿素在四氧化钌氧化体系或铬酸类氧化剂的作用下氧化得到青蒿素。
青蒿素2
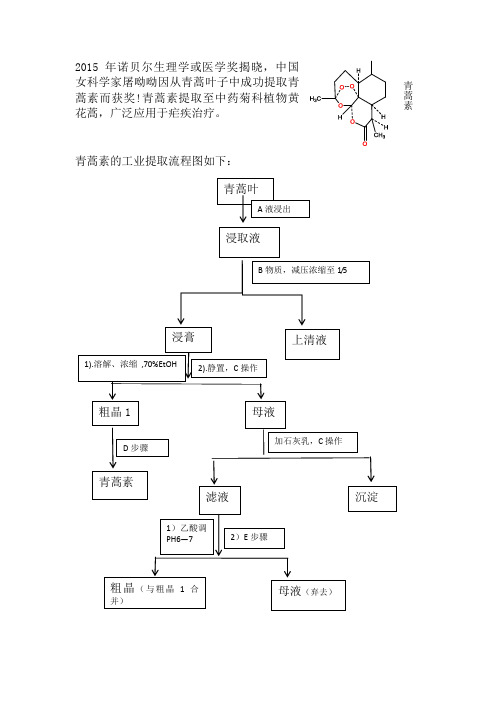
2015年诺贝尔生理学或医学奖揭晓,中国
女科学家屠呦呦因从青蒿叶子中成功提取青Array蒿素而获奖!青蒿素提取至中药菊科植物黄
花蒿,广泛应用于疟疾治疗。
青蒿素的工业提取流程图如下:
请回答下列问题:
1.青蒿素的分子式_______,可溶于氯仿,具有______性;
2.青蒿素的浸出在85%的A 液中最佳,A 的相对分子质量为46,可与金属钠反应,试写出A 与钠反应的化学方程式__________
3.青蒿素的浸取液具有颜色,请问B 是_______,作用是_______
4.C 操作是________,D 步骤是________,E 步骤是________
5.蒿甲醚(C 16H 25O 5)是一种抗疟疾作用为青蒿素的10—20倍的物质,其合成路线如下:
青蒿素被NaBH 4还原成X
X →Y
的反应方程式_______________
6.青蒿素的提取过程中还可以得到青蒿酸(C
15H 22O 2),结构如下:
青蒿酸可发生如下反应:
K 的分子式为C 15H 22
O 3,具有三个六元环,
能与金属钠发生反应生成氢气,试写出 J →K 的化学反应方程式______________
试题内容与课标要求一致性评价
试题内容认知层次与课标认知层次
试题内容认知层
次比率与课标认知层次比率
注:X 代表课标认知层次,Y 代表试题内容认知层次。
表中数字代表按试题内容或课标要求进行编码赋分的值。
因为:
故求得P=0.909,由此可知所出试题与课标内容一致性较好。
青蒿素的化学全合成.总结

青蒿素的合成与研究进展摘要:青蒿素是目前世界上最有效的治疗疟疾的药物之一,存在活性好、毒副作用小、市场需求大、来源窄等特点。
目前,青蒿素的获取途径主要有直接从青蒿中提取、化学合成和生物合成。
本综述将针对近年来青蒿素的发展特点及合成方法进行论述。
关键词:青蒿素;合成方法;研究进展青蒿素是中国学者在20世纪70年代初从中药黄花蒿(Artem isia annua L1 )中分离得到的抗疟有效单体化合物,是目前世界上最有效的治疗脑型疟疾和抗氯喹恶性疟疾的药物, 对恶性疟、间日疟都有效,可用于凶险型疟疾的抢救和抗氯喹病例的治疗.青蒿素还具有抑制淋巴细胞的增殖和细胞毒性的用1;具有影响人体白血病U937细胞的凋亡及分化的作用2;还具有部分逆转MCF-7/ARD细胞耐药性作用3;还具有抑制人胃癌裸鼠移植瘤的生长的作用4;还具有一定的抗肿瘤作用5等.除此之外,青蒿素及其衍生物还具有生物抗炎免疫作用、生物抗肿瘤作用、抑制神经母细胞瘤细胞增殖的作用等。
世界卫生组织确定为治疗疟疾的首选药物,具有快速、高效、和低毒副作用的特征.6。
因在发现青蒿素过程中的杰出贡献,屠呦呦先后被授予2011年度拉斯克临床医学研究奖和2015年诺贝尔医学奖.1 青蒿素的理化性质及来源青蒿素的分子式为C15H22O5, 相对分子质量为282。
33.是一种含有过氧桥结构的新型倍半萜内酯,有一个包括过氧化物在内的1,2,4-三烷结构单元,它的分子中还包括7个手性中心,合成难度很大.中国科学院有机所经过研究,解决了架设过氧桥难题,在1983年完成了青蒿素的全合成.青蒿素也有一些缺点,如在水和油中的溶解度比较小,不能制成针剂使用等。
2青蒿中提取青蒿素青蒿素是从菊科植物黄花蒿中提取出来的含有过氧桥的倍半萜内酯类化合物,在治疗疟疾方面具有起效快、疗效好、使用安全等特点。
目前主要的提取方法有溶剂提取法、超临界提取法、超声波萃取法、微波萃取法、其他萃取法等。
青蒿素

青蒿素工业化生产流程
青蒿素
• 青蒿素是从复合花序植物黄花蒿中提取得到的一种无色针 状晶体,化学名称为(3R,5aS,6R,8aS,9R,12S,12aR)-八氢3,6,9-三甲基-3,12-桥氧-12H-吡喃〔4,3-j〕-1,2-苯并二塞-10 (3H)-酮。分子式为C15H22O5。是继乙氨嘧啶、氯喹、 伯喹之后最有效的抗疟特效药,尤其是对于脑型疟疾和抗 氯喹疟疾,具有速效和低毒的特点,曾被世界卫生组织称 做是“世界上唯一有效的疟疾治疗药物”。抗疟疾作用机 理主要在于在治疗疟疾的过程通过青蒿素活化产生自由基, 自由基与疟原蛋白结合,作用于疟原虫的膜系结构,使其 泡膜、核膜以及质膜均遭到破坏,线粒体肿胀,内外膜脱 落,从而对疟原虫的细胞结构及其功能造成破坏。根据世 卫组织的统计数据,自2000年起,撒哈拉以南非洲地区约 2.4亿人口受益于青蒿素联合疗法,约150万人因该疗法避 免了疟疾导致的死亡。因此,很多统→高压泵 →萃取釜 →分离器(分离 器Ⅰ和分离器 Ⅱ) → 冷却系统(循环)黄花蒿草经粉碎筛 分后装入萃取器。从钢瓶出来的CO2冷却成液态,再由高 压泵压缩后进入缓冲罐,经预热器进入萃取器,与原料黄 花蒿进行接触和传质,溶有溶质的超临界CO2经两级预 热、两级减压后进入分离器Ⅰ 和分离器Ⅱ。从分离器 Ⅱ 顶部出来的CO2 (约为5 MPa)经冷却系统循环使用。预 热器、 萃取器和分离器温度均由恒温水浴控制恒定温度。
材料与方法
• 原料:黄花蒿全草 ,自然晒干,粉碎、筛分 40~60 目和 60~ 80 目 ,石油醚索氏抽提法测得青蒿素质量分数为 0.487 % ,按中 国药典(2000)标准烘干法测得水的质量分数为 11.3 % ,湖南华 立(吉首) 青蒿素制药有限公司生产青蒿素标样 ,纯度 99.8 % ; CO2,纯度≥99.9 % ,含水率≤0.02 %无异味 。 • 器材 :HA121O 50O 01 型超临界萃取装置 ,萃取器容积 1 L ,设 计压力 50 MPa 两级分离器容积均为0. 6 L ,设计压力 30 MPa , 最高操作温度 75℃,最大体积流量 50 L/ h 。
青蒿素的合成生物学研究进展

青蒿素的合成生物学研究进展一、本文概述青蒿素,源自菊科植物青蒿(Artemisia annua L.),是一种具有显著抗疟活性的天然产物,自20世纪70年代被发现以来,已成为全球抗击疟疾的重要武器。
然而,青蒿素的天然来源有限,化学合成成本高昂,且存在环境污染等问题,这使得青蒿素的可持续供应面临挑战。
近年来,随着合成生物学的发展,利用合成生物学方法生产青蒿素成为研究热点。
本文将对青蒿素的合成生物学研究进展进行全面概述,探讨如何利用合成生物学技术提高青蒿素的产量、优化生产过程,以及面临的挑战和未来的发展方向。
本文首先回顾了青蒿素的研究历程和其在全球抗击疟疾中的作用,指出合成生物学在青蒿素生产中的潜在价值和重要性。
随后,综述了目前青蒿素合成生物学研究的主要成果,包括青蒿素生物合成途径的解析、关键酶的发现与改造、以及基于代谢工程的青蒿素高产菌株的构建等。
在此基础上,讨论了合成生物学方法在青蒿素生产中的优势与挑战,如提高青蒿素产量的同时保持其生物活性、优化生产过程的可持续性、以及降低生产成本等。
展望了青蒿素合成生物学研究的未来发展方向,包括利用新兴技术如CRISPR-Cas9基因编辑系统、合成基因组学等进一步提高青蒿素产量和质量,以及推动青蒿素合成生物学技术的产业化应用。
二、青蒿素生物合成途径解析青蒿素是一种具有高效抗疟活性的天然产物,其独特的化学结构和强大的生物活性使其成为全球公共卫生领域关注的焦点。
为了深入理解青蒿素的生物合成机制并进一步提高其产量,科学家们对青蒿素的生物合成途径进行了详尽的解析。
青蒿素的生物合成起始于异戊烯基焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP),这两个分子在甲羟戊酸途径(MVA途径)或2-C-甲基-D-赤藓糖醇4-磷酸途径(MEP途径)中生成。
随后,通过一系列酶促反应,包括预青蒿酸合成酶、青蒿酸合成酶和青蒿素合成酶等,逐步转化为青蒿素的前体物质青蒿酸。
青蒿酸经过青蒿素合成酶的催化,形成青蒿素。
青蒿素的物理提取及胆红素的化学提取

青蒿素的物理提取及胆红素的化学提取天然产物常用的提取方法用如下几种,1.浸渍法:根据溶剂的温度可分为热浸、温浸和冷浸等数种。
2.渗漉法:将中药粗粉装入渗漉筒中,用适当的溶剂润湿膨胀24h~48h,然后不断地添加新溶剂。
煎煮法煮法是我国最早使用的传统的提取方法3.回流提取法:应用有机溶剂加热提取时,需采用回流加热装置,以免溶剂挥发损失。
4.连续提取法:应用挥发性有机溶剂提取天然药物有效成分,不论小型实验或大型生产,均以连续提取法为好,而且需用溶剂量较少,提取成分也较完全。
实验室常用脂肪提取器或称索氏提取器。
物理法提取有机物的有点是操作简单,使用时候方便,快速,节约成本!化学方法的有点是加快反应速度,提取物相比较而言,要纯度更高!但是价格上来讲,要费用高些!在提取纯度更高的有机物,或者量较少的有机物时候,采用化学方法提取,较为适宜!青蒿素的物理提取青蒿素最佳提取工艺研究青蒿素为菊科植物青蒿中的主要活性成分之一,具有抗疟疾作用。
目前由于提取工艺不成熟,提取率较低,导致成本偏高。
从而导致每年有大量的青蒿材料被浪费,为了充分利用资源,我公司组织对青蒿素的提取工艺进行研究验证,为工业化生产探索道路。
该母液中所含杂质主要为低极性成分,故宜选用极性较大且对青蒿素有较好溶解性的溶剂。
根据青蒿素易溶于氯仿、丙酮、乙酸乙酯和苯,可溶于乙醇、乙醚,微溶于冷石油醚,几乎不溶于水的性质,结合文献[5],最终选用有强渗透能力、对青蒿素有较好溶解性、且能与萃取剂建立良好液-液平衡且价廉低毒的乙醇作提取溶剂。
1仪器与试药紫外选用日本岛津紫外分光光度仪;万分之一天平(上海);青蒿素标准品购自中国药品生物制品检定所;青蒿药材购自重庆市酉阳县,有效成份含量为4·15%;所用试剂均为分析纯。
2试验方法与结果2·1提取工艺称取青蒿叶粗粉1 000 g置10 000mL圆底烧瓶中,加5 000 mL的70%乙醇,回流提取4次,每次1 h,趁热滤过, 80℃回收溶剂至约1 000 mL,用乙酸乙酯萃取至完全,萃取液浓缩成浸膏,用70%乙醇热溶,加2·5%活性碳脱色,趁热滤过,回收乙醇至无醇味,静置,得黑色柏油状黏液。
青蒿素的工业生产流程

青蒿素的工业生产流程吉财2013122691青蒿是我国的传统中药,民间用于消暑、退热、治感冒等,青蒿还具有抗疟、抗血吸虫、抗病毒与增强机体免疫等作用。
在我国数百名科学工作者的协作中,从青蒿中提取了它的抗疟有效成分,一种新型倍半萜内酯,后命名为青蒿素,青蒿素为无色针状结晶,分子式为C15H22O5,其结构式如图1,熔点为156-157℃,易溶于氯仿、丙酮、乙酸乙酯和苯,可溶于乙醇、乙醚,微溶于冷石油醚,几乎不溶于水。
因其具有特殊的过氧基团,对热不稳定,易受湿、热和还原性物质的影响而分解[1] 。
国内外大量的理化试验、药理研究和临床应用表明青蒿素是抗疟的有效成分,认为青蒿素的发现是抗疟研究史上的重大突破,并成为世界卫生组织推荐的抗疟药品,特别是对脑型疟疾和抗氯喹性疟疾有很好疗效[2]。
近年来青蒿素的抗疟活性在世界范围内被广泛关注,在疟疾流行地区青蒿素的需求量增加。
此后又发展了一系列现已作为正式抗疟药物的青蒿素的衍生物,此时我国研制的青蒿素类抗疟药物以高效、安全、对抗药性疟疾有特效而风靡全球,1995年蒿甲醚被WTO列入国际药典,这是我国第一个被国际公认的独创新药。
青蒿素的化学结构十分独特,自上市至今20多年,尚未发生抗药性的病例。
1 仪器、试剂与材料50ml圆底烧瓶、回流冷凝管、721型分光光度计(上海分析仪器厂)、分析天平(上海精科天平厂)、微量移液管(上海求精玻璃仪器厂)、电热恒温水浴锅、恒温烘箱、干燥器、柱层析、硅胶薄层板(由青岛海洋化工厂生产,薄层层析板用硅胶G加0.3%CM C-Na制备而成。
显色剂为2%香草醛--浓硫酸(1:1)混合液。
喷雾后,电吹风加热显色)等。
乙醚、乙醇、氢氧化钠、乙酸乙酯、异丙醇、石油醚均为分析纯。
青蒿的原材料及其标准样由海裕药业提供。
2 方法与步骤2.1提取称取100g青蒿叶粉(过30目筛),加入8倍石油醚(800毫升,沸程60—90℃),水浴55℃搅拌回流提取5小时,第二次提取加入6倍石油醚(600毫升,沸程60—90℃),水浴55℃搅拌回流提取3小时,第三次提取加入4倍石油醚(400毫升,沸程60—90℃),水浴55℃搅拌回流提取2小时,得滤液一、二、三,分装,渣子回收尽石油醚重复使用。
青蒿素提取

-1-
因此,针对其母液研究开发青蒿素的提取纯化工艺具有工业价值。
1.5.1 预试实验 称取等量母液 3 份,用 85%乙醇使之完全分散,过滤,滤液分别用含 30%乙酸乙酯的
石油醚、石油醚和乙酸乙酯萃取至醇层在 TLC 检测中显示不出青蒿素斑点。结果发现 30% 乙酸乙酯的石油醚和石油醚的萃取次数相同;石油醚的萃取次数比乙酸乙酯多。
1.5.2 石油醚和乙酸乙酯的萃取效果研究
青蒿素是我国科研人员从青蒿中分离得到的一种全新抗疟有效成分,已在临床应用 30 多年,一直未发现疟原虫对其产生耐药性。“以青蒿素为主的联合疗法”使用 3 天就可见效, 较传统氯喹疗法减少了 4 天的时间[1]。目前,WHO已将青蒿素为基础的联合疗法列为治疗 疟疾的首选方法。
青蒿素虽然已经可以人工全合成,但其成本很高,无法工业化生产。目前,青蒿素的主 要来源仍然是从植物黄花蒿中提取分离。黄花蒿分布较广,但由于产地的不同,所含青蒿素 的差异极大(0.1%-1.3%)其中仅有部分产地(重庆、四川、广西、云南等地)的黄花蒿具 有工业价值。青蒿素原料药的 90%来自中国。
母液 materials
(g)
85%乙醇 85%ethanol
(ml)
活性炭 active carbon
(g)
萃取剂 extracting
solvent
结晶溶剂 crystallizing
solvent
25
225
0.25
PE
PE
25
225
0.25
从黄花蒿中提取青蒿素的工业流程

从黄花蒿中提取青蒿素的工业流程下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!青蒿素是一种重要的抗疟药物,广泛应用于世界各地的疟疾治疗。
工业酒精冷浸法提取青蒿素

工业酒精冷浸法提取青蒿素
李自勇;秦海敏;喻宗沅;尤庆亮;徐小军
【期刊名称】《精细石油化工进展》
【年(卷),期】2008(009)001
【摘要】以青蒿为原料,采用工业酒精冷浸法提取青蒿素.通过实验确定最佳工艺条件为:酒精体积(mL)与青蒿质量(g)比为10:1,分3次提取,母液体积(mL)为青蒿质量(g)的2.5倍,萃取剂乙酸乙酯与母液体积比为1:1,分4次萃取,用活性炭脱色、结晶及重结晶,干燥得白色针状的青蒿素晶体,得到的青蒿素产品产率可达2.73‰,纯度可达99%.该工艺具有操作安全,提取率高,生产成本低,产品含量高的特点.
【总页数】3页(P35-37)
【作者】李自勇;秦海敏;喻宗沅;尤庆亮;徐小军
【作者单位】湖北省化学研究院,武汉,430074;湖北省化学研究院,武汉,430074;湖北省化学研究院,武汉,430074;湖北省化学研究院,武汉,430074;湖北省化学研究院,武汉,430074
【正文语种】中文
【中图分类】TQ46
【相关文献】
1.真空浓缩法与旋转蒸发法提取青蒿素的比较 [J], 张瑜文;谢学立;黄绵佳;李佳潼;吴岚芳
2.蜂胶醇冷浸法提取物中总黄酮含量的测定 [J], 张建和;符伟玉;佘戟
3.冷浸法提取丹参脂溶性部位工艺研究 [J], 林忠泽;刘东辉;关世侠
4.冷浸法提取川乌杀虫活性物质的工艺研究 [J], 许勇华;饶琼;舒少华
5.蓝莓花青素冷浸法的提取研究 [J], 陈婷婷
因版权原因,仅展示原文概要,查看原文内容请购买。
青蒿素合成途径

青蒿素合成途径
青蒿素是一种重要的抗疟药物,其合成途径主要有两种:全合成和半合成。
全合成是指从基本化学品出发,经过多步合成,最终得到青蒿素。
这种方法的优点是可以控制反应条件和产物纯度,但是合成步骤繁琐、成本高昂,不适合大规模生产。
半合成则是利用天然物质青蒿素的结构基础,通过一些改进的反应方法,合成类似青蒿素的化合物。
这种方法的优点在于节约时间和成本,适合产量较大的工业化生产。
目前,半合成途径已成为青蒿素工业生产的主要方法。
通过对青蒿素分子结构的深入研究,不断改进合成方法,可以提高产物纯度和产量,为抗疟药物生产提供更好的支持。
- 1 -。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
青蒿素的工业生产流程
吉财2013122691
青蒿是我国的传统中药,民间用于消暑、退热、治感冒等,青蒿还具有抗疟、抗血吸虫、抗病毒与增强机体免疫等作用。
在我国数百名科学工作者的协作中,从青蒿中提取了它的抗疟有效成分,一种新型倍半萜内酯,后命名为青蒿素,青蒿素为无色针状结晶,分子式为
C15H22O5,其结构式如图1
,熔点为156-157℃,易溶于氯仿、丙酮、乙酸乙酯
和苯,可溶于乙醇、乙醚,微溶于冷石油醚,几乎
不溶于水。
因其具有特殊的过氧基团,对热不稳定,
易受湿、热和还原性物质的影响而分解[1] 。
国内外
大量的理化试验、药理研究和临床应用表明青蒿素
是抗疟的有效成分,认为青蒿素的发现是抗疟研究
史上的重大突破,并成为世界卫生组织推荐的抗疟
药品,特别是对脑型疟疾和抗氯喹性疟疾有很好疗
效[2]。
近年来青蒿素的抗疟活性在世界范围内被广泛关注,在疟疾流行地区青蒿素的需求量增加。
此后又发展了一系列现已作为正式抗疟药物的青蒿素的衍生物,此时我国研制的青蒿素类抗疟药物以高效、安全、对抗药性疟疾有特效而风靡全球,1995年蒿甲醚被WTO列入国际药典,这是我国第一个被国际公认的独创新药。
青蒿素的化学结构十分独特,自上市至今20多年,尚未发生抗药性的病例。
1 仪器、试剂与材料
50ml圆底烧瓶、回流冷凝管、721型分光光度计(上海分析仪器厂)、分析天平(上海精科天平厂)、微量移液管(上海求精玻璃仪器厂)、电热恒温水浴锅、恒温烘箱、干燥器、柱层析、硅胶薄层板(由青岛海洋化工厂生产,薄层层析板用硅胶G加0.3%CM C-Na制备而成。
显色剂为2%香草醛--浓硫酸(1:1)混合液。
喷雾后,电吹风加热显色)等。
乙醚、乙醇、氢氧化钠、乙酸乙酯、异丙醇、石油醚均为分析纯。
青蒿的原材料及其标准样由海裕药业提供。
2 方法与步骤
2.1提取
称取100g青蒿叶粉(过30目筛),加入8倍石油醚(800毫升,沸程60—90℃),水浴55℃搅拌回流提取5小时,第二次提取加入6倍石油醚(600毫升,沸程60—90℃),水浴55℃搅拌回流提取3小时,第三次提取加入4倍石油醚(400毫升,沸程60—90℃),水浴55℃搅拌回流提取2小时,得滤液一、二、三,分装,渣子回收尽石油醚重复使用。
2.2柱层析
2.2.1装柱
2倍原料硅胶(200克100—200目),干法装柱:打开层析柱的下端阀门,在柱的上端入一漏斗,硅胶经漏斗成一细流慢慢均匀地加入柱中,中间不能间断,装好后,柱上端放一层脱脂棉,压紧,填实,用石油醚走通即可上药。
2.2.2上药
将提取滤液按先后次序加入柱中(先加第一次提取滤液),完后用200ml石油醚洗涤。
2.2.3洗脱
洗脱液为石油醚---异丙醇(体积比95:5)混合液。
分段(每100毫升为一段)收集,薄层检测(展开剂为石油醚--乙醚=6:4),收集合格段。
2.3浓缩
先常压浓缩(温度小于70℃)青蒿素段层析液,然后减压再浓缩至有晶体析出为止,静置12小时,过滤得粗晶和母液。
母液再减压浓缩再结晶,合并两次粗晶,剩下母液可与下批一起再上柱。
2.4重结晶
将结晶用90%乙醇60毫升加热(温度小于70℃)溶解,趁热真空抽滤,滤液静置12小时结晶,过滤,母液再减压浓缩再结晶过滤,合并晶体,60℃真空烘干得产品0.40克,收率0.40%。
2.5定性定量测定
2.5.1定性测定:硅胶薄层检测法吸取一定量样品青蒿素溶液,点样于以硅胶G制作的薄板上,在距薄层一端1.5厘米平行线上点7个样品点,间隔9毫米,其中2、6位上点对照样品溶液,采用石油醚(沸程60—90℃):乙醚= 6 :4作展开剂,再挥去溶剂,喷以显色剂2%香草醛—浓硫酸,在80℃箱中烘半小时取出,结果青蒿素的色点由黄变绿再变为海蓝色。
同时可根据海蓝色斑点的深浅和大小与对照品比较,粗略估算与结果一致。
(1)工艺简单,操作容易,周期短,成本底,收率高:
1)所需设备简单,在选溶剂时选用了可回收溶剂—石油醚,它降低成本的同时也保护了环境;
2)目前对青蒿素的提取主要有:水蒸汽蒸馏[3]、有机溶剂萃取[4-6]、超临界流体萃取[7]、微波萃取等方法[8]。
水蒸汽蒸馏法工艺简单,操作容易,周期较长,成本低,但只适用于青蒿中挥发性成分的提取,不能提取青蒿素;有机溶剂法提取青蒿素,工艺路线成熟,操作容易,周期短,成本底,易于工业化;超临界流体萃取和微波萃取周期短,但成本太高,不适用于工业化生产;
3)它与传统的冷提相比增加了加热和搅拌,从而缩短了时间,提高了提取效率。
(2)溶剂---石油醚(沸程60—90℃):在选择溶剂时有乙醚、氯仿、正己烷、石油醚可选,最后选取了石油醚,是因为参照了文献[13 ],氯仿和乙醚在波长200-240nm之间有很强的杂质峰,其中氯仿提取产物中杂质峰最强,乙醚次之,此两种溶剂的杂质峰远远大破碎原料浸泡(石油醚)搅拌、加热(反复进行)合并提取液硅胶柱层析精品粗品浸膏浓缩结晶重结晶于石油醚。
正己烷虽然杂质峰较弱,但提取率较石油醚低。
考虑到乙醚和氯仿的挥发性、刺激性气味和正己烷回收温度较高,超过了60℃,而青蒿素在温度超过60℃以后则过氧桥结构被很快破坏,完全失去药效。
所以4种溶剂中石油醚为较适宜的溶剂。
(3)吸附剂---硅胶:
1)它是应用最广泛的一种吸附剂,化学惰性强,具有较大的吸附量,易制备不同类型、孔径、表面积的多孔硅胶[14];
2)易再生:用600℃的火烧就可以再生,从而节约能源,降低成本。
(4)原料粉碎度---30目:粉碎是天然产物制备过程中的必要环节,可增加原料的表面积,促进有效成分的溶解与传递,加速有效成分的浸出;但过细,原料比表面积太大,吸附作用增强,反而影响扩散速度,同时影响过滤,最终影响提取率[15]。
参考文献
[1]于宗德,孙芳华,青蒿素理化性质及其测定方法的研究进展[J],江西农业大学学报,1999,4:606-611.
[2]陈杨,朱世民,陈洪渊,青蒿素类抗疟研究进展,药学学报,1998,33(3):234-239.
[3] 屠呦呦,药学学报,1981,16(5):366. [4] Vonwiller S C,Planta Med,1993,32(5):59-62.
[5] Klayman D L,J of Nat Prod、2004,47(4):715.
[6] Singh A,.Planra Med,1998,54(6):474.
[7] 葛发欢,中药材,1995,18(6):316.
[8] Xu Zhu J,Huang D Z,et al.Tetrahed ron,1986,42:819-828.
[9] Schmid G,Hofheinz W.J.Am.Chem.Soc.,2005,114:974-979.
[10] MeiXG,Huang W,Wang C G,Production of taxol by two-phase culture Tax us cell suspension[J].Biotechnology(生物技术),2000,10(1):10-12.
[11] Hu P,Yuan Y J, Miao Z Q.Effccts of fed-batch carbohy-drate,nitrogen phosphorus on grow th of Taxus chinensisvar mairei cell during su spension culture[J].Chin Tradit Herb Drugs(中草药),2002,33(1):28-31.
[12] Shen X K,Yan K D,L uo Z Y.Determ of artcm is in content by ultravio let meter[J].Chin Pham A nal(药物分析杂志),1999,3(2):24-26.
[13] 张积强,陈强,青蒿中青蒿素含量的测定,陕西化工1996(3):34-35.
[14] 韦国锋,覃特云,提取青蒿素实验条件的研究,左江民族医学学报,1999,17(2):137.
[15] 李国栋,周全,赵长文,青蒿素类药物的研究现状[J],中国药学杂志,1998,33(7):385.。
