分析化学试题---含答案--期末复习
分析化学期末考试题A及答案

分析化学期末考试题A及答案一、选择题(每题2分,共20分)1. 以下哪种物质不是分析化学中常用的指示剂?A. 酚酞B. 甲基橙C. 硫酸铜D. 酚红答案:C2. 在酸碱滴定中,滴定终点的判断依据是:A. 滴定体积B. 溶液颜色变化C. 滴定速度D. 溶液的pH值答案:B3. 原子吸收光谱法中,待测元素的原子化方式不包括:A. 火焰原子化B. 石墨炉原子化C. 化学原子化D. 电化学原子化答案:C4. 以下哪种仪器不适用于液相色谱分析?A. 紫外检测器B. 荧光检测器C. 质谱仪D. 红外光谱仪答案:D5. 质谱分析中,分子离子峰通常指的是:A. 最大质量的离子峰B. 质量最小的离子峰C. 质量比最大的离子峰D. 质量比最小的离子峰答案:A二、填空题(每题2分,共20分)1. 在紫外-可见光谱分析中,______是分子吸收紫外光或可见光后,分子内部电子跃迁到高能级轨道的过程。
答案:电子跃迁2. 色谱分析中,______是指固定相与移动相之间的相互作用。
答案:色谱保留3. 原子吸收光谱分析中,______是指样品中待测元素的原子化效率。
答案:原子化效率4. 电位滴定法中,______是指溶液中待测离子的活度。
答案:活度5. 质谱分析中,______是指分子离子峰的质荷比。
答案:分子离子峰的质荷比三、简答题(每题10分,共30分)1. 简述高效液相色谱(HPLC)与薄层色谱(TLC)的主要区别。
答案:高效液相色谱(HPLC)与薄层色谱(TLC)的主要区别在于:(1)HPLC使用高压泵推动流动相通过柱子,而TLC使用毛细作用力使溶剂上升。
(2)HPLC的分离效率和速度通常高于TLC。
(3)HPLC可以连接多种检测器进行定量分析,而TLC通常用于定性分析。
2. 解释什么是标准溶液,并说明其在分析化学中的重要性。
答案:标准溶液是指已知准确浓度的溶液,通常用于校准仪器或作为分析过程中的参照物。
在分析化学中,标准溶液的重要性在于:(1)提供准确浓度的参照,确保分析结果的准确性。
(完整)分析化学期末试题及参考答案

分析化学期末试题班级 学号 姓名一、单项选择题(15分,每小题1分)1、在以EDTA 为滴定剂的络合滴定中,都能降低主反应能力的一组副反应系数为( A )。
A 、αY (H ), αY (N ),αM (L );B 、αY (H ), αY(N),αMY ;C 、αY (N ), αM (L),αMY ;D 、αY (H ),αM(L ),αMY 。
2、在EDTA 络合滴定中,使滴定突跃增大的一组因素是( B ). A 、C M 大,αY(H )小,αM(L)大,K MY 小; B 、C M 大,αM (L)小,K MY 大,αY(H) 小; C 、C M 大,αY(H )大, K MY 小,αM (L)小; D 、αY(H )小,αM (L)大,K MY 大,C M 小;3、以EDTA 为滴定剂,下列叙述错误的是( D )。
A 、在酸度较高的溶液中,可形成MHY 络合物。
B 、在碱性较高的溶液中,可形成MOHY 络合物。
C 、不论形成MHY 或MOHY ,滴定反应进行的程度都将增大。
D 、不论溶液pH 值的大小,只形成MY 一种形式络合物。
4、在络合滴定中,有时出现指示剂的“封闭”现象,其原因为( D ). (M :待测离子;N:干扰离子;In :指示剂)A 、''NY MY K K >;B 、''NYMY K K <;C 、''MY MIn K K >;D 、''MYNIn K K >. 5、在用EDTA 测定Ca 2+、Mg 2+的含量时,消除少量Fe 3+、Al 3+干扰的下述方法中,哪一种是正确的( C )。
A 、于pH=10的氨性缓冲溶液中直接加入三乙醇胺;B 、于酸性溶液中加入KCN,然后调至pH=10;C 、于酸性溶液中加入三乙醇胺,然后调至pH=10的氨性溶液;D 、加入三乙醇胺时,不需要考虑溶液的酸碱性.6、在1 mol ·L -1HCl 介质中,滴定Fe 2+ 最好的氧化—还原方法是( B )。
分析化学总复习题及答案

分析化学复习题答案一、名词解释1.分析结果与真实值接近的程度,其大小可用误差表示。
2.平行测量的各测量值之间互相接近的程度,其大小可用偏差表示。
3.是由某种确定的原因所引起的误差,一般有固定的方向(正负)和大小,重复测定时重复出现。
包括方法误差、仪器或试剂误差及操作误差三种。
4.是由某些偶然因素所引起的误差,其大小和正负均不固定。
5.是指在分析工作中实际上能测量到的数字。
通常包括全部准确值和最末一位欠准值(有±1个单位的误差)。
6.指少量测量数据平均值的概率误差分布。
可采用t分布对有限测量数据进行统计处理。
7.用于判断某一分析方法或操作过程中是否存在较大的系统误差和偶然误差的检验。
包括t 检验和F检验。
8.滴定剂的量与被测物质的量正好符合化学反应式所表示的计量关系的一点。
9.滴定终止(指示剂改变颜色)的一点。
10.滴定终点与化学计量点不完全一致所造成的相对误差。
可用林邦误差公式计算。
11.描述滴定过程中溶液浓度或其相关参数随加入的滴定剂体积而变化的曲线。
12.在化学计量点前后±0.1%,溶液浓度及其相关参数发生的急剧变化为滴定突跃。
13.滴定分析中通过其颜色变化来指示化学计量点到达的试剂。
有两种不同颜色的存在型体。
14.浓度准确已知的试剂溶液,常用作滴定剂。
15.可用于直接配制或标定标准溶液的物质。
16.以滴定过程中溶液pH值的变化对滴定体积(或滴定百分数)作图而得的曲线。
17.化学计量点附近(±0.1%)pH的突变。
18.滴定终点与化学计量点不一致引起的误差,与指示剂的选择有关。
19.能给出质子或接受质子的溶剂。
包括酸性溶剂、碱性溶剂和两性溶剂。
20.为一定温度时金属离子与EDTA配合物的形成常数,以K MY表示,此值越大,配合物越稳定。
21.一种能与金属离子生成有色配合物的有机染料显色剂,来指示滴定过程中金属离子浓度的变化。
22.某些金属离子与指示剂生成极稳定的配合物,过量的EDTA不能将其从MIn中夺取出来,以致于在计量点附近指示剂也不变色或变色不敏锐的现象。
《分析化学》期末考试试卷附答案

《分析化学》期末考试试卷附答案一、填空题(每空2分,共40分)1.测定一物质中某组分的含量,测定结果为(%):59.82,60.06,59.86,60.24。
则平均偏差为;相对平均偏差为;标准偏差为;相对标准偏差为;置信区间为(18.33,05.0t)2.系统误差的减免是采用标准方法与所用方法进行比较、校正仪器及做试验和试验等方法减免,而偶然误差则是采用的办法减小。
3.有一磷酸盐混合溶液,今用标准盐酸滴定至酚酞终点时耗去酸的体积为V1;继续以甲基橙为指示剂时又耗去酸的体积为V2。
当V1=V2时,组成为;当V1<V2时,组成为。
(V1>0,V2>0)4.NH4CN质子条件为5.在含有Ca2+、Ag2+混合溶液中,在pH=12条件下,用EDTA标准溶液滴定其中的Ca2+。
加入三乙醇胺的作用是,加入NaOH的作用是。
6.某有色溶液,当液层厚度为1cm时,透过光强度为入射光强的80%。
若通过5cm的液层时,光强度将减弱%。
7.强碱滴定弱酸的滴定曲线中,滴定突跃的大小与和有关。
8.当电流等于扩散电流一半时,滴汞电极的电位称为。
不同离子在不同介质中具有特征值,是极谱分析的基础。
9.组分分子从气相到气-液界面进行质量交换所遇到的阻力,称为。
10.分子的外层电子在化学能的作用下使分子处于激发态,再以无辐射弛豫转入第一电子激发态的最低振动能级,然后跃迁回基态的各个振动能级,并产生辐射。
这种发光现象称为。
二、选择题(每题3分,共30分)1.下列有关随机误差的论述中不正确的是()A.随机误差是由一些不确定的偶然因素造成的;B.随机误差出现正误差和负误差的机会均等;C.随机误差在分析中是不可避免的;D.随机误差具有单向性2.下列各酸碱对中,属于共轭酸碱对的是()A.H2CO3——CO32-B.H3O+——OH—C.HPO42-——PO43-D.NH3+CH2COOH——NH2CH2COO—3.已知H3PO4的pK a1=2.12,pK a2=7.20, pK a3=12.36,若用NaOH滴定H3PO4,则第二个化学计量点的pH值约为()A.10.7 B.9.7 C.7.7 D.4.94.EDTA与金属离子形成螯合物时,其螯合比一般为()A.1:1 B.1:5 C.1:6 D.1:45.用异烟酸-吡唑酮作显色剂可测定水中CN-的含量。
2024年6月份考试 1238分析化学期末复习题

1238 分析化学复习题1、银量法中,以铁铵矾作指示剂,用NH4SCN为标准溶液滴定溶液中的Ag+,称为()法。
A、莫尔B、佛尔哈德C、碘D、法扬斯答案: B2、各次测定值与平均值之差称为()。
A、误差B、公差C、相对偏差D、偏差答案: D3、配制1mol ·L-1 NaOH溶液500ml,应称取()g固体NaOH。
A、 2B、 5C、10D、 20答案: D4、将2.4374修约为四位有效数字是()。
A、 2.437B、 2.438C、 2.43D、 2.436答案: A5、从1L1mol ·L-1的NaOH溶液中取出100mL,取出的溶液中NaOH的物质的量浓度是多少 mol ·L-1? ()A、 0.5B、 1C、 1.5D、 2答案: BA、称量瓶B、容量瓶C、锥形瓶D、安瓿答案: A7、进行有危险性的工作应()。
A、穿戴工作服B、戴手套C、有第二者陪伴D、自己独立完成答案: C8、在进行容量仪器的矫正时所用的标准温度是()℃。
A、 15B、 20C、18D、 19答案: B9、滴定管在记录读数时,小数点后应保留()位。
A、 1B、 2C、 3D、 4答案: B10、下面不宜加热的仪器是()。
A、试管B、坩埚C、蒸发皿D、移液管答案: D11、现需要配制0.1000mol/L KCl溶液,下列仪器中最合适的量器是()。
A、容量瓶B、量筒C、刻度烧杯D、酸式滴定管答案: AA、眼睛看着滴定管中液面下降的位置B、眼睛注视滴定管流速C、眼睛注视滴定管是否漏液D、眼睛注视被滴定溶液颜色的变化答案: D13、放出移液管中的溶液时,当液面下降至管尖后,应等待()以上。
A、 5sB、10sC、15sD、 20s答案: C14、制作馒头时,需加入面碱(主要含碳酸钠),如果面碱放多了,蒸出的馒头会发黄,且口感不好。
为除去过多的面碱,做馒头时可加入适量的()。
A、食醋B、食盐C、料酒D、味精答案: A15、下列关于浓硫酸的描述错误的是()。
分析化学题库+参考答案

分析化学题库+参考答案一、单选题(共100题,每题1分,共100分)1.一般情况下,EDTA与金属离子形成的配位化合物的配位比是A、1∶1B、2∶1C、3∶1D、1∶2正确答案:A2.明矾中铝含量的测定应选用()A、EDTA滴定法B、沉淀滴定法C、两者均可用D、两者均不可用正确答案:A3.不属于仪器分析法的特点是()A、灵敏B、快速C、准确D、适合于常量分析E、适用于微量分析正确答案:D4.下列是四位有效数字的是()A、1.00B、1.005C、1.1050D、pH=12.00E、2.1000正确答案:B5.物质的量浓度相同,体积也相同的一元酸和一元碱恰好中和时,溶液A、显酸性B、显碱性C、显中性D、无法确定E、以上均不是正确答案:D6.直接碘量法不能在下列条件下测定()A、中性B、酸性C、弱碱性D、加热正确答案:D7.钙、锌等离子含量的测定应选用()A、EDTA滴定法B、沉淀滴定法C、两者均可用D、两者均不可用正确答案:A8.溴甲酚绿-甲基红指示剂与酚酞指示剂比较具有的特点()A、变色敏锐B、变色范围窄C、两者均是D、两者均不是正确答案:C9.能够用于沉淀滴定的沉淀反应不需要符合的条件是()A、沉淀反应必须能迅速定量完成B、生成的沉淀溶解度必须足够小C、必须有沉淀生成D、必须有适当的指示化学计量点的方法E、必须用AgNO3作滴定液正确答案:E10.用于准确移取一定体积溶液的量器()A、移液管B、滴定管C、量瓶D、锥形瓶E、试剂瓶正确答案:A11.下列哪一种酸只能用非水酸碱滴定A、HCOOH(Ka=1.77×10-4)B、HAc(Ka=1.76×10-5)C、H3BO3(Ka=7.3×10-10)D、苯甲酸(Ka=6.46×10-5)正确答案:C12.下列哪种误差属于操作误差()A、操作人员看错砝面值B、操作者对终点颜色的变化辨别不够敏锐C、加错试剂D、溶液溅失E、用银量法测定氯化物时,滴定时没有充分振摇使终点提前正确答案:B13.减小偶然误差在方法A、多次测量取平均值B、回收实验C、空白试验D、对照试验正确答案:A14.在用HCl滴定液滴定NaOH溶液时,记录消耗HCl溶液的体积正确的是()A、24.100mIB、24.1mlC、24.1000mlD、24.10mlE、24ml正确答案:D15.间接碘量法中用基准物质标定Na2S2O3溶液时,要加入过量的KI,对KI的作用理解不正确的是()A、增大析出I2的溶解度B、作为还原性C、防止I2的挥发D、使反应快速、完全E、作为氧化剂正确答案:E16.下列物质中,可以用氧化还原滴定法测定含量的物质是()A、醋酸B、盐酸C、硫酸D、草酸正确答案:D17.在银量法中要用到的基准物质是()A、Na2CO3B、邻苯二甲酸氢钾C、NaClD、硼砂E、ZnO正确答案:C18.将4克氢氧化钠溶于水中,制成1升溶液,其物质的量为A、4克B、0.1摩尔C、0.1摩尔/升D、1摩尔正确答案:B19.直接碘量法适宜的酸碱度条件是A、弱酸性B、中性C、弱碱性D、强碱性E、A+B+C正确答案:E20.在滴定分析中,对滴定液的要求有:A、准确的浓度B、无色C、性质稳定D、无氧化性E、A+C正确答案:E21.在标定HCL溶液浓度时,某同学4次测定结果分别为0.1018mol/L.0.1017mol/L.0.1018mol/L.0.1019mol/L,而准确浓度为0.1036mol/L,该同学的测量结果为()A、准确度较好,但精确度较差B、准确度较好,精确度也好C、准确度较差,但精确度较好D、准确度较差,精确度较差正确答案:C22.用ZnO标定EDTA溶液浓度时,以EBT作指示剂调解溶液酸度应用()A、六次甲基四安B、氨水C、NH3-NH4ClD、A+BE、B+C正确答案:E23.间接碘量法滴定时的酸度条件为()A、中性或弱酸性B、强碱性C、弱碱性D、强酸性E、弱酸性正确答案:A24.可用来标定NaOH滴定液的基准物是A、邻苯二甲酸氢钾B、硼砂C、无水碳酸钠D、草酸钠E、甲酸正确答案:A25.影响氧化还原反应平衡常数的因素是A、反应物浓度B、温度C、催化剂D、反应产物浓度E、以上均不是正确答案:B26.用 Na2C2O4(A)标定 KMnO4(B)时,其反应系数之间的关系为:A、nA = 5/2 nBB、nA = 2/5 nBC、nA = 1/2 nBD、nA = 1/5 nBE、以上均不是正确答案:A27.影响消耗滴定液的量()A、溶液的浓度B、沉淀的溶解度C、两者都有关D、两者都无关正确答案:A28.用酸碱滴定法测定醋酸的含量()A、超微量分析B、常量分析C、半微量分析D、微量分析E、电位分析正确答案:B29.间接碘量法中,滴定至终点的溶液放置后(5min内)又变为蓝色的原因是()A、空气中氧的作用B、溶液中淀粉过C、KI加量太少D、反应速度太慢E、待测物与KI反应不完全正确答案:E30.在定性化学分析中一般采用()A、常量分析B、仪器分析C、化学分析D、微量分析E、半微量分析正确答案:A31.酸,碱的强度越大()A、ka小于或等于10-7B、间接法配制C、cka³10-8D、Ka>10-7E、突越范围越大正确答案:E32.对直接碘量法与间接碘量法的不同之处描述错误有()A、指示剂不同B、终点的颜色不相同C、加入指示剂的时间不同D、滴定液不同正确答案:A33.AgNO3应储存在A、棕色试剂瓶B、白色容量瓶C、白色试剂瓶D、棕色滴定管正确答案:A34.用基准物质邻苯二甲酸氢钾标定NaOH溶液的浓度,选用的指示剂()A、甲基橙B、酚酞C、两者均可D、两者均不可正确答案:B35.用0.1000mol/LHCl溶液滴定25.00mlNaOH,终点消耗20.00ml,则NaOH溶液的浓度为()A、0.1000mol/LB、0.1250mol/LC、0.08000mol/LD、1.000mol/LE、0.08mol/L正确答案:C36.非水碱量法常用的溶剂是A、醋酐B、稀醋酸C、水D、无水乙醇E、冰醋酸正确答案:E37.提高分析结果准确度的主要方法不包括()A、增加平行测定次数B、减小测量误差C、消除偶然误差D、消除系统误差E、增加有效数字的位数正确答案:E38.下列属于碱性溶剂的是()A、乙二胺B、乙醇C、水D、苯E、乙酸正确答案:A39.提高氧化还原反应的速度可采取()措施。
分析化学(期末考试及答案)

分析化学(答案在最后一页)一、单选题1.有些指示剂可导致EDTA与MIn之间的置换反应缓慢终点拖长,这属于指示剂的()(A)僵化现象(B)封闭现象(C)氧化变质现象(D)其它现象2.在pH为4.42的水溶液中,EDTA存在的主要型体是()(A)H4Y (B)H3Y-(C)H2Y23. 用双指示剂法测某碱样时,若V1<V2,则组成为()(A) NaOH+Na2CO3 (B)Na2CO3(C) NaOH (D)Na2CO3+NaHCO34.酸碱滴定法选择指示剂时可以不考虑的因素是()(A)指示剂的颜色变化(B)指示剂的变色范围(C)指示剂相对分子量的大小(D) 滴定突跃范围5.某弱碱HA的Ka=1.0x10-5,其0.10mol--1溶液的pH值为()(A) 3.00 (B) 5.00 (C) 9.006. 在分光光度分析中,用1cm的比色皿测得某一浓度溶液的透光率为T,若浓度增加一倍,透光率为()(A)T2 (B)T/2 (C) 2T (D)√T7.示差分光光度法所测吸光度相当于普通光度法中的()(A)Ax (B) As (C)As-Ax (D)Ax-As8.测定铁矿石铁含量时,若沉淀剂为Fe(OH)3.称量形为Fe2O3,以Fe3O4表示分析结果,其换算因数是()(A)M Fe3O4M Fe2O3(B)M Fe3O4M Fe(OH)3(C) 2M Fe3O43M Fe2O39.用BaSO4沉淀法测S2-时,有Na2SO4共沉淀,测定结果()(A)偏低(B)偏高(C) 无影响(D)无法确定10.以K2CrO4为指示剂测定Cl-时应控制的酸度为()(A)PH为11-13 (B)PH为6.5-10.0(C) PH为4-6 (D)PH为1-311.pH=10.36的有效数字位数是()(A)四位(B)三位(C) 两位(D)一位12.下列四种离子中,不适于用莫尔法,以AgNO3溶液直接滴定的是()(A)Br-(B) CI-(C)CN-(D)I-13.下列属于自身指示剂的是()(A)邻二氮菲(B)淀粉指示剂(C) KMnO4 (D)二苯胺磺酸钠14.在Ca2+、Mg2+、Fe3+、Al3+混合溶液中,用EDTA测定Fe3+、Al3+含量时,为了消除Ca2+、Mg2+的干扰,最简便的方法是()(A)沉淀分离法(B)控制酸度法(C) 配位掩蔽法(D)溶剂萃取法15.用双指示剂法测某碱样时,若V1>V2,则组成为()(A)NaOH+Na2CO3 (B) NaOH (C) Na2CO3 (D)Na2CO3+NaHCO316.下列滴定中只出现一个滴定突跃的是( )(A)HCI滴定Na2CO3(B)HCI滴定NaOH+Na3PO4(C)NaOH滴定H2C2O4(D)NaOH滴定H3PO417.某弱碱MOH的Kb=1.0x10-5,其0.10moll-1溶液的pH值为()(A)3.00 (B)5.00 (9) 9.00 (D)11.0018.减小随机误差的措施是( )(A)增加平行测定次数(B)校正测量仪器(C) 对照试验(D)空白试验19.有色配位化合物的摩尔吸光系数与下列()因素有关(A)配位化合物的稳定性(B)有色配位化合物的浓度(C)入射光的波长20.在吸收光谱曲线上,随着物质浓度的增大,吸光度A增大,而最大吸收波长将()(A)为零(B)不变(C) 减小(D)增大21.用重量法测定Ca2+时,应选用的沉淀剂是()(A) H2SO4 (B)Na2CO3 (C)(NH4)2C2O4 (D)Na3PO422.为了获得纯净而且易过滤的晶形沉淀,要求()(A)沉淀的聚集速率大于定向速率(B)溶液的过饱和度要大(C)沉淀的相对过饱和度要小(D)溶液的溶解度要小23.以K2CrO4为指示剂测定Cl-时,应控制的酸度为()(A)pH为1-3 (B)pH为4-6 (C)pH为6.5-10.024.可用于滴定I2的标准溶液是( )(A)H2SO4 (B)KbrO3 (C) Na2S2O325. 用下列哪一标准溶液滴定可以定量测定碘?()(A) Na2S (B)Na2SO3 (C) Na2SO4 (D)Na2S2O326.用重铬酸钾法测定铁矿石中铁的含量时选用下列哪种还原剂?()(A)二氯化锡(B)双氧水(C)铝(D)四氯化锡27.用SO42-使Ba2+形成BaSO4沉淀时,加入适当过量的SO42-,可以使Ba2+沉淀的更完全,这是利用何种效应?()(A)盐效应(B)酸效应(C) 络合效应(D)溶剂化效应(E)同离子效应28.用0.1mol/LHCl滴定0.1mol/LNaOH时的pH突跃范围是9.7-4.3,若用1mol/LHCI滴定1mol/LNaOH时的pH突跃范围是()(A)9.7~4.3 (B)8.7~4.3 (C) 10.7 ~3.3 (D)8.7~5.329.衡量色谱柱柱效能的指标是( )(A) 相对保留值(B) 分离度(C)塔板数(D)分配系数30.若两电对在反应中电子转移数分别为1和2,为使反应完全程度达到99.9%,两电对的条件电位差至少应大于()(A)0.09V (B) 0.18V (C) 0.27V (D)0.36V31.佛尔哈德法测Ag+,所用滴定标准溶液、pH条件和应选择的指示剂是()(A)NH4SCN,碱性,K2CrO4;(B)NH4SCN,酸性,NH4Fe(SO4)2(C) AgNO3,酸性,NH4Fe(SO4)2(D)AgNO3,酸性,K2Cr207;(E)NH4SCN,碱性,NH4Fe(SO4)232. 用异烟酸-吡唑酮作显色剂可测定水中CN-的含量,浓度为Cmol/L的氟化物溶液显色后,在一定条件下测得透光率为T,若测量条件不变,只改变被测物浓度为1/3C,则测得的透光率'T为()(A)T1/2 (B)T1/3 (C) T1/4 (D)T/333. EDTA与金属离子形成整合物时,其整合比一般为()(A) 1:1 (B) 1:5 (C) 1:6 (D) 1:434.已知H3PO4的pKa1=2.12,pKa2=7.20,pKa3=12.36,若用NaOH滴定H3PO4,则第二个化学计量点的pH值约为()(A)10.7 (B)9.7 (C) 7.7 (D)4.935.需0.1MHCl溶液,请选最合适的仪器量取浓酸()(A) 量筒(B)容量瓶(C) 移液管(D)酸式滴定管36.下列各酸碱对中,属于共轭酸碱对的是()(A)H2CO3-CO32-(B)H3O+--OH-(C) HPO42---PO43 (D)NH3+CH2COOH-NH2CH2COO-37.下列有关随机误差的论述中不正确的是()(A)随机误差是由一些不确定的偶然因素造成的(B)随机误差出现正误差和负误差的机会均等(C)随机误差在分析中是不可避免的(D)随机误差具有单向性38.欲取50ml某溶液进行滴定,要求容器量取的相对误差≤0.1%,下列容器中应选哪种?()(A) 50ml滴定管(B)50ml容量瓶(C) 50ml量筒(D)50ml移液管39.使用碱式滴定管滴定的正确操作方法应是下面哪种?()(A)左手捏于稍高于玻璃近旁(B)右手捏于稍高于玻璃球的近旁(C)左手捏于稍低于玻璃球的近旁40.配制0.1M的NaS2O3标准液,取一定量的Na2S2O3晶体后,下列哪步正确?()(A) 溶于沸腾的蒸馏水中,加0.1gNa2CO3放入棕色瓶中保存(B)溶于沸腾后冷却的蒸馏水中,加0.1gNa2CO3放入棕色瓶中保存(C) 溶于沸腾后冷却的蒸馏水中,加0.1gNa2CO3放入玻璃瓶中保存41.如果要求分析结果达到0.1%的准确度,滴定时所用滴定剂溶液的体积至少应为多少ml?()(A) 10ml (B) 10.00ml (C) 18ml (D) 20ml42.EDTA在PH<1的酸性溶液中相当于几元酸?()(A) 3 (B) 5 (C) 4 (D) 2 (E) 643.不含其它干扰性杂质的碱试样,用0.1000MHCl滴定至酚酞变色时,用去Hcl20.00ml加入甲基橙后,继续滴定至终点又用去HCl10.00ml,此试样为下列哪种组成?()(A) NaOH,Na2CO3 (B)Na2cO3(C)Na2CO3,NaHCO3 (D)NaHCO3,NaOH44.用含有微量杂质的草酸标定高锰酸钾浓度时,得到的高锰酸钾的浓度将是产生什么结果?()(A) 偏高(B)偏低(C) 正确(D)与草酸中杂质的含量成正比45.用邻苯二甲酸氢钾滴定1mol/LNaOH溶液时,最合适的指示剂是( )(A)甲基红(PH=4.4~6.2)(B)百里酚酞(PH=9.4~10.6)(C)酚酞(PH=8.3~10.0)(D)甲基橙(PH=3.1~4.4)46.间接碘量法中,硫代硫酸钠标准溶液滴定碘时,应在哪种介质中进行( )(A)酸性(B)碱性(C)中性或微酸性(D)HCL介质47.用碘量法进行氧化还原滴定时,错误的操作是( )(A)在碘量瓶中进行(B)避免阳光照封(C)选择在适宜酸度下进行(D)充分摇动48.选择氧化还原指示剂时,应该选择( )(A)指示剂的标准电位愈接近滴定终点电位好(B)指示剂的标准电位愈接近滴定终点电位的差越大越好(C)指示剂的标准电位越负越好(D)指示剂的标准电位越正越好49.酸碱滴定中指示剂选择依据是( )(A)酸碱溶液的浓度(B)酸碱滴定PH突跃范围(C)被滴定酸或碱的浓度(D)被滴定酸或碱的强度50.对于滴定分析法,下述( )是错误的.(A)是以化学反应为基础的分析方法(B)滴定终点的到达要有必要的指示剂或方法确定(C)所有的化学反应原则上都可以用于滴定分析(D)滴定分析的理论终点和滴定终点经常不完全吻合51.Na2S2O3放置较长时浓度将变低的原因为( )(A)吸收空气中的CO2.(B)被氧化(C)微生物作用52.直接配制标准溶液时,必须使用( )(A)分析纯试剂(B)高纯或优级纯试剂(C)基准物53. SI为( )的简称(A)国际单位制的基本单位(B)国际单位制(C)法定计量单位54.分析化学中常用的法定计量单位符号Mr其代表意义为( )(A)质量(B).摩尔质量(C)相对分子质量(D).相对原子量55.我国化工部标准中规定:基准试剂颜色标记为()(A)红色(B)蓝色(C)绿色(D)浅绿色56.做为基准试剂,其杂质含量应略低于( )(A)分析纯(B)优级纯(C)化学纯(D)实验试剂57.下面数据中是四位有效数字的是()(A)0.0376 (B)1396(C)0.07520 (D)0.050658.市售硫酸标签上标明的浓度为96%,一般是以( )表示的(A)体积百分浓度(B)质量体积百分浓度(C)质量百分浓度59.下列计量单位中属于我国选定的非国际单位制( )(A)米(B)千克(C)小时(D)摩尔1-5:ACDCA 6-10:ADCAB 11-15:CDCBA 16-20:CDACB 21-25:CCCCD 26-30:AEBBC 31-35:BBABA 36-40:CDDBB 41-45:DEABC 46-50:CDABC 51-55:CCBCD 56-59:BCCC二、判断题1.称量物体时应将物体从天平左门放入左盘中央,将砝码从右门放入右盘中央(√)2.称量物体的温度,不必等到与天平室温度一致即可进行称量(×)3. 天平需要周期进行检定,砝码不用进行检定(×)4.在滴定管下端有尖嘴玻璃管和胶管连接的称为酸式滴定管(×)5.打开干燥器的盖子时,应用力将盖子向上掀起(×)6.圆底烧瓶不可直接用火焰加热(√)7.玻璃容器不能长时间存放碱液(√)8.准确度高必须要求精密度也高,但精密度高,并不说明准确度也高,准确度是保证精密度的先绝条件(×)9.准确度的高底常以偏差大小来衡量(×)10.所谓饱和溶液是指再也不能溶解溶质的溶液(×)11.在溶解过程中,溶质和溶剂的体积之和一定就是溶液的总体积(×)12.容量分析一般允许滴定误差为1%(×)13.酸碱滴定中有时需要用颜色变化明显的变色范围较窄的指示剂即混合指示剂(√)14.天平室要经常敞开通风,以防室内过于潮湿(×)15.滴定管内壁不能用去污粉清洗,以免划伤内壁,影响体积准确测量(√)。
《分析化学》期末考试复习题及参考答案
分析化学复习题(课程代码 252402)一、填空题1、定量分析的过程通常包括_______________________________________________;定量分析的精密量器是指_____________________________________________。
2、配位滴定法中常见的滴定方式包括_______________________________________。
3、0.02000 mol·L-1的K2Cr2O7标准溶液(Mr=294.18)对Fe 2O3(M r=159.67)的滴定度为_____________________________________________________;已知试样中As2S3(M r =246.0)的质量分数为0.2000,则换算成BaSO4(M r =233.39)的质量分数为____________________________。
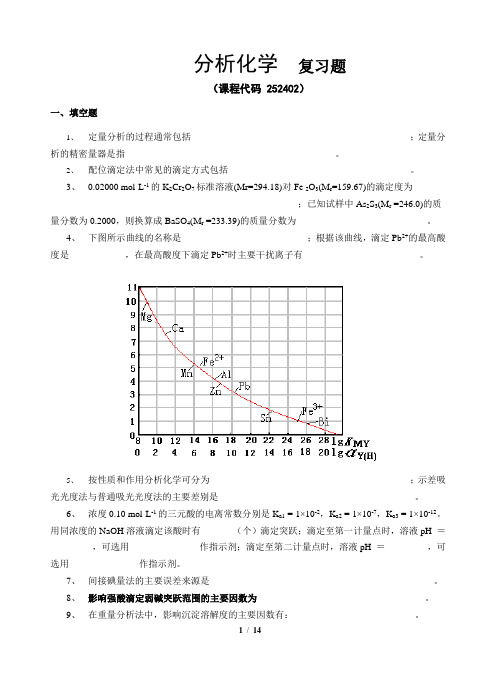
4、下图所示曲线的名称是___________________________;根据该曲线,滴定Pb2+的最高酸度是____________,在最高酸度下滴定Pb2+时主要干扰离子有_________________________。
5、按性质和作用分析化学可分为___________________________________________;示差吸光光度法与普通吸光光度法的主要差别是__________________________________________。
6、浓度0.10 mol·L-1的三元酸的电离常数分别是K a1 = 1×10-2,K a2 = 1×10-7,K a3 = 1×10-12。
用同浓度的NaOH溶液滴定该酸时有_______(个)滴定突跃;滴定至第一计量点时,溶液pH =_________,可选用_______________作指示剂;滴定至第二计量点时,溶液pH =_________,可选用_______________作指示剂。
分析化学期末考试复习题及参考答案-高起本

《分析化学》复习题一、填空题1、滴定管一次读数误差为±0.01 mL ,若滴定相对误差不大于±0.1%, 则滴定剂用量至少应为mL ,最好使体积在 mL 左右,以减小相对误差。
2、某学生分析氯化物中氯的含量,重复测定四次,结果如下:52.68%,53.17%,52.73%,52.67%。
用Q 检验法判断数据53.17%在置信度为90%时是否应当舍弃(已知Q 0.90,4=0.76),舍弃商Q 等于 ,结论是 (填舍弃或保留)。
3、莫尔法与佛尔哈德法的指示剂分别为 、 。
4、光度法测定某物质,若有干扰,应根据 和 原则选择波长。
5、NaOH 滴定HCl 时,浓度增大10倍,则滴定曲线突跃范围增大 个pH单位。
6、在一定条件下用Ce(SO 4)2标准溶液滴定相同浓度的Fe 2+溶液,已知)Ce /Ce (34++O 'ϕ=1.44V ,)Fe /Fe (23++O 'ϕ=0.68V , 则化学计量点时溶液电势为 V 。
7、在分光光度法中,以 为纵坐标,以 为横坐标,可得光吸收曲线。
浓度不同的同种溶液,其最大吸收波长 ,相应的吸光度大小 。
8、电位分析中,电位保持恒定的电极称为 电极,常用的有 电极和 电极。
9、高效液相色谱分析中,如果样品组分的分配比范围很宽,宜采用措施;在气相色谱分析中,如果样品组分的沸点范围很宽,宜采用措施,这些操作的目的都是为了改善分离效果。
10、在原子吸收法中,火焰原子化器与石墨炉原子化器相比较,后者测定的灵敏度更。
11、EDTA滴定中,介质pH越低,则αY(H)值越_ __,O'K越_ __,滴定的pM 突跃越_ __。
(填“大”、“小”)12、用普通吸光光度法测得标准溶液c1的透光率为20%,待测溶液透光率为12%,若以示差法测定,以标准溶液c1作参比,则待测溶液透光率为_ __,相当于将仪器标尺扩大_ __倍。
13、用KMnO4滴定H2C2O4溶液,第一滴KMnO4滴入后紫色褪去很慢,而随着滴定的进行反应越来越快,这是由于反应生成的有作用。
分析化学试卷5套及答案

分析化学试卷5套及答案《分析化学》期末试卷(B)一、是非题(本大题共10小题,每小题1分,共10分)1.化学分析法的测定灵敏度高,因此常用于微量分析。
( )2.分析数据中,凡是“0”都不是有效数字。
( )3.纯度很高的物质均可作为基准物质。
( )4.用HCl溶液滴定Na2CO3基准物溶液以甲基橙作指示剂,其物质量关系为n(HCl)∶n(Na2CO3)=1∶1。
( )5.酸碱滴定中,只有当溶液的pH突跃超过2个pH单位,才能指示滴定终点。
( )6.标定高锰酸钾溶液时,为使反应较快进行,可以加入Mn2+。
( )7.AgCl的Ksp=×10-10比Ag2CrO4的Ksp=9×10-12大,所以,AgCl在水溶液中的溶解度比Ag2CrO4大。
( )8.用佛尔哈德法测定Cl-时,如果生成的AgCl沉淀不分离除去或加以隔离,AgCl沉淀可转化为AgSCN沉淀。
但用佛尔哈德法测定Br-时,生成的AgBr沉淀不分离除去或不加以隔离即可直接滴定。
( )9.重量分析法要求沉淀溶解度愈小愈好。
( )10.吸光光度法只能测定有颜色物质的溶液。
( )二、选择题 (本大题共20题,每小题分,共30分)1.试样预处理的目的不是为了()(A)使被测物成为溶液; (B)使被测组分生成沉淀(C)使被测物变成有利测定的状态; (D)分离干扰组分2.下列论述正确的是:()(A)准确度高,一定需要精密度好;(B)进行分析时,过失误差是不可避免的;(C)精密度高,准确度一定高;(D)精密度高,系统误差一定小;3.称取含氮试样0.2g,经消化转为NH4+后加碱蒸馏出NH3,用10 mL mol·L-1HCl吸收,回滴时耗去mol·L-1 NaOH mL。
若想提高测定准确度, 可采取的有效方法是 ( )(A) 增加HCl溶液体积 (B) 使用更稀的HCl溶液(C) 使用更稀的NaOH溶液 (D) 增加试样量4.在酸碱滴定中被测物与滴定剂浓度各变化10倍,引起的突跃范围的变化为()。
分析化学练习题含答案

分析化学练习题含答案一、单选题(共60题,每题1分,共60分)1、用K2Cr2O7滴定Fe2+时,常用H2SO4—H3PO4混合酸作介质,加入H3PO4的主要作用是()。
A、增大溶液的酸度B、增大滴定的突跃范围C、保护Fe2+免被空气氧化D、可以形成缓冲溶液正确答案:B2、当Al3+和Zn2+共存时,要用EDTA滴定Zn2+,使Al3+不干扰,最简便的处理方法是()。
A、调节溶液至适宜的酸度B、加入适量的NaF作掩蔽剂C、加入氨水生成Al(OH)3沉淀D、调节强碱性生成AlO2.正确答案:B3、用同一浓度的NaOH滴定相同浓度和体积的不同的一元弱酸,对Ka较大的一元弱酸,下列说法正确的是()。
A、消耗NaOH溶液多B、化学计量点的pH较高C、突跃范围大D、指示剂变色不敏锐正确答案:C4、下列试剂中,可作为基准物质的是()。
A、NaOHB、HClC、KMnO4D、K2Cr2O7正确答案:D5、下列因素中,()引起的误差不属于系统误差。
A、电源波动频繁使天平的零点和停点测定不够准确B、天平不等臂C、滴定管的刻度不够准确D、蒸馏水中含有微量干扰物质6、在pH=10.0时,用0.02mol·L.1的EDTA滴定20.00mL0.02mol·L.1的Ca2.溶液,计量点的pCa值是()。
A、4.1B、10.7C、5.95D、6.1正确答案:D7、下列滴定法中,不用另外加指示剂的是()。
A、碘量法B、高锰酸钾法C、甲醛法D、重铬酸钾法正确答案:B8、用间接碘量法测定胆矾(CuSO4·5H2O)中的铜含量时,加入过量KI前常常加入NaF(或NH4HF2),其目的是()。
A、与Cu2+定量作用B、减少CuI对I2的吸附C、掩蔽Fe3+D、使淀粉的变色变得比较锐敏正确答案:C9、用酸碱滴定法测定CaCO3含量时,不能用HCl标液直接滴定而需用返滴法是由于()。
A、CaCO3难溶于水与HCl反应速度慢B、CaCO3与HCl反应不完全C、CaCO3与HCl不反应D、没有适合的指示剂正确答案:A10、用HCl标准溶液滴定Na2CO3至NaHCO3,则THCl/Na2CO3表示CHCl的表达式为()。
药学专业分析化学期末复习题(含参考答案)

药学专业分析化学复习题一单项选择题1 重量分析中样品杂质被其沉淀属于AA 方法误差B 仪器误差C 试剂误差D 操作误差2 用加热法驱除水分以测定CaSO4·1/2H2O中结晶水的含量,称取试样0.2000g,已知天平的称量误差为±0.1mg,问分析结果应以几位有效数字报出DA 1B 2C 3D 43在下列各组酸碱物质中,哪些属于共轭酸碱对DA H3PO4--Na2HPO4B H2SO4--SO42-C H2CO3-CO32-D (CH2)6N4H+--(CH2)6N44标定EDTA时常用基准物质BA 无水Na2CO3B ZnOC NaClD Na2C2O45 用配位滴定法测Al3+采用BA 直接滴定法B返滴定法 C 置换滴定法D间接滴定法6 在EDTA法中,K MIn>K MY时会产生CA 僵化现象B 氧化变质现象C 封闭现象D 掩蔽现象7 下列因素使配位滴定突跃变小的是CA 配合物的稳定常数越大B 溶液PH越大C 配位效应影响越大D 被滴定金属离子浓度越大8 用基准K2Cr2O7标定Na2S2O3溶液属于何种滴定方式CA 直接B 剩余C 置换D 间接9氧化还原滴定突跃范围大小与哪一个因素有关AA △φ’B △φ’InC φInD 标准电极电位10 间接碘量法滴至终点后,若产生即时“回蓝”现象,可能是由于CA 试样中杂质的干扰B 空气中氧气氧化碘离子C 第一步反应不完全D 淀粉指示剂变质11关于氧化还原指示剂,说法不正确的是BA 指示剂的变色点时φIn=φ’InB 指示剂在作用时不消耗标准溶液C 氧化态与还原态颜色应明显不同D 是通用型指示剂12下列可在弱碱性条件下进行的是DA 用Na2S2O3溶液测CuSO4·5H2O含量B 间接碘量法C KMnO4法D 直接碘量法13银量法中三种指示剂法都不能在何种溶液中进行CA 强酸性B 弱碱性C 强碱性D 弱酸性14 形成晶形沉淀的条件CA 稀快搅热陈B 浓快搅热陈C 稀慢搅热陈D 浓慢搅热陈15沉淀生成速度过快,易形成DA 吸附B 后沉淀C 混晶D吸留二 填空1 从碘量法本身来说, 间接碘量法中引入误差的主要因素是__I 2_的挥发_和__I -_被氧气氧化_______________.2 氧化还原滴定法的指示剂分为_氧化还原指示剂,__自身指示剂,__特殊指示剂_.3 恒重是指试样_连续两次干燥或灼烧后的质量差不超过±0.3mg 即为恒重。
《 分析化学 》课程期末考试试卷 (1)

《分析化学》课程期末考试试卷一.单选题。
每题1分,共20分。
1、根据“四舍六入五留双”的修约原则,下列哪项是错误的() [单选题] *A、保留五位有效数字:7.28355→7.2836B、保留四位有效数字:17.4551→17.45(正确答案)C、保留三位有效数字:2.005→2.00D、保留四位有效数字:14.446→14.45E、保留四位有效数字:15.0250→15.022、下列哪种情况应采用返滴定法() [单选题] *A、用AgNO3标准溶液测定NaCl试样含量B、用HCl标准溶液测定Na2CO3试样含量C、用EDTA标准溶液测定Al3+试样含量(正确答案)D、用Na2S2O3标准溶液测定K2Cr2O7试样含量E、用EDTA标准溶液测定骨钙3、下列各项所造成的误差那一项属于系统误差() [单选题] *A、滴定管的读数15.05ml记为15.50mlB、滴定时温度有变化C、称重时天平的平衡点有变动D、用1:10的HCl代替1:1的HCl(正确答案)E、滴定过程中有溶液溅出4、下列滴定分析法的特点哪一项是错误的() [单选题] *A、操作简便、快速B、应用范围广C、准确度高D、可测痕迹量组分(正确答案)E、相对误差可达到0.1%5、强碱滴定强酸时,浓度均增大10倍,则滴定突跃范围将() [单选题] *A、增大0.5个pH单位(正确答案)B、增大1个pH单位C、增大1.5个pH单位D、增大2个pH单位E、不变6、将pH=1和pH=14的两种强电解质溶液按等体积混合,混合溶液pH为() [单选题] *A、1B、7C、7.5D、13E、13.65(正确答案)7、配制HClO4-冰醋酸溶液要加入计算量的醋酐,其目的是() [单选题] *A、增大样品溶解能力B、增大样品的酸碱性C、除去HClO4冰醋酸中的水分(正确答案)D、增大突跃范围使终点敏锐E、增强溶剂的区分(均化)效应8、在EDTA标准溶液的标定过程中采用的缓冲溶液是() [单选题] *A、醋酸-醋酸盐缓冲溶液B、磷酸-磷酸盐缓冲溶液C、硼酸-硼酸盐缓冲溶液D、枸橼酸-枸橼酸钠缓冲溶液E、氨-氯化铵缓冲溶液(正确答案)9、EDTA在什么酸度下主要以Y4-的形式存在() [单选题] *A、pH<2.0B、pH=2.7-6.2C、pH=2.0-2.7D、pH=6.2-10.2E、pH>10.2(正确答案)10、标定Na2S2O3标准溶液,常用下列何种基准物质() [单选题] *A、重铬酸钾(正确答案)B、铬酸钾C、草酸D、碳酸钠E、高锰酸钾11、引起酸差的溶液,其pH() [单选题] *A、pH<1(正确答案)B、pH>1C、pH>9D、pH<9E、pH<212、能级跃迁所需能量最小的是() [单选题] *A、σ→σ*B、σ→π*C、π→π*D、n→σ*E、n→π*(正确答案)13、激发光、荧光、磷光三者的波长关系正确的是() [单选题] *A、λ激发光>λ荧光>λ磷光B、λ激发光<λ荧光<λ磷光(正确答案)C、λ激发光=λ荧光=λ磷光D、λ激发光>λ磷光>λ荧光E、λ磷光>λ激发光>λ荧光14、在一般的质谱图上出现非整数质核比的峰,它可能是() [单选题] *A、分子离子峰B、碎片离子峰C、亚稳离子峰(正确答案)D、同位素峰E、同位素峰或碎片离子峰15、红外光谱上的特征区的波数范围是() [单选题] *A、4000~1300cm-1(正确答案)B、3000~1300cm-1C、2000~1300cm-1D、1375~720cm-1E、1300~400cm-116、在CH3CH2CH3 的高分辨NMR谱上,CH2质子的吸收峰分裂为() [单选题] *A、三重峰B、四重峰C、六重峰D、七重峰(正确答案)E、八重峰17、某化合物的质谱图中,检测出分子离子峰的质荷比m/z为115,化合物含有() [单选题] *A.偶数个氮原子B、奇数个氮原子(正确答案)C.任意数目的氮原子D.没有氮原子E、都不对18、对称峰的拖尾因子符合要求的范围是() [单选题] *A、0.85~1.15B、0.90~1.10C、0.95~1.05(正确答案)D、0.99~1.01E、0.2~0.819、用气相色谱法进行定量时,要求混合物中每一个组分都出峰的是() [单选题] *A、外标法B、内标法C、内标对比法D、归一化法(正确答案)E、外标一点法20、高效液相色谱法的定性指标是() [单选题] *A、峰面积B、保留时间(正确答案)C、半高峰宽D、峰高E、标准偏差二、判断题(每题2分,共30分)1、定量分析中,系统误差影响测定结果的精密度,偶然误差影响测定结果的准确度。
分析化学试题(含答案)

分析化学试题(含答案)一、单选题(共64题,每题1分,共64分)1.用EDTA滴定Co2+时(CCo终=0.01mol/L),其允许最小pH值为()。
A、4.0B、5.0C、6.0D、7.0正确答案:A2.将甲基橙指示剂加到一无色水溶液中,溶液呈黄色,该溶液的酸碱性为()。
A、中性B、碱性C、酸性D、不能确定其酸碱性正确答案:D3.按一般吸光光度法以试剂空白作参比测得某试液的透光率为5%;现改用示差法,以一般吸光光度法测得透光率为10%的标准溶液做参比,则该试液的透光率为()。
A、50%B、5%C、10%D、90%正确答案:A4.配位滴定法以EDTA滴定金属离子时,终点的颜色是()。
A、游离指示剂的颜色B、指示剂配合物的颜色C、EDTA配合物的颜色D、EDTA配合物与指示剂配合物的混合色正确答案:A5.以甲基红为指示剂,能用NaOH标准液准确滴定的酸是()。
A、硫酸(pKa2=1.92)B、草酸(pKa1=1.25,pKa2=4.29)C、乙酸(pKa=4.75)D、甲酸(pKa=3.75)正确答案:A6.用0.1mol/L的NaOH标液滴定0.1mol/L氨水,当溶液的pH=9.25时,氨水被滴定的百分数为()。
(氨水的pKb=4.75)A、125%B、75%C、50%D、25%正确答案:C7.用碘量法测定漂白粉中的有效氯(Cl)时,常用()作指示剂。
A、甲基橙B、淀粉C、铁铵矾D、二苯胺磺酸钠正确答案:B8.浓度为0.1000mol/L的HCl标准溶液对CaCO3的滴定度是()g/mL。
A、0.01B、0.01000C、3.646×10-3D、5.000×10-3正确答案:D9.用碱式滴定管滴定时,手指应捏在玻璃珠的()。
A、正中B、随意C、上半部边缘D、下半部边缘正确答案:C10.相对标准偏差(n<20)的表达式为()。
A、Xdi.×100%B、Xndi1..×100%C、Xndi.×100%D、Xndi12..×100%正确答案:D11.浓度和体积相同的两份KHC2O4·H2C2O4溶液,一份可与VmL0.1500mol/LNaOH溶液完全中和,另一份加H2SO4后,用KMnO4溶液滴定至终点,也需要VmLKMnO4溶液。
分析化学复习题及答案

分析化学复习题及答案1. 定量分析的任务是测定物质中有关组分的()A、元素B、原子团C、化合物D、相对含量(正确答案)E、离子2. 研究物质化学结构的是()A、定性分析B、定量分析C、结构分析(正确答案)D、重量分析E、仪器分析3. 滴定分析法属于()A、色谱法B、光谱法C、化学分析法(正确答案)D、定量分析法•E、仪器分析法4. 根据分析任务的不同将分析化学分为()A、无机化学、有机化学B、定量分析、定性分析、结构分析(正确答案)C、常量分析、微量分析D、重量分析、滴定分析E、化学分析、仪器分析5. 微量分析取试样体积一般为()A、>10mLB、10-0.1mLC、1-0.01mL(正确答案)D、<0.01mLE、<10Ml6. 根据分析方法的原理不同将分析化学分为()A、常量分析、微量分析B、定性分析、定量分析、结构分析C、重量分析、滴定分析D、光学分析、色谱分析E、化学分析、仪器分析(正确答案)7. 常量分析称量试样的质量一般在()A、>0.1g(正确答案)B、0.1-0.01gC、10-0.1mgD、<0.1mgE、<100mg8. 下列关于有效数字记录、修约、运算规则说法错误的是()A、四舍六入五留双B、记录测量数据时,只允许保留一位可疑数字C、数字修约应一次完成D、几个数据相加或相减时,应该以有效数字最少的数据为依据进行修约(正确答案)E、当修约精密度如标准偏差时,一般采用“只进不舍”的方法9. 分析化学可以应用于以下哪些方面()A、生命科学(正确答案)B、环境科学(正确答案)D、食品安全分析(正确答案)E、农业科学(正确答案)10. 下列属于分析化学的任务是()A、确定物质体系的化学组成(正确答案)B、测定物质组分的相对含量(正确答案)C、确定物质的化学结构(正确答案)D、确定药物的功效E、采用各种方法和手段11. 分析化学研究物质的()等化学信息有关的理论和技术A、组成(正确答案)B、气味C、结构(正确答案)D、颜色E、形态(正确答案)12. 定性分析的任务是鉴定物质的()A、元素(正确答案)B、离子(正确答案)C、原子团(正确答案)D、官能团(正确答案)E、化合物(正确答案)13. 根据分析任务不同将分析化学分为()A、定性分析(正确答案)B、化学分析C、仪器分析D、定量分析(正确答案)E、结构分析(正确答案)14. 按照分析方法分类,可以将分析化学分为()B、仪器分析(正确答案)C、定性分析D、定量分析E、结构分析15. 有效数字由()组成A、测量数字和非测量数字B、有效数字和无效数字C、整数和小数D、准确数字和可疑数字(正确答案)E、以上说法都不对16. 分析化学中,数字分为哪两类()A、准确值B、估计数字C、可疑数字D、测量所得数字(正确答案)E、非测量所得数字(正确答案)HYPERLINK "javascript:void(0)"17. 化学分析法是利用物质的化学反应为基础的分析方法对(正确答案)错18. 化学分析法一般适用于微量组分或痕量组分的分析对错(正确答案)19. 分析化学是研究获取物质化学组成、结构和形态等化学信息的有关理论和技术的一门科学对(正确答案)错20. 依据分析原理的不同,将分析化学分为重量分析和滴定分析对错(正确答案)21. 仪器分析法通常适用于常量组分或半微量组分分析对错(正确答案)22. 仪器分析法是以物质的物理或物理化学性质为基础的分析方法对(正确答案)错23. 滴定分析中,指示剂变色时,称为()A、终点(正确答案)B、化学计量点C、中和点D、计量点E、滴定度24. 化学计量点与滴定终点的关系是()A、两者越接近,误差越大B、两者越接近,误差越小(正确答案)C、两者必须吻合D、两者毫无关系E、以上都不对25. 滴定分析一般要求相对误差()A、大于0.2%B、小于0.2%(正确答案)C、大于0.1%D、小于0.1%E、大于1%26. 滴定分析法主要用于()A.仪器分析B、常量分析(正确答案)C、定性分析D、重量分析E、以上都可以27.测定样品中CaCO的含量时,常采用下列哪种方法()A、直接滴定法B、剩余滴定法(正确答案)C、置换滴定法D、间接滴定法E、以上都不对28. 沉淀滴定法的条件有()A、反应迅速、定量B、沉淀的溶解度必须很小C、有适当的指示终点的方法D、沉淀的吸附现象不影响滴定终点的确定E、以上都是(正确答案)29. 铬酸钾指示剂法说法正确的是()A、指示剂的用量要适当B、在中性或弱碱性条件下进行C、滴定时充分振摇,防止沉淀吸附而导致终点提前D、预先分离干扰离子E、以上都正确(正确答案)30. 铁铵矾指示法包括()A、直接滴定法和返滴定法(正确答案)B、沉淀滴定法和非沉淀滴定法C、氧化滴定和还原滴定D、变色滴定和不变色滴定E、称量法和容积法31. 铬酸钾指示剂法反应终点的颜色为()A、橘色B、橙色C、砖红色(正确答案)D、粉红色E、紫红色32.铁铵矾指示剂法反应到终点的颜色为()A、白色B、红色(正确答案)C、黄色D、蓝色E、紫色33. 银量法是以碘盐沉淀反应为基础的沉淀滴定方法对错(正确答案)34. 沉淀滴定法是以沉淀反应为基础的滴定分析方法对(正确答案)错35. 常用与标定盐酸的基准物质是()A、邻苯二甲酸氢钾B、氯化钠C、无水碳酸钠或硼砂(正确答案)D、氢氧化钠E、氢氧化钾36. 下列盐溶液的浓度均为0.1mol/L,其中能用NaOH标准溶液直接滴定的是()A、NaClB、Na 2SO 4C、NaNO3D、NaCO3E、HCl(正确答案)37. 测定试样中CaCO3的含量时,常采用下列哪种方法()A、直接滴定法B、剩余滴定法(正确答案)C、置换滴定法D、间接滴定法E、配位滴定法38. 色谱法按色谱原理不同分为()A、吸附色谱、分配色谱、离子交换色谱、凝胶色谱(正确答案)B、柱色谱、薄层色谱、纸色谱C、气相色谱、液相色谱、高效液相色谱D、气-液色谱、气-固色谱、液-液色谱、液-固色谱E、柱色谱、高效液相色谱、纸色谱39. 将“45.215”修约为4位有效数字,结果应为()A、45.2150B、45.21C、45.22(正确答案)D、45.2E、45.2040. 下列酸中,可以用氧化还原滴定法测定的是()A、盐酸B、硫酸C、醋酸D、草酸(正确答案)E、碳酸41. 直接采用标准溶液对试样溶液进行滴定的方法是()A、直接滴定法(正确答案)B、间接滴定法C、配位滴定法D、氧化还原滴定法E、以上都不是42. 为了缩小酸碱指示剂的变色范围,使变色更敏锐,常采用的措施是()A、多加一些指示剂B、加热C、将标准溶液稀释D、用混合指示剂(正确答案)E、以上方法都可行43. 碘量法是利用()来进滴定的氧化还原滴定法。
《分析化学》期末试卷及答案

《分析化学》期末考试试卷
出卷人:
_ 审核人:
系级
班 姓名
题号 一
二
三
四
得分
评分人
一、填空 (每空 1 分,共 20 分)
学号
成绩
五 总分
1. 定量分析过程包括 取样 , 溶(熔)样,分析方法选择, 干扰杂质的分离 和分析测定 数据处理及结果的报出等步骤。 2. 碘量法主要的误差来源是I2 的挥发___和I-的氧化 ,为减小上述原因所造成的误差,滴 定时的速度可 快些 ,溶液不需剧烈摇动 。 3. 系统误差影响分析结果的: 准确度 ;偶然误差影响分析结果的: 精密度 。 4. 莫尔法与佛尔哈德法的指示剂分别为 铬酸钾(K2CrO4) 、铁铵钒(NH4Fe(SO4)2)。 5. 配位滴定中,由于 H+的存在,使 EDTA 参加主反应能力降低的现象,称为酸效应。 6. 滴定分析对滴定反应的基本要求是反应定量完全进行、 反应速度快、 有指示终点的方法。 7. 酸碱滴定曲线是以 PH 值 变化为特征的。 8. 在氧化还原滴定中常用的指示剂是 自身指示剂、 特殊指示剂和氧化还原指示剂。 9. 在滴定过程中,指示剂发生颜色变化的转变点称为 滴定终点 。
D. 滴定碘的颜色褪去
读书破万卷 下笔如有神
读书破万卷 下笔如有神
二、选择(每小题 2 分,共 40 分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 161. 间接碘量法加入淀粉指示剂的时间是( B )。 A. 滴定开始前 B. 滴定至接近终点时 C. 滴定至中途
2. 用佛尔哈德法测定的条件是( D )。
分析化学期末复习题(二)

分析化学期末复习题(二)一、选择题( 共10题20分)1. 2 分以下说法错误的是--------------------------------------------------------------------------------( )(A) 摩尔吸光系数e随浓度增大而增大(B) 吸光度A随浓度增大而增大(C) 透射比T随浓度增大而减小(D) 透射比T随比色皿加厚而减小2. 2 分某一NaOH和Na2CO3混合液,用HCl溶液滴定,以酚酞为指示剂,耗去HClV1(mL), 继以甲基橙为指示剂继续滴定,又耗去HCl V2(mL),则V1与V2的关系是-------------------------( )(A) V1 = V2(B) V1 = 2V2(C) 2V2 = V2(D) V1> V23. 2 分当两电对的电子转移数均为1时,为使反应完全度达到99.9%,两电对的条件电位至少相差----------------------------------------------------------------------------------------------------( )(A) 0.09V (B) 0.18V (C) 0.27V (D) 0.36V4. 2 分用NaOH标准溶液测定FeCl3溶液中的游离HCl时,Fe3+将产生沉淀而引起干扰,可消除其干扰的物质是----------------------------------------------------------------------------------------( )(A) Na2H2Y (B) CaY2-(C) 柠檬酸三钠(D)三乙醇胺5. 2 分符合比尔定律的有色溶液,浓度为c时,透射比为T0,浓度增大一倍时,透射比的对数为-------------------------------------------------------------------------------------------------------------( )(A) T0/ 2 (B) 2T0(C) (lg T0)/2 (D) 2lg T06. 2 分配制含锰0.1000mg/mL的KMnO4溶液100.0mL,需取0.018000mol/L KMnO4溶液(在酸性溶液中作氧化剂)的体积为----------------------------------------------------------------------( )[M r(KMnO4)=158.03,A r(Mn)=54.94](A) 14.15mL (B) 8.09mL (C) 10.11mL (D) 6.07mL7. 2 分已知在0.5mol/LH2SO4介质中, ϕ¢ (Ce4+/Ce3+)=1.44V ϕ¢(Fe3+/Fe2+)=0.68V。
分析化学期末考试题A及答案

分析化学期末考试题A及答案一、选择题(每题2分,共20分)1. 以下哪种物质是强酸?A. 醋酸B. 碳酸C. 硫酸D. 磷酸答案:C2. 酸碱滴定中,终点的判断依据是:A. 颜色变化B. pH值C. 体积变化D. 温度变化答案:A3. 标准溶液的配制中,需要使用的主要仪器是:A. 量筒B. 容量瓶C. 烧杯D. 滴定管答案:B4. 原子吸收光谱法中,分析元素的依据是:A. 原子的电子结构B. 原子的核结构C. 原子的振动频率D. 原子的转动频率答案:A5. 以下哪种方法属于非破坏性分析?A. 火焰光度法B. 原子吸收光谱法C. 质谱法D. 红外光谱法答案:D6. 紫外-可见光谱法中,最大吸收波长称为:A. 吸收峰B. 吸收边C. 吸收谷D. 吸收顶答案:B7. 以下哪种物质是强碱?A. 氢氧化钠B. 氢氧化铵C. 氢氧化钙D. 氢氧化镁答案:A8. 电位滴定法中,电位突跃的点称为:A. 终点B. 起始点C. 平衡点D. 等电点答案:A9. 色谱法中,用于分离混合物的物理过程是:A. 扩散B. 吸附C. 溶解D. 沉淀答案:B10. 以下哪种物质是还原剂?A. 氧气B. 氢气C. 氯气D. 溴气答案:B二、填空题(每空2分,共20分)1. 酸碱滴定中,______是滴定过程中的指示剂。
答案:酚酞2. 原子吸收光谱法中,______是分析元素的光谱线。
答案:吸收线3. 标准溶液的配制中,______是保证溶液浓度准确的关键步骤。
答案:标定4. 紫外-可见光谱法中,______是测量物质对特定波长光的吸收强度。
答案:比色法5. 色谱法中,______是色谱图上的峰高或峰面积。
答案:色谱峰6. 电位滴定法中,______是测量电极电位变化的仪器。
答案:pH计7. 非破坏性分析中,______是分析过程中不改变样品化学性质的方法。
答案:光谱分析8. 强酸和强碱在水溶液中完全离解,其离子浓度等于______。
分析化学期末复习模拟试卷(二)及答案

《分析化学》期末复习模拟试卷(一)一、单项选择题(请将答案填入下表,每题1分,共20分)1.在滴定分析中,对滴定反应的要求是:A。
反应必须定量完成B。
反应必须有颜色变化C.滴定剂必须与被测物1:1反应D.滴定剂必须是基准物2.以下有关系统误差描述正确的是:A。
系统误差具有随机性B。
系统误差在分析过程中不可避免C.系统误差具有单向性D。
系统误差是由一些不确定的偶然因素造成的3.实验室两位新分析人员对同一样品进行分析,得到两组分析结果。
考察两组分析结果的精密度是否存在显著性差异,应采用的检验方法是:A.t检验ﻩB.F检验ﻩ C.Q检验ﻩD.格鲁布斯法4.用HCl溶液滴定NaOH和Na2CO3的混合溶液,以酚酞为指示剂,消耗HCl溶液V1mL,再以甲基橙为指示剂继续滴定,消耗HCl溶液V2mL,则V和V2的关系是:1A.V1=2V2B.V1=V2 C.2V1=V2D.V1〉V25.以下溶液稀释10倍,pH值改变最小的是:A.0。
1mol·L-1 NH4Ac溶液B.0。
1mol·L-1 NaAcC.0。
1mol·L—1HAc D.0。
1mol·L—1HCl 6.甲基橙(pKa=3。
4)的变色范围为3.1-4。
0,若用0.1mol·L-1NaOH滴定0.1mol·L—1HCl,则刚看到混合色时,[In]/[HIn]的比值为:A。
10。
0B。
2.0C.1。
0 D.0。
57.KMnO4溶液的浓度为0.02000mol·L-1,则的值(单位:g·mL—1,MF=55.85g·mol -1)为:eA。
0。
001117B.0。
006936 C.0.005585 D.0.10008.配位滴定中如以PAN为指示剂,则整个滴定过程溶液温度不能低于80℃,否则会由于PAN溶解度降低而导致终点滞后,这种现象被称为指示剂的:A.僵化 B.封闭ﻩ C.变质ﻩﻩ D.变性9.现要用EDTA滴定法测定某样品中Zn2+的含量,为了减少滴定误差,则用于标定EDTA的基准物质应为:A.Pb(NO3)2ﻩB.Na2CO3C.Zn ﻩ D.CaCO310.对配位反应中的条件稳定常数,正确的叙述是:A。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一.选择题(每题2分,共30分。
把正确选项的字母写在题后的括号内)1. 定量分析中,精密度与准确度之间的关系是 ( )(A)精密度高,准确度必然高(B)准确度高,精密度也就高(C)精密度是保证准确度的前提(D)准确度是保证精密度的前提2. 可用下列何种方法减免分析测试中的系统误差()(A)进行仪器校正(B)增加测定次数(C)认真细心操作(D)测定时保证环境的湿度一致3. 测定试样中CaO的质量分数,称取试样0.9080g,滴定耗去EDTA标准溶液20.50mL,以下结果表示正确的是 ( )(A)10% (B)10.1% (C)10.08% (D)10.077%4. 在滴定分析中,一般用指示剂颜色的突变来判断化学计量点的到达,在指示剂变色时停止滴定。
这一点称为()(A)化学计量点(B)滴定误差(C)滴定终点(D)滴定分析5. 滴定管可估读到±0.01mL,若要求滴定的相对误差小于0.1%,至少应耗用体积()mL(A) 10 (B) 20 (C) 30 (D) 406. 共轭酸碱对的Ka 与Kb的关系是()(A)Ka Kb= 1 (B)KaKb=Kw(C)Ka/Kb=Kw(D)Kb/Ka=Kw7. 酸碱滴定中选择指示剂的原则是()(A)指示剂变色范围与化学计量点完全符合(B)指示剂应在pH =7.00时变色(C)指示剂的变色范围应全部或部分落入滴定pH突跃范围之内(D)指示剂变色范围应全部落在滴定pH突跃范围之内8. 测定(NH4)2SO4中的氮时,不能用NaOH直接滴定,这是因为()(A)NH3的Kb太小(B)(NH4)2SO4不是酸(C)(NH4)2SO4中含游离H2SO4(D)NH4+的Ka太小9. 一般情况下,EDTA与金属离子形成的配合物的配位比是()(A)1:1 (B)2:1 (C)1:3 (D)1:210. 铝盐药物的测定常用配位滴定法。
加入过量EDTA,加热煮沸片刻后,再用标准锌溶液滴定。
该滴定方式是()。
(A)直接滴定法(B)置换滴定法(C)返滴定法(D)间接滴定法11. 间接碘量法中加入淀粉指示剂的适宜时间是()。
(A)滴定开始前(B)滴定至近终点时(C)滴定开始后(D)滴定至红棕色褪尽至无色时12. 下述()说法是正确的。
(A)称量形式和沉淀形式应该相同(B)称量形式和沉淀形式可以不同(C)称量形式和沉淀形式必须不同(D)称量形式和沉淀形式中都不能含有水分子13. 晶形沉淀的沉淀条件是()(A)稀、热、快、搅、陈 (B) 浓、热、快、搅、陈(C)稀、冷、慢、搅、陈 (D) 稀、热、慢、搅、陈14. 关于以K2CrO4为指示剂的莫尔法,下列说法正确的是()(A)本法可测定Cl—和Br—,但不能测定I—或SCN—(B)滴定应在弱酸性介质中进行(C)指示剂K2CrO4的量越少越好(D)莫尔法的选择性较强15. 有A、B两份不同浓度的有色溶液,A溶液用1.0cm吸收池,B溶液用3.0cm 吸收池,在同一波长下测得的吸光度值相等,则它们的浓度关系为 ( )(A)A是B的1/3 (B)A等于B(C)B是A的3倍(D)B是A的1/3二.填空(30分)1.分析化学按任务可分为____________分析和____________分析;按测定原理可分为____________分析和____________分析。
2. 化学定量分析方法主要用于_____ 量组分的测定,即含量在______%以上的组分测定。
3.电光分析天平的最小分度值为___mg/格,如果要求分析结果达到1.0‰的准确度,则用减量法称取试样时,至少应称取__g。
4.滴定分析所用的准确量取液体体积的玻璃量器有_______,_______,______等。
5.已知NH3的Kb=1.8×10-5,由NH3- NH4Cl组成的缓冲溶液pH缓冲范围是__________。
6.甲基橙的变色范围是pH=__~__,当溶液的pH小于这个范围的下限时,指示剂呈现___色,当溶液的pH大于这个范围的上限时则呈现___色,当溶液的pH处在这个范围之内时,指示剂呈现___色。
7.EDTA是一种氨羧配位剂,全称为______________,配位滴定中常使用其二钠盐,EDTA二钠盐在水溶液中有______种存在型体。
8.KMY′叫做__________________,它表示有_______________存在时配位反应进行的程度,若只考虑酸效应,KMY ′与KMY的关系式为____________________________________。
9.碘量法测定可用直接和间接两种方式。
直接法以_______为标液,测定________物质。
间接法以________和_________为标液,测定__________物质。
10.用KMnO4法测定物质含量时常需在强酸性介质中进行,但一般不用盐酸或硝酸酸化试样,原因是________________________________,__________________________________。
11.在邻二氮菲光度法测定微量铁的实验中,向含铁试液中加入盐酸羟胺、邻二氮菲和醋酸-醋酸钠溶液的作用分别是____________________、____________________、____________________。
12.用2.5gNa2S2O3·5H2O(M=248.2g/mol)配制成一升溶液,其浓度约为____________mol/L。
三.计算题:(40分)1.分析铁矿石中Fe2O3含量,测定5次,结果分别为67.48%、67.37%、67.47%、67.43%和67.40%,求分析结果的平均值、平均偏差和标准偏差。
(5分)2.称取无水碳酸钠基准物0.1500g,标定HCl溶液时消耗HCl溶液体积25.60mL,计算HCl溶液的浓度。
已知碳酸钠的摩尔质量为106.00g/mol(5分)3.用CaCO3基准物质标定EDTA的浓度,称取0.1005g CaCO3基准试剂, 溶解后定容为100.0mL。
移取25.00mL钙溶液,在pH=12时,以待标定的EDTA滴定之,用去24.90mL。
(1)计算EDTA的浓度;(2)计算EDTA对ZnO和Fe2O3的滴定度。
(12分)4.称取软锰矿试样0.5000g,加入0.7500gH2C2O4·2H2O及稀硫酸,加热至反应完全。
过量的草酸用30.00mL0.02000mol/L的KMnO4溶液滴定至终点,求软锰矿的氧化能力(以已知)(8分)5.测定肥皂中氯化钠的含量。
称取试样5.25g,溶解后加入c(AgNO)=0.10263mol/L的硝酸银标准溶液25.00mL,定容至200.0mL,过滤后取滤液100.0mL,用c(NHSCN)=0.1010 mol/L的硫氰酸氨标准溶液滴定至终点,耗去12.01mL。
已知4氯化钠的摩尔质量为58.44 g/mol,求该皂中氯化钠的质量分数。
(10分)分析化学试题答案(B卷)一.选择题(30分)1.C2.A3.C4.C5.B6.B7.C8.D9.A 10.C11.B 12.B 13.D 14.A 15.D一.填空(30分)1.定性、定量、化学、仪器2.常量,1%3.0.1;0.24.移液管、滴定管、容量瓶5.8.26~10.266.3.1~4.4;红;黄;橙7.乙二胺四乙酸,七8.条件稳定常数,副反应,lg KMY ′=lg KMY-lgαY(H)9. I2,还原性,I2和Na2S2O3,氧化性10.氯离子具有还原性,硝酸具有氧化性,影响实验结果11.还原Fe3+为Fe2+,显色剂、缓冲溶液控制溶液pH为 5~6 12.0.010 mol•L-1三.计算题(共40分)1. 67.43%(1分), 0.04%(2分), 0.05%(2分)2.c(HCl)=0.1106 mol/L (5分)3. c(EDTA)=0.01008 mol/L (5分)TEDTA/ZnO= 8.204×10-4g/mL (3分)(4分)4. 77.36% (8分)5.ω(NaCl)=0.155%(10分)。
