氯元素的发现史
4.2富集在海水中的元素氯
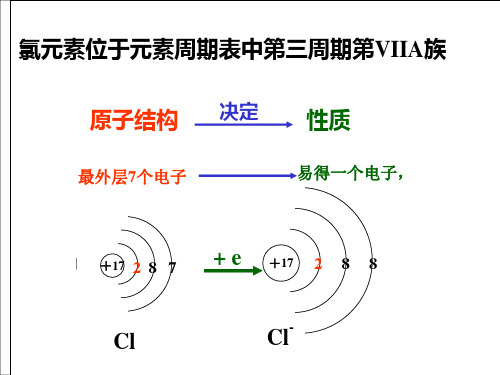
决定
结构
性质
体现
决定
用途
体现
请看故事
话说第一次世界大战期间,德国法西斯曾利
用我发动了惨无人道的战争。一次德军与英、法 军战士在比利时的伊普尔对峙,黎明时,英法军 前线战壕的士兵突然看到一股阴森森的黄绿色气 体逐渐向前袭来,(这是德军用炮弹施放了我) 一时间黄烟滚滚,风沙大作,随着风势剧增,但 见无数士兵大咳不止,疼痛难忍,以致精神失常, 倒地身亡,阵地上陈尸千万,使我犯下了滔天罪 行。在此,我这个不孝的子弟氯气,向大家谢罪, 我要改过自新,为人类造福。
点燃 2Na + Cl2 === 2 NaCl
反应规律:生成高价的氯化物
? FeCl3和CuCl2能用它们的金属与盐 酸反应制取吗?
一定条件(点燃或光照)下氯气能与氢气反应
实验现象
纯净的氢气可以在氯气中安静地燃烧,发 出苍白色火焰,放出大量的热,瓶口有白 雾产生;生成的气体HCl有刺激性气味, 极易溶于水,遇空气中水蒸气,呈现雾状。 HCl的水溶液叫氢氯酸,亦称盐酸。
A、280mL
B、440mL
C、500mL
D、720mL
8、氯气能使湿润的蓝色石蕊试纸
A、褪色
B、变成红色
C、先褪色后变红 D、先变红后褪色
A 、9∶4∶2 B、9∶4∶1
C、2∶1∶1 D、2∶1∶1
7、标准状况下,有O2和Cl2组成的混合气体共 500mL,通入H2使其恰好完全燃烧,用水吸收 生 成 物 得 250mL 溶 液 , 从 中 取 出 25mL , 用 0.125mol.L-1NaOH溶液20mL恰好中和,则与混 合气体反应的H2的体积为
光
2HClO=2HCl+O2↑
化学元素发现历史

化学元素发现历史化学元素的发现史1 H 氢 1766年,英国卡文迪许(731-1810)发现2 He 氦 1868年,法国天文学家让逊(1824-1907)和英国洛克尔(1836-1920)利用太阳光谱发现。
1895年,英国化学家莱姆塞制得。
3 Li 锂 1817年,瑞典人J.A.阿弗事聪在分析锂长石时发现4 Be 铍 1798年,法国路易.尼古拉.沃克兰发现5 B 硼 1808年,英国戴维、法国盖.吕萨克和泰纳尔发现并制得6 C 碳古人发现7 N 氮 1772年,瑞典舍勒和丹麦卢瑟福同时发现氮气,后由法国拉瓦锡确认为一种新元素8 O 氧1771年,英国普利斯特里和瑞典舍勒发现9 F 氟1786年化学家预言氟元素存在,1886年由法国化学家莫瓦桑用电解法制得氟气而证实10 Ne 氖 1898年,英国化学家莱姆塞和瑞利发现11 Na 钠 1807年,英国化学家戴维发现并用电解法制得12 Mg 镁 1808年,英国化学家戴维发现并用电解法制得13 Al 铝中国古人发现并使用。
(1825年,丹麦H.C.奥斯特用无水氯化铝与钾汞齐作用,蒸发掉汞后制得)14 Si 硅 1823年,瑞典化学家贝采尼乌斯发现它为一种元素15 P 磷 1669年,德国人波兰特通过蒸发尿液发现16 S 硫古人发现(法国拉瓦锡确定它为一种元素)17 Cl 氯1774年,瑞典化学家舍勒发现氯气,1810年英国戴维指出它是一种元素18 Ar 氩 1894年,英国化学家瑞利和莱姆塞发现19 K 钾 1807年,英国化学家戴维发现并用电解法制得20 Ca 钙 1808年,英国化学家戴维发现并用电解法制得 21 Sc 钪1879年,瑞典人尼尔逊发现22 Ti 钛 1791年,英国人马克.格列戈尔从矿石中发现23 V 钒 1831年,瑞典瑟夫斯特木研究黄铅矿时发现,1867年英国罗斯特首次制得金属钒24 Cr 铬 1797年,法国路易.尼古拉.沃克兰在分析铬铅矿时发现25 Mn 锰 1774年,瑞典舍勒从软锰矿中发现26 Fe 铁古人发现27 Co 钴 1735年,布兰特发现28 Ni 镍中国古人发现并使用。
卤素元素的发现顺序

卤素元素的发现顺序
卤素元素是指位于元素周期表第七族中的五种元素,包括氟、氯、溴、碘和石碳酸,它们在化学性质上具有相似的特点,如高亲电性、强氧
化性和易揮发性等。
这些元素的发现顺序是一个非常有趣的历史故事,下面就让我们分点分布来了解一下吧。
一、氯元素
1. 1774年,瑞典化学家卡尔·威廉·谷神父通过对盐酸的实验发现了氯,但当时他并没有认出这是新元素。
2. 1810年,英国化学家霍夫曼利用电化学方法成功制备出氯元素,并确认了它是一种新元素。
二、碘元素
1. 1811年,法国化学家布尔丹和柯尔德发现一种新的化合物,它能产生紫色的蒸气,这种物质后来被称为碘化氢。
2. 1812年,英国化学家戈登从碘化氢中成功分离出了碘元素。
三、溴元素
1. 1825年,法国化学家巴罗瓦通过实验获得了溴酸,但他并没有真正地分离出溴元素。
2. 1826年,德国化学家巴利在海水中发现了一种新的元素,它能够与铁离子形成红棕色的化合物,这就是溴元素。
四、氟元素
1. 1886年,美国化学家莫尔斯利和汉福德通过电解氟化铝得到了纯氟元素。
2. 这是最后一个被发现的卤素元素,也是最具挑战性的元素之一。
五、石碳酸
1. 1898年,法国化学家莫伦发现了一种新的无机物质,它能够与铵盐反应产生沉淀,这就是石碳酸。
2. 石碳酸并不是一种卤素元素,但由于它在性质上与卤素元素十分相似,所以通常也被归为卤素元素的一员。
以上就是卤素元素的发现顺序。
通过对这些元素的研究,我们可以更好地理解它们的化学性质,并且应用于日常生活和工业生产中。
关于氯的知识点总结

关于氯的知识点总结1. 氯的性质氯是一种具有刺激性气味和呈现黄绿色的气体。
它是一种高度活泼的元素,在常温常压下以二原子分子(Cl2)的形式存在。
而在化合物中,氯离子以Cl-的形式存在。
氯的密度比空气大约2.5倍,但是它几乎无溶解性。
气态氯具有很强的氧化性,能够与绝大多数金属和非金属发生反应,有些反应还很剧烈。
此外,氯具有很强的毒性,长期接触会对人体健康产生危害。
2. 氯的用途氯的用途非常广泛,主要包括以下几个方面:(1)工业生产:氯广泛应用于化工行业,作为制取氯化物、各种有机氯化物、氯胺类杀菌剂、医药中间体等的原料。
(2)水处理:氯被广泛应用于工业生产和日常生活中的水处理,用于消毒和杀菌。
氯气或次氯酸盐是目前最常见的水处理消毒剂。
(3)医疗卫生:氯化合物被应用于制备药物、诊断试剂和消毒杀菌用品。
氯也是一种重要的医疗用途消毒剂。
(4)制冷剂:氯气被用作一种重要的工业制冷剂,在制冷技术中发挥重要作用。
3. 氯的历史氯元素最早由瑞典化学家卡尔·威廉·舍勒于1774年在氢氯酸钠中发现。
1807年,英国化学家亨利·戈德发现了氯气,并将其命名为“氯”,来自于古希腊单词“chloros”,意为“黄绿色”。
在19世纪中叶,法国化学家雅克·路易斯·盖伊-吕萨克首次工业生产氯气。
20世纪上半叶,氯被广泛应用于工业生产、医疗卫生和日常生活中,并成为工业化社会中不可或缺的重要元素。
4. 氯的环境影响氯在人类社会的发展中发挥了重要作用,但它也对环境产生了一定的影响。
氯的工业生产和使用会产生大量废气、废水和废渣,其中含有氯化物、有机氯化合物、氯酸盐等。
这些废物对环境和生物系统造成毒性和污染,对人类健康和环境保护产生危害。
此外,氯化合物在自然界中难以降解,对土壤和水体的持久性污染也是一个严重问题。
因此,科学家和环保人士一直致力于研究氯的环境影响,并提出了一系列环境保护措施,以减少氯污染对环境和生物系统的影响。
第四章第二节——氯

漂白粉的漂白原理:它的水溶液与空气中的CO2接触 反应生成次氯酸的过程。 Ca(ClO)2 + CO2 + H2O === CaCO3↓ + 2HClO
5.与盐溶液的反应
与FeCl2 、NaBr、KI等盐溶液反应(表现氯气的强 氧化性) 2Fe2+ + Cl2 === 2Fe3+ + 2Cl-
原因: AgNO3溶液除可以与Cl-形成
AgCl白色沉淀外,还可以与CO32形成AgCO3白色沉淀,但AgCl不与 稀硝酸反应; AgCO3可与稀硝酸反应, 沉淀溶解。
[小结]
氯离子检验的一般步骤:
加硝酸银溶液 加稀硝酸
①待测液 ②待测液
白色沉淀 白色沉淀
加稀硝酸
加硝酸银溶液
科学视野 成盐元素
卤素
1. 氯气与金属反应
2Na + Cl2 == 2NaCl 反应现象 现象: 剧烈燃烧,发出黄色火焰,生成白色的烟 Cu +Cl2 == CuCl2
点燃 点燃
点燃
反应现象
现象:剧烈燃烧,生成棕黄色的烟。 2Fe +3Cl2 == 2FeCl3 反应现象 现象: 剧烈燃烧,生成棕色的烟。
反应规律:1、氯气可与大多数金属(除Au、Pt外)反 应,生成高价金属的氯化物
性 有氧化性, 质 无酸性和 漂白性
只有酸性
实验室中使用的氯水只能现配现用,并盛放在棕色试剂瓶中
思考与交流
4.氯气与碱溶液的反应
1.漂白液 制法:Cl2与NaOH溶液反应 Cl2 + 2NaOH == NaCl + NaClO + H 2O
高一化学 第二节 氯 课件

相 同 点:最外层7个电子 核电荷数递增 递变规律: 电子层数递增 原子半径依次增大
氯气的化学性质
和金属反应 2Na + Cl2 == 2NaCl
H2 + Cl2 == 2HCl
点燃 点燃
和非金属反应
和水反应 Cl2 + H2O == HCl + HClO
和碱反应 2NaOH + Cl2 == NaCl + NaClO + H2O
元素的金属性和非金属性递变小结
H Li
金 属 性 逐 渐 增 强
Na
F Cl Br I At
非 金 属 性 逐 渐 增 强
K Rb Cs
三、卤素单质及其化合物的用途
1.碘单质(Ⅰ2)被用于制作碘酊 (别名:碘酒)
用于一般皮肤消毒和 手术前手术局部皮肤的 消毒 。
2.溴化银(AgBr)被用于制作感光胶卷 和变色玻璃
②、
氧化性: Cl2>Br2>I2 还原性:I->Br->Cl-
单质的氧化性越强,阴离子的还原性越弱
元素非金属性强弱判断依据:
1.根据非金属单质与H2化合生成氢化物的难易 或氢化物的稳定性程度。越容易与H2化合,则 生成的氢化物越稳定,非金属性越强。 2.根据非金属元素最高价氧化物对应的水化物 酸性强弱。酸性越强,则元素的非金属性越强。 3. 根据对应阴离子还原性强弱判断。阴离子还 原性越弱,则元素非金属性越强。
感光胶卷
变色眼镜
原理: 2AgBr
光照
CuO 无色透明晶体 黑色小颗粒
2Ag+Br2
暗红色
3.碘化银(AgⅠ)被用于人工降雨
500℃
光
生成氢化物的 稳定性 HF很稳定 HCl稳定
富集在海水中的元素——氯ying

四.氯气的实验室制法
在实验室里,氯气可以用浓盐酸与二氧化锰共热来制取
原 理 MnO2+4HCl(浓)== MnCl2 + Cl2 ↑ + 2H2O
氧化剂 还原剂 还原产物 氧化产物
实 验 装 置
实验室制氯气的其它方法: 2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
(溶液由浅绿色变成棕黄色)
2Br― +Cl2==2Cl―+Br2 ④ 与溴化钾溶液反应:_________________________
三、氯离子(Cl-)的检验
?
某溶液中加入AgNO3溶液产生白色沉淀,则可确 定该溶液中一定有氯离子,这种说法对不对? + + Cl– == AgCl CO32- == Ag2CO3 2Ag+ Ag2CO3 +
2NaOH+Cl2=NaClO+NaCl+H2O 2Ca(OH)2+2Cl2==Ca(ClO)2+CaCl2+2H2O 漂白粉、漂粉精
有效成分 :
想一想
Ca(ClO)2 氯气跟碱反应的化学方程式有规律吗? 氯气+碱 氯化物+次氯酸盐+水
1789年,英国化学家台奈特就是把Cl2通入石灰 乳中制成了漂白粉,将HClO的漂白性从实验室带 进了“寻常百姓家”。
3.强氧化性
漂白作用
可用于自来水的杀菌、消 毒,也可用做漂白剂。
实验4-4及4-5
现象: 干燥红纸没有褪色,润湿红纸褪色。
氯水(氯气溶于水)成分的分析
1、氯水呈黄绿色说明有: Cl2 2、加入碳酸钠溶液有气体说明有:H+ 3、氯水能杀菌、消毒、漂白说明有: HClO 4、滴加硝酸银有白色沉淀说明有:Cl5、滴有硫氰化钾的硫酸亚铁溶液中加入 新制的氯水变血红色,说明有:Cl2
最帅的化学家——戴维!(下)

最帅的化学家——戴维!(下)话说拉瓦锡最早将生石灰纳入他的第一张元素表中,戴维在电解了苛性钠、苛性钾以后,将目光对准了生石灰。
在当时,生石灰和苦土(氧化镁)、重晶石(硫酸钡)、碳酸锶合称碱土,因为它们的化合物都有着碱的特性,溶液可以让石蕊试纸变蓝。
戴维想,既然苛性碱都被电解了,就用同样的方法电解碱土。
可是一切并不像戴维想的那么顺利,电流经过的导线上似乎出现了金属的薄膜,但瞬间就变暗了。
他建造了更大的电池组,可是事倍功半,只得到几小粒新的金属,还是跟铁丝的合金。
▲钙的发现者又是戴维。
(哎,我为什么要说又啊?)在戴维一筹莫展的时候,贝采尼乌斯出马了。
他写信给戴维,劝戴维不要用铁丝,而是用一个水银柱来通电。
戴维一看就明白了,新的金属分离出来以后,溶解在水银里,形成汞齐,之后再将水银蒸发掉,剩下的当然就是纯的新金属。
戴维使用这种方法,一下子将钙、镁、钡、锶四种碱土元素都提取了出来,因为钙是从白垩中提取出来的,所以用白垩(拉丁文calcis)来命名这种新元素:Calcium。
戴维没有花多少时间去研究这些新的碱土元素,因为它们正是如自己预言的那样出现了:“之所以会认为钾有问题(轻、在水面上跳舞等),是因为我们看惯了旧金属,我们一定会再发现几种新金属,将钾和铁之间的空隙完全填满。
”▲钙,银白色的金属光泽。
除了上述几种元素以外,戴维 1808年试图电解硼酸盐的水溶液,得到了一些棕色的沉积物,他认为这可能是一种元素。
后来他用钾去还原三氧化二硼,得到了一定数量棕色的硼,他也借此宣布这是一种新元素,成为硼元素的发现者。
后来,法国科学家盖吕萨克在高温下用铁还原硼酸得到了硼,证明了硼酸是硼的氧化物。
但是,由于硼在高温下极易与氧化合,因此他俩制得的硼都不纯。
一直到1909年,美国化学家EzekielWeintraub才制得了纯硼。
▲高纯的硼是这样的,从分解出硼到纯硼的制得,花了100年时间。
就这样,戴维总共发现了钾、钠、镁、钙、锶、钡、硼七种元素,是发现自然元素最多的化学家,堪称“元素之王”!他并没有停止努力,而是准备用他的利器电流来挑战化学元素界的最高难度——分解氟化物。
氯气的发现与制备—孟明哲

实质:-1价的氯离子在酸性环 Nhomakorabea下被氧化为0 价的氯气
盐酸的作用: 还原剂和酸
思考:
1.为什么要用浓HCl,用稀HCl行吗? 答:不行。浓HCl比稀HCl的还原性强,稀HCl不反应 2.用浓NaCl溶液行吗? 答:不行。反应必须在酸性条件下才能进行
练习1、某化学兴趣小组利用MnO2和浓盐酸及如图装置制备氯气。下列分析中不正 确的是 A.①中可用分液漏斗代替长颈漏斗 B.①中缺少加热装置
或
氯气的收集和尾气处理装置
Cl2 Cl2
有毒气体必需 进行尾气处理
收集 装置
NaOH
尾气处理 装置
4、制备氯气
(1)连接仪器:从下到上,从左到右
(2)检查气密性: 关闭分液漏斗开关,用酒精灯微热,有气泡生成,冷 却后导管中能形成一段稳定的水柱说明气密性良好
(3)加药品
固体药品 液体药品
圆底烧瓶 分液漏斗
6.验满方法
将湿润的淀粉KI试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证 明已集满
Cl2 + 2 KI =I2 + 2KCl
探究反应实质
∆ 4HCl(浓) + MnO2 =MnCl2 + 2H2O + Cl2
-1
+4 ∆+2
0
2Cl +4H+ + MnO2 =Mn2+ + 2H2O + Cl2
专题3 从海水中获得的化学物质
3.1.1 氯气的发现与制备
平泉一中化学教师孟明哲
浩翰的大海
海水晒盐
有数据指出,每一立方千米的海水 中含氯化钠4×107t,而氯气又是重要的化 工原料,那么是谁发现了氯气,实验室和 工业生产中怎样制备氯气呢?
氯

启示
启示1:科学研究需要有正确的理论作指导, 启示1 科学研究需要有正确的理论作指导, 错误的理论只能浪费时间和精力。 错误的理论只能浪费时间和精力。 启示2:科学研究需要以大量事实为依据,只 启示2 科学研究需要以大量事实为依据, 的理论, 有大量事实才能推翻错误 的理论,建立正确 的理论或推动科学理论的发展。 的理论或推动科学理论的发展。 启示3 启示3:科学研究需要有热爱科学的思想和奉 献科学的精神。 献科学的精神。
氯气的特殊性
4、氯气和碱溶液的反应 、 [推测 根据前面所学知识,推的方程式 溶液反应的方程式 Cl2 + 2NaOH == NaCl + NaClO +H2O
漂白粉的制取
方法: 氯气通入 通入石灰乳 方法 将氯气通入石灰乳
说明书
漂白粉(次氯酸钙) 漂白粉(次氯酸钙) 化学式( 化学式(Ca(ClO)2) 写出相应的方程式 性状: 性状:漂白粉为白色粉 末固体, 末固体, 主要用作染 2Ca(OH)2 + 2Cl2 == CaCl2 、医药、矿业行业的2H2O Ca(ClO)2 + 料 +医药、 水处理;自来水消毒、 水处理;自来水消毒、 游泳池、鱼塘杀菌, 游泳池、鱼塘杀菌,蔬 主要成分 有效成分 饲养场的消毒、 菜、饲养场的消毒、净 水
科学史话-----氯的发现史 氯的发现史 科学史话
吕萨克和泰纳的实验 盖吕萨克和泰纳的实验,对盐酸的组成作出 吕萨克和泰纳的实验, 了正确的结论, 了正确的结论,但是氯气在他们的眼里仍然是 一种化合物 因为法国的化学家拉瓦锡 化合物。 法国的化学家拉瓦锡, 一种化合物。因为法国的化学家拉瓦锡,在提 出燃烧的氧化理论的时候,也提出了“ 出燃烧的氧化理论的时候,也提出了“氧是成 酸元素”的论点,认为一切酸的成分都有氧, 酸元素”的论点,认为一切酸的成分都有氧, 这个观点深深地印在广大化学家的脑子里
卤族元素的发现史及其性质

1886年,法国化学家莫瓦桑采取液态氟化氢作电解质,并 在这种不导这么多化学家的努力,虽然都没有制得单质氟, 但他们的经验和教训都是极为宝贵的,为后来制取氟创造 了有利条件。
电的物质中加入一种导电体进行实验,发现在阳极上放出 呈黄绿色的气体。氟元素终于被成功分离了!而莫瓦桑因 长期接触含氟的剧毒气体,年仅54岁便与世长辞。
u大家熟悉的红药水,也是溴与汞的化合物.此外,青霉素等抗菌素 生产也需要溴,溴还是制造农业杀虫剂的原料.
u溴可以用来制作防爆剂.把溴的一种采购化合物与铅的一种有机 化合物同时掺入汽油中,可以有效地防止发动机爆烯.
3.溴的用途
灭火器中也有溴,我们平时看到的诸如“1211”灭火 器,就是分子里面有一个溴原子的多卤代烷烃,不仅 能扑灭普通火险,在泡沫灭火器无法发挥作用的时候, 例如油火,它也能扑灭火险.
u现在医院里普遍使用的镇静剂,有一ห้องสมุดไป่ตู้就是用溴 的化合物制成的,如溴化钾、溴化钠、溴化铵等, 通常用以配成“三溴片”,可治疗神精衰弱和歇 斯底里症。
➢ 1825年德国海德堡大学学生罗威把家乡克罗次纳的一种矿
泉水通入氯气,产生一种红综色的物质。这种物质用乙醚提 出,再将乙醚蒸发, 则得到红综色的液溴。所以他也是独 立发现溴的化学家。
2.溴的性质
液溴,在常温下为深红棕色液体,可溶于水,100克水能溶解约 3克溴。挥发性极强,有毒,蒸气强烈刺激眼睛、粘膜等。水溶 液称为溴水。溴单质需要存储容器的封口带有水封,防止蒸气 逸出危害人体。有氧化性,有多种可变化合价,常温下与水微 弱反应,生成氢溴酸和次溴酸。加热可使反应加快。氢溴酸是 一种强酸,酸性强于氢氯酸。溴一般用于有机合成等方面。还 可用于一些物质的萃取(如碘)
118种化学元素科技发现史

118种化学元素科技发现史前5000年原子序82 铅:Pb 铅古人发现。
前4000年原子序29 铜:Cu 铜古人发现。
前3100年原子序51 锑:Sb 锑古人发现。
前2600原子序79 金:Au 金古人发现。
前2000年原子序26 铁:Fe 铁古人发现。
前1500年原子序80 汞:Hg 汞古希腊人发现。
三千年前原子序30 锌:Zn 锌中国古人发现。
前7世纪原子序50 锡:Sn 锡古人发现。
前600年原子序47 银:Ag 银古人发现。
317原子序33 砷:As 砷公元317年,中国葛洪从雄黄、松脂、硝石合炼制得,后由法国拉瓦锡确认为一种新元素。
14501669原子序15 磷:P 磷1669年,德国人波兰特通过蒸发尿液发现。
1735原子序27 钴:Co 钴1735年,布兰特发现。
1735原子序78 铂:Pt 铂1735年,西班牙安东尼奥.乌洛阿在平托河金矿中发现,1748年有英国化学家W.沃森确认为一种新元素。
1751原子序28 镍:Ni 镍中国古人发现并使用。
1751年,瑞典矿物学家克朗斯塔特首先认为它是一种元素。
1766原子序1 氢:H 氢1766年,英国贵族亨利.卡文迪西(1731-1810)发现。
氢[hydrogen],金属氢[Hydrogenium]。
气体元素符号。
无色无臭无味。
是元素中最轻的。
工业上用途很广。
1770原子序16 硫:S 硫古人发现(法国拉瓦锡确定它为一种元素)。
1771原子序8 氧:O 氧1771年,英国普利斯特里和瑞典舍勒发现;中国古代科学家马和发现(有争议)。
1772原子序7 氮:N 氮1772年,瑞典化学家卡尔.威廉.舍勒和法国化学家拉瓦节和蘇格兰化学家丹尼尔.卢瑟福(1749-1819) 同时发现氮气。
1774原子序17 氯:Cl 氯1774年,瑞典化学家舍勒发现氯气,1810年英国戴维指出它是一种元素。
1774原子序25 锰:Mn 锰1774年,瑞典舍勒从软锰矿中发现。
氯元素相关的知识

氯元素氯,原子序数17,原子量35.4527,氯单质为黄绿色气体,有窒息性臭味;熔点-10 0.98°C,沸点-34.6°C,气体密度3.214克/升,20°C时1体积水可溶解2.15体积氯气。
氯相当活泼,湿的氯气比干的还活泼,具有强氧化性。
除了氟、氧、氮、碳和惰性气体外,氯能与所有元素直接化合生成氯化物;氯还能与许多化合物反应,例如与许多有机化合物进行取代反应或加成反应。
氯的产量是工业发展的一个重要标志。
氯主要用于化学工业尤其是有机合成工业上,以生产塑料、合成橡胶、染料及其他化学制品或中间体,还用于漂白剂、消毒剂、合成药物等。
氯气具有毒性,每升大气中含有2.5毫克的氯气时,即可在几分钟内使人死亡氯元素通常的化合价态:-1,0,+1,+2,+3,+4,+5,+7[编辑本段]结构①原子结构:氯原子最外层有7个电子,反应中易得到1个电子或共用一个电子对达到稳定结构。
②分子结构:氯分子为双原子分子,分子式Cl₂③离子结构:氯离子最外层有8个电子,因而很稳定原子和离子左为氯离子右为氯原子[编辑本段]物理性质①颜色\气味\状态:通常情况下为有刺激性气味的黄绿色的气体。
②密度:比空气密度大,标况时是71/22.4=3.17g/L 。
③易液化。
熔沸点较低,压强为101kPa、温度为-34.6℃时易液化。
液态氯为金黄色。
如果将温度继续冷却到-101℃时,液氯变成固态氯。
液氯④溶解性:易溶于有机溶剂,难溶于饱和食盐水。
1体积水在常温下可溶解2体积氯气,形成盐酸和次氯酸,产生的次氯酸具有漂白性,可使蛋白质变质,且见光易分解。
[编辑本段]化学性质化学式:Cl₂①毒性氯气是一种有毒气体,它主要通过呼吸道侵入人体并溶解在黏膜所含的水分里,生成次氯酸和盐酸,对上呼吸道黏膜造成有害的影响:次氯酸使组织受到强烈的氧化;盐酸刺激黏膜发生炎性肿胀,使呼吸道黏膜浮肿,大量分泌黏液,造成呼吸困难,所以氯气中毒的明显症状是发生剧烈的咳嗽。
氯元素相关的知识

氯元素氯,原子序数17,原子量35.4527,氯单质为黄绿色气体,有窒息性臭味;熔点-10 0.98°C,沸点-34.6°C,气体密度3.214克/升,20°C时1体积水可溶解2.15体积氯气。
氯相当活泼,湿的氯气比干的还活泼,具有强氧化性。
除了氟、氧、氮、碳和惰性气体外,氯能与所有元素直接化合生成氯化物;氯还能与许多化合物反应,例如与许多有机化合物进行取代反应或加成反应。
氯的产量是工业发展的一个重要标志。
氯主要用于化学工业尤其是有机合成工业上,以生产塑料、合成橡胶、染料及其他化学制品或中间体,还用于漂白剂、消毒剂、合成药物等。
氯气具有毒性,每升大气中含有2.5毫克的氯气时,即可在几分钟内使人死亡氯元素通常的化合价态:-1,0,+1,+2,+3,+4,+5,+7[编辑本段]结构①原子结构:氯原子最外层有7个电子,反应中易得到1个电子或共用一个电子对达到稳定结构。
②分子结构:氯分子为双原子分子,分子式Cl₂③离子结构:氯离子最外层有8个电子,因而很稳定原子和离子左为氯离子右为氯原子[编辑本段]物理性质①颜色\气味\状态:通常情况下为有刺激性气味的黄绿色的气体。
②密度:比空气密度大,标况时是71/22.4=3.17g/L 。
③易液化。
熔沸点较低,压强为101kPa、温度为-34.6℃时易液化。
液态氯为金黄色。
如果将温度继续冷却到-101℃时,液氯变成固态氯。
液氯④溶解性:易溶于有机溶剂,难溶于饱和食盐水。
1体积水在常温下可溶解2体积氯气,形成盐酸和次氯酸,产生的次氯酸具有漂白性,可使蛋白质变质,且见光易分解。
[编辑本段]化学性质化学式:Cl₂①毒性氯气是一种有毒气体,它主要通过呼吸道侵入人体并溶解在黏膜所含的水分里,生成次氯酸和盐酸,对上呼吸道黏膜造成有害的影响:次氯酸使组织受到强烈的氧化;盐酸刺激黏膜发生炎性肿胀,使呼吸道黏膜浮肿,大量分泌黏液,造成呼吸困难,所以氯气中毒的明显症状是发生剧烈的咳嗽。
氯

氯,CHLORINE,源自chloros,意为“绿黄”,1774年发现。
它能和其他元素化合的数目,差不多和氟一样多,只是略逊一筹而已。
它有足够的强烈作用力,能用来制造漂白剂,本身是一种消毒剂和有毒的气体。
纯氯通常是由电解食盐(NaCl)所收集来的。
氯的发现简史卡尔·威廉·舍勒(K.W.Scheele,1742-1786)在1774年,瑞典化学家舍勒(Scheele K W,1742-1786)在从事软锰矿的研究时发现:软锰矿与盐酸混合后加热就会生成一种令人窒息的黄绿色气体,这种气体微溶于水,使水显酸性。
能漂白有色花朵和绿叶,还能和各种金属发生反应。
当时,大化学家拉瓦锡认为氧是酸性的起源,一切酸中都含有氧。
舍勒及许多化学家都坚信拉瓦锡的观点,认为这种黄绿色的气体是一种化合物,是由氧和另外一种未知的基所组成的,所以舍勒称它为“氧化盐酸”。
但英国化学家戴维(Davy S H,1778-1829)却持有不同的观点,他想尽了一切办法也不能从氧化盐酸中把氧夺取出来,他怀疑氧化盐酸中根本就没有氧存在。
1810年,戴维以无可辩驳的事实证明了所谓的氧化盐酸不是一种化合物,而是一种化学元素的单质。
他将这种元素命名为“Chlorine”。
它的希腊文原意是“绿色”。
中文译名为氯。
汉弗莱·戴维(Humphry·Davy,1778—1829)氯单质及其性质氯气Cl2是一种黄绿色的气体,标准状况下,1LCl2重3.21g大约是同体积空气质量的倍。
Cl2极易液化,如果使之冷却至239K或常温时在0.6MPa下,氯气就会变成黄绿色油状液体。
液氯在172K还可以凝固成黄色固体。
氯气具有强烈的窒息气味,有毒!吸入少量时会刺激鼻腔和喉头黏膜,引起胸部疼痛和咳嗽,吸入大量就会窒息死亡。
发生氯气中毒时可吸入酒精和乙醚的混合蒸气作为解毒剂。
吸入氨水蒸气也有效。
氯气可用于纸浆和棉布的漂白,也可用于饮水的消毒。
氯的发现史

氯的发现史化学元素是组成我们日常生活的基本物质,它们的发现和研究对人类产生了极为重要的影响。
在众多元素之中,氯是一种具有极为重要意义的元素。
本文将从历史和化学角度,介绍氯的发现史。
历史部分早在古希腊时期,人们发现了一种盐酸,但当时并不知道其中的化学元素。
直到1774年,瑞典化学家舒尔茨( C.W. Scheele )使用盐酸和银制备了一种白色沉淀,即今天所知的氯化银。
通过实验,舒尔茨猜测这种沉淀可能是一种新的化学元素。
但是,他当时只限于初步实验,没有发表相关研究成果。
随后,在1810年左右,英国化学家戈尔顿( H. Davy )研究氯气和氯化物的性质,也从实验中发现类似舒尔茨的白色沉淀。
他使用电解法将氯气和水分离,得到了一个稳定的氧化物。
这个方法被证明非常有用,为后来卡斯珀·尼科尔斯·埃加德( Caspar Niemann Egart )采用分析技术研究氯气银化核的方法提供了基础。
1842年,法国化学家巴利安提出,氯化物不能凭空存在,因为氯取代汞成ol的珠子要比汞多出”胶状物”来。
他简单地替换了汞离子为铵离子,并更改了实验条件,得出了关于氯离子结构和性质的详尽数据。
他的理论和实验为今天仍广泛流行的原子价理论奠定了基础。
化学部分氯是第三组卤素元素,是一种非常活泼的化学元素,其化学性质独特而广泛。
氯的原子序数是17,元素符号为Cl。
氯的原子密度比空气大2.5倍,具有刺激味,能深入呼吸道,引起高度的昏迷和窒息。
氯的轻、重同位素都具有放射性,而且有大量的放射性同位素。
其中,放射性同位素氯-36被广泛应用于岩石测年、血流量测量和气储量测量领域。
此外,氯和氢能形成氫氯化物,也称为盐酸,是制造纸张和塑料等工业材料的重要原料。
值得一提的是,氯的主要用途之一是用于水处理和消毒。
氯气加入水中后,会形成次氯酸和水解产物,能够有效地杀灭水中的细菌和病毒,保障人们的生命健康。
但同时,水中的氯也可能对人体健康产生潜在的危害。
[课外阅读]氯气的故事
![[课外阅读]氯气的故事](https://img.taocdn.com/s3/m/2ea52769e2bd960590c67788.png)
[课外阅读]氯气的故事古代的炼金术士们用王水(一般用三份盐酸与一份硝酸相混合)溶子。
当他们在实验室里加热王水的时候,便会发生一种刺激性很强的烟雾,当时他们还不知道这种烟雾就是氯气,然而至少可以说,古炼金术就已经接触过氯这种元素了。
氯气的发现应该归功于瑞典化学家舍勒(1742年~1786年),他是在1774年发现这种气体的,当他加热黑色的二氧化锰与盐酸的混合物时,发现产生了一种烟雾,并与加热王水时所生成的烟雾是完全一样的。
在氯这种元素被发现以后,当时人们把它叫做脱燃素的盐酸气,因为按照当时流行的说法,把盐酸中所含的氢称为燃素,这样在制备氯气的过程中,锰取盐酸中的氢,从而得到氯气,用当时的术语便是锰取燃素,因此就被叫做盐酸脱掉燃素以后产生的一种气体。
舍勒制备了氯气以后,把它溶解在水中,却发现这种水溶液对纸张、蔬菜和花都具有水久性的漂白作用;他还发现氯气能与金属氧或金属化合物发生化学反应。
从1774年舍勒发现氯气以后,一直到1810年,这种气体的性质先后经过贝托霍、拉瓦锡、盖一吕萨克、泰纳、贝采利乌斯等人的研究,然而第一个指出氯气是一种化学元素的科学家却是戴维,他在伦敦英国皇家学会上宣布这种由舍勒发现的气体是一种新的化学元素,它在盐酸中与氢化合。
他将这种化学元素定名为氯,这个名称出自希腊文“Chloros”,这个词有多种解释,例如“绿色”“绿色的”“绿黄色”或“黄绿色”。
戴维的这种推论获得了公认,只有贝采利乌斯持有异议,因为他一直认为盐酸是一种含有氧的酸。
1785年贝莱梯,1786年卡斯登各自在有水汽存在的情况下,将舍勒所发现的这种气体加以冷却,随后他们便获得了一种黄色结晶物质(实际上它就是氯的水合物),他们暗示,舍勒所发现的气体不是一种简单的物质,当然就不是一种化学元素。
1805年诺斯莫尔将这种气体液化,他在描述其实验时说:“当我把这种含氧的盐酸气(诺斯莫尔和贝采利乌斯的认识是一样的,他们都认为氯气是盐酸与氧气的化合物,所以把这叫做含氧的盐酸气)压缩1 到一个2 英寸的接受容器中,它立刻转变成了一种黄色的液体,它在普通4 的大气压力下具有极大的挥发性,当把耐压的接受容器的阀门打开时,这种液体物质便立即完全挥发了。
氯的发现史

氯的发现史
氯是一种非常重要的元素,它在生活中有着广泛的应用。
然而,氯的发现史却并不是一帆风顺的。
下面,我们就来看看氯的发现史。
氯的发现可以追溯到17世纪。
当时,人们已经知道了许多元素,但是氯却一直没有被发现。
直到1774年,瑞典化学家卡尔·威廉·舍勒(Carl Wilhelm Scheele)在实验中发现了一种新的气体,他将其命名为“氧化酸性气体”。
这种气体后来被证明就是氯气。
然而,舍勒并没有公开发表他的发现,而是将其保密了起来。
直到一年后,英国化学家约瑟夫·普利斯特利(Joseph Priestley)也在实验中发现了氯气,并将其命名为“腐蚀气体”。
普利斯特利公开发表了他的发现,并将氯气的性质进行了详细的研究。
随着氯气的发现,人们开始研究它的性质和应用。
在19世纪初期,氯气被用于消毒和漂白。
然而,氯气有着强烈的刺激性和毒性,使用起来非常危险。
因此,人们开始寻找更加安全的氯化剂。
在1824年,英国化学家迈克尔·法拉第(Michael Faraday)发现了一种新的氯化剂——氯酸钾。
这种化合物可以在水中溶解,释放出氯离子,从而起到氯化剂的作用。
氯酸钾的发现极大地促进了氯化剂的应用,使得氯的使用更加安全和方便。
总的来说,氯的发现史经历了一个漫长的过程。
从最初的发现到氯化剂的应用,人们不断地探索和研究,最终使得氯的应用更加广泛
和安全。
今天,氯已经成为了生活中不可或缺的元素,它在消毒、漂白、制药等方面都有着重要的应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氯元素的发现史
瑞典化学家舍勒于1774年用浓盐酸与二氧化锰反应制得了氯气。
但它究竟是游离态的单质气体还是化合态的气体,仍然不清楚。
后来法国化学权威贝托雷继续研究氯气。
他首先将氯气通入一个冷的空玻璃瓶里,让氯气里的含酸蒸气受冷凝结,再将除去酸蒸气的氯气依次通入三个盛满水的瓶子使氯气溶于水。
他发现溶有氯气的水溶液,在有光照的地方可以分解成盐酸和氧气。
我们现在知道,氯和水反应生成的次氯酸在光照下分解
Cl
2 + H
2
O = HCl + HClO
2HClO = 2HCl + O
2
贝托雷以此判断出氯气是盐酸和氧结合成的:
氯=盐酸+氧基
氯气是盐酸和氧结合得很松散的化合物,因此露置在阳光下就分解了。
其实在当时人
们已经用过许多强烈的药剂或其它手段来处理氯气,都未能使它分解为盐酸和氧。
贝托雷的判断显然跟其它一些研究是矛盾的。
他得出这个错误判断的表面原因,似乎在于他忽视了水和氯气的反应。
但更深层的原因,是他深受拉瓦锡“所有的酸中都含有氧基”结论的影响。
拉瓦锡在提出燃烧的氧化理论的同时,提出了“氧是成酸元素”的论点,认为一切酸中均含有氧。
按照这一理论,盐酸应是一种氧化物的水化物,如硫酸、磷酸
一般(我们姑且把它写成 HClO
m
)。
而氯气是盐酸经二氧化锰氧化得来的,应该含有更
多的氧(即应该写成 HClO
m+n
),当时将氯气称作“氧化盐酸”。
结果氯气不仅不是一种单质,反而比盐酸具有更复杂的结构、更大的分子量。
贝托雷的实验很和“逻辑”地证明了拉瓦锡的论点。
1809年法国化学家盖.吕萨克和泰纳,用分解法研究盐酸的组成。
当时金属钾已被戴维用电解法制得,并证明钾是一种元素。
于是他们就用金属钾和铁等与盐酸气(HCl)反应,看它是不是能够放出氯气。
实验得出结果后,他们说:“我们考察金属钾对于盐酸气的反应。
在寻常温度时,这个反应很慢;但钾熔融时立刻在盐酸气中发光燃烧,结果得到氯化钾和氢。
在这个实验中收集的氢气之量,恰与钾和水接触时发生的相等。
我们在暗红热时,用盐酸气通过擦净的铁屑,许多氢气放出,而不觉有盐酸混合在内,同时得到氯化铁;残渣铁屑并没有氧化。
当中等温度时,用盐酸气通过既熔而又研成细粉的一氧化铅,又收集到氢,不过已与氧化合变成水的状态了。
”
这些实验证明,不是氯气分解成盐酸和氧,而是盐酸分解成氯和氢。
在同一年盖.吕萨克和泰纳用合成法证明了盐酸的组成。
他们把同量的氢气和氯气混合在一起,静置数日,或稍微加热,或露置日光中,都能化合成盐酸气。
这个实验证明了盐酸气是氢气和氯气的化合物,而且是这两种气体化合而成的唯一物质,其变化应该表示为:
氯+氢=盐酸气(HCl)
盖.吕萨克和泰纳的实验,对盐酸的组成作出了正确的结论,但是氯气在他们的眼里仍然是一种化合物。
原因如上文所说,拉瓦锡的“氧是成酸元素”的论点已深深地印在广大化学家的脑子里。
盖.吕萨克和泰纳是深信这个论点的,因而他们认为氯是某种“基”的氧化物。
既然氯气是某种基的氧化物,那么盐酸就应该是某种基跟氧和氢的化合物:盐酸=某种基+氧+氢
如果联系贝托雷的结论,可以看出他们的矛盾之处。
而最终解决这个问题的是戴维。
戴维在研究碲的化学性质时发现碲化氢是一种酸,但是它并不含有氧,使他开始怀疑氧是否存在于所有的酸中。
为了寻找更多的证据,戴维开始研究起盐酸。
按照拉瓦锡的观点,舍勒用浓盐酸与二氧化锰作用制得的黄绿色气体是氧化盐酸,而盐酸是由氧和另外一种未知的基所组成的,氧化盐酸则是由这种基与更多的氧化合而成的。
但是戴维想尽了一切办法也不能从氧化盐酸中把氧夺取出来。
他说:“即使木炭被伏打电堆烧成白热状态,也不能使氧化盐酸气发生任何变化,我多次重复这种实验,结果都是一样,因此我怀疑这些物质中是否存在着氧。
” 他重做盖.吕萨克和泰纳合成盐酸的实验,并证实氯和氢化合成盐酸的结论是正确的,除了稍有水的痕迹外,没有其它杂质。
既然实验中没有发现氯气或盐酸中有氧存在,为什么我们硬要说它们含有氧呢?他感到只有认为氯是一种元素,那么有关氯的所有实验才能得到合理的解释。
1810年11月,戴维在英国皇家学会宣读了他的论文,正式提出氯是一种元素。
戴维宣称,只要不存在水,氧化盐酸所发生的一切反应都不会产生氧,他认为最好把氧化盐酸看成是一种不能被分解的物质——元素。
他认为事实表明,拉瓦锡和法国化学学派所持的见解,表面看起来很漂亮,也能令人满意,但是从现在已经掌握的知识来考察,它不过是建立在假设基础上的理论。
戴维以无可辩驳的事实确认所谓的“氧化盐酸”决不是一种化合物,而是一种化学元素,他将这种元素命名为Chlorine(中译名为氯),意为黄绿色的。
他指出所有的剧烈发光、发热的反应(如铁丝、铜丝、氢气在氯气中的燃烧)都是氧化反应,氯和氧一样都可以助燃,氧化反应不一定非要有氧气参加,经氧化反应生成的酸中也不一定含有氧。
戴维在确认氯是一种单质而非化合物的同时,出色地发展了拉瓦锡的燃烧的氧化理论。
戴维还提出,在酸中氧是非本质性的,无氧酸中不含氧;但是酸中都含有氢,氢在酸中具有重要意义。
这个见解未引起人们的注意。
直到1837年,德国化学大师李比希对酸类进行了全面的综合分析研究之后,放弃了酸的二元论(酸基 + 水),振兴了戴维关于酸的氢学说。
氯气自1774年被舍勒发现,到1810年被戴维确认为是一种元素,其间经历了36年。
