食品中沙门氏菌定性 志贺氏菌 金黄色葡萄球菌检验原始记录
食品中沙门氏菌定性 志贺氏菌 金黄色葡萄球菌检验原始记录

JZJC-04-SP-48
样品编号
检验日期
环境温度
℃
环境湿度
%(RH)
检验使用仪器设备
T-200型电子天平(000000349)
电热恒温培养箱(000000011)
检验依据
GB 4789.4-2016食品安全国家标准食品微生物学检验沙门氏菌检验
GB 4789.5-2012食品安全国家标准食品微生物学检验志贺氏菌检验
试样菌在不同平板上的菌落特征
平板
试样菌的菌落特征
是否为典型或可疑菌落特征
Baird-Parker平板
血平板
结果报告:在25 g(mL)样品中金黄色葡萄球菌。
校核:检验员:
2分离取增菌后的志贺氏菌增菌液分别划线接种于XLD琼脂平板和MAC琼脂平板或志贺氏菌显色培养基平板上,于36℃,培养24 h,观察各个平板上生长的菌落形态。
试样菌在不同选择性琼脂平板上的菌落特征
选择性琼脂平板
试样菌的菌落特征
是否为典型或可疑菌落特征
MAC琼脂
XLD琼脂
志贺氏菌显色培养基
结果报告:综合以上鉴定的结果,报告25 g(mL)样品中志贺氏菌。
GB4789.10-2016食品安全国家标准食品微生物学检验金黄色葡萄球菌检验
沙门氏菌定性检验步骤及记录
1前增菌以无菌操作取检样25 g(mL),放入盛有225 mL BPW中,振荡(涡旋)混匀后,于36℃培养18 h。
2增菌轻轻摇动培养过的样品混合物,移取1 mL,转种于10 mL TTB内,于42℃培养24h。同时,另取1 mL,转种于10 mL SC内,于36℃培养24 h。
3.分离分别用接种环取增菌液1环,划线接种于一个BS琼脂平板和一个XLD琼脂平板(或HE琼脂
微生物检验原始记录
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠菌群:检验依据:GB 4789.3-2010
检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:。
熟肉抽检项目说明

嘉兴文件要求抽检项目有:菌落总数、大肠菌群、致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、副溶血性弧菌、02)、亚硝酸盐、色素
根据抽检的样品品种不同,检验项目也不同,现统一为:
1、卤味店抽检的散装熟肉制品:菌落总数、大肠菌群、致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、副溶血性弧菌、02)、亚硝酸盐(注:用于红烧的熟肉制品)
2、餐饮单位抽检的熟肉制品:
例1:白切鸡:菌落总数、大肠菌群、致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、副溶血性弧菌、02)、色素(注:与实验室已沟通,采样单写上去,由实验室决定,若颜色较黄,他们做色素,若颜色较白的,他们不做色素)
例2:猪头肉、鸭肉、鸡爪、腌制鱼等熟肉制品:菌落总数、大肠菌群、致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、副溶血性弧菌、02)、亚硝酸盐
另说明:除白切鸡外,其余色素不做,因红烧的做色素意义不大。
食品中金黄色葡萄球菌及沙门氏菌的检测分析

食品中金黄色葡萄球菌及沙门氏菌的检测分析发表时间:2018-01-22T15:02:36.540Z 来源:《中国蒙医药》2017年第16期作者:肖慧[导读] 通过PCR检测方法对速冻食品中的沙门氏菌和金黄色葡萄球菌进行检测,能够有效检测出起始菌落数量相对较低的菌落。
湖南省怀化市辰溪县疾病预防控制中心 419500【摘要】目的:对食品中的金黄色葡萄球菌和沙门氏菌进行检测,分析其检测效果。
方法:对速冻食品通过PCR检测的方式进行检测,分析检测结果。
结果:PCR检测方法能够有效检测出速冻食品中的金黄色葡萄球菌和沙门氏菌,效果显著。
结论:通过PCR检测方法对速冻食品中的沙门氏菌和金黄色葡萄球菌进行检测,能够有效检测出起始菌落数量相对较低的菌落,该方法值得在食品检测中推广使用。
【关键词】金黄色葡萄球菌;沙门菌;食品;检测;PCR检测伴随着我国经济的发展进步,生活水平也在逐步提升,饮食习惯也在发生改变。
目前速冻食品由于其营养丰富和方便快捷的特点受到了众多消费者的广泛欢迎,在我国食品工业中逐渐占据了重要的地位[1-2]。
但是,在速冻食品的食品检测中,能够发现一些食源性致病菌,最具有代表性的就是沙门氏菌和金黄色葡萄,这类细菌会影响速冻食品的安全,引发众多的人类疾病,必须对其投入足够的重视[3-4]。
为了有效保证速冻食品的安全,减少由于食品导致的人类疾病,必须及时采取确实有效的致病菌检测方法对食品安全进行检测,PCR 检测技术就是其中具有代表性的一种检测方法[5-6]。
1.一般资料与方法1.1一般资料材料和试剂:金黄色葡萄球菌、沙门氏菌、粪肠球菌、弗氏柠檬酸杆菌、大肠杆菌、坂崎肠杆菌、微球菌等供试菌群。
专用的细菌培养基。
细菌DNA提取试剂盒、引物合成、多重PCR试剂盒。
仪器和设备:高速离心机、漩涡混合器、电泳仪、凝胶图像分析仪、紫外分光光度计、梯度PCR扩增仪。
1.2方法通过查阅相关的文献研究成果,为多重PCR检测提供靶基因,包括金黄色葡萄球菌的nuc基因以及沙门氏菌的invA基因,二者引物设计如下表1所示。
微生物检验结果报告注意事项

微生物检验结果报告注意事项一、涉及定性项目的检验结果报告沙门氏菌、志贺氏菌、金黄色葡萄球菌、单核细胞增生李斯特氏菌、大肠杆菌O157:H7、空肠弯曲杆菌、副溶血性弧菌(定性)等,如果检样是称重取样,则最后检测结果一定报告为检出/25g或未检出/25g。
如果检样是体积取样,则最后检测结果一定报告为检出/25mL或未检出/25mL。
检测标准要求g必须要小写,mL中m必须小写,L则必须大写。
记录中所有有用的信息必须填上,无法填充的用“/”划掉。
二、菌落总数检验结果报告1.菌落总数小于100CFU时,按“四舍五入”原则修约以整数报告,如80.5CFU可修约报告为81CFU;80.4CFU则修约报告为80CFU。
2.菌落总数大于等于100CFU时,左边数第3位数字采用四舍五入原则修约后,取前2位数字,后面位数用0代替,也可用10的指数形式表示:如10-2两平板平均菌落数为238CFU/g,可修约为240CFU/g,最后报告为24000CFU/g或2.4×104CFU/g。
3.霉菌、酵母菌、乳酸菌、蜡样芽孢杆菌、产气荚膜梭菌报告形式和菌落总数一样。
4.称重取样以CFU/g为单位报告,体积取样以CFU/mL为单位报告。
三、大肠菌群检验结果报告。
LST初发酵,产酸产气,接种BGLB复发酵后仍产酸产气,则证明样品受到了大肠菌群污染,可检索MPN表,得出相应结果。
检测时如果采用(10-1,10-2,10-3)三个稀释度,最后BGLB产气管为(2,0,0),查MPN表可得出大肠菌群检测值为9.2MPN/g;检测时如果采用(100,10-1,10-2)三个稀释度,最后BGLB产气管仍为(2,0,0),查MPN表可得大肠菌群检测值为0.92MPN/g;如果采用(10-2,10-3,10-4)三个稀释度,最后BGLB产气管仍然为(2,0,0),查MPN表可得大肠菌群检测值为92MPN/g。
称重取样以MPN/g为单位报告,体积取样以MPN/mL为单位报告。
食品中常见病原微生物检验技术

食品中常见病原微生物检验技术
第28页
食品中常见病原微生物检验技术
第30页
• P150
• (1) A1:经典反应判定为沙门氏菌属。如尿素、氰化钾和赖氨 酸脱羧酶3项中有1项异常,按表可判定为沙门氏菌属。如有2项 异常,为非沙门氏菌属。
(2)A2:补做甘露醇和山梨醇试验,沙门氏菌靛基质阳性变体 两项试验结果均为阳性,但需要结合血清学判定结果进行判定。
菌落;但无混浊带及透明圈。
▪
在血平板上,形成菌落较大,圆形、光滑凸起、湿
润、 金黄色(有时为白色),菌落周围可见完全透明溶
血圈。 食品中常见病原微生物检验技术
第70页
B-P平板
食品中常见病原微生物检验技术
第76页
¥7(90mm)
Baird-Parker(BP培养基/贝尔德帕克平板) 用于凝固酶阳性葡萄球菌分离和菌落计数用。
食品中常见病原微生物检验技术
第55页
金黄色葡萄球菌致病性
致病力强弱主要取决于其产生毒素和侵袭性酶:
a.溶血毒素:外毒素,分甲、乙、丙、丁、戊五种,能损伤血小板,破坏溶酶体,引 发肌体局部缺血和坏死; b.杀白细胞素:可破坏人白细胞和巨噬细胞; c.血浆凝固酶:侵入人体时,该酶使血液或血浆中纤维蛋白沉积于菌体表面或凝固, 妨碍吞噬细胞吞噬作用。 葡萄球菌形成感染易局部化与此酶相关; d.脱氧核糖核酸酶:产生脱氧核糖核酸酶能耐受高温,可用来作为依据判定金黄色葡 萄球菌; e.肠毒素:产生数种引发急性胃肠炎蛋白质性肠毒素,现已判定出葡萄球菌肠毒素有 A、B、C1~C3、D、E、G、H共9种。肠毒素A是最常见。
•
表面光滑菌落,菌落色素不稳定,但多数为金黄色。
➢
Baird-Parker琼脂平板(BP平板) 、血平板 、血浆凝固
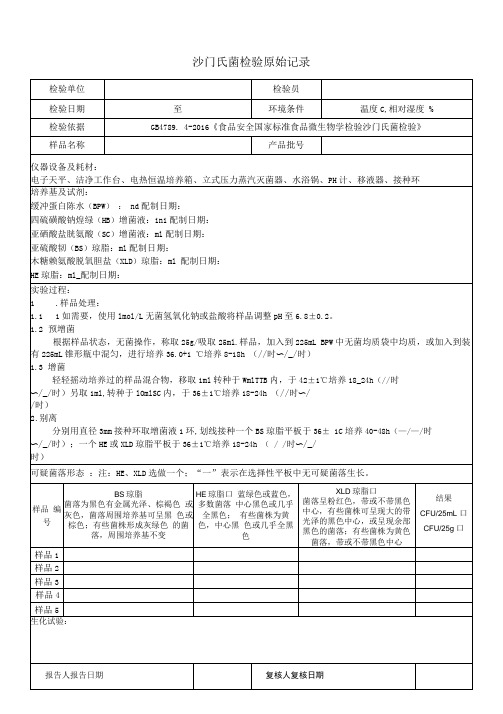
沙门氏菌检验原始记录
/时)
2.别离
分别用直径3mm接种环取增菌液1环,划线接种一个BS琼脂平板于36±1C培养40-48h(—/—/时
〜/_/时);一个HE或XLD琼脂平板于36±1℃培养18-24h( / /时〜/_/
时)
可疑菌落形态 :注:HE、XLD选做一个;“一”表示在选择性平板中无可疑菌落生长。
样品 编号
BS琼脂
菌落为黑色有金属光泽、棕褐色 或灰色,菌落周围培养基可呈黑 色或棕色;有些菌株形成灰绿色 的菌落,周围培养基不变
HE琼脂口 蓝绿色或蓝色,多数菌落 中心黑色或几乎全黑色; 有些菌株为黄色,中心黑 色或几乎全黑色
XLD琼脂口
菌落呈粉红色,带或不带黑色 中心,有些菌株可呈现大的带 光泽的黑色中心,或呈现余部 黑色的菌落;有些菌株为黄色 菌落,带或不带黑色中心
1.2预增菌
根据样品状态,无菌操作,称取25g/吸取25ml.样品,加入到225mL BPW中无菌均质袋中均质,或加入到装 有225mL锥形瓶中混匀,进行培养36.0+1℃培养8-18h(//时〜/_/时)
1.3增菌
轻轻摇动培养过的样品混合物,移取1ml转种于WmlTTB内,于42±1℃培养18_24h(//时
结果
CFU/25mL口
CFU/25g口
样品1
样品2
样品3
样品4
样品5
生化试验:
报告人报告日期
复核人复核日期
沙门氏菌检验原始记录
检验单位
检验员
检验日期
至
环境条件
温度C,相对湿度 %
检验依据
GB4789. 4-2016《食品安全国Biblioteka 标准食品微生物学检验沙门氏菌检验》
011-微生物致病菌检测原始记录

永修县疾病预防控制中心YXCDC(原)-011-01食品中致病菌检测原始记录(一)共 2 页第 1 页样品名称:批号:样品编号:检测项目:收样日期:检测日期:检测环境条件(温﹑湿度等):℃%检测依据:检测仪器名称﹑型号:检测记录与结果:36 ℃36 ℃36 ℃沙门氏菌:25g/ml样品+225ml BP →取10ml → 100mlMM→WS平板→4h 18~24h 18~24h ()可疑菌落生长,进一步鉴定结果见生化鉴定本。
结果:36 ℃36℃志贺氏菌:25g/ml样品+225ml GN→SS平板→6~8h 18~24h()可疑菌落生长,进一步鉴定结果见生化鉴定本。
结果:36 ℃36℃金黄色葡萄球菌:25g/ml样品+225ml 7.5%Nacl 肉汤增菌液→血平板→18~24h 18~24h()可疑菌落生长,进一步鉴定结果见生化鉴定本。
结果:36 ℃36℃溶血性链球菌:25g/ml样品+225ml 1%葡萄糖肉汤增菌液→血平板→18~24h 18~24h()可疑菌落生长,进一步鉴定结果见生化鉴定本。
结果:36 ℃42℃36℃致泻性大肠埃希氏菌:25g/ml样品+225ml 营养肉汤→ 30ml肠道菌增菌肉汤→麦康凯平板→ 6h 18~24h 18~24h ()可疑菌落生长,生化鉴定结果见生化鉴定本,血清学试验. 结果:36 ℃36℃O157:H7:25g/ml样品+225ml EC营养肉汤→麦康凯平板→18~24h 18~24h()可疑菌落生长,生化鉴定结果见生化鉴定本,血清学试验.结果:37℃37℃副溶血性弧菌:25g/ml样品+225ml,取10ml →100ml氯化钠结晶紫增菌液,接种嗜盐菌琼脂平板→()18~24h18~24h ()可疑菌落生长。
进一步鉴定见生化鉴定本结果:检验者:复核者:完成时期:年月日原始记录随样品送检单、检验样品登记及流程单、检验报告书底稿、检验报告书等合并归档保存。
致病菌检测原始记录

抗原的准备 多价菌体抗原(O)鉴定 多价鞭毛抗原(H)鉴定
血清学鉴定结果
结果报告
金黄色葡萄球菌(定性) GB 4789.10--______
样品处理 取检样25g(mL),加至盛有225mL10%氯化钠胰酪胨大豆肉汤的无菌锥形瓶中,充分混匀。
增菌
将上述样品均液,于 ___℃ 培养___h;
选择性平板
致病菌检测原始记录
产品名称 产品形态 检测项目
□沙门氏菌
包装规 格样品数 量
□金黄色葡萄球菌
送样单 位送样时 间
收样人员 留样量
□志贺氏菌
检测环境
温度: ℃ 湿度: % 检测日期
沙门氏菌 GB 4789.4--______
增菌
ቤተ መጻሕፍቲ ባይዱ
25g(mL)样品+BPW 225mL,混匀,于 ___℃ 培养___h; 1mL前增菌液+10mLTTB增菌液,于 ___℃ 培养___h;
三糖铁琼脂反应
生化 鉴定
斜面
葡萄糖铵 尿素酶
产气 KCN
℃培养时间 h
菌落特征
硫化氢
葡萄糖 半固体
管
西蒙氏柠 赖氨酸脱 鸟氨酸脱 革兰氏染 氧化酶试
檬酸盐
羧酶
羧酶
色
验
水杨苷
七叶苷
β半乳糖 苷
甘露醇
棉子糖
甘油
靛基质
血清学鉴定 结果报告
检测:
审核:
检毕日期
年月日
选择性平板 培养温度 ℃培养时间 h
分离 培养
□BS □XLD
□显色培养基
生化反应 生化 初步鉴定
斜面
三糖铁琼脂反应
赖氨酸脱
底层
微生物检验结果报告注意事项

微生物检验结果报告注意事项一、涉及定性项目的检验结果报告沙门氏菌、志贺氏菌、金黄色葡萄球菌、单核细胞增生李斯特氏菌、大肠杆菌O157:H7、空肠弯曲杆菌、副溶血性弧菌(定性)等,如果检样是称重取样,则最后检测结果一定报告为检出/25g或未检出/25g。
如果检样是体积取样,则最后检测结果一定报告为检出/25mL或未检出/25mL。
检测标准要求g必须要小写,mL中m必须小写,L则必须大写。
记录中所有有用的信息必须填上,无法填充的用“/”划掉。
二、菌落总数检验结果报告1.菌落总数小于100CFU时,按“四舍五入”原则修约以整数报告,如80.5CFU可修约报告为81CFU;80.4CFU则修约报告为80CFU。
2.菌落总数大于等于100CFU时,左边数第3位数字采用四舍五入原则修约后,取前2位数字,后面位数用0代替,也可用10的指数形式表示:如10-2两平板平均菌落数为238CFU/g,可修约为240CFU/g,最后报告为24000CFU/g或2.4×104CFU/g。
3.霉菌、酵母菌、乳酸菌、蜡样芽孢杆菌、产气荚膜梭菌报告形式和菌落总数一样。
4.称重取样以CFU/g为单位报告,体积取样以CFU/mL为单位报告。
三、大肠菌群检验结果报告。
LST初发酵,产酸产气,接种BGLB复发酵后仍产酸产气,则证明样品受到了大肠菌群污染,可检索MPN表,得出相应结果。
检测时如果采用(10-1,10-2,10-3)三个稀释度,最后BGLB 产气管为(2,0,0),查MPN表可得出大肠菌群检测值为9.2MPN/g;检测时如果采用(100,10-1,10-2)三个稀释度,最后BGLB产气管仍为(2,0,0),查MPN表可得大肠菌群检测值为0.92MPN/g;如果采用(10-2,10-3,10-4)三个稀释度,最后BGLB产气管仍然为(2,0,0),查MPN表可得大肠菌群检测值为92MPN/g。
称重取样以MPN/g为单位报告,体积取样以MPN/mL 为单位报告。
053-食物中毒检测原始记录

GB14938-94和检测项目下的括号内
仪器名称、编号
□HH-B11-600型电热恒温培养箱(F055)
□LRH-150型生化培养箱(F017)
检测项目
血清学试验
生化试验或其它试验
选择试验
结果
选择试验
结果
选择试验
结果
选择试验
结果
沙门氏菌
(GB/T4789.4-2003)
凝集试验阳性的单价O血清:
阴性对照
试验结果
全自动免疫荧光
酶标法(VIDAS SET金葡球菌肠毒素检测规程)
将样品按1:1的比例加入提取液,26℃静置30min,吸取上清液,煮沸15mim,离心,取0.5ml上机测试。
备注
注:1.检验项目和革兰氏染色镜检在“□”内用“√”选择;2.“试验结果”:“+”表示阳性;“-”表示阴性。
GN:
SS平板:
EMB平板:
□G-杆菌
□非G-杆菌
TSI:H2S:
蜡样芽胞杆菌(GB/T4789.14-2003)
MYP:
□G+芽胞杆菌
□非G+芽胞杆菌
产气荚膜梭菌(GB/T4789.13-2003)
SPS:
□G+粗大杆菌
□非G+粗大杆菌
注:1.检验项目和革兰氏染色镜检在“□”内用“√”选择;2.生化试验:“+”表示阳性;“-”表示阴性;“↑”表示产气;3.增菌液生长情况:“+”表示增菌液有菌生长,混浊,“-”表示增菌液无菌生长,澄清,4.分离培养:“+”表示有可疑菌生长,“-”表示无可疑菌生长;5.“血清学试验”:凝集效果为“++++、+++、++、+、—”表示。
食品微生物检验原始记录

食品微生物检验原始记录HSCDC/ZJ-19-8A 共页第页样品名称样品编号受检单位样品批号检测环境温度(T):℃;相对湿度(RH):% 接样日期年月日检测地点□净化室1 □净化室2 □BSL-2 检测起止日期年月日~月日检测依据□GB/T4789.2-2008 □GB/T4789.3-2008第一法□GB/T4789.4-2008 □GB/T4789.5-2003 □GB/T4789.10-2008 □GB/T4789.11-2003 □GB/T4789.15-2003检测仪器□电子天平(型号:SC6010)编号00-2 □霉菌培养箱(型号:WJP-150)25~28℃编号04-16 □电热恒温培养箱(型号:DNP-9272)36±1℃编号□04-15 □04-24 □05-11□均质器(型号:BJ-IV)编号08-J3转速8000r/min 时间□1分钟□2分钟□3分钟培养基□平板计数琼脂ML □LST肉汤ML □BGLB肉汤ML □虎红琼脂ML □BPW ML □TTB ML □SC ML □BS平板ML □XLD平板ML □GN ML □SS平板ML □EMB平板ML □API20E生化鉴定试剂盒□7.5%氯化钠肉汤ML □Baird-Parker平板ML □血平板ML □兔血浆ML □葡萄糖肉浸液肉汤ML □其他样品制备 固体和半固体样品:无菌称取25g,置于盛有225ml生理盐水的无菌灭菌杯内,进行均质处理。
液体样品:吸取25ml于样品于225ml生理盐水中,混匀。
液体样品:直接吸原液检验。
BPW ℃,h TTB ℃,h SC ℃,h GN ℃,h7.5%氯化钠肉汤℃,h;葡萄糖肉浸液肉汤℃,h。
其它(生化试验、血清凝集试验等):检测者:审核者:。
127食品中沙门氏菌、志贺氏菌、金黄色葡萄球菌检验记录

食品中沙门氏菌、志贺氏菌、金黄色葡萄球菌检验记录样品编号: 第 页/共 页 样 品 名 称 样 品 批 号样 品 数 量 样 品 性 状包 装 情 形收 样 日 期 年 月 日 检 测 环 境 温度: ℃ ; 湿度(RH ): % 检 验 日 期 年 月 日 检 测 地 点 □净化室 □BSL-2完 成 日 期年 月 日检 验 项 目 □沙门氏菌 □志贺氏菌 □金黄色葡萄球菌检 测 依 据 □GB 4789.4-2010 □G B 4789.5-2012 □GB 4789.10-2010检 测 仪 器 □电子天平(型号:BSA2202S )□隔水式恒温培养箱(型号:GHP-9270)36℃□隔水式恒温培养箱(型号:GHP-9050)42℃ □厌氧罐□无菌均质器(型号:Scientz-04)中速 时间 □1分钟 □2分钟培 养 基 □BPW □TTB □SC □沙门显色琼脂 □BS 琼脂 □HE 琼脂 □XLD 琼脂 □TSI 琼脂□志贺氏菌肉汤 □MAC 琼脂 □API20E 生化鉴定试剂盒(法国梅里埃公司)□7.5%NaCl 肉汤 □金葡显色琼脂 □B-P 琼脂 □血平板 □血浆凝固酶试剂 (其余为北京路桥公司产品)样 品 制 备□固体和半固体样品: 无菌称取25g 样品放入盛有225ml 灭菌(BPW 、志贺氏菌肉汤、7.5%NaCl 肉汤)的无菌均质袋中,用拍击式均质器拍打1mi n ~2min 。
□液体样品:无菌吸取25ml 样品于225ml 灭菌( BPW 、志贺氏菌肉汤、7.5%NaCl 肉汤)中,充分混匀。
□根据样品性质,用无菌4%或40%NaOH 调节样品匀液的pH 值在6.5~7.5之间步骤及结果: 1、沙门氏菌 前增菌/增菌(温度和时间)分离培养菌落形态生化试验选择性平板℃ h TSI API20E 结果 %BPW ℃,h : 日 时 分至 日 时 分二增菌 ℃ h : 日 时 分至日 时 分显色平板结果报告:□XLD □HE 标准菌株2、志贺氏菌增菌(温度和时间)分离培养菌落形态生化试验选择性平板 ℃ h TSI API20E 结果 % 志贺菌肉汤(厌氧培养)℃ h : 日 时 分至 日 时 分显色平板结果报告:□MA C □XLD标准菌株3、金黄色葡萄球菌增菌和分离培养菌落形态鉴定7.5%NaCl 肉汤 ℃,h : 日 时 分 至 日 时 分选择性平板 ℃h镜检 凝固酶试验B-P 平板血平板标准菌株结果报告:其它:检验者: 审核者: 年 月 日。
由金黄色葡萄球菌引起食物中毒的实验室检测分析

由金黄色葡萄球菌引起食物中毒的实验室检测分析发表时间:2013-11-01T10:15:10.420Z 来源:《中外健康文摘》2013年第29期供稿作者:冼桂江郭永强蔡周梅彭美薇盘珍梅[导读] 葡萄球菌在自然界中广泛存在,食品从原料、生产加工、藏运输、流通经营、到消费者食用,都有可能受到污染。
冼桂江郭永强蔡周梅彭美薇盘珍梅 (广西梧州市疾病预防控制中心 543002)【中图分类号】R446 【文献标识码】A【文章编号】1672-5085(2013)29-0223-02【摘要】目的调查本次食物中毒的原因,为临床诊断和现场处理提供可靠的依据。
方法依据GB/T4789-2010、GB17012-1997、WS/T8、T13、T80、T81、T82-1996 等方法对样品进行致病菌检测。
结果 3份腹痛、腹泻病人的肛拭子标本中均检出金黄色葡萄球菌,3份可疑食品中有一份检出金黄色葡萄球菌。
结论这是一起由金黄色葡萄球菌感染引起的食物中毒。
【关键词】食物中毒实验室检测金黄色葡萄球菌1 调查资料梧州市某大酒店200多名员工于2012年6月11日11时左右,在单位食堂集体进午餐,其中9名员工进食了同事从广州带回的卤鸭食品(封口塑料袋包装),中午13时30分左右,该9名员工中有5名出现恶心、呕吐、腹痛、腹泻等症状,其中3名症状较重的患者到当地医院就珍;其他未食卤鸭食品的员工未出现上述症状。
2 实验室检测2.1 标本来源2.1.1 采集3名到医院就诊的患者肛拭子标本,置C-B运送培养基中保存。
2.1.2 在酒店现场采集患者吃剩的周黑鸭脖、绝味鸭脖、绝味鸭翅共3份可疑食品。
2.1.3 上述标本采集完毕后均在4h内送达实验室进行检测。
2.2 培养基与试剂各种常见食物中毒致病菌的增菌培养基、分离及鉴定培养基、各种生化鉴定管均由北京陆桥生物技术有限公司生产,各种显色培养基由上海科玛嘉公司生产,沙门氏菌、志贺氏菌和致泻性大肠埃希氏菌诊断血清由宁波天润生物药业有限公司生产,兔血浆由青岛海博生物公司生产,以上培养基与试剂均在有效期内使用。
沙门、金黄色葡萄球菌食品原始记录

分离
划线接种于BS琼脂平板培养℃h
空白:□NG□G
阳对:□NG□G
样品-1:□NG□G
菌落特征为黑色有金属光泽。棕褐色或灰色部分为灰绿色
样品-2:□NG□G
样品-3:□NG□G
样品-4:□NG□G
样品-5:□NG□G
划线接种于XLD琼脂平板培养℃h
空白:□NG□G
阳对:□NG□G
样品-1:□NG□G
PITC/JJ01-WJ02-0002/2-2
二、金黄色葡萄球菌检验(第二法)
1.称取g/mL样品加入225mL磷酸缓冲液的无菌均质袋中,制备10倍系列稀释样品匀液。适宜的稀释度接种三个Bp平板培养℃h。空白。
稀释度
平板菌落数
平板1(0.3mL)
平板2(0.3mL)
平板3(0.4mL)
总数
样品
1
100
阳性对照
阴性对照可Leabharlann 菌落123
4
5
样品-1
样品-2
样品-3
样品-4
样品-5
注:+凝集–不凝集
3.结果报告
样品-1 CFU/g
样品-2 CFU/g
样品-3 CFU/g
样品-4 CFU/g
样品-5 CFU/g
4.结论
□符合□不符合
标准要求:n=5,c=1,m=100CFU/g,M=1000CFU/g
菌落特征为粉红色带或不带黑色中心
样品-2:□NG□G
样品-3:□NG□G
样品-4:□NG□G
样品-5:□NG□G
生化鉴定
血清鉴定
结果报告25g(ml)
样品-1
样品-2
样品-3
金黄色葡萄球菌、沙门氏菌检验原始记录
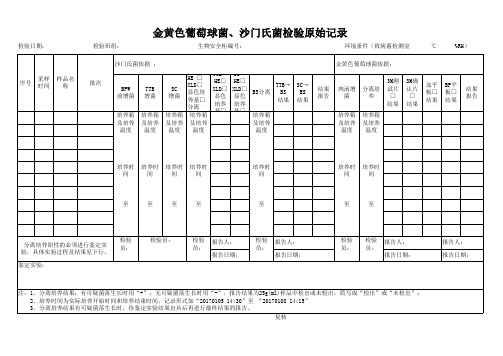
培养时 培养时
间
间
至
至
分离培养阳性的必须进行鉴定实 验,具体实验过程及结果见下行。
鉴定实验:
检验 员:
检验员:
检验 报告人: 员:
报告日期:
检验 报告人: 员:
报告日期:
检验 员:
检验 报告人: 员:
报告日期:
报告人: 报告日期:
注:1、分离培养结果:有可疑菌落生长时用“+”;无可疑菌落生长时用“-”,报告结果为25g(ml)样品中检出或未检出,简写成“检出”或“未检出”; 2、培养时间为实际培养开始时间和培养结束时间,记录形式如“20170105 14:30”至 “20170108 14:15” 3、分离培养结果有可疑菌落生长时,待鉴定实验结果出具后再进行最终结果的报告。
BS分离
培养箱 及培养
温度
TTB→ BS 结果
SC→ BS 结果
金黄色葡萄球菌依据:
结果 报告
肉汤增 菌
分离培 养
3M测 试片 □ 结果
培养箱 培养箱 及培养 及培养
温度 温度
3M确 认片 □ 结果
血平 板□ 结果
BP平 板□ 结果
结果 报告
培养时 培养时 培养时 培养时
间
间
间
间
至
至
至
至
培养时 间至ຫໍສະໝຸດ 复核检验日期:序号
采样 时间
样品名 称
检验班组:
金黄色葡萄球菌、沙门氏菌检验原始记录
生物安全柜编号:
环境条件(致病菌检测室
℃
%RH)
批次
沙门氏菌依据 :
BPW 前增菌
培养箱 及培养
温度
TTB 增菌
微生物检测原始记录

□天平8-01 □培养箱8-11 □生化培养箱8-21 □显微镜8-31
实验地点
1014室
环境条件
27 ℃ 相对湿度77 %
样品处理
无特殊情况,按相应国标方法处理。
培养基等
特殊试剂
见HNCDC08050
项目
沙门氏菌
志贺氏菌
金黄色葡萄球菌
溶血性链球菌
增菌与
分离
PB:36℃培养,起17日10时0分止17日14时0分,MM:42℃和SC:36℃培养起10月17日15时55分止10月18日15时0分,BS平皿:36℃培养起10月18日15时30分止10月20日14时0分.SS平皿:36℃培养起10月18日15时30分止10月20日14时0分.有/无可疑菌落
GN:36℃培养,起17日10时0分止17日17时30分,MAC和SS平皿:36℃培养起10月17日18时0分止10月19日17时30分.
有/无可疑菌落
7.5%NaCl肉汤:36℃:培养起10月17日10时0分止10月18日10时0分,血和Baird-Parker平皿36℃:培养起10月18日10时40分止10月19日10时40分.
止10月19日10时40分.
有/无可疑菌落
葡萄糖肉浸液::36℃培养
起10月17日10时0分
止10月18日10时0分,
血平皿36℃培养
起10月18日10时40分
止10月19日10时40分
有/无可疑菌落
生化试验
三糖铁:斜面- 底层+
产气+ 硫化氢+
其它生化试验:
靛基质- pH7.2尿素-
氰化钾- 赖氨酸+
项目
沙门氏菌
志贺氏菌
金黄色葡萄球菌
溶血性链球菌
食品金黄色葡萄球菌检验原始记录
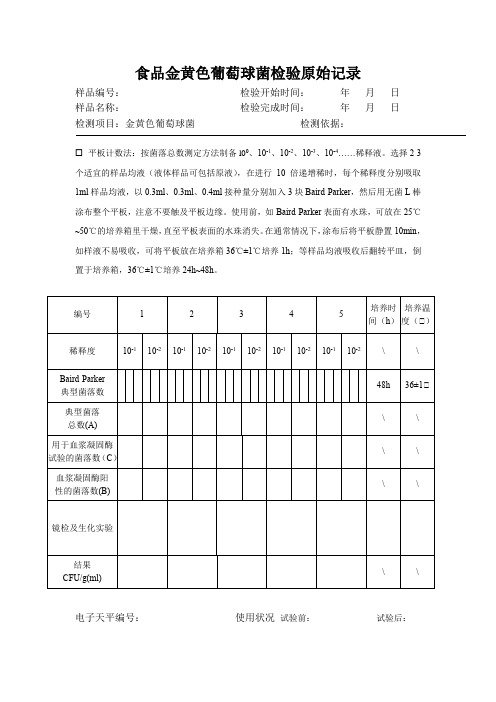
食品金黄色葡萄球菌检验原始记录
样品编号:检验开始时间:年月日
样品名称:检验完成时间:年月日
检测项目:金黄色葡萄球菌检测依据:
平板计数法:按菌落总数测定方法制备l00、10-1、10-2、10-3、10-4……稀释液。
选择2-3个适宜的样品均液(液体样品可包括原液),在进行10倍递增稀时,每个稀释度分别吸取1ml样品均液,以0.3ml、0.3ml、0.4ml接种量分别加入3块Baird-Parker,然后用无菌L棒涂布整个平板,注意不要触及平板边缘。
使用前,如Baird-Parker表面有水珠,可放在25℃~50℃的培养箱里干燥,直至平板表面的水珠消失。
在通常情况下,涂布后将平板静置10min,如样液不易吸收,可将平板放在培养箱36℃±1℃培养1h;等样品均液吸收后翻转平皿,倒置于培养箱,36℃±1℃培养24h~48h。
电子天平编号:使用状况试验前:试验后:
培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:
样品编号:
定性检验:称取25g样品至盛有225ml7.5%氯化钠肉汤的无菌均质杯/均质袋内,均质。
若为液体,吸取25ml样品至盛有225ml7.5%氯化钠肉汤的无菌锥形瓶(加适量玻璃珠),振荡混匀。
将上述样品匀液于36±1℃培养18~24h。
将增菌后的培养物分别划线接种到Baird-Parker 平板和血平板36±1℃培养24~48h和18~24h。
然后进行鉴定生化实验。
注:+生长或有可疑菌落;-未生长或无可疑菌落。
电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
沙门氏菌定性检验步骤及记录
1前增菌以无菌操作取检样25 g(mL),放入盛有225 mL BPW中,振荡(涡旋)混匀后,于36℃培养18 h。
2增菌轻轻摇动培养过的样品混合物,移取1 mL,转种于10 mL TTB内,于42℃培养24h。同时,另取1 mL,转种于10 mL SC内,于36℃培养24 h。
选择性琼脂平板
试样菌的菌落特征
是否为典型或可疑菌落特征
BS琼脂
HE琼脂
XLD琼脂
沙门氏菌属显色培养基
5结果与报告
综合以上鉴定的结果,报告25 g(mL)样品中沙门氏菌。
志贺氏菌的检验步骤及记录
1增菌:以无菌操作取检样25 g(mL),加入装有225mL灭菌的志贺氏菌增菌肉汤,振荡(涡旋)混匀后,41.5℃,厌氧培养20 h.
试样菌在不同平板上的为典型或可疑菌落特征
Baird-Parker平板
血平板
结果报告:在25 g(mL)样品中金黄色葡萄球菌。
校核:检验员:
2分离取增菌后的志贺氏菌增菌液分别划线接种于XLD琼脂平板和MAC琼脂平板或志贺氏菌显色培养基平板上,于36℃,培养24 h,观察各个平板上生长的菌落形态。
试样菌在不同选择性琼脂平板上的菌落特征
选择性琼脂平板
试样菌的菌落特征
是否为典型或可疑菌落特征
MAC琼脂
XLD琼脂
志贺氏菌显色培养基
结果报告:综合以上鉴定的结果,报告25 g(mL)样品中志贺氏菌。
食品中沙门氏菌定性志贺氏菌金黄色葡萄球菌检验原始记录
JZJC-04-SP-48
样品编号
检验日期
环境温度
℃
环境湿度
%(RH)
检验使用仪器设备
T-200型电子天平(000000349)
电热恒温培养箱(000000011)
检验依据
GB 4789.4-2016食品安全国家标准食品微生物学检验沙门氏菌检验
GB 4789.5-2012食品安全国家标准食品微生物学检验志贺氏菌检验
3.分离分别用接种环取增菌液1环,划线接种于一个BS琼脂平板和一个XLD琼脂平板(或HE琼脂
平板或沙门氏菌属显色培养基平板)。于36℃分别培养24 h(XLD琼脂平板、HE琼脂平板、沙门氏菌属显色培养基平板)或48 h(BS琼脂平板),观察各个平板上生长的菌落形态。
试样菌在不同选择性琼脂平板上的菌落特征
金黄色葡萄球菌定性检验步骤及记录
1增菌:以无菌操作取检样25 g(mL),加入装有25mL7.5 %氯化钠肉汤,振荡(涡旋)混匀后,36℃培养h。
2分离:将上述培养物,分别划线接种到Baird-Parker平板和血平板,血平板36℃培养24 h。
Baird-Parker平板36℃培养48 h。观察各个平板上生长的菌落形态。
