实验三 氯离子选择性电极的测试和应用
氯离子选择性电极的测试和应用资料共21页文档

21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈
23、一切节省,归根到底都归结为时间的节省。——马克思 24、意志命运往往背道而驰,决心到最后会全部推倒。——莎士比亚
25、学习是劳动,是试和应用资料
11、获得的成功越大,就越令人高兴 。野心 是使人 勤奋的 原因, 节制使 人枯萎 。 12、不问收获,只问耕耘。如同种树 ,先有 根茎, 再有枝 叶,尔 后花实 ,好好 劳动, 不要想 太多, 那样只 会使人 胆孝懒 惰,因 为不实 践,甚 至不接 触社会 ,难道 你是野 人。(名 言网) 13、不怕,不悔(虽然只有四个字,但 常看常 新。 14、我在心里默默地为每一个人祝福 。我爱 自己, 我用清 洁与节 制来珍 惜我的 身体, 我用智 慧和知 识充实 我的头 脑。 15、这世上的一切都借希望而完成。 农夫不 会播下 一粒玉 米,如 果他不 曾希望 它长成 种籽; 单身汉 不会娶 妻,如 果他不 曾希望 有小孩 ;商人 或手艺 人不会 工作, 如果他 不曾希 望因此 而有收 益。-- 马钉路 德。
谢谢!
分析化学实验—氯离子选择性电极测定氯离子浓度

分析化学实验
实验目的
• 了解氯离子选择性电极的基本性能; • 掌握氯离子选择性电极的使用方法 • 学会使用酸度计测量电动势
实验原理
• 氯离子选择性电极是由AgCl和Ag2S的粉末混 合物压制成的敏感膜,当将氯离子选择性电极 浸入含Cl-)。
PB-10使用说明
插上电源预热 10-15min。
按Mode键,调 解PB-10为电 位模式,显示 读数是若干MV。
待读数稳定后 记录数据。
实验原理
• 以氯离子选择性电极为指示电极,双液接甘汞电 极为参比电极,插入试液中组成工作电池,当氯 离子浓度在1~10-4mol/L范围内,在一定的条件下, 电池电动势与氯离子活度的对数成线性关系。
实验步骤
• 配制盐酸的标准溶液 • 测定电动势 绘制E-pCl 曲线,求出转换系
数。
氯离子选择性电极测定氯离子浓度
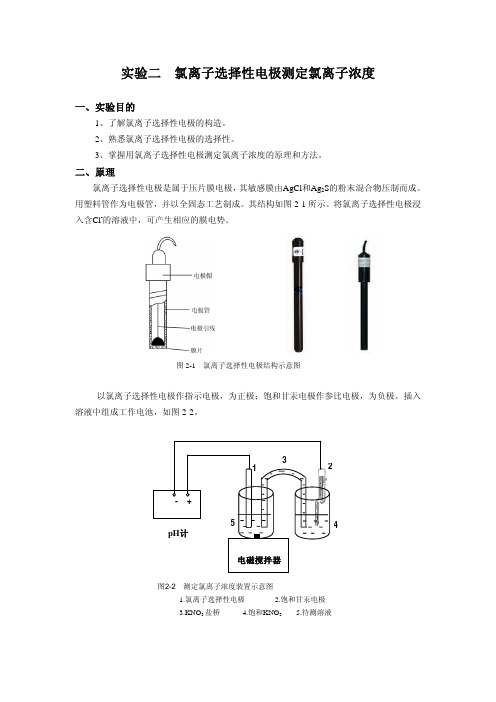
实验二氯离子选择性电极测定氯离子浓度一、实验目的1、了解氯离子选择性电极的构造。
2、熟悉氯离子选择性电极的选择性。
3、掌握用氯离子选择性电极测定氯离子浓度的原理和方法。
二、原理氯离子选择性电极是属于压片膜电极,其敏感膜由AgCl和Ag2S的粉末混合物压制而成。
用塑料管作为电极管,并以全固态工艺制成。
其结构如图2-1所示。
将氯离子选择性电极浸入含Cl-的溶液中,可产生相应的膜电势。
图2-1 氯离子选择性电极结构示意图以氯离子选择性电极作指示电极,为正极;饱和甘汞电极作参比电极,为负极。
插入溶液中组成工作电池,如图2-2。
4图2-2 测定氯离子浓度装置示意图1.氯离子选择性电极2.饱和甘汞电极3.KNO3 盐桥4.饱和KNO35.待测溶液电池电动势:' 2.303lg[])2.303)2.303E RT K Cl nF RT K pCl FRT K pCl F ϕϕϕϕ=−=−−=+−=+膜甘甘甘(( 电池电动势E 与氯离子浓度的负对数呈线性关系。
利用标准曲线法,在一定条件下,分别测出一系列不同浓度的氯离子标准溶液的电池电动势E ,以标准溶液的浓度的负对数为横坐标,相应的电池电动势为纵坐标,在坐标纸上描点作图,就可制得标准曲线。
若在同样条件下测未知溶液的电池电动势,即可由标准曲线得知被测溶液的氯离子浓度的负对数,从而求得被测溶液中氯离子的浓度。
离子选择性电极对特定的离子有电位响应,因而用来测定该离子。
但离子选择性电极并不是专一性电极,除对特定离子有响应外,对于某些其他离子也会有响应,只是响应程度不同或响应较小。
一般情况下,阳离子不干扰阴离子选择性电极,阴离子不干扰阳离子选择性电极。
但如与膜表面上的离子反应生成一种新的、不容性的化合物时,无论阴离子或阳离子都会出现干扰。
Ag +,Hg 22+, Hg 2+等阳离子对氯离子的测定有干扰,可用EDTA 掩蔽以消除干扰。
Br -,I -,S 2-,CN -等阴离子对氯离子的测定也有干扰,S 2-离子可以加PbCO 3除掉。
氯离子选择性电极的测试及应用共21页文档

56、极端的法规,就是极端的不公。 ——西 塞罗 57、法律一旦成为人们的需要,人们 就不再 配享受 自由了 。—— 毕达哥 拉斯 58、法律规定的惩罚不是为了私人的 利益, 而是为 了公共 的利益 ;一部 分靠有 害的强 制,一 部分靠 榜样的 效力。 ——格 老秀斯 59、假如没有法律他们会更快乐的话 ,那么 法律作 为一件 无用之 物自己 就会消 灭。— —洛克
60、人民的幸福是至高无个的法。— —西塞 罗
谢谢!
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事卜 生 54、 唯 书 籍 不 朽。——乔 特
55、 为 中 华 之 崛起而 读书。 ——周 恩来
离子选择性电极法测定氯离子

离子选择性电极法测定氯离子
离子选择性电极法是一种测定溶液中特定离子浓度的重要分析技术。
它利用离子选择性电极测定样品中目标离子的浓度。
本文将介绍离子选择性电极法测定氯离子的原理、优点和步骤。
一、原理
氯离子选择性电极是一种有机薄膜电极,其极性反应式为:
AgCl(s) + e^- ⇌ Ag(s) + Cl^-
该电极的膜材料一般是聚氯乙烯或聚乙烯基丙烯酸酯。
电极内部填充了含有壳聚糖或氨基磺酸等选择性载体的溶液,可以选择对氯离子具有高选择性的载体,以达到准确测定氯离子浓度的目的。
二、优点
1、对氯离子具有高度选择性;
2、测量灵敏度高,响应迅速;
3、操作简便,仪器设备简单,易于操作;
4、可在线监测氯离子浓度,无需样品处理。
三、步骤
1、准备工作:将氯离子选择性电极校准好,准备好样品和标准溶液;
2、校准电极:将氯离子选择性电极放在500mL 0.1mol/L NaCl溶液中,分别记录电极电势值和温度。
然后将电极放在1.0×10^-3mol/L NaCl溶液中,测量电极电势。
将以上两组数据带入电极响应函数,求出氯离子浓度;
3、测定样品中氯离子浓度:将氯离子选择性电极放入要测试的样品中,记录电极电势值和温度,带入电极响应函数求出氯离子浓度。
在实际应用中,需要根据具体测量要求选择合适的氯离子选择性电极型号和电极响应函数,同时注意电极的维护和保养。
离子选择性电极法除了测定氯离子浓度外,还可用于测定其他离子的浓度,如钙离子、氟离子等。
氯离子选择性电极与氯离子浓度符合能斯特方程

氯离子选择性电极与氯离子浓度符合能斯特方程氯离子选择性电极是一种用于测量氯离子浓度的电极,它可以测量氯离子的电位,反映氯离子浓度。
氯离子选择性电极是一种非常有效和便捷的测量手段,它所提供的数据对于理解氯离子的特性具有重要意义。
此外,氯离子选择性电极可以测量氯离子浓度,并且能与氯离子浓度的变化符合能斯特方程。
能斯特方程是一个数学方程,用于描述给定浓度的溶液中盐离子的活度。
它可以用来解释氯离子选择性电极的反应,从而测量氯离子的电位。
它可以用于测量各种物质的电位,包括氯离子浓度。
能斯特方程表明,溶液中的活度和溶质的浓度是正相关的。
更具体而言,氯离子选择性电极可以利用能斯特方程来测量溶液中氯离子浓度的变化。
它可以用开放系统来测量溶液中的氯离子浓度,模拟其反应。
当溶液的浓度发生变化时,能斯特方程可以使氯离子选择性电极能够精确测量浓度的变化。
由于能斯特方程的精确性,氯离子选择性电极可以用来测量有关氯离子激励的关键数据。
氯离子选择性电极可以用于测量氯离子浓度,以实现更高精度的测量结果。
它可以用于监控溶液中氯离子浓度的变化,以及氯离子浓度升高或降低的状态。
此外,氯离子选择性电极还可以用来检测氯离子从一种物质到另一种物质的过渡。
因此,氯离子选择性电极在溶液中氯离子浓度的测量中具有重要意义。
在实际应用中,氯离子选择性电极可以用于测量氯离子的电位,并且可以与氯离子浓度的变化符合能斯特方程。
它可以用于监控氯离子的数量,以便进行更精确的测量。
此外,它还可以用来模拟氯离子从一个物质过渡到另一个物质的情况。
因此,氯离子选择性电极可以用来测量氯离子浓度,与氯离子浓度的变化符合能斯特方程,从而提高测量精度。
至此,本文介绍了氯离子选择性电极与氯离子浓度符合能斯特方程。
氯离子选择性电极可以用于测量氯离子浓度,从而实现更高精度的测量结果。
能斯特方程可以用来模拟氯离子浓度的变化,从而提高测量的准确性。
因此,氯离子选择性电极的应用可以帮助人们更好地掌握氯离子浓度的变化,从而改善氯离子浓度测量的准确性。
实验三 水中氯离子的测定-沉淀滴定法和电位滴定法

实验三、水中氯离子的测定(沉淀滴定法和电位滴定法)1.沉淀滴定法此法依据《水质氯化物的测定硝酸银滴定法》(GB 11896-89)一、实验目的和要求学习银量法测定氯含量的原理和方法;掌握AgNO3标准溶液的配制和标定方法。
二、实验原理在中性至弱碱性范围内(pH6.5—10.5),以铬酸钾为指示剂,用硝酸银滴定氯化物时,由于氯化银的溶解度小于铬酸银的溶解度,氯离子首先被完全沉淀出来后,然后铬酸盐以铬酸银的形式被沉淀,产生砖红色,指示滴定终点到达。
该沉淀滴定的反应如下:Ag++Cl—→AgCl↓2Ag++CrO4→Ag2CrO4↓(砖红色)三、实验仪器和设备(1)锥形瓶,250mL;(2)滴定管,25mL,棕色;(3)移液管,10mL,25mL,50mL;(4)容量瓶,100mL,1000mL。
四、实验试剂和材料分析中仅使用分析纯试制及蒸馏水或去离子水。
(1)氯化钠标准溶液,C(NaCl)=0.0141mol/L,相当于500mg/L氯化物含量:将氯化钠(NaCl)置于瓷坩埚内,在105℃下烘干2h。
在干燥器中冷却后称取8.2400g,溶于蒸馏水中,在容量瓶中稀释至1000mL。
用移液管吸取10.0mL,在容量瓶中准确稀释至100mL。
1.00mL此标准溶液含0.50mg氯化物(C1-)。
(2)硝酸银标准溶液,C(AgNO3)=0.0141mol/L:称取2.3950g于105℃烘半小时的硝酸银(AgNO3),溶于蒸馏水中,在容量瓶中稀释至1000mL,贮于棕色瓶中。
用氯化钠标准溶液(1)标定其浓度:用移液管准确吸取25.00mL氯化钠标准溶液于250mL或100mL锥形瓶中,加蒸馏水25mL。
另取一锥形瓶,量取蒸馏水50mL作空白。
各加入1mL铬酸钾溶液(3),在不断的摇动下用硝酸银标准溶液滴定至砖红色沉淀刚刚出现为终点。
计算每毫升硝酸银溶液所相当的氯化物量,然后校正其浓度,再作最后标定。
1.00mL 此标准溶液相当于0.50mg氯化物(C1—)。
氯离子选择性电极测定水中氯含量

氯离子选择性电极测定水中氯含量(标准加入法)一、实验目的:1、了解氯离子选择性电极的基本性能;2、掌握氯离子选择性电极的使用方法;3、掌握标准加入法测定水中含氯量的原理和操作方法;4、 学会使用酸度计测量电动势;二、基本操作:pHS-3D 型酸度计测量电动势方法如下:1、 打开电源开关,仪器进入测量状态2、 把离子选择性电极和参比电极夹在电极架上;3、 用蒸馏水清洗电极头部,再用被测溶液清洗一次;4、 把离子选择性电极的插头持入测量电极插座处;5、 把参比电极接入仪器后部的参比电极接口处;6、 把两电极插在被测溶液中,将溶液搅拌均匀;7、 按模式键至温度档(温度符号闪烁),再按上下键调节温度至室温(溶液温度),再按确定键将更改值输入;8、按模式键至显示“测试”读取数据。
三、实验原理氯离子选择性电极是由AgCl 和Ag 2S 的粉末混合物压制成的敏感膜,当将氯离子选择性电极浸入含Cl -的溶液中,可产生相应的膜电势(膜电势的大小与Cl -活度的对数值成线形关系)。
以氯离子选择性电极为指示电极,双液接甘汞电极为参比电极,插入试液中组成工作电池,当氯离子浓度在1~10-4mol/L 范围内,在一定的条件下,电池电动势与氯离子活度的对数成线性关系。
2.303lg Cl RT E K nF α-=-标准加入法是先测量电极在未知试液中的电动势,然后加入小体积待测组分的标准溶液,混合均匀后再测混合液中的电动势,根据两次测量的差值,代入公式计算待测组分的浓度。
先取体积为V x 、浓度为c r,x 的样品溶液,测得电动势E x ,再在样品溶液中加入体积为V s 、浓度为c r,s 的标准溶液,测得电动势E x+s ,参比电极作正极,指示电极作负极时,对阴离子,得x r,x lg c S K E +=)lg(s x r,x x r,s x V V V c V c S K E ss +++=+E -E E ∆=+x s xr s x ss r,c V V V c ∆=+1110-S E -c c )(r x r,∆∆=四、实验步骤1、将氯离子选择性电极和双盐桥甘汞参比电极与酸度计接好,通电预热15分钟,使仪器稳定;(思考题1)2、按模式键至温度档(温度符号闪烁),再按上下键调节温度至室温(溶液温度),再按确定键将更改值输入。
氯离子含量检测方法

氯离子含量检测方法以氯离子含量检测方法为题,本文将介绍几种常见的氯离子含量检测方法。
一、氯离子含量检测方法之离子色谱法离子色谱法是一种常用的氯离子含量检测方法。
该方法通过离子色谱仪来分离和检测样品中的氯离子。
首先,将样品溶解在水中,然后通过离子交换柱将样品中的其他离子和杂质分离出来,最后通过检测器检测样品中的氯离子含量。
离子色谱法具有高灵敏度、分析速度快、操作简单等优点,因此在水质检测和环境监测等领域得到广泛应用。
二、氯离子含量检测方法之氯离子选择电极法氯离子选择电极法是一种常用的氯离子含量检测方法。
该方法利用氯离子选择电极的选择性吸附和电势变化来检测样品中的氯离子含量。
通过将氯离子选择电极浸入样品中,利用电势差的变化来确定氯离子的含量。
氯离子选择电极法具有响应快、操作简单、准确度高等特点,因此在水处理、食品加工等领域广泛应用。
比色法是一种常用的氯离子含量检测方法。
该方法通过测量样品中氯离子与某种试剂发生反应后的溶液颜色的变化来确定氯离子的含量。
比色法根据不同的试剂选择,可以实现不同灵敏度的氯离子含量检测。
比色法具有简单、快速、便携等特点,因此在现场检测和快速检测中得到广泛应用。
四、氯离子含量检测方法之电导率法电导率法是一种常用的氯离子含量检测方法。
该方法通过测量样品中的电导率来确定氯离子的含量。
氯离子是电解质溶液中的主要离子之一,因此样品中氯离子的含量与电导率呈正相关关系。
电导率法具有操作简便、分析速度快、结果准确等优点,因此在水质监测和环境监测中得到广泛应用。
离子色谱法、氯离子选择电极法、比色法和电导率法是常用的氯离子含量检测方法。
这些方法各具特点,可以根据具体需求选择合适的方法进行氯离子含量检测。
在实际应用中,应根据样品特点、分析要求和设备条件等因素综合考虑,选择最合适的检测方法,以确保结果的准确性和可靠性。
实验十三 氯离子选择性电极的测试和应用

实验十三氯离子选择性电极的测试和应用Ⅰ、目的要求1.了解氯离子选择电极的基本性能及其测试方法,同时掌握氯离子选择性电极、玻璃电极、参比电极等的正确使用方法。
2.掌握用氯离子选择性电极测定氯离子浓度的基本原理。
3.掌握PHS—2C或是3B型酸度计的使用方法。
Ⅱ、基本原理氯离子选择性电极是一种测定水溶液中氯离子浓度的分析工具。
目前广泛应用于水质、土壤、地质、生物、医药、食品等部门。
其结构简单,使用方便。
本实验所用的电极是把AgCl和Ag2S的沉淀混合物压成膜片,用塑料管作为电极管,并以全固态工艺制成的。
电极结构如图1所示。
一、电极电位与离子浓度的关系氯离子选择性电极,是以AgCl作为电化学活性物质,它与Ag–AgCl电极十分相似。
当它与被测溶液接触时,就发生离子交换反应,结果在电极膜片表面建立具有一定电位梯度的双电层,这样,电极与溶液之间就存在着电位差,在一定条件下,其电极电位ф与被测溶液中的银离子活度a Ag+之间有以下关系:令AgCl的活度积为K ap,即K ap = a Ag+〃a Cl-式(1)可表示为在测量时,选取饱和甘汞电极作参比电极,两者在被测溶液中组成可逆电池,若фSCE为饱和甘汞电极的电位,则上述可逆电池的电动势为令则由于a Cl- = c Cl-〃γCl-式中c Cl-和γCl-分别为氯离子的浓度和活度系数,又令于是有E0′除与活度系数有关外,它还与膜片制备工艺有关,只是在活度系数恒定,并在一定条件下才可把它看作为常数。
这样一来,E与ln c Cl-或P c Cl-之间应呈线性关系。
只要测定不同浓度的E值,并将E对ln c Cl-或P c Cl-作图,就可了解电极的性能,并可确定其测量范围。
氯离子选择性电极的测量范围约为10-1 ~5×10-5摩尔浓度。
二、电极的选择性和选择性系数离子选择性电极常会受到溶液中其他离子的影响。
即,在同一电极膜上,往往可以有多种离子进行不同程度的交换。
实验三-氯离子选择性电极的测试和应用

实验三-氯离⼦选择性电极的测试和应⽤实验三氯离⼦选择性电极的测试和应⽤⼀、实验⽬的1、了解氯离⼦选择性电极的基本性能及其测定⽅法。
2、掌握⽤氯离⼦选择性电极测定氯离⼦浓度的基本原理。
3、了解酸度计测量直流毫伏值的使⽤⽅法。
⼆、实验仪器和药品酸度计,电磁搅拌器,217型饱和⽢汞电极,氯离⼦选择性电极,100ml 容量瓶,50mL 、10mL 移液管。
KCl (AR ),KNO 3(AR ),0.1%Ca(AC)2溶液,风⼲⼟壤样品。
三、实验原理1、电极电势与离⼦浓度的关系以氯离⼦选择性电极为指⽰电极,双液接⽢汞电极为参⽐电极,插⼊试液中组成⼯作电池(图3-11)。
当氯离⼦浓度在10-1~10-5mol ·L 范围内,在⼀定的条件下,电池电动势与氯离⼦活度的对数成线性关系。
ln ln ln Cl Cl Cl RT RT RT E E a E c E c F F Fθθθγγ--±-=-=-=- 在测定中,只要固定离⼦强度,则γ±可视为定值。
只要测出不同Cl c -值时的电动势E ,做ln Cl E c --图(标准曲线),就可⽤了解电极的性能。
并可从图中求出待测溶液的Cl -浓度。
2、电极的选择性和选择性系数离⼦选择性电极常会受到溶液中其它离⼦的影响。
也就是说,在同⼀电极膜上,往往可以有多种离⼦进⾏不同程度地交换。
离选择性电极的特点就在于对特定离⼦具有较好的选择性,受其它离⼦的⼲扰较⼩。
电极选择性的好环,常⽤选择性系数来表⽰。
但是,选择性系数与测定⽅法、测定条件以及电极的制作⼯艺有关,同时也与计算时所⽤的公式有关。
⼀般离⼦选择性电极的选择性系数k ij 可表⽰为:ln()i j Z Z i ij j RT E E a k a nF θ=±+式中,i 和j 分别代表待测离⼦和⼲扰离⼦,Z i 及Z j 分别代表i 和j 离⼦的电荷数;ij k 为该电极对j 离⼦的选择系数。
氯离子选择性电极与氯离子浓度符合能斯特方程

氯离子选择性电极与氯离子浓度符合能斯特方程氯离子选择性电极(ISE)是一种常见的用于测量氯离子浓度的分析仪器,它可以用来显示溶液中可测量物质含量的实时浓度。
氯离子是一种重要的水体污染物,因此,关于与氯离子浓度有关的知识及其准确测量方法的分析,对于水体质量管理监测非常重要。
其中极其重要的一点是,ISEs要符合能斯特方程。
能斯特方程(Nernst Equation)是一种物理化学方程式,用于计算有效浓度梯度感应开路电压,是ISE检测氯离子浓度的基础方法。
所谓“有效浓度梯度感应开路电压”,指在半电极体系中有氯离子活化的条件下,当浓度梯度存在时,所产生的开路电压,这种电压与物质的分布和浓度有关,而这种电压在选择性电极上反映出来,形成了ISE的选择性原理。
在选择性电极的设计的过程中,应该满足能斯特方程的条件,因为它描述了在半电极系统中有效活化的条件下,半电极的开路电压的大小,这是电极选择性的基础。
能斯特方程的推导是通过电势强度和热力学来解释的,可以表达为:E=E0+ (RT/nF) * ln(A/C)其中,E0为半电位均衡实验时产生的电压,R为常数,T为热力学温度,n为活化子数,F为电子伏特,A为两个半电极之间的活化物质,C是被量化的浓度。
根据上面的推理,由于系统中氯离子浓度的变化,ISEs的输出电压也随之变化,而这些变化刚好符合能斯特方程的定义,因此,ISE的设计应该符合能斯特方程,以确保在检测氯离子浓度时,结果是准确可靠的。
在实际操作中,ISE上的电压变化范围大约为60-190mV,每一个mV的变化,大约等于0.1ppm的氯离子浓度变化。
因此,可以根据ISE 上的电压变化,实时反映溶液中的氯离子浓度变化。
在选择ISE的过程中,应该综合考虑电极的性能,检测范围等需求,以及ISE的限制条件,如温度,PH,氯离子对应的电位活化系数,测量精度等,以保证ISE的准确度与可靠性。
此外,ISE的原理和原理都是由能斯特方程支撑的,这意味着在检测氯离子浓度时,用户还要保证ISE的工作状态,如检查ISE的供电是否稳定,检查电极是否损坏,以及检查电位系统是否处于均衡状态等,这些都会影响测量结果的准确度,如果不处理好,就会影响检测结果的准确性,从而影响氯离子浓度的准确测量。
氯离子选择性电极的测试和应用

2.配制0.100M的KNO3溶液和0.100M的 NaCl溶液各500ml。
Ⅳ、实验步骤
三、土壤样品的处理 1.在干燥洁净的烧杯中用台秤称取风干土壤样品 W克(约10克),加入0.1% Ca(Ac)2溶液V ml(约 100ml),搅动几分钟,静置澄清或过滤。 2.用干燥洁净的吸管吸取澄清液30~40ml,放 入干燥洁净的50ml烧杯中,待测。
Ⅱ、基本原理
二、电极的选择性和选择性系数 离子选择性电极常会受到溶液中其他离子的影 响。即,在同一电极膜上,往往可以有多种离子进 行不同程度的交换。离子选择性电极的特点就在于 对其特定离子具有较好的选择性,受其他离子的干 扰较小。电极选择性的好坏,常用选择性系数来表 示。 但是,选择性系数与测定方法、测定条件以及 电极的制作工艺有关,同时也与计算时所用公式有 关。一般离子选择性电极的选择性系数 Kij,可定义 为
Ⅱ、基本原理
二、电极的选择性和选择性系数
式中符号,对阳离子取“ + ”,阴离子取“ - ”; ai 为 被测离子的活度,zi为该离子所带的电荷数;aj为干 扰离子的活度, zj 为干扰离子所带的电荷数。如用 于表示Br- 对氯离子选择性电极的干扰,式( 6)可 具体表示为 由式(6)可知,Kij越小,表示j离子对被测离子i的 干扰越小,也就表示电极的选择性越好。
Ⅱ、基本原理
二、电极的选择性和选择性系数 测定Kij最简单的方法是分别溶液法。就是分 别测定在具有相同活度的离子 i 和 j 这两个溶液 中该离子选择电极的电极电位E1和E2。显然, E1= E0± RT/nF ln( ai+0) E2= E0± RT/nF ln( 0+Kij· aj) 因为ai=aj,所以,两电位之差
ห้องสมุดไป่ตู้
氯离子选择性电极的测定及应用

所以上式可改写为:
实验测定时,把饱和甘汞电极和氯离子选择电极插入待测溶液中就会组成原电池。则该电池的可逆电动势为:
令
一定温度下,E'和E''均可视为常数,得:
即E与 之间呈线性关系。只要测定与不同Cl-的浓度值相对应的E值并作图就可了解氯离子选择电极的性能。其直线部分就是就是该氯离子选择电极的测量范围。
西安交通大学实验报告
课程:
物理化学
实验日期:
专业班号:
组别:
交报告日期:
姓名:
学号:
同组者:
教师审批:
实验名称:氯离子选择性电极的测定及应用
一、实验目的
1.掌握氯离子选择性电极的基本原理;
2.了解氯离子选择性电极的性能及使用方法。
二、实验原理
1.电极电势与离子浓度的关系
氯离子选择性电极是以AgCl作为电化学活性物质,当它与被测溶液接触时,就会发生离子交换反应,从而在电极与溶液之间产生电势差。一定条件下:
六、思考与讨论:
(一)误差分析:
1.实验测量过程中,测定每组数据时温度存在波动,影响电极电势的测定;
2.溶液的配置过3的纯度有限,使得溶液的浓度与要求值有偏差,造成实验误差;
3.实验中用于配置溶液的容量瓶未烘干,致使容量瓶刻线以上有水滴影响定容,影响实际的溶液浓度;
三、实验仪器和药品
氯离子电极1支、饱和甘汞电极1支、PHS-2型酸度计1台、500mL容量瓶2个、250mL容量瓶2个、磁力搅拌器1台、25mL移液管1支、10.0g/L NaCl溶液、3.00g/L NaCl、未知液、NaCl(分析纯)、KNO3(分析纯)。
四、实验步骤
1.仪器安装:氯离子选择电极在使用前,应先在0.001mol/L的KCl溶液中浸泡1h使其活化,然后在蒸馏水中充分浸泡,必要时可重新抛光膜片表面。饱和甘汞电极的内管充装饱和KCl溶液,外管充装饱和KNO3溶液。安装好仪器。附近环境应无浓盐酸等酸雾,也无强烈电磁场干扰。
离子选择性电极法测定氯的实验教学问题解析

(O 一 ) 式中, 、 、x 分别为未知溶液和标准溶液的浓 1 1 ~, c c V、 度 、 积 ,E为 加入 标准 溶液前 后 的 电位 差 , 233 T n 。 体 A S为 .0 R / F
p ra tp sto Th l cr c mi a n l sso h r p rin a c u t d f r3 o tn o iin. e ee to he c la ay i ft e p o o to c o n e o 0% ~4 0% ,a d i wa i iu tt o r l n t sd f c l o c nto
r V
理论知识 , 更好地学 习化学专业课 。随着现代科 学技术 的发 展 ,
仪 器 分 析 的 应用 日益 广 泛 , 药 品 检 验 、 在 医学 检 验 、 生 检 验 、 卫 环 境保护 、 品保健和生物监测 等各领域 都发挥着重 要作用 。 食
是微量的标准溶液 , 即 》 , 故可得到近似的计算公式 : ==
高等学校的实践 教学在 本科教 学体 系中居 于重要 的地位 , 它能够有效提高学生 的观察能力 、 动手能力和解决 问题的能力 ,
有助于培养高素质 的创新人才 ~ 。仪 器分析实 验是化学及相 关学科专业 的实践教学课程 , 使学生 了解各 种仪器 的结 构 , 熟悉 各种仪器 的基本操作 及原理 , 理解 仪器分 析理论课 所涉及 到 的
t e e p rme t h e ul wa o ra c r c n e e t blt . Ma y a p c s t a n u n e te r s ls we e a ay e h x e i n ,t e r s t s p o c u a y a d r p aa i y i n s e t h tif e c d h e u t r n l z d l c mp e e sv l n o d rt t n a dz t d n ci n,S ha h oe pr c s e a r ce tf n g r u . o r h n iey i r e o sa d r ie su e ta to O t tt e wh l o e sb c me mo e s in i c a d r o o s i i Ke r s:c lrde in s l cie e e to e;sa d r ddto t o y wo d ho i o ee tv lcr d tn a d a i n meh d;e p rme t lr s ls n y i i xe i n a e u t ;a a ss l
氯离子选择性电极的测试和应用资料

Kij的测定
当zi=zj时,测定kij最简单的方法是分别
溶液法。就是分别测定在具有一样活度的离子i
和j这两个溶液中该离子选择性电极的电位E1和
E2,那么:
E1E0R nF Tlnai 0
(6)
E2E0R nF lTn0kijaj
(7) (8)
RT
EE1E2nF lnkij
对于阴离子选择性电极:
2.理解酸度计的使用方法〔测量直流毫伏值〕 。
3. 理解固定离子强度的意义及方法。 。
主菜单
上一步
完成
三、实验原理
离子选择性电极是一种分析测量工具,可以通 过简单的电势测量直接测定溶液中某一离子的活度。 该技术广泛应用于海洋、土壤、地质、化工、医学 等各个领域中。
本实验所用的氯离子选择性电极是把AgCl和 Ag2S的沉淀混合物压成膜片,用塑料管作为电极管, 并以全固态工艺制成。其构造如以下图所示。
们测出不同CCl-值时的电位值E,作E-lnCCl-图,就可
理解电极的性能,并可确定其测量范围。氯离子选择
性电极的测量范围约为10-1mol·dm-3~10-5mol·dm-3。
2. 离子选择性电极的选择性及选择系数
离子选择性电极对待测离子具有特定的响应特性,但
其它离子仍可对其产生一定的干扰。电极选择性的好
来水稀释至刻度,测定其电位值,从标准曲线上求 得相应的氯离子浓度。 7. 土壤中NaCl含量的测定
(1) 在枯燥干净的烧杯中用台称称取风干土壤样 品W克(约10g),参加0.1%Ca(Ac)2溶液VmL(约 100mL),搅动几分钟,静置澄清或过滤。
(2) 用枯燥干净的吸管汲取澄清液30mL~40mL, 放入枯燥干净的50mL烧杯中,测定其电位值。
实验八_氯离子选择性电极性能的测试及自来水中氟含量的测定

实验八 氯离子选择性电极性能的测试及自来水中氟含量的测定氯离子选择性能的测试一、实验目的了解离子选择性电极的主要特征,掌握离子选择性电极测定电位选择性系数的原理、方法及操作技术。
二、实验原理与技术离子选择性电极是一种电化学传感器,它对特定的离子有电位响应。
但任何一支离子选择性电极不可能只对溶液中的某特定离子有响应,对其他某些离子也会有响应,若把氯离子选择性电极侵入含有Br -溶液时,也会产生膜电位。
当Cl -和Br -共存于溶液中时,由于Br -存在必然会对Cl -的测定产生干扰。
为了表明共存离子对电位的“贡献”,可用一个扩展的能斯特公式描述:)a a lg(nFR 303.2K b /n j ij i K T E +±= 式中:i 为被测离子;j 为干扰离子;n 和b 分别为被测离子和干扰离子的电荷数;K ij 为电位选择系数。
从上式可以看出,电位选择系数愈小,电极对被测离子的选择性愈好。
测定K ij 的方法可以用分别溶液法和混合溶液法,本实验采用混合溶液法测定K ij 。
混合溶液法是i 、j 离子共存于溶液中,实验中配制一系列含有固定活度的干扰离子和不同活度的被测离子的标准溶液,分别测量电位值,绘成曲线,如图所示。
曲线中的斜线部分(ai >a j )的能斯特方程为:111lg 303.2a nFRT K E ±= 在曲线的水平部分(a j >a i ),电极对i 离子的响应可以忽略,电位值完全由j 离子决定,则:b n j ij a K nFRT K E /22lg 303.2±= 假定K 1=K 2,且两斜率相同,在两直线的交点处E 1=E 2,可以得出下述公式:b /nji ij a /a =K 因此可以求得K ij 值,这一方法也称为固定干扰法,本实验以Br -为干扰离子,测定氯离子选择性电极的电位选择系数-Br ,-Cl K 。
三、实验用品1、仪器pHS-3D 型酸度计;电磁搅拌器;217型饱和甘汞电极;PCl-1型氯离子选择性电极;容量瓶;移液管。
氯离子选择电极

电化学实验二、氯离子选择电极测定水样中氯离子的浓度【预习】1. PXSJ -216F 型离子计使用说明。
2. 氯离子选择电极使用注意事项。
3. 双液接饱和甘汞电极使用注意事项。
4. 直接电位法基本原理。
【实验目的】1. 掌握用标准曲线法测定氯离子浓度的原理和方法。
2. 学会PXSJ -216F 型离子计测定离子浓度的方法。
3. 了解测定氯离子浓度时的干扰因素。
【实验原理】以待测离子的选择电极为指示电极,饱和甘汞电极(SCE )为参比电极,浸入待测试液中组成原电池,通过对电池电动势的测量,进而求出待测离子的浓度。
电池表示为:( - )离子选择电极∣试液 ¦¦ KCl (饱和), Hg 2Cl 2(s) ∣Hg ( + )电池电动势为: SCE E ϕϕ-=离子 电动势与离子浓度的关系为:pCl nFRT K E 303.2+= 由上式可知:E 与pCl 成线性关系。
通过测定一系列已知氯离子浓度的标准溶液的E 值,绘制E - pCl 标准曲线。
由水样测得的E 值,通过标准曲线可求算出水样中氯离子浓度。
【仪器与试剂】PXSJ -216F 型离子计,氯离子选择电极,JB-10型搅拌器,双液接饱和甘汞电极,温度传感器(温度电极),100ml 容量瓶5个,10ml 、25ml 移液管,50ml 小烧杯,洗瓶,洗耳球,小镊子,搅拌子,滤纸条等。
1.00⨯10-1 mol/L NaCl 标准溶液,0.1 mol/L KNO 3 溶液,10-3 mol/L NaCl 溶液(活化电极用),水样,0.1mol/L NaBr 和0.1mol/L NaSO 4溶液。
【实验步骤】1.标准溶液的配制:由1.00⨯10-1mol/L NaCl标准溶液,用100.00ml容量瓶,用逐级稀释法配制浓度为 1.00⨯10-2、5.00⨯10-3、1.00⨯10-3、5.00⨯10-4、1.00⨯10-4 mol/L的一组标准溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验三 氯离子选择性电极的测试和应用
一、 实验目的
1、了解氯离子选择性电极的基本性能及其测定方法。
2、掌握用氯离子选择性电极测定氯离子浓度的基本原理。
3、了解酸度计测量直流毫伏值的使用方法。
二、实验仪器和药品
酸度计,电磁搅拌器,217型饱和甘汞电极,氯离子选择性电极,100ml 容量瓶,50mL 、10mL 移液管。
KCl (AR ),KNO 3(AR ),0.1%Ca(AC)2溶液,风干土壤样品。
三、 实验原理
1、电极电势与离子浓度的关系
以氯离子选择性电极为指示电极,双液接甘汞电极为参比
电极,插入试液中组成工作电池(图3-11)。
当氯离子浓度
在10-1~10-5mol ·L 范围内,在一定的条件下,电池电动
势与氯离子活度的对数成线性关系。
ln ln ln Cl Cl Cl RT RT RT E E a E c E c F F F
θθθγγ--±-=-=-=- 在测定中,只要固定离子强度,则γ±可视为定值。
只要测
出不同Cl c -值时的电动势E ,做ln Cl E c --图(标准曲线),
就可用了解电极的性能。
并可从图中求出待测溶液的Cl -浓度。
2、电极的选择性和选择性系数
离子选择性电极常会受到溶液中其它离子的影响。
也就是说,在同一电极膜上,往往可以有多种离子进行不同程度地交换。
离选择性电极的特点就在于对特定离子具有较好的选择性,受其它离子的干扰较小。
电极选择性的好环,常用选择性系数来表示。
但是,选择性系数与测定方法、测定条件以及电极的制作工艺有关,同时也与计算时所用的公式有关。
一般离子选择性电极的选择性系数k ij 可表示为:
ln()i j Z Z i ij j RT E E a k a nF θ=±+
式中,i 和j 分别代表待测离子和干扰离子,Z i 及Z j 分别代表i 和j 离子的电荷数;ij k 为该电极对j 离子的选择系数。
式中“-”及“+”分别适用于阴、阳离子选择性电
极。
ij k 越小,表示j 离子对被测离子的干扰越小。
当Z i =Z j 时,测定ij k 最简单
的方法是分别溶液法:分别测定在具有相同活度的离子i 和j 这两个溶液中该离子选择性电极的电动势E 1和E 2。
12()ln ij E E nF k RT
-= 四、 实验步骤
1、标准溶液配制
配100mL0.1mol·L -1 KCl 标准溶液,用0.1 mol·L -1 KNO 3溶液逐级稀释配5×10-2,1×10-2、5×10-3、1×10-3、5×10-4、1×10-4 mol·L -1 KCl 标准溶液。
2、安装仪器
3、标准曲线测量
校正仪器后,用蒸馏水洗净电极,用滤纸吸干,将电极依次从稀到浓插入标准溶液中测定电动势。
4、选择系数测定
配制0.01 mol·L -1的KCl 和KNO 3溶液各100mL ,分别测定电动势值。
5、自来水中氯离子含量的测定
称 0.1011g KNO 3于100mL 容量瓶中(目的:保持相同的离子强度),用自来水稀释至刻度,测定其电动势值,从标准曲线上求得相应的氯离子浓度。
6、土壤中NaCl 含量的测定
(1)用台秤称风干土壤样品约10g ,加入0.1% Ca(AC)2溶液约100mL ,搅动几分钟,静置澄清。
(2)用干燥洁净的吸管吸澄清液30-40mL ,放人干燥洁净的50mL 烧杯中,测定其电动势值。
五、 数据处理
1、以标准溶液的E 对lgC 作图绘制标准曲线。
2、计算k Cl-NO3-。
3、从标准曲线上查出被测自来水中氯离子的浓度,
4、 计算风干土壤中NaCl 的含量:NaCl%100%1000CxVM W
=⨯ 式中,Cx 为从标准曲线上查得的样品中Cl -浓度;V (mL )为0.1%Ca(AC)2溶液的体积;M 为NaCl 的摩尔质量;W 为土壤质量(单位:g )。
六、 注意事项
1、氯离子选择性电极在使用前应在10-3 mol·L -1 KCl 溶液中浸泡活化1h ,然后在蒸馏水中充分浸泡方可使用,这样可缩短电极响应时间并改善线性关系;电极响应膜切勿用手指或尖硬的东西碰划,以免沾上油污或损坏,影响测定;使用后立即用蒸馏水反复冲洗,以延长电极使用寿命。
2、双液接甘汞电极在使用前应拔去加在KCl 溶液小孔处的橡皮塞,以保持足够的液压差,并检查KCl 溶液是否足够;由于测定的是Cl -,为防止电极中Cl -的渗入被测液而影响测定,需要加饱和KNO 3溶液作为外盐桥。
由于Cl -不断渗入外盐桥,所以外盐桥内的KNO 3溶液不能长期使用,应在每次实验后将其倒掉洗净,放干,在下次使用时重新加入饱和KNO 3溶液。
3、氯离子选择性电极宜浸在蒸馏水中,长期不用可洗净干放,但在使用前需要用蒸馏水充分浸泡,必要时可重新抛光膜片表面。
4、安装电极时,两支电极不要彼此接触,也不要碰到杯底或杯壁。
5、每次测试前,需要少量被测液将电极与烧杯淋洗三次。
6、切勿把搅拌珠连同废液一起倒掉。
