宋天佑版无机化学 第14章碳族元素
碳族元素学习笔记无机化学

碳族元素预习笔记一、碳族元素通性1、原子结构性质⑴相似性:•外层电子构型:ns²np²气态氢化物的通式:RH4最高价氧化物对应的水化物通式为H2RO3或R(OH)4⑵递变性•+2价化合物主要氧化态稳定性:由上至下逐渐增强+4价化合物主要氧化态稳定性:由上至下逐渐减弱但铅(Ⅱ)化合物稳定性高于铅(Ⅳ),铅(Ⅳ)本身为强氧化剂。
•熔沸点降低(锡和铅反常),单质密度逐渐增大•金属性增强,非金属性减弱,(由于半径不断增大,原子核对外层电子引力变小所致)•最高价氧化物对应水化物的酸性减弱(最高价氧化物对应的酸举个例子解释:碳酸H2CO3。
(HO)2-CO连接一个氧原子,氧原子强吸电子作用导致碳原子电子云密度下降,对应的碳原子同样要从羟基上边多取电子,那么最终结果就是羟基氧原子再把和氢原子公用的电子对拉向自己。
那么此时氢原子是缺电子的,就会很容易电离。
氢原子越缺电子越容易电离;那么对应的中心原子越吸电子,氢原子就越缺电子。
所以从上到下,元素原子电负性减弱,吸电子能力减弱,自然氢离子电离能力减弱,酸性减弱。
)•氢化物的稳定性减弱•第一电离能:由碳至铅逐渐减小(同主族由上至下半径增大,更易失去最外层电子)特殊:锡<铅•熔沸点:由碳至铅逐渐减小(碳、硅为原子晶体,锗、锡、铅为金属晶体)二、元素的成键特性⒈碳:①共价键(sp:CO sp²:乙烯 sp³:甲烷):碳碳,碳氢,碳氧键键能大,稳定,因此碳氢氧可形成多种有机化合物。
②以碳酸盐的形式存在于自然界中2.硅:①硅氧四面体形式存在(石英,硅酸盐矿)②硅硅,硅氧,硅氢键较弱,可形成有机化合物但数量较少3.锡铅:①离子键(+2氧化态,SnO、PbO +4氧化态,SnCl4)②共价键(+4氧化态,SnO、PbO2)二、碳及其化合物1.单质(三种同素异形体)①金刚石:结构:sp³杂化,原子晶体,五个碳原子构成正四面体性质:硬度最大,熔沸点很高(由于其为空间网状结构),无色透明,不导电,化学惰性,但800°C以上与空气反应成CO2②石墨:结构:sp²杂化,层状原子晶体,每层上的碳原子各提供一个含成单电子的p轨道形成大π键层与层之间靠分子见作用力结合在一起。
[实用参考]无机化学-碳族元素.ppt
![[实用参考]无机化学-碳族元素.ppt](https://img.taocdn.com/s3/m/b8f4c5919ec3d5bbfc0a744d.png)
直线形 直线形
C2H2、HCN CO
2019/8/9 4
一、碳族元素在自然界的分布 二、碳族元素的单质 三、氧化物 四、含氧酸及其盐 五、氢化物 六、卤化物和硫化物
2019/8/9 5
一、自然界的分布
C 单质状态:主要是金刚石和石墨。化合
物:煤、石油、天然气、动植物、
石灰石、白云石、CO2等。
Si靠Si-O键联结成各种链状、层状和立体
2019/8/9 15
Pb: 质软、密度大(11.35g·cm-3),纯铅在空气中不稳定 →Pb(OH)2或Pb2(OH)2CO3
C(石墨)→(金刚石)石理墨:转化为金刚石的机
△fGmθ/kJ·mol-1 0
ρ/g·cm-3
2.260
2.9 ⑴ 溶剂说:石墨先溶解 3.515 在溶剂(金属催化剂)
△fHmθ/kJ·mol-1
O
1.897 中成为单个碳原子,然 后在冷却时直接生成金
反应的特点? 吸热、体积减小 刚石。
欲使反应正向进行,采取的措施?⑵ 固相转化说:石墨的
第十四章 碳族元素
§14-1 碳族元素的通性 §14-2 碳族元素的单质及其化合物 §14-3 无机化合物的水解性
2019/8/9 1
元素符号 C Si Ge Sn
Pb
价电层结构 2s22p2 3s23p2 4s24p2 5s25p2
6s26p2
电负性
2.01 1.96(Ⅳ) 2.33 (Ⅳ) 2.25 1.90 (Ⅳ) 1.80(Ⅱ) 1.87 (Ⅱ)
2019/8/9 9
上图:纳米管在预先做 好阵列的硅晶片上催化 生长的结果。把Si晶片 置于一个充满乙烯容器 内,在特定的晶面上涂上 催化剂,加热后,高纯 的碳管以惊人的速度生 长,其速度可以达到每 小时500英里。
无机化学之 碳族元素

14-1-1
1
(2)石墨 )
碳元素的单质
碳的同素异形体
硬度较小, 熔点较高, 硬度较小 , 熔点较高 , 表 现出一定程度的化学活性。 现出一定程度的化学活性。 碳原子以 sp2 杂化 , 形成 杂化, 片层结构 。 CI2N00254.jpg
电子, 每个碳原子的未参与杂化的 p 电子,形成大 Πn键。这 n 些离域电子使得石墨具有良好导电性。层间的分子间力很 些离域电子使得石墨具有良好导电性。 所以层间易于滑动,故石墨质软具有润滑性。 弱,所以层间易于滑动,故石墨质软具有润滑性。可制作 电极、热电偶、坩锅、铅笔芯等。 电极、热电偶、坩锅、铅笔芯等。
2
二氧化碳
碳的含氧化合物
用于制备纯碱、小苏打、碳酸氢氨、 工业上 CO2 用于制备纯碱、小苏打、碳酸氢氨、啤 酒、饮料、干冰。 饮料、干冰。 在常压下,干冰不经熔化,于 194.5 K 时直接升华气 在常压下,干冰不经熔化, 化,因此常用来做制冷剂和人工造雨。 因此常用来做制冷剂和人工造雨。 气中能继续燃烧, 着火的镁条在 CO2 气中能继续燃烧,所以 CO2 不助 燃也是相对的。 燃也是相对的。
14-1-1 14-
2
碳单质的还原性
碳
单质
在 (d) (b) 两线交点所对应的温度 T1 ≈ 1200K 下,反 θ θ 相等, 应 (d) 和反应 (b) 的 ∆rGm 相等,反应 (1) 的∆rGm =0 碳还原氧化锌的反应就可自发进行。 当 T > T1 时,碳还原氧化锌的反应就可自发进行。
第 14 章 碳族元素
14 - 1
碳族元素
C Si Ge ns2np2 0、+2、+4 、 、 +2 氧化态稳定性增强 氧化态稳定性增强 +4 氧化态稳定性减弱 氧化态稳定性减弱 ns2 稳定性 稳定性↑──惰性电子对效应 惰性电子对效应 Sn Pb
宋天佑无机化学教程元素部分化学方程式

第十一章 碱金属和碱土金属化学方程式(或离子方程式)条件 3Ca +N 2=Ca 3N 2 410℃ 6Li +N 2=2Li 3N △ 2Na +2H 2O =2NaOH +H 2↑ Ca +2H 2O =Ca(OH)2+H 2↑2Na ·n Hg +2H 2O =2NaOH +H 2↑+2n HgZrO 2+2Ca =Zr +2CaO △ 2Na +H 2=2NaH△ TiCl 4+4NaH =Ti +2H 2↑+4NaCl△ KH +H 2O =KOH +H 2↑ 2Na +2NaOH =2Na 2O +H 2↑ △ 3NaN 3+NaNO 2=2Na 2O +5N 2↑ △ 10K +2KNO 3=6K 2O +N 2↑△ 2BaO +O 2=2BaO 2>500℃4KOH(s)+4O 3(g)=4KO 3(s)+2H 2O(s)+O 2(g)2KO 3=2KO 2+O 2↑ 4KO 3+2H 2O =4KOH +5O 2↑ Be(OH)2+2H +=Be 2++2H 2O Be(OH)2+2OH -=[Be(OH)4]2- Be(OH)2+2OH -=BeO 22-+2H 2ONa ++Zn 2++3UO 22++9Ac -+9H 2O =NaZn(UO 2)3(Ac)9·9H 2O ↓2K ++Na ++[Co(NO 2)6]3-=K 2Na[Co(NO 2)6]↓ MgCl 2·6H 2O =Mg(OH)Cl +HCl ↑+5H 2O△ MgCl 2·6H 2O =MgCl 2+6H 2O HCl 气氛,△CuSO 4·5H 2O =CuSO 4+5H 2O △ CaCl 2·6H 2O =CaCl 2+6H 2O △ 4LiNO 3=2Li 2O +4NO 2+O 2↑773KK2[FeIO6]+Li+=KLi[FeIO6]↓+K+Mg2++CaO+H2O=Mg(OH)2+Ca2+Mg(OH)2+2HCl+4H2O=MgCl2·6H2OMgCl2=2Mg+Cl2↑通电2MgO+2Cl2+C=2MgCl2+CO2高温CaMg(CO3)2=MgO+CaO+2CO2↑1150℃2MgO+CaO+FeSi=2Mg+CaSiO3+Fe 高温KCl(l)+Na=NaCl+K(g) △2RbCl(l)+Ca=CaCl2+2Rb(g) △BaSO4+4C=BaS+4CO↑高温BaSO4+4CO=BaS+4CO2↑高温2BaS+2H2O=Ba(OH)2+Ba(HS)2Ba(OH)2+CO2=BaCO3↓+H2OBa(HS)2+CO2+H2O=BaCO3↓+2H2S2LiAl(SiO3)2+K2SO4=Li2SO4+KAl(SiO3)2高温2LiF+Na2CO3=Li2CO3+Na2F 熔融2LiAl(SiO3)2+9CaO=Li2O+CaO·Al2O3+4[2CaO·SiO2] 高温第十二章硼族元素化学方程式(或离子方程式)条件4B+3O2=2B2O3高温4B+6H2O(g)=2H3BO3+3H2赤热B+3HNO3(浓)=H3BO3+3NO2↑2B+2NaOH+3KNO3=2NaBO2+3KNO2+H2O 熔融2MnB+6H+=B2H6↑+2Mn3+4BCl3+3LiAlH4=2B2H6+3LiCl+3AlCl3乙醚4BF3+3NaBH4=2B2H6+3NaBF4乙醚B2O3+2Al+3H2=B2H6+Al2O3AlCl3,加温加压2B2H6=B4H10+H25B4H10=4B5H11+3H22CH4=C2H2+3H21500℃B2H6+3O2=B2O3+3H2O 自燃B2H6(g)+6Cl2(g)=2BCl3(g)+6HCl(g) 低温B2H6+6H2O=2B(OH)3+6H2B2H6+2LiH=2LiBH4乙醚3B2H6+6NH3=2B3N3H6+12H2高温B2O3+3H2O=2H3BO3B2O3+H2O(g)=2HBO2CoO+B2O3=Co(BO2)2熔融H3BO3+H2O⇌[B(OH)4]-+H+H3BO3+2C3H5(OH)3⇌[B(C3H6O3)2]-+3H2O+H+B(OH)3+H3PO4=BPO4↓+3H2O3C2H5OH+B(OH)3=(C2H5O)3B+3H2O 浓H2SO4[B4O5(OH)4]2-+5H2O=H3BO3+2[B(OH)4]-BCl3+NH3=BN+3HCl 1000K BF3+3H2O=B(OH)3+3HFBF3+HF=H++[BF4]-BCl3+3H2O=B(OH)3+3HClB2O3+3Mg=3MgO+2B 高温2BBr+3H2=2B+6HBr 钨丝,高温Mg2B2O5·H2O+2NaOH=2NaBO2+2Mg(OH)2高温4NaBO2+CO2+10H2O=Na2B4O7·10H2O+Na2CO3Na2B4O7+H2SO4+5H2O=4H3BO3+Na2SO42H3BO3=B2O3+3H2O △Mg2B2O5·H2O+2H2SO4=2H3BO3+2MgSO4△2Al+3S=Al2S3高温2Al+Fe2O3=2Fe+Al2O3点燃4Al·n Hg+3O2+2n H2O=2Al2O3·n H2O+n Hg2Al+3H2SO4=Al2(SO4)3+3H2↑Al+6HNO3=Al(NO3)3+3NO2↑+3H2O2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑3n LiH+n AlCl3=(AlH3)n+3n LiCl 乙醚4LiH+AlCl3=LiAlH4+3LiCl 乙醚Al2O3+3H2SO4=Al2(SO4)3+3H2OAl2O3+2NaOH+3H2O=2Na[Al(OH)4]3K2S2O7+Al2O3=Al2(SO4)3+3K2SO4共熔Al(OH)3+3HCl=AlCl3+3H2OAl(OH)3+NaOH=Na[Al(OH)4]AlO2-+2H2O=Al(OH)3↓+OH-Al3++3H2O=Al(OH)3↓+3H+2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑2Al(OH)3↓+3H2SO4=Al2(SO4)3+6H2O2Al+3Cl2=2AlCl3△2Al2O3+6Cl2+3C=4AlCl3+3CO2高温Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 加压煮沸2Na[Al(OH)4]+CO2=2Al(OH)3↓+Na2CO3+H2O2Al(OH)3+12HF(aq)+3Na2CO3=2Na3AlF6↓+CO2↑+9H2O2Al(OH)3=Al2O3+3H2O 焙烧2Ga+3H2SO4=Ga2(SO4)3+3H2↑2In+3H2SO4=In2(SO4)3+3H2↑2Tl+H2SO4=Tl2SO4+H2↑2Ga+2NaOH+6H2O=2Na[Ga(OH)4]+3H2↑2M(OH)3=M2O3+3H2O(M=Ga、In、Tl)△Tl2O3=Tl2O+O2↑△2In(OH)3+3H2SO4=In2(SO4)3+6H2OIn2(SO4)3+3H2S=In2S3↓+3H2SO4Tl2(SO4)3+4FeSO4=Tl2SO4+2Fe2(SO4)3Tl(NO3)3+SO2+2H2O=TlNO3+H2SO4+2HNO3Tl(NO3)3+3KI=3KNO3+TlI↓+I2↓2Tl3++H2S+2OH-=Tl2S↓+2H2OTlCl3=TiCl+Cl2↑TiCl+H2SO4=TlHSO4+HCl3TlNO3+Cl2=Tl(NO3)3+2TlCl32TiCl+2Cl2+4H2O=2TlCl3·4H2O2Na[Ga(OH)4]+CO2=2Ga(OH)3↓+Na2CO3+H2O第十三章 碳族元素化学方程式(或离子方程式)条件 SiO 2+2C =Si +2CO ↑2C +O 2=2CO Si +O 2=SiO 2 2Hg +O 2=2HgO 4Ag +O 2=2Ag 2O 2Zn +O 2=2ZnO 2Mg +O 2=2MgO 2Ca +O 2=2CaO CaCO 3=CaO +CO 2↑CaCO 3+2HCl(稀)=CaCl 2+H 2O +CO 2↑CO 2+Ca(OH)2=CaCO 3+H 2OHCOOH =CO ↑+H 2O 热浓H 2SO 4 H 2C 2O 4(s)=CO ↑+CO 2↑+H 2O热浓H 2SO 4Ni(CO)4(l)=Ni +4CO ↑ △ CO +Cl 2=COCl 2 催化剂或光照 CO +NaOH =HCOONa 高温、高压 CO +H 2→多种有机化合物 催化剂CO +PdCl 2+H 2O =Pd ↓+CO 2+HCl2Mg 2++2CO 32-+H 2O =Mg(OH)2·MgCO 3+CO 2↑Mg 2++HCO 3-=MgCO 3↓+H +Na 2CO 3=Na 2O +CO 2↑ 850℃ MgCO 3=MgO +CO 2↑ 540℃ 2NaHCO 3=Na 2CO 3+H 2O +CO 2↑270℃ H 2CO 3=H 2O +CO 2↑ 常温 CH 4+4Cl 2=CCl 4+4HCl >300℃ CS 2+2Cl 2=CCl 4+2S FeS ,△ CS 2+3O 2=CO 2+2SO 2点燃5CS 2+4MnO 4-+12H +=5CO 2↑+10S ↓+4Mn 2++6H 2OK 2S +CS 2=K 2CS 3 K 2O +CO 2=K 2CO 3 C +2S(g)=CS 2 红热 CH 4+4S =CS 2+2H 2S催化剂,600℃Mg 2C 3+4H 2O =2Mg(OH)2+CH ≡C —CH 3↑Al 4C 3+12H 2O =4Al(OH)3+3CH 4↑Si +2Cl 2=SiCl 4(l) 400~600℃ SiCl 4+2H 2=Si(纯)+4HCl催化,电炉3Si +18HF +4HNO 3=2H 2SiF 6+4NO ↑+8H 2OSi +2NaOH +8H 2O =Na 2SiO 3+2H 2↑SiO 2+4Mg =Mg 2Si +2MgO 灼烧 Mg 2Si +4HCl =SiH 4↑+2MgCl 2 SiCl 4+LiAlH 4=SiH 4↑+LiCl +AlCl 3乙醚 SiH 4+2O 2=SiO 2+2H 2OSiH 4+8AgNO 3+2H 2O =SiO 2↓+8HNO 3+8Ag ↓ SiH 4+2MnO 4-=2MnO 2↓+SiO 32-+H 2O +H 2↑ SiH 4+(n +2)H 2O =SiO 2·n H 2O ↓+4H 2↑OH - SiO 2+Na 2CO 3=Na 2SiO 3+CO 2 熔融 SiO 44-+4H +=H 4SiO 4↓ H 6Si 2O 7+H 4SiO 4=H 8Si 3O 10+H 2O H 6Si 2O 7+H 8Si 3O 10=H 12Si 5O 16+H 2OSiX 4+4H 2O =H 4SiO 4↓+4HX ↑(X =F 、Cl 、Br 、I )SiF 4+2HF =H 2SiF 6 SiO 2+2Cl 2+C =SiCl 4+CO 2 高温 SiO 2+4HF =SiF 4↑+2H 2OSiO 2+2CaF 2+H 2SO 4=2CaSO 4+SiF 4↑+2H 2OGe +2Br 2=GeBr 4220℃Sn +O 2=SnO 2 △ Sn +2S =SnS 2 △ Pb +S =PbS △ Ge +2H 2=GeH 4 750~800℃Sn +2HCl(浓)=SnCl 2+H 2↑ Pb +4HCl(浓)=H 2PbCl 4+H 2↑ Ge +4HCl(g)=GeCl 4+2H 2干燥,△Ge +4HNO 3(浓)=GeO 2(s)+4NO 2↑+2H 2O Sn +4HNO 3(浓)=SnO 2(s)+4NO 2↑+2H 2O Pb +4HNO 3(浓)=Pb(NO 3)2+2NO 2↑+2H 2O 3Pb +8HNO 3(稀)=3Pb(NO 3)2+2NO ↑+4H 2OPb +OH -+2H 2O =[Pb(OH)3]-+H 2↑ Sn +2OH -+4H 2O =[Sn(OH)6]2-+2H 2↑△ GeO 2+H 2=GeO +H 2O △ Ge(OH)2+NaOH =NaHGeO 2+H 2O Ge +4H 2SO 4=Ge(SO 4)2+2SO 2+4H 2OGeCl 4+4TlAc =GeAc 4+4TlCl在乙酐中 2SnO =SnO 2+Sn 强热 2SnO +2Cl 2=SnO 2+SnCl 4 △ PbO +OH -=HPbO 2-Pb 2++2OH -=Pb(OH)2↓ Pb(OH)2+NaOH =NaHPbO 2+H 2O Pb(OH)2+2HCl(热)=PbCl 2+2H 2O Pb 3O 4+8HAc =PbAc 4+2PbAc 2+4H 2O△ PbAc 2+NaClO +2NaOH =PbO 2↓+2NaAc +NaCl +H 2O△ 5PbO 2+2Mn 2++4H +=5Pb 2++2MnO 4-+2H 2O 微热 Pb 3O 4+4HNO 3=2Pb(NO 3)2+2PbO 2+2H 2OPbO 2+4HCl =PbCl 2+Cl 2↑+2H 2O2Fe3++Sn2+=2Fe2++Sn4+2Sn2++O2+4H+=2Sn4++2H2O2HgCl2+SnCl2+2HCl=Hg2Cl2↓+H2SnCl6Hg2Cl2+SnCl2+2HCl=2Hg↓+H2SnCl6Ge(OH)2+2NaOH=Na2GeO3+H2O+H2↑SnCl4+2Cl-=SnCl62-PbI2+2I-=PbI42-SnCl2+H2O=Sn(OH)Cl↓+HClPb2++S2-=PbS↓3SnS2+6NaOH=Na2SnO3+Na2SnS3+3H2OGeS2+Na2S=Na2GeS3SnS2+Na2S=Na2SnS32PbS+3O2=2PbO+2SO2焙烧4As+10NaOH+2NaNO3=4Na3AsO4+5H2↑+N2↑第十四章 氮族元素化学方程式(或离子方程式)条件 N 2+3H 2=2NH 3 高温高压,催化剂N 2+O 2=2NO 放电 3Ca +N 2=Ca 3N 2 410℃ 6Li +N 2=2Li 3N △ NH 4NO 2(aq)=2H 2O +N 2↑ △ NH 4Cl +NaNO 2=NaCl +2H 2O +N 2↑ △ (NH 4)2Cr 2O 7(s)=Cr 2O 3+4H 2O +N 2△ 2NH 3=NH 4++NH 2-2Na +2NH 3=2Na ++NH 2-+H 2↑ Na +n NH 3(l)=2Na ++e(NH 3)n-AgCl +2NH 3=[Ag(NH 3)2]++Cl - 2NH 3+3O 2(纯)=2N 2+6H 2O 燃烧 4NH 3+5O 2=4NO +6H 2O Pt ,△ 2NH 3+3Cl 2=N 2+6HCl 2NH 3+3Br 2=N 2+6HBr 2NH 3+3CuO =N 2+3Cu +3H 2O△ NH 3+HNO 2=N 2+2H 2O 3Mg +2NH 3(g)=Mg 3N 2+3H 2 △ 2Na +2NH 3(l)=2NaNH 2+H 2 NH 4Cl(浓)+3Cl 2=4HCl +NCl 3 COCl 2+4NH 3=CO(NH 2)2+2NH 4Cl SOCl 2+4NH 3=SO(NH 2)2+2NH 4ClHgCl 2+2NH 3·H 2O =Hg(NH 2)Cl ↓+NH 4Cl +2H 2ONH 3·H 2O ⇌NH 4++OH -In 2(SO 4)3+6NH 3·H 2O =2In(OH)3↓+3(NH 4)2SO 4ZnCl 2+2NH 3·H 2O =Zn(OH)2↓+2NH 4Cl2CuSO4+2NH3·H2O=Cu2(OH)2SO4↓+(NH4)2SO4(NH4)3PO4=3NH3+H3PO4△(NH4)2SO4=NH3+NH4HSO4△NH4HCO3=NH3+CO2+H2O △NH4HS=NH3+H2S △NH4NO3=N2O+2H2O △3H2+N2=2NH3催化剂,高温高压2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3△Ca3N2+6H2O=3Ca(OH)2+2NH3↑2NH3+NaClO=N2H4+NaCl+H2ON2H4+2H2O2=N2↑+4H2ON2H4+4AgBr=N2↑+4Ag↓+4HBrN2H4+2I2=N2↑+4HIN2H4(g)+O2=N2+2H2O 燃烧N2H4+HNO2=2H2O+HN33N2H4=N2↑+4NH3↑Si催化,△CO3++6N2H4=[Co(N2H4)6]3+Pt2++2NH3+N2H4=[Pt(NH3)2(N2H4)6]2+3NH2OH=NH3+N2↑+3H2O4NH2OH=2NH3+N2O↑+3H2O2NO+3H2+H2SO4=(NH2OH)2·H2SO4铂,木炭2NH2OH+2AgBr=2Ag↓+N2↑+2HBr+2H2ONH3OH++HNO2=N2O↑+H3O++H2ONH3OH++2HNO3=3HNO2+H3O+NaNO3+3NaNH2=NaN3+3NaOH+NH3↑熔融2HN3=H2↑+3N2↑△2AgN3=2Ag+3N2↑△2NaN3=2Na+3N2↑300℃NH 4NO 3=N 2O ↑+2H 2O△ 2NO +O 2=2NO 2 NO +NO 2=N 2O 3 低温 N 2O 3=NO +NO 2 △ 2NO 2⇌N 2O 4N 2O 4+H 2O =HNO 3+HNO 2 2NO 2+2OH -=NO 3-+NO 2-+H 2O 2HNO 2=NO ↑+NO 2↑+H 2O △ 2HNO 2+2I -+2H +=2NO ↑+I 2↓+2H 2O 5NO 2-+2MnO 4-+6H +=5NO 3-+2Mn 2++3H 2ONO +NO 2+H 2O =2HNO 2 低温 H ++NO 2-⇌HNO 2HNO 3=H ++NO 3-4HNO 3=4NO 2+2H 2O +O 2 光照 2HNO 3=N 2O 5+H 2O强脱水剂Cu +4HNO 3=Cu(NO 3)2+NO 2↑+2H 2OS +2HNO 3=H 2SO 4+2NO ↑4Zn +10HNO 3(稀)=4Zn(NO 3)2+N 2O ↑+5H 2O 4Zn +10HNO 3(很稀)=4Zn(NO 3)2+NH 4NO 3+3H 2OMnS +2HNO 3(极稀)=Mn(NO 3)2+H 2S ↑ Zn +2HNO 3(极稀)=Zn(NO 3)2+H 2↑ Au +HNO 3+4HCl =HAuCl 4+NO ↑+2H 2O 3Pt +4HNO 3+18HCl =3H 2PtCl 6+4NO ↑+8H 2ONaNO 3=NaNO 3+ 12O 2↑△ 2Pb(NO 3)2=2PbO +4NO 2↑+O 2↑ △ 2AgNO 3=2Ag +2NO 2↑+O 2↑ △ NH 4NO 3=N 2O ↑+2H 2O△Mg(NO 3)2·6H 2O =Mg(OH)NO 3+HNO 3+5H 2O△ 4NH 3+5O 2=4NO +6H 2OPt ,△ 2NO +O 2=2NO 2 3NO 2+H 2O =2HNO 3+NO ↑ NaNO 3+H 2SO 4(浓)=NaHSO 4+HNO 34NH 3+3F 2=NF 3+3NH 4F Cu 2NF 3+2AlCl 3=N 2+3Cl 2+2AlF 3 70℃ 2NF 3+3H 2O(g)=NO +NO 2+6HF火花 2NCl 3=N 2+3Cl 2 90℃ NCl 3+3H 2O =NH 3+3HClO3Br(g)+2P =2PBr 3 4P +3S =P 4S 3 △ P +Al =AlP 650~700℃ 2P +3Zn =Zn 3P 2500~600℃2P +5CuSO 4+8H 2O =5Cu +2H 3PO 4+5H 2SO 4 11P +15CuSO 4+24H 2O =5Cu 3P +6H 3PO 4+15H 2SO 4P 4+3NaOH +3H 2O =PH 3↑+3NaH 2PO 2 Ca 3(PO 4)2(s)+3SiO 2(s)=3CaSiO 3(l)+P 2O 5(g)电炉高温 P 2O 5(g)+5C(s)=2P(g)+5CO(g) 电炉高温PH 4++H 2O =PH 3↑+H 3O + PH 3(g)+HI(g)=PH 4I(s)8CuSO 4+PH 3+4H 2O =H 3PO 4+4H 2SO 4+4Cu 2SO 4 4Cu 2SO 4+PH 3+4H 2O =H 3PO 4+4H 2SO 4+8Cu ↓3Cu 2SO 4+2PH 3=3H 2SO 4+2Cu 3P ↓ Ca 3P 2+6H 2O =Ca(OH)2↓+2PH 3↑PH 4++OH -=PH 3↑+H 2OP 4(g)+6H 2=4PH 3激光 P 4(s)+3OH -+3H 2O =3H 2PO 2-+PH 3↑2P 2H 4+7O 2=2P 2O 5+4H 2O P 4O 6+6H 2O(冷)=4H 3PO 3 5P 4O 6+18H 2O(热)=8P +12H 3PO 4 P 4O 6+6H 2O(热)=PH 3+3H 3PO 42P 4O 6=3P 2O 4+2P(红磷) △ P 4O 10+2H 2O =4HPO 3 4HPO 3+2H 2O =2H 4P 2O 7 P 4O 10+6H 2O =4H 3PO 4 P 4O 10+2H 2SO 4=2SO 3+4HPO 3Fe 3++PO 43-=FePO 4↓ FePO 4+PO 43-=[Fe(PO 4)2]3- PO 43-+H 2O =H PO 42-+OH - PO 43-+3Ag +=Ag 3PO 4↓ PO 3-+Ag +=AgPO 3↓ P 2O 74-+4Ag +=Ag 4P 2O 7↓PO 43-+12MoO 42-+24H ++3NH 4+=(NH 4)3PMo 12O 40·6H 2O ↓+6H 2OPO 43-+Mg 2++NH 4+=MgNH 4PO 4↓ H 3PO 2+I 2+H 2O =H 3PO 3+2HI H 3PO 3+I 2+H 2O =H 3PO 4+2HI HPO 32-+2Ag +=Ag 2HPO 3↓ Ag 2HPO 3+H 2O =H 3PO 4+2AgH 2PO 2-+4Ag ++2H 2O =4Ag ↓+H 3PO 4+3H + H 2PO 2-+Ni 2++H 2O =Ni ↓+HPO 32-+3H +2H 3PO 2=H 3PO 4+PH 3↑2H 2PO 2-+OH -=PO 43-+PH 3↑+H 2O4H3PO3=3H3PO4+PH3↑PX5+4H2O=H3PO4+5HX(X=F、Cl、Br、I)PX5+2H2O=P(OH)2X3+2HX(X=F、Cl、Br、I)P(OH)2X3=POX3+H2O(X=F、Cl、Br、I)PCl3+3H2O=H3PO3+3HClPCl3+3C6H5OH=(C6H5O)3P+3HClPCl5=PCl3+Cl2473KP4S10=P4S7+3S 沸腾3P+5HNO3+2H2O=3H3PO4+5NO↑△3As+5HNO3+2H2O=3H3AsO4+5NO↑△3Sb+5HNO3+8H2O=3H[Sb(OH)6]+5NO↑△Bi+4HNO3=Bi(NO3)3+NO↑+2H2O2As+3H2SO4(浓)=As2O3+3SO2↑+3H2O2Sb+6H2SO4(浓)=Sb2(SO4)3+3SO2↑+6H2O2Bi+6H2SO4(浓)=Bi2(SO4)3+3SO2↑+6H2O2As+6NaOH=2Na3AsO3+3H2↑熔融FeAsS=FeS+As △FeAsS2+Fe=2FeS+As △Sb2S3+3Fe=3FeS+2Sb △Bi2S3+3Fe=3FeS+2Bi △2Sb2S3+9O2=2Sb2O3+6SO2△Sb2O3+3C=2Sb(g)+3CO(g) △Na3As+3H2O=3NaOH+AsH3↑Na3As+3HCl=3NaCl+AsH3↑Mg3Sb2+6HCl=3MgCl2+2SbH3↑Mg3Bi2+6HCl=3MgCl2+2BiH3↑As2O3+6Zn+12HCl=2AsH3↑+6ZnCl2+3H2OSb3++3Zn+3H+=SbH3↑+3Zn2+2SbH3=2Sb+3H2△2AsH 3=2As +3H 2300℃ 2As +5ClO -+6OH -=2AsO 43-+5Cl -+3H 2O 2AsH 3+12AgNO 3+3H 2O =As 2S 3+12HNO 3+12Ag ↓As 2O 3+6NaOH =2Na 3AsO 3+3H 2O As 2O 3+6HCl(浓)=2AsCl 3+3H 2OAs(OH)3=As(OH)2++OH -H 3AsO 3=H ++H 2AsO 3-AsO 33-+I 2+2OH -=AsO 43-+2I -+H 2OSb 2O 3+6HCl(浓)=2SbCl 3+3H 2O Bi 2O 3+6HCl(浓)=2BiCl 3+3H 2O NaH 2AsO 4=NaAsO 3+H 2O△ AsO 43-+12MoO 42-+24H ++3NH 4+=(NH 4)3AsMo 12O 40↓+12H 2O△ AsO 43-+Mg 2++NH 4+=MgNH 4AsO 4↓ 2AsO 43-+6H ++5H 2S =As 2S 5↓+8H 2O H 3AsO 4+2I -+2H +=H 3AsO 3+I 2+H 2OSb 2O 5+10HCl =2SbCl 5+5H 2O SbCl 5+2H 2O =SbO 2Cl ↓+4HCl Bi 3++Cl 2+6OH -=BiO 3-+2Cl -+3H 2O 5BiO 3-+Mn 2++14H +=5Bi 3++2MnO 4-+7H 2OAsCl 3+3H 2O =H 3AsO 3+3HCl SbCl 3+H 2O =SbOCl ↓+2HCl Bi(NO 3)3+H 2O =BiONO 3↓+2HNO 32M +3X 2=2MX 3(M =P 、As 、Sb 、Bi ;X =F 、Cl 、Br 、I )△ M 2O 3+6HCl =2MCl 3+3H 2O (M =P 、As 、Sb 、Bi )As 2S 3+6NaOH =Na 3AsS 3+Na 3AsO 3+3H 2OSb 2S 3+6HCl(浓)=2SbCl 3+3H 2S ↑Sb2S3+6NaOH=Na3SbS3+Na3SbO3+3H2OBi2S3+6HCl(浓)=2BiCl3+3H2S↑4AsS5+24NaOH=5Na3AsS4+12H2O+3Na3AsO4Sb2S5=Sb2S3+2S↓Sb2S3+6HCl=2SbCl3+3H2S↑As2S3+3Na2S=2Na3AsS3Sb2S3+3Na2S=2Na3SbS32Na3AsS3+6HCl=6NaCl+As2S3↓+3H2S↑2(NH4)3SbS4+6HCl=6NH4Cl+Sb2S5↓+3H2S↑2Bi(NO3)3+3H2S=Bi2S3↓+6HNO32Sb(NO3)3+3H2S=Sb2S3↓+6HNO32AsCl3+3H2S=As2S3↓+6HCl 浓HCl 2Na3AsS3+6HCl=6NaCl+3H2S↑+As2S3↓2Na3AsS4+6HCl=6NaCl+3H2S↑+As2S5↓第十五章氧族元素化学方程式(或离子方程式)条件2BaO2=2BaO+O2↑△2NaNO3=2NaNO2+O2↑△2KClO3=2KCl+3O2↑MnO2,△3Fe+2O2=Fe3O4点燃2Mg+O2=2MgO 点燃2H2+O2=2H2O 点燃2H2S+3O2=2SO2+2H2O 点燃2H2S+O2=2S+2H2O 点燃4NH3+3O2=2N2+6H2O 点燃4NH3+5O2=4NO+6H2O Pt催化,点燃2CO+O2=2CO2点燃2Sb2S3+9O2=2Sb2O3+6SO2△3O2=2O3高压放电2I-+O3+2H+=I2↓+H2O+O22HI+2O3=I2↓+H2O+O23SO2+O3=3SO3PbS(黑)+4O3=PbSO4(白)+4O2O3⇌O2+O 紫外线Mg+2H2O(热)=Mg(OH)2+H2↑Mg+H2O(蒸汽)=MgO+H23Fe+4H2O(蒸汽)=Fe3O4+4H2Na2O+H2O=2NaOHSO2+H2O=H2SO3P4S10+16H2O=4H3PO4+10H2S↑H2O2+Ba(OH)2=BaO2(s)+2H2O2I-+2H++H2O2=I2↓+2H2OPbS+4H2O2=PbSO4+4H2O2[Cr(OH)4]-+3H 2O 2+2OH -=2CrO 42-+8H 2OMn(OH)2+H 2O 2=MnO 2+2H 2O2MnO 4-+5H 2O 2+6H +=2Mn 2++5O 2↑+8H 2OCl 2+H 2O 2=2HCl +O 2 H 2O 2+Ag 2O =2Ag ↓+O 2↑+H 2O2H 2O 2=2H 2O +O 2↑Cr 2O 72-+4H 2O 2+2H +=2CrO 5+5H 2O 4CrO 5(蓝色)+12H +=4Cr 3++6H 2O +7O 2↑2NH 4HSO 4=(NH 4)2S 2O 8+H 2↑ 电解 (NH 4)2S 2O 8+2H 2O =2NH 4HSO 4+H 2O 2BaO 2+H 2SO 4=BaSO 4↓+H 2O 2BaCO 3=BaO +CO 2↑ 2BaO +O 2=2BaO 2>500℃Na 2O 2+2NaH 2PO 4=2Na 2HPO 4+H 2O 2 3FeS 2+12C +8O 2=6S +Fe 3O 4+12CO2H 2S +O 2=2S +2H 2O 2H 2S +SO 2=3S +2H 2O催化剂,△ S +O 2=SO 2 点燃 S +3F 2=SF 6 C +2S =CS 2 1973K Hg +S =HgS △ Fe +S =FeS点燃 S +2HNO 3=H 2SO 4+2NO ↑ 3S +6NaOH =2Na 2S +Na 2SO 3+3H 2O△ FeS +2HCl =H 2S ↑+FeCl 2 FeS +H 2SO 4=H 2S ↑+FeSO 4H 2S +I 2=S +2HIH 2S +4Br 2+4H 2O =H 2SO 4+8HBr2Fe 3++H 2S =2Fe 2++S ↓+2H + 2S 2-+O 2+2H 2O =2S ↓+4OH - Na 2S +H 2O =NaOH +NaHS 2CaS +2H 2O =Ca(HS)2+Ca(OH)2↓ Ca(HS)2+2H 2O =2H 2S ↑+Ca(OH)2↓S 2-+S =S 22-S 22-+S =S 32- S x -12-+S =S x 2-(x =2~6) S 22-+2H +=S ↓+H 2S ↑ GeS +Na 2S 2=GeS 2+Na 2S As 2S 3+2Na 2S 2=As 2S 5+2Na 2SAs 2S 3+3S 2-=2AsS 33-SnS 2+S 2-=SnS 32- HgS +S 2-=HgS 22- CO 2+Ca(OH)2=CaCO 3 SnS +Na 2S 2=SnS 2+Na 2S SnS 2+Na 2S =Na 2SnS 3 2Na 2SO 3+O 2=2Na 2SO 4 H 2SO 3+I 2+H 2O =H 2SO 4+2HI H 2SO 3+2H 2S =3S +3H 2O SO 2+2CO =S +2CO 2 铝矾土 4Na 2SO 3=3Na 2SO 4+S ↓+H 2O 2H 2SO 4(浓)+Zn =SO 2↑+ZnSO 4+2H 2O 2H 2SO 4(浓)+Cu =SO 2↑+CuSO 4+2H 2OS +O 2=SO 2 点燃 2H 2S +3O 2=2SO 2+2H 2O点燃4FeS 2+11O 2=8SO 2+2Fe 2O 3 高温 SO 32-+2H +=SO 2↑+H 2O 2H 2SO 4(浓)+S =3SO 2↑+2H 2O 2NaHSO 3=Na 2S 2O 5+H 2O△ SO 2+Cl 2=SO 2Cl 2活性炭 SO 2Cl 2+2H 2O =H 2SO 4+2HCl ↑HCl +SO 3=HSO 3Cl HSO 3Cl +H 2O =H 2SO 4+HCl ↑MgSO 4=MgO +SO 34Ag 2SO 4=8Ag +2SO 3+2SO 2↑+3O 2↑△ 2FeSO 4=Fe 2O 3+SO 3+SO 2↑ △ 2FeO +SO 3=Fe 2O 3+SO 2↑ 2NaHSO 4=Na 2S 2O 7+H 2O 强热 3K 2S 2O 7+Fe 2O 3=Fe 2(SO 4)3+3K 2SO 4 共熔 3K 2S 2O 7+Al 2O 3=Al 2(SO 4)3+3K 2SO 4共熔 S 2O 72-+H 2O =2HSO 4-Na 2SO 3+S =Na 2S 2O 32Na 2S +Na 2CO 3+4SO 2=Na 2S 2O 3+CO 2 S 2O 32-+2H +=SO 2↑+S ↓+H 2O S 2O 32-+4Cl 2+5H 2O =2SO 42-+8Cl -+10H +2S 2O 32-+I 2=S 4O 62-+2I - Ag 2S 2O 3+H 2O =Ag 2S ↓+H 2SO 4 PbS 2O 3+H 2O =PbS ↓+H 2SO 4 Ag 2S 2O 3+2Na 2S 2O 3=Na 4[Ag 2(S 2O 3)3] AgBr +2S 2O 32-=[Ag(S 2O 3)2]3-+Br - Ag ++2S 2O 32-=[Ag(S 2O 3)2]3-[Ag 2(S 2O 3)3]4-+2H +=Ag 2S +SO 42-+2S +2SO 2+H 2O2Mn 2++5S 2O 82-+8H 2O =2MnO 4-+10SO 42-+16H +Ag +,△Cu +K 2S 2O 8=CuSO 4+K 2SO 4 2K 2S 2O 8=2K 2SO 4+2SO 3+O 2↑△ 2NaHSO 4+H 2SO 3+Zn =Na 2S 2O 4+ZnSO 3+2H 2O2Na 2S 2O 4=Na 2SO 3+SO 2+Na 2S 2O 3△ Se +2Cl 2=SeCl 4Se +2H 2SO 4(浓)=2SO 2↑+H 2SeO 3+H 2O△ Te +2Br 2=TeBr 4△ Al 2Se 3+6H 2O =2Al(OH)3↓+3H 2Se ↑ Al 2Te 3+6H 2O =2Al(OH)3↓+3H 2Te ↑ TeO 2+2NaOH =Na 2TeO 3+H 2O H 2SeO 3+2SO 2+H 2O =Se ↓+2H 2SO 4 5H 2SeO 3+2HClO 3=5H 2SeO 4+Cl 2↑+H 2O 3TeO 2+H 2Cr 2O 7+6HNO 3+5H 2O =3H 6TeO 6+2Cr(NO 3)3H 2SeO 4+2HCl =H 2SeO 3+Cl 2↑+H 2O 2Au +6H 2SeO 4=Au 2(SeO 4)3+3H 2SeO 3+3H 2OH 2TeO 4+2HCl =H 2TeO 3+Cl 2↑+H 2O Se +2H 2SO 4=SeO 2+2SO 2↑+2H 2O Cu 2Se +6H 2SO 4=SeO 2+2CuSO 4+4SO 2↑+6H 2O Ag 2Se +4H 2SO 4=SeO 2+Ag 2SO 4+3SO 2↑+4H 2ONa 2TeO 3+H 2SO 4=TeO 2+Na 2SO 4+H 2O第十六章卤素化学方程式(或离子方程式)条件-I-+I2=I32Cr+3Cl2=2CrCl3△Cd+Cl2=CdCl2△2Ag+Cl2=2AgCl △Cl2+H2=2HCl hνBr2+H2=2HBr △I2+H2=2HI △Xe+F2=XeF2△2S+Cl2=S2Cl2△S+Cl2=SCl2△2P+3Cl2=2PCl3PCl3中2F2+2H2O=4HF+O2Cl2+H2O=HCl+HClOCl2+2OH-=Cl-+ClO-+H2O3Cl2+6OH-=5Cl-+ClO3-+3H2O △2NaCl+2H2O=H2↑+Cl2↑+2NaOH 电解MnO2+4HCl(浓)=MnCl2+2H2O+Cl2△2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2+8H2OK2PbF6=K2PbF4+F2△BrF5=BrF5+F2△2KMnO4+2KF+10HF+3H2O2=2K2MnF6+8H2O+3O2SbCl5+5HF=SbF5+5HClK2MnF6+2SbF5=KSbF6+MnF4423KMnF4=MnF3+12F2↑2Br-+Cl2=Br2+2Cl-383K 3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑5HBr +HBrO 3=3Br 2+3H 2OMnO 2+2NaBr +3H 2SO 4=Br 2+MnSO 4+2NaHSO 4+2H 2O 2NaBr +3H 2SO 4(浓)=Br 2+2NaHSO 4+SO 2↑+2H 2O2IO 3-+6HSO 3-=2I -+6SO 42-+6H +5I -+IO 3-+6H +=3I 2+3H 2O 2I -+MnO 2+4H +=2H 2O +I 2↓+Mn 2+2NaI +MnO 2+3H 2SO 4=I 2↓+MnSO 4+2NaHSO 4+2H 2O 8NaI +9H 2SO 4(浓)=4I 2↓+8NaHSO 4+H 2S ↑+2H 2OSiO 2+4HF(aq)=SiF 4↑+2H 2O 4HF(aq)+O 2=2I 2+2H 2O NaCl +H 2SO 4(浓)=NaHSO 4+HCl ↑2NaBr +3H 2SO 4(浓)=SO 2↑+Br 2+2NaHSO 4+2H 2O 8NaI +9H 2SO 4(浓)=H 2S +4I 2↓+8NaHSO 4+4H 2O2HX =H 2+X 2(X =F 、Cl 、Br 、I )△ 2HI ⇌H 2+I 2CaF 2+H 2SO 4(浓)=CaSO 4+2HF ↑ △ NaCl +H 2SO 4(浓)=NaHSO 4+HCl ↑ △ NaBr +H 3PO 4(浓)=NaH 2PO 4+HBr ↑ △ NaI +H 3PO 4(浓)=NaH 2PO 4+HI ↑△ H 2+Cl 2=2HCl点燃 PX 3+3H 2O =H 3PO 3+3HX ↑(X =F 、Cl )2P +3Br 2=2PBr 3 PBr 3+3H 2O =H 3PO 3+3HBr ↑ 2P +3Br 2+6H 2O =2H 3PO 3+6HBr ↑2P +3I 2=2PI 3 PI 3+3H 2O =H 3PO 3+3HI ↑ 2P +3I 2+6H 2O =2H 3PO 3+6HI ↑Zn +2HCl =ZnCl 2+H 2↑CuO +2HCl =CuCl 2+H 2O NaOH +HCl =NaCl +H 2O CaCO 3+2HCl =CaCl 2+H 2O +CO 2↑Sn +2Cl 2=SnCl 4 高温,干燥 2Al +3I 2=2AlI 3 高温,干燥TiO 2+C +2Cl 2=TiCl 4+CO 2 AgNO 3+KCl =KNO 3+AgCl ↓ AgCl +KI =KCl +AgI ↓ Ag ++Cl -=AgCl ↓ PbCl 2+2Cl -=[PbCl 4]2- Hg 2++2I -=HgI 2↓ HgI 2+2I -=[HgI 4]2-F 2+Cl 2=2ClF 250℃ Br 2+Cl 2=2BrClI 2+3F 2=2IF 3 -45℃,CCl 3F 中BrF 5+2Br 2=5BrF △ ClF +F 2=ClF 3 △ ICl +H 2O =HIO +HCl BrF 5+3H 2O =HBrO 3+5HF 2BrF 3=BrF 2++BrF 4-AgF +BrF 3=AgBrF 4=Ag ++BrF 4-SbF 5+BrF 3=BrF 2++SbF 6-KI +I 2=KI 3 CsBr +IBr =CsIBr 2 CsI +Br 2=CsIBr 2 KCl +ICl =KICl 2 KI 3=KI +I 2△CsBrCl 2=CsBr +Cl 2 △ CsBrCl 2=CsCl +BrCl △ 2HClO =2HCl +O 2↑ h ν 3HClO =2HCl +HClO 3↑ △ 2HClO =Cl 2O ↑+H 2O 干燥剂 3BrO -=2Br -+BrO 3-△ 3I 2+6OH -=5I -+IO 3-+3H 2O HClO +HCl =Cl 2↑+H 2O2KI +NaClO +H 2SO 4=NaCl +I 2+K 2SO 4+H 2O NaClO +MnSO 4+2NaOH =MnO 2↓+Na 2SO 4+NaClCl 2O +H 2O =2HClO 2Cl 2+2HgO =HgCl 2·HgO +Cl 2O 2Cl 2+2HgO +H 2O =HgCl 2·HgO +2HClO2Cl 2+H 2O =H ++Cl -+HClO Cl 2+H 2O +CaCO 3=CaCl 2+CO 2+2HClOCl 2+2OH -=ClO -+Cl -+H 2O 8HClO 2=6ClO 2+Cl 2↑+4H 2O 2NaClO 3+SO 2+H 2SO 4=2ClO 2+2NaHSO 4 2ClO 2+2OH -=ClO 2-+ClO 3-+H 2O2ClO 2+Na 2O 2=2NaClO 2+O 2 Ba(ClO 2)2+H 2SO 4=BaSO 4+2HClO 23NaClO 2=2NaClO 3+NaCl 受热或撞击2HClO 3=2HCl +3O 2↑ h ν 4HClO 3=3HClO 4+2HCl△ 8HClO 3(浓)=4HClO 4+2Cl 2↑+3O 2↑+2H 2O△ 4HBrO 3(浓)=2Br 2↑+5O 2↑+2H 2O△ 2KClO 3=2KCl +3O 2↑ MnO 2,△ 4KClO 3=3KClO 4+KCl400℃2Zn(ClO 3)2=2ZnO +2Cl 2+5O 2△ 2HIO 3=I 2O 5+H 2O443K HClO 3+6I -+5H +=3I 2+Cl -+3H 2O2KClO 3+3S =3SO 2↑+2KCl 研磨 3X 2+6OH -=5X -+XO 3-+3H 2O 3I 2+10HNO 3=6HIO 3+10NO ↑+2H 2O KBr +3Cl 2+3H 2O =KBrO 3+6HCl Ba(ClO 3)2+H 2SO 4=BaSO 4↓+2HClO 3 4HClO 4(浓)=2Cl 2↑+7O 2↑+2H 2O 2HClO 4+I 2+4H 2O =2H 5IO 6+Cl 2↑ △ Zn +2HClO 4=Zn(ClO 4)2+H 2↑5H 5IO 6+2Mn 2+=2MnO 4-+5IO 3-+11H ++7H 2OKClO 4+H 2SO 4(浓)=KHSO 4+HClO 4 NaBrO 3+XeF 2+H 2O =NaBrO 4+Xe +2HF NaBrO 3+F 2+2NaOH =NaBrO 4+2NaF +H 2OCl 2+IO 3-+3OH -=H 3IO 62-+2Cl - △ Ba 5(IO 6)2+5H 2SO 4=BaSO 4↓+2H 5IO 6IO 3-+H 2O =IO 4-+H 2↑ 通电 HCOONH 4=HCN +2H 2O P 2O 5 NH 3+CH 4=HCN +3H 2 1200℃,Pt NaNH 2+C =NaCN +H 2↑ 600℃ CaCN 2+Na 2CO 3+C =2NaCN +CaCO 3熔融 CaC 2+N 2=CaCN 2+C 1000℃ (NH 4)2CO =HCNO +NH 3↑ △ 2AgSCN +Br 2=2AgBr +(SCN)22CuSO 4+4KCN =Cu 2(CN)2+(CN)2↑+2K 2SO 4 △ CN -+2OH -+Cl 2=CNO -+Cl -+H 2O2CNO-+4OH-+3Cl2=2CO2+6Cl-+N2+2H2O (CN)2+H2O=HCN+HCNO(CN)2+2OH-=CN-+CNO-+H2O]-+Na+AgCN+NaCN=[Ag(CN)2]-Hg(SCN)2+SCN-=[Hg(SCN)3]-+I-AgI+2CN-=[Ag(CN)2]3-x(x=1~6)Fe3++x SCN-=[Fe(SCN)x第十七章氢和稀有气体化学方程式(或离子方程式)条件H2+2Na=2NaH 高温H2+Ca=CaH2高温CuO+H2=Cu+H2O 高温WO3+3H2=W+3H2O 高温CaO+Mg+H2=CaH2+MgO 高温PdCl2+H2=Pd↓+2HClTiCl4+2H2=Ti+4HCl 高温2LiCl+Mg+H2=2LiH+MgCl2△FeS2+2H2=Fe+2H2S >900℃CO+2H2=CH3OH(g) 温度、压力,催化剂CH4+H2O=CO+3H2高温,催化剂CH4+CO2=2CO+2H2高温,催化剂H2O+CO=H2+CO2500℃,催化剂CaC2+5H2O(g)=CaCO3+CO2+5H2高温(CH3)2Be+LiAlH4=BeH2+LiAlH2(CH3)2乙醚(C4H9)2Be=BeH2+2C4H8△NaH+H2O=H2↑+NaOH2CO2+BaH2=2CO+Ba(OH)2△4LiH+AlCl3=LiAlH4+3LiCl 乙醚2LiH+B2H6=2LiBH4乙醚(CH3O)3B+4NaH=NaBH4+3CH3ONa 250℃Xe+F2=XeF2△Xe+2F2=XeF4△,加压XeF4+Xe=2XeF2400℃Xe+3F2=XeF6△,加压XeF2+H2=Xe+2HF 400℃XeF6+3H2=Xe+6HFXeF 2(aq)+2HCl(aq)+H 2O =NaBrO 4+Xe ↑+2HF XeF 2+H 2O =Xe ↑+ 12O 2↑+2HF3XeF 4+6H 2O =XeO 3+2Xe ↑+12HF + 32O 2↑3XeF 4+6H 2O =2XeO +XeO 4+12HF2XeO =O 2+2Xe XeO 4= 12O 2+XeO 3XeF 6+3H 2O =XeO 3+6HF XeF 6+H 2O =XeOF 4+2HF XeO 3+OH -⇌HXeO 4-HXeO 4-+2OH -=XeO 64-+Xe ↑+O 2↑+2H 2O XeO 3+4NaOH +O 3+6H 2O =Na 4XeO 6·8H 2O +O 22XeF 6+3SiO 2=2XeO 3+3SiF 4↑ BaXeO 6+2H 2SO 4=XeO 4+2BaSO 4+2H 2OCl 2+2OH -=Cl -+ClO -+H 2O 4P +3NaOH +H 2O =Na 2SiO 3+2H 2↑ Be +2NaOH +2H 2O =Na 2[Be(OH)4]+H 2↑第十八章 铜、锌副族元素化学方程式(或离子方程式)条件 2Cu +O 2=2CuO△ 2Cu +O 2+H 2O +CO 2=Cu(OH)2·CuCO 3 2Cu +8NH 3+O 2+2H 2O =2[Cu(NH 3)4]2++4OH - 2Cu +8CN -+2H 2O =2[Cu(CN)4]3-+2OH -+H 2↑2Cu +4HCl +O 2=2CuCl 2+2H 2O 4Ag +4HCl +O 2=4AgCl +2H 2O 2Cu +2H 2SO 4+O 2=2CuSO 4+2H 2O Cu +4HNO 3(浓)=Cu(NO 3)2+2NO 2↑+2H 2O 3Cu +8HNO 3(稀)=3Cu(NO 3)2+2NO ↑+4H 2O Cu +2H 2SO 4(浓)=CuSO 4+SO 2↑+2H 2O △ 5Cu +4H 2SO 4(浓)=Cu 2S ↓+3CuSO 4+4H 2O Ag +2HNO 3(浓)=AgNO 3+NO 2↑+H 2O 3Ag +4H ++NO 3-=3Ag ++NO ↑+2H 2O 2Ag +2H 2SO 4(浓)=Ag 2SO 4+SO 2↑+2H 2O △ Au +HNO 3+4HCl =H[AuCl 4]+NO ↑+2H 2O4CuCl +O 2=2CuO +2CuCl 2 2CuI +3MnO 2=2CuO +Mn 3O 4+I 2△ Cu 2O +BaO 2=2CuO +BaO △ 2CuI +2Hg(g)=Hg 2I 2+2Cu CuBr +Fe 2+=Fe 3++Cu +Br - 2Cu +(aq)=Cu +Cu 2+(aq) Cu 2O +H 2SO 4=CuSO 4+Cu +H 2O2Ag ++Mn 2++4OH -=2Ag ↓+MnO(OH)2↓+H 2O2AgOH =Ag 2O +H 2O △ 2Ag 2O =4Ag +O 2↑△2Ag2X=4Ag+X2↑(X=Cl、Br、I)光照]-+4OH-4Ag+O2+8CN-+2H2O=4[Ag(CN)2]-+4OH-4Au+O2+8CN-+2H2O=4[Au(CN)22Cu+8HCl(热、浓)=2H3[CuCl4]+H2↑CuO+H2SO4=CuSO4+H2OCu(OH)2+H2SO4=CuSO4+2H2O2Cu2++4I-=2CuI↓+I2↓2Cu2++4CN-=(CN)2+2CuCN↓]2-2Cu2++8CN-(过量)=(CN)2+2[Cu(CN)3Cu2++Cu+6Cl-=2[CuCl3]2-△[CuCl3]2-=CuCl↓+2Cl-2CuCl2+SO2+2H2O=2CuCl↓+H2SO4+2HClCu(OH)2=CuO+H2O 微热4CuO=2Cu2O+O2↑>1000℃CuSO4+2NaOH=Cu(OH)2↓+Na2SO4+Cu(OH)2+4NH3·H2O=[Cu(NH3)4](OH)2+4H2O NH4 3Au+=Au3++2Au↓AuCl3+H2O=H[AuCl3(OH)]2CuO+2KO2=2KCuO2+O2↑△AgNO3+2KCl+2F2=KAgF4+KNO3+Cl2△2CuFeS2+O2=Cu2S+2FeS+SO2焙烧2FeS+3O2=2FeO+2SO2高温FeO+SiO2=FeSiO3高温2Cu2S+3O2=2Cu2O+2SO2高温2Cu2O+Cu2S=6Cu+6SO2↑高温]-+4OH-4Au+8CN-+2H2O+O2=4[Au(CN)22[Au(CN)2]-+Zn=[Zn(CN)4]2-+2Au4Ag+8CN-+2H2O+O2=4[Ag(CN)2]-+4OH-2[Ag(CN)2]-+Zn=[Zn(CN)4]2-+2AgAgCl+2CN-=[Ag(CN)2]-+Cl-Ag2S+4NaCN=2Na[Ag(CN)2]+Na2S2Zn+O2=2ZnO △2Cd+O2=2CdO △2Hg+O2=2HgO △Hg+S=HgS 研磨4Zn+2O2+CO2+3H2O=ZnCO3·3Zn(OH)2Zn+2H+=Zn2++H2↑Hg+2H2SO4(热、浓)=HgSO4+SO2↑+2H2OHg+4HNO3=Hg(NO3)2+2NO2↑+2H2O6Hg(过量)+8HNO3(冷)=3Hg2(NO3)2+2NO↑+4H2OHg+4HI=H2[HgI4]+H2↑Zn+2NaOH+2H2O=Na2[Zn(OH)4]+H2↑ZnO+H2SO4=ZnSO4+2H2OM(OH)2=MO+H2O △Hg2++2OH-=HgO↓+H2O2HgO=2Hg+O2↑HgS+O2=Hg+SO2焙烧2ZnS+3O2=2ZnO+2SO2焙烧2HgO+N2H4=2Hg+N2↑+2H2OHg2++Cu=Hg+Cu2+2HgCl2+H2C2O4=Hg2Cl2↓+2HCl+2CO2↑HgCl2+H2O2+2NaOH=Hg↓+O2↑+2NaCl+2H2OZnCl2+H2O=Zn(OH)Cl+HClFeO +2H[ZnCl 2(OH)]=Fe[ZnCl 2(OH)]2+H 2O 2Hg(NO 3)2+H 2O =HgO ·Hg(NO 3)2+2HNO 3HgCl 2+H 2O =Hg(OH)Cl +HCl HgCl 2+2NH 3=Hg(NH 2)Cl ↓+NH 4ClHg 2++2KI =HgI 2↓+2K + HgI 2+2KI =K 2[HgI 4] Hg 2Cl 2=Hg +HgCl 2h ν Hg 22++2OH -=Hg ↓+Hg(OH)2↓Hg(OH)2=HgO +H 2O Hg 2Cl 2+Cl 2=2HgCl 23Hg 2(NO 3)2+8HNO 3(热)=6Hg(NO 3)2+2NO ↑+4H 2O 2Hg 2(NO 3)2+2NH 2OH(冷)=4Hg +N 2O ↑+4HNO 3+H 2OHg 22++Cu =2Hg +Cu 2+ Hg 22++2OH -=Hg ↓+[HgI 4]2- Hg 2CO 3=Hg +HgO +CO 2↑ h ν Hg 2Cl 2+2NH 3=Hg +Hg(NH 2)Cl +NH 4Cl2ZnS +3O 2=2ZnO +2SO 2 焙烧 2CdS +3O 2=2CdO +2SO 2 焙烧 ZnO +C =Zn(g)+CO(g) >1100℃Cd 2++Zn =Cd +Zn 2+第十九章钛、钒副族元素化学方程式(或离子方程式)条件Ti+O2=TiO2高温3Ti+2N2=Ti3N4高温Ti+2Cl2=TiCl4高温2Ti+6HCl(浓)=2TiCl3+3H2↑△Ti+6HF(aq)=[TiF6]2-+2H++2H2↑△TiO2+2H2SO4(浓)=Ti(SO4)2+2H2O △TiO2+H2SO4(浓)=TiOSO4+H2O △Ti4++H2O⇌TiO2++2H+Ti(SO4)2+H2O⇌TiOSO4+H2SO4TiO2+2KHSO4=TiOSO4+K2SO4+H2O 熔融TiO2+MgO=MgTiO3熔融TiO2+BaCO3=BaTiO3+CO2↑熔融FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O △H2TiO3=TiO2+H2O 煅烧TiBr4+4NaOH=Ti(OH)4↓+4NaBrTi(SO4)2+4H2O=Ti(OH)4↓+2H2SO4TiCl4+2H2O=TiO2↓+4HClTiCl4+H2O=TiOCl2↓+2HCl 在盐酸中Ti+2Cl2=TiCl4>300℃TiO2+2Cl2+C=TiCl4+CO2煅烧2TiCl4+Zn=2TiCl3+ZnCl22TiCl4+H2=2TiCl3+2HCl 800℃3TiCl4+Ti=4TiCl3600℃Ti3++Fe3++H2O=TiO2++Fe2++2H+2NH2OH+2Ti2(SO4)3+2H2O=(NH4)2SO4+4TiOSO4+H2SO42FeTiO3+7Cl2+6C=2TiCl4+2FeCl3+6CO 900℃TiCl 4(g)+2Mg(l)=Ti +2MgCl 2(l) △ TiO 2+2CaH 2=Ti +2CaO +2H 2 900℃ ZrOCl 2+(x +1)H 2O =ZrO 2·x H 2O +2HClZr +4KOH =K 4ZrO 4+2H 2↑ 熔融 ZrSiO 4+K 2[SiF 6]+2SiO 2高温 4V +5O 2=2V 2O 5 660℃ V +2Cl 2=VCl 4高温 V +8HNO 3=V(NO 3)4+4NO 2↑+4H 2O 2NH 4VO 3=V 2O 5+2NH 3↑+H 2O >400℃2VOCl 3+3H 2O =V 2O 5↓+6HCl V 2O 5+6NaOH =2Na 3VO 4+3H 2O V 2O 5+H 2SO 4(稀)=(VO 2)2SO 4+H 2O V 2O 5+6HCl(稀)=2VOCl 3+3H 2O V 2O 5+6HCl(稀)=2VOCl 2+Cl 2↑+3H 2OV 2O 5+2H 2=V 2O 3+2H 2O△ 6VSO 4+2KMnO 4+H 2O =2V 2(SO 4)3+V 2O 3↓+2MnO 2↓+2KOHV 2O 3+NH 2OH =2VO 2↓+NH 3↑ 2VO 2+2HNO 3=V 2O 5↓+2NO 2↑+H 2OV 2O 5+2H 2O 2=2HVO 4+H 2O KVO 4+H 2O =KVO 3+H 2O 2 [VO 2(O 2)2]3-+4H +⇌[V(O 2)2]++2H 2O2H 3VO 4+H 2S +4H +=2VO 2++6H 2O +S ↓ 2H 3VO 4+HCOOH +4H +=2VO 2++CO 2↑+6H 2OH 3VO 4+2HI +3HCl =VCl 3+4H 2O +I 2↓ 2VO 2++3Zn +8H +=2V 2++3Zn 2++4H 2O 5V 2++MnO 4-+8H +=5V 3++Mn 2++4H 2O 5V 3++MnO 4-+H 2O =5VO 2++Mn 2++2H +5VO 2++MnO 4-+H 2O =5VO 2++Mn 2++2H +4FeO ·V 2O 3+5O 2=4V 2O 5+2Fe 2O 3 焙烧 2V 2O 5+4NaCl +O 2=4NaVO 3+2Cl 2 焙烧 V 2O 3+Na 2CO 3+O 2=2NaVO 3+2CO 2焙烧 4Nb +5O 2=2Nb 2O 5 高温 4Ta +5O 2=2Ta 2O 5 高温 3NbCl 5+Nb 2O 5=5NbOCl 3 高温 3TaCl 5+Ta 2O 5=5TaOCl 3 高温 Nb 2O 5+3H 2=2NbO +3H 2O 1200℃ Ta 2O 5+3C =2TaO +3CO ↑1100℃ 2NbOCl 3+(x +3)H 2O =Nb 2O 5·x H 2O +6HCl第二十章 铬、锰副族元素化学方程式(或离子方程式)条件 4Cr +3O 2=2Cr 2O 3 加强热 Cr +2HCl =CrCl 2+H 2↑ 4CrCl 2+4HCl +O 2=4CrCl 3+2H 2O 2Cr(OH)2=Cr 2O 3+H 2O +H 2↑ 干燥 Cr 3++3OH -=Cr(OH)3 Cr(OH)3+OH -=[Cr(OH)4]- Cr 2O 3+3H 2SO 4=Cr 2(SO 4)3+3H 2O Cr 2O 3+2NaOH +3H 2O =2Na[Cr(OH)4]Cr(OH)3+3H +=Cr 3++3H 2O CrCl 3·6H 2O =Cr(OH)Cl 2+5H 2O +HCl ↑ △ 2Cr 3++CO 32-+6H 2O =2Cr(OH)3↓+3CO 2↑+3H 2O2Cr 3++3S 2-+6H 2O =2Cr(OH)3↓+3H 2S ↑ 2[Cr(OH)4]-+3H 2O 2+2OH -=2CrO 42-+8H 2O 4Cr 2O 3+16KClO 3=8K 2CrO 4+14ClO 2↑+Cl 2↑ 熔融 Cr 2O 3+2HClO 4=2CrO 3+Cl 2↑+H 2O +2O 2↑ 2Cr 3++3PbO 2+H 2O =3Pb 2++Cr 2O 72-+2H +Cr 3++3NH 3·H 2O =Cr(OH)3+3NH 4+K 2Cr 2O 7+4KCl +3H 2SO 4(浓)=2CrO 2Cl 2↑+3K 2SO 4+3H 2O△ K 2Cr 2O 7+14HCl =2KCl +2CrCl 3+3Cl 2↑+7H 2O△ 4CrO 3=2Cr 2O 3+3O 2↑ △ 2CrO 2Cl 2+3H 2O =H 2Cr 2O 7+4HClPb 2++CrO 42-=PbCrO 4↓2Pb 2++Cr 2O 72-+H 2O =2PbCrO 4↓+2H + 4Fe(CrO 2)2+8Na 2CO 3+7O 2=8Na 2CrO 4+2Fe 2O 3+8CO 2△。
无机化学课件碳族元素

高温
SiO2 + CaO
CaSiO3
高温
SiO2+2C 高温 Si + 2CO↑
SiO2 + CaCO3
CaSiO3 + CO2 ↑
二氧化硅与二氧化碳的比较
二氧化碳CO2 二氧化硅SiO2
物质分类
均属于酸性氧化物
与碱性氧化 物反应
CO2 + CaO=CaCO3
高温 CaO+SiO2 CaSiO3
与碱反应 与水反应
(Cr 3+)
[Cr(OH)3 (s)]
3. 碳酸盐的热稳定性较差,它们的差别可用极化理 论解释(如碱土金属的碳酸盐),金属离子极化力越大,
稳定性越差。稳定性的顺序为:
碳酸盐﹥酸式盐﹥碳酸
碳酸正盐与酸式盐的比较
正盐
酸式盐
水溶 性
热稳 定性
钾钠铵盐易溶于水、其它难溶
K2CO3、Na2CO3受热难分解 CaCO3、(NH4)2CO3受热易分解
通常用二氧化硅和金属氧化物的形式表示。主要用
于建筑材料,实验室常见的有分子筛与沸石(铝硅酸 盐)。见打★的阅读材料。
硅酸钠:Na2SiO3可以写成 Na2O ·SiO2
高岭石:Al2(Si2O5)(OH)4
Al2O3 ·2SiO22H2O
钙长石:CaAl2SiO6
CaO ·Al2O3 ·SiO2
特殊玻璃: 钢化玻璃、光学玻璃、 化学玻璃、有色玻璃、 变色玻璃、电加温玻璃、钾玻璃、 微晶玻璃、 石英玻璃
§13.2
碳族元素包括:
碳族元素----P555-582
碳C、硅Si、锗Ge、锡Sn、铅Pb
碳族元素的价层电子构型:
ⅣA —— ns2np2
本节要求:
无机化学 第14章 碳族元素

与碱性氧化物反应
NiO+SiO2 Na 2SiO3
与HF作用
SiO 2 4HF SiF4 (g) 2H2 O
32
CO2无毒,含量过高时会导致缺氧而窒息。 CO2也不助燃,含量达到2.5%时,火焰会熄灭。 “干冰”可升华,蒸发比较慢,常作制冷剂。 CO2的临界温度为304K,加压被液(258K, 1.545MPa),可装入钢瓶运输。CO2可作为 优良溶剂进行超临界萃取,如从甜橙皮中萃 取柠檬油,从茶叶中萃取咖啡因等。 12
21
由于碳原子无3d轨道,它的配位数已饱和,不 能接受H2O分子配位,因而都不能水解。 CCl4可以用CS2在催化剂的作用下氯化而制得:
CS2 + 3Cl2 CCl4 + S2Cl2
CCl4广泛用做有机物的溶剂,也是常用的 灭火剂。由于它能和钠作用生成NaCl,所以不 能用它扑灭燃烧的金属钠。
CaCO3 + HCl CaCl2 + H2O + CO2
13
碳酸及其盐 CO2能溶于水,但溶解度不大,298K时, 1L水中溶1.45g(约0.033mol)。水溶液中大 部分为CO2•H2O,极小为部分H2CO3。 它是 一种弱酸,仅存在于水溶液中,pH约等于4。 -7 = × H 2 CO 3 H HCO 3 K 1 4.2 10 2-11 = HCO 3 H CO 3 K 2 4.8×10 CO32-的结构: CO32-(6+3×8+2=32e-) 与 BF3(5+3×9=32e-)
2 2Mg 2CO 3 H 2O 2 H 2O 2Cu 2 2CO 3
2
Mg 2 (OH) 2 CO 3 (s) CO 2 (g) Cu 2 (OH) 2 CO 3 (s) CO 2 (g)
无机化学反应式-碳族元素
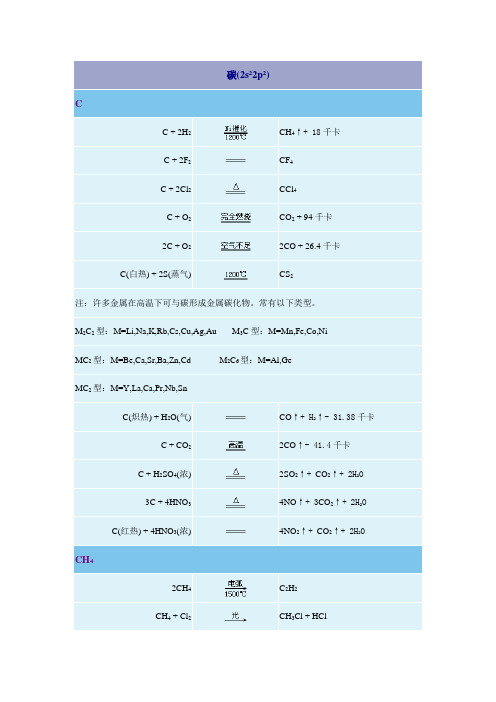
CH4
2CH4 CH4 + Cl2 C 2H 2 CH3Cl + HCl
CH3Cl + Cl2 CH2Cl2 + Cl2 CHCl3 + Cl2 CH4 + 2O2 CH4 + O2 CH4 + O2 2CH4 + O2 CH4 + H2O(气) + 49 千卡 2CH4 + 2NH3 + 3O2 CH4 + CO2 + 59 千卡
3SiO2 + 2MgO + 2MgCl2 3SiO2 + 3CaO·P2O5 3SiO2 + 2Ca3(PO4)2 + 10C 2SiO2 + 3Al2O3 SiO2 + 4NaOH 2SiO2 + 2NaOH SiO2 + 2NaOH SiO2 + 2Ca(OH)2 SiO2 + 6NaF + 4HCl SiO2 + 2CaF2 + 2H2SO4(浓) 3SiO2 + 3CaF2 3SiO2 + 2MgCl2 2SiO2 + 4NaHF2 + 4HF SiO2 + Na2SO4 SiO2 + MgSO4 SiO2 + MgSO4 + CaSO4 SiO2 + CaSO4 2SiO2 + 4KNO3 SiO2 + Na2CO3 SiO2 + CaCO3
取粗硅的反应) SiO2 + 2C SiO2 + 2C 工业上制纯硅的方法: Si(粗) + 3HCl(干燥气) SiHCl3(纯的) + H2 SiHCl3 + H2↑ + Q Si(纯) + 3HCl SiO + CO(所得产物需迅速冷却,否则发 SiO2 + C 生岐化反应) 2SiO(蒸气) SiO + 2NaOH SiO2 + Si 3SiO2 + 4M M2SiO3 + 4M SiO2 + 2Mg Si + 2Mg SiO2 + Mg SiO2 + Mg2O SiO2 + 2M2O SiO2 + Na2O SiO2 + CaO Si + SiO2(歧化反应) Na2SiO3 + H2 2SiO(黄棕色固体) 2M2SiO3 + Si 3M2O + Si 2MgO + Si + 89 千卡 Mg2Si SiO + MgO M2SiO3(M 表示非金属) M4SiO4 Na2SiO3 CaSiO3 Si + 2CO - Q Si + 2CO↑(在电炉内制得粗硅)
碳族元素-碳的单质、碳纳米管(无机化学碳族元素备课笔记)

13.1碳及其化合物1、单质(1)金刚石金刚石(俗称钻石)为原子晶体,每个碳原子均以sp3杂化状态与相邻的四个碳原子结合成键,形成正四面体构型、空间网状结构的原子型晶体。
其熔沸点高,硬度大(所有物质中硬度最大,莫氏硬度为10),难溶于溶剂,不导电,化学性质不活泼。
几乎对所有化学试剂显惰性,但在空气中加热800℃以上燃烧CO2。
(莫氏硬度:又名莫斯硬度,表示矿物硬度的一种标准。
1812年由德国矿物学家莫斯(Frederich Mohs)首先提出。
应用划痕法将棱锥形金刚钻针刻划所试矿物的表面而发生划痕,用测得的划痕的深度分十级来表示硬度:滑石1(硬度最小),石膏2,方解石3,萤石4,磷灰石5,正长石6,石英7,黄玉8,刚玉9,金刚石10,硬度值并非绝对硬度值,而是按硬度的顺序表示的值。
)金刚石有各种颜色,从无色到黑色都有,以无色的为特佳。
它们可以是透明的,也可以是半透明或不透明。
多数金刚石大多带些黄色。
金刚石的折射率非常高,色散性能也很强,这就是金刚石为什么会反射出五彩缤纷闪光的原因。
金刚石在X射线照射下会发出蓝绿色荧光。
1977年12月21日,在山东省临沭县常林大队,女社员魏振芳发现1颗重158.786克拉的优质巨钻----中国最大的金刚石,全透明,色淡黄,可称金刚石的“中国之最”。
被命名为“常林钻石”.(约鸡蛋黄大小,右图)。
世界上最大的工业用金刚石和宝石级金刚石均产于巴西,都超过3100克拉(1克拉=200毫克)。
现在人造金刚石已经广泛用于生产和生活中,虽然造出大颗粒的金刚石还很困难(所以大颗粒的天然金刚石仍然价值连城),但是已经可以制成了金刚石的薄膜、金刚石小晶体。
常林钻石用途:金刚石是自然界中最坚硬的物质,因此也就具有了许多重要的工业用途,如精细研磨材料、高硬切割工具、各类钻头、拉丝模。
还被作为很多精密仪器的部件。
关于人造金刚石:直接法人造金刚石或利用瞬时静态超高压高温技术,或动态超高压高温技术,或两者的混合技术,使石墨等碳质原料从固态或熔融态直接转变成金刚石,这种方法得到的金刚石是微米尺寸的多晶粉末。
第十四章碳族元素Chapter14Thecarbonfamilyelements14章第十四章碳族元

C60为第一个五边形间互不相邻的碳笼 不存在六边形的最小碳笼为C20
32个面,60个顶点,90条棱 12个正五边形和20个正六边形 F+V=E+2
Fullerene Discoverers Win Chemistry Nobel
The Nobel Prize in chemistry was awarded today to two Americans and one British researcher for their discovery of fullerenes, a new class of all-carbon molecules shaped like hollow balls.
《无机化学》第3版 宋天佑 14_碳族元素

CaCO3 难溶,而 C(a HCO3)2 的溶解度比它大些。
其原因是 CaCO3 中 Ca2+ 和 CO32- 电荷高,是 + 2 对 - 2,相 互间的引力要大些,故不易溶解。
但 Ca2+ 和 HCO3- 之间的引 力相对小些,是 + 2 对 1,较易 于溶解。
14. 1. 2 碳的含氧化合物
碳的氧化物主要有两种: 一氧化碳和二氧化碳。
1. 一氧化碳
CO 为无色无臭有毒气体,在 水中溶解度较小。
实验室中制取 CO 经常采用 两种方法:
① 向热浓硫酸中滴加甲酸
HCOOH —热浓—H—2SO—4 CO↑ + H2O
② 使草酸与浓硫酸共热
H2C2O4(s)—热浓—H—2SO—4 CO ↑+ CO2 ↑+ H2O
通入水蒸气时,发生另一反应
C + H2O —— CO + H2 △rHm = 131 kJ•mol-1
得到的气体体积组成为 CO 40%, CO2 5%,H2 50%。
这种混合气体称为水煤气。
发生炉煤气和水煤气都是工业 上的燃料气。
CO 为还原性气体,是冶金工 业的还原剂,可以将金属氧化物矿 物还原成金属。
CaCO3 —— Ca2+ + CO32Ca(HCO3)2 —— Ca2+ + 2HCO3-
所以通入 CO2 ,可以将 CaCO3 转化成Ca(HCO3)2 而发生溶解:
CaCO3 + CO2 + H2O —— Ca(HCO3)2
Na2CO3,K2CO3 和(NH4)2CO3 等均易溶于水。
碳族元素及其化合物

碳族元素及其化合物
碳族元素及其化合物
从表中有关数据可知,碳族元素从上至下金属性增强,碳 和硅是非金属元素,锗、锡和铅是金属元素。它们单质的化学 性质都不太活泼,从碳至铅活泼性略有增强。
碳处于第二周期,半径小,电负性较大,与同族其他元素 相比表现出许多特殊性。碳和硅的同种原子间可形成键,并能 与氢形成一系列碳氢化合物和硅氢化合物,这是它们的重要特 征。硅和锗是重要的半导体元素。碳、硅、锗、锡、铅及其化 合物在材料领域有广泛应用。
碳族元素及其化合物
二、 碳及其重要化合物 1. 碳的同素异形体
碳可形成立方系金刚石结构的 原子晶体、六方系的石墨和富勒烯 C60等三种同素异形体。它们的结 构模型如图8-3所示。
碳族元素及其化合物
图8-3 金刚石、石墨和富勒烯的结构
碳族元素及其化合物
金刚石是具有立方对称结构的原子晶体,而石墨是六方层状结构。 在石墨晶体中,同层C—C键键长为142 pm,层与层之间以范德华力 结合,C原子之间相距335 pm。
碳族元素及其化合物
3. 碳酸及其盐
二氧化碳溶于水可得到碳酸,但在水溶液中大部分CO2与 H2O分子形成不太紧密的水合物,只有一小部分生成H2CO3,经 测定在饱和CO2的水溶液中[CO2]/[H2CO3]=600/1。
碳酸为二元弱酸,碳酸盐有正盐(碳酸盐)和酸式盐(碳酸 氢盐)两种类型。碱金属(Li除外)和铵的碳酸盐易溶于水,其 他金属的碳酸盐难溶于水。因此自然界中存在很多碳酸盐矿物, 如大理石CaCO3、菱镁矿MgCO3、菱铁矿FeCO3、白铅矿 PbCO3、孔雀石CuCO3·Cu(OH)2等。对于难溶的碳酸盐来说,相 应的酸式碳酸盐溶解度大。
碳族元素及其化合物
CO2是无色无嗅的气体,加压易液化。在低温下CO2凝为 白色雪花状固体,压紧可成块状,故称干冰,可作致冷剂。 CO2的临界温度为304 K,加压可液化(258 K,1.545 MPa),一般储存在钢瓶中,便于运输和计量。在临界温度 下,CO2可作为优良溶剂进行超临界萃取,选择性地分离各种 有机物,如从茶叶中提取咖啡因。它也是主要的温室效应气体, 其排放量受到《京都议定书》的限制。
(优质)宋天佑《无机化学》PPT课件

(1) 气体 (2) 稀溶液的性质 (3) 晶体结构基本概念 (4) 酸碱理论 (5) 化学反应速率
1. 1 理想气体
1. 1. 1 理想气体的状态方程
符合下面两条假定的气体,叫做 理想气体:
(1) 气体分子的自身体积可以 忽略,分子可看成有质量的几何点。
(2) 分子间的作用力可以 忽略,分子与分子之间、分子与 器壁之间的碰撞,可认为是完全 弹性碰撞 —— 无动能损失。
各种不同物质的稀溶液,其化 学性质各不相同,这是显然的。
但稀溶液的某些共性,与溶质 的种类无关,只与溶液浓度相关。
我们把这类性质称为稀溶液 的依数性。
溶液的饱和蒸气压降低,就 是一种依数性。它与溶质的种类 无关,只与溶液浓度相关。
1. 2. 3 溶液沸点升高 1. 饱和蒸气压图
物质的饱和蒸气压 p,对温度 T 做图,即得到物质的饱和蒸气压图。
下面是水,水溶液体系的饱和蒸 气压图。
p/Pa
1.013 10 5
l1 l2
A A′
l1 水线 l2 水溶液线
在密闭容器中,在纯溶剂的单 位表面上,单位时间里,有 N0 个 溶剂分子蒸发到上方空间中。
上方空间里溶剂分子个数逐渐 增加,密度增加,压力也增加。
随着上方空间里溶剂分子个数 的增加,分子凝聚回到液态的机会 增加。
凝聚回到液态的分子个数 也在增加。
当密度达到一定数值时,凝聚 回来的分子的个数也达到 N0 个。
摩尔分数 x(质)=
x(剂)=
n(质) n(剂)+ n(质)
n(剂) n(剂)+ n(质)
显然有 x(质) + x(剂) = 1
对于稀溶液,n(质)<< n(剂), 故有
无机化学第十五章碳族元素

05
碳族元素的前景展望
新材料和新能源的发展
新材料
碳族元素如硅、锗等在新型材料领域具有广泛的应用前景, 如硅基太阳能电池、锗基半导体材料等。随着科技的发展, 碳族元素有望在新型材料领域发挥更大的作用。
新能源
碳族元素在新能源领域如燃料电池、锂电池等也有着重要的 应用,其性能和安全性不断提高,有助于推动新能源产业的 发展。
THANKS
感谢观看
碳族元素在工业中有许多应用,如硅 和锗用于半导体材料,锡用于制造合 金和焊料,铅用于电池和颜料等。
02
碳族元素的通性
碳族元素的原子结构
原子结构相似
碳族元素原子的最外层电子数均 为4,容易形成共价键。
电子构型相同
碳族元素的电子构型为ns²np²,其 中n为能级数。
价电子构型相似
碳族元素的价电子构型为(ns²)(np²), 表现出相似的化学性质。
锗
较少见,主要存在于硫化物矿 中。
锡和铅
存在于地壳中的多种矿石和岩 石中。
碳族元素的主要用途
碳
用于制造各种有机化合物,如塑 料、合成纤维、染料等,也是钢
铁和其他金属的合金元素。
硅
用于制造半导体器件、集成电 路、太阳能电池等,也是建筑 和耐火材料的重要成分。
锗
用于制造电子器件、光纤通信 、红外光学仪器等。
碳族元素在环境保护中的作用
空气净化
碳族元素如硅和锗等可用于空气净化技术,通过吸附和催化作用去除空气中的有害物质,提高空气质 量。
水处理
碳族元素可用于水处理技术,如硅藻土和活性炭等,能够有效去除水中的杂质和有害物质,保障饮用 水安全。同时,碳族元素还可用于土壤修复和废物处理等领域,为环境保护做出贡献。
精编无机化学教学课件 14章 碳族元素

C60的结构
Fullerite
2 碳单质的还原性
碳单质最重要的化学性质是它的还原性。是通过自身被氧化为CO或 CO2将别的物质置换出来,起到还原的作用。大量的研究的到下图:
图中 反应C+O2=CO2 的rS≈0, 反应2C+O2= 2CO的 rS>0, 反应2CO+O2=2CO2 rS <0。 三条直线交于983K。 高于此温度,2C+O2=2CO的反应倾向大, 低于此温度,2CO+O2=2CO2的反应倾向更大。 生成CO的直线向下倾斜,这使得几乎所有金 属的rG−T直线在高温下都能与C-CO直线 相交。能够被碳还原,碳为一种广泛应用的
金刚石的结构
(2)石墨 石墨具有层状结构,层内每个碳原子都以 sp2 杂化轨道与邻近的三 个碳原子形成共价单键,构成六角平面的网状结构,这些网状结构又 连成片状结构。同一层中的每个碳原子均剩余一个未参加杂化的 2p 轨 道,其中有一个未成对电子,同层中碳原子的 2p 轨道相互重叠,形成 一个垂直于平面层的由 Ne 个原子 Ne 个电子形成的大π键。大π键的电 子可以在整个平面层中流动,所以石墨具有层向的良好导电性和导热 性。石墨的层与层之间距离较大,层与层之间的作用力是范德华力, 容易沿着与层平行的方向滑动、裂解,因此石墨质软且具有润滑性。
石墨的结构
(3)碳原子簇 由 N 个碳原子组成的 CN 分子(N < 200),称为碳原子簇,它们的 结构为封闭的多面体的圆球形或椭球形。
C60 是由 60 个碳原子联结的多边形所构成的近似圆球的分子。C60 是一个直径为 1 nm 的空心圆球, 60 个碳原子围成直径为 0.7 nm 的球 形骨架, 球心到每个碳原子的平均距离为 0.35 nm。在球面上有 60 个顶 点,由 60 个碳原子组成 12 个五元环面、20 个六元环面和 90 条棱。
学习_课件14碳族元素_a张
30
2、 C与Si的比较
C
Si
杂化态
sp sp2 sp3
sp3 sp3d2
C.N.max
键离解能
4
6
C-C 345.6 > Si-Si 222
/kJ·mol-1
C-H 411 > Si-H 295
∴ C-C 键距短,烷种类多;
18
工业上CO2 用于制备纯碱、小苏打、碳酸氢铵、 啤酒、饮料、干冰。 在常压下,干冰不经熔化,于 194.5 K 时直接升 华气化,因此常用来做制冷剂和人工造雨。 着火的镁、Na、K在 CO2 气中能继续燃烧,所以 CO2 不助燃也是相对的。
19
3、碳酸及其盐
5s
CO2溶于水,大部分CO2•H2O,极小部分
Na2CO3 CaCO3
PbCO324 ZnCO3
4. 碳化物
根据与碳直接结合的原子的性质的不同,碳化物可以分 成离三子类型碳化物
碳与IA,IIA,IIIA 族金属形成的碳化物,不一定有离 子键
Mg2C3 如4HC2aOC2,2MMgg(O2CH3),2 AHlC4C3C等 C。H3
间充型碳化物
在加2热H2情↑ 况下,硅也能跟一些非金属反应。高温下化学性质活泼。
2Mg + Si = Mg2Si
SiC 2000CC Si 3 N 4 1000CN2
Si
400C Cl2 SiCl 600C O3 SiO
4 2
硅与氢氟酸反应:Si + 4HF = SiF4 + 2H2 SiF4 + 2HF =
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
SnO2:难溶水的白色固体,两性偏酸.
SnO2+2NaOH(熔融)=Na2SnO3+H2O PbO(密陀僧):黄色、难溶于水,两性偏碱。溶HAc 和HNO3→Pb2+ PbO2:暗棕色,难溶于水,两性偏酸.强氧化性。 * PbO2+4HCl(浓)=PbCl2→+Cl2↑+2H2O
Pb的 氧化物
* 2PbO2+2H2SO4(浓)=2PbSO4→+O2↑+2H2O
2012-10-27 7
fH fG
m m
0 0
碳 纳 米 管
2012-10-27 8
在硅晶片表面或晶片被侵蚀的洞中垂直生长的纳米管。每一个茎状的结构都由 成千上万个纳米管构成。阵列下面的黑色影斑是催化剂。看上去枯萎了的阵列 是因为它们生长后被浸过液体,当浸体蒸发后,纳米管便枯萎了。
2012-10-27 16
三、氧化物
HCOOH H 2C2O4
浓 H2S O4 △ 浓 H2S O4 △
1.CO和CO2
C O ↑ + H 2O C O2↑ ( N a OH 吸 收 ) + CO ↑ + H2O
发生炉煤气(C+空气→CO+N2)
水煤气 C+H2O →CO+H2
工 业 : Ca CO3( 石 灰 石 ) 实 验 室 : C a C O 3+ 2 H C I
2012-10-27 9
下图:分子内力(Intramolecular forces)使直径5-10 nm 的碳纳米 管彼此粘在一起,随着纳米管的 飞速生长,他们便会拉着邻居一 起长。 如果生长环境不理想,催 化剂过多或过少,这种粘着力就 使纳米管阵列长成出棱角、花饰、 线条和其它结构 上图:纳米管在预先做 好阵列的硅晶片上催化 生长的结果。把Si晶片 置于一个充满乙烯容器 内,在特定的晶面上涂上 催化剂,加热后,高纯 的碳管以惊人的速度生 长,其速度可以达到每 小时500英里。
Pb3O4+4HI=2PbI2+PbO2+2H2O
Pb3O4+8HI=3PbI2+I2+4H2O
2012-10-27 22
四、含氧酸及其盐
1.碳酸和碳酸盐
碳酸(H2CO3 ) 二元弱酸 碳酸盐 ⑴ 水溶性 S(难溶正盐)<S(相应酸式盐)
S(CaCO3)< S[Ca(HCO3)2]
* S(易溶正盐)>S(相应酸式盐) S(Na2CO3)>S(NaHCO3)
煅烧
C O2↑ + Ca O
C O 2↑ + C a C I 2+ H 2O
2 * 2 2 2 2
∶C
O ∶
CO : [ KK ( 2 s ) ( 2 s ) ( 2 p y ) ( 2 p z ) ( 2 p x ) ]
〃 〃 ∶O 〃
〃 C 〃
〃 O ∶ 〃 〃
2012-10-27 17
正盐:铵及碱金属盐易溶,
Li2CO3溶解度很小。其余难溶。 酸式盐易溶。 易溶盐:
100℃溶解度
Na2CO3 45
NaHCO3 16
K2CO3 156
KHCO3 60
(g/100gH2O)
2012-10-27 23
溶解度的反常是由于HCO3-离子通过氢键 形成双聚或多聚链状离子的结果。
2-
OH O C O
2012-10-27 15
Pb: 质软、密度大(11.35g· -3),纯铅在空气中不稳定 cm
→Pb(OH)2或Pb2(OH)2CO3 化工厂或实验室可用铅做耐酸反应器的衬里和储存、 输送酸液的管道设备( PbCl2、PbSO4等难溶)。不能输送 饮用水(有毒)。可输送硬水[难溶保护膜PbSO4,Pb2(OH) 2CO3] 。 Pb易溶于稀HNO3、浓硫酸[Pb(HSO4)2]和浓盐酸 [H2PbCl4]。冷浓HNO3中钝化. 注意:日常生活中,接触铅的机会很多。铅是使用以蓄电池 为主,包括铅包电线、铅管板、自来水管道、软焊条、颜 料、涂料、化学试剂、药品以至化妆品等。由此引起的铅 污染不容忽视。
3.金刚石的人工合成
欲使反应正向进行,采取的措施?⑵ 固相转化说:石墨的 ----高温、高压、催化剂。
碳原子间的键不发生断 裂,而是在催化剂的作 用下,按一定方向位移 直接转化为金刚石结构。
2012-10-27 14
4.硅、锗、锡、铅单质
Si:原子晶体,灰黑色,硬、脆,能刻划玻璃。低温下稳定, 只与强氧化剂和强碱作用,高温时可与许多物质反应。 高纯硅可作半导体材料。 * Si+2OH- +H2O=SiO32-+2H2↑ Ge:原子晶体,比Si活泼,能溶于氧化性酸得到Ge(Ⅳ), 难溶于NaOH,不与空气中的O2、H2O,非氧化性酸作用。高 纯锗也是较好的半导体材料。 Sn:灰锡(α)←→白锡(β)←→脆锡(γ) 白锡:有延展性金属,<286K逐步转化为粉末状灰锡而自行 毁坏(锡疫).马口铁为镀锡薄铁. Sn+2HCl(热、浓)=SnCl2+H2↑ 3Sn+8HNO3(冷、稀)=3Sn(NO3)2+2NO↑+4H2O Sn+4HNO3(浓)=H2SnO3(SnO2·2O)→+4NO2↑+H2O H Sn+2OH-+2H2O= Sn(OH)42-+H2↑
-200
-1
2C+O2 → 2CO (c) C + O 2→ C O 2
△ rG m / K J 〃 m o L
-400
Y
-600
2 M n + O 2→ 2 M n O ( d )
°
-800
A I 2O 3
b.p
2 M g + O 2→ 2 M g O 2 C a + O 2→ 2 C a O
-1000
* 5PbO2+2Mn2++4H+=2MnO4-+5Pb2++2H2O PbO2+2NaOH=Na2PbO3+H2O
2012-10-27 21
Pb3O4 :(铅丹、红铅),红色粉末.做红 色颜料,油漆船舶和桥梁钢架. * Pb3O4+4HNO3=2Pb(NO3)2+PbO2→+2H2O Pb3O4+8HCl=3PbCl2+Cl2+4H2O
C 碱金属碳酸盐>碱土金属碳酸盐>过渡金属碳酸 盐
Na2CO3
难
CaCO3
1170K
CuCO3
473K
2012-10-27 25
(3)水解性
金属离子(碱金属除外)
N a2C O3
碳 酸 盐 → (或 氢 氧 化 物 → 或 碱 式 碳 酸 盐 )
① 氢氧化物沉淀:S氢氧化物<S碳酸盐
Al3+、Fe3+、Cr3+、Sn2+、Sn4+、Sb3+等(水解性强)
第十四章 碳族元素
§14-1 碳族元素的通性
§14-2
§14-3
碳族元素的单质及其化合物
无机化合物的水解性
2012-10-27 1
元素符号
C
Si
Ge
Sn
5s25p2
Pb
6s26p2
价电层结构 2s22p2 3s23p2 4s24p2 电负性 主氧化数 晶体类型
2.25 1.90 2.01 (Ⅳ)
1.96(Ⅳ) 2.33 (Ⅳ) 1.80(Ⅱ) 1.87 (Ⅱ) +4,+2 (+4)+2
2Fe3++3CO32-+3H2O = 2Fe(OH)3→+3CO2↑ ② 碱式碳酸盐:S氢氧化物≈ S碳酸盐
Mg2+、Pb2+、Cu2+、Bi3+、Zn2+ 、Hg2+ 、Cd2+等
2Cu2++2CO32-+H2O = 2Cu2(OH)2CO3→+CO2↑ ③ 碳酸盐沉淀:S氢氧化物>S碳酸盐 Ca2+、Sr2+、Ba2+、Ni2+、Ag+、Mn2+等(难水解) Ba2++CO32- = BaCO3→
+4(+2) +4(+2) +4,+2
原子晶体
金属晶体
2012-10-27 2
特点:
1.惰性电子对效应:C,Si +Ⅳ氧化态稳定,Pb 是+Ⅱ氧化态稳定。 2.C-C,C-H,C-O键能很高,奠定了有机化合物众 多的基础。 3.Si-Si键能低,所以硅链不会太长,硅化合物 比碳化合物少得多。 Si-O键能高,对应化合物多。
SiO2+2OH-=SiO32-+H2O
SiO2+Na2CO3=Na2SiO3+CO2↑ 光缆:高纯SiO2熔融体中拉出的直径约100μm的细丝(光 导纤维)→光缆
2012-10-27 20
3.Sn、Pb的氧化物
SnO:难溶于水的黑色固体,两性。
Sn的 氧化物
SnO+2HCl=SnCl2+H2O SnO+2NaOH=Na2SnO2+H2O
2.冶金工业中碳的还原反应
-200 2CO+O2→2CO2(a)
-400
C+O2→CO2(b)
2C+O2→2CO(c)
273 983 1273 (T/K) 2273
-600 △Gθ
2012-10-27 12
2 H g + O 2→ H g O
