含有多个手性碳原子的立体异构体中
05立体化学
班级 学 号 姓 名2.( )。
A .(1)和(2)各有一对立体异构体 4.的相互关系是( )。
A .对映异构体 D .不同的化合物5.一对构型式的相互关系是( )。
A .对映异构体 D .不同的化合物6.一对投影式的相互关系是( )。
A .对映异构体 D .不同的化合物7.一对投影式的相互关系是( )。
A .对映异构体 8.下列酒石酸的构型为( )。
A .2R ,3R密封线教研室 主 任 教务处 验收人考 试 时 间总主考班级 学 号 姓 名D .2S ,3R9.内消旋酒石酸与外消旋酒石酸什么性质相同?( ) A .熔点 B .沸点C .在水中溶解度D .比旋光度10.下列四个结构式中,哪一个结构式代表的化合物与其它三个结构式代表的化合物不同?( )A .B .C .D .11.4-羟基-2-溴环己烷羧酸有多少个可能的立体异构体?( ) A .2个 B .4个 C .6个 D .8个 12.有三个手性碳原子,有的时候C-3是伪手性,有的时候是非手性,因此有几个内消旋体?( ) A .3 B .2 C .1 D .013.1,2,3,4,5,6-环己六醇的所有异构体(包括顺反、旋光)共有几种?( ) A .7B .8C .9D .1014.判断左式手性碳的构型,应是( )。
A .,所以是R B .,所以是SC .,所以是R D .,所以是S15.4-羟基-2-溴环己烷羧酸最稳定的立体异构体是( )。
A .B .C .D .16.(R )-(-)-1-氯-2-甲基丁烷自由基氯代反应时,所得产物的分子式为,试预测能有几个馏分?( ) A .3 B .4 C .5 D .617.下列化合物中哪一个能拆分出对映异构体?( )密封线教研室 主 任 教务处 验收人考 试 时 间总主考班级 学 号 姓 名A .B .C .D .18.指出下列各组异构体中,哪组是对映体?( )A .B .C .19.化合物之间的相互关系是( )。
生物化学名词解释

18.盐析:在蛋白质溶液中加入一定量的高浓度中性盐,使蛋白质溶解度降低并沉淀析出的现象。
1加的现象。
20.蛋白质的变性作用:蛋白质分子的天然构象遭到破坏导致其生物活性丧失的现象。
24.层析:按照在移动相(可以是气体或液体)和固定相(可以是液体或固体)之间的分配比例将混合成分分开的技术。
25.单核苷酸:核苷与磷酸缩合生成的磷酸酯。
26.磷酸二酯键:单核苷酸中,核苷的戊糖与磷酸的羟基之间形成的磷酸酯键。
27.不对称比率:不同生物的碱基组成有很大的差异,用不对称比率(A+T)/(G+C)表示。
70.电泳:带电颗粒在电场作用下,向着与其电性相反的电极移动。(也称离子泳)
71.沉降系数:单位离心场强度的沉降速度。
72.糖缀合物:糖类物质与蛋白质或脂质等生物分子形成的共价缀合物。(也称糖复合物,如糖蛋白,蛋白聚糖,糖脂和脂多糖等)
73.相变温度:在某一温度之上膜脂快速运动,由固体转变为流体的温度。
59.非竞争性抑制作用:抑制剂与酶活性中心外的其他位点可逆的结合,使酶的空间结构改变,使酶催化活性降低,不影响酶与底物分子的结合,同时酶与底物的结合也不影响酶与抑制剂的结合。底物与抑制剂之间没有竞争关系,这种抑制作用称为非竞争性抑制作用。
60.皂化值:皂化1g油脂所需的KOH的毫克数。
61.异头物:仅在氧化数最高的碳原子(异头碳)具有不同构型的糖分子的两种异构体。
50.诱导酶:指当细胞中加入特定诱导物后诱导产生的酶。
51.酶原:酶的无活性前体,通常在有限度的蛋白质水解作用后,转变为具有活性的酶。
52.酶的比活力:比活力是指每毫克蛋白质所具有的活力单位数
第十四讲 第六章 立体化学(2)
CH3
CH3NH HO
2H 1H
CH3
H H
2 1
NHCH3 OH
CH3
CH3NH H
2H 1 OH
CH3
H HO
2 1
NHCH3 H
C6H5
C6H5
C6H5
C6H5
第
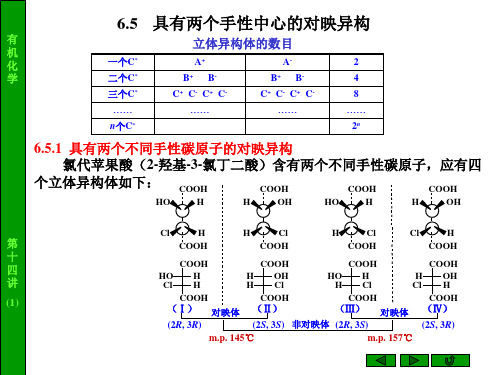
(Ⅰ)(1S, 2R) (Ⅱ)(1R, 2S) (Ⅲ)(1R, 2R) (Ⅳ)(1S, 2S)
十
对映体
对映体
四 讲
麻黄碱,熔点都是34°C,其盐酸 -麻黄碱,熔点都是118°C,其
6.11 不含手性中心化合物的对映异构
有
机 6.11.1 丙二烯型化合物
化
当丙二烯型分子两端碳原子各连接了两个不同的原子或基团时,这样
学 的化合物就可以存在一对对映体。
(1)两个双键相连
a
SP
a
CCC
b SP2
SP2
b
实例:a=苯基,b=萘基,
手性轴(a≠b时)
1935年拆分。
2, 3-戊二烯
H3C
化
HOOC
COOH HOOC
H
学
H COOH
HH
( I) 顺式
H
(II)
COOH HOOC
对映体
(III)
H
(顺反异构体)非对映体
反式
1, 2-环丙烷二甲酸有三种立体异构体,其中(I)中有1个σ,无旋光性,
无对映异构体;(II)与(III)中无σ又无 i ,均有旋光性,是对映异构体,
(II)与(III) 等量混合组成外消旋体。
3号碳有手性
(2S, 4S)
(2R, 4R)
(2R, 3R, 4S)
名词解释 有机化学

学习好资料欢迎下载构造异构:指分子式相同而分子中的原子或原子团相互连接的顺序和方式不同引起的异构顺反异构:指原子或原子团在空间的排布方式不同而产生的异构体对映异构:指两种立体结构之间存在实物与镜像的关系,相互对应而不能重叠的立体异构体手性分子:不能与其镜像重叠的分子手性碳原子:连有四个不同的原子或原子团的碳原子称为手性碳原子加成反应:两个或多个分子互相作用,生成一个加成产物的反应称为加成反应马氏规则:不对称烯烃与卤化氢发生亲电加成反应,HX中的氢原子主要加成到含氢较多的双键碳原子上,而亲电试剂的其余部分则加成到另一个双键碳原子上。
取代反应:是指有机化合物受到某类试剂的进攻,致使分子中一个基(或原子)被这个试剂所取代的反应。
消除反应从分子内消去一个简单分子,形成不饱和烃的反应称为消除反应扎依采夫规则当有不同的消除取向时,形成的烯烃是氢从含氢较少的碳上消除碘仿反应:用I2的NaOH溶液作为反应试剂的卤仿反应称为碘仿反应。
酯化反应:是醇跟羧酸或含氧无机酸生成酯和水的反应酰化反应在有机物分子中的氧、氮、碳、硫等原子上引入酰基的反应称为酰化反应脱羧反应羧酸分子中失去羧基放出二氧化碳的反应叫做脱羧反应康尼查罗反应在浓碱的作用下不含α-H的醛可以发生两分子间的氧化-还原反应,其中一份子醛被氧化为羧酸盐,另一分子醛被还原为醇,称为歧化反应或康你查罗反应醇脂肪烃、脂环烃或芳香烃侧链中碳原子上的氢被羟基取代的化合物酚芳烃环上的氢被羟基取代的化合物醛羰基与一个氢原子和一个烃基相连的化合物酮羰基与两个烃基相连的化合物羧酸分子中含有羧基的有机化合物称为羧酸取代羧酸羟分子中的氢原子被羧基取代的衍生物叫取代羧酸羧酸衍生物指羧酸的羟基被其他基团取代的有机化合物胺氨分子中氢原子被烃基取代而形成的一类化合物。
重氮化合物由烷基与重氮基相连接而生成的有机化合物偶氮化合物偶氮基─N=N─与两个烃基相连接而生成的化合物变旋光现象糖的结晶在水中比旋光度自行转变为定值的现象。
立体化学名词解释

立体化学名词解释手性中心:通常来说,手性中心即为手性碳,但也有个别特殊的比如S\N\P等也可以形成手性中心。
含有手性碳一定有手性中心,含有手性中心不一定有手性碳。
一般来说,碳原子上连接有四个不同的基团,那么这个碳原子成为手性碳原子。
差向异构体:在立体化学中,含有多个手性碳原子的立体异构体中,只有一个手性碳原子的构型不同,其余的构型都相同的非对应异构体叫做差向异构体。
在有机物中,差向异构体的区别通常位于单个非对称碳原子上,一般地,这个碳会被标示出来,如D-葡萄糖的C2异构体D-甘露糖。
若未标示出,通常假定为C2,比如,D-葡萄糖的差向异构体为D-甘露糖。
非对应异构体:分子具有两个或多个手性中心,并且分子间为非镜像的关系的立体异构体。
对应异构体:互为镜像关系的立体异构体,称为对映异构体。
对映异构体都有旋光性,其中一个是左旋的,一个是右旋的。
所以对映异构体又称为旋光异构体。
手性轴:分子的轴上原子不是对称地被取代,而使分子整体产生手性,这种轴称为手性轴。
例如:在某些丙二烯、联苯和螺环化合物中就可能存在手性轴。
含有手性轴的分子,虽无手性中心,但分子整体具有手性,能以一对对映体存在。
构型异构体:构造相同但构型不同的分子成为构型异构体。
构型异构体包括对映异构体和非对映异构体。
拆分剂:利用化学拆分法把外消旋体混合物拆成右旋及左旋光学异构体的过程中所加添的光学活性试剂。
在拆分外消旋的酸时则用旋光性的碱作为拆分剂; 拆分外消旋的碱则可用旋光性酸,拆分外消旋氨基酸则可利用酶(如L-α-氨基酰化酶)作为拆分剂。
互变异构体:两个异构体通过官能团的改变,使两个异构体迅速地相互转化构成处于动态平衡的混合物,称为互变异构。
这两个异构体称为互变异构体。
构象异构体:以单键连接的共价键化合物的分子中,原子或原子团所处空间位置不同而形成的异构体,这类异构体彼此很难分离开来,因为只要分子的原子空间中键轴发生转动,即可互相转变。
外消旋体:又称dL-体,是指互为对映的左旋体和右旋体以等量混合而形成的不具旋光性的混合物或分子复合物。
含两个手性碳原子化合物的对映异构

含两个⼿性碳原⼦化合物的对映异构含两个⼿性碳原⼦化合物的对映异构→含两个相同⼿性碳原⼦化合物的对映异构含两个不相同⼿性碳原⼦化合物的对映异构含两个相同⼿性碳原⼦化合物的对映异构分⼦中含有两个相同⼿性碳原⼦(两个⼿性碳原⼦上连有同样的四个不同的原⼦或原⼦团)的化合物,如酒⽯酸分⼦中的两个⼿性碳原⼦上都连有-OH、-H、-COOH、和CH (OH)COOH。
它的费歇尔投影式如下:(Ⅰ)和(Ⅱ)互为对映体,(Ⅲ)和(Ⅳ)是同⼀种物质。
如果把(Ⅲ)在纸⾯上旋转180°就得到(Ⅳ):这是因为(Ⅲ)的C-2和C-3间有⼀对称⾯,可以把整个分⼦分成两部分,其上下两部分互为实物与镜像关系,就是分⼦内存在互相对映的两部分。
两个⼿性碳原⼦的旋光度⼀样,但旋光⽅向却相反,正好互相抵消⽽失去旋光性。
这种化合物称为“内消旋体”(meso-form),常⽤“m”表⽰,所以⼜称m-酒⽯酸。
酒⽯酸的⽴体异构体实际上只有三种,即左旋体、右旋体和内消旋体。
右旋酒⽯酸和左旋酒⽯酸是互为对映体,它们和内消旋体酒⽯酸是⾮对映体。
等量的右旋体和左旋体混合可组成外消旋体。
内消旋体和外消旋体虽然都没有旋光性,但它们却有本质上的差别。
前者是⼀个化合物,不能拆分成两部分。
⽽后者是⼀种混合物(由等量对映体组成),可以⽤特殊⽅法拆分成两个旋光异构体。
乳酸含有⼀个⼿性碳原⼦,分⼦中⽆对称因素,有旋光性,是⼿性分⼦。
内消旋体酒⽯酸分⼦中虽然含有两个⼿性碳原⼦,却没有旋光性,因分⼦内有对称因素(对称⾯),故不是⼿性分⼦。
由此可见,含有⼀个⼿性碳原⼦的分⼦必定有⼿性。
但是含有两个或更多个⼿性碳原⼦的分⼦却不⼀定有⼿性。
所以,我们决不能说凡是含有⼿性碳原⼦的分⼦就⼀定具有⼿性。
诚然,⼿性碳原⼦是使分⼦具有⼿性的原因,但决定⼀个分⼦是否有⼿性的根本原因是视其有⽆对称因素。
含两个⼿性碳原⼦化合物的对映异构→含两个不相同⼿性碳原⼦化合物的对映异构含两个不相同⼿性碳原⼦化合物的对映异构含两个相同⼿性碳原⼦化合物的对映异构乳酸含有⼀个⼿性碳原⼦,有⼀对对映体。
酶催化的立体选择性反应在手性药物合成中的应用

综述与专论酶催化的立体选择性反应在手性药物合成中的应用王峥,周伟澄(上海医药工业研究院,上海200437)摘要:酶催化的立体选择性反应是当今手性药物合成研究的热点之一,本文按化学反应类型综述了酶催化的水解、酰化、还原、氧化和还原氨化这5种反应在手性药物合成中的应用,重点强调立体选择性。
关键词:酶催化;手性药物;合成;应用;综述中图分类号:R499文献标识码:A文章编号:1001-8255(2006)07-0498-07酶催化的立体选择性反应是当今手性药物合成研究的热点之一,与经典的有机合成相比,酶催化的反应条件温和,立体选择性好,可避免因反应条件苛刻而导致的消旋化、异构化及重排等副反应[1 ]。
三废污染较少,被称为绿色化学。
此外,作为反应催化剂的酶可循环使用。
目前,工业用酶大部分来自微生物,少数来自植物和动物,也可通过基因工程和蛋白质工程等现代生物技术大规模生产,具有广阔的应用前景和商业价值。
本文通过酶催化的化学反应类型综述其在手性药物合成中的应用,重点强调其立体选择性。
1 水解反应水解反应在酶催化手性合成中应用最为广泛,酯、环氧化物等可通过酶的立体选择性水解、分离得到光学纯的单一异构体。
此类反应一般在水中进行,有时也加入有机溶剂以增加底物的溶解度,溶媒的水分子参与反应。
1.1 阿巴卡韦的合成阿巴卡韦(abacavir,1)是由GlaxoSmithKline 公司研发的核苷类抗病毒药物,临床上用于治疗HIV 感染。
1 含有两个手性碳原子,有4 个立体异构体,其中(1S,4R)- 型为药用,有多种合成途径[2]。
用环戊二烯和乙醛酸经Diels-Alder 加成和酰化反应主要得一对对映体(1R,4S,5R)和(1S,4R,5S)-4-endo-4- 丁酰氧基-2- 氧杂双环[3.3.0]辛-7- 烯-3- 酮(4a 和4b),脂肪酶Amano PS 能选择性水解4a 得(1R, 4S,5R)- (-)-4-endo-4- 羟基-2- 氧杂双环[3.3.0]辛-7- 烯-3- 酮( 3 a ) [ 3 ] ,而4b 不被水解。
手性碳原子举例

手性碳原子举例手性碳原子(chiral carbon atom)是指与四个各不相同原子或基团相连的碳原子,用c*表示。
所有含一个手性碳原子的化合物,都有一对对映异构体。
含有两个不相同的手性碳原子的化合物有4个旋光异构体(两对对映异构体)。
判断方法1.手性碳原子一定就是饱和状态碳原子;2.手性碳原子所连接的四个基团要是不同的。
旋光性对大多数有机分子而言,分子的手性主要是由分子中的手性碳原子引起的。
手性分子均具有旋光性,非手性分子均不具有旋光性。
例如,丙酸分子实物与镜像可以完全重叠,分子中存在一个对称平面,没有手性,因此无旋光性;乳酸(2-羟基丙酸)分子实物和镜像不能完全重叠,分子中没有对称面也没有对称中心,具有手性,因此有旋光性。
所以,化合物的手性是产生旋光性的充分和必要条件。
内外消旋体某些化合物分子中存在手性碳原子,但由于分子内存在对称因素,使得分子没有旋光性,如(2r,3s)-酒石酸,此类化合物称为内消旋体。
内消旋体和外消旋体都无旋光性,但外消旋体可拆分为左旋体和右旋体,内消旋体不能拆分。
分类手性碳原子和手性分子的分类。
手性碳原子:把与四个相同原子或基团相连的碳原子称作手性碳原子。
存有不含一个手性碳原子、不含二个手性碳原子、不含三个手性碳原子、不含四个手性碳原子的分子等。
有的分子C99mg手性碳原子。
手性分子的分类:按是否含手性碳原子,可以把手性分子分为具有手性碳原子的手性分子和不具有手性碳原子的手性分子。
但含多个手性碳原子的分子的异构体不一定都是手性分子。
大学有机化学6对映异构

旋光 度
旋光性物质
手性分子
偏振光的振动方向 发生旋转
上页 下页 返回 退出
6.3.1 物质对偏振光的作用
6.3.2 旋光仪工作原理示意图
上页 下页 返回 退出
6.3.3 比旋光度
比旋光度
[ ]
l C
-样品的旋光度
C-溶液的浓度 l- 管长
若被测物质是纯液体,则:
对称面
上页 下页 返回 退出
对称中心:设想分子中有一个点,从分子任何一个原
子出发,向这个点作一直线,再从这个点将直线延长 出去,则在与该点前一线段等距离处,可以遇到一个 同样的原子,这个点就是对称中心。
对称中心
动画 上页 下页 返回 退出
交替对称轴(旋转反映轴):设想分子中有一条直线,
当分子以此直线为轴旋转360/n后,再用一个与此直线 垂直的平面进行反映,如果得到的镜象与原来分子完 全相同,这条直线就是交替对称轴。
动画 上页 下页 返回 退出
R/S标记法:
COOH CH3 OH
优先次序: OH>COOH>CH3>H
命名为:(R)-2-羟基丙酸
HOOC H3 C HO H
优先次序: OH>COOH>CH3>H
命名为:(S)-2-羟基丙酸
上页 下页 返回 退出
在费歇尔投影式上进行R/S标记:
小基 在横 线上
COOH H CH3 OH
上页 下页 返回 退出
6.4 含有一个手性碳原子的化合物的对映异构
CH3C*HOHCOOH(乳酸)
H
*
H
*
HOOC
C CH3 HO
乳酸
有机化学手性碳原子化合物

(3) 对映体 (4)
167℃
167℃
-9.3°
+9.3°
外消旋体 m.p 157℃
结论: 异构体数目—— 2n = 22 = 4非(对映n:体 手性碳原子数目) 对映体数目—— 2n – 1 = 2(2-1)= 2(对)
二. 含两个相同手性碳原子化合物的对映异构
COOH
H
OH
HO
H
COOH
HO
H
末端两苯环不在同平面上。
对映异构
子
内消旋体
3-C—— 非手性碳
3-C——假手性碳
不含手性碳原子化合物的对映异构
即:含手性轴及手性面化合物的对映异构
一、含手性轴的化合物
1. 丙二烯型化合物
手性轴 H
H
CC C
CH3
CH3
中心碳原子两个 键平面正
交, 两端碳原子上四个基团, 两两处于互为垂直的平面上。
H
CCC
CH 3
CH 3
H
H
CCC
CH 3
CH 3
7
C3H 6
4 1 C3H
H
2 3
H
5
7
C3H 1
4
6 C3H
H2 3
H
5
sp sp2
当A≠B ,分子有手性。
A
A' Cl
Cl
CCC
C=C=C (有手性)
B
B' H
H
C H 3
类似物:
C l
无
H
H
H H O O C
有
H C O O H
2. 联苯型化合物
a c
d b
第2章 糖化学(环境生物化学)

-D-Glucopyranose
D-葡萄糖椅式构象的透视式
H CH2OH H HO HO H H HO OH
H H CH2OH H
O
O OH
HO HO H H HO H
-D-吡喃葡萄糖
-D-吡喃葡萄糖
-型的构象比较稳定
•葡萄糖的构型象问题: 链式结构 Fisher式
1
哈迈斯式
1
构象式
OH
• 费歇尔提出单糖的环状 结构:单糖分子中的醛 基和其他碳原子的羟基 能发生环状反应,称为 半缩醛反应,并且以环 状的半缩醛为主。
CH 2
HC HC O
CH CH
HC CH O
CH CH
• 半缩醛羟基:C1上的醛基成环后形成的新的 羟基。 • 半缩醛羟基(或半缩酮)的羟基与决定直链 结构构型(D或L)的碳的羟基处于碳链的同 一边为α 型;反之,在不同边为β 型 • 异头物:只是在羰基碳原子上的构型不同的 同分异构体称为异头物。决定异头现象的碳 原子称为异头碳原子。 α-D-吡喃葡萄糖和β-D-吡喃葡萄糖只是C1上的结构不同。
向左旋转称为左旋性用l或表示构型是人为规定的而旋光为规定的而旋光性是用旋光仪测定时偏振面偏转的实际方向光仪测定时偏振面偏转的实际方向透视形式费希尔形式透视形式费希尔形式cccoohhohhohhd赤藓糖cccoohhohhohhl阿苏糖cccoohhohhohhl赤藓糖cccoohhohhohhd阿苏糖三碳醛糖与酮糖中的不对称碳原子的数目三碳醛糖与酮糖中的不对称碳原子的数目醛糖酮糖醛糖酮糖四碳醛糖与酮糖中的不对称碳原子的数目四碳醛糖与酮糖中的不对称碳原子的数目醛糖酮糖五碳醛糖与酮糖中的不对称碳原子的数目五碳醛糖与酮糖中的不对称碳原子的数目醛糖酮糖醛糖酮糖六碳醛糖与酮糖中的不对称碳原子的数目六碳醛糖与酮糖中的不对称碳原子的数目醛糖酮糖醛糖酮糖醛糖酮糖二
王镜岩版生物化学名词解释

多糖;是由糖苷键结合的糖链,至少要超过10个的单糖组成的聚合糖高分子碳水化合物构型:分子中由于各原子或基团间特有的固定的空间排列方式不同而使它呈现出不同的较定的立体结构构象:由于分子中的某个原子(基团)绕C-C单键自由旋转而形成的不同的暂时性的易变的空间结构形式,不同的构象之间可以相互转变,在各种构象形式中,势能最低、最稳定的构象是优势构象。
旋光率;偏振光通过单位厚度旋光物质后其偏振面旋转的角度。
醛糖:一类单糖,该单糖中氧化数最高的C原子(指定为C-1)是一个醛基,有醇和醛性质。
酮糖:多羟基酮称为酮糖对映体;互为旋光异构体的两种化合物,由于其中一个不对称碳原子的取代基在空间上取向不同而互成物体与镜像的关系,并且两者在空间上不能重叠,它们被称为对映体差象异构体;在立体化学中,含有多个手性碳原子的立体异构体中,只有一个手性碳原子的构型不同,其余的构型都相同的非对映体叫差向异构体。
异头物;是指在羰基碳原子上的构型彼此不同的单糖同分异构体形式。
异头碳;单糖由直链变成环状结构时,羰基碳原子成为新的手性中心,导致C1差向异构化,产生两个非对映异构体。
在环状结构中,半缩醛碳原子称为异头碳原子。
半缩醛;两个含α-H的醛酮分子发生缩合反应,结果生成β-羟基醛酮糖脎,是糖类的苯肼衍生物。
淀粉:D-葡萄糖以α-1,4-糖苷键首尾相连,在支链处为α-1,6-糖苷键的多聚高分子化合物。
糖元;结构与支链淀粉相似,主要是α-D-葡萄糖,按α(1→4)糖苷键缩合失水而成,另有一部分支链通过α(1→6)糖苷键连接纤维素;由D-葡萄糖以β-1,4糖苷键组成的大分子多糖肽聚糖;肽聚糖存在于真细菌中的革兰氏阳性菌和革兰氏阴性菌的细胞壁中。
是由乙酰氨基葡萄糖、乙酰胞壁酸与四到五个氨基酸短肽聚合而成的多层网状大分子结构。
皂化值;皂化1克试样油所需氢氧化钾的毫克数。
碘值;表示有机化合物中不饱和程度的一种指标。
指100g物质中所能吸收碘的克数。
生物化学名词解释

生化考研精解名词第一章糖类(p6)6.构型(configuration):在立体化学中,因分子中存在不对称中心而产生的异构体。
有D 型和L型两种。
构型的改变涉及光学活性的变化。
7.构象(conformation):分子中由于共价单键的旋转所表现出的原子或基团的不同空间排列。
构象的改变不涉及共价键的断裂和重新组成,也无光学活性的变化。
12.差向异构体(epimer):在立体化学中,含有多个手性碳原子的立体异构体中,只有一个手性碳原子的构型不同,其余的构型都相同的非对映体叫差向异构体。
anomeric carbon):单糖由直链变成环状结构时,羰基碳原子成为新的手性中心,导致C1差向异构化,产生两个非对映异构体。
在环状结构中,半缩醛碳原子称为异头碳原子。
15.半缩醛(hemiacetal):醛基和一个醇基缩合形成的产物。
通过该反应,使单糖形成环状结构。
16.变旋(mutarotation):当一种旋光异构体如糖,溶于水中转变成几种不同旋光异构体的平衡混合物时,随着时间而发生的旋光变化。
18.糖苷键(glycosidic bond):一个单糖或糖链还原端半缩醛上的羟基与另一个分子(如醇、糖、嘌呤或嘧啶)的羟基、胺基或巯基之间缩合形成的缩醛键或缩酮键。
常见的糖苷键有O-糖苷键和N-糖苷键。
22.淀粉(starch):由D-葡萄糖单体组成的同聚物。
包括直链淀粉和支链淀粉两种类型,为植物中糖类的主要贮存形式。
23.糖原(glycogen):①一种广泛分布于哺乳类及其他动物肝、肌肉等组织的、多分散性的高度分支的葡聚糖,以α-1,4-糖苷键连接的葡萄糖为主链,并有相当多α-1,6分支的多糖,用于能源贮藏。
②完全由葡萄糖组成的分支长链多糖。
为动物中糖类的主要贮存形式。
25.纤维素(cellulose):①葡萄糖分子通过β-1,4-糖苷键连接而形成的葡聚糖。
通常含数千个葡萄糖单位,是植物细胞壁的主要成分。
②由葡萄糖单元共价连接的长链所组成的结构多糖。
大学有机化学第八章 立体化学

l --- 样品池的长度,单位为dm;
c --- 为样品的浓度,单位为g•ml-1。
8.3
含一个手性碳原子的化合物的对映异构
8.3.1手性碳原子(不对称碳原子)
— 与四个不相同的原子或基团相连
的碳原子为不对称碳或手性碳原子或
手性中心,在结构式中用﹡标出。
8.3.2 含一个手性碳原子的化合物的对映异构 例如乳酸:
COOH C HO H3C H
H
COOH C OH CH3
用透视式书写旋光异构体比较直观,原子或原子团在 空间的排列易观察,但对于结构复杂的分子透视式几
乎无法表示。
(2)、费歇尔(Fischer)投影式表示法 1891年Fischer提出了以他姓氏为名称的投影结构 式书写方法。这种投影式是按照碳的四面体结构, 按规定的原则将分子结构投影到平面上,用所得到 的平面投影式来表示分子的立体结构。
S
a HO
b COOH H c CH3
若最小基团在横键:
a→b→c顺时针-S; (逆时针-R)
R
a HO
b COOH
若最小基团在竖键: a→b→c顺时针-R; (逆时针-S)
CH3 c
H
标记下列旋光异构体的构型:
CH3 Cl H
立体化学
对映异构体 •凡是手性分子,必有互为镜象的构型.分子的手性是 存在对映体的必要和充分条件. • 互为镜象的两种构型的异构体叫做对映体. • 一对对映体的构造相同,只是立体结构不同,这种立 体异构就叫 对映异构 .如乳酸是手性分子,故有对映 体存在:
乳酸的对映体
旋光性和比旋光度 旋光性
• 对映体的一般物理性质(熔点,沸点,相对密度...,以
A B C D
A' B' A' 旋光性物质 D'
A
乳酸
α
目镜(亮)
起偏镜
盛液管
检偏镜
旋光仪(polarimeter)
比旋光度 • 由旋光仪测得的旋光度,甚至旋光方向,不仅与物质 的结构有关,而且与测定的条件(样品浓度,盛放样品 管的长度,偏正光的波长及测定温度等)有关.
(1) 比旋光度--通常把溶液的浓度规定为1g/mL,盛液管 的长度规定为1dm,并把这种条件下测得的旋光度叫比 旋光度.一般用[]表示. • 比旋光度只决定于物质的结构.各种化合物的比旋光 度是它们各自特有的物理常数.
两个横在两边的键—向纸面前方伸出的键. •在纸面上旋转180º —不变;旋转90º 或270º 或翻身—镜象
•
注意:从构型上不能判定物质是否是左右旋;本节
内容只表明左右旋某物质是什么形式的构型(分子中 各原子或基团在空间的排列方式)。
构型的标记 •构造相同,构型不同的异构体在命名时,有必要对它 们的构型给以一定的标记。 • 如乳酸:CH3CHOHCOOH 有两种构型。 • 构型的标记方法有两种: (1)过去常用D—L法 (以甘油醛为对照标准): • 右旋甘油醛的构型定为D型,左旋甘油醛的构型定为 L型。凡通过实验证明其构型与D-相同的化合物,都 叫D型,在命名时标以“D”。而构型与L-甘油醛相同 的,都叫L型,在命名时标以“L”。 • D、L只表示构型,而不表示旋光方向。 • 旋光方向以“+”(右旋)、“-”(左旋)表示。
立体构型的表示法

差向异构体:
含有多个手性碳原子的对映异构体相应的手性碳只有一个构型不 同,其余构型都相同的两种异构体称为差向异构体(表里异构 体); C2构型不同称为C2差向异构体。
几何异构体命名原则
CHO
HgO
H OH CH2OH H
COOH OH CH2OH H
COOH OH CH3
(D)-(+)- 甘油醛
(D)-(-)- 甘油酸
(D)-(-)-乳酸 乳酸
绝对构型( 绝对构型(R,S系)
1951年J.M.Bijvcet通过X射线分析法,这种实 际测定的构型,称为绝对构型(用R,S表 绝对构型( 绝对构型 , 表 示)。
CHO H HO H H OH H OH OH CH2OH HO OH OH CH2OH CHO OH
赤式和苏式
a d d b c c d c b a c d
赤式
苏式
Newman式 式
Newman交叉式
Newman重叠式
手性化合物表示法
旋光性表示法:
d-(右旋)或(+)l-(左旋)或(-)dl-(外消旋)(±)-, meso-(内消旋)
构型表示法:
D-,L-型(相对构型) R,S-型(绝对构型)
相对构型(D系列/L系列)
在1951年以前,人们人为规定右旋甘油醛,具有(Ⅰ) 的构型 ,称为D-(+)-甘油醛。左旋甘油醛具有(Ⅱ) 的构型,称为L-(-)-甘油醛。
CHO H OH CH2OH
CHO OH H CH2OH Nhomakorabea(Ⅰ)( Ⅱ)
D-(+)-甘油醛
《有机化学》徐寿昌第二版第8章立体化学
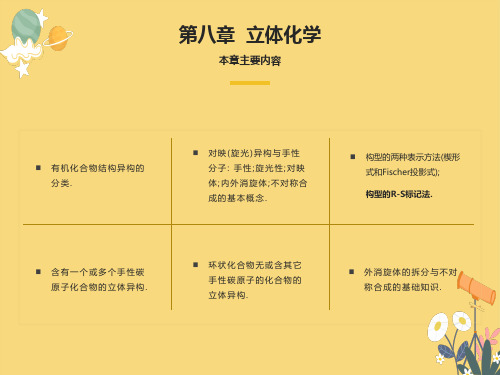
③分子的对称性与手性的关系
考察分子的对称性,要考察的对称因素有以下四种: ——设想分子中有一条直线,当分子以此直线为轴旋转360º/n后,(n=正整数),得到的分子与原来的分子相同,这条直线就是分子的n重对称轴.
有2重对称轴的分子(C2)
(1) 对称轴(旋转轴) -- Cn
旋转180º n=2
在有机化学中,绝大多数非手性分子都具有对称面或对称中心,或者同时还具有4重对称轴.没有对称面或对称中心,只有4重交替对称轴的非手性分子是个别的.
手性分子的一般判断:只要一个分子既没有对称面,又没有对称中心,就可以初步判断它是手性分子.
凡是手性分子,必有互为镜象的构型.分子的手性是存在对映体的必要和充分条件. 互为镜象的两种构型的异构体叫做对映异构体,简称对映体. 一对对映体的构造相同,只是立体结构不同,这种立体异构就叫对映异构.
(2)有机化合物的同分异构现象及分类
立体异构 Stereo-
顺反;Z、E异构(烯烃) 对映异构
isomerism 本章主要讨论立体化学中的对映异构.
同分异构
构造异构
constitution 碳链异构(如:丁烷/异丁烷) 官能团异构(如:乙醚/丁醇) 位置异构(如:1-丁烯/2-丁烯) 构型异构 configuration 构象异构(如:乙烷的交叉式与重叠式) conformation
◆ 由旋光仪测得的旋光度,甚至旋光方向,不仅与物质结构有关,而且与测定的条件(样品浓度,盛放样品管的长度,偏正光的波长及测定温度等)有关.
(1) 比旋光度—在溶液浓度规定为1g/mL,盛液管的长度规定为1dm的条件下测得的旋光度叫比旋光度.一般用[]表示. 比旋光度[]只决定于物质的结构,各种化合物的比旋光度是它们各自特有的物理常数.
有机化学基础知识点整理有机分子的立体异构体的分类和性质

有机化学基础知识点整理有机分子的立体异构体的分类和性质有机化学中,分子的立体异构体是指具有相同分子式但在空间构型上存在差异的化合物。
立体异构体的存在使得有机化合物的结构更加多样化,也对其性质和反应方式产生重要影响。
本文将对有机分子的立体异构体进行分类和性质的整理,帮助读者更好地理解有机化学中的立体异构现象。
一、立体异构体的分类1. 光学异构体光学异构体是指分子中存在手性中心,即具有非对称碳原子的立体异构体。
根据手性中心的数量,光学异构体可以分为单手性体和双手性体。
单手性体:分子中只含有一个手性中心,拥有一个手性异构体。
例如,L-葡萄糖和D-葡萄糖就是分子中只含有一个手性中心的单手性体。
它们的手性中心分别位于第4个碳原子上。
双手性体:分子中含有两个或多个手性中心,拥有多种手性异构体。
例如,甘油(glycerol)就是一个具有两个手性中心的双手性体,它有八种可能的手性异构体。
2. 构象异构体构象异构体是指化学键的旋转或移动并不改变分子中原子的相对位置,只改变分子整体构型的立体异构体。
构象异构体的存在是由于共轭双键的旋转或单键自由旋转,使得分子可以存在多种构象。
例如,正丁烷(n-butane)就存在两种构象异构体:赤/顺丁烷(即完全反式构象,所有碳碳键都直接相对)和反/反丁烷(即完全顺式构象,所有碳碳键都相邻)。
3. 空间异构体空间异构体是指分子在空间结构上存在不同的立体异构体。
它是由于分子中原子或基团的排列顺序不同而导致的。
空间异构体主要包括顺反异构体和E/Z异构体。
顺反异构体:当分子中存在两个相同的基团,它们围绕一个单一的化学键旋转,可以形成两种顺反异构体。
例如,2-溴丁烷可以存在顺-2-溴丁烷和反-2-溴丁烷两种形式。
E/Z异构体:当分子中存在不同的基团,它们围绕一个双键旋转形成两种异构体。
例如,巴比妥酸(barbituric acid)可以存在E-巴比妥酸和Z-巴比妥酸两种形式。
二、立体异构体的性质立体异构体的存在对于有机化合物的性质和反应具有重要影响。
手性碳原子判断方法

手性碳原子判断方法手性碳原子是有四个不同的取代基围绕着碳原子排列而成的立体异构体,也就是说,手性碳原子是一个碳原子上有四个不同的基围绕着它排列而成的四面体。
手性碳原子是有光学活性的,也就是说它们可以使平面偏振光旋转。
在有机化学中,手性碳原子的判断是非常重要的,因为手性碳原子的存在会导致分子的立体异构体,从而影响到分子的化学性质和生物活性。
因此,准确判断手性碳原子是有机化学研究中的一个重要课题。
手性碳原子的判断方法有很多种,下面我们将介绍其中一些常用的方法。
首先,最简单的方法就是通过手性碳原子周围的取代基来判断。
当一个碳原子上的四个取代基都不相同时,这个碳原子就是手性碳原子。
例如,当一个碳原子上的四个取代基分别为A、B、C、D时,如果A不等于B不等于C不等于D,那么这个碳原子就是手性碳原子。
其次,可以通过空间构型来判断手性碳原子。
在有机化合物中,手性碳原子的立体构型可能是R型或S型。
R型和S型是用来描述手性碳原子的立体构型的术语。
通过判断手性碳原子的立体构型,可以确定其是否为手性碳原子。
另外,还可以通过手性碳原子对映体的形成来判断手性碳原子。
手性碳原子对映体是指具有手性碳原子的分子与其镜像分子。
手性碳原子对映体是一对立体异构体,它们具有相同的物理性质,但具有不同的化学性质。
通过手性碳原子对映体的形成,可以判断手性碳原子的存在。
最后,还可以通过光学活性来判断手性碳原子。
手性碳原子具有光学活性,可以使平面偏振光旋转。
通过测量手性碳原子对偏振光的旋转方向和角度,可以判断手性碳原子的存在。
综上所述,手性碳原子的判断方法有很多种,可以通过取代基、空间构型、手性碳原子对映体和光学活性来判断。
在有机化学研究中,准确判断手性碳原子是非常重要的,因为它关系到分子的立体异构体和化学性质。
因此,对手性碳原子的判断方法需要我们进行深入的研究和探讨,以便更好地理解有机化合物的结构和性质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
—— 设想分子中有一条直线 , 当分子以此直线为轴 旋转360º /n后,(n=正整数),得到的分子与原来的分子 相同,这条直线就是n重对称轴.
有2重对镜面) —— 设想分子中有一平面 , 它可以把分子分成互为 镜象的两半,这个平面就是对称面.如:
有对称面的分子 (氯乙烷)
顺反,Z、E异构
8.1 手性和对映体 生活中的对映体 (1)-镜象
沙漠胡杨
生活中的 对映体(2) -镜象
左右手互为镜象
井冈山风景
桂林风情
镜像与手性的概念
左手和右手不能叠合
左右手互为镜像
• 一个物体若与自身镜像不能叠合,叫具有手性.
•在立体化学中,不能与镜像叠合的分子叫手性分子, 而能叠合的叫非手性分子.
(3) 对称中心
——设想分子中有一个点,从分子中任何 一个原子出发 , 向这个点作一直线 , 再从 这个点将直线延长出去,则在与该点前一 线段等距离处,可以遇到一个同样的原子, 这个点就是对称中心.如:2,4-二甲基-环 丁烷-1,3-二羧酸和E-1,2-二氯乙烯
有对称中心的分子
(4) 交替对称轴(旋转反映轴) —— 设想分子中有一条直线 , 当分子以此直线为轴 旋转360º /n后,再用一个与此直线垂直的平面进行反 映(即作出镜像),如果得到的镜像与原来的分子完全 相同,这条直线就是交替对称轴.如:2,3,7,8-四 氯螺[4,4]壬烷
(二) 对映异构体 •凡是手性分子 , 必有互为镜像的构型 . 分子的手性是 存在对映体的必要和充分条件. • 互为镜像的两种构型的异构体叫做对映体. • 一对对映体的构造相同 ,只是立体结构不同 , 这种立 体异构就叫 对映异构 .如乳酸是手性分子 , 故有对映 体存在:
乳酸的对映体
8.2 旋光性和比旋光度 8.2.1 旋光性
• 饱和碳原子具有四面体结构. (sp3杂化) 例: 乳酸(2-羟基丙酸CH3-CHOH-COOH) 的立体结构:
乳酸的分子模型图
两个乳酸模型不能叠合
• 乳酸的两个模型的关系象左手和右手一样,它们
不能相互叠合,但却互为镜像.
(一) 分子的对称性与手性的关系 •考察分子的对称性,要考察的对称因素有以下四种 (1) 对称轴(旋转轴)
l
式中:
--液体的密度(g/cm3).
(3) 比旋光度的表示方法
•通常将测定时的温度和偏正光的波长标出: • 溶剂对比旋光度也有影响,所以也要注明溶剂. 例: 在20℃时,以钠光灯为光源测得葡萄糖水溶液的 比旋光度为右旋52.5°,记为:
t
20 D
52.5(水)
4
(Ⅰ) 旋转90º 后得(Ⅱ), (Ⅱ)作镜象得(Ⅲ), (Ⅲ)等于(Ⅰ)
有4重交替对称轴的分子
• 对称性与手性的关系: A: 非手性分子 ——凡具有对称面、对称中心或交 替对称轴的分子. B: 手性分子——既没有对称面,又没有对称中心,也 没有4重交替对称轴的分子,都不能与其镜像叠合,都 是手性分子. C:对称轴的有无对分子是否具有手性没有决定作用. • 在有机化学中 , 绝大多数非手性分子都具有对称面或 对称中心,或者同时还具有4重对称轴. • 没有对称面或对称中心,只有4重交替对称轴的非手性 分子是个别的. •手性分子的一般判断:只要一个分子既没有对称面,又 没有对称中心,就可以初步判断它是手性分子.
• “ D”代表钠光波长 .因钠光波长 589nm 相当于太
阳光谱中的D线.
8.3 含有一个手性碳原子的化合物的对映异构
•手性碳原子的概念— 在有机化合物中,手性分子大
空间的排列方式)不同的化合物是立体异构体.
• 本章主要讨论立体化学中的对映异构.
同分异构现象
碳链异构(如:丁烷/异丁烷) 构造异构 官能团异构(如:醚/醇) constitutional 位置异构(如:辛醇/仲辛醇)
同分异构 isomerism
立体异构 Stereo-
构型异构 configurational 对映,非对映异构 构象异构 conformational
有机化学 Organic Chemistry
第八章 立体化学
立体化学是有机化学的重要组成部分 . 它的主 要内容是研究有机化合物分子的三度空间结构(立 体结构),及其对化合物的物理性质和化学反应的影
响.
立体异构体——分子的构造(即分子中原子相互联结
的方式和次序 ) 相同 , 只是立体结构 ( 即分子中原子在
•对映体是一对相互对映的手性分子 ,它们都有旋光
性,两者的旋光方向相反,但旋光能力是相同的.
8.2.2 比旋光度 • 由旋光仪测得的旋光度 ,甚至旋光方向 ,不仅与物质 的结构有关 , 而且与测定的条件 ( 样品浓度 , 盛放样品 管的长度,偏正光的波长及测定温度等)有关.
(1) 比旋光度--通常把溶液的浓度规定为1g/mL,盛液管 的长度规定为1dm,并把这种条件下测得的旋光度叫比 旋光度.一般用[]表示. • 比旋光度只决定于物质的结构 .各种化合物的比旋光 度是它们各自特有的物理常数.
• 对映体的一般物理性质(熔点,沸点,相对密度...,以
及光谱)都相同,只有对偏振光的作用不同.
偏正光的形成
偏正光的旋转
旋光性的表示方法: • 旋光性--能旋转偏正光的振动方向的性质叫旋光性 • 旋光性物质(或叫光活性物质)--具有旋光性的物质. • 右旋物质--能使偏正光的振动方向向右旋的物质. 通常用 “d” 或 “+” 表示右旋. • 左旋物质--能使偏正光的振动方向向左旋的物质. 通常用 “ l ” 或 “-” 表示左旋. • 旋光度-- 偏正光振动方向的旋转角度.用“”表 示. •在有机化学中,凡是手性分子都具有旋光性(有些手 性分子旋光度很小);而非手性分子则没有旋光性.
旋光仪(polarimeter)
(2) 比旋光度的测定与换算 用任一浓度的溶液,在任一长度的盛液管中进行 测定 , 然后将实际测得的旋光度 , 按下式换算成比 旋光度[]:
式中: C--溶液浓度 (g/mL); l --管长(dm)
• 若被测得物质是纯液体,则按下式换算:
l C
