有机波谱分析期末复习总结
有机波谱分析复习分析解析

OH CH3
主要产物为
CH3 H OH CH3 -H2O CH3 CH3 重排
过程如下:
-H CH3 CH3
λmax= 217(基本值)+20(环烷基×4) +5(环外双键×1)= 242 (nm) , 与实测值相符 。
3.由某挥发油中分得一种成分,其UV λmax= 268 nm,初步确定该化合物的 结构可能为A或B,请用UV 光谱作出判 断。
组合后,可能的结构式为
H3CO
O C CH2CH3
结构验证:其与不饱和度相符,与标准 谱图对照结构正确。
7.根据1HNMR谱图推断C8H8O2的结 构。
(1)不饱和度U=5,可能含有苯环,还有一个双 键或环; (2)δ=12.9,积分1H,单峰,重水交换峰消失, 推测可能含有-COOH; (3)δ=7~8,积分为4H,裂分为四重峰且峰型 对称,推测可能含有苯环且是对位取代; (4)δ=2.1 积分为3H,单峰,推测为甲基 -CH3; 组合后,可能的结构式为
+
m/z=88
m/z=73
9.
O CH3CH2CNHCH2CH3
170.8
的13C谱峰归属。
42.3 23.3 11.2 23.2
O CH3CH2CNHCH2CH3 23.2 42.3 170.8 23.3 11.2
180
160
140
120
100 PPM
80
60
40
20
0
10.
O
的13C谱峰归属。
43.2 24.5
24.5
HOOC
CH3
8. 核磁共振的条件
(1)自旋量子数I≠0的原子核,都具 有自旋现象,或质量数A或核电荷数 二者其一为奇数的原子核,具有自旋 现象;(2)自旋量子数I=1/2的原子 核是电荷在核表面均匀分布的旋转球 体,核磁共振谱线较窄,最适宜于核 磁共振检测,是NMR研究的主要对 象。
《波谱分析》期末复习资料

《波谱分析》期末复习资料·《波谱分析》期末复习资料⼀、名词解释:1、摩尔吸光系数;根据⽐尔定律,吸光度A与吸光物质的浓度c和吸收池光程长b 的乘积成正⽐。
当c的单位为g/L,b的单位为cm时,则A = abc,⽐例系数a称为吸收系数,单位为L/g.cm;当c的单位为mol/L,b的单位为cm时,则A = εbc,⽐例系数ε称为摩尔吸收系数,单位为L/mol.cm,数值上ε等于a与吸光物质的摩尔质量的乘积。
它的物理意义是:当吸光物质的浓度为1 mol/L,吸收池厚为1cm,以⼀定波长的光通过时,所引起的吸光度值A。
ε值取决于⼊射光的波长和吸光物质的吸光特性,亦受溶剂和温度的影响。
显然,显⾊反应产物的ε值愈⼤,基于该显⾊反应的光度测定法的灵敏度就愈⾼。
2、⾮红外活性振动;物质分⼦吸收红外光发⽣振动和转动能级跃迁,必须满⾜两个条件:1. 红外辐射光量⼦具有的能量等于分⼦振动能级能量差△E2. 分⼦振动时必须伴随偶极矩的变化,具有偶极矩的变化的分⼦振动是红外活性振动,否则是⾮红外活性振动。
3、弛豫;⼈们把向平衡状态恢复的过程称为弛豫过程。
原⼦核从激化的状态回复到平衡排列状态的过程叫弛豫过程。
这个过程遵循指数变化规律,其时间常数称为弛豫时间。
弛豫过程所需的时间叫弛豫时间。
即达到热动平衡所需的时间。
热动平衡即因热量⽽导致的动态平衡。
4、碳谱的γ-效应;5、麦⽒重排是MCLATTERTY对质谱分析中离⼦的重排反应提出的经验规则。
具有不饱和官能团C=X(X为O、S、N、C等)及其γ-H原⼦结构的化合物,γ-H原⼦可以通过六元环空间排列的过渡态,向缺电⼦(C=X+ )的部位转移,发⽣γ-H的断裂,同时伴随C=X 的β键断裂(属于均裂),这种断裂称为McLafferty重排,简称麦⽒重排(麦⽒于1956年发现),例如:2-戊酮在质谱中,位于含有杂原⼦双键的γ-位氢原⼦,通过六员过渡态转移到杂原⼦上的过程称之为麦⽒重排。
(一到四章)有机化合物波谱解析复习指导

第一章紫外光谱一、名词解释1、助色团:有n电子的基团,吸收峰向长波方向移动,强度增强.2、发色团:分子中能吸收紫外或可见光的结构系统.3、红移:吸收峰向长波方向移动,强度增加,增色作用.4、蓝移:吸收峰向短波方向移动,减色作用.5、增色作用:使吸收强度增加的作用.6、减色作用:使吸收强度减低的作用.7、吸收带:跃迁类型相同的吸收峰.二、选择题1、不是助色团的是:DA、-OHB、-ClC、-SHD、 CH3CH2-2、所需电子能量最小的电子跃迁是:DA、σ→σ*B、 n →σ*C、π→π*D、 n →π*3、下列说法正确的是:AA、饱和烃类在远紫外区有吸收B、 UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移4、紫外光谱的峰强用εmax表示,当εmax=5000~10000时,表示峰带:B很强吸收B、强吸收 C、中强吸收 D、弱吸收5、近紫外区的波长为:CA、 4-200nmB、200-300nmC、200-400nmD、300-400nm6、紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:BA、R带B、B带C、K带D、E1带7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了CA、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状8、紫外光谱是带状光谱的原因是由于:DA、紫外光能量大B、波长短C、电子能级差大D、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因9、π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大:AA、水B、乙醇C、甲醇D、正己烷10、下列化合物中,在近紫外区(200~400nm)无吸收的是:AA、 B、 C、 D、11、下列化合物,紫外吸收λmax值最大的是:A(b)A、 B、 C、 D、12、频率(MHz)为4.47×108的辐射,其波长数值为AA、σ→σ*B、π→π*C、n→σ*D、n→π*第二章红外光谱一、名词解释:1、中红外区2、fermi共振3、基频峰4、倍频峰5、合频峰6、振动自由度7、指纹区8、相关峰9、不饱和度10、共轭效应11、诱导效应12、差频二、选择题(只有一个正确答案)1、线性分子的自由度为:AA:3N-5 B: 3N-6 C: 3N+5 D: 3N+62、非线性分子的自由度为:BA:3N-5 B: 3N-6 C: 3N+5 D: 3N+63、下列化合物的νC=C的频率最大的是:( )A B C D答案:CH2CH2CH21651 1657 1678 1680O O1716 1745 1775 1810 OOCH24、下图为某化合物的IR图,其不应含有:DA:苯环 B:甲基 C:-NH2 D:-OH5、下列化合物的νC=C的频率最大的是:A B C D答案:1646 1611 1566 164116506、亚甲二氧基与苯环相连时(1,2亚甲二氧基苯:),其亚甲二氧基的δCH 特征强吸收峰为:AA:925~935cm-1B:800~825cm-1C:955~985cm-1D:1005~1035cm-17、某化合物在3000-2500cm-1有散而宽的峰,其可能为:AA:有机酸 B:醛 C:醇 D:醚8、下列羰基的伸缩振动波数最大的是:C9、中三键的IR区域在:BA ~3300cm-1B 2260~2240cm-1C 2100~2000cm-1D 1475~1300cm-110、偕三甲基(叔丁基)的弯曲振动的双峰的裂距为:DA 10~20 cm-1 B15~30 cm-1 C 20~30cm-1 D 30cm-1以上第三章核磁共振一、名词解释1、化学位移2、磁各向异性效应3、自旋-自旋驰豫和自旋-晶格驰豫4、屏蔽效应5、远程偶合6、自旋裂分7、自旋偶合8、核磁共振CRORACROHBCROFCROClC DC NR9、屏蔽常数10.m+1规律11、杨辉三角12、双共振13、NOE效应14、自旋去偶15、两面角16、磁旋比17、位移试剂二、填空题1、1HNMR化学位移δ值范围约为 0~14 。
有机波谱期末复习.

A、1种B、2种C、3种D、4种
2、下列各组化合物按13C化学位移值从大到小排列的顺序为:C
(sp3<sp<sp2)(苯环<脂酰胺<醛酮)
A、a>b>c>d B、d>c>b>a C、c>d> b > a D、b>c>a>d
3、下述化合物碳谱中的甲基碳的化学位移范围为:A
21、当采用60MHz频率照射时,对羟苯乙羟酸分子中苯环上的四个氢呈现两组峰,分别为6.84和7.88ppm,偶合常数为8 Hz,试问该两组氢核组成何种系统?D
(位移》J用AX(7.88-6.84)*60=62.4>>J)
A、A2B2B、A2X2C、AA`BB`D、AA`XX`
22、在刚性六元环中,相邻两个氢核的偶合常数Jaa值范围为A
A、0-1Hz B、1-3Hz C、6-10Hz D、12-18Hz
16.没有自旋的核为C
A、1H B、2H C、12CD、13C
17、当采用60MHz频率照射时,某被测氢核的共振峰与TMS间的频率差(△ν)为430Hz,问该峰化学位移(δ)是多少ppm?C
A、4.3 B、43 C、7.17 D、6.0
(苯3个吸收带K(>200),B(230-270),E2(200-204))
A、R带B、B带C、K带D、E1带
7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了C
(决定了电子跃迁的类型,决定了吸收峰位置)
A、吸收峰的强度B、吸收峰的数目
C、吸收峰的位置D、吸收峰的形状
8、紫外光谱是带状光谱的原因是由于:D
有机波谱分析要点例题和知识点总结

有机波谱分析要点例题和知识点总结一、有机波谱分析概述有机波谱分析是研究有机化合物结构的重要手段,它主要包括红外光谱(IR)、紫外可见光谱(UVVis)、核磁共振(NMR)和质谱(MS)等技术。
通过对这些波谱数据的解析,可以确定有机化合物的分子结构、官能团种类、化学键的性质等信息。
二、红外光谱(IR)(一)原理红外光谱是基于分子振动和转动能级的跃迁而产生的吸收光谱。
不同的官能团在特定的波数范围内会产生特征吸收峰。
(二)要点1、官能团的特征吸收峰例如,羰基(C=O)在 1700 1750 cm⁻¹有强吸收峰;羟基(OH)在 3200 3600 cm⁻¹有宽而强的吸收峰。
2、影响吸收峰位置的因素包括诱导效应、共轭效应、氢键等。
(三)例题例 1:某化合物的红外光谱在 1720 cm⁻¹有强吸收峰,可能含有什么官能团?答案:羰基(C=O)。
例 2:一个化合物在 3400 cm⁻¹有宽而强的吸收峰,在 1050 1100 cm⁻¹有吸收峰,推测其结构。
答案:可能含有羟基(OH)和醚键(COC)。
三、紫外可见光谱(UVVis)(一)原理基于分子中价电子的跃迁而产生的吸收光谱。
(二)要点1、生色团和助色团生色团如羰基、双键等能在紫外可见区域产生吸收;助色团如羟基、氨基等能增强生色团的吸收。
2、影响吸收波长的因素包括共轭体系的大小、取代基的性质等。
(三)例题例 1:某化合物在 250 nm 处有强吸收,可能的结构是什么?答案:可能含有共轭双键。
例 2:比较两个化合物的紫外吸收波长,一个有苯环,一个有苯环和一个羟基取代。
答案:含羟基取代的化合物吸收波长可能更长。
四、核磁共振(NMR)(一)原理利用原子核在磁场中的自旋能级跃迁产生的吸收信号。
(二)要点1、化学位移不同环境的氢原子或碳原子具有不同的化学位移值,可用于判断官能团的位置。
2、耦合常数相邻氢原子之间的相互作用导致峰的分裂,耦合常数可提供关于分子结构的信息。
有机波谱分析期末复习总结

有机波谱分析期末复习总结名词解析发⾊团(chromophoric groups):分⼦结构中含有π电⼦的基团称为发⾊团,它们能产⽣π→π*和n→π*跃迁从⽽你呢个在紫外可见光范围内吸收。
助⾊团(auxochrome):含有⾮成键n电⼦的杂原⼦饱和基团本⾝不吸收辐射,但当它们与⽣⾊团或饱和烃相连时能使该⽣⾊团的吸收峰向长波长移动并增强其强度的基团,如羟基、胺基和卤素等。
红移(red shift):由于化合物结构发⽣改变,如发⽣共轭作⽤引⼊助⾊团及溶剂改变等,使吸收峰向长波⽅向移动。
蓝移(blue shift):化合物结构改变时,或受溶剂的影响使吸收峰向短波⽅向移动。
增⾊效应(hyperchromic effect):使吸收强度增加的作⽤。
减⾊效应(hypochromic effect):使吸收强度减弱的作⽤。
吸收带:跃迁类型相同的吸收峰。
指纹区(fingerprint region):红外光谱上的低频区通常称指纹区。
当分⼦结构稍有不同时,该区的吸收就有细微的差异,并显⽰出分⼦特征,反映化合物结构上的细微结构差异。
这种情况就像⼈的指纹⼀样,因此称为指纹区。
指纹区对于指认结构类似的化合物很有帮助,⽽且可以作为化合物存在某种基团的旁证。
但该区中各种官能团的特征频率不具有鲜明的特征性。
共轭效应 (conjugated effect) :⼜称离域效应,是指由于共轭π键的形成⽽引起分⼦性质的改变的效应。
诱导效应(Inductive Effects):⼀些极性共价键,随着取代基电负性不同,电⼦云密度发⽣变化,引起键的振动谱带位移,称为诱导效应。
核磁共振:原⼦核的磁共振现象,只有当把原⼦核置于外加磁场中并满⾜⼀定外在条件时才能产⽣。
化学位移:将待测氢核共振峰所在位置与某基准物氢核共振峰所在位置进⾏⽐较,其相对距离称为化学位移。
弛豫:通过⽆辐射的释放能量的途径核由⾼能态向低能态的过程。
分⼦离⼦:有机质谱分析中,化合物分⼦失去⼀个电⼦形成的离⼦。
有机波谱分析总结

有机波谱分析总结有机波谱分析是有机化学中一项重要的分析技术,通过对有机化合物的波谱进行分析,可以确定其结构和功能基团,对于有机合成、药物研发等领域有着广泛的应用。
本文将对有机波谱分析的原理、常见波谱技术和分析方法以及应用进行总结。
一、有机波谱分析原理有机波谱分析主要基于分子中所包含的原子核和电子的转动、振动和电子能级跃迁引起的辐射吸收或发射现象。
通过测量分子在不同频率范围内所吸收或发射的辐射能量,可以得到不同类型的波谱。
有机波谱分析常用的波谱包括红外光谱、质谱、核磁共振谱和紫外可见光谱。
二、常见的有机波谱技术1.红外光谱(IR):红外光谱是根据有机化合物中的官能团和化学键所具有的振动频率的不同来进行分析的。
通过红外光谱可以确定有机化合物中的官能团,如羧酸、醇、醛等。
红外光谱具有非破坏性、操作简便的特点,广泛应用于有机合成、药物研发等领域。
2.质谱(MS):质谱是通过对有机化合物中分子离子和碎片离子质量进行测量来分析有机化合物的分子结构。
质谱具有高灵敏度、高分辨率的特点,可以确定分子的组成和相对分子质量,对于有机化合物的鉴定具有重要意义。
3.核磁共振谱(NMR):核磁共振谱是根据核磁共振现象进行分析的。
通过测量有机化合物中原子核受到外加磁场影响的吸收或发射的辐射能量,可以得到有机化合物中原子核的位置、种类和环境。
核磁共振谱具有高分辨率、非破坏性和无辐射的特点,广泛应用于有机合成、物质鉴定和生物医学研究等领域。
4.紫外可见光谱(UV-Vis):紫外可见光谱是通过测量有机化合物在紫外可见光区域吸收或发射的辐射能量,以确定有机化合物的电子能级和共轭体系的存在与否。
紫外可见光谱具有高灵敏度和快速测量的特点,常用于有机合成、化学动力学和药物研发等领域。
三、有机波谱分析方法1.结构鉴定法:通过与已知化合物的波谱进行对比,确定未知化合物的结构。
结构鉴定法常用于核磁共振谱和质谱。
2.定量分析法:通过测定化合物在特定波长或波数处的吸光度或吸收峰面积,来确定有机化合物的含量。
有机化合物波谱解析复习

有机化合物波谱解析复习有机化合物波谱解析复习名词解释助色团有n电子的基团,吸收峰向长波方向移动,强度增强. 发色团红移吸收峰向长波方向移动增色作用强度增加蓝移吸收峰向短波方向移动,减色作用.强度增加增色作用使吸收强度增加的作用.减色作用使吸收强度减低的作用.吸收带跃迁类型相同的吸收峰.不是助色团的是:A、-OHB、-ClC、-SHD、CH3CH2-答案:D所需电子能量最小的电子跃迁是:A、σ→σ*B、n →σ*C、π→π*D、n →π*答案:D下列说法正确的是:A、饱和烃类在远紫外区有吸收B、UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移答案:D近紫外区的波长为:A、4-200nmB、200-300nmC、200-400nmD、300-400nm答案:C紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:A、R带B、B带C、K带D、E1带答案:B下列化合物中,在近紫外区(200~400nm)无吸收的是:A、B、C、D、答案:A下列化合物,紫外吸收λmax值最大的是:A、B、C、D、x答案:D问答题• 如何用紫外光谱区别顺反异构体 • 如何用紫外光谱区别互变异构体一化合物初步推断其结构不是A 就是B ,经测定UV λmax EtOH=352nm ,试问其结构为何?:• 基值共轭二烯:217 • 同环二烯:1*36 • 环外双键:2*5 • 烷基:6*5答案:293基值共轭二烯:215 共轭双键:30同环二烯:1*39 环外双键:3*5 烷基:a10, b12,r2*18 答案:357第二章 红外光谱 名词解释 费米共振 基频峰 振动自由度 不饱和度 特征区 指纹区 特征峰 相关峰 质量效应 共轭效应 诱导效应 振动偶合效应选择题1、线性分子的自由度为:A :3N-5 B: 3N-6 C: 3N+5 D: 3N+62、非线性分子的自由度为:A :3N-5 B: 3N-6 C: 3N+5 D: 3N+63、某化合物在3000-2500cm -1有散而宽的峰,其可能为:33HOOC 3OA : 有机酸B :醛C :醇D :醚4、下列羰基的伸缩振动波数最大的是:4、 中三键的IR 区域在:A ~3300cm -1B 2300~2200cm -1C 2260~2100cm -1D 1475~1300cm -15、偕三甲基(特丁基)的弯曲振动的双峰的裂距为A 10~20 cm -1B 15~30 cm -1C 20~30cm -1D 30cm -1以上问答题1.用红外光谱法区别下列各对化合物。
有机化合物波谱解析复习总结

(一)常用解谱数据总结关于数据,是一定要记的···大家想怎么记爱怎么记就怎么记吧,建议自己总结,这样记的好一些。
下面是鄙人的,嘻嘻。
(老师PPT上有很多总结的)一、氢谱化学位移值δ(ppm)影响化学位移值的因素:只有空间效应和共轭效应是屏蔽效应增大,向高场位移,即σ↑,δ↓.(一)0.4~4.0为饱和C上的H① 0.4~1.8 连饱和C的饱和C上的H② 1.8~2.5 连不饱和C的饱和C上的HI. 1.8~2.1 连C=C、C≡C的饱和C上的HII. 2.1~2.5 连C=O、N、S、苯环的饱和C上的H③ 3.0~4.6 连-O-的饱和C上的H其中,4.1左右可能有酯基④例外的:2.3~3.0是叁键上的H(二)4.6~8.0为不饱和C上的H① 4.6~6.0 C=C上的H② 6.0~8.0 苯环上的H(三)4.0~5.5为脂肪醇-OH的H若有0.5~1.0,为稀溶液(四)3.5~7.7为酚的-OH的H若有10~16,为分子内氢键(五)9.0~10.0为H-C=0的H(六)10.5~13为-COOH的H(七)胺类①~1.0 脂肪胺②4~5(气泡峰)芳香胺③6~7(气泡峰)酰胺,仲胺类其它:J值:①任何情况下J顺<J反②总体情况:J苯环H<J邻(烯H)<J邻(烷H)<J偕H③苯环H:J对<J间<J邻(J对0 ~1Hz;J间1~3Hz;J邻6~12Hz)④烯烃H:J邻(顺)<J邻(反)(J邻(顺)6~14Hz;J邻(反)11~18Hz)⑤烷烃H:J邻6~8Hz⑥同碳上的H:J偕10~16Hz要求掌握给图能测量算得J值,再推化合物种类。
二、碳谱碳谱的DEPT值:季碳消失!θ=45°,季C消失;θ=90°,季C消失,只有CH向上;θ=135°,季C消失,只有CH2向下。
COM谱:峰全部为单峰。
OFR谱:裂分峰只有同一C上的,临近C不影响裂分。
波谱考点

一、紫外光谱1.郎伯-比耳定理A = log(I0/I1 ) = log(1/T ) = €*c*I2.溶剂极性作用极性增大使π—π*红移,n—π*跃迁蓝移,精细结构消失3.作用:推测化合物分子骨架1)200-800nm 没有吸收,说明分子中不存在共轭结构(-C=C-C=C-,-C=C-C=O,苯环等),可能为饱和化合物。
2)200-250nm有强吸收峰,为发色团的K带,说明分子中存在上述共轭结构单元。
3)250-300nm 有中等强度的吸收峰,为苯环的B带,说明为芳香族化合物。
4)270-350nm有弱吸收峰,为R带,可能为羰基化合物、烯醇等。
5)样品有颜色,说明分子中含较大的共轭体系,或为含N化合物。
二、红外光谱1.分子的振动造成偶极矩的改变产生红外吸收分子的振动的频率与化学键的强度和原子的质量相关红外光谱通过测定分子中化学键的振动频率来确定官能团下面式子中力常数k:与键长、键能有关:键能↑(大),键长↓(短),k↑。
2.红外活性1)必须是能引起分子偶极矩变化的振动才能产生红外吸收光谱2)极性键通常有红外活性3)对称分子中的非极性键通常没有红外活性或吸收很弱3.振动中偶极矩变化越大,吸收强度越大4.特征吸收频率具有同一类型化学键或官能团的不同化合物,其红外吸收频率总是出现在一定的频率范围内,我们把这种能代表某基团,并有较高强度的吸收峰,称为该基团的特征吸收峰(又称官能团吸收峰)。
5.各种官能团的红外吸收位置6.影响红外光谱吸收强度的因素1)极性大的基团,吸收强度大,C=O比C=C强,C=N比C=C强2)使基团极性降低的诱导效应使吸收强度减小,使基团极性增大的诱导效应使吸收强度增加3)共轭效应使π电子离域程度增大,极化程度增大,吸收强度增加4)振动耦合使吸收增大,费米共振使倍频或组频的吸收强度显著增加5)形成氢键使振动吸收峰变强变宽6)能级跃迁的几率,v=0→v=2比v=0→v=1能阶大,但几率小,吸收峰弱诱导效应、共轭效应、中介效应(共振效应)、环的张力、空间障碍、氢键、质量效应7.官能团特征吸收位置1)烷烃特征吸收位置2)烯烃特征吸收位置3)烯烃=C-H的面外弯曲振动——判断双键的取代类型4)炔烃特征吸收位置a)炔键C-H伸缩振动:3340-3300厘米-1,波数高于烯烃和芳香烃,峰形尖锐b)CC叁键伸缩振动:2100厘米-1 ,峰形尖锐,强度中到弱。
有机波谱分析复习纲要(红外、质谱)

有机波谱分析复习纲要第一章 红外和拉曼光谱一.主要光谱信息1.峰的数目:与分子基团有关2.峰的位置:结构定性的主要依据3.峰的形状:宽窄,结构定性的辅助手段4.峰的强度:高低,结构定性的辅助手段,可作为定性的依据二.基本原理1.红外吸收:分子吸收特定频率的红外光,引起辐射光强的改变2.波长(μm)或波数(1/cm)为横坐标,百分透过率(T%)或吸光度(A)为纵坐标记录(A=lg1/T)3.吸收带分类1)很强吸收带(vs,T%<10)2)强吸收带(s,10<T%<40)3)中强吸收带(m,40<T%<90)4)弱吸收带(w,T%>90)5)宽吸收(b)4.红外光区分类5.产生条件:1)辐射光谱能量与振动跃迁所需能量相等2)辐射与物质之间必须有耦合作用在振动过程中,只有偶极矩发生改变的振动 (△μ≠ 0),才是红外活性振动6.振动自由度非线性分子振动自由度为(3n-6)线性分子振动自由度为(3n-5)7.分子的振动方式1)分类(变形振动亦称弯曲振动) 2)频率大小反对称伸缩振动>对称伸缩振动>>弯曲振动面内弯曲振动>面外弯曲振动8.红外光谱谱带1)基频带:基态向第一振动激发态的跃迁2)泛频带(跃迁几率小,强度弱,难检出)a.倍频带:基态向第二、三……振动激发态的跃迁b.和频带:分子吸收光子后同时发生频率为ν和ν'的跃迁,此时产生的跃迁为(ν+ν')的峰c.差频带:吸收峰和发射峰重叠时产生峰(ν-ν')3)振动耦合带:当分子中两个基团共用一个原子时,如果这两个基团的基频振动频率相同或相近,就会发生相互作用,使原来的两个基团的基频振动频率距离加大,形成两个独立的吸收峰4)费米共振带:当强度很弱的的倍频带或组频带与另一强的基频带接近时,发生耦合,相互作用而产生很强的吸收峰或发生裂分,产生费米共振三.影响振动频率的关键因素1.发生震动能级跃迁所需能量大小取决于键两端原子的折合质量(μ)和键力常数(k)(其中k为键力常数,μ为折合质量)1)键力常数:a.键长越短,键级越大,表示键越强,键力常数就越大b.k越大,表示原子振动离开平衡位置很小的距离时,就会受到很大的回复力,所以就相对不容易振动2)折合质量2.电子效应1)诱导效应a.机理:通过使分子中的电子云分布发生变化,引起k的变化,从而影响振动频率b.分类①推电子效应:导致羰基的成键电子云移向氧原子更加偏离几何中心,使羰基的双键性降低,羰基伸缩振动向低频位移动②拉电子效应:使羰基的成键电子云更加接近几何中心,导致羰基的双键性增强,羰基伸缩振动向高频位移动2)共轭效应共轭效应通过π-键电子传递,导致双键的极性增强,双键性降低,伸缩振动频率向低波数位移3)超共轭效应当C-Hσ键和π键(或p轨道)处于平行位置时,会产生离域现象,产生和共轭效应相似的效应3.场效应原子或基团间不是通过化学键,而是它们的静电场通过空间相互作用分子中带部分负电的溴原子和氧原子空间接近,电子云相互排斥,产生相反的诱导极化,使溴原子和氧原子的负电荷相应减小,羰基极性降低,双键性增强,伸缩振动频率增加4.空间效应1)定义:环张力和空间位阻2)环张力影响:随着环的缩小,环内键角缩小,成环σ键的p电子成分增加,键长变长,振动谱带向低波数位移3)空间位阻分子中存在某种或某些基团因空间位阻影响到分子中正常的共轭效应或杂化状态时,导致振动谱带位移5.跨环效应通过空间发生的电子效应(a) (b) (c)(b)中羰基极性增强,双键程度下降羰基频率向低波段移动,(c)中羰基峰消失,出现羟基峰极性基团的伸缩振动频率通常随溶剂极性增加而降低(红外光谱通常在非极性溶剂中测量)四.红外光谱的四大区1.第一峰区(3700~2500)X-H (X=O,N,C)1)O-H伸缩振动a.醇与酚①游离:~3600 中等强(m)②缔合:~3300 宽强 (s,b)(氢键存在向低波数移动)(区别伯仲叔醇:C-O伸缩振动峰位置的差异;区别酚醇:苯基特征吸收峰及高波数的的C-O峰)注意:样品中有水时,出现O-H伸缩及弯曲振动干扰判断b.羧酸①二聚体:~3000 宽散(波数降低,由于共振结构,氢键不断变化)(区别羧酸与醇酚:有羰基峰)2)N-H伸缩振动a.胺类①伯胺:~3500,~3400 尖弱(较低波数处可能出现第三条)②仲胺:~3400③叔胺无吸收b.酰胺类①游离态:~3450②伯酰胺:~3350,~3150③仲酰胺:~3200④叔酰胺无吸收(区别胺与酰胺:)c.铵盐3000~2250 强/中宽,多重 m/s.b.(与羧酸O-H类似,但波数更低)(区别胺与铵盐:铵盐谱带更宽,波数更低;区别铵盐与羧酸:铵盐谱带更宽,波数更低,且羧酸有羰基的特征吸收带) 3)C-H伸缩振动a.炔烃:~3300 尖强(与羰基共轭无影响)(区别炔烃与醇酚胺:比缔合态的O-H吸收弱,N-H吸收强,谱带尖锐)b.烯/芳烃: ~3050 m/w(羧酸,缔合羟基,酰胺等可能掩盖,环丙烷~3060干扰)c.饱和烃基①伯碳:~2960(s),~2870(m)②仲碳:~2926(s),~2850(s)③叔碳:~2890(被伯仲碳掩盖,无实际价值)d.醛基:~2850 m,~2720 we.巯基:~2550 尖2.第二峰区(2500~1900)1)C≡C伸缩振动炔烃:~22002)C≡N伸缩振动氰基:~22503)N≡N伸缩振动重氮基:~2260(s)4)累积双键(X=Y=Z)的伸缩振动a.O=C=O:~2349b.C=C=C:~2025(m),~1070(w)c.N=C=O:~2260(s),~1410(w)d.N=N=N:~2140(s),~1265(w)5)X-H(X=B,P,Se,Si)(s/m)a.有机硼化物:~2495b.有机膦化物:~2365c.有机硒化物:~2290d.有机硅化物:~22303.第三峰区(1900~1500)1)C=O伸缩振动(s)a.酮①R-CO-R: ~1715②R-CO-Ph:~1690①游离 ~1760②缔合 ~1720(在~3000出现s.b.,结合可以判断)d.酯① ~1740②不饱和酯 ~1760③不饱和酸酯 ~1715(在~1200出现2~3条s.b,结合可以判断)e.酰胺①酰胺Ⅰ带:~1665②酰胺Ⅱ带:~1550③酰胺III带:~1300f.酸酐①开链酸酐:~1850(s),~1780(s-,弱于前者)②环酸酐:~1830(s-),~1770(s,强于前者)2)C=C伸缩振动 (相比于C=C吸收频率较低,强度也弱得多) a.烯烃:~1630(结合~3050峰)b.苯环:~1600,~1500 2~3条3)硝基 ~1550,~1345 s.b.双峰4)亚硝基 ~15505)N-H弯曲振动a.伯胺 ~1600b.仲胺 ~15354.第四峰区(1500~650)(指纹区)1)C-H弯曲振动(烃类化合物)a.烷烃①伯碳:~1450(m),~1380(w)②仲碳:~1450(m)b.烯烃/芳香烃①RCH=CH2:~990(s),~910(s)②RR'C=CH2:~890(s)③RCH=CHR'(trans-):~970(s)④RCH=CHR'(cis-):~690(m)(不特征)c.芳香烃①环呼吸振动:~1600,~1500②面内弯曲振动:~1250(干扰大)③面外弯曲振动:PhCH3:~750,~700o-CH3PhCH3:~750m-CH3PhCH3:~780,~700p-CH3PhCH3:~8102)C-O伸缩振动a.醇①伯醇:~1050(s)②仲醇:~1100(s)③叔醇:~1150(s)(结合~3600/3300判断)b.酚 ~1200c.醚①对称:~1150②不对称:~1250,~1050d.酯~1200 2~3条(s)e.酸酐①开链酐:~1110②环酐:~12603)C-Cl:~7004)C-Br:~5505)C-S:~7006)C-N:~12307)Ar-N=:~13058)R-N=:~12309)-NH2:~78510)-NO2:~1350第二章 有机质谱一.基本原理1.质谱是化合物电离后按照质量数与所带电荷数之比被仪器分离并以离子质荷比与其相对强度记录下来的谱, 谱图与分子结构有关2.光谱信息:唯一可以给出分子量, 确定分子式的方法3.结构组成1)进样系统2)离子源离子化方法:a.电子轰击(EI)①电离效率高,产生较多碎片峰,可提供丰富的结构信息②分子离子峰较弱或不出现b.化学电离源(CI)①电离能小,质谱峰数少②准分子离子峰大c.场电离源(FI)电离温和,碎片少,主要产生分子离子峰d.场解析源(FD)①适于非挥发性且分子量上万的分子电离②产生分子离子峰和准分子离子峰e.快电子轰击(FAB)①适用于挥发性极低、极性很强的有机化合物、离子型化合物、热不稳定和分子量较大的化合物②会出现基质分子产生的相应的峰及基质分子与样品分子的结合峰f.电喷雾电离(ESI)①低分子量化合物产生单电荷离子(失去或得到1个质子)②高分子量生物大分子和聚合物产生多电荷离子③可能生成加合物和/或多聚体3)质量分析器4)检测器4.主要技术指标1)质量范围:指质谱计所检测的单电荷离子的质荷比范围2)分辨率(R)a.含义:质谱计分开相邻两离子质量的能力b.R=m/Δm(Δm为质谱计可分辨的相邻两峰的质量差,m为可分辨的相邻两峰的平均质量)5.质谱术语1)基峰2)质荷比3)低分辨率质量:组成离子的各元素同位素的原子核的质子和中子数目之和4)精确质量:基于精确原子量6.质谱中的离子:1)分子离子:z=1时, 其m/z等于天然丰度最大的同位素的原子量之和2)碎片离子:广义上指除分子离子以外的所有离子3)重排离子:经过重排,断裂一个以上化学键所生成的离子4)母/子离子:任何一个离子进一步裂解为质荷比较小 的离子,前者是后者的母离子或前体离 子,后者是前者的子离子5)奇/偶电子离子:带有未配对电子的离子为奇电子离子,无未配对电子的离子为偶电子离子6)多电荷离子:一个分子丢失一个以上(通常两个)电子所形成的离子7)准分子离子:比分子量多(或少)一的离子或准分子离子8)同位素离子:非单一同位素的元素在电离过程中产生同 位素离子,同位素离子构成同位素峰簇二.分子离子和分子式1.分子离子峰的识别1)假定分子离子峰2)判断是否合理:相邻碎片离子间的Δm/z=1,2,3,15,16,17,18,203)判断是否符合氮律:a.不含N或含偶数N的有机分子, 其分子离子峰的m/z为 偶数b.含奇数N的有机分子, 其分子离子峰的m/z为奇数2.分子离子峰的相对强度(RI)1)不稳定的分子,大分子,其分子离子的RI较弱2)稳定的分子, 大共轭分子, 其分子离子的RI较强3)脂肪族醇,胺,亚硝酸酯,硝酸酯,硝基化合物及多支链化合物分子离子峰通常很弱或不出现三.分子式判断1.分子式是否合理1)是否符合氮律2)不饱和度是否合理(UN>0)UN=(n+1)+a/2-b/2(其中,n为分子中4价原子数目,a为三价原子,b为一价原子)3)同位素峰簇的相对丰度a.S:32:33:34=100:0.8:4.4b.Si:28:29:30=100:5.1:3.4c.Cl:35:37≈3:1d.Br:79:81≈1:1三.有机质谱中的裂解反应1.分子中n电子比π电子易丢失,π电子比σ电子易丢失2.离子的正电荷愈分散,离子的稳定愈大3.分类1)自由基位置引发的裂解反应(α裂解)2)自由基位置引发的重排反应(γ氢重排)3)电荷位置引发的裂解反应(i裂解)OE+型(偶电子离子型),EE+型(奇电子离子型)4.一般的裂解规律1)偶电子规律a.偶电子离子裂解通常只能生成偶电子离子,质荷比较小的奇电子离子往往是由质荷比较大的奇电子离子裂解产生b.判断奇电子离子峰:①不含氮化合物质荷比为偶数值的峰为奇电子离子峰②含氮化合物,分子离子或碎片离子含奇数个氮,其质荷比为奇数时为奇电子离子③含氮化合物,分子离子或碎片离子含偶数个氮,其质荷比为偶数时为奇电子离子2)烃类化合物的裂解规律优先失去大的基团生成稳定的正碳离子3)含杂原子化合物的裂解规律α裂解和i裂解为主4)羰基化合物的裂解规律α裂解和i裂解为主5)逆D-A反应(RDA)6)氢的重排反应a.McLafferty重排(γ氢重排,六元环过渡态)b.自由基引发或正电荷诱导,经过四、五、六元环过渡态氢的重排c.长链酯基的双氢重排d.偶电子离子氢的重排经过四元环过渡态的β氢重排,使偶电子离子进一步裂解,生成质荷比较小的奇电子离子和稳定的小分子 e.芳环的邻位效应邻位取代芳环中,取代基通过六元环过渡态氢的重排,失去中性分子,生成奇电子离子的裂解过程四.各类有机化合物的质谱1.烃类1)直链烃a.弱分子离子峰可见b.M-29(C2H5),43+14n(CnH2n+1)峰(其中43,57往往是基峰)(伴随CnH2n-1,CnH2n峰群)2)支链烃a.分子离子峰弱或不见b.M-15峰(可能含有侧链甲基)c.侧链优先断裂,失去大基团,支链处峰强度增大3)环烷烃a.分子离子峰较强b.出现41,55,69峰4)烯烃a.α断裂 41峰(CH2=CH-CH2+) 基峰或强峰b.γ-氢重排 42峰(CH2=CH-CH3+·) 基峰或强峰c.41+14n峰(伴随CnH2n+1,CnH2n峰群)d.环己烯及其衍生物发生RDA反应或裂解生成稳定的环烯离子5)芳香烃a.分子离子峰强或中强b.α断裂,产生91的基峰或强峰c.γ-H的重排,产生m/z为92的奇电子离子峰d.进一步裂解产生78,52或66,40峰2.含氧化合物1)醇/酚a.分子离子峰弱或不出现b.α裂解:31+14n的含氧碎片离子峰c.M-18(H2O),M-18-28(C2H2)H2n-1,CnH2n+1峰群e.例①环己醇②苄醇③苯酚2)醚a.弱分子离子峰b.α断裂,碳-碳σ键断裂:31+14n峰c.i异裂,碳-氧σ键断裂:43+14n峰d.伴有CnH2n , CnH2n -1 峰e.区别醇:无M-18,M-18-28失水峰f.双取代芳香醚取代基位置对其质谱有较大影响(见四.1.5) 例.对二甲氧基苯邻二甲氧基苯3.含硫化合物1)硫醇a.分子离子峰强b.出现M-33(-SH),M-34(-SH2),33,34峰c.出现含硫碎片离子峰47+14n(CnH2n+1S)d.伴有CnH2n,CnH2n-1,CnH2n+1峰2)硫醚a.分子离子峰较强b.生成CnH2n+1S+系列含硫碎片离子峰4.含氮化合物1)脂肪胺a.分子离子峰弱b.30+14n的含氮特征碎片离子峰c.44(or 44+14n),58(or 58+14n)的峰为基峰或强峰2)环己胺a.分子离子峰相对较强b.出现56峰 (CH2=CH-CH=NH2+)c.类似于环己醇裂解3)苯胺5.卤代烃1)分子离子峰强度由氟向碘依次增大2)卤素存在特征:a.氟:M-19(-F),M-20(-HF)b.氯、溴:①M-35(-Cl),36(-HCl),M-79(-Br),79(Br+)6.羰基化合物1)醛a.α断裂:产生M-1(-H),M-29(-CHO),29(强,HCO+)峰b.有明显的分子离子峰c.43+14n特征碎片离子峰(脂肪醛)2)酮3)羧酸a.弱分子离子峰b.出现M-17(-OH),M-45(-COOH),45(-COOH)峰c.γ-H重排生成60峰4)酯类a.小分子酯有明显的分子离子峰b.甲酯,乙酯出现M-31(-OCH3),M-45(-OC2H5)峰c. γ-H的重排生成m/z为74+14n的峰d.乙酯以上的酯双氢重排生成61+14n的偶电子离子5)酰胺有明显的分子离子峰(β改为α)7.双取代芳环-邻位效应芳环的邻位取代基间容易形成六元环过渡态,发生氢的重排裂解8.非氢重排1)环化取代重排2)消去重排a.烷基迁移b.苯基迁移c.烷氧基迁移d.氨基迁移。
有机波谱分析总结

需要掌握旳概念:
红移 蓝移 增(减)色效应 吸收带旳分类(文件中直接出现):
K(R/B/E)带吸收
常见类型有机物旳紫外光谱
烷烃 含杂原子旳饱和化合物 共轭烯烃
(1)Woodward-Fieser规则 链状、环状共轭烯烃波长计算措施
(2)Fieser-Kuhn规则 用于推算分子中具有四个以上旳双键
能够指示 (CH2)n旳存在 鉴别烯烃旳取代程度和构型信息 推定苯环旳取代类型
红外光谱在定性分析中旳应用
红外光谱旳解析环节 1.了解样品概况
a.样品起源 b.样品旳物理性质 c.样品旳化学性质 d.元素分析成果及分子量,求出分子式 e.红外光谱测试条件
2.计算分子旳不饱和度 所谓不饱和度,是指分子中具有双键、三
官能团(特征频率)区
4000-1300cm-1 基团旳特征吸收峰位于此区 吸收峰比较稀疏 可分为三个波段
①4000-2500cm-1 x-H伸缩振动区(x=O、N、C等) Ⅰ:>3000cm-1 旳C-H吸收峰,则预示化合物为不饱和 Ⅱ:<3000cm-1 有吸收,则预示化合物是饱和旳
②:2500-2023cm-1 叁键和合计双键区 ③:2023-1500cm-1 双键伸缩振动区
各类有机化合物旳化学位移
①饱和烃
-CH3: -CH2: -CH:
CH3=0.791.10ppm CH2 =0.981.54ppm CH= CH3 +(0.5 0.6)ppm
O CH3 N CH3
C C CH3 O C CH3
CH3
H=3.2~4.0ppm H=2.2~3.2ppm H=1.8ppm H=2.1ppm H=2~3ppm
b.全方面考虑。
《波谱分析》南京工业大学期末复习1(1)

《波谱分析》期末复习一、判断题正确填‘’,错误的填‘’1.电磁辐射的波长越长,能量越大。
()2. 当分子受到红外激发,其振动能级发生跃迁时,化学键越强吸收的光子数目越多。
()3. 核磁共振波谱法与红外光谱法一样,都是基于吸收电磁辐射的分析法。
()4. (CH3)4Si 分子中1H核共振频率处于高场,比所有有机化合物中的1H核都高。
()5. 根据N规律,由C,H,O,N组成的有机化合物,N为奇数,M一定是奇数;N为偶数,M也为偶数。
()二、选择题1、光或电磁辐射的二象性是指(D )A、电磁辐射是由电矢量和磁矢量组成B、电磁辐射具有波动性和电磁性C、电磁辐射具有微粒性和光电效应D、电磁辐射具有波动性和微粒性2、光量子的能量与电磁辐射的的哪一个物理量成正比(A )A、频率B、波长C、周期D、强度3、可见光区、紫外光区、红外光区和无线电波四个电磁波区域中,能量最大和最小的区域分别为( A )A、紫外光区和无线电波B、紫外光区和红外光区C、可见光区和无线电波D、可见光区和红外光区4、紫外光谱的产生是由电子能级跃迁所致,能级差的大小决定了( C )A、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状5、紫外光谱是带状光谱的原因是由于( C )A、紫外光能量大B、波长短C、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因D、电子能级差大6、化合物中,下面哪一种跃迁所需的能量最高?( A )A、σ→σ﹡B、π→π﹡C、n→σ﹡D、n→π﹡7、红外光可引起物质的能级跃迁是(C )A、分子的电子能级的跃迁,振动能级的跃迁,转动能级的跃迁B、分子内层电子能级的跃迁C、分子振动能级及转动能级的跃迁D、分子转动能级的跃迁8、红外光谱解析分子结构的主要参数是(B )A、质核比B、波数C、偶合常数D、保留值9、CH3-CH3的哪种振动形式是非红外活性的( A )A、νC-CB、νC-HC、δasCHD、δsCH10、化合物中只有一个羰基,却在1773cm-1和1736cm-1处出现两个吸收峰这是因为:( C )A、诱导效应B、共轭效应C、费米共振D、空间位阻11、一种能作为色散型红外光谱仪的色散元件材料为:(D)A、玻璃B、石英C、红宝石D、卤化物结体12、预测H2S分子的基频峰数为:( B )A、4B、3C、2D、113. 在偏共振去偶谱中,RCHO的偏共振多重性为(C )A、四重峰B、三重峰C、二重峰D、单峰14、化合物CH3-CH=CH-CH=O的紫外光谱中,λmax=320nm(εmax=30)的一个吸收带是(B )A K带B R带C B带D E2带15、质谱图中强度最大的峰,规定其相对强度为100%,称为(B )A、分子离子峰B、基峰C、亚稳离子峰D、准分子离子峰16、分子式为C5H10O的化合物,其1H-NMR谱上只出现两个单峰,最有可能的结构式为(B )A、(CH3)2CHCOCH3B、(CH3)3C-CHOC 、CH3CH2CH2COCH3D、CH3CH2COCH2CH317、若外加磁场的强度H0逐渐加大时,则使原子核自旋能级的低能态跃迁到高能态所需的能量是如何变化的?( B )A、不变B、逐渐变大C、逐渐变小D、随原核而变18、下列哪种核不适宜核磁共振测定(A)A、12CB、15NC、19FD、31P19、苯环上哪种取代基存在时,其芳环质子化学位值最大( D )A、–CH2CH3B、–OCH3C、–CH=CH2D、-CHO20、质子的化学位移有如下顺序:苯(7.27)>乙烯(5.25) >乙炔(1.80) >乙烷(0.80),其原因为:(D)A、诱导效应所致B、杂化效应所致C、各向异性效应所致D、杂化效应和各向异性效应协同作用的结果21、确定碳的相对数目时,应测定( D )A、全去偶谱B、偏共振去偶谱C、门控去偶谱D、反门控去偶谱22、1J C-H的大小与该碳杂化轨道中S成分( B )A、成反比B、成正比C、变化无规律D、无关23、在质谱仪中当收集正离子的狭缝位置和加速电压固定时,若逐渐增加磁场强度H,对具有不同质荷比的正离子,其通过狭缝的顺序如何变化?(B)A、从大到小B、从小到大C、无规律D、不变24、含奇数个氮原子有机化合物,其分子离子的质荷比值为:( B )A、偶数B、奇数C、不一定D、决定于电子数25、二溴乙烷质谱的分子离子峰(M)与M+2、M+4的相对强度为:( C )A、1:1:1B、2:1:1C、1:2:1D、1:1:2三、问答题1、摩尔吸光系数;答:浓度为1mol/L,光程为1cm时的吸光度2、非红外活性振动;答:分子在振动过程中不发生瞬间偶极矩的改变。
有机波谱分析总结

4~8
分子缔合
10.5~16
一、紫外光谱UV:(200nm~400nm)
π→π*
n→π*
丁二烯
217(21000)
—CHO
210(强)
285~295(10~30)
R2C=O
~195(1000)
270~285
—NO2
~210(强)
~270(10~20)
芳香族(255分裂成多个峰)
184(47000)204(6900)255(230)
一、紫外光谱UV:(200nm~400nm)
π→π*
n→π*
丁二烯
217(21000)
—CHO
210(强)
285~295(10~30)
R2C=O
~195(1000)
270~285
—NO2
~210(强)
~270(10~20)
芳香族(255分裂成多个峰)
184(47000)204(6900)255(230)
1275~1020
N—H
3490~3400
三、核磁共振
δ
—CH3
0.9
—CH2
1.33
—CH
1.5
—CH—CH= CH2
1.59~2.24
—CH—C≡CH
1.8~2.8
CH2= CH2
5.25
CH≡CH
1.7~3.0
芳烃
6.3~8.5
芳香杂环
6.0~9.0
卤代烃
2.16~4.4
相邻碳质子
1.25~1.55
酚:O—H
4~8
分子缔合
10.5~16
一、紫外光谱UV:(200nm~400nm)
波谱分析报告考试复习的总结

波谱分析(spectra analysis)波谱分析的内涵与外延:定义:利用特定的仪器,测试化合物的多种特征波谱图,通过分析推断化合物的分子结构。
特定的仪器:紫外,红外,核磁,质谱,(X-射线,圆二色谱等)特征波谱图: 四大谱;X-射线单晶衍射,圆二色谱等化合物:一般为纯的有机化合物分子结构:分子中原子的连接顺序、位置;构象,空间结构仪器分析(定量),波谱分析(定性)综合性、交叉科学(化学、物理、数学、自动化、计算机)作用:波谱解析理论原理是物理学,主要应用于化学领域(天然产物化学和中药化学、有机化学、药物化学等),在药物、化工,石油,食品及其它工业部门有着广泛的应用;分析的主要对象是有机化合物。
课程要求:本课将在学生学习有机化学、分析化学、物理化学等课程的基础上,系统讲授紫外光谱(UV)、红外光谱(IR)、核磁共振光谱(NMR)和质谱(MS)这四大光谱的基本原理、特征、规律及图谱解析技术,并且介绍这四大光谱解析技术的综合运用,培养学生掌握解析简单有机化合物波谱图的能力。
为学习中药化学有效成分的结构鉴定打下基础。
第一章紫外光谱(ultraviolet spectra,UV)一、电磁波的基本性质和分类1、波粒二象性光的三要素:波长(λ),速度(c),频率 (v)电磁波的波动性光速 c:c=3.0 x 1010 cm/s波长λ:电磁波相邻波峰间的距离。
用 nm,μm,cm,m 等表示频率v:v=c/ λ,用 Hz 表示。
电磁波的粒子性光子具有能量,其能量大小由下式决定:E = hν = hc/λ (式中E为光子的能量,h为普朗克常数,其值为6.624× 10-34j.s ) 电磁波的分类2、分子的能量组成(能级图)E 分子= E平+ E转+ E振+E电子能量大小: E转< E振< E电子不同能级跃迁对应的电磁波区域紫外光谱远紫外(4~200nm):又叫真空紫外区近紫外(200~400nm):又叫石英紫外区,最为常用。
波谱分析期末知识总结

波谱分析期末知识总结一、波谱分析的基本原理1.1 原子和分子能级波谱分析的基础是物质中原子或分子的能级结构。
原子或分子的能级是指在不同能量水平上的电子分布情况。
能级之间的能量差决定了原子或分子在吸收或发射辐射时的能量差异。
1.2 吸收和发射辐射原子或分子能级之间的跃迁可以通过吸收或发射辐射来实现。
当原子或分子吸收能量与能级差相等的辐射时,电子会从较低能级跃迁至较高能级,形成吸收峰。
相反,当电子从较高能级跃迁至较低能级时,会发射辐射,形成发射峰。
1.3 分子结构和波谱特征物质的波谱特征与其分子结构密切相关。
分子中不同原子的振动、转动和电子的跃迁等运动方式会对辐射产生不同的影响,从而在波谱上表现出不同的特征峰。
二、波谱分析的技术和仪器2.1 紫外-可见光谱紫外-可见光谱是一种常用的波谱分析技术,用于研究物质在紫外或可见光区的吸收或发射特性。
紫外-可见光谱的测量仪器主要有分光光度计和光源。
2.2 红外光谱红外光谱是一种用于研究物质在红外波段的吸收特性的技术。
红外光谱的测量仪器主要有红外光谱仪和样品室。
红外光谱可以用于确定化学键、鉴定有机物和研究分子结构等。
2.3 核磁共振核磁共振是一种基于核自旋和外磁场相互作用的波谱技术。
核磁共振的测量仪器主要包括核磁共振仪和样品盒。
核磁共振可以用于确定物质的结构、研究分子间相互作用等。
2.4 质谱质谱是一种用于研究物质的分子结构和相对分子质量的技术。
质谱的测量仪器主要有质谱仪和样品处理系统。
质谱可以用于定量分析、鉴定有机物和研究分子结构等。
三、波谱分析的应用3.1 化学分析波谱分析在化学分析中广泛应用。
通过测量样品在不同波长或波数下的吸收或发射特性,可以确定样品的成分和浓度。
常用的波谱分析技术包括紫外-可见光谱、红外光谱、核磁共振和质谱等。
3.2 材料科学波谱分析在材料科学中的应用主要用于研究材料的结构和性质。
通过测量材料的吸收或发射峰,可以确定材料的化学成分、晶体结构、晶格缺陷等信息。
有机化学波谱分析知识要点

波谱分析第一章 紫外光谱1、为什么紫外光谱可以用于有机化合物的结构解析?紫外光谱可以提供:谱峰的位置(波长)、谱峰的强度、谱峰的形状。
反映了有机分子中发色团的特征,可以提供物质的结构信息。
2、紫外-可见区内(波长范围为100-800 nm )的吸收光谱。
3、Lamber-Beer 定律 适用于单色光• 吸光度: A = lg(I 0/I) = εlc • 透光度:-lg T = εbcA :吸光度;l :光在溶液中经过的距离;ε:摩尔吸光系数,为浓度在1mol/L 的溶液中在1 cm 的吸收池中,在一定波长下测得的吸光度;c :浓度。
4、有机物分子中含有π键的不饱和基团称为生色团;有一些含有n 电子的基团(如—OH 、—OR 、—NH 2、—NHR 、—X 等),它们本身没有生色功能(不能吸收λ>200 nm 的光),但当它们与生色团相连时,就会发生n —π共轭作用,增强生色团的生色能力(吸收波长向长波方向移动,且吸收强度增加),这样的基团称为助色团。
5、λmax 向长波方向移动称为红移,向短波方向移动称为蓝移(或紫移)。
吸收强度即摩尔吸光系数ε增大或减小的现象分别称为增色效应或减色效应。
6、电子跃迁的类型:1. σ→σ*跃迁:饱和烃(甲烷,乙烷);E 很高,λ<150 nm (远紫外区)。
2. n→σ*跃迁:含杂原子饱和基团(-OH ,-NH 2);E 较大,λ150~250 nm (真空紫外区)。
3. π→π*跃迁:不饱和基团(-C=C-,-C=O );E 较小,λ~ 200 nm ,体系共轭,E 更小,λ更大;该吸收带称为K 带。
4. n→π*跃迁:含杂原子不饱和基团(-C≡N ,C=O ):E 最小,λ 200~400 nm (近紫外区)该吸收带称为R 带。
7、λmax 的主要影响因素:1. 共轭体系的形成使吸收红移;2. pH 值对光谱的影响:碱性介质中,λ↑,吸收峰红移,ε↑ 3. 极性的影响:π→π*跃迁:极性↑,红移,λ↑;ε↓。
有机波谱分析复习参考含答案
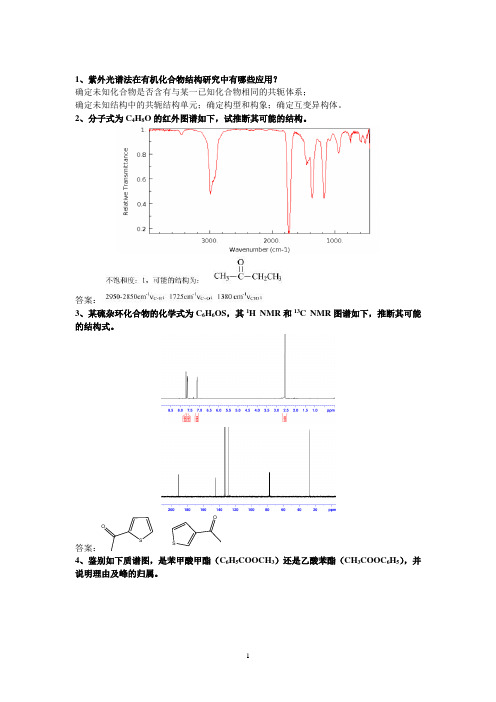
1、紫外光谱法在有机化合物结构研究中有哪些应用?确定未知化合物是否含有与某一已知化合物相同的共轭体系;确定未知结构中的共轭结构单元;确定构型和构象;确定互变异构体。
2、分子式为C4H8O的红外图谱如下,试推断其可能的结构。
答案:3、某硫杂环化合物的化学式为C6H6OS,其1H NMR和13C NMR图谱如下,推断其可能的结构式。
答案:SOSO4、鉴别如下质谱图,是苯甲酸甲酯(C6H5COOCH3)还是乙酸苯酯(CH3COOC6H5),并说明理由及峰的归属。
答案:C 6H 5COOCH 35、某化合物的紫外光谱:OH H C m ax 52λ 262nm (m ax ε15);红外光谱:3330~2500cm -1间有强宽吸收,1715 cm -1处有强宽吸收;核磁共振氢谱:δ11.0处为单质子单峰,δ2.6处为四质子宽单峰,δ2.12处为三质子单峰,质谱如图所示。
参照同位素峰强比及元素分析结果,分子式为C 5H 8O 3,试推测其结构式。
答案:CH 3COCH 2CH 2COOH1、紫外光谱在有机化合物结构鉴定中的主要贡献是什么?答:在有机结构鉴定中,紫外光谱在确定有机化合物的共轭体系、生色团和芳香性等方面有独到之处2、红外光谱产生必须具备的两个条件是什么?答:一是红外辐射的能量应与振动能级差相匹配,即E 光=△E ν,二是分子在振动过程中偶极矩的变化必须不为零。
3、核磁共振谱是物质内部什么运动在外部的一种表现形式?答:是具有核磁矩的原子核的自旋运动在外部的一种表现形式。
4、解释什么是碳谱的γ-效应答:当取代基处在被观察的碳的γ位,由于电荷相互排斥,被观察的碳周围电子云密度增大,δC 向高场移动。
6、根据图 6-1~图6-4推断分子式为C 11H 20O 4未知物结构答案:1.当体系的共轭双键增多时,紫外光谱图会发生什么变化?阐明发生变化的原因。
答:当体系的共轭双键增多时,吸收光会向长波方向移动,即发生红移现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
名词解析发色团(chromophoric groups):分子结构中含有π电子的基团称为发色团,它们能产生π→π*和n→π*跃迁从而你呢个在紫外可见光范围内吸收。
助色团(auxochrome):含有非成键n电子的杂原子饱和基团本身不吸收辐射,但当它们与生色团或饱和烃相连时能使该生色团的吸收峰向长波长移动并增强其强度的基团,如羟基、胺基和卤素等。
红移(red shift):由于化合物结构发生改变,如发生共轭作用引入助色团及溶剂改变等,使吸收峰向长波方向移动。
蓝移(blue shift):化合物结构改变时,或受溶剂的影响使吸收峰向短波方向移动。
增色效应(hyperchromic effect):使吸收强度增加的作用。
减色效应(hypochromic effect):使吸收强度减弱的作用。
吸收带:跃迁类型相同的吸收峰。
指纹区(fingerprint region):红外光谱上的低频区通常称指纹区。
当分子结构稍有不同时,该区的吸收就有细微的差异,并显示出分子特征,反映化合物结构上的细微结构差异。
这种情况就像人的指纹一样,因此称为指纹区。
指纹区对于指认结构类似的化合物很有帮助,而且可以作为化合物存在某种基团的旁证。
但该区中各种官能团的特征频率不具有鲜明的特征性。
共轭效应 (conjugated effect) :又称离域效应,是指由于共轭π键的形成而引起分子性质的改变的效应。
诱导效应(Inductive Effects):一些极性共价键,随着取代基电负性不同,电子云密度发生变化,引起键的振动谱带位移,称为诱导效应。
核磁共振:原子核的磁共振现象,只有当把原子核置于外加磁场中并满足一定外在条件时才能产生。
化学位移:将待测氢核共振峰所在位置与某基准物氢核共振峰所在位置进行比较,其相对距离称为化学位移。
弛豫:通过无辐射的释放能量的途径核由高能态向低能态的过程。
分子离子:有机质谱分析中,化合物分子失去一个电子形成的离子。
基峰:质谱图中表现为最高丰度离子的峰。
自旋偶合:是磁性核与邻近磁性核之间的相互作用。
是成键电子间接传递的,不影响磁性核的化学位移。
麦氏重排(McLafferty rearrangement):具有不饱和官能团 C=X(X为O、S、N、C等)及其γ-H原子结构的化合物,γ-H原子可以通过六元环空间排列的过渡态,向缺电子(C=X+ )的部位转移,发生γ-H的断裂,同时伴随 C=X的β键断裂,这种断裂称为麦氏重排。
自旋偶合:是磁性核与邻近磁性核之间的相互作用。
是成键电子间接传递的,不影响磁性核的化学位移。
自旋裂分:因自旋偶合而引起的谱线增多现象称为自旋裂分。
5.紫外光谱的应用(1).主要用于判断结构中的共轭系统、结构骨架(如香豆素、黄酮等)(2).确定未知化合物是否含有与某一已知化合物相同的共轭体系。
(3).可以确定未知结构中的共轭结构单元。
(4).确定构型或构象(5).测定互变异构现象6.分析紫外光谱的几个经验规律(1).在200~800nm区间无吸收峰,结构无共轭双键。
(2).220~250nm,强吸收(εmax在104~2⨯104之间),有共轭不饱和键(共轭二烯,α,β-不饱和醛、酮)(3).250~290nm,中等强度吸收(εmax 1000~10000) ,通常有芳香结构。
(4).250~350nm,中低强度吸收 (ε10~ 100),且200 nm以上无其他吸收,则含有带孤对电子的未共轭的发色团。
(羰基或共轭羰基)(5).有多个吸收峰,有的在可见区,则结构中可能有长链共轭体系或稠环芳香发色团。
如有颜色,则至少有4~5个共轭的发色团。
(6).利用溶剂效应、pH影响:增加溶剂极性:K带红移、R带紫移,εmax变化大时,有互变异构体存在。
pH变化:碱化后谱带红移,酸化后又恢复,则有酚羟基、烯醇存在;酸化后谱带紫移,有芳胺存在。
(2).红外光谱原理分子中键的振动频率:分子的固有性质,它随着化学键力常数(K)的增大而增加,同时也随着原子折合质量(μ)的增加而降低6.红外光谱在结构解析中的应用(1).确定官能团(2).确定立体化学结构的构型(3).区分构象异构体(4).区分互变异构体与同分异构体2.1H-NMR(氢核磁共振)(1).化学位移的定义(2).常见结构类型的质子化学位移Ar-H C=CH ≡CH RH CH CH2 CH37.28 5.28 2.88 ~1 1.55 1.20 0.87-COOH -CHO ArOH ROH (RNH2)10~12 9~10 4 ~8 0.5 ~53.核磁共振(NMR spectroscopy)—碳谱(13C-NMR)(1).为结构解析提供的信息化学位移(1~250);分辨率高,谱线简单,可观察到不含质子基团;驰豫时间对碳谱是重要参数,可识别季碳,可给出化合物骨架信息。
缺点:测定需要样品量多,测定时间长,而吸收强度一般不代表碳原子个数,与种类有关。
(2).常见一些基团的化学位移δ值①.脂肪C: δ<50②.连杂原子C: C-O, C-N, C-S δ:50-100③.C-OCH3: δ 55;④.糖端基C : δ 95-105⑤.芳香碳,烯碳: δ 98-160⑥.连氧芳碳: δ 140-165⑦.C=O: δ 168-220(3).影响化学位移因素①.碳的杂化方式:δsp3 < δ sp < δ sp2②.碳核的电子云密度:电子云密度↑,↓δ高场位移③.取代基的诱导效应和数目:取代基数目↑, 影响↑,↑δ,诱导效应随相隔键的数目增加而减弱; 随取代基电负性↑,δ↑④.γ效应(γ-旁式,γ-gauch)效应:较大基团对γ-位碳上的氢通过空间有一种挤压作用,使电子云偏向碳原子,使碳化学位移向高场移动,这种效应称为γ-效应。
其中γ-顺效应更强。
⑤.共轭效应:与双键共轭,原双键端基 C2 ↓δ,内侧C1 ↑δ,与羰基共轭, C=O的↓δ⑥.分子内部作用:分子内氢键使C=O的↑δ2试述核磁共振产生的条件是什么?答(1)自旋量子数I≠0的原子核,都具有自旋现象,或质量数A或核电荷数二者其一为奇数的原子核,具有自旋现象。
(2)自旋量子数I=1/2的原子核是电荷在核表面均匀分布的旋转球体,核磁共振谱线较窄,最适宜于核磁共振检测,是NMR研究的主要对象。
4 什么是K带吸收?什么是R带?答(1)共轭非封闭体系烯烃的π→π*跃迁均为强吸收带,ε≧104,称为K带吸收。
(2)n→π*跃迁λmax270-300nm,ε﹤100,为禁阻跃迁,吸收带弱,称R带。
1 什么是氮规则?能否根据氮规则判断分子离子峰?答:(1)在有机化合物中,不含氮或含偶数氮的化合物,分子量一定为偶数(单电荷分子离子的质核比为偶数);含奇数氮的化合物分子量一定为奇数。
反过来,质核比为偶数的单电荷分子离子峰,不含氮或含偶数个氮。
(2)可以根据氮规则判断分子离子峰。
化合物若不含氮,假定的分子离子峰质核比为奇数,或化合物只含有奇数个氮,假定的分子离子峰的质核比为偶数,则均不是分子离子峰。
3红外光谱分为哪几个区及各区提供哪些结构信息?答:红外光谱分四个区:(1)第一峰区(3700-2500cm-1):此峰区为X-H伸缩振动吸收范围。
X代表O,N,C对应于醇、酚、羧酸、胺、亚胺、炔烃、烯烃、芳烃及饱和烃类的O-H,N-H,C-H伸缩振动。
(2)第二峰区(2500-1900cm-1):三键,累积双键及B-H,P-H,I-H,Si-H等键的伸缩振动吸收谱带位于此峰区。
谱带为中等强度吸收或弱吸收。
(3)第三峰区(1900-1500cm-1):双键(包括C=O,C=C,C=N,N=O等)的伸缩振动谱带位于此峰区,对于判断双键的存在及双键的类型极为有用。
另外,N-H弯曲振动也位于此峰区。
(4)第四峰区(1500-400cm-1):此峰区又称指纹区,X-C键的伸缩振动及各类弯曲振动位于此峰区。
不同结构的同类化合物的红外光谱的差异,在此峰区会显示出来。
4.何谓化学位移?它有什么重要性?在1H-NMR中影响化学位移的因素有哪些?答:由于氢核在不同化合物中所处的环境不同,所受到的屏蔽作用也不同,由于屏蔽作用所引起的共振时磁场强度的移动现象称为化学位移.由于化学位移的大小与氢核所处的化学环境密切相关,因此有可能根据化学位移的大小来考虑氢核所处的化学环境,亦即有机物的分子结构特征.由于化学位移是由核外电子云密度决定的,因此影响电子云密度的各种因素都会影响化学位移,如与质子相邻近的元素或基团的电负性,各项异性效应,溶剂效应,氢键等。
4试说明有机化合物的紫外吸收光谱的电子跃迁有哪几种类型及吸收带类型。
答:跃迁的类型有:σ→σ*, n →σ*, π→π *,n→π *。
(1)σ→σ*跃迁:σ→σ*跃迁需要的能量高,对应波长小于150nm,近紫外光谱观测不到。
(2)n→σ*跃迁:含杂原子O,N,S,X饱和烃的衍生物,其杂原子未成键电子向σ*跃迁,其对应波长位于170-180nm,近紫外光谱观测不到。
(3)π→π* 跃迁:π电子较易激发。
非共轭跃迁,对应波长为160-190nm;共轭跃迁,π→π*能量降低,对应波长增大,红移到近紫外区或可见光区,强度大,称为K带。
(4)n→π*跃迁:发生在碳原子或其他原子与带有未成键的杂原子形成的化合物中,如C=O,C=S,N=O等,跃迁波长位于270-290nm,但该跃迁为禁阻跃迁,出现弱吸收带,称为R 带。
红外光谱,紫外光谱,核磁共振,质谱;1H-NMR,13C-NMR,2D-NMR;EI-MS,FAB-MS,ESI-MS。
答:红外光谱:以波长或波数为横坐标,以强度或其他随波长的性质为纵坐标所得到的反映红外射线与物质相互作用的谱图。
紫外光谱:紫外光谱是分子中某些价电子吸收了一定波长的电磁波,由低能级跃近到高能级而产生的一种光谱,也称之为电子光谱。
核磁共振:全旬是核磁共振成像又称自旋成像也称磁共振成像,是磁矩不为零的原子核,在外磁场作用下自旋能级发生塞曼分裂,共振吸收某一定频率的射频辐射的物理过程。
质谱:是一种测量离子荷质比的分析方法,其基本原理是使试样中各组分在离子源中发生电离,生成不同荷质比的带正电荷的离子,经加速电场的作用,形成离子束,进入质量分析器。
各波谱技术名称和特点:⑴红外光谱:主要用于检查功能基;⑵紫外光谱:主要用于检查共轭体系或不饱和体系大小;⑶核磁共振光谱:主要用来提供分子中有关氢及碳原子的类型、数目、互相连接方式、周围化学环境,以及构型、构象的结构信息等;⑷质谱:主要用于检测和确证化合物分子量及主要结构碎片。
