高二化学有机化学基础复习
必修二化学有机总结

必修二化学有机总结一、有机化学基础知识1. 有机化学的定义有机化学是研究有机化合物及其反应规律的科学。
2. 元素的电子结构有机化学中最重要的元素是碳和氢。
碳元素的电子结构为 1s² 2s² 2p²,有四个价电子,可形成四个共价键。
3. 有机物的命名有机物的命名可采用系统命名法和常用名称两种方式。
其中,系统命名法通过规则确定化合物的命名,而常用名称则是根据它们的历史、地理或化学性质确定的。
4. 功能团有机物的功能团是由原子团组成的,能够赋予分子特定的化学性质。
一些常见的功能团包括烷基、烯基、炔基、羟基、醛基、酮基、羧基、胺基等。
二、有机反应的基本概念1. 有机反应的类型有机反应可以分为取代反应、加成反应、消除反应和重排反应等几种类型。
这些反应可以通过配分子方程式描述,并且具有一定的反应机理。
2. 功能团的反应不同的功能团通常会发生特定类型的反应,如烷烃会发生燃烧反应、烯烃会发生加成反应等。
了解不同功能团的反应特性有助于预测和理解化学反应的过程。
三、有机化合物的合成1. 合成方法有机化合物的合成方法多种多样,包括取代反应、加成反应、消除反应、重排反应等。
根据反应条件和反应物的不同,合成路线也会有所差异。
2. 保护基和去保护在有机化合物的合成过程中,为了保护某些功能团不发生不需要的反应,常常需要引入保护基。
合成完成后,再通过去保护反应将保护基去除。
3. 合成策略有机化合物的合成通常需要从较简单的起始物出发,通过多步反应逐步构建目标化合物的骨架。
因此,灵活的合成策略和适当的选择反应法则对于高效合成具有重要意义。
四、有机化合物的结构表征和性质研究方法1. 光谱分析光谱分析是研究化合物结构和性质的重要手段。
常用的有机化合物分析方法包括红外光谱、质谱、核磁共振等。
2. 结构确定通过解读和分析光谱数据,可以确定有机化合物的结构和功能团。
3. 化学性质研究通过实验手段,可以研究有机化合物的化学性质,如燃烧性质、溶解性质、反应性质等。
高二化学有机知识点归纳总结

高二化学有机知识点归纳总结高二有机化学在化学考试中是占很多的分数,如果没有掌握好有机物知识点化学就危险了。
以下是小编整理的高二化学有机物知识点归纳,希望分享给大家提供参考和借鉴。
1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有:(1)、实验室制乙烯(170℃)(2)、蒸馏(3)、固体溶解度的测定(4)、乙酸乙酯的水解(70-80℃)(5)、中和热的测定(6)制硝基苯(50-60℃)〔说明〕:(1)凡需要准确控制温度者均需用温度计。
(2)注意温度计水银球的位置。
3.能与Na反应的有机物有:醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有:(1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物(2)含有羟基的化合物如醇和酚类物质(3)含有醛基的化合物(4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)6.能使溴水褪色的物质有:(1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成)(2)苯酚等酚类物质(取代)(3)含醛基物质(氧化)(4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应)(5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化)(6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。
)7.密度比水大的液体有机物有:溴乙烷、溴苯、硝基苯、四氯化碳等。
8、密度比水小的液体有机物有:烃、大多数酯、一氯烷烃。
9.能发生水解反应的物质有:卤代烃、酯(油脂)、二糖、多糖、蛋白质(肽)、盐。
10.不溶于水的有机物有:烃、卤代烃、酯、淀粉、纤维素11.常温下为气体的有机物有:分子中含有碳原子数小于或等于4的烃(新戊烷例外)、一氯甲烷、甲醛。
高二有机化学合成知识点

高二有机化学合成知识点有机化学合成是有机化学领域中最为重要的分支之一,涉及到有机化学反应的设计和实施,以合成特定的有机物为目标。
本文将介绍高二有机化学合成的一些基础知识点。
一、醇的合成1.1 醇的加成反应醇可以通过烷烃与氢气在催化剂存在下发生加成反应得到。
例如,乙烷经过加热和催化剂存在下,可以得到乙醇:C2H6 + H2 → C2H5OH1.2 醇的卤代烷反应卤代烷可以和氢氧化钠(NaOH)反应生成醇。
例如,氯乙烷与NaOH反应生成乙醇:C2H5Cl + NaOH → C2H5OH + NaCl1.3 醇的脱水反应醇经过脱水反应可以生成烯醇。
例如,乙醇经过加热和催化剂存在下,可以得到乙烯:C2H5OH → C2H4 + H2O二、醛和酮的合成2.1 卡宾加成反应醛和酮可以通过卡宾加成反应合成。
卡宾是一种中性的碳离子,具有两个非配对电子。
例如,乙酸乙酯可以和氢氧化钠反应生成乙醛:CH3COOC2H5 + NaOH → CH3CHO + NaOC2H52.2 烯酮的酸催化合成烯酮可以通过酸催化的反应合成。
例如,乙酸可以和丙酮反应生成烯酮:CH3COOH + CH3COCH3 → CH3COCH2COCH3 + H2O三、酸酐的合成3.1 酸酐的酯化反应酸酐可以通过酯化反应合成。
例如,醋酸和乙醇反应生成乙酸乙酯:CH3COOH + C2H5OH → CH3COOC2H5 + H2O3.2 酸酐的酸催化反应酸酐可以通过酸催化的反应合成。
例如,醋酸可以和水反应生成醋酸酐:CH3COOH + H2O → CH3COOH四、芳香化合物的合成4.1 Friedel-Crafts反应芳香烃可以通过Friedel-Crafts反应合成。
例如,苯和甲酸氯反应生成苯甲酸:C6H6 + HCOCl → C6H5COOH + HCl4.2 Nucleophilic aromatic substitution反应芳香环上的取代基可以通过亲核芳香取代反应引入,生成新的芳香化合物。
高二必修二有机化学知识点总结

【导语】在⾼⼆化学的学习中,是否曾经也有过感慨:有机化学虐我千百遍,我始终待它初恋?下⾯是由为您带来⼀篇⾼⼆必修⼆有机化学知识点,欢迎翻阅。
⾼⼆必修⼆有机化学知识点总结(⼀) 1.有机物的溶解性 (1)难溶于⽔的有:各类烃、卤代烃、硝基化合物、酯、绝⼤多数⾼聚物、⾼级的(指分⼦中碳原⼦数⽬较多的,下同)醇、醛、羧酸等。
(2)易溶于⽔的有:低级的[⼀般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、⼆糖。
(它们都能与⽔形成氢键)。
2.能使酸性⾼锰酸钾溶液KMnO4/H+褪⾊的物质 1)有机物:含有C=C、—C≡C—、—OH(较慢)、—CHO的物质苯环相连的侧链碳上有氢原⼦的苯的同系物(但苯不反应) 2)⽆机物:与还原性物质发⽣氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+ 3.与Na反应的有机物:含有—OH、—COOH的有机物 与NaOH反应的有机物:常温下,易与含有酚羟基、—COOH的有机物反应 加热时,能与卤代烃、酯反应(取代反应) 与Na2CO3反应的有机物:含有酚羟基的有机物反应⽣成酚钠和NaHCO3; 含有—COOH的有机物反应⽣成羧酸钠,并放出CO2⽓体; 含有—SO3H的有机物反应⽣成磺酸钠并放出CO2⽓体。
与NaHCO3反应的有机物:含有—COOH、—SO3H的有机物反应⽣成羧酸钠、磺酸钠并放出等物质的量的CO2⽓体。
4.既能与强酸,⼜能与强碱反应的物质 (1)2Al + 6H+ == 2 Al3+ + 3H2↑ 2Al + 2OH- + 2H2O == 2 AlO2- + 3H2↑ (2)Al2O3 + 6H+ == 2 Al3+ + 3H2O Al2O3 + 2OH- == 2 AlO2- + H2O (3)Al(OH)3 + 3H+ == Al3+ + 3H2O Al(OH)3 + OH- == AlO2- + 2H2O (4)弱酸的酸式盐,如NaHCO3、NaHS等等 NaHCO3 + HCl == NaCl + CO2↑ + H2O NaHCO3 + NaOH == Na2CO3 + H2O NaHS + HCl == NaCl + H2S↑ NaHS + NaOH == Na2S + H2O (5)弱酸弱碱盐,如CH3COONH4、(NH4)2S等等 2CH3COONH4 + H2SO4 == (NH4)2SO4 + 2CH3COOH CH3COONH4 + NaOH == CH3COONa + NH3↑+ H2O (NH4)2S + H2SO4 == (NH4)2SO4 + H2S↑ (NH4)2S +2NaOH == Na2S + 2NH3↑+ 2H2O有机化学知识点 (6)氨基酸,如⽢氨酸等 H2NCH2COOH + HCl → HOOCCH2NH3Cl H2NCH2COOH + NaOH → H2NCH2COONa + H2O (7)蛋⽩质分⼦中的肽链的链端或⽀链上仍有呈酸性的—COOH和呈碱性的—NH2,故蛋⽩质仍能与碱和酸反应。
有机化学基础复习题

高二化学有机化学基础模块试题质量检测一、选择题1.诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是A .纤维素、脂肪B .蛋白质、高级烃C .淀粉、油脂D 蛋白质、硬化油2.北京奥运会火炬“祥云”燃烧系统内装环保型燃料——丙烷。
下列关于丙烷说法不正确的是A .分子中的碳原子不在同一条直线上B .光照下能够发生取代反应C .比丁烷更容易液化D .是石油分馏的一种产品3.常温常压下为气体的有机物是①一氯甲烷 ②二氯甲烷 ③甲醇 ④甲醛 ⑤甲酸 ⑥甲酸甲酯A .①②B .②④⑤C .③⑤⑥D .①④4.下列物质中,在一定条件下既能发生水解反应,又能发生银镜反应的是A .蔗糖B .葡萄糖 c .麦芽糖 D .乙酸甲酯5.下列有机物中加入溴水,充分振荡后静置,观察到水层变为无色,有机溶液层为橙黄色,该有机物是A .苯B .1-己烯C .1,3-丁二烯D .乙醛6.能在KOH 的醇溶液中发生消去反应的是7.下列实验能成功的是A .将乙酸和乙醇混合加热制乙酸乙酯B .苯和浓溴水反应制溴苯C .32CH CH Br 中滴加3AgNO 溶液观察是否有浅黄色沉淀,判断卤代烃的类型D .用4CuSO 溶液和过量NaOH 溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀8.鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌作用。
已知角鲨烯分子有30个碳原子,其中有6个碳碳双键,且不含环状结构,则其分子式为A .3060C HB .3056C H C .3052C HD .3050C H9.下列化学用语正确的是( )A.聚丙烯的结构简式:B.丙烷分子的比例模型:C.四氯化碳分子的电子式:D.2-乙基-1,3-丁二烯分子的键线式:10.有机物的天然提取和人工合成往往得到的是}昆合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是A .分离、提纯→确定化学式→确定实验式→确定结构式B .分离、提纯→确定实验式→确定化学式→确定结构式C .分离、提纯→确定结构式→确定实验式→确定化学式D .确定化学式→确定实验式→确定结构式→分离、提纯11.对于玻璃器皿上粘有的一些水洗不掉的残留物,其洗涤方法正确的是①残留在试管内壁上的碘,用酒精洗涤。
高二化学有机知识点总结(12篇)

高二化学有机知识点总结(12篇)篇1:高二化学知识点总结1.制硝基苯(―NO2,60℃)、制苯磺酸(―SO3H,80℃)、制酚醛树脂(沸水浴)、银镜反应、醛与新制的Cu(OH)2悬浊液反应(热水浴)、酯的水解、二糖水解(如蔗糖水解)、淀粉水解(沸水浴)。
2.常用新制Cu(OH)2、溴水、酸性高锰酸钾溶液、银氨溶液、NaOH 溶液、FeCl3溶液。
3.Cu(OH)2共热产生红色沉淀的):醛类(RCHO)、葡萄糖、麦芽糖、甲酸(HCOOH)、甲酸盐(HCOONa)、甲酸酯(HCOOCH3)等。
14X(卤原子:氯原子等)、―OH(羟基)、―CHO(醛基)、―COOH(羧基)、―COO―(酯基)、―CO―(羰基)、―OC=C(碳碳双键)、―C≡C―(碳碳叁键)、―NH2(氨基)、―NH―CO―(肽键)、―NO2(硝基)。
1、电解池:把电能转化为化学能的装置。
(1)电解池的构成条件①外加直流电源;②与电源相连的两个电极;③电解质溶液或熔化的电解质。
(2)电极名称和电极材料①电极名称阳极:接电源正极的为阳极,发生x氧化xx反应;阴极:接电源负极的为阴极,发生xx还原xx反应。
②电极材料惰性电极:C、Pt、Au等,仅导电,不参与反应;活性电极:Fe、Cu、Ag等,既可以导电,又可以参与电极反应。
2、离子放电顺序(1)阳极:①活性材料作电极时:金属在阳极失电子被氧化成阳离子进入溶液,阴离子不容易在电极上放电。
②惰性材料作电极(Pt、Au、石墨等)时:溶液中阴离子的放电顺序(由易到难)是:S2->I->Br->Cl->OH->含氧酸根离子。
(2)阴极:无论是惰性电极还是活性电极都不参与电极反应,发生反应的是溶液中的阳离子。
3、阳离子在阴极上的放电顺序是:Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+>Al3+>Mg2+>Na+1.纯碱、苏打:Na2CO32.小苏打:NaHCO33.大苏打:Na2S2O34.石膏(生石膏):CaSO4・2H2O5.熟石膏:2CaSO4・.H2O6.莹石:CaF27.重晶石:BaSO4(无毒)8.碳铵:NH4HCO39.石灰石、大理石:CaCO310.生石灰:CaO11.食盐:NaCl12.熟石灰、消石灰:Ca(OH)213.芒硝:Na2SO4・7H2O(缓泻剂)14.烧碱、火碱、苛性钠:NaOH15.绿矾:FaSO4・7H2O16.干冰:CO217.明矾:KAl(SO4)2・12H2O18.漂:Ca(ClO)2、CaCl2(混合物)19.泻盐:MgSO4・7H2O20.胆矾、蓝矾:CuSO4・5H2O21.双氧水:H2O223.石英:SiO224.刚玉:Al2O325.水玻璃、泡花碱:Na2SiO326.铁红、铁矿:Fe2O327.磁铁矿:Fe3O428.黄铁矿、硫铁矿:FeS229.铜绿、孔雀石:Cu2(OH)2CO330.菱铁矿:FeCO331.赤铜矿:Cu2O32.波尔多液:Ca(OH)2和CuSO433.玻璃的主要成分:Na2SiO3、CaSiO3、SiO234.天然气、沼气、坑气(主要成分):CH435.水煤气:CO和H236.王水:浓HNO3、浓HCl按体积比1:3混合而成。
高二有机化学知识点归纳

高二有机化学知识点归纳一、有机化合物的分类有机化合物种类繁多,按照不同的分类标准可以分为不同的类别。
1、根据碳骨架分类链状化合物:这类化合物分子中的碳原子相互连接成链状。
环状化合物:分子中含有碳环,又分为脂环化合物(如环己烷)和芳香族化合物(如苯)。
2、根据官能团分类烃:仅由碳和氢两种元素组成的有机化合物,包括烷烃、烯烃、炔烃和芳香烃等。
烃的衍生物:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物,常见的官能团有卤素原子(X)、羟基(OH)、醛基(CHO)、羧基(COOH)、酯基(COO)等。
二、烃1、烷烃通式:CₙH₂ₙ₊₂(n≥1)。
结构特点:碳原子之间以单键相连,形成链状结构,剩余价键均与氢原子结合。
物理性质:随着碳原子数的增加,烷烃的熔沸点逐渐升高,密度逐渐增大;常温下,碳原子数小于或等于 4 的烷烃为气态。
化学性质:通常情况下性质稳定,在光照条件下能与氯气等发生取代反应。
2、烯烃通式:CₙH₂ₙ(n≥2)。
结构特点:含有碳碳双键,双键碳原子上的两个价键与其他原子或原子团相连。
化学性质:能发生加成反应(如与氢气、卤素单质、卤化氢等)、氧化反应(能使酸性高锰酸钾溶液褪色)。
3、炔烃通式:CₙH₂ₙ₋₂(n≥2)。
结构特点:含有碳碳三键。
化学性质:与烯烃类似,能发生加成反应和氧化反应。
4、芳香烃苯:具有平面正六边形结构,分子中的碳碳键是介于单键和双键之间的独特的键。
能发生取代反应(如卤代、硝化等),但难以发生加成反应。
三、烃的衍生物1、卤代烃定义:烃分子中的氢原子被卤素原子取代后的产物。
化学性质:能在氢氧化钠水溶液中发生水解反应生成醇,在氢氧化钠醇溶液中发生消去反应生成烯烃。
2、醇定义:羟基与烃基或苯环侧链上的碳原子相连的化合物。
分类:根据羟基所连碳原子的类型,分为伯醇、仲醇和叔醇。
化学性质:能与金属钠反应产生氢气,能发生消去反应生成烯烃(在浓硫酸、加热条件下,醇分子中与羟基相连碳原子的邻位碳原子上脱去一个氢原子,形成碳碳双键),能发生催化氧化反应(醇分子中羟基所连碳原子上有氢原子时,能被氧化为醛或酮)。
高二有机化学基础复习

2. 苯酚的化学性质
1. 酸性
与金属钠取代反应:
与NaOH中和反应
2. 与浓溴水取代反应:定量分析
3. 与FeCl3显色反应:检验
酸性大小:H2CO3>苯酚>HCO3-
3. 溴乙烷的性质
1. 碱性水溶液中水解
2. 碱醇条件下消去
厦门双十中学
烃的衍生物性质
4. 乙醛的化学性质
CH3COOH、C6H5COOH、OHC-COOH、HCOOH
2. 下列物质中,一定是同系物的是( ) A. C2H4和C4H8 B. CH3Cl和CH2Cl2 C. C4H10和C7H16 D. 硬脂酸和油酸
链烃
环烃
烷烃
烯烃
炔烃
脂环烃
芳香烃
卤代烃
醇
酚
醛
酮
羧酸
酯
是否含碳、氢以外的元素
碳骨架形状
官能团类别
官能团类别
饱和烃:
不饱和烃:
脂肪烃
烷烃、环烷烃
烯烃、炔烃、芳香烃
环烷烃
有机化合物分类
厦门双十中学
1. 由下列五种基团:-OH、-CH3、-COOH、-C6H5(苯基)、-CHO,两种不同的集团两两组合,形成的有机化合物的水溶液能使紫色石蕊试液变红的有
C
3. 降冰片烯属于 。
环烃、不饱和烃
H2CO3非有机物;
C6H5OH酸性太弱,不能使得紫色石蕊试液变色。
基本概念例题
厦门双十中学
基本概念例题
A. 丙三醇、氯仿、乙醇钠 B. 苯、汽油、无水酒精 D. 福尔马林、白酒、醋 D. 甘油、冰醋酸、煤
厦门双十中学
厦门双十中学
有机实验
高中化学有机化学知识点归纳

高中化学有机化学知识点归纳有机化学是化学的一个重要分支,研究含碳的化合物的结构、性质和反应。
在高中化学学习过程中,有机化学是一个重要的内容,以下是对高中化学有机化学知识点的归纳:1. 有机化合物的命名有机化合物的命名是有机化学的基础,主要有两种命名法,一种是按照IUPAC命名法,另一种是通用命名法。
按照IUPAC命名法,有机化合物命名顺序为:找到最长碳链、确定主链的编号方向、找出取代基的位置、命名取代基、确定双键或环烷的位置等。
通用命名法则是直接根据化学结构,给予化合物一个通用名称。
2. 有机物的结构式有机物的结构式包括:分子式、结构式、分子结构式、键线结构式、空间结构式等。
结构式能直观表现出有机物的结构,有助于理解有机化合物的性质和反应。
3. 有机物的同分异构体同分异构体是指化学式相同,结构式和物理性质却不同的化合物。
同分异构体主要有链式异构体、支链异构体、环状异构体、位置异构体等。
4. 有机物的性质有机物的性质主要包括:饱和、不饱和、烷烃、烯烃、炔烃、芳香烃等。
有机物在化学反应中常常表现出特定的性质和反应活性。
5. 有机物的化学反应有机物的化学反应包括:燃烧、卤代反应、加成反应、消除反应、重排反应、酯化反应、醇醚反应等。
有机化合物在不同条件下会发生不同的化学反应。
6. 有机物的制备方法有机化合物的制备方法包括:实验室制备、化学合成、生物合成等。
根据有机物的结构和性质,可以采取不同的方法来制备有机化合物。
总的来说,高中有机化学知识点的归纳包括有机物的命名、结构式、同分异构体、性质、化学反应和制备方法等内容。
通过系统的学习和积累,可以更好地理解和掌握有机化学知识,为日后的学习和研究打下坚实的基础。
希望以上内容对您有所帮助。
高二化学选修《有机化学》复习提纲
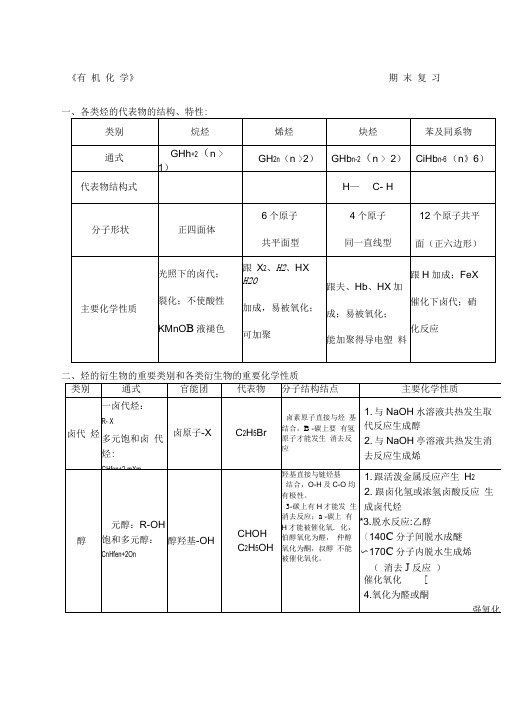
《有机化学》期末复习一、各类烃的代表物的结构、特性:二、烃的衍生物的重要类别和各类衍生物的重要化学性质三、重要的有机反应及类型1取代反应(1) 酯化反应(2) 水解反应aOH卜CHCI+H2O ? C 2H OH+HCI CH 3COOC I+HO H+CH 3COOH+HOH(3)(4)(5)2. 加成反应CH~CH^ CH 2+KBr+HO CH,—C —H + H 3 —*CH 3CH 2OH ,氧化反应 ''(2) 醇、醛的催化氧化:CH 3CHO + 2Cu(OH> + NaO^-CHCOONa + Cd + 3HO (4)被强氧化剂氧化:烯、炔、醇、醛、酚、苯的同系物等被酸性高锰酸钾氧化(1) 能与H 加成的反应:(烯、炔、苯环、醛基、酮)6. 聚合反应7. 中和反应CH )—C —OH T HaOH —- CH,—C —(Th +四、重要的反应.,1. 能使溴水(Br 2/H 2O )褪色的物质CH,—CH —CHj(烯烃与 X 2、H 2O HX H 2)CLCH, CH=CH a + Htl 3 乙醇HO C HOH170绡 尸严LH OHCHjoHCH f +HbO CHkCH-CHBr+KOHCH, C-0H4.(1)燃烧反应:2C 2Hb +5Q 4CG+2HO?2CH a CHOH+O2CH 3CHO+22OAg 550 °CI2CHj —C —Oil2CHCHO+O(3)被弱氧化剂氧化:CHCHO + 2Ag(NH)2OHIICHj —C —ONH*+ 2 AgJ +3NH + H 2O①通过加成反应使之褪色:含有…、-CW 的不饱和化合物②通过取代反应使之褪色:酚类(注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀[三溴苯酚]。
)③通过氧化反应使之褪色:含有-CH 0(醛基)的有机物(有水参加反应)(注意:纯净的只含有一CH(醛基)的有机物不能使溴的四氯化碳溶液褪色)2. 能使酸性高锰酸钾溶液KMn OH+褪色的物质含有…」、-y、-0H (较慢)、-CH0的物质与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应)3.与Na反应的有机物:-OH、-COOH与NaOH反应的有机物:酚羟基、-COOH加热时能与卤代烃、酯反应(取代反应)与NaCO反应的有机物:酚羟基反应生成酚钠和NaHCO -COOH反应放出CO 气体。
高二化学选修5《有机化学基础》知识点整理

高二化学选修5《有机化学基础》知识点整理班级姓名学号一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(....-.29.8....CCl....℃.)....2.F.2.,沸点为..3.Cl..,.沸点为...-.24.2.....CH....℃.).氟里昂(氯乙烯(...HCHO....,沸点为....℃.).甲醛(....-.21..℃.)...2.==CHCl....-.13.9....CH......,沸点为氯乙烷(....℃.).一溴甲烷(CH3Br,沸点为3.6℃)....12.3....CH..2.C.l.,沸点为..3.CH四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
高二《有机化学基础》知识总结

1、常温常压下为气态的有机物:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。
2、碳原子较少的醛、醇、羧酸(如甘油、乙醇、乙醛、乙酸)易溶于水;液态烃(如苯、汽油)、卤代烃(溴苯)、硝基化合物(硝基苯)、醚、酯(乙酸乙酯)都难溶于水;苯酚在常温微溶与水,但高于65℃任意比互溶。
3、所有烃、酯、一氯烷烃的密度都小于水;一溴烷烃、多卤代烃、硝基化合物的密度都大于水。
4、能使溴水反应褪色的有机物有:烯烃、炔烃、苯酚、醛、含不饱和碳碳键(碳碳双键、碳碳叁键)的有机物。
能使溴水萃取褪色的有:苯、苯的同系物(甲苯)、CCl4、氯仿、液态烷烃等。
5、能使酸性高锰酸钾溶液褪色的有机物:烯烃、炔烃、苯的同系物、醇类、醛类、含不饱和碳碳键的有机物、酚类(苯酚)。
6、碳原子个数相同时互为同分异构体的不同类物质:烯烃和环烷烃、炔烃和二烯烃、饱和一元醇和醚、饱和一元醛和酮、饱和一元羧酸和酯、芳香醇和酚、硝基化合物和氨基酸。
7、无同分异构体的有机物是:烷烃:CH4、C2H6、C3H8;烯烃:C2H4;炔烃:C2H2;氯代烃:CH3Cl、CH2Cl2、CHCl3、CCl4、C2H5Cl;醇:CH4O;醛:CH2O、C2H4O;酸:CH2O2。
8、属于取代反应范畴的有:卤代、硝化、磺化、酯化、水解、分子间脱水(如:乙醇分子间脱水)等。
9、能与氢气发生加成反应的物质:烯烃、炔烃、苯及其同系物、醛、酮、不饱和羧酸(CH2=CHCOOH)及其酯(CH3CH=CHCOOCH3)、油酸甘油酯等。
10、能发生水解的物质:金属碳化物(CaC2)、卤代烃(CH3CH2Br)、醇钠(CH3CH2ONa)、酚钠(C6H5ONa)、羧酸盐(CH3COONa)、酯类(CH3COOCH2CH3)、二糖(C12H22O11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)(—C6H10O5—n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
11、能与活泼金属反应置换出氢气的物质:醇、酚、羧酸。
高二化学知识点大全有机物

高二化学知识点大全有机物在高中化学中,有机物是化学知识中的一个重要部分。
有机物主要由碳元素构成,可以分为多个类型,如碳氢化合物、醇类、酮类等等。
下面将介绍一些高二化学中的有机物知识点。
一、碳氢化合物(烃类)碳氢化合物是由碳和氢元素构成的化合物,是有机化合物的基础。
根据碳原子之间的连接方式,碳氢化合物可以分为脂肪烃、环烃和烯烃等几种类型。
1. 脂肪烃:由碳原子形成直链或支链结构。
常见的脂肪烃有甲烷、乙烷、丙烷等。
脂肪烃是石油和天然气的主要组成部分,也是常见的燃料。
2. 环烃:由碳原子形成环状结构。
常见的环烃有环己烷、环丁烷等。
环烃在化学工业中广泛应用,如用于合成塑料和橡胶等。
3. 烯烃:含有至少一个碳-碳双键的烃类化合物。
例如乙烯是一种重要的烯烃,广泛应用于化学工业中。
二、醇类醇类是由氧原子连接到一个或多个碳原子上的有机化合物,通式为R-OH。
醇可以分为一元醇、二元醇、三元醇等多个类型。
1. 一元醇:醇分子中只有一个羟基(-OH)存在。
例如乙醇、甲醇等。
2. 二元醇:醇分子中有两个羟基存在。
例如乙二醇。
三、酮类酮类是由碳原子形成一个羰基(C=O)的有机化合物。
酮类的通式为R1-CO-R2,其中R1和R2可以是不同的有机基团。
四、醛类醛类是由碳原子形成一个羰基(C=O)和一个氢原子的有机化合物。
醛类的通式为R-CHO,其中R可以是不同的有机基团。
五、有机酸有机酸是由碳原子形成羧基(-COOH)的有机化合物。
常见的有机酸包括甲酸、乙酸等。
六、酯类酯类是由醇和有机酸反应生成的化合物。
酯类的通式为R-COO-R',其中R和R'可以是不同的有机基团。
七、氨基酸氨基酸是由一个氨基和一个羧基(-COOH)组成的化合物。
氨基酸是生物体内合成蛋白质的基本单位。
以上是一些高二化学中的有机物知识点介绍,有机物在日常生活中广泛存在,了解有机物的性质和应用对于学生学习化学和理解化学现象非常重要。
希望本文能为您提供有机物方面的基础知识,以便更好地理解和应用化学知识。
高二有机化学知识点总结

高二有机化学知识点总结有机化学是高中化学中的重要内容之一,它研究的是碳元素以及其在化合物中的特性和反应。
在高二阶段,我们学习了许多有机化学的基本知识和反应类型。
下面是对高二有机化学知识点的总结。
一、有机化合物的结构与命名1. 有机化合物的结构:有机化合物由碳、氢和其他元素如氧、氮、硫等构成。
它们的基本结构有直链烷烃、环烷烃、烯烃、炔烃等。
碳原子是四价的,可以形成共价键。
2. 有机化合物的命名:有机化合物的命名使用国际命名法(IUPAC命名法)。
按照此规则,命名步骤包括确定主链、编号、命名取代基等。
二、有机化合物的性质1. 燃烧性质:大多数有机化合物可以燃烧。
它们在氧气中燃烧时,产生二氧化碳和水,并释放出能量。
2. 溶解性质:有机化合物通常可以溶解于有机溶剂中,如醇、醚等。
这是因为它们之间可以形成分子间力,如氢键、范德华力等。
三、有机化学反应类型1. 加成反应:加成反应是指有机化合物中的两个分子相互作用,形成一个新的分子。
例如,醇与酸发生酯化反应,醇中的-OH基与酸中的-COOH基结合,生成酯。
2. 消除反应:消除反应是指有机化合物中的一个分子分解成两个或更多小分子。
例如,醇在酸性条件下可以脱水生成烯烃。
3. 取代反应:取代反应是指有机分子中的一个原子或原子团被另一种原子或原子团替代。
例如,卤代烃与氢氧化钠反应生成醇。
4. 氧化还原反应:氧化还原反应是指有机化合物中的电子的转移。
例如,醇经过氧化反应可以生成醛或酮。
四、官能团的反应1. 醇的反应:醇可以发生酯化、氧化、脱水等反应。
2. 酮的反应:酮可以进行氧化、羟醛反应等。
3. 羧酸的反应:羧酸可以发生酯化、脱羧等反应。
4. 醛的反应:醛可以进行还原、缩醛等反应。
五、重要的有机化合物1. 烷烃:烷烃是由碳和氢构成的碳氢化合物,分为饱和烷烃和不饱和烯烃、炔烃。
2. 醇:醇是含有-OH官能团的有机化合物,根据-OH所连接的碳原子数目不同,可以分为一元醇、二元醇等。
高二化学有机知识点整理与归纳

高二化学有机知识点整理与归纳一、有机代表物质的物理性质1. 状态固态:饱和高级脂肪酸、脂肪、TNT、萘、苯酚、葡萄糖、果糖、麦芽糖、淀粉、纤维素、醋酸(16.6℃以下)气态:C4以下的烷烃、烯烃、炔烃、甲醛、一氯甲烷液态:油状: 硝基苯、溴乙烷、乙酸乙酯、油酸粘稠状: 石油、乙二醇、丙三醇2. 气味无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味)稍有气味:乙烯特殊气味:苯及同系物、萘、石油、苯酚刺激性:甲醛、甲酸、乙酸、乙醛甜味:乙二醇、丙三醇、蔗糖、葡萄糖香味:乙醇、低级酯苦杏仁味:硝基苯3. 颜色白色:葡萄糖、多糖淡黄色:TNT、不纯的硝基苯黑色或深棕色:石油4. 密度比水轻的:苯及苯的同系物、一氯代烃、乙醇、低级酯、汽油比水重的:硝基苯、溴苯、乙二醇、丙三醇、CCl4、氯仿、溴代烃、碘代烃5. 挥发性:乙醇、乙醛、乙酸6. 升华性:萘、蒽7. 水溶性:不溶:高级脂肪酸、酯、硝基苯、溴苯、烷烃、烯烃、炔烃、苯及同系物、萘、蒽、石油、卤代烃、TNT、氯仿、CCl4 能溶:苯酚(0℃时是微溶) 微溶:乙炔、苯甲酸易溶:甲醛、乙酸、乙二醇、苯磺酸与水混溶:乙醇、苯酚(70℃以上) 、乙醛、甲酸、丙三醇二、有机物之间的类别异构关系1. 分子组成符合CnH2n(n≥3)的类别异构体: 烯烃和环烷烃;2. 分子组成符合CnH2n-2(n≥4)的类别异构体: 炔烃和二烯烃;3. 分子组成符合CnH2n+2O(n≥3)的类别异构体: 饱和一元醇和饱和醚;4. 分子组成符合CnH2nO(n≥3)的类别异构体: 饱和一元醛和饱和一元酮;5. 分子组成符合CnH2nO2(n≥2)的类别异构体: 饱和一元羧酸和饱和一元酯;6. 分子组成符合CnH2n-6O(n≥7)的类别异构体: 苯酚的同系物,芳香醇及芳香醚;如n=7,有以下五种: 邻甲苯酚,间甲苯酚,对甲苯酚;苯甲醇;苯甲醚.7. 分子组成符合CnH2n+2O2N(n≥2)的类别异构体: 氨基酸和硝基化合物.三、能发生取代反应的物质1. 烷烃与卤素单质: 卤素单质蒸汽(如不能为溴水)。
高中二年级化学有机化学基础

高中二年级化学有机化学基础在高中化学课程中,有机化学是一个非常重要的分支。
它研究碳及其化合物,包括碳氢化合物和含氧、氮、硫等杂原子的有机化合物。
有机化学的基础知识是我们进一步学习并理解有机化合物性质和化学反应机制的基础。
下面,我将从有机化学的结构、命名规则以及有机反应中的重要概念等方面展开介绍。
一、有机化学的结构有机化学的核心是研究碳的化学性质及其化合物的性质。
碳原子有四个价电子,可以形成共价键,而且碳原子容易形成稳定的共价键,这使得碳原子能够形成很多不同的化学物质。
碳与其他原子(如氢、氧、氮等)形成不同的键构成了有机化合物,这些键的特性决定了有机化合物的性质。
有机化合物的基本结构由碳骨架和官能团组成。
碳骨架是由多个碳原子连成的链状、环状或支链状结构,这种结构决定了有机化合物的物理性质和化学性质。
而官能团则是有机化合物中决定其化学性质的部分,如羟基、酮基、酯基等。
二、有机化学的命名规则有机化合物的命名规则是为了统一和准确地表示化合物的结构和性质。
有机化合物的命名采用系统命名法,根据化合物的结构和功能基团来进行命名。
系统命名法有一定的规则和步骤,主要分为三个方面:基础名称、功能基团和位置编号。
基础名称是根据碳骨架的长度和结构来确定的。
一般来说,碳骨架的长度决定了有机化合物的前缀和中缀,而碳骨架的结构则决定了有机化合物的后缀。
功能基团是有机化合物中决定其化学性质的部分,也是命名中的重要元素。
根据有机化合物中的官能团不同,可以添加相应的前缀或后缀来表示。
例如,羢基、醇基、酸基等。
位置编号是用来指示官能团在碳骨架中的位置的。
在命名中,需要确定官能团在碳骨架中的位置,并使用适当的编号来表示。
三、有机反应中的重要概念有机反应是研究有机化合物之间的化学反应及其反应机理的。
了解有机反应的重要概念有助于我们理解有机化学的性质和应用。
1. 亲核试剂和电子受体:亲核试剂具有孤立电子对,它们能够与电子不足的原子或离子形成共价键。
高二化学知识点:有机化学知识归纳

高二化学知识点:有机化学知识归纳高二化学是高中生学好高中化学的重要组成部分,学好化学直接影响着高中三年理综的成绩。
下面是为大家汇总的高二化学知识点:有机化学知识归纳。
一、同系物结构相似,在分子组成上相差一个或若干个CH2原子团的物质物质。
同系物的判断要点:1、通式相同,但通式相同不一定是同系物。
2、组成元素种类必须相同3、结构相似指具有相似的原子连接方式,相同的官能团类别和数目。
结构相似不一定完全相同,如CH3CH2CH3和(CH3)4C,前者无支链,后者有支链仍为同系物。
4、在分子组成上必须相差一个或几个CH2原子团,但通式相同组成上相差一个或几个CH2原子团不一定是同系物,如CH3CH2Br和CH3CH2CH2Cl都是卤代烃,且组成相差一个CH2原子团,但不是同系物。
5、同分异构体之间不是同系物。
二、同分异构体化合物具有相同的分子式,但具有不同结构的现象叫做同分异构现象。
具有同分异构现象的化合物互称同分异构体。
1、同分异构体的种类:⑴ 碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。
如C5H12有三种同分异构体,即正戊烷、异戊烷和新戊烷。
⑵ 位置异构:指官能团或取代基在在碳链上的位置不同而造成的异构。
如1-丁烯与2-丁烯、1-丙醇与2-丙醇、邻二甲苯与间二甲苯及对二甲苯。
⑶ 异类异构:指官能团不同而造成的异构,也叫官能团异构。
如1-丁炔与1,3-丁二烯、丙烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与果糖、蔗糖与麦芽糖等。
⑷ 其他异构方式:如顺反异构、对映异构(也叫做镜像异构或手性异构)等,在中学阶段的信息题中屡有涉及。
以上是高二化学知识点:有机化学知识归纳,谢谢查阅。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[单选]在OSI模型中,传输层为第()层A.3B.4C.6D.7 [单选]对于有抗冻、抗渗要求的混凝土用砂,其云母含量不应大于()。A.1.0%B.2.0%C.3.0% [单选]下列关于会计凭证,表述错误的是()。A.会计凭证是记录经济业务、明确经济责任的书面证明B.会计凭证是登记账簿的依据C.填制原始凭证是会计处理程序的第一个关键步骤D.会计凭证根据填制的程序和用途不同分为原始凭证和记账凭证 [单选]预算线向右上方平行移动的原因是()A.商品X的价格下降了B.商品Y的价格下降了C.商品X和Y的价格按同样的比率下降D.商品X和Y的价格按同样的比率上升 [单选]关于校对的说法,错误的是()。A.校对工作具有"校异同"和"校是非"两大功能B.校异同的唯一依据是原稿C.校是非是指判断原稿中的是非D.校异同又称"活校" [单选]患儿男,8个月,6个月时出现表情呆滞、烦躁、智力发育明显落后,血清苯丙氨酸60mg/L,诊断为苯丙酮尿症。对于该患儿的饮食护理,理想的糖类、蛋白质、脂肪的比例为()A.20∶30∶50B.30∶20∶50C.40∶15∶35D.60∶15∶25E.70∶10∶30 [单选]下列乳腺癌中哪一种癌在超声显示上有特征性()。A.黏液癌B.导管内乳头状癌C.未分化癌D.腺癌E.以上都不是 [多选]涂尔干认为社会事实具有的特点有()A.外在性B.客观性C.普遍性D.强制性 [问答题,简答题]与传统建筑材料相比较,塑料有哪些优缺点? [单选,A2型题,A1/A2型题]治疗中风闭证首选下列哪组腧穴()A.关元、神阙B.百会、神庭、大椎、太冲C.人中、十二井、太冲、丰隆D.足三里、关元、气海E.太阳、头维、三阴交、太溪 [单选]卷烟生产企业在生产环节销售的所有牌号、规格的卷烟需要核定最低计税价格的,由主管税务机关受理后层报()。A、省局税务机关核定。B、财政部核定。C、国家税务总局核定,财政部备案。D、市局税务机关核定。 [单选,B1型题]药品通用名称()A.应当印刷在药品标签的边角B.应当印刷在药品标签的底部C.应当印刷在药品标签的右上角D.其字体以单字面积计不得大于通用名称所用字体的二分之一E.应当显著、突出,其字体、字号和颜色必须一致 [单选]关于仲裁协议,说法正确的是:()A.仲裁协议可以通过电子邮件的方式订立B.仲裁协议仅约定纠纷适用的仲裁规则的,以制作该仲裁规则的仲裁委员会为确定的仲裁委员会,仲裁协议有效C.仲裁协议未约定仲裁规则的,仲裁协议无效D.以口头方式订立的仲裁协议有效 [单选,A2型题,A1/A2型题]pT0的含义是()A.术前影像证实早期癌B.术前已判定为原位癌C.术后病理检查发现原位癌D.术后组织病理学检查未发现原发肿瘤E.术后病理检查诊断明确分型 [多选,案例分析题]李师傅,男,50岁。是一名采矿工人。工龄30年,胸闷10年,近1个月加重,出现气短,呼吸困难,轻微胸痛,在双下胸部,阵发性,查体:双肺听诊呼吸音降低,两下肺细小干湿啰音,心律齐,未闻及病理性杂音。初步可诊断为()。A.石棉肺B.矽肺C.尘肺病D.肺炎E.心功能 [单选]在乳腺癌全野切线源皮距照射定位时,下列哪项描述是错误的()A.放好内外切线野的铅丝,向内切野方向转动机架50度左右,将内切野的内缘放在铅丝处B.升降床并左右移床至源皮距100cmC.透视并转动机架同时调节治疗床使两根铅丝与射野中心重叠并切肺1.5~2cmD.用虚线画上内切线 [单选,A1型题]下列有关偏倚分类,正确的是()A.分为选择偏倚、失访偏倚、信息偏倚和混杂偏倚四类B.分为失访偏倚、回忆偏倚和调查偏倚三种C.分为选择偏倚、信息偏倚和混杂偏倚三种D.分为Berkson偏倚,Neyman偏倚,检出征候偏倚和时间偏倚四种E.以上均正确 [单选]港口与航道程施工总承包特级资质企业近3年年平均工程结算收入应为()以上。A.8亿元B.10亿元C.15亿元D.20亿元 [单选,A1型题]有关乳腺的淋巴引流途径,下列不正确的是()A.锁骨下淋巴结是最主要的引流区域B.两侧乳房间皮下有交通淋巴管C.乳房的深部淋巴网可引流到肝D.胸大、小肌之间有引流的淋巴结E.两侧胸骨旁淋巴结之间没有直接的淋巴交通 [单选,A1型题]参与促进乳腺发育及泌乳功能的激素,错误的是()A.雌激素B.甲状旁腺素C.胎盘催乳素D.皮质醇E.胰岛素 [单选]假定某公司的税后利润为500000元,按法律规定,至少要提取50000元的公积金。公司的目标资本结构为长期有息负债∶所有者权益=1:1,该公司第二年投资计划所需资金600000元,当年流通在外普通股为100000股,若采用剩余股利政策,该年度股东可获每股股利为()元。A、3B、2C、4D [单选,A2型题,A1/A2型题]我国法定的职业肿瘤是()A.紫外线所致皮肤癌B.电离辐射所致白血病C.氯甲醚所致肺癌D.苯胺所致膀胱癌E.镍和镍化合物所致肺癌 [判断题]如果两条平行线路长度相等,则可以装设横差保护。()A.正确B.错误 [单选]M型超声心动图的主动脉根部波群不能检查什么解剖标志A.右室流出道B.左室后壁C.主动脉瓣D.主动脉E.左房腔 [填空题]细度一般是指()方孔筛筛余的百分比。 [问答题,案例分析题]背景材料: [单选,A1型题]儿童生活安排基本原则中,错误是()A.针对不同年龄阶段和不同健康状况儿童制定作息制度B.根据大脑皮质功能活动特点及脑力工作能力变化规律安排日常生活C.既能满足规定的学习任务,又能满足生活需要D.学校、托幼机构与家庭作息时间一致E.学校和家长可根据孩子个体的 [单选]会计核算中产生权责发生制和收付实现制两种记账基础的前提是()。A.会计主体B.持续经营C.货币计量D.会计分期 [判断题]狭义的银行卡则指由商业银行发行的银行卡。A.正确B.错误 [单选]船舶对水航速VL,对地航速VG,船速VE,如果VG<VL<VE,则船舶航行在()情况下。A.顺风顺流B.顶风顶流C.顺风顶流D.顶风顺流 [多选]关于《药典》的正确叙述是()A.是一个国家药品标准的重要参考书B.《药典》的作用是控制药品质量的标准C.一、二部《药典》都包括凡例、正文、附录、索引D.具有法律的约束性E.二部收录中药材及制剂 [问答题,简答题]主变的作用? [单选]冰区航行,遇到冰山时应及早在()保持适当距离避离,如在大风浪天气发现有碎冰集结时,应在()航行。A.上风;上风B.下风;下风C.上风;下风D.下风;上风 [单选,A2型题,A1/A2型题]电子伏特(eV)与焦耳(J)的关系是()A.1eV=1.6×10-19JB.1J=1.6×10-19eVC.1eV=1JD.1eV=1.6×1019JE.以上都不对 [单选]柜员可以通过()交易增加、删除机构尾箱。A.0043B.0044C.0045D.0046 [单选,A1型题]下列何种降血糖药易引起乳酸血症()。A.正规胰岛素B.阿卡波糖C.格列本脲D.甲苯磺丁脲E.苯乙双胍 [填空题]目前,我国钢筋混凝土高层建筑框架、框架—剪力墙结构体系单位面积的重量(恒载与活荷载)大约为();剪力墙、筒体结构体系为()。 [单选]危机干预需要评估的下列哪项是错误的()A.现场干预B.认知状态C.情绪状态D.意志行为E.应对方法资源 [单选,A1型题]预防医学是研究()A.人体健康与环境的关系B.个体与群体的健康C.人群的健康D.社会环境与健康的关系E.健康和无症状患者 [单选]仓储管理包括()两部分。A.仓库管理和库存管理B.仓库管理和储存管理C.库房管理和储存管理D.库
