氨基酸的理化性质
常见的氨基酸的分类特点及理化性质

非极性氨基酸的理化性质
2
疏水性
非极性氨基酸具有很强的疏水性。
4
溶解性
非极性氨基酸在水中的溶解度较低,但在有机溶剂如酒精或丙酮中的溶解度较高。
8
热稳定性
非极性氨基酸的烷基或芳基结构使其具有较高的热稳定性,可以在较高温度下保持结构完整。 非极性氨基酸由于其疏水性,在蛋白质折叠过程中通常会聚集在蛋白质的内部,形成疏水性核心,使得蛋白质整体结 构更加紧密和稳定。
氨基酸的酸碱性
氨基酸中的氨基(-NH2)和羧基(-COOH)具有不同的酸碱性。氨基是弱碱性基 团,而羧基是弱酸性基团。在水溶液中,氨基和羧基会发生质子交换反应,形 成两性离子。这种两性离子的pH值称为氨基酸的等电点(pI)。
1-14
—
pH
pH 值范围
氨基酸在不同pH值下会呈现不同的 离子形式,从而影响其理化性质和
抗原-抗体反应、免 疫标记等
氨基酸的生物学功能
蛋白质合成
氨基酸是构建生物体内蛋白质 的基本单位,是决定蛋白质结构 和功能的关键要素。
能量来源
通过代谢氧化,某些氨基酸可以 向细胞提供ATP,满足机体的能 量需求。
细胞信号传导
部分氨基酸及其代谢产物可作 为细胞间信号传递的载体,调节 生理过程。
抗氧化防护
农业应用
氨基酸可用作生物农药和 叶面肥料,提高作物抗病虫 能力和产量。还可用于饲 料添加,改善动物营养和生 长。
工业生产
许多工业合成过程需要用 到氨基酸,如制药、化工、 材料等领域。它们可作为 原料、催化剂或中间体。
氨基酸的研究进展
持续创新
科学家们不断探索新的技术和方法来研 究氨基酸的结构、性质和功能,推动着这 一领域的持续创新。
各种氨基酸理化性质-20101202综述

分子式:C2H5NO2 化学式:NH2CH2COOH 结构式
分子量:75.07
物化性质:甘氨酸是20个氨基酸中最简单的一个,是一个非极性的氨基酸。白
色单斜晶系 或六方晶系晶体,或白色结晶粉末,无臭,有特殊甜味; 相对密度1.16,熔点 248℃(分解),易溶于水;在水中的溶解度: 25℃ 时为 25g/100ml,50℃时为 39.1g/100ml,75℃时为 54.4g/100ml,100℃时为67.2g /100ml;极 难溶于乙醇,在100g无水 乙醇中约溶解 0.06 g,几乎不溶于丙酮 和乙醚;等电点6.06。
2.合成法:合成法很多,一种是由异丁酸与氨生成氨基异丁醇,再与氰化氢合 成氨基异丁腈,然后水解而成。一种是由异丁醛与氰化氢合成羟基异丁腈,水解 得DL-缬氨酸,经化学法或酶法拆分得L-缬氨酸。也可由异丁醛与氰化钠和氯化铵 直接合成氨基异丁腈,再水解而成。上述三种方法的得率为36%~40%。合成法 所得为外消旋体,须经外消旋拆开。旋光拆开的方法很多,如用酰基-DL-氨基
各种氨基酸性质
酸的酶进行水解,再利用游离氨基酸与酰化体的溶解度差进行分离。化学合成法生产 成本高,反应复杂,步骤多,且有许多副产物。
3.发酵法:利用微生物发酵法生产L-缬氨酸具有原料成本低、反应条件温和及易实 现大规模生产等优点,是一种非常经济的生产方法。 (1)添加前体物发酵法:又称微生物转化法。这种方法使用葡萄糖作为发酵碳源 ,再添加特异的前体物质即在氨基酸生物合成途径中的一些合适中间代谢产物,以避 免氨基酸生物合成途径中的反馈调节作用,经微生物作用将其有效转化为目的氨基酸 。由于其前体物质如丙酮酸等稀少或价格昂贵,目前已少采用此法生产L-缬氨酸。 (2)直接发酵法:是借助于微生物具有合成自身所需氨基酸的能力,通过对特定微 生物ide诱变处理,选育出营养缺陷型及氨基酸结构类似物抗性突变株,以解除代谢调 节中的反馈抑制和反馈阻遏作用,从而达到过量累积某种氨基酸的目的。目前,世界 上L-缬氨酸均采用直接发酵法生产。国外曾对发酵法所用L-缬氨酸优良生产菌株的诱 变育种和代谢调节作了一些研究,而国内尚处于研究与小规模生产阶段,菌株产酸水 平不高,生产水平和产量远不能满足市场需求。因此,以微生物发酵法生产L-缬氨酸 的研究具有重要的意义。
第三章 氨基酸

有如下结构通式。
-氨基酸的通式
COOH H 2N C R H
不变部分
可变部分
-氨基酸的分子构型
1、氨基酸的分类
各种氨基酸的区别在于侧链R基的不同。 20种蛋白质氨基酸按R的极性可分为非极性氨基酸、 极性性氨基酸、酸性氨基酸和碱性氨基酸;按R基的结 构可分为脂肪族氨基酸、芳香族氨基酸及杂环氨基酸3 大类。
( 3 ) 酰 化 反 应
五、氨基酸的化学性质
1.-氨基参与的反应
O R1 C X + H 2N R2 CH COO
-
X = -C l, O H ,-O C O R
OH
-
O R1 C HN
R2 CH COO
-
用途:用于保护氨基以及肽链的氨基端测定等。
( 4 ) 烃 基 化 反 应
五、氨基酸的化学性质
含羟基氨基酸有 含硫氨基酸有
Ser
Cys
Thr
Met
Tyr
一氨基一羧基氨基酸又称中性氨基酸,一氨 基二羧基氨基酸又称酸性氨基酸(Glu、Asp),二 氨基一羧基氨基酸又称碱性氨基酸(Arg、Lys、 His) 。脯氨酸和羟脯氨酸是亚氨酸,因存在于 天然蛋白,习惯上也列入氨基酸。 蛋白质中存在的氨基酸皆为L-型,但在微生 物体内及抗菌素中亦有D-型氨基酸存在(自由或 肽结合形式)。
1.-氨基参与的反应
Cl
C H2 C H2 C l S: R1
R2
C H2 C H2 S
+
H 2N
CH
COO
-
R1
-
R 1 S C H 2 N H C H (R 2 )C O O
用途:是鉴定多肽N-端氨基酸的重要方法。
蛋白质的基本结

(一)氨基酸的理化性质:一般物理性质,旋光 活性,光吸收性,解离性质,等电点,化学性 质。
(二)氨基酸的分离和分析
P46-65(氨基酸的化学合成,自学内容)
第一页,编辑于星期二:二十一点 三十七分。
(一)氨基酸的理化性质
1、一般物理性质
◆无色晶体,熔点较高 (200℃~300℃)水中溶解度 各不同,取决于侧链。氨基酸 能使水的介电常数增高。氨基 酸的晶体是离子晶体。氨基酸是 离子化合物。
半胱氨酸
汞苯甲酸
基 的
-OOC CHCH2 SH + H O -H g+
性
NH3+
C O O -
质
-OOCCHCH2 S Hg+ NH3+
络合物
COO-
作用:与金属离子的螯合性质可用于体内解毒。
第三十一页,编辑于星期二:二十一点 三十七 分。
◆巯基的还原活性:
半胱氨酸的巯基具有还原性,很容易被氧化成二硫键, 两分子半胱氨酸通过二硫键(-s-s-)连接成的化合物叫 胱氨酸,二硫键也容易被还原成巯基。
质 缓冲作用。血红蛋白含有较
多的Pro残基。
O H 2 N CH C OH
CH 2
N NH
组氨酸
第三十六页,编辑于星期二:二十一点 三十七 分。
组氨酸的咪唑基也可以发生烷基化反应,例 如多种水解酶活性中心的组氨酸可以与烷基 化试剂反应,生成烷基化咪唑衍生物,从而 影响到酶的活性。
第三十七页,编辑于星期二:二十一点 三十七 分。
-O O C C H C H 2 S H N H 3+
-O O C C H C H 2 S H N H 3+
2蛋白质的基本结构单位—氨基酸

三、 氨基酸的理化性质
(一)氨基酸的一般物理性质
1.氨基酸的旋光性
除甘氨酸外,氨基酸含有一个手性-碳原子,因此 都具有旋光性。比旋光度是氨基酸的重要物理常数 之一,是鉴别各种氨基酸的重要依据。
氨基酸的结构
α—氨基酸除甘氨酸外都具有光学活性。 通常(+)表示右旋体dewtroisomer),(-) 表示左旋体(Levoisomer),L与D只代表立 体异构型,不表示旋光性。例如人体蛋白质的 α—氨基酸均为L—型,但有左右旋之别。天冬 氨酸(Asp)、谷氨酸(Glu)、赖氨酸 (Lys)、异亮氨酸(Ile)等为L(+);而亮 氨酸(Leu)、丝氨酸(Ser)、苏氨酸 (Thr)、半胱氨酸(Cys)等都为L(-)。
Alanine Valine Leucine
脂肪族氨基酸
O H2N CH C CH2 CH CH3 CH3 OH
-氨基异己酸
氨基酸的结构
甘氨酸
丙氨酸 缬氨酸 亮氨酸
Glycine
Alanine Valine Leucine
脂肪族氨基酸
异亮氨酸 Ileucine
-氨基--甲基戊酸
氨基酸的结构
二、氨基酸的分类
(一)根据来源分:内源氨基酸和外源氨基酸 (二)从营养学角度分:必需氨基酸和非必需 氨基酸
(三)根据是否组成蛋白质来分:蛋白质中常见 氨基酸、蛋白质中稀有氨基酸和非蛋白氨基酸
1、蛋白质中常见氨基酸的结构
甘氨酸 Glycine
脂肪族氨基酸
O H2N CH C H
氨基乙酸
OH
氨基酸的结构
氨基酸的结构
天冬酰胺 Asparagine
谷酰胺 Glutamine
H2 N CH2 CH2 C NH2 O
氨基酸的分类特点和理化性质

氨基酸的分类特点和理化性质氨基酸是构成蛋白质的基本单位,具有多种功能和作用。
根据它们的理化性质和分类特点,氨基酸可以分为非极性氨基酸、极性氨基酸和特殊氨基酸。
1.非极性氨基酸:非极性氨基酸的中心原子由一个氨基基团(NH2)、一个羧基(COOH)、一个氢原子(H)和一个碳原子(C)组成。
这类氨基酸的侧链由多种有机基团组成,不带任何阳离子或阴离子功能性团。
它们通常不溶于水,但溶于有机溶剂。
在生物体内,非极性氨基酸主要负责蛋白质的折叠和稳定。
在非极性氨基酸中,最简单的是甘氨酸、丙氨酸和异亮氨酸等。
这些氨基酸的侧链中带有碳和氢原子,由于不带电荷,属于非极性,因此有亲水性较强。
2.极性氨基酸:这类氨基酸的侧链通常包含含氧或氮等具有强电负性的原子,可以形成氢键、离子键等。
大多数极性氨基酸具有亲水性,能与水进行相互作用,因此溶解度较高。
极性氨基酸可以进一步分为酸性和碱性氨基酸。
-酸性氨基酸:这类氨基酸的侧链含有羟基和羧基,具有负电荷。
代表性的酸性氨基酸有天冬氨酸和谷氨酸等。
这些氨基酸在水溶液中具有酸性,能够释放出负电荷的氢离子,与基性氨基酸发生中和反应。
-碱性氨基酸:这类氨基酸的侧链含有氨基和胺基等功能性团,在水溶液中带正电荷。
代表性的碱性氨基酸有赖氨酸和精氨酸等。
这些氨基酸能够接受负电荷的氢离子,与酸性氨基酸发生中和反应。
3.特殊氨基酸:这是一类在生物体中含量较少,具有特殊功能和结构的氨基酸。
代表性的特殊氨基酸有脯氨酸、半胱氨酸、甲硫氨酸等。
这些氨基酸的结构中具有额外的官能团,能够参与特殊的生化反应和代谢途径。
总的来说,氨基酸的分类特点主要根据其理化性质和功能特点来区分。
非极性氨基酸主要由碳和氢原子组成,溶解度较低,主要负责蛋白质的结构稳定;极性氨基酸具有亲水性,溶解度较高,包括酸性和碱性两种,具有酸碱中和的作用;特殊氨基酸则具有特殊的结构和功能,用于特定的生化反应和代谢途径。
这些特征使得氨基酸能够在生物体内进行多种功能的发挥,并形成复杂的蛋白质结构。
蛋白质、氨基酸理化性质和提取

加热变性沉淀法
利用生物分子与配基之间所具有的专一而又可逆的 亲和力,使生物分子分离纯化
将酶等两性物质的等电点特性与离子交换层析的特 性结合在一起,实现组分分离
3.离心分离
• 离心分离是借助离心机旋转所产生的离心力,根据物质 颗粒的沉降系数、质量、密度及浮力等因子的不同,而使物 质分离的技术。
常用的离心方法:
✓密度梯度离心:样品在密度梯度介质中进行离心,使沉 降系数比较接近的组分得以分离
✓差速离心采用不同的离心速度和离心时间,使沉降速度 不同的颗粒分批分离
离心分离的条件
1. 离心力-由离心速度决定,用转子每分钟的转数表示。
2. 离心时间-指颗粒从样品液的液面完全沉降到离心管底的时间
3.温度和pH值
• 离心温度一般控制在4℃左右,对于某些热稳定性较好的蛋白质等, 也可在室温下进行离心。但在超速或高速离心时,转子高速旋转会 发热,从而引起温度升高。故必须采用冷冻系统,使温度保持在一 定范围内。
蛋白质的理化性质 和提取工艺
目录
一、两性性质及等电点 二、胶体性质 三、变性与复性作用 四、蛋白质的沉淀作用和沉降作用 五、蛋白质的颜色反应 六、蛋白质的紫外吸收性质
七、蛋白质的提取工艺特性
一、两性性质及等电点
蛋白质分子中氨基酸残基的侧链上存在游 离的氨基和羧基,因此蛋白质与氨基酸一样 具有两性解离性质,具有特定的等电点(pI)。
氨基酸的理化性质

氨基酸的理化性质生化1. 氨基酸的理化性质两性解离等电点紫外吸收核酸的紫外吸收最大值2. 蛋白质的分子结构一级顺序肽键二硫键二级主链氢键三级全部疏水作用离子键氢键范德华力四级亚基氢键离子键3. 蛋白质的变性空间构象破坏理化性质改变生物活性丧失4. DNA双螺旋结构反向平行互补双链==手螺旋横纵5. 转运RNA结构稀有碱基茎环结构二级三级6. DNA变性氢键断裂只改变二级不改变核苷酸排列增色效应解链吸光值增加融解温度Tm紫外吸收值达最大的%时的温度7. 酶结构结合酶酶蛋白辅助因子辅酶辅基必需集团活性中心结合集团催化集团£8. 值等于2005Y25, —个简单的酶促反应,当[S] Km A,反应速度最大B,反应速度太慢难以测出C,反应速度与底物浓度成正比D,增加底物浓度反应速1度不变E,增加底物浓度反应速度降低时9. 可逆性抑制竞争性非竞争性反竞争性Km丙二酸琥珀酸脱氢酶琥珀酸磺胺二氢叶酸合成酶对氨基苯甲酸210. 变构酶速度方程式米氏方程,呈型曲线多为多亚基构成,亚基,亚基:中心,中心: 11. 同工酶催化化学反应,分子结构理化性质免疫学性质乳酸脱氢LDH1 LDH2 LDH3 LDH5#肌酸激酶CK1 CK2 CK312. 糖酵解的调节6-磷酸果糖激酶-1激活AMP ADP 1,6-双磷酸果糖::、2,6-双磷酸果糖:: 抑制ATP、柠檬酸丙酮酸激酶激活1,6-双磷酸果糖抑制ATP、丙氨酸己糖激酶抑制长链脂酰CoA13. 底物水平磷酸化1,3-二磷酸甘油酸3-磷酸甘油酸磷酸甘油酸激酶磷酸烯醇式丙酮酸丙酮酸丙酮酸激酶琥珀酰CoA琥珀酸琥珀酰CoA合成酶脱氢琥珀酸延胡索酸琥珀酸脱氢酶14. 糖异生己糖激酶葡萄糖-6-磷酸酶6-磷酸果糖激酶-1果糖双磷酸酶-1丙酮酸激酶丙酮酸羧化酶磷酸烯醇式丙酮酸羧激酶乙酰CoA丙酮酸羧化酶丙酮酸脱氢酶15. 脂酸氧化限速酶肉碱脂酰转移酶I过程脱氢加水再脱氢硫解、NADH+乙酰CoA16. 能量计算17. 酮体生成关键酶羟甲基戊二酸单酰CoA合成酶肝内生成,肝外利用:肝脏没有318. 脂酸合成原料关键酶乙酰CoA羧化酶激活抑制19. 胆固醇原料分子乙酰CoA、分子ATP及分子NADPH+限速酶HMG CoA还原酶20. 胆固醇的转化Qal胆汁酸::类固醇激素7-脱氢胆固醇:维生素:21. 呼吸链递电子体不递氢递氢体也递电子2.细胞色素223. 抑制剂呼吸链抑制剂鱼藤酮粉蝶霉素A异戊巴比妥Cyt与Cyt抗霉素A二巯基丙醇CO解偶联剂与脱离二硝基苯酚24. 高能化合物磷酸肌酸磷酸烯醇式丙酮酸乙酰磷酸ATP GTP UTP CTP乙酰CoA25. 脱氨基作用转氨酶氧化脱氨基嘌呤核苷酸循环26. 氨的转运丙氨酸- 葡萄糖循环谷氨酰胺27. 鸟氨酸循环限速酶氨基甲酰磷酸合成酶CPS-I 变构激活剂生成一份子尿素需要消耗个高能磷酸键瓜氨酸精氨酸鸟氨酸28. 脱羧基作用氨基酸脱羧酶氨酸- 氨基丁酸氨酸牛磺酸氨酸组胺氨酸5- 羟色胺酸氨酸腐氨精脒精胺429. 一碳单位30. 苯丙氨酸和酪氨酸代谢苯丙氨酸酪氨酸多巴多巴胺去甲肾上腺素肾上腺素黑色素对羟本丙酮酸延胡索酸乙酰乙酸苯丙酮酸31. 核苷酸合成原料和分解产物嘌呤原料天冬氨酸谷氨酰胺C02 —碳单位甘氨酸嘧啶原料天冬氨酸谷氨酰胺C02嘌呤产物尿酸:,,,:嘧啶产物-丙氨酸:,:-氨基异丁酸::32. 脱氧核苷酸的生成在磷酸核苷:N P:上进行:N代表A、G U、C:dTMP由甲基化生成33. 抗代谢物嘌呤类似物6-巯基嘌呤::IMP AMP GMP氨基酸类似物氮杂丝氨酸::UTP CTP叶酸类似物氨碟令氨甲喋呤::dUMP dTMP嘧啶类似物5-氟尿嘧啶::dUMP dTMP次黄嘌呤类似物别嘌呤醇::IMP 尿酸阿糖胞苷CDP dCDP 34. DNA复制的酶学DNA聚合酶解螺旋酶弓I物酶单链DNA结合蛋白DNA拓扑异构酶DNA连接酶DNA聚合酶延长修复原核DNA-pol DNA-pol真核DNA-pol DNA-pol除了DNA-polIII 只有外切酶活性, 其余都有双向外切酶活性I拓扑酶II催化3,5 磷酸二酯键DNA聚合酶RNA聚合酶DNA连接酶DNA拓扑异构酶逆转录酶引物酶535. DNA 生物合成过程起始DnaA 辨别起始点DnaB: : 解螺旋SSB 稳定单链DnaG: : 合成短链RNA 引物:提供末端: 终止后冈崎片段的连接水解引物填补空隙连接缺口36. RNA 聚合酶亚基辨认起始点转录延长仅需要核心酶RNA聚合酶I II IIIS-rRNA S-rRNA,tRNA,snRNA37. 转录后修饰mRNA l子结构聚腺苷酸尾巴mRNA的剪接tRNA 剪切: : 剪接: :添加: : 化学修饰: :外显子内含子38. 遗传密码的特点起始密码终止密码39. 乳糖操纵子三个结构基因一个操纵序列阻遏蛋白一个启动序列RNA 聚合酶一个调节基因阻遏蛋白40. 顺式作用元件启动子启动子是的结合位点至少包括转录起始点和以上的功能组件TATA 盒是的结合位点41. 重组DNA 技术常用工具酶限制性核酸内切酶DNA 连接酶DNA 聚合酶I Klenow 片段反转录酶67。
蛋白质氨基酸共有的理化性质

蛋白质氨基酸共有的理化性质氨基酸是有机化学中的一类结构相对简单的有机化合物,是生物体具有高度组成和功能的重要的组成单位。
氨基酸的分子中包含一个氨基(乙胺基)和一个酸基(羧基),至少包含C、H、O、N 四种化学元素,以脱水缩合方式联接,以-CO-NH-结构连接在一起,因此氨基酸又被称为“二元碱型”。
根据氨基酸的最终加成体,氨基酸可以分为四类:α-酰胺型氨基酸、γ-胺基酸、内酰胺型氨基酸和醛胺型氨基酸。
氨基酸含有一个醇类基团(-HCH2R),是一种典型的碱性氨基,具有较强的核碱反应性质;一个酸类基团(-COOH),具有较强的酸性,可以参与酸基反应;一个酰胺基团(-CO-NH2),可以参与水解、脱水缩合、氨基缩合等反应;一个连接二氧基(-C=O),可形成共价键,是大分子在线缆和蛋白质等生物大分子结构的重要构成部分。
氨基酸的分子结构和分子量,严格来说,其理化性质差别较大:在常温常压下,氨基酸的熔点差异也较大,如γ-氨基丙酸的熔点为172℃,苯丙氨酸的为267℃,而丙二酸的熔点却只有85℃;折射率差异也较大,如右旋糖胺酸的折射率只有1.541,苯兰氨酸的折射率却高达1.641;氨基酸盐的溶解度差别较大,如γ-氨基丙酸钠的溶解度,在0℃下为214g/100ml,而甲基羟基脯氨酸钠在0℃下的溶解度仅为0.15g/100ml;氨基酸的碱度,离子均衡常数和酸度,也有一定差异;氨基酸的质荷比也有较大差异,如精氨酸的质荷比为-0.77,而去氧多巴的质荷比为-1.1等。
通过氨基酸的对比可以发现,同类氨基酸的理化性质具有一定的相似性,它们的分子量和分子式有一定的相似性,比较类似的氨基酸的折射率、熔点等特征也很接近,具有一定的重要性和系统性,可以说是一种有效性的划分。
在生物体中,氨基酸是蛋白质构成的基础,因此不同的氨基酸对它具有重要的作用,通过彼此之间的复合、折叠、加工等,可以组成不同的分子和不同的空间结构,使得蛋白质的形态更加的复杂和丰富,从而发挥出不同的生物学功能,一般来讲,氨基酸的变化越多,蛋白质的功能越丰富、越精确。
氨基酸的理化性质
三、氨基酸的理化性质2、氨基酸的两性解离1、两性离子(dipolarrion,dipolar利用滴定曲线计算氨基酸的等电点等电点侧链R基不解离的中性氨基酸(有两个解离基团)丙氨酸缬氨酸1.氨基酸的光学异构体NH2氨基酸的重要化学反应茚三酮反应(ninhydrin reaction):α-H艾德曼反应(Edman 艾德曼反应(Edman肽键(peptide bond)的化合物。
二肽(dipeptide);寡肽丝氨酰甘氨酰酪氨酰丙氨酰亮氨酸H 2NC αHC βH 2C γH 2 -C –NH-CH-CONHCH 2COOHOCH 2SH (谷氨酸)γ(半胱氨酸)(甘氨酸)还原型谷胱甘肽(GSH )γGlu-Cys-GlyS SγGlu-Cys-Gly氧化型谷胱甘肽(GSSG )COOH蛋白质的结构层次蛋白质一级结构Sanger 1955成功地测定了胰岛素二条多肽链上氨一级结构是蛋白质功能多样性的基础蛋白质二级结构1.肽键中C-N 的键长0.132nm,介于C-N(0.147nm)与C=N(0.127nm),具有双键性1α-螺旋分为右手和左手两种螺旋氢键联系。
在α-螺旋体中每隔三个氨基酸残基可形成一个氢键,氢键是每个氨基酸残基上的N-H氢和它前面第四个残C=O氧之间形成的。
2、β-折叠(β-plated sheet)β-折叠结构中两个氨基酸残基之间的轴心距为3、β-转角(β-turn)4、无规则卷曲Ⅱ型β–转角的第三个残基总是Gly超二级结构结构域蛋白质三级结构三级结构蛋白质四级结构维持蛋白质空间结构作用力4、范德华引力:是分子间弱的作用力。
蛋白质结构与功能的关系第六节蛋白质的重要性质1.为什么蛋白质的水溶液是一种比较稳定的亲水胶体?其原因有二: 2.蛋白质沉淀蛋白质盐溶与盐析现象:有机溶剂3. 蛋白质的两性解离和等电点电泳现象 4. 蛋白质变性与复性引起蛋白质变性的因素:5. 蛋白质的呈色反应Folin-酚试剂反应 米伦反应(Millon reaction):蛋白质溶液5. 蛋白质紫外吸收:第七节蛋白质分离提纯的一般原则一般原则:蛋白质在细胞中以复杂的混合物1. 根据分子量大小不同的分离方法2.利用溶解度差别的分离方法3. 根据电荷不同的分离方法电泳法4.根据生物学特异性的分离方法蛋白质分子量的测定分子量(kD)肽链数目残基数目沉降系数(S):物质颗粒在单位离心场中的沉淀速度为恒定值1 S=1×10-13srRNA。
氨基酸基本的理化性质
活性类型
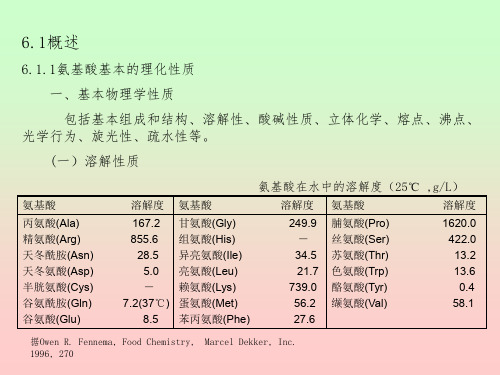
抗菌肽 枯草菌素 乳酸链球菌素 Lactocin S 橡胶素 神经肽 脑啡肽 α -内啡肽 强啡肽 韩蛙皮素 激素肽及激素调节肽 催产素 促肾上腺皮质激素 加压素 Amylin 免疫活性肽 α -干扰素 白细胞介素-2 抗癌多肽 肿瘤坏死因子 环己肽
氨基酸数
未知 34 33 43
5 16 17 14
739.0 56.2 27.6
脯氨酸(Pro) 丝氨酸(Ser) 苏氨酸(Thr) 色氨酸(Trp) 酪氨酸(Tyr) 缬氨酸(Val)
1620.0 422.0 13.2 13.6 0.4 58.1
据Owen R. Fennema, Food Chemistry, Marcel Dekker, Inc. 1996, 270
(二)氨基酸的疏水性
氨基酸的疏水性,是影响氨基酸溶解行为的重要因素,也是影响蛋白 质和肽的物理化学性质(如结构、溶解度、结合脂肪的能力等)的重要因 素。
按照物理化学的原理,疏水性可被定义为:在相同的条件下,一种溶 于水中的溶质的自由能与溶于有机溶剂的相同溶质的自由能相比所超过的 数值。估计氨基酸侧链的相对疏水性的最直接、最简单的方法就是实验测 定氨基酸溶于水和溶于一种有机溶剂的自由能变化。
RCH2SCH2COOH
避免巯基氧 同上
苹果酸酐*****
R CH2 S CHCOOH CH2COOH
(250nm)
对汞代苯甲酸
R CH2SHg
COOH
测定巯基含量
官能团及反应
试剂和条件
产物
评价
含量
D.羟基 酯化
E.-SCH3(Met) 1.烷烃化
2.β -丙醇酸
N-乙基马来亚胺 DTNB******
食品营养与检测《氨基酸的理化性质》

内容总结
一、 两性解离及等电点。+H+。氨基酸能与许多重金属离子如Cu2、Co2、Mn2、Fe2等产生螯合物。氨基酸经高温或或细菌作用发生脱羧基 反响生成胺。变质的食物不能吃,其原因之一是氨基酸脱羧基的产物胺赋予食物不良的气味和毒性。氨基酸分子中有共轭双键而对紫外光有吸收作 用,最大吸收峰在 280 nm 附近,且光吸收强度与氨基酸浓度成正比。氨基酸与茚三酮水合物共热,可生成蓝紫色化合物,其最大吸收峰在570nm 处
O
NH2-CH-C +
H OH
甘氨酸
O
NH-CH-C
HH
OH
甘氨酸
-HOH
O
O
NH2-CH-C-N-CH-C
H
H H OH
肽键
甘氨酰甘氨酸
第三页,共八页。
氨基酸通过肽键形成的化合物称为肽。 • 两分子氨基酸缩合形成二肽 • 三分子氨基酸缩合那么形成三肽……以至高分子多
肽。肽键是蛋白质分子中氨基酸之间相互连接的根 本方式
一、 两性解离及等电点
氨基酸是两性电解质,其解离方式取决于所处溶液的酸碱度。
等电点〔pI〕 处于一定PH溶液时,氨基酸分子解离后所带正、负电荷相等时,溶液 的pH值称为该氨基酸的等电点。
第一页,共八页。
R CH COOH +OH-
NH3+
+H+
酸性
pH=pI
中性
第二页,共八页。
+OH+H+
碱性
2 成肽反响
第八页,共八页。
第四页,共八页。
3 与金属离子的螯合作用
• 氨基酸能与许多重金属离子如Cu2、Co2、Mn2、Fe2等产生螯合物
氨基酸的理化性质

氨基酸的理化性质
一、两性解离及等电点
➢定义:氨基酸是两性电解质,其解离程度取决于所处溶液的酸碱度。
➢等电点(pI):在某一pH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性。
此时溶液的pH 值称为该氨基酸的等电点。
➢等电点计算:
➢备注:pI值等于两性离子两边pK值之和的平均值。
➢溶液的pH偏离pI越远,氨基酸带净电荷越多,在电场中越容易分离。
➢pI时氨基酸溶解度最小,容易聚集沉淀。
二、光学性质
1.旋光性:除甘氨酸外,其他氨基酸有不对称C原子,可以用旋光仪测定其旋光性。
➢左旋:Ser、Leu、Pro、Trp、Phe等。
➢右旋:Ala、Ile、Glu、Asp、Val、Lys、Arg等。
2.光吸收:R基团含有芳香环共轭双键系统的色氨酸、酪氨酸、苯丙氨酸,在近紫外区(220—300nm)有光吸收,其最大光吸收(λmax)分别为279nm,278nm和259nm。
蛋白质由于含有这些氨基酸,一般最大光吸收在280nm波长处,因此能利用紫外分光光度法很方便的测定蛋白质含量。
三、重要化学反应
1.茚三酮反应:在ph5-7和80—100°条件下,氨基酸与茚三酮可生成蓝紫色化合物,其最大吸收峰在570nm处。
常作为氨基酸定量分析方法。
脯氨酸或羟脯氨酸与茚三酮生成黄色化合物。
此反应经常用于氨基酸的定性和定量分析。
第一章氨基酸

第一章氨基酸(amino acid)的结构与性质第一节氨基酸的结构与分类一、氨基酸的结构组成蛋白质的基本单位是氨基酸。
如将天然的蛋白质完全水解,最后都可得到约二十种不同的氨基酸。
从氨基酸的结构通式可以看出:构成蛋白质的氨基酸均为L—α—氨基酸。
除R 为H(甘氨酸)外,其余氨基酸均具有旋光性。
*在空间各原子有两种排列方式:L—构型与D—构型,它们的关系就像左右手的关系,互为镜像关系,下图以丙氨酸为例:二、氨基酸的分类:1.按氨基酸分子中羧基与氨基的数目分:酸性氨基酸:一氨基二羧基氨基酸,有天冬氨酸、谷氨酸;碱性氨基酸:二氨基一羧基氨基酸,有赖氨酸、精氨酸、组氨酸;中性氨基酸:一氨基一羧基氨基酸,有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸。
2.按侧基R 基的结构特点分:脂肪族氨基酸芳香族氨基酸:苯丙氨酸、色氨酸、酪氨酸杂环氨基酸:脯氨酸、组氨酸3.按侧基R 基与水的关系分:非极性氨基酸:有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸;极性不带电氨基酸:天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸;极性带电氨基酸:天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸。
4. 按氨基酸是否能在人体内合成分:必需氨基酸:指人体内不能合成的氨基酸,必须从食物中摄取,有八种:赖氨酸、色氨酸、甲硫氨酸、笨丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苏氨酸。
非必需氨基酸:指人体内可以合成的氨基酸。
有十种。
半必需氨基酸:指人体内可以合成但合成量不能满足人体需要(特别是婴幼儿时期)的氨基酸,有两种:组氨酸、精氨酸。
三、稀有氨基酸:参加天然蛋白质分子组成的氨基酸,除了上述20 种有遗传密码的基本氨基酸之外,在少数蛋白质分子中还有一些不常见的氨基酸,称为稀有氨基酸。
它们都是在蛋白质分子合成之后,由相应的常见氨基酸分子经酶促化学修饰而成的衍生物。
氨基酸的分类和重要的理化性质

N NH
酸性氨基酸
天冬氨酸 Aspartate
O H 2 N CH C OH
CH 2 CO OH
酸性氨基酸
天冬氨酸 Aspartate 谷氨酸 Glutamate
O H 2 N CH C OH
CH 2 CH 2 CO OH
含羟基氨基酸
丝氨酸 Serine
O H 2N CH C OH
CH 2 OH
(
2、氨基酸的化学性质
1
)
-氨基参与的反应
与
亚
NH2
硝 R-CH-COOH+HNO2
O H R -C H -C O O H +N 2+H 2O
酸
反 用途:范斯来克法定量测定氨基酸及蛋白质水解程度 应 的基本反应。
反( 应2
) 与 甲 醛 发 生 羟 甲 基 化
氨基酸的化学性质
-氨基参与的反应
COO-
( 4
氨基酸的化学性质
)
-羧基参与的反应
脱 羧
1
反
N H 3 +
应
RC H C O O -
R C H 2N H 2+H ++C O 2
用途:酶催化的反应。
(
氨基酸的化学性质
5 )
-羧基参与的反应
成
氨基酸与碱作用生成相应的盐。氨基
盐 酸的碱金属盐能溶于水,而重金属盐则
反 不溶于水。
应
.
媛媛老师,祝您: 教师 节快乐,天天快乐! O(∩_∩)O~~
CH3
脂肪族氨基酸
甘氨酸 丙氨酸 缬氨酸
Glycine Alanine Valine
O H 2N CH C OH
各种氨基酸理化性质-20101202.

三、氨基酸的理化性质
氨基酸通式是H2NCHRCOOH。根据氨基连结在羧酸中碳原子的位置,可分 为α、β、γ、δ……的氨基酸( C……C―C―C―C―COOH)。
由于结构相似,具有一些共同的性质。它们都是无色结晶;熔点约在230℃以 上,大多没有确切的熔点,熔融时分解并放出CO2;都能溶于强酸和强碱溶液 中,除胱氨酸、酪氨酸、二碘甲状腺素外,均溶于水;除脯氨酸和羟脯氨酸外 ,均难溶于乙醇和乙醚
氨基酸基础知识
极性中性氨基酸:色氨酸、酪氨酸、丝氨酸、半胱氨酸、蛋氨酸(甲硫氨酸)
、天冬酰胺、谷氨酰胺、苏氨酸
酸性氨基酸:天冬氨酸、谷氨酸 碱性氨基酸:赖氨酸、精氨酸、组氨酸
其中:属于芳香族氨基酸的是:色氨酸、酪氨酸、苯丙氨酸 属于亚氨基酸的是:脯氨酸 含硫氨基酸包括:半胱氨酸、蛋氨酸(甲硫氨酸) 注意:在识记时可以只记第一个字,如碱性氨基酸包括:赖精组
工艺培训 邬斌
2010年12月1日
目 录
氨基酸基础知识
各种氨基酸性质
氨基酸基础知识
一、氨基酸的定义
氨基酸:含有氨基(―NH2 )和羧基(―COOH),并且氨基和羧基都直 接连接在一个-CH-结构上的一类有机化合物的通称。生物功能大分子蛋白质的 基本组成单位,是构成动物营养所需蛋白质的基本物质。
二、氨基酸的分类
物理性质:本品为白色结晶或结晶性粉末;无臭,味微甜而后苦 ;在水中
溶解,在乙醇中几乎不溶;等电点6.00。
化学性质:具有氨基酸的通性。 生产工艺: 目前,L-缬氨酸的生产方法有提取法、合成ቤተ መጻሕፍቲ ባይዱ、发酵法等。
1.提取法:动物血粉、蚕蛹及毛发水解液中L-缬氨酸的含量较高,从动物血粉 和蚕蛹水解液中,应用离子交换技术从混合氨基酸中分离L-缬氨酸,分离的效率高 ,提取操作简单,生产周期短,但成本高,不适合现代化大工业生产猪血粉中提 取L-缬氨酸的回收率为14.7%;蚕蛹水解液中分离L-缬氨酸,回收率为23.68%
氨酸物质理化性质

氨酸物质理化性质
氨酸简介
氨酸是一种重要的氨基酸,它是构成蛋白质的基本组成单元之一。
氨酸具有特殊的理化性质,本文将从分子结构、溶解性和酸碱
性等方面介绍氨酸的理化性质。
分子结构
氨酸的分子式为C3H7NO2,含有一个氨基(-NH2)和一个羧基(-COOH)。
氨基酸的分子结构使其具有极性和亲水性,可溶于水和其他极性溶剂。
溶解性
氨酸是可溶于水的。
当氨酸溶于水时,其分子会与水分子发生
氢键作用,形成溶液。
氨酸在水中的溶解度受温度和pH值的影响,其溶解度随温度升高而增加。
此外,氨基酸还可与其他极性或有机
溶剂发生溶解。
酸碱性
氨酸是一种兼具酸性和碱性的氨基酸,具有缓冲作用。
在中性条件下,氨酸的羧基会失去一个质子,呈酸性。
而在碱性条件下,氨基会接受一个质子,呈碱性。
氨酸的等电点(pI)在pH约为6的时候,此时其带电物质最少,呈中性。
总结
氨酸作为重要的氨基酸,具有独特的理化性质。
它的分子结构使其具有极性和亲水性,可溶于水和其他极性溶剂。
氨酸还具有酸碱性,在不同的pH值条件下呈现酸性或碱性。
对于进一步研究氨酸的应用和化学反应机理有重要意义。
参考文献
- [参考文献1]
- [参考文献2]
- [参考文献3]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三、氨基酸的理化性质
2、氨基酸的两性解离
1、两性离子(dipolarrion,dipolar
利用滴定曲线计算氨基酸的等电点等电点
侧链R基不解离的中性氨基酸(有两个解离基团)
丙氨酸缬氨酸
1.氨基酸的光学异构体
NH
2
氨基酸的重要化学反应
茚三酮反应(ninhydrin reaction):α-
H
艾德曼反应(Edman 艾德曼反应(Edman
肽键(peptide bond)
的化合物。
二肽(dipeptide);寡肽丝氨酰甘氨酰酪氨酰丙氨酰亮氨酸
H 2NC αHC βH 2C γH 2 -C –NH-CH-CONHCH 2COOH
O
CH 2SH (谷氨酸)γ
(半胱氨酸)
(甘氨酸)
还原型谷胱甘肽(GSH )
γGlu-Cys-Gly
S S
γGlu-Cys-Gly
氧化型谷胱甘肽(GSSG )
COOH
蛋白质的结构层次
蛋白质一级结构
Sanger 1955成功地测定了胰岛素二条多肽链上氨一级结构是蛋白质功能多样性的基础
蛋白质二级结构
1.
肽键中C-N 的键长0.132nm,介于C-N
(0.147nm)与C=N(0.127nm),具有双键性
1
α-螺旋分为右手和左手两种螺旋
氢键联系。
在α-螺旋体中每隔三个氨基酸残基可
形成一个氢键,氢键是每个氨基酸残基上的N-H氢和它前面第四个残
C=O氧之间形成的。
2、β-折叠(β-plated sheet)
β-折叠结构中两个氨基酸残基之间的轴心距为
3、β-转角(β-turn)
4、无规则卷曲Ⅱ型β–转角的第三个残基总是Gly
超二级结构
结构域
蛋白质三级结构
三级结构
蛋白质四级结构
维持蛋白质空间结构作用力
4、范德华引力:是分子间弱的作用力。
蛋白质结构与功能的关系第六节蛋白质的重要性质
1.
为什么蛋白质的水溶液是一种比较稳定的
亲水胶体?其原因有二: 2.蛋白质沉淀
蛋白质盐溶与盐析现象:
有机溶剂
3. 蛋白质的两性解离和等电点
电泳现象 4. 蛋白质变性与复性
引起蛋白质变性的因素:
5. 蛋白质的呈色反应
Folin-酚试剂反应 米伦反应(Millon reaction):蛋白质溶液
5. 蛋白质紫外吸收:第七节蛋白质分离提纯的一般原则
一般原则:蛋白质在细胞中以复杂的混合物
1. 根据分子量大小不同的分离方法
2.利用溶解度差别的分离方法
3. 根据电荷不同的分离方法
电泳法
4.根据生物学特异性的分离方法
蛋白质分子量的测定
分子量(kD)
肽链数目
残基数目
沉降系数(S):物质颗粒在单位离心场中
的沉淀速度为恒定值1 S=1×10-13s
rRNA。
