批生产指令单(包装)
批生产记录的制定填写存档及变更的标准操作程序

批生产记录的制定填写存档及变更的标准操作程序批生产记录的制定、填写、存档及变更的标准操作程序一、目的:建立一个批生产记录的制定、填写、存档及变更的标准操作程序程序,使之规范化。
二、适用范围:适用于生产车间所有批生产记录。
三、责任者:班组长、质量监督员、操作工。
四、程序:1 批生产记录的格式由车间主任根据产品的工艺规程制定,生产部负责人审核后,由总经理审核批准,最后由生产部印发执行。
2批生产记录随生产工艺规程一同下发到相关岗位。
由各岗位操作工人负责填写,具体填写时要注意以下几点:2.1 内容真实,记录及时,不得提前或滞后填写。
2.2 字迹端正清晰,不得用铅笔或圆珠笔填写。
2.3 不得撕毁或任意涂改,需要更改时,应划去后在旁边重写,签名并标明日期。
2.4 按表格内容填写齐全,不得留有空格,如无内容填写时要用“——”表示,以证明不是填写者疏忽。
内容与上项相同时应重新抄写,不得用“″”或“同上”表示。
2.5 品名不得简写,应按标准名称填写。
2.6 与其他岗位有关的操作记录应做到一致性、连贯性。
2.7 操作者、复核者均应填全名,不得只写姓或名。
2.8 填写日期一律横写,并不得简写,例如 2010 年 04 月 06 日不得写成“2010/4/6”,“2010/6/4”。
2.9 有数字计算的数据填写,根据工艺要求,采取“四舍六入五留双”的原则省略多余数字。
3 每批产品生产完毕后,其记录由班组长汇总,并检查是否收集齐全,填写完整。
生产部负责人审核后再交品管部负责人审核,审核无误后再交回生产部。
4 批生产记录由生产部班组长按批号装订成册交公司档案室归档保存,保存至保健品失效期后一年,未规定保健品失效期的批记录至少保存三年。
批生产记录如由于生产工艺变更等原因而要求变更,按本文件第1条进行。
五、批生产记录和原始记录管理规程1 内容和要求:1.1 批生产记录和原始记录是保健品生产、质量保证和经济活动情况的直接反映,是企业管理的重要内容和基础工作。
批生产记录、批包装记录管理规程
1.目的:建立生产记录的编制、填写、审核和保管的规程。
2.范围:一切与生产有关的原始记录、报告单、台帐、凭证。
3.责任:生产部、质量部、供储部、销售部、各生产车间。
4.内容:4.1.编制生产记录的要求:4.1.1.每批药品均应有相应的批生产记录,可追溯该批药品的生产历史以及与质量有关的情况。
4.1.2.批生产记录应依据现行批准的工艺规程的相关内容制定。
记录的设计应避免填写差错。
批生产记录的每一页应标注药品的名称、规格和生产批号。
4.1.3.原版空白的批生产记录应经过生产管理负责人和质量管理负责人的审核和批准,并签注姓名和日期。
批生产记录的复制和发放均应按照批准的书面程序进行控制并记录,每批药品的生产只能发放一份原版空白批生产记录的复制件。
4.1.4.生产开始前应进行检查,确保设备和工作场所没有上批遗留的产品、文件或与本批产品生产无关的物料,设备处于已清洁及待用状态。
检查情况应有记录。
4.1.5.在生产过程中,每项操作进行时应及时记录,操作结束后,应由生产操作负责人确认并签注姓名和日期。
4.2.批生产记录的内容应包括:4.2.1.产品名称、规格、生产批号;4.2.2.生产以及中间工序开始、结束的日期和时间;4.2.3. 每一生产工序的负责人签字;4.2.4.生产步骤操作人员的签名,必要时,还应有操作(如称量)复核人员的签名;4.2.5.每一原辅料的批号以及实际称量的数量(包括投入的,回收或返工处理产品的批号及数量)4.2.6.所有相关生产操作或活动、工艺参数及控制范围,以及所用主要生产设备的编号;4.2.7.中间控制和所得的结果的记录以及操作人员的签名;4.2.8.不同生产工序的产量及必要的物料平衡计算;4.2.9特殊问题的记录,包括对偏离生产工艺规程的偏差情况的详细说明或调查报告,并经签字批准。
4.3.编制批包装记录的要求:4.3.1.每批产品或每批产品中部分产品的包装,都应有相应的批包装记录,可追溯该批药品的包装操作以及与质量有关的情况。
中药饮片——包装批生产记
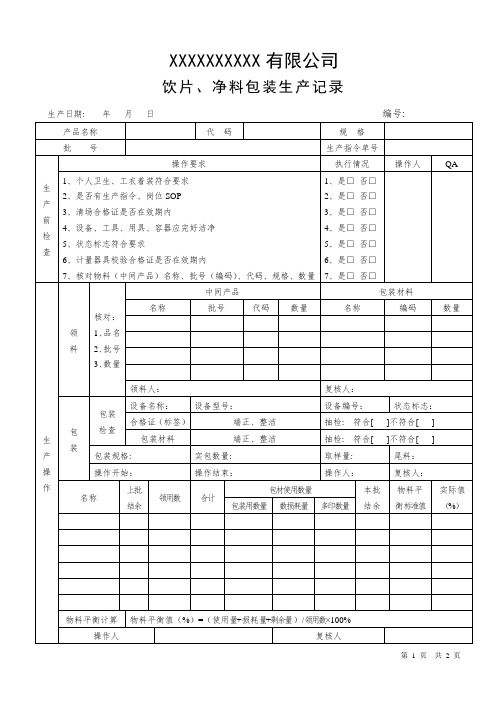
饮片、净料包装生产记录
生产日期:年月日编号:
产品名称
代码
规格
批号
生产指令单号
生
产
前
检
查
操作要求
执行情况
操作人
QA
1、个人卫生、工衣着装符合要求
2、是否有生产指令、岗位SOP
3、清场合格证是否在效期内
4、设备、工具、用具、容器应完好洁净
5、状态标志符合要求
6、计量器具校验合格证是否在效期内
操作人
复核人
XXXXXXXXXX有限公司
饮片、净料包装生产记录
生产日期:年月日编号:
产品(kg)
入库时间
入库人:
复核人:
入库数量(kg)
入库时间
入库人:
复核人:
入库数量(kg)
入库时间
入库人:
复核人:
合计
合计人:
复核人:
收率计算
物料平衡标准
标准值
实际值
结论
内包物料平衡公式
端正、整洁
抽检:符合[ ]不符合[ ]
包装材料
端正、整洁
抽检:符合[ ]不符合[ ]
包装规格:
实包数量:
取样量:
尾料:
操作开始:
操作结束:
操作人:
复核人:
名称
上批结余
领用数
合计
包材使用数量
本批结余
物料平衡标准值
实际值(%)
包装用数量
数损耗量
多印数量
物料平衡计算
物料平衡值(%)=(使用量+损耗量+剩余量)/领用数×100%
内包工序物料平衡(%)=(合格品数量+废弃数量+取样量)/投料量(半成品)×100%
生产指令工单
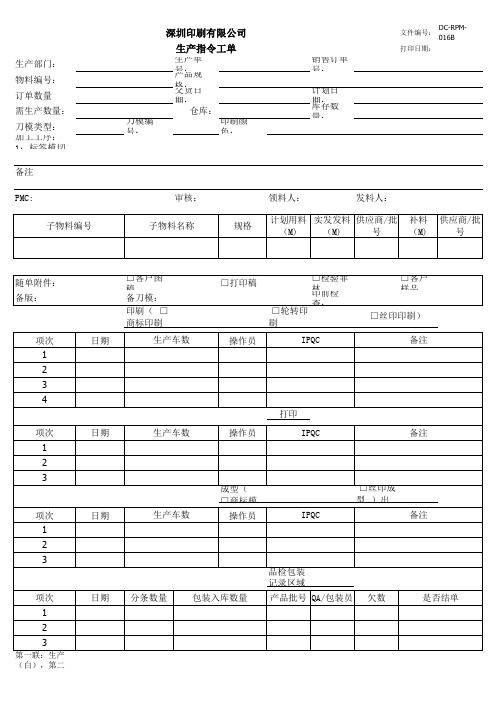
备注
PMC:
子物料编号
刀模编 号:
深圳印刷有限公司
生产指令工单 生产单 号产:品规 格交:货日 期:
仓库: 印刷颜 色:Fra bibliotek销售订单 号:
计划日 期 库: 存数 量:
文件编号:
DC-RPM016B
打印日期:
审核: 子物料名称
操作员
IPQC
□客户 样品
□丝印印刷)
备注
日期
生产车数
操作员
打印 IPQC
备注
日期
生产车数
成型( □商标模
操作员
IPQC
□丝印成 型 )出
备注
日期 分条数量
包装入库数量
品检包装 记录区域
产品批号 QA/包装员
欠数
是否结单
领料人:
发料人:
规格
计划用料 实发发料 供应商/批 补料 供应商/批
(M)
(M)
号
(M)
号
随单附件: 备版:
项次 1 2 3 4
项次 1 2 3
项次 1 2 3
项次 1 2 3
第一联:生产 (白),第二
日期
□客户图 稿 备刀模: 印刷( □ 商标印刷
生产车数
□打印稿
□检验菲 林 印前检 查: □轮转印 刷
感冒清热颗粒批生产指令及记录

生产车间:制剂车间1. 工艺操作:执行感冒清热颗粒工艺规程SOP-SC-4003-02。
2. 限额物料:按批领用量领取本批所需物料。
指令下达人:批准人:日期:年月日6. 干燥:将湿颗粒放入沸腾制粒机中烘干,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
7. 完工清场:开始时间:结束时间:感冒清热颗粒制剂批生产记录二、感冒清热颗粒混合工序批生产记录1. 工前准备2. 整粒:用快速整粒机整粒,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
3. 总混:用三维运动混合机混匀,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
注:半成品检验报告单附后4. 完工清场:开始时间:结束时间:感冒清热颗粒批包装指令1. 工艺操作执行感冒清热颗粒工艺规程SOP-SC-4003-02。
2. 工作标准指令下达人:批准人:日期:年月日感冒清热颗粒制剂批包装记录颗粒分装装量抽检称量记录产品名称:批号:设备名称:全自动颗粒包装机设备编号:SC0710190 每15分钟抽检一次感冒清热颗粒制剂批包装记录二、感冒清热颗粒外包装工序批包装记录1. 工前准备2. 包装材料领取及喷码记录2.1根据批包装指令,领取相应的包装材料。
2.2在小盒及外箱上喷上批号、有效期至,操作执行《外包装岗位标准操作规程》SOP–SC-1008-02。
3. 装小盒:将数好的药品﹑说明书装入小盒中,执行《外包装岗位标准操作规程》。
4. 装箱:按规定将小盒、合格证装入纸箱,执行《外包装岗位标准操作规程》。
5. 打包:按规定,将包装完毕纸箱打包,执行《外包装岗位标准操作规程》。
工序负责人:日期:年月日6.销毁:本批报废销毁包装材料,操作执行《标签及类标签物管理规程》SMP-WL-1016-02。
成品记录表感冒清热颗粒批包装指令1. 工艺操作执行感冒清热颗粒工艺规程SOP-SC-4003-02。
2. 工作标准指令下达人:批准人:日期:年月日感冒清热颗粒制剂批包装记录颗粒分装装量抽检称量记录产品名称:批号:设备名称:全自动颗粒包装机设备编号:SC0710190 每15分钟抽检一次感冒清热颗粒制剂批包装记录二、感冒清热颗粒外包装工序批包装记录1. 工前准备2. 包装材料领取及喷码记录2.1根据批包装指令,领取相应的包装材料。
片剂批生产记录表格模板

片剂批生产记录
产品名称
批号
成品量
生产周期:车间审核意见
规格
理论量
包装规格
********有限公司
月日至年月
审核人审核日期
日期
领料人
领料单
保管人
批生产指令单
起草人审核人接收人
称量配料岗位生产记录
年月曰
物料核对记录年月曰
清场记录
年月曰
原产品名称: 批 号: 调换产品名称: 批 号: 清场人: 质监员:
清场日期:年月日时 有效期至:年月日时
备注
清场人:
质监员:
清场合格证(正本)
M-J
>
岗
位:
称量配料
粉碎岗位生产记录
产品名称生产日期规格
清场记录
年月日
混合制粒干燥岗位生产记录
年月曰产品名称规格
清场记录
年月曰
整理总混岗位生产记录
年月曰
清场记录
年月曰
清场人:质监员:
填充装囊岗位生产记录
年月日
清场记录
年月日
领料单
保管人:
退料单
日期:年月日
退料人:
塑瓶内包装岗位生产记录
年月日
清场记录
年月日。
产品生产指令单

② 所有设备应有“完好”证、“已清洁”状态标示; ③ 所有物料应有“物料卡”、半成品(中间体)应有“流转证”;
④ 严格执行各岗位操作法、设备操作规程;
制表:
⑤ 严格执行洁净区操作规程。
审核 :
批准 :
产品名称 订单号码 产品批号 指令执行日期 接受部门 序号 物料编码
品名
XX有限公司
产品生产指令单
产品规格
成品编号
计划批量
指令工序
接受人
单位
需领用量
接受日期
备注
工艺要求: ① 严格按各工序标准操作法进行操作; ② 配制后进行中间体检验,不合格中间体不许流入下道工序; ③ 灌装后进行半成品检验,不合格半成品不许包装入库。
大容量注射剂批生产记录(包装)

合格证
ml
---------------
本厂刻签工序
说明书
ml
----------------
本厂刻签工序
工艺要求及操作方法
实际操作
1、检查有清场合格证、批包装指令、且设备完好,方可操作。
2、核对物料的品名、规格、数量与批包装指令无误。
检查结果:□合格□不合格
检查人:
3、贴签:核对标签与批包装指令无误,检查贴签的质量,标签倾斜度:目测外观,不得歪斜,没有白瓶流入下一工序。本批贴签结束,剩余的标签,污、损的标签交刻签人员,计数销毁。
不得少装,装箱时要注意,不得把瓶身上的标签碰烂,本批装箱完毕,
污、损的合格证及剩余的合格证交刻签人员记数销毁,清理现场卫生,
合格证与标签已核对□,每箱已放入一张合格证且无白瓶装箱□
有否剩余的合格证:□有,□没有
装箱员:
准备进行下一批的生产。
03:
04:
05:
06:
07:
08:
09:
10:
6、放说明书:核对说明书与标签的品名、规格、要一致,每箱放入一张说明书,放上盖板,合上盖,传给封箱机进行胶带封口,更换装箱的品种或规格时,剩余的说明书全部退回领用处。
7、封箱:核对纸箱的品名、规格及封箱打印的批号、生产日期、有效期要与标签上的一致,检查箱子二个侧面打印的字迹必须清楚并且一致。亚批的符号:01或02字迹必须清楚。
纸箱及封箱打印的已与标签核对□
箱子二个侧面打印的字迹清楚并且一致□。
封箱人:
8、二条包装线同时包装时,必须同时包装同一批号同一柜次的灭菌产品。
检查:执行正确□
检查人:
9、入库:将封箱后的产品码入周转车上,运输至仓库,包装完毕与仓库人员清点本批入库数。
感冒清热颗粒批生产指令及记录
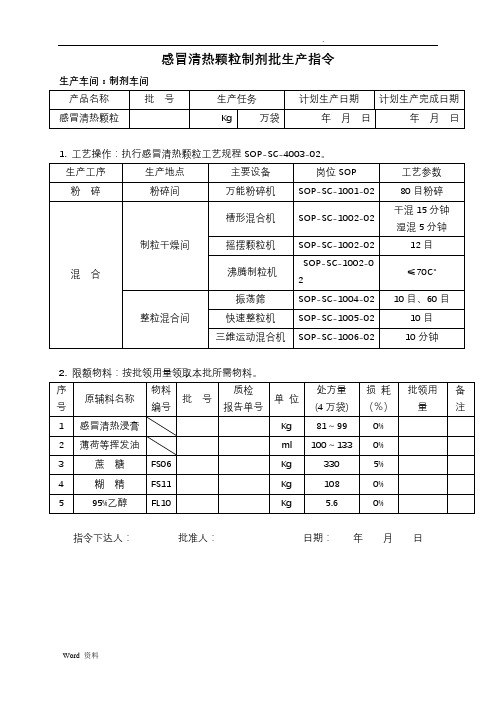
感冒清热颗粒制剂批生产指令生产车间:制剂车间1. 工艺操作:执行感冒清热颗粒工艺规程SOP-SC-4003-02。
2. 限额物料:按批领用量领取本批所需物料。
指令下达人:批准人:日期:年月日感冒清热颗粒制剂批生产记录操作规程》SOP–SC-1001-02。
3. 粉碎:操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
5. 混合﹑制粒:操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
6. 干燥:将湿颗粒放入沸腾制粒机中烘干,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
7. 完工清场:开始时间:结束时间:感冒清热颗粒制剂批生产记录二、感冒清热颗粒混合工序批生产记录1. 工前准备2. 整粒:用快速整粒机整粒,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
3. 总混:用三维运动混合机混匀,操作执行《制粒岗位标准操作规程》SOP–SC-1002-02。
注:半成品检验报告单附后4. 完工清场:开始时间:结束时间:感冒清热颗粒批包装指令1. 工艺操作执行感冒清热颗粒工艺规程SOP-SC-4003-02。
2. 工作标准指令下达人:批准人:日期:年月日感冒清热颗粒制剂批包装记录SOP–SC-1006-02。
颗粒分装装量抽检称量记录产品名称:批号:设备名称:全自动颗粒包装机设备编号:SC0710190 每15分钟抽检一次感冒清热颗粒制剂批包装记录二、感冒清热颗粒外包装工序批包装记录1. 工前准备2. 包装材料领取及喷码记录2.1根据批包装指令,领取相应的包装材料。
2.2在小盒及外箱上喷上批号、有效期至,操作执行《外包装岗位标准操作规程》SOP–SC-1008-02。
3. 装小盒:将数好的药品﹑说明书装入小盒中,执行《外包装岗位标准操作规程》。
4. 装箱:按规定将小盒、合格证装入纸箱,执行《外包装岗位标准操作规程》。
5. 打包:按规定,将包装完毕纸箱打包,执行《外包装岗位标准操作规程》。
GMP批生产指令发布与备料操作规程

页码:文件编号:生效日期: 再版日期:第1页/共2页SMP-PM-01012-1标准管理规程STANDARD MANAGEMENT PROCEDURESubject题目:批生产指令发布与备料操作规程Issued by颁发部门:质量部Written by起草人:Date日期:Dept. Head Approval 部门主管审核:Date日期:QA Director Approval QA 主管审核:Date日期:Approved by批准:Date日期:Dispense分发:生产部、质量部、供销部1.目的建立批生产指令发布与备料操作规程,使生产车间与仓库的领发料得以规范进行。
2.适用范围适用于本公司产品批生产指令发布与备料过程。
3.责任者仓库保管员、工艺员负责实施,车间主任、质量部QA主管、质量部负责人负责检查监督。
4.内容4.1.生产批指令的编制4.1.1.车间工艺员根据生产计划提前开具某一产品的批生产/配制指令单SRP-PM-030008;批包装指令SRP-PM-030009一式二份。
4.1.2.指令的内容:产品名称、规格、批量、批号;原辅材料/包装材料的名称、规格、需用量。
4.1.3.对原、辅材料/包装材料的要求在说明栏内清楚注明。
4.1.4.批生产/配制指令单由工艺员编制,车间主任审核签字后交质量部审核。
4.2.质量部审核程序4.2.1.质量部接到批生产/配制指令后,先由QA主管根据生产计划、产品工艺规程、所用原辅材料质量标准审核原辅材料是否检验合格,用量计算是否正确。
QA主管审核无误签字后交质量部负责人。
页码:文件编号:生效日期: 再版日期:第2页/共2页SMP-PM-01012-1标准管理规程STANDARD MANAGEMENT PROCEDURESubject题目:生产批指令发布与备料操作规程Issued by颁发部门:质量部4.2.2.质量部负责人审核后签字,将指令单送回生产部。
GMP批生产指令管理规程

页码:文件编号:生效日期: 再版日期:第1页/共2页SMP-PM-01009-1标准管理规程STANDARD MANAGEMENT PROCEDURESubject题目:批生产指令管理规程Issued by颁发部门:质量部Written by起草人:Date日期:Dept. Head Approval 部门主管审核:Date日期:QA Director Approval QA 主管审核:Date日期:Approved by批准:Date日期:Dispense分发:质量部、生产部1.目的通过批生产指令的监督、执行,保证均衡、规范生产。
2.适用范围适应于该批产品的管理。
3.职责3.1.生产部负责执行本规程。
3.2.质量负责监督本规程的执行。
4.内容4.1.批生产指令下达要求4.1.1.生产部须根据《生产计划》及商务部门临时要求,制订每批产品各生产车间的《批生产指令单》。
4.1.2.SMP-PM-01009-1-R-001《批生产指令单》中的产量根据设备能力合理制订,不能随意增加。
4.1.3.SMP-PM-01009-1-R-001《批生产指令单》,一式四份,生产部、生产车间、仓库、质量部各留存一份。
4.1.4.SMP-PM-01009-1-R-001《批生产指令单》须提前一天送至相应生产车间、物料仓库,以便相应部门有足够的时间做准备。
页码:文件编号:生效日期: 再版日期:第2页/共2页SMP-PM-01009-1标准管理规程STANDARD MANAGEMENT PROCEDURESubject题目:批生产指令管理规程Issued by颁发部门:质量部4.1.5.生产部根据SMP-PM-01009-1-R-001《批生产指令单》下达各SMP-PM-01009-1-R-002《工序生产指令单》和SMP-PM-01009-1-R-003《批包装指令单》给各工序,各工序严格按照《工序生产指令单》执行。
4.2.批生产指令执行要求4.2.1.生产部根据SMP-PM-01009-1-R-001《批生产指令单》,领取原辅材料。
生产指令单

生产订单号:客户白德生客户名称缅甸柚木g041 8,000要求交货日期交货日期产品编号wp1947 1.5 22背景色编号br-15压花编号r43滚筒编号内环尺寸od=33100包装规格纸箱规格其他要求部门项目生产时间完成时间消耗工时操作员实际生产数量不良产品类型、数量生产审批质量确认388部门项目生产时间完成时间工时消耗操作工实际生产数量不良产品类型,数量生产签署质量确认81部门项目生产时间、完工时间、工时、操作人员实际生产数量,不良品类型、数量、生产审批、质量确认、80个部门、项目生产时间、完工时间、工时、操作人员实际生产数量、不良产品类型、数量、生产批准、质量确认、f、质量确认16 swl-p-120713025订单号(订单数量(m)7月12日7月12日25、产品规格4-3厚度(mm)宽度(mm)成品号(带标识的零件m4909-1 m4909-2 NW(kg/体积)GW(kg/箱)生产机械需求(kg)异常情况描述,生产机器需求(体积)异常情况描述分析,生产设备需求(量)异常情况描述分析及异常情况描述分析生产设备需求分析(案例)异常情况描述分析表:沈兆芬审核人:黄伟审核人:生产订单号:客户帕特森客户品名缅甸柚木I015 10,000交货日期要求交货日期产品编号wp1947 1.5 22背景色br-15压花编号r43滚筒编号内环尺寸od=33100包装规格纸箱规格其他要求部门项目产品抽吸时间完成时间消耗工时操作员实际生产数量不良产品类型,批量生产批准质量确认483部门生产时间,完成时间,时间消耗,工时,实际生产数量,不良产品类型,数量生产批准,质量确认100部门项目生产时间,完成时间,消耗工时,操作员实际生产数量,不良产品类型、数量生产、质量确认20 swl-p-120905019订单号(订单号9月15日,产品规格3-3厚度(mm)宽度(mm)成品编号(带标识的零件4909-1 m4909-2净重(kg/卷)GW(kg/纸箱生产机需求(kg)异常说明,生产机械需求(数量)异常情况分析产品描述、生产机器需求(数量)异常分析、情况描述与分析生产机器需求(箱)异常情况描述与分析:沈兆芬审核员:黄伟批准人:生产指令是计划部下达到现场指导现场生产安排的报告。
批生产记录

中药饮片批生产记录
产品名称
产品代号产品规格
产品批号
成品数量
QA
车间主任
|
生产日期:
制定人/日期
审核人/日期
批准人/日期
泰州仁济中药饮片有限公司
批生产汇总表
填表人:
批生产包装指令单
产品名称:规格:产品代号:批号:批量:
中药饮片净制岗位生产记录
中药饮片洗润岗位生产记录
中药饮片煅制岗位生产记录
中药饮片切制岗位生产记录
中药饮片干燥岗位生产记录
中药饮片粉碎、过筛岗位生产记录
1/2
中药饮片蒸煮岗位生产记录
中药饮片炒制岗位生产记录
中药饮片炒制岗位生产记录
内包装岗位生产记录
外包装岗位生产记录
批生产记录确认记录
QA:生产部:车间主任:车间工艺员:#。
生产指令单

生产订单号:客户白德生客户名称缅甸柚木g041 8,纸箱内环生产日期要求每小时生产一次成品捆扎完成时间1个月,包装工要求每小时生产一个成品,每件产品包装一个月,一个月,一个月类型,数量生产批准质量确认388部门项目生产时间完成时间工时消耗操作员实际生产数量不良产品类型,数量生产签署质量确认81部门项目生产时间,完成时间,工作时间,操作人员实际生产数量,不良品类型、数量、生产批准、质量确认、80个部门、项目生产时间、完成时间、工作时间、操作人员实际生产数量、缺陷产品类型、数量、生产批准、质量确认、f、质量确认16 swl-p-120713025订单号(订单数量(m)7月7月12日12日25日,产品说明书4-3厚度(mm)宽度(mm)成品编号(带标识零件m4909-1 m4909-2 NW(kg/体积)GW(kg/箱)生产机械需求(kg)异常情况描述,生产设备需求(体积)异常情况描述分析情况描述分析和异常情况描述分析生产设备需求分析(案例)异常情况描述分析表:沈兆芬审核员:黄伟审核员:生产订单号:客户帕特森客户名称缅甸柚木I015 10000交货期要求交货期产品编号wp19471.5 22底色br-15压花编号r43滚筒编号内圈尺寸od=33100包装规格纸箱规格其他要求部门产品吸风时间完成时间消耗工时操作工实际生产数量不良产品类型,批生产批准质量确认483部门生产时间、完成时间、时间消耗、工时、实际生产数量、不良品类型、数量生产批准、质量确认100部门项目生产时间、完成时间、消耗工时、操作人员实际生产数量,不良产品类型、数量生产、质量确认20 swl-p-120905019订单号(订单号9月15日,产品规格3-3厚度(mm)宽度(mm)成品编号(标注零件4909-1 m4909-2净重(kg/卷)GW(kg/纸箱生产机需求(kg)异常说明,生产机械需求(数量)异常情况分析产品描述、生产机械需求(数量)异常分析、情况描述及生产机械需求分析(箱)异常情况描述与分析:沈兆芬审核员:黄伟批准:生产指令是计划部到达现场指导现场生产安排的报告。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
批包装指令单第页/共页
R-08-SC--002-03
待包装产品名称
规格
产品代码
产品批号
待包装产品数量
包装形式
计划包装数量
生产日期
(有效期)
有效期至
(箱)
执行产品工艺规程(编码:)
指令日期:年月日
包装日期:年月日至年月日
包装材料名称
代码
领料数量
(单位)
备注
备注:
起草人/日期
审核人/日期
批准人/日期
批生产指令单第页/共页
R-08-SC--001-03
产品名称
xxxxx注射液
规格
产品代码
产品批号
批量
5000L
内包装形式
执行产品工艺规程编码:()
指令日期:年月日
生产日期:年月日
处方(制成1000ml)
生产处方(制成5000L)
原辅料名称
数量
原辅料名称
代码
批准用量
备注:
原料折算:
起草
