水质碱度酸碱指示剂滴定法
水中碱度的测定

水中碱度的测定(酸碱滴定法)水的碱度是指水中所含能够接受质子的物质总量一、实验目的通过实验掌握水中碱度的测定方法,进一步掌握滴定终点的判断二.实验原理酸碱滴定法1)适应范围本方法适用于天然水,循环水及炉水中碱度的测定方法。
2)测定原理采用连续滴定方法测定水中的碱度.首先以酚酞为指示剂,用HNO3标准溶液滴定至终点溶液由红色变成无色,用量为P(mL);接着以甲基橙为指示剂,继续用同浓度的HNO3溶液滴定溶液由橙黄色变为橙红色,用量为M(mL)。
三、仪器与试剂1。
C(HNO3)=0.1000mol/L标准滴定溶液。
(配制与标定在实验(一)中已讲过,这里就不在重述)2.甲基橙指示剂:称取0.05g甲基橙溶于100ml蒸馏水中3.酚酞指示剂:称取0.5g酚酞溶于50mL 95%乙醇中,用水稀释至100mL4.酸式滴定管100mL 一支5.锥形瓶 250mL 三支6.移液管 100mL 一支7.无CO 2蒸馏水 四、实验步骤1、用移液管吸取两份水样和一份无CO 2蒸馏水各100mL,分别放入250mL 锥形瓶中,加入4滴酚酞指示剂,摇匀.2、若溶液呈红色,用0.1000mol/L HNO 3溶液滴定至刚好无色(可与无CO 2蒸馏水的锥形瓶作颜色比较)。
记录滴加的用量(P )。
若加入酚酞指示剂后溶液无色,则不需要用HNO 3溶液滴定。
按着下步骤操作.3、再于每瓶中加3滴甲基橙指示剂,摇匀。
4、分两种情况:其一若水样变成橘黄色,则继续用C HNO3=0.1000mol/L 标准液滴定至刚刚变成橙红色为止(可与无CO 2蒸馏水的锥形瓶颜色作比较),记用量(M ).其二如果加入甲基橙溶液后溶液变为橙红色,则不需要用HNO 3溶液滴定。
5.实验结果记录6.计算:总碱度(CaO 计,mg/L)=1000*V04.28*M P C )(总碱度(CaCO3计,mg/L)=1000*V05.50*MPC)(式中V—水样的体积,mL;C—硝酸标准滴定溶液的浓度,mol/L;P—滴定酚酞碱度时,消耗硝酸标准滴定溶液的体积,mL;M—滴定甲基橙碱度时,消耗硝酸标准滴定溶液的体积,mL;28。
水中碱度测定实验报告

一、实验目的1. 掌握水中碱度的测定方法。
2. 了解不同指示剂在不同pH值下的变色情况。
3. 熟悉酸碱滴定的原理和操作步骤。
二、实验原理水中碱度是指水中所含能与强酸发生中和作用的全部物质,即能接受质子H的物质的总量。
本实验采用酸碱滴定法测定水中碱度,以酚酞和甲基橙为指示剂,分别滴定水样中的OH-和CO32-。
三、实验仪器与试剂1. 仪器:酸式滴定管、锥形瓶、移液管、洗耳球、玻璃棒、烧杯、电子天平、pH 计、蒸馏水、标准HCl溶液(0.1000mol/L)、酚酞指示剂、甲基橙指示剂。
2. 试剂:酚酞指示剂(0.5g酚酞溶于50mL 95%乙醇中,用水稀释至100mL)、甲基橙指示剂(0.05g甲基橙溶于100mL蒸馏水中)、无CO2蒸馏水。
四、实验步骤1. 标准溶液的配制与标定(1)配制0.1000mol/L HCl标准溶液:称取3.65g HCl(分析纯),加入少量蒸馏水溶解,转移至1000mL容量瓶中,用水定容至刻度。
(2)标定HCl标准溶液:准确移取25.00mL HCl标准溶液于锥形瓶中,加入2滴酚酞指示剂,用0.1000mol/L NaOH标准溶液滴定至溶液呈微红色,记录消耗的NaOH体积。
2. 水样碱度的测定(1)取100mL水样于锥形瓶中,加入2滴酚酞指示剂,用HCl标准溶液滴定至溶液由红色变为无色,记录消耗的HCl体积P。
(2)继续加入2滴甲基橙指示剂,用HCl标准溶液滴定至溶液由橙黄色变为橙红色,记录消耗的HCl体积M。
五、实验结果与分析1. 计算水样碱度根据实验数据,计算水样碱度如下:OH-碱度= C(HCl) × P × 1000 / 1000CO32-碱度= C(HCl) × (M - P) × 1000 / 1000其中,C(HCl)为HCl标准溶液的浓度(mol/L),P和M分别为酚酞和甲基橙指示剂滴定所消耗的HCl体积(mL)。
水质碱度检测

水质碱度的测定1 主题内容与适用范围本方法适用于水样中碱度的测定。
2 原理用酚酞做指示剂,用标准酸溶液滴定水样,达到终点,所测得的碱度称为酚酞碱度,此时水样中所含全部氢氧根和二分之一碳酸根与酸化合。
在滴定酚酞碱度的水样中加入甲基橙指示剂,继续用标准酸溶液滴定达到终点时(包括酚酞碱度的用量),所测得的碱度称为甲基橙碱度,也称总碱度,此时水样中所含碳酸氢根全部被中和。
3 仪器及用具3.1 三角烧瓶:250mL;3.2 滴定管:50mL。
4 试剂4.1 盐酸标准溶液: 0.1mol/L。
4.2 酚酞指示剂: 10g/L的95%乙醇溶液。
4.3 甲基橙指示剂:1g/L的水溶液。
5 分析步骤5.1 酚酞碱度的测定(P-碱)量取100mL水样于三角烧瓶中,加三滴酚酞指示剂,若不显色,说明酚酞碱度为零,若显红色,用盐酸标准溶液滴定至红色刚好褪去为终点,记录盐酸标准溶液用量(V1)。
5.2 总碱度的测定(T-碱)在测定酚酞碱度后的水样中,再加入1滴甲基橙指示剂,继续用盐酸标准溶液滴定至刚好出现橙红色为终点。
记录下盐酸标准溶液的用量(包括酚酞碱度用量)V2。
6 计算c×V2酚酞碱度(meq/L) = ---------------100c×V3总碱度(meq/L) = ---------------100式中:c ---- 盐酸标准溶液浓度,mol/L;V2 --- 用酚酞指示剂时,滴定消耗盐酸标准溶液体积,mL;V3 ----- 用甲基橙指示剂后,滴定消耗盐酸标准溶液体积,mL。
注:设水中的碱度全部由氢氧化物、碳酸盐、重碳酸盐形成,并认为不存在其它弱无机酸和有机酸,并假定氢氧化物与重碳酸根不共存的条件下,水中氢氧化物、碳酸根、碳酸氢根的关系如下表毫克当量/升(meq/L)值100.08×÷2即为以碳酸钙计的毫克/升(mg/L)值。
1酸碱滴定法:碱度的测定
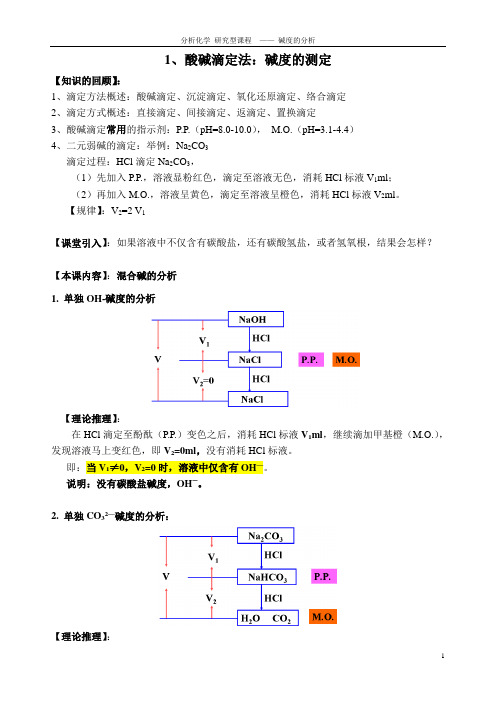
1、酸碱滴定法:碱度的测定【知识的回顾】:1、滴定方法概述:酸碱滴定、沉淀滴定、氧化还原滴定、络合滴定2、滴定方式概述:直接滴定、间接滴定、返滴定、置换滴定3、酸碱滴定常用的指示剂:P.P.(pH=8.0-10.0),M.O.(pH=3.1-4.4)4、二元弱碱的滴定:举例:Na2CO3滴定过程:HCl滴定Na2CO3,(1)先加入P.P.,溶液显粉红色,滴定至溶液无色,消耗HCl标液V1ml;(2)再加入M.O.,溶液呈黄色,滴定至溶液呈橙色,消耗HCl标液V2ml。
【规律】:V2=2 V1【课堂引入】:如果溶液中不仅含有碳酸盐,还有碳酸氢盐,或者氢氧根,结果会怎样?【本课内容】:混合碱的分析1. 单独OH-碱度的分析【理论推理】:在HCl滴定至酚酞(P.P.)变色之后,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),发现溶液马上变红色,即V2=0ml,没有消耗HCl标液。
即:当V1≠0,V2=0时,溶液中仅含有OH—。
说明:没有碳酸盐碱度,OH—。
2. 单独CO32—碱度的分析:【理论推理】:在HCl滴定至酚酞(P.P.)变色之后,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),滴定至溶液变红色,消耗HCl标液V2 ml,且V1=V2。
即:当V1=V2时,溶液中仅含有OH—。
说明:只有碳酸盐碱度,CO32—。
3. 单独HCO3—(重碳酸盐)碱度的分析:【理论推理】:向溶液中加入指示剂酚酞(P.P.),溶液不显粉红色,即消耗HCl标液V1=0ml,继续滴加甲基橙(M.O.),溶液呈现橙黄色,滴定至溶液变红色,消耗HCl标液V2 ml。
即:当V1=0,V2≠0时,溶液中仅含有HCO3—。
说明:只有碳酸盐碱度,HCO3—。
4. CO32—和HCO3—碱度的分析:【理论推理】:向溶液中加入指示剂酚酞(P.P.),溶液显粉红色,滴定至粉红色消失,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),溶液呈现橙黄色,滴定至溶液变红色,消耗HCl标液V2 ml。
碱度的测定

碱度的测定(酸碱滴定法)1.仪器(1)25mL酸式滴定管(2)5mL或10mL微量滴定管(3)250mL锥形瓶(4)100mL移液管2.试剂及配制(1)1%酚酞指示剂(以乙醇为溶剂)准确称取1g酚酞,溶于乙醇(95%),用乙醇(95%)稀释至100 ML。
(2)0.1%甲基橙指示剂准确称取 0.1g甲基橙,溶于70℃的水中,冷却,稀释至100mL。
(3)甲基红-亚甲基蓝指示剂:准确称取0.125g甲基红和0.085g亚甲基蓝,在研钵中研磨均匀后,溶于100mL95%乙醇中。
(4)c(1/2H2SO4)=0.1000mol/L、0.0500 mol/L、0.0100 mol/L标准溶液c(1/2H2SO4)=0.1000mol/L配制:量取3ml浓硫酸(密度1.84g/ml)缓缓注入1000mL蒸馏水或除盐水中,冷却、摇匀。
配制c(1/2H2SO4)=0.0500 mol/L、0.0100 mol/L硫酸标准溶液,用c(1/2H2SO4)=0.1000mol/L硫酸标准溶液稀释至2倍、10倍制得。
3. 测定方法(1)大碱度水样(如锅水、化学净水、冷却水、生水等)的测定方法:取100mL透明水样,置于250mL锥形瓶中,加入2~3滴酚酞指示剂,此时若溶液显红色,则用c(1/2H2SO4)=0.1000mol/L或0.0500 mol/L标准溶液滴定至恰无色,记录耗酸体积V1,然后再加入2滴甲基橙指示剂,继续用上述硫酸标准溶液滴定至溶液呈橙红色为止,记录第二次耗酸体积V2(不包括V1)。
(2)小碱度水样(如凝结水、高纯水、给水等)的测定方法:取100mL透明水样,置于250mL锥形瓶中,加入2~3滴酚酞指示剂,此时溶液若显红色,则用微量滴定管以c(1/2H2SO4)=0.0100 mol/L标准溶液滴定至恰无色,记录耗酸体积V1,然后再加入2滴甲基红-亚甲基蓝指示剂,再用上述硫酸标准溶液滴定,溶液绿色变为紫色,记录耗酸体积V2(不包括V1)(3)无酚酞碱度时的测定方法:上述两种方法,若加酚酞指示剂后溶液不显色,可直接加甲基橙或甲基红-亚甲基蓝指示剂,用硫酸标准溶液滴定,记录耗酸体积V2(4)碱度的计算上述被测定水样的酚酞碱度(JDp)和全碱度(JD)按下式计算:JDp= c(1/2H2SO4)×V1×10JD= c(1/2H2SO4)×V2×10式中:c(1/2H2SO4)----标准溶液浓度;V 1、V2两次滴定时所耗硫酸标准溶液的体积碱度的基本单元采用mol/L(毫摩尔/升)(5)将测定结果填入《化验记录表》中。
碱度的测定方法

碱度的测定方法
碱度是指溶液中存在的碱性物质的浓度或活性。
测定溶液的碱度可以使用多种方法,以下为一些常用的方法:
1. 酸碱滴定法:这是最常用的测定碱度的方法之一。
首先,用一种已知浓度的酸溶液滴定待测碱溶液,直到pH值达到中性(pH=7)。
根据已知酸溶液滴定的体积和浓度,可以计算出待测碱溶液的浓度。
2. pH计法:pH计是一种能够测量溶液酸碱性的仪器。
通过将电极浸入待测溶液中,pH计可以测量溶液的pH值。
根据pH 值可以判断溶液的酸碱性质,从而推测出溶液的碱度。
但是需要注意,pH计只能测量溶液的pH值,对于碱度的直接测定需要通过其他方法进行。
3. 酸碱指示剂法:酸碱指示剂是一种可以根据溶液的酸碱性质而发生颜色变化的物质。
在测定碱度时,可以将适量的酸碱指示剂添加到待测溶液中,根据颜色变化的出现来判断溶液的碱度。
4. 电位滴定法:电位滴定法是一种基于电位的测定方法,利用电位计对待测溶液进行电位测量。
通过准确测量酸碱反应过程中电位的变化,可以计算出溶液的碱度。
需要注意的是,不同的测定方法适用于不同的碱性物质和待测溶液的特性。
在选择测定方法时,应根据实际情况选择合适的方法,以确保测定结果的准确性。
[精彩]水质酸碱度的测定1
![[精彩]水质酸碱度的测定1](https://img.taocdn.com/s3/m/fbbb01c727fff705cc1755270722192e453658fe.png)
水质酸碱度的测定一、实验目的水的酸碱度是判断水质和废水处理控制的重要指标,本实验的目的是掌握碱度的检测方法:指示剂滴定法。
二、实验原理酸/碱度是指水中所含能与强碱/强酸发生中和作用的物质的总和,酸碱度和pH值既有区别又有联系。
酸碱指示剂滴定法:用标准的氢氧化钠/硫酸溶液滴定水样至一定pH 值,根据其所消耗的试剂量计算酸度/碱度。
通常分为两种酸度/碱度:一是用酚酞作指示剂(其变色pH 为8.3)测得的酸度称为酚酞酸度(总酸度)/碱度;二是用甲基橙作指示剂(变色pH 约4.3)测得的酸度称甲基橙酸度/碱度(总碱度)。
三、实验仪器、药品试剂实验仪器:电子天平、50mL酸式滴定管、250mL锥形瓶、铁架台、烧杯、洗瓶;药品试剂:除盐水、C1/2H2SO4约0.05mol/L、无水碳酸钠、甲基橙指示剂(1g/L)、溴甲酚绿-甲基红指示剂。
四、实验步骤1.C1/2H2SO4的标定:准确称量已在250℃下干燥过的4h基准无水碳酸钠0.11±0.001g,置于250mL锥形瓶中,计下实际称量的无水碳酸钠的质量m,加50mL除盐水溶解,再加2滴溴甲酚绿-甲基红指示剂,用硫酸溶液滴定至刚出现红色,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止,计下消耗的硫酸体积V。
C(1/2H2SO4)=m/0.05299×V式中:C(1/2H2SO4) ──硫酸标准滴定溶液的物质的量浓度,mol/L;m ──称量无水碳酸钠质量,g;V ──滴定用去硫酸溶液实际体积,mL;0.05299 ──与1.00mL硫酸标准滴定溶液C(1/2H2SO4)=1.000mol/L〕相当的以克表示的无水碳酸钠的质量。
2.取地表水样100mL于锥形瓶内,滴入两滴甲基橙指示剂,以标定后的C1/2H2SO4滴定至由黄色变为橙色即为终点,计下消耗的C1/2H2SO4体积V1;3.重复第2步再测两次,计下体积V2、V3;4.取自来水样重复步骤2和3,测得自来水消耗的C1/2H2SO4体积;五、数据处理以mmol/L表示总碱度A T,其计算公式如下:A T=V1*c*1000/V o式中:V1——滴定时消耗的C1/2H2SO4体积(mL);c ——C1/2H2SO4浓度(mol/L);V o——水样取样体积,这里是100mL。
碱度和硬度的测定原理

碱度和硬度的测定原理
碱度和硬度是水质检测中常用的参数。
下面是碱度和硬度的测定原理。
碱度的测定原理:
碱度反映了水中碱性物质的含量,常用指标是水中的碳酸盐硬度。
常见的测定方法有酚酞法和酸碱滴定法。
酚酞法:该方法通过酚酞指示剂的变色反应来测定水中的碱度。
首先,将酚酞指示剂加入待测水样中,逐滴加入盐酸溶液直到溶液转为红色。
通过计算所使用的盐酸溶液的体积,可以确定水样中的碱度。
酸碱滴定法:该方法通过滴定剂和酸碱指示剂的反应来测定水中的碱度。
首先,将滴定剂(例如盐酸或硝酸)滴入待测水样中,滴定至溶液的pH值达到指示剂的变色点。
通过计算所使用的滴定剂的体积,可以确定水样中的碱度。
硬度的测定原理:
硬度是水中钙和镁离子的含量,可以分为总硬度和临时硬度两种。
常见的测定方法有EDTA滴定法和复合指示剂法。
EDTA滴定法:该方法通过EDTA (乙二胺四乙酸)与水样中的钙、镁离子生成络合物的滴定反应来测定水中的硬度。
首先,将专用指示剂(例如二甲基黄)加入水样中,直到溶液转为蓝色。
然后,滴定EDTA溶液直至溶液由蓝色转变为粉红
色。
通过计算所使用的EDTA溶液的体积,可以确定水样中的硬度。
复合指示剂法:该方法将复合的指示剂(例如酞菁T)与水样中的钙、镁离子生成络合物的反应来测定水中的硬度。
复合指示剂可在不同硬度的水样中产生颜色的变化,根据颜色的变化可以确定水样中的硬度。
总的来说,碱度和硬度的测定原理基于滴定反应或指示剂的变色反应,通过计算所使用的试剂体积,可以确定水样中的碱度和硬度。
水中碱度测定方法

水中碱度测定方法嘿,朋友们!今天咱就来聊聊水中碱度测定方法这档子事儿。
你说这水啊,就像个神秘的盒子,里面藏着好多我们不知道的秘密呢,碱度就是其中之一。
那怎么才能知道水里碱度有多少呢?先来说说第一种方法,酸碱指示剂滴定法。
这就好比是一场赛跑,酸碱指示剂就是那个裁判,看着酸和碱在水里赛跑,啥时候颜色一变,咱就知道比赛结束啦!通过滴加酸液,看着指示剂颜色的变化,就能确定碱度啦。
这是不是挺有意思的呀?就好像我们看着一场精彩的比赛,等着决出胜负呢!还有一种方法叫电位滴定法,这个就有点高大上啦!就好像是给水里的碱度装上了一个超级敏锐的探测器,能精确地捕捉到每一点变化。
它可比我们的眼睛厉害多啦,能察觉到那些细微的反应,然后准确地告诉我们碱度的数值。
你想想,这多神奇呀!再说说比色法吧,这就像是给水里的碱度拍了张照片,然后通过和标准照片对比,就能知道碱度的情况啦。
这是不是有点像我们平时对比照片看自己美不美呀?哈哈!每种方法都有它的特点和适用场景呢!就像我们不同的人有不同的本领一样。
比如酸碱指示剂滴定法简单直观,电位滴定法精确可靠,比色法快速方便。
那我们在实际操作的时候,可就得根据具体情况来选择啦!要是随便乱用方法,那可不行哦,就像你不能穿着拖鞋去跑步比赛一样,那不得闹笑话嘛!我们在测定水中碱度的时候,可得细心再细心,就跟照顾小宝宝似的。
稍微不注意,可能结果就不准确啦!那可就白忙活一场咯。
而且啊,操作的时候一定要严格按照步骤来,一步都不能马虎。
这可不是开玩笑的呀,朋友们!总之呢,水中碱度测定方法有好几种,我们要了解它们的优缺点,根据实际情况选择合适的方法。
这样才能准确地知道水里碱度的情况,这对很多领域都非常重要呢!比如水处理、环境监测等等。
所以说呀,可别小瞧了这小小的碱度测定,它背后可有大学问呢!大家都记住了吗?。
总酸度及总碱度测试方法

总酸度及总碱度测试方法总酸度(Total acidity)和总碱度(Total alkalinity)是水质分析中常用的指标,用于描述水溶液中酸性和碱性物质的浓度和性质。
下面将介绍一些常见的总酸度和总碱度测试方法。
总酸度测试方法:1.pH滴定法:这是一种常见的总酸度测试方法。
首先将待测水样与指示剂(一般为溴酚蓝或溴酚绿)混合,然后用1M的NaOH溶液滴定到水样中,直到颜色发生可见变化。
通过记录所需的NaOH体积,可以计算出总酸度。
2.酸碱指示剂法:使用酸碱指示剂(如中性红或酚酞)来检测酸性水溶液。
这些指示剂在不同pH值下会显示不同的颜色。
通过将指示剂加入待测水样,并观察颜色的变化,可以判断总酸度的高低。
3.电位滴定法:这是一种精确的总酸度测试方法。
首先将待测水样与电极连接,然后在特定的条件下进行电位测量。
通过向水样中滴加标准化的酸溶液,直到pH值达到特定值时停止滴定。
通过记录消耗的酸溶液体积,可以计算出总酸度。
总碱度测试方法:1.酸碱度滴定法:将待测水样与酸碱指示剂混合,并滴加酸溶液直到溶液的颜色发生变化。
通过记录酸溶液的体积,可以计算出总碱度。
2.酸度滴定法:这是一种常见的总碱度测试方法。
将待测水样与缓冲溶液和指示剂混合,然后滴加酸溶液,直到颜色发生变化。
通过记录消耗的酸溶液体积,可以计算出总碱度。
3.粗滴定法:将待测水样与几滴试液混合,并不断搅拌。
通过观察溶液的颜色变化,可以粗略地估计总碱度的浓度。
需要注意的是,在使用这些方法进行总酸度和总碱度测试之前,应先标定所使用的试剂和仪器,以确保测试结果的准确性。
此外,不同的水质分析方法可能适用于不同类型的水样,因此需要根据实际情况选择合适的测试方法。
酸碱滴定法滴定碱度要点
酸碱滴定法滴定碱度要点一、实验时间、地点2012年10月11日第一工业中心二、实验目的1. 学会酸碱滴定法测定碱度;2. 巩固滴定操作和终点颜色的判断。
三、实验原理利用酸和碱在水中以质子转移反应为基础的滴定分析方法。
可用于测定酸、碱和两性物质。
其基本反应为H ﹢+OH ﹣=H2O 也称中和法,是一种利用酸碱反应进行容量分析的方法。
水样用酸标准溶液滴定至规定的pH 值,其终点可由加入的酸碱指示剂在该pH 值时颜色的变化来判断。
当滴定至酚酞指示剂由红色变为无色时,溶液pH 值即为8.3,指示水中氢氧根离子已被中和,碳酸盐均被转为重碳酸盐(HCO 3-),反应如下:OH -+H +→H 2O CO 3-+H +→HCO 3-深圳职业技术学院Shenzhen Polytechnic 项目实训(验)报告Training Item Report当滴定至甲基橙指示剂由橘黄色变成橘红色时,溶液的pH值为4.4~4.5,指示水中的重碳酸盐(包括原有的和碳酸盐转化成的重碳酸盐)已被中和,反应如下:HCO?-+H+→CO?↑+H?O根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量,可以计算出水中碳酸盐、重碳酸盐及总碱度。
上述计算方法不适用于污水及复杂体系中碳酸盐和重碳酸盐的计算。
四、实验内容分别取5中碱度水样于250ml锥形瓶中,分别滴入1-2滴酚酞试剂,溶液变成红色后,用浓度为0.1的盐水滴定至刚好褪色,记录滴定管中盐酸标准溶液用量V1。
向上述锥形瓶中加入甲基橙指示剂3滴,混匀;若水样变为桔黄色,继续用HCl标准溶液滴定,直至刚刚变为桔红色为止,记录盐酸标准溶液用量V2。
五、实验环境和器材1.酸式滴定管,25ml。
2.锥形瓶,250ml。
3.酚酞指示液:称取0.5g酚酞溶于50ml 95%乙醇中,用水稀释至100ml。
4.甲基橙指示剂:称取0.05g甲基橙溶于100ml蒸馏水中。
5.碱度水样1、碱度水样2、碱度水样3、碱度水样4、碱度水样5。
用颜色指示剂滴定法测定酸值和碱值的试验方法

用颜色指示剂滴定法测定酸值和碱值的试验方法
颜色指示剂滴定法是一种常用的测定酸值和碱值的试验方法。
具体操作步骤如下:
1. 准备试样:取一定量待测溶液样品,装入容量瓶中。
2. 酸度测定:取一定量的试样溶液,加入几滴酸性颜色指示剂(如酚酞),溶液会变成粉红色。
然后滴加标准酸溶液,同时轻轻搅拌溶液。
当溶液变成浅粉红色时,停止滴定。
记录滴加的标准酸溶液的体积V1。
3. 碱度测定:取一定量的试样溶液,加入几滴碱性颜色指示剂(如甲基橙),溶液会变成橙黄色。
然后滴加标准碱溶液,同时轻轻搅拌溶液。
当溶液变成浅橙黄色时,停止滴定。
记录滴加的标准碱溶液的体积V2。
4. 酸碱值计算:根据标准酸溶液和标准碱溶液的滴定体积V1
和V2,可以计算出待测溶液的酸碱值。
酸度值等于标准酸溶
液滴定体积V1乘以标准酸溶液的浓度,碱度值等于标准碱溶
液滴定体积V2乘以标准碱溶液的浓度。
需要注意的是,在进行滴定前要仔细选择合适的颜色指示剂,确保其颜色变化范围与待测溶液的酸碱范围相匹配。
另外,在滴定过程中,要轻轻搅拌溶液,确保滴加的标准溶液充分混合。
最后,记得记录标准溶液的浓度,以便计算待测溶液的酸碱值。
水质 总碱度的测定 全自动电位滴定法-2024标准

水质 总碱度的测定——全自动电位滴定法1 范围下列术语和定义适用于本文件2.1滴定终点titration 本文件规定了全自动电位滴定法测定水中总碱度的方法。
本文件适用于地浊度的水源水和生活饮用水中总碱度的测定。
2术语和定义endpoint溶液中被测水样pH 随滴定的过程变化而变化,当水样pH 为4.0时,此时定义为滴定终点。
3 方法原理测定水样碱度,玻璃电极为指示电极,饱和甘汞电极为参比电极,用酸标准溶液滴定,通过终点pH 或电位滴定仪指示。
当甲基橙为酸碱滴定终点指示剂时,甲基橙变色时的水样的pH 在4.3~4.5;当水样组分复杂时,可以降低pH 指示终点。
电位滴定法通过实时记录酸标准溶液消耗体积V 与水样pH 值之间关系,绘制滴定曲线。
之后,直接滴定到指定终点计算出相应组分含量。
4. 试剂和材料4.1纯水,GB/T6682,三级。
使用之前煮沸15 min ,冷却至室温,以除去其中溶解的二氧化碳。
4.2碳酸钠标准溶液(Na 2CO 3 ρ=0.025 mol/L )。
称取2.6498 g (250 ℃ 烘干4h )的无水碳酸钠,溶于少量纯水(4.1),定容至1000mL 容量瓶中,混匀待用。
4.3盐酸标准溶液(HCl ρ≈0.050 mol/L )移取4.0~4.5 mL 浓盐酸用纯水(4.1)稀释,定容至1000 mL 容量瓶中,混匀待用。
再移取25.00 mL 碳酸钠标准溶液于150 mL 搅拌杯中,加入25 mL 纯水(4.1)放入电位滴定台上,插入电极,启动电位滴定仪,用盐酸标准溶液滴定至终点。
当pH 为4.0时,电位滴定仪自动停止滴定,记录消耗体积,计算出盐酸标准溶液浓度:c (H +)= 25.00×0.0500V (1)c (H +)—— 盐酸标准溶液浓度(mol/L );V —— 盐酸标准溶液用量,单位为毫升(mL );5仪器和设备5.1自动电位滴定仪:pH 范围1.0~14.0,分辨率0.1 (包含温度自动补偿装置) 。
碱度的测定---酸碱滴定法

碱度的测定---酸碱滴定法碱度的测定---酸碱滴定法1、主题本文件规定了碱度测定的操作方法2、适用范围适用于锅炉水、冷却水和天然水等碱度的测定3、依据本规程依据GB/T 6276.1,1996 (使用范围)4、流程4.1吸取 4.2加入 4.3加2-3 4.4计算水样50ml酚酞3滴,滴甲基酚酞碱度=CV/V 1s至250ml若显红色橙,用盐*1000 锥形瓶内用盐酸滴酸标准溶全碱度=C(V+V)/V 12s? ? ? 至无色。
液滴至橘*1000 红色为终点。
5、内容5.1 方法提要水的碱度是指水中含有能够接受氢离子的物质的量,如:氢氧根、碳酸盐、重碳酸盐、磷酸盐、磷酸氢盐、硅酸盐、硅酸氢盐、亚硫酸盐、腐殖酸盐、氯等,都是水中的碱性物质,他们都与酸进行反应。
因此选用适宜的指示剂,以标准溶液对其进行滴定,便可测出水中碱度的含量。
碱度可分为酚酞碱度和全碱度两种。
酚酞碱度是以酚酞作指示剂测得的碱度,其终点PH值为8.3。
全碱度是以甲基橙作指示剂测得的碱度,其终点PH值为4.2。
若碱度很小时,全碱度宜用甲基红---亚甲基蓝作指示剂,终点的PH值为5.0。
5.2 试剂及配制5.2.1 0.1%的酚酞溶液:称取0.1g酚酞溶于50mL无水乙醇中,再加50mL蒸馏水。
5.2.2 0.1%的甲基橙溶液:称取0.1g甲基橙溶于100mL蒸馏水。
5.2.4 0.100mol/L HCL 、 0.050mol/L HCL 、 0.010mol/L HCL 标准溶液5.3 操作步骤5.3.1 大碱度水样(如:锅炉水、化学净水、冷却水、生水等)的测定:取100mL透明水样注入锥形瓶中,加2,3滴酚酞指示剂,此时若显红色,则用0.100mol/L HCL或0.050mol/L HCL标准溶液滴定至红色刚消失,记录盐酸用量V;然后再加入甲基橙指示剂2,3滴,继续滴定至由淡黄色变为橙色,记1 录用量V。
25.3.2 小碱度水样(如:凝结水、高纯水、给水等)的测定:取100mL透明水样注入锥形瓶中,加2,3滴酚酞指示剂,此时若显红色,则用0.100mol/L HCL标准溶液滴定至红色刚消失,记录盐酸用量V;然后再加1入甲基橙指示剂2,3滴,继续滴定至由淡黄色变为橙色,记录用量V; 25.3.3 无酚酞碱度的测定方法上述方法,若加入酚酞指示剂后溶液不显色,可直接加入甲基橙指示剂2,3滴,继续滴定至由淡黄色变为橙色,记录用量V; 25.4 计算公式酚酞碱度: (JD)酚=CV/V *1000 mmol/L 1s全碱度: (JD)全=C(V+V)/V *1000 mmol/L 12s式中: C --- HCL标准溶液浓度V ---水样的体积 s5.5允许误差取平均测定结果的算术平均值为测定结果,平均测定结果允许差为1.5mg/L。
水质碱度测定操作规程

水质碱度测定操作规程(酸碱滴定法)引用国标:GB/T15451方法提要水的碱度是指水中含有能接受氢离子的物质的量,例如氢氧根、碳酸盐、重碳酸盐、磷酸盐、磷酸氢盐、硅酸盐、硅酸氢盐、亚硫酸盐、腐植酸盐和氯等,都是水中常见的碱性物质,它们都与酸进行反应。
因此选用适宜的指示剂,以标准酸溶液对它们进行滴定,便可测出水中碱度的含量。
碱度可分为酚酞碱度和全碱度两种,酚酞碱度是以酚酞作指示剂时所测出的量,其终点的pH值为8.3全碱度是以甲基橙作指示剂时测出的终点pH值为4.2,若碱度很小时全碱度宜以甲基红—亚甲基蓝作指示剂,终点的pH值为5.0。
试剂及配制1、10g/L的酚酞酒精溶液:称取1g酚酞,溶于乙醇(95%),用乙醇(95%)稀释至100mL。
2、1g/L的甲基橙溶液:称取0.1g甲基橙,溶于70℃的水中,冷却,稀释至100mL。
3、甲基红亚甲基蓝指示剂:准确称取0.125g甲基红和0.085g亚甲基蓝在研钵中研磨均匀后,溶于100mL95%乙醇中。
4、0.10moL/LHCl、0.050moL/LHCl、0.010moL/LHCl标准溶液。
操作步骤1、大碱度水样(如锅炉水、化学净水、冷却水、生水等)的测定:取100mL透明水样注入锥形瓶中,加2~3滴酚酞指示剂,此时若显红色,则用0.100moL/L或0.0500moL/L盐酸标准溶液滴至红色刚消失,记录盐酸溶液的用量V1;然后再加入甲基橙指示剂2~3滴继续用盐酸标准溶液滴定至由淡黄色变为橙色,记录用量V2(不包括V1)。
2、小碱度水样(如凝结水、高纯水、给水等)的测定:取100mL透明水样注入锥形瓶中,加2~3滴酚酞指示剂,此时若显红色。
则用微量滴定管以0.0100moL/L盐酸标准溶液滴至红色刚消失,记录盐酸溶液的用量V1;然后再加入甲基红—亚甲基蓝指示剂2~3滴继续用盐酸标准溶液滴定至由绿色变为紫色,记录用量V2(不包括V1)。
3、无酚酞碱度的测定方法:上述二法,若加入酚酞指示剂后溶液不显色可直接加甲基橙或甲基红—亚甲基蓝指示剂,用盐酸标准溶液滴定,记录耗酸体积V2。
水质碱度的测定方法验证报告

水质碱度的测定《水和废水监测分析方法》(第四版增补版)国家环境保护总局(2002年)第三篇第一章十二碱度(总碱度、重碳酸盐和碳酸盐)酸碱指示剂滴定法验证报告1、目的通过对实验人员、设备、物料、方法,环境的能力确认,验证实验室均已达到各种要求,具备开展此实验的能力。
2、方法简介水样用标准酸溶液滴定至规定的PH值,其终点可由加入的酸碱指示剂在PH值时颜色的变化来判断。
当滴定至酚酞指示剂由红色变为无色时,溶液PH值即为8.3,指示水中氢氧根离子已被中和,碳酸盐均被转为重碳酸盐,当滴定至甲基橙指示剂由橘黄色变成橘红色时,溶液的PH值为4.4-4.5,指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和,根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量,可以计算出水中碳酸盐、重碳酸盐及总碱度。
3、仪器设备及药品验证情况3.1使用仪器设备:25ml酸式滴定管、250ml锥形瓶3.2设备验证情况设备验收合格。
4、环境条件验证情况4.1本方法对环境无特殊要求。
4.2目前对环境的设施和监控情况天平室环境指标:温度:27℃;湿度62%。
4.3环境验证条件符合要要求5、人员能力验证5.1该项目人员配备情况有二名以上符合条件的实验人员。
5.2人员培训及考核情况通过培训,考核合格,相关记录见人员技术档案。
6、标准物质及试剂验证情况6.1方法所需标准(物质)溶液及试剂情况6.1表6.2配备情况6.2表7、方法验证情况7.1方法要求7.11检出限:方法无要求精密度:方法无要求准确度:加标回收率在90%-110%之间7.2目前该项目本实验的精密度、检出限、准确度的实际水平7.21精密度:根据计算公式P=T,M=0时计算如下表:表7.21测得实验室内相对标准偏差为0.23%,符合要求。
7.22准确度在已知样品浓度53.7mg/L的样品中加入1ml浓度为5mg/L的氢氧化钠溶液, 加标后测得含量如下:7.22加标回收率测定结果表7.23检出限7.23空白测定结果表一般根据所用滴定管产生的最小液滴的体积进行计算,计算公式为:100005.50)(/mg a 3⨯⨯+=VM P C L CO C )计(以式中:C ————盐酸标准溶液浓度mol/L ;P ————以酚酞为指示剂,消耗盐酸标准溶液的体积ml; M ————以甲基橙为指示剂,消耗盐酸标准溶液的体积ml; V ————取样的体积ml;测得检出限为0.631mg/L,验证合格。
水碱度的测定方法

水碱度的测定方法
水碱度咋测呢?其实有好几种方法呢!比如酸碱滴定法。
先取一定量的水样,加入指示剂,像酚酞啥的。
如果水变红色了,就用酸标准溶液滴定,直到红色刚好消失。
这就测出了酚酞碱度。
然后接着加甲基橙指示剂,继续滴定,直到溶液变成橙色,这就得到了总碱度。
那测的时候有啥要注意的呢?哎呀,那可不少!比如水样要取干净,不能有杂质。
还有滴定的速度不能太快,不然结果可就不准啦!
这过程安全不?稳定不?放心吧!只要你按照正确的方法操作,那肯定是安全又稳定的。
就像你走路走得稳稳当当的,不会摔跤。
这水碱度测定有啥用呢?应用场景可多啦!像污水处理厂,得知道水的碱度,才能更好地处理污水呀!还有工业用水,碱度不合适可能会影响生产呢!它的优势就是能快速准确地知道水的性质,就像你有一双火眼金睛,一下子就能看出水的好坏。
我给你说个实际案例哈。
有个工厂,之前不知道水的碱度,生产老是出问题。
后来一测,发现碱度太高了。
调整了用水之后,生产就顺顺利利的啦!这效果,杠杠的!
所以说,水碱度的测定很重要哦!大家一定要重视起来。
(完整版)酚酞指示剂测定水中碱度环境监测第四版

(环境)水质卫生检验方法标准HZHJSZ00130水质碱度总碱度酸碱指示剂滴定法HZ-HJ-SZ-0130水质碱度(总碱度重碳酸盐和碳酸盐)的测定酸碱指示剂滴定法水的碱度是指水中所含能与强酸定量作用的物质总量。
水中碱度的来源是多种多样的地表水的碱度基本上是碳酸盐重碳酸盐及氢氧化物含量的函数,所以总碱度被当作这些成分浓度的总和。
当水中含有硼酸盐磷酸盐或硅酸盐等时,则总碱度的测定值也包含它们所起的作用。
废水及其他复杂体系的水体中还含有有机碱类金属水解性盐类等,均为碱度组成部分。
在这些情况下碱度就成为一种水的综合性特征指标,代表能被强酸滴定的物质的总和。
碱度的测定值因使用的终点pH 值不同而有很大的差异,只有当试样中的化学组成已知时才能解释为具体的物质。
对于天然水和未污染的地表水可直接用酸滴定至pH8.3 时消耗的量为酚酞碱度;以酸滴定至pH 为4.4~4.5 时消耗的量为甲基橙碱度;通过计算可求出相应的碳酸盐重碳酸盐和氢氧根离子的含量。
对于废水污水则由于组分复杂,这种计算无实际意义往往需耍根据水中物质的组分确定其与酸作用达终点时的pH 值,然后用酸滴定以便获得分析者感兴趣的参数并作出解释。
碱度指标常用于评价水体的缓冲能力及金属在其中的溶解性和毒性,是对水和废水处理过程的控制的判断性指标,若碱度是由过量的碱金属盐类所形成,则碱度又是确定这种水是否适宜于灌溉的重要依据。
用标准酸滴定水中碱度是各种方法的基础,有两种常用的方法即酸碱指示剂滴定法和电位滴定法电位滴定法。
根据电位滴定曲线在终点时的突跃确定特定pH 值下的碱度,它不受水样浊度色度的影响适用范围较广用指示剂判断滴定终点的方法简便快速,适用于控制性试验及例行分析,二法均可根据需要和条件选用。
样品采集后应在4 保存分析前不应打开瓶塞不能过滤稀释或浓缩样品应于采集后的当天进行分析特别是当样品中含有可水解盐类或含有可氧化态阳离子时应及时分析。
一原理水样用标准酸溶液滴定至规定的pH 值,其终点可由加入的酸碱指示剂在该pH 值时颜色的变化来判断:当滴定至酚酞指示剂由红色变为无色时溶液pH 值即为8.3 指示水中氢氧根离子(OH-)已被中和,碳酸盐(CO32-)均被转为重碳酸盐(HCO3-) 反应如下OH-+H+H2O=CO32-+H+ +HCO3-当滴定至甲基橙指示剂由桔黄色变成桔红色时溶液的pH 值为4.4~4.5 指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和反应如下HCO3+H+=H2O+CO2根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量可以计算出水中碳酸盐重碳酸盐及总碱度。
酸度和碱度

酸度和碱度酸度和碱度(一)酸度酸度是指水中所含能与强碱发生中和作用的物质的总量。
这类物质包括无机酸、有机酸、强酸弱碱盐等。
地面水中,由于溶入二氧化碳或被机械、选矿、电镀、农药、印染、化工等行业排放的含酸废水污染,使水体pH值降低,破坏了水生生物和农作物的正常生活及生长条件,造成鱼类死亡,作物受害。
所以,酸度是衡量水体水质的一项紧要指标。
测定酸度的方法有酸碱指示剂滴定法和电位滴定法。
1.酸碱指示剂滴定法用标准氢氧化钠溶液滴定水样至肯定pH值,依据其所消耗的量计算酸度。
随所用指示剂不同,通常分为两种酸度:一是用酚酞作指示剂(其变色pH为8.3)测得的酸度称为总酸度(酚酞酸度),包括强酸和弱酸;二是用甲基橙作指示剂(变色pH约3.7)测得的酸度称强酸酸度或甲基橙酸度。
酸度的单位在《水和废水监测分析方法》中规定用CaCO3mg/L 表示。
2.电位滴定法以pH玻璃电极为指示电极,甘汞电极为参比电极,与被测水样构成原电池并接入pH计,用氢氧化钠标准溶液滴定至pH计指示4.5和8.3,据其相应消耗的氢氧化钠溶液量分别计算两种酸度。
本方法适用于各种水体酸度的测定,不受水样有色、浑浊的限制。
测定时应注意温度、搅拌状态、响应时间等因素的影响。
(二)碱度水的碱度是指水中所含能与强酸发生中和作用的物质总量,包括强碱、弱碱、强碱弱酸盐等。
天然水中的碱度重要是由重碳酸盐、碳酸盐和氢氧化物引起的,其中重碳酸盐是水中碱度的重要形式。
引起碱度的污染源重要是造纸、印染、化工、电镀等行业排放的废水及洗涤剂、化肥和农药在使用过程中的流失。
碱度和酸度是判定水质和废水处理掌控的紧要指标。
碱度也常用于评价水体的缓冲本领及金属在其中的溶解性和毒性等。
测定水中碱度的方法和测定酸度一样,有酸碱指示剂滴定法和电位滴定法。
前者是用酸碱指示剂指示滴定尽头,后者是用pH计指示滴定尽头。
水样用标准酸溶液滴定至酚酞指示剂由红色变为无色(pH8.3)时,所测得的碱度称为酚酞碱度,此时OH—已被中和,CO32—被中和为HCO3—;当连续滴定至甲基橙指示剂由桔黄色变为桔红色时(pH约4.4),所测得的碱度称为甲基橙碱度,此时水中的HCO3—也已被中和完,即全部致碱物质都已被强酸中和完,故又称其为总碱度。
水质碱度酸碱指示剂滴定法

水质-碱度-酸碱指示剂滴定法水质碱度(总碱度、重碳酸盐和碳酸盐)的测定酸碱指示剂滴定法水的碱度是指水中所含能与强酸定量作用的物质总量。
水中碱度的来源是多种多样的。
地表水的碱度,基本上是碳酸盐、重碳酸盐及氢氧化物含量的函数,所以总碱度被当作这些成分浓度的总和。
当水中含有硼酸盐、磷酸盐或硅酸盐等时,则总碱度的测定值也包含它们所起的作用。
废水及其他复杂体系的水体中,还含有有机碱类、金属水解性盐类等,均为碱度组成部分。
在这些情况下,碱度就成为一种水的综合性特征指标,代表能被强酸滴定的物质的总和。
碱度的测定值因使用的终点pH值不同而有很大的差异,只有当试样中的化学组成已知时,才能解释为具体的物质。
对于天然水和未污染的地表水,可直接用酸滴定至pH8.3时消耗的量,为酚酞碱度。
以酸滴定至pH为4.4~4.5时消耗的量,为甲基橙碱度。
通过计算可求出相应的碳酸盐、重碳酸盐和氢氧根离子的含量;对于废水、污水,则由于组分复杂,这种计算无实际意义,往往需耍根据水中物质的组分确定其与酸作用达终点时的pH值。
然后,用酸滴定以便获得分析者感兴趣的参数,并作出解释。
碱度指标常用于评价水体的缓冲能力及金属在其中的溶解性和毒性,是对水和废水处理过程的控制的判断性指标。
若碱度是由过量的碱金属盐类所形成,则碱度又是确定这种水是否适宜于灌溉的重要依据。
用标准酸滴定水中碱度是各种方法的基础。
有两种常用的方法,即酸碱指示剂滴定法和电位滴定法。
电位滴定法根据电位滴定曲线在终点时的突跃,确定特定pH值下的碱度,它不受水样浊度、色度的影响,适用范围较广。
用指示剂判断滴定终点的方法简便快速、适用于控制性试验及例行分析。
二法均可根据需要和条件选用。
样品采集后应在4℃保存,分析前不应打开瓶塞,不能过滤、稀释或浓缩。
样品应于采集后的当天进行分析,特别是当样品中含有可水解盐类或含有可氧化态阳离子时,应及时分析。
1.原理水样用标准酸溶液滴定至规定的pH值,其终点可由加入的酸碱指示剂在该pH值时颜色的变化来判断。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
水质碱度(总碱度、重碳酸盐和碳酸盐)的测定酸碱指示剂滴定法水的碱度是指水中所含能与强酸定量作用的物质总量。
水中碱度的来源是多种多样的。
地表水的碱度,基本上是碳酸盐、重碳酸盐及氢氧化物含量的函数,所以总碱度被当作这些成分浓度的总和。
当水中含有硼酸盐、磷酸盐或硅酸盐等时,则总碱度的测定值也包含它们所起的作用。
废水及其他复杂体系的水体中,还含有有机碱类、金属水解性盐类等,均为碱度组成部分。
在这些情况下,碱度就成为一种水的综合性特征指标,代表能被强酸滴定的物质的总和。
碱度的测定值因使用的终点pH值不同而有很大的差异,只有当试样中的化学组成已知时,才能解释为具体的物质。
对于天然水和未污染的地表水,可直接用酸滴定至时消耗的量,为酚酞碱度。
以酸滴定至pH为~时消耗的量,为甲基橙碱度。
通过计算可求出相应的碳酸盐、重碳酸盐和氢氧根离子的含量;对于废水、污水,则由于组分复杂,这种计算无实际意义,往往需耍根据水中物质的组分确定其与酸作用达终点时的pH值。
然后,用酸滴定以便获得分析者感兴趣的参数,并作出解释。
碱度指标常用于评价水体的缓冲能力及金属在其中的溶解性和毒性,是对水和废水处理过程的控制的判断性指标。
若碱度是由过量的碱金属盐类所形成,则碱度又是确定这种水是否适宜于灌溉的重要依据。
用标准酸滴定水中碱度是各种方法的基础。
有两种常用的方法,即酸碱指示剂滴定法和电位滴定法。
电位滴定法根据电位滴定曲线在终点时的突跃,确定特定pH值下的碱度,它不受水样浊度、色度的影响,适用范围较广。
用指示剂判断滴定终点的方法简便快速、适用于控制性试验及例行分析。
二法均可根据需要和条件选用。
样品采集后应在4℃保存,分析前不应打开瓶塞,不能过滤、稀释或浓缩。
样品应于采集后的当天进行分析,特别是当样品中含有可水解盐类或含有可氧化态阳离子时,应及时分析。
1.原理水样用标准酸溶液滴定至规定的pH值,其终点可由加入的酸碱指示剂在该 pH值时颜色的变化来判断。
当滴定至酚酞指示剂由红色变为无色时,溶液pH值即为,指示水中氢氧根离子(OH-)已被中和,碳酸盐(CO32-)均被转为重碳酸盐(HCO3-),反应如下:OH-+H+―H2OCO32-+H+―HCO3–当滴定至甲基橙指示剂由桔黄色变成桔红色时,溶液的pH值为~,指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和,反应如下:HCO3+H+―H2O+CO2根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量,可以计算出水中碳酸盐、重碳酸盐及总碱度。
上述计算方法不适用于污水及复杂体系中碳酸盐和重碳酸盐的计算。
2.干扰及消除水样浑浊,有色均干扰测定,遇此情况,可用电位滴定法测定。
能使指示剂褪色的氧化还原性物质也干扰测定。
例如水样中余氯可破坏指示剂(含余氯时,可加入1~2滴L硫代硫酸钠溶液消除)。
3.方法的适用范围此法适用于不含有上述干扰的物质的水样。
4.试剂4.1无二氧化碳水。
用于制备标准溶液及稀释用的蒸馏水或去离子水,临用前煮沸15min,冷却至室温。
pH值应大于,电导率小于2μS/cm。
4.2酚酞指示液。
称取1g酚酞溶于100mL 95%乙醇中,用L氢氧化钠溶液滴至出现淡红色为止。
4.3甲基橙指示剂。
称取甲基橙溶于100mL蒸馏水中。
4.4碳酸钠标准溶液(1/2Na2CO3 L)。
称取 (于250烘干4h)的无水碳酸钠(Na2CO3),溶于少量无二氧化碳水中,移入1000mL容量瓶中,用水稀释至标线,摇匀,贮于聚乙烯瓶中。
保存时间不要超过一周。
4.5盐酸标准溶液L)。
用分度吸管吸取 mL浓盐酸(?=mL),并用蒸馏水稀释至1000mL,此溶液浓度≈L,其准确浓度按下法标定:用无分度吸管吸取碳酸钠标准溶液于250mL锥形瓶中,加无二氧化碳水稀释至约100mL,加入3滴甲基橙指示液,用盐酸标准溶液滴定至由桔黄色刚变成桔红色,记录盐酸标准溶液用量,按下式计算其准确浓度:式中:c----盐酸标准溶液浓度(mol/L);V----盐酸标准溶液用量(mL)。
5.仪器5.1酸式滴定管,25mL。
5.2锥形瓶,250mL。
6.操作步骤6.1分取100mL水样于250mL锥形瓶中,加入4滴酚酞指示液摇匀,当溶液呈红色时,用盐酸标准溶液滴定至刚刚褪至无色,记录盐酸标准溶液用量。
若加酚酞指示剂后溶液无色,则不需用盐酸标准溶液滴定,并接着进行下项操作。
6.2向上述锥形瓶中加入3滴甲基橙指示液,摇匀,继续用盐酸标准溶液滴定至溶液由桔黄色刚刚变为桔红色为止。
记录盐酸标准溶液用量。
7.结果计算对于多数天然水样,碱性化合物在水中所产生的碱度,有五种情形。
为说明方便,令以酚酞作指示剂时,滴定至颜色变化。
所消耗盐酸标准溶液的量为P mL,以甲基橙作指示剂时盐酸标准溶液用量为MmL,则盐酸标准溶液总消耗量为T=M+P。
第一种情形,P=T或M=0时:P代表全部氢氧化物及碳酸盐的一半,由于M=0表示不含有碳酸盐,亦不含重碳酸盐。
因此P=T=氢氧化物。
第二种情形,P>1/2T时;说明M>O,有碳酸盐存在,且碳酸盐=2M=2(T-P)。
而且由于P>M,说明尚有氢氧化物存在,氢氧化物=T-2(T-P)=2P-T。
第三种情形,P=1/2T,即P=M时;M代表碳酸盐的一半,说明水中仅有碳酸盐。
碳酸盐=2P=2M=T。
第四种情形,P<1/2T时;此时M>P,因此M除代表由碳酸盐生成的重碳酸盐外,尚有水中原有的重碳酸盐。
碳酸盐=2P,重碳酸盐=T-2P。
第五种情形,P=0时;此时,水中只有重碳酸盐存在。
重碳酸盐=T=M。
以上五种情形的碱度示于表1中:表6-1 碱度的组成按下述公式计算各种情况下总碱度、碳酸盐、重碳酸盐的含量。
(1)总碱度(以CaO计,mg/L) =c(P+M)××1000/V计,mg/L) =c(P+M)××1000/V 总碱度(以CaCO3式中:c----盐酸标准溶液浓度(mol/L);氧化钙(1/2CaO)摩尔质量(g/mol)碳酸钙(1/2CaCO3)摩尔质量(g/mol)(2)当P=T时,M=02-)=0碳酸盐(CO3-)=0重碳酸盐(HCO3(3)当 P>1/2T 时碳酸盐碱度(以CaO计,mg/L)=c(T-P)××1000/ V碳酸盐碱度(以CaCO计,mg/L)=c(T-P)××1000/ V32-,mol/L)=c(T-P)×1000/ V 碳酸盐碱度(1/2CO3-)=0重碳酸盐碱度(HCO3(4)当P=1/2T时,P=M碳酸盐碱度(以CaO计,mg/L)=c·P××1000/V计,mg/L)=c·P××1000/V 碳酸盐碱度(以CaCO32-,mol/L)=c·P×1000 / V 重碳酸盐碱度(1/2CO3-)=0重碳酸盐碱度(HCO3(5)当P<1/2T时:碳酸盐碱度(以CaO计,mg/L)=c·P××1000/V计,mg/L)=c·P××1000/V 碳酸盐碱度(以CaCO32-,mol/L)=c·P×1000/V碳酸盐碱度(1/2CO3重碳酸盐碱度(以CaO计,mg/L)=c·(T-2P)××1000/V重碳酸盐碱度(以CaCO计,mg/L)=c·(T-2P)××1000/V3-,mol/L)=c·(T-2P)×1000/V重碳酸盐碱度(HCO3(6)当 P=0时2-)=0碳酸盐(CO3重碳酸盐碱度(以CaO计,mg/L)=c·M××1000/V计,mg/L)=c·M××1000/V重碳酸盐碱度(以CaCO3-,mol/L)=c·M×1000/V重碳酸盐碱度(HCO38.精密度和准确度-含量为L时,总碱度的五个实验室对人工配制的统一标准进行方法验证的结果如下:在HCO3室内相对标准偏差为%;室间相对标准偏差为 %;相对误差为%;加标回收率为±%。
取15个地表水水样进行测定,浓度范围在~L时,相对标准偏差为~%,加标回收率为~102%。
注意事项:(1)若水样中含有游离二氧化碳,则不存在碳酸盐,可直接以甲基橙作指示剂进行滴定。
(2)当水样中总碱度小于20mg/L时,可改用L盐酸标准溶液滴定,或改用 10mL 容量的微量滴定管,以提高测定精度。
9.参考文献《水和废水监测分析方法》编委会编,水和废水监测分析方法(第三版),~238,中国环境科学出版社,北京,1997。
