双液系气液平衡相图的绘制华南师范大学物化实验
双液系气-液平衡相图绘制华师华南师范大学物理化学实验报告

实验报告姓名学号专业化学(师范)年级、班级课程名称物理化学实验实验项目实验类型 验证 设计 综合实验时间实验指导老师马国正实验评分一、实验目的(1)用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图。
并找出恒沸点混合物的组成及恒沸点的温度。
(2)掌握测定双组分液体的沸点及正常沸点的测定方法。
(3)了解阿贝折光仪的构造原理,熟悉掌握阿贝折光仪的使用方法。
二、实验原理(1)沸点的定义沸点是液体饱和蒸汽压和外压相等时的温度,双液系的沸点不仅于外压有关,而且还与两种液体的相对含量有关。
(2)理想二组分系统的拉乌尔定律理想的二组分体系在全部浓度范围内符合Raoult定律。
结构相似、性质相似的组分间可以形成近似的理想体系,这样可以形成简单的T-x(y)图。
大多数情况下,曲线将出现或正或负的偏差。
当这一偏差足够大时,在T-x(y)曲线上将出现极大点(负偏差)或极小点(正片差)。
这种最高和最低沸点称为恒沸点,所对应的溶液称为恒沸混合物。
(3)平衡时气相、液相的组成确定回流冷凝法保持气液相对量不变,测定双液系沸点,通过阿贝折射仪测定其液相折射率确定气液相平衡时的组成,通过双液系气液平衡时的组成对校正后的沸点作图,得到在1个大气压下乙醇-乙酸乙酯气液平衡相图。
三、仪器与试剂沸点仪(1套)小试管(5mL带软木塞)(若干)阿贝折射仪(1台)烧杯(2个)1/10温度计(50~100℃)(1支)吸管(2支)擦镜纸乙酸乙酯(A.R.)无水乙醇(A.R.)不同比例的乙醇-乙酸乙酯混合液丙酮(C.P.)无水乙醇(A.R.)四、实验步骤(1)折射率-体积分数工作曲线取几滴纯乙醇、纯乙酸乙酯分别测定其折射率,两点作n D26−φ工作曲线(n-V)。
(2)折射率-摩尔分数工作曲线在n D26−φ线上取8个点,利用乙醇、乙酸乙酯密度合量比(%)等条件将以上点对应的体积分数换算成摩尔分数,按对应的折射率重新绘n D26−x点,再将点连成平滑曲线,即为n D26−x工作曲线(n-x)(3)溶液的沸点与平衡气-液相组成测定a)样品I-VI分别为乙醇体积分数为5%、15%、22%、38%、50%、90%的乙醇-乙酸乙酯混合液。
实验四 双液系气液平衡相图

实验五 双液系气液平衡相图一、实验目的1. 绘制在p ө下环已烷—异丙醇双液系的气液平衡相 图,了解相图和相律的基本概念; 2. 掌握回流冷凝法测定双组分液体的沸点及正常沸点的方法;3. 了解阿贝折光仪的构造原理,熟悉掌握用折光率确定二元液体组成的方法。
二、实验原理1、 气—液相图图5.1 沸点测定仪示意图根据相律f=C-Φ+2,对于一个气—液共存的二组分体系,其自由度f =2,若再确定一个变量,整个体系的存在状态就可以用二维图形来描述。
通常测定一系列不同配比溶液的沸点及气液两相的组成,就可绘制气—液相图。
压力不同时,双液系的相图将略有差异。
本实验要求将外压校正到101325kPa 。
完全互溶双液系恒定压力下的沸点-组成图可以分成三类:⑴溶液沸点介于两纯组分沸点之间(图5.1);⑵溶液存在最低沸点(图5.2);⑶溶液存在最高沸点(图5.3)。
t/ ℃ p=常数 t/ ℃ p=常数 t/ ℃ p=常数g g gl l lA xB → B A x B → B A x B → B 图(5.1) 图(5.2) 图(5.3)2、 沸点测定仪本实验所用沸点仪如图5.1所示的。
本实验是利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成沸点数据可直接由温度计获得,气、液相组成可通过测定其折光率,然后由组成-折光率曲线中最后确定。
三、仪器 试剂蒸气压测定装置1套;真空泵1台;数字式气压计1台;电加热器1只;温度计2支;数字式真空计1台;磁力搅拌器1台;异丙醇(分析纯)。
四、实验步骤1. 按仪器装置图接好测量线路,所有接口须严密封闭,将液体装入平衡管。
2. 系统检漏缓慢旋转三通活塞,使系统通大气,开启冷却水,接通电源使真空正常转后,调节活塞使系统减压至1104后关闭活塞,此时系统处于真空状态。
若漏气则分段检查直至不漏气才可进行实验。
3. 测不同温度下液体的饱和蒸气压转动三通活塞使系统与大气相通,开动搅拌机并水浴加热。
双液体系气-液平衡相图的绘制及思考题

双液体系气一液平衡相图的绘制一、实验目的1.绘制环己烷一异丙醇双液体系的沸点组成图,确定其恒沸组成和恒沸温度.2.掌握回流冷凝管法测定溶液沸点的方法.3.掌握阿贝折射仪的使用方法.二、实验原理两种液体物质混合而成的两组分体系称为双液系.根据两组分间溶解度的不同,可分为完全互溶、局部互溶和完全不互溶三种情况.两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,那么混合物的组成与平衡时气相的组成不同.当压力保持一定,混合物沸点与两组分的相对含量有关.恒定压力下,真实的完全互溶双液系的气-液平衡相图〔T-x〕,根据体系对拉乌尔定律的偏差情况,可分为3类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯一苯体系,如图〔a〕所示.〔2〕最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸一水体系,如图〔b〕所示.〔3〕最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合上图为二组分真实液态混合物气一液平衡相图〔T-x图〕后两种情况为具有恒沸点的双液系相图.它们在最低或最高恒沸点时的气相和液相组成相同,因而不能象第一类那样通过反复蒸储的方法而使双液系的两个组分相互别离,而只能采取精储等方法别离出一种纯物质和另一种恒沸混合物.为了测定双液系的T—x相图,需在气一液平衡后,同时测定双液系的沸点和液相、气相的平衡组成.本实验以环己烷一异丙醇为体系,该体系属于上述第三种类型,在沸点仪中蒸储不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T-x相图.本实验中两相的成分分析均采用折光率法测定.三、仪器与试剂1、仪器:沸点仪1台;调压变压器1台;阿贝折射仪1台;温度计〔0-100C〕1支;长滴管1个;短滴管2支;2、试剂:环己烷〔分析纯〕;异丙醇〔分析纯〕异丙醇一环己烷标准溶液〔异丙醇分别为0.20,0.40,0.50,0.60,0.80,0.90〕四、主要实验步骤1.测定环己烷、异丙醇及标准溶液的折射率调节阿贝折射仪,用一支枯燥的短滴管吸取环己烷数滴,注入折射仪的加液孔内,测定其折射率n,读数两次,取其平均值.然后翻开棱镜组,待环己烷挥发后,再用擦镜纸轻轻吸去残留在镜面上的液体,合上棱镜组.同样测定异丙醇及各标准溶液的折射率.记录室内大气压力.2.测定溶液的沸点及平衡时气一液两相的折射率〔1〕将枯燥洁净的沸点仪装置好,检查带有温度计的软木塞是否塞紧.用漏斗从支管参加25mL异丙醇溶液于烧瓶中,将温度计水银球中部位于液面为度.接通冷凝水和电源,调节调压器加热电压.将溶液缓缓加热,当液体沸腾后,再次调节加热电压和冷凝水流量,使蒸气在冷凝液倾回烧瓶,反复两次,待温度稳定后记下沸点,停止通电,充分冷却后,分别测定气相冷凝液和液相的折射率.(2)将上述操作步骤分别逐次参加环己烷1mL、2mL、3mL、4mL、5mL、10mL,测定其液体的沸点及气相冷凝管和液相的折射率.(3)将沸点仪内的溶液倒入回收瓶,用少许环己烷洗涤沸点仪2-3次,用电吹风吹干沸点仪,然后参加环己烷25mL,1mL,4mL,5mL,同法测量其沸点及气相冷凝液和液相的折射率.记录数据.五、数据处理与结果讨论表一:异丙醇一环己烷标准溶液表二:异丙醇—环己烷溶液66图一:异丙解一环己烷标准溶液42n率射折3y=-0.0396x+1.4178R=0.992214/1 ^1 98330.20.40.60.81W〔异丙醇〕图二:环己烷-乙醇气液相图78■76■74-72-T.70■68-66-64・0.00.20.40.60.81.0X六、误差分析1、仪器可能存在系统误差2、两个组使用的温度计不同,也不是同一个人读数,温度可能存在误差3、折射仪测折射率时可能有读数误差4、在用移液管移取试剂时出现读数和操作误差.七、思考题1.测定溶液的沸点和气、液二相组成时,是否要把沸点仪每次都要烘干?为什么?答:不用.由于测定混合样时,其沸点及气液组成都是实验直接测定的,绘制图像只与这几组数据有关,并不需要测定物质的准确组成,与试样的量无关.2.你认为本实验所用的沸点仪有哪些缺乏?如何改良?答:我们组使用的沸点仪装气相溶液的凹槽太小,在取溶液测折射率时,最多只能测两次,如果测错就没方法再测一次,数据会有误差.还有就是在测定折射率之前需要将沸点仪中的溶液冷却至室温,这样比拟耗时.八、实验考前须知1.电阻丝不能露出液面,一定要浸没于溶液中,以免通电红热后引起有机溶剂燃烧.电阻丝两端电压不能过大,过大会引起有机溶剂燃烧或烧断电阻丝.2.测量过程中一定要到达气液平衡状态,即体系的温度保持稳定,才能测定其沸点及气相冷凝液和液相的折射率.3.在测定其气相冷凝液和液相的折射率时要保持温度一致.4.使用阿贝折射仪时,棱镜上不能接触硬物,擦拭棱镜时需要用擦镜纸等柔软的纸.双百方案试题所属单位姓名一、多项选择题〔此题共20小题,每题0.5分,总分值10分;每题给出的多个选项中,可能有多项符合题意,把所选项前的字母填在题后的方括号内〕1.AIS信号的全称是,该信号的内容是o〔DG〕A.接收信号丧失,B.远端缺陷指示,C误码对告信号,D.告警指示信号,E.全0码,F.PRB纲,G.1000码,G.全1码,2.携带MS-AIS告警的字节是.〔G〕A.B1,B.E1,C.H1,D.A1,E.H2,F.J0G.K2,H.V53.ZTE155M光口和LUCENT155M光口对接时,我网管上出现HP-RDI告警,可能原因〔BC〕.A.我光板接收到LUCENT光板送来的H1、H2是全1码;B.LUCEN优板接收到我光板送来的H1、H2是全1码;C.我光板向LUCEN仪板发的H1、H2和LUCENT光板不匹配;D.LUCEN仪板向我光板发的H1、H2和LUCENT光板不匹配;E.LUCEN仇板有MS-AIS告警.4.用DOWNLOAD不能连接上网元NCP的原因有〔ABE〕.网段;B.网线是平行网线;C.没有运行SYSCONFIGg序修改效劳器主机地址;D.没有设置接入网元为本网元;E.NCP板没有拨码成全ON的状态.5.设备通断电必须注意〔ABCE〕A.必须先检查从电源柜/头柜到SDH设备连接的电源线路正确、良好;B.电源柜/头柜电源开关闭合前,必须将SDH设备电源箱的空开和PWCK上的开关置断开状态并将所有单板拔出成浮插状;C.电源柜/头柜电源开关闭合前,必须用万用表检查电源柜/头柜输出电压在SDH设备工作电压范围内;D.测试SDH设备电源箱空开和工作地间电压正常后即可插入单板到位并闭合空开;E.16#PWCK和36#PWCK独立在位测试工作良好后才能并行插入一同工作.6.ZXSM-150/600/2500配置成2.5G设备时,K1、K2字节的处理由板完成.〔C〕上检测.〔A.收,B.发,C 收发同时,D.收、发二者之一 8. AU-AIS 是在光板上检测到的告警,该告警.〔D 〕A.可以下传B.不可以下传C.可以下传也可以不下传D.根据时隙配置决定是否下传9. ZXSM-150/600/2500设备组网为二纤通道保护环时,如果光纤有多处接错,但是光板工作正常且没有任何告警,那么2M 业务.〔C 〕11. ZXSM-10G 系统使用G.652光纤传输,改善色散受限距离,以下哪个方法没有用到〔D 〕.A 、色散补偿单元B 、预喟啾C 带外FECD 、带内FEC12. ZXSM-150/600/2500设备组网为二纤通道保护环时,环上开通的2M 业务最多可到达〔设备等级为 STM —N 〕.〔B 〕A.63X 双/B.63X13. ZXSM-150/600/2500设备组网为二纤通道保护环,某点带有光支路,去光支路的业务在环上能够被保护,这是在上实现的.〔CD 〕A.APS 保护倒换协议根底B.交叉板时分对TU12的优选C.TU-AIS 和TU-LOP 检测根底14. ZXONME100网管支持两种协议栈,它们是〔FC 〕A.MPS,B.PPP,C.UDP,D15. 在E100网管中,通信主机地址是指的地址.〔BC 〕A.操作系统所在计算机的地址;B.SQL 数据库所在计算机的地址;C.SMCCSERVER 在计算机的地址;D.SMCCCLIEN 所在计算机的地址; 16、假设某网元同时有大量以下的BBE 事件出现,应先处理哪种性能事件:〔A 〕A.MS-BBEB.HP-BBE D.HP-FEBBE7.AU-AIS 是在光板上检测到的告警,它是在光板的C.LP-BBEE.RS-BBE17、SDH 同步网所广泛采用的同步方式是.〔A 〕A 、全同步方式中的等级主从同步方式.B 、伪同步方式同准同步方式相结合的同步方式.C 、伪同步方式.D 、准同步方式或异步方式. 18、时钟等级中,质量等级最高的是.〔C 〕 A 、SDH 网元日^钟SECB 、转接局从时钟SSU-A C 、基准主时钟PRCD 、端局从时钟SSU-B19、STM-N 的复用方式是.〔A 〕nm-1561nmnm-1565nmnm-1600nmD.1540nm-1560nm二、判断题〔此题共16小题,每题0.5分,?t 分8分;请判断每题给出的说法是否符合事实,并把您的判断 结果填在题后的方括号内;假设符合事实,请填,否那么填“X 〞〕1.1310nm 的光板使用光功率计只能在1310nm 波长上测量到光功率.〔x 〕2 .当TU12通道配置良好后,2M 支路板的终端侧环回的结果是让对端支路上挂的误码仪无AIS 告警.〔X 〕3 .环回分为硬件环回和软件环回,硬件环回就是直接将光板或者支路板的物理端口本身收发直接相连.〔V 〕4 .高阶告警的产生往往会引发低阶的告警〔V 〕5 .如果本端将2M 物理端口配置时隙上到光板上,但对端没有配置时隙,这是用2M 误码仪连接本端该2M 端口,误码仪上会出现“通道告警指示〞和“不同步告警指示〞.〔,〕6 .交换机上报的AIS 是传输设备送来的〔V 〕7、SFE 系列的单板工作在虚拟网桥模式下,实际上就是一个L2交换机.〔V 〕 8. STM-4是四个STM-1所有业务和开销的字节间插而来〔X 〕9. ZXSM-150/600/2500中的OHP^g 成所有SOHFF 销字节的处理.〔X 〕10、在DWDM 中,监控通道独立于主通道,目前我国使用的监控通道为1510nm .〔V 〕 11.SDH 勺带宽利用率比PDH 的带宽的利用率高.〔X 〕12.10G 系统中,业务总线、开销总线和时钟总线均为双总线.〔V 〕 13.10G 系统中,业务板对K1、K2不进行处理〔X 〕A.字节间插B.C.帧间插D.20.目前常用的掺饵光纤放大器 比特间插 统计复用EDFA 的工作波长范围为〔A14、中兴ZXWM—32系列DWDM产品通过B1、J咛节的检测,可以准确定位故障发生位置,区分SDH^和DWDM段的故障.〔V〕sDWDM系统平滑升级到10Gb/s系统.〔V〕16、在DWDM系统中,OMU的类型不同,一般所需配置的OBA的设备类型也不相同.〔V〕三、填空题〔此题共50个空,每空0.5分,总分值25分;请把符合题意的内容填写在横线上〕1.如果本端光板没有收到对端送来的光信号,网管上会报光信号丧失、不可用时间开始的告警.2.如果光路连接中有鸳鸯纤,可以在网管上通过插入告警的操作来判断并排除.3.如果疑心某块PWC幽时钟单元有问题,可以在网管上通过倒换时钟板的操作来判断并排除..4.如果接收到的J1字节和预定值不同,网管上会出现高阶跟踪标识失配〔TIM〕的告警.5.MS-AISHP-AISR-LOSLP-AIS^警抑制的顺序是R-LOS>MS-AIS>HP-AIS>LP-AIS.〔说明:顺序错误不给分〕6.DWDM的波长不应与ITU-T规定的标准波长有太大的偏差,否那么严重的会引起系统的崩溃.其最大偏差为_20_.7.根据放大器在系统中位置的不同,光纤放大器分为OPAOBAOLA8.EDFA的商用化促使了DWDM的开展,但是EDFA也有其局限性:光浪涌现象、非线性效应、色散问题〔至少三个〕.9.DWDM系统对光源的要求是标准稳定的波长、满足长距离传输要求〔或色散小〕10、对于目前使用的32波DWDM设备,相邻波长之间的频率间隔为100GHz,其中第一波的中央频率为.11.应用在ZXSM-II上面的SFE8以太网板,它可以完成8个局域网口和8个广域网方向的任意交换,因此组网水平很强;广域网方向的带宽可调,带宽最小为&带宽总和最大为155M.SFE8单板可以传送VLAN业务,除了支持传统的基于端口号的端口组模式外,还支持—干线模式和接入模式.由于VLAN标记头中定义了3个比特用做业务的优先级指示,所以可定义高优先级的业务抢占更高的带宽,实现QOS勺功能.在系统带宽小于业务带宽的时候,为了预防系统口的丢包现象,可以启用单板的流量限制功能.为了预防业务成环,单板软件可以运行生成树协议.在虚拟网桥中创立VLAN之前,需要事先创立一个客户,由于VLAN是由它来治理的,否那么VLAN无法创立.、1310nn1550nm850nm长距、STM-16级另1550nm窗口的光模块.13.在10G设备中假设从OL1X8中抽取时钟,只能从前两路抽取时钟.14,复用段保护发生倒换的条件R-LOSMS-AISLOF〔至少三个〕.15.A1、A2的功能是帧定位.它产牛的主要告警有OOF、LOF F M2字节产生的一对对告告警信息分别为MS-BBEMS-REI,K1,K2字节的功能是复用段倒换信令字节.K1、K2产生的一对对告告警信息分别为MS-AIS、MS-RDI16、ZXSM-10GNCP的运行程序包括NCP程序和数据配置程序两局部,其中NCP程序存储在Flashdisk.II型机的NCP程序存储在EPROM;10G中用telnet命令登录到NCP上,用FTP程序下载NCP程序.四、简做题〔此题共5小题,总分值24分;请把符合题意的答案写在试卷空白处〕1.4个波分通道串连测试,试画出4波系统的误码串联检测方法.〔5分〕2.请解释什么是“会聚〞和“共享〞?〔5分〕共享:多个用户口共享一个系统口;会聚:多个系统口共享一个用户口;3.在SDH环网中,公务和时钟的配置应注意哪些考前须知,为什么?针对这些考前须知应采取哪些措施〔4分〕4、10G设备APS协议处理在交叉板,那k1,k2字节其他板就不要处理,对吗,?请简述理由.〔5分〕5.请画图说明光口和电口的各种环回.〔6分〕五、应用题〔此题共3小题,总分值33分;请把符合题意的答案写在试卷空白处〕注意:应用题必须写出分析过程1、在下面的32路DWDM 系统中,设此合波器的插入损耗为 c 、d 、e 几个功率限制点的单波功率,假设在此系统中,线路的系统衰耗为22db/80km,请给出未加衰耗 器以前c 、d 、e 段光缆的最远传递距离.假设组网初期只用了4波,请给出b 点的合波功率.假设浪光缆只 有60km,D 段光缆为80km,E 段光缆恰好,请在添加必要的衰减器.b 、c 、d 、e 的光功率各1分;光缆距离每段1分,b 点合波2分;衰耗器每加对一个1分,大小正常1分. (请写出分析过程,直接写出答案不得分,共计12分.)答案:A 点OTU 的功率限制为-3dB,根据P Z =P O +10lgn(n=32波),B=-18dB.,所以P b =3dB .C 我的单波功率为5dB .D 点的单波功率为5.E 点的单波功率为5dB .F 点的单波功率为一3dB .(2)、由于C 点使用的是2220的光线路放大器,其增益为22dB.而线路衰耗为80km/22dB ,根据线路放 大器的增益根据线路的衰耗而定的原那么,因此球的最大传输距离为80kmoD 段后的线形放大器的增益 为27,所以其最大传输距离为(27+22)X80=98.18km .E 段的段距为15-(-3)+17]X80+22=90.90km .(3)、当此系统中只承载4波业务时,B 点的分波功率为-18,其合波功率为—18+10lg4=-12dB .(4)、由于C 点的单波功率为5dB,而B 点后的放大器类型为2520,此时B 点的单波光功率应为5-25=-20dBo 而此时的单波为-3-15=-18,因此应在B 点加一个3dB 的衰耗器.由于C 段的距离为60km,此时线路衰减为22X60+80=16.5dB .此时入2220放大器的光功率为5-16.5= -11.5dB .而D 点的光功率为5,因此2220前的光功率应为5-22=-17,因此在C 点应增加一个5dB 的衰耗器. D 段的距离为80km,此时线路衰耗为22dB .此时入2720光放大器的光功率为5-22=-16dB,E 我的单波光功率为5dB ,因此2720光放大器的光功率应为5-27=-22dB .因此应在D 点增加一个5dB 的衰减器.由于E 段的距离恰好,1712放大器恰好可以补偿E 段的线路损耗,因此不需要增加衰耗器.2、如下图子网,A 为网管计算机接入网元,一日用户忽然发现网管计算机无法监控网元,而业务却15db,a 点的光功率限制在3dB,请给出a 、b 、并没有中断,由于网管无法监控到网元,因此用户更换了一块没有任何数据的NCP备板,发现网管还是无法监控到子网,紧接着用户将B的NCP^与A的NC服对调,发现网管仍然无法监控到NCP反请问:用户两次操作会产生什么影响?为什么?〔6分〕网管DB3、如果通道保护环因局方条件不具备〔例如某个站的机房没有建好或光缆没有铺好等因素〕尚未建成, 而数据已下发,那么相应的设备必然会有光接收信号丧失告警,用户觉得告警看着不舒服,所以拿尾纤把告警的光口环了起来,请分析这样做可能出现的问题,并找出解决的方法.〔5分〕4、如下图:A、B两块SFE到.网为点对点的一条链路.A板启用一个用户口Y1和两个系统口XI、X2;B板启用两个系统口XI、X2和一个用户口Y1.用户通过A板的用户口Y1接入到以太网交换机,组网采用虚拟网桥模式,所有的端口位于同一个VLAN.请分析如此组网产生的问题.〔5分〕Y 1L2交换机A B5、时隙配置中,把一个AUG的业务配置到了四块支路板EP1上去,业务均为双向的配置.问时分占用多少?为什么?〔5分〕答案:因级联最多支持三级,现在是一个AUG的业务配置到了四块支路板,所以不再支持级联. 支路板收信号时交叉板可以利用空分并发,发信号时四块支路板都要进时分合成一个AUG送给光板,所以时分占用4Xi。
物化实验课件-实验十四-完全互溶双液系气液平衡相图.docx

完全互溶双液系气液平衡相图的绘制一. 实验目的1. 测定常压下坏己烷一乙醇二元系统的气液平衡数据,绘制沸点一组成相图。
2. 学握双组分沸点的测定方法,通过实验进一步理解分憎原理。
3. 掌握阿贝折射仪的使用方法。
二. 实验原理完全互溶双液系:两液体能按任意比例相互溶解的体系。
依据相律:J' = C + 2・0,当和数①二1, >ar=3,系统的状态需用三维图描述。
如果固定一个变量,f*max-2,系统的状态川二维图描述。
通常周定压力,当固定系统的压力为大气压时,气-液两相平衡温度为沸点温度。
恒压下将完全互溶双 液体系蒸饴,测定饰出物(气相)和蒸馄液(液相)的组成,就能找出平衡时气、液两相的成分并绘l\\ T-x 图。
恒定压力下,真实的完全互溶双液系的气一液平衡相图(厂一力,根据体系对拉乌尔定律的偏差情况, 可分为3类:(1) -般偏差:混合物的沸点介丁-两种纯组分之间,如甲苯一苯体系,如图1(a )所示。
(2) 最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如图 1(b )所示。
(3) 最大正偏差:存在一个鮫大蒸汽压值,比两个纯液体的蒸汽压都犬,混合物存在着最低沸点,如图1 (c ))所示。
后两种情况在T-x 图上有最窩或最低点,这些点称为恒沸点,相应的溶液称为恒沸点混介物。
恒沸点 混合物蒸饰时,所得的气相与液相组成和同,因此通过蒸憎无法改变其组成,精係只能分离出一种纯物质 和另--种恒沸混合物。
本实验的原理:1. 木实验是用冋流冷凝法测定坏己烷〜乙醉体系的沸点~组成图。
2. 在恒压下将溶液蒸饰,测定气相绸出液和液相蒸徭液的组成就能绘出其八兀图。
3. 用阿贝折射仪测定不同组成的体系,在沸点温度时气、液相的折射率,再从折射率~组成工作曲线上 査得相应的组成,然后绘制T_x 图三. 仪器与试剂(1) 仪器:恒温槽1台;阿贝折射仪1台;沸点仪1套;移液管(lml 2支、10ml 1支);具塞小试管9X B(a)(b) (c)图1二组分真实液态混合物气一液平衡相图 (T-x 图)支(2)试剂:环己烷(A.R.):无水乙醇(A.R.)图2 图3(1).沸点仪结构(图2)1 •温度计;2•进样口:3■加热丝;4•气相冷凝液取样口5-气相冷凝液(2)阿贝折射仪(图3)1 •底座;2-棱镜转动手轮;3•圆盘组(内有刻度板);4-小反光镜;5-支架;6-读数镜筒;7■•目镜;8■■望远镜筒;9-示值调节螺钉;10-阿米西棱镜手轮;11-色散值刻度圈;12-棱镜锁紧扳手;13-棱镜组;14 •温度计座;15-恒温器接头:16-保护罩:17•主轴:18 •反光镜四.实验步骤:1.调节恒温桝温度,通恒温水丁-阿贝折射仪中。
实验四双液系的气——液平衡相图的绘制

向港040940538实验四双液系的气——液平衡相图的绘制一、实验目的1、用沸点仪测定大气压下—环己烷或异丙醇—环己烷双液系气—液平衡时气相与液相组成及平衡温度,绘制温度--组成图,确定恒沸混合物的组成及恒沸点的温度。
2、了解物化实验中光学方法的基本原理,学会阿贝折光仪的使用。
3、进一步理解分馏原理。
二、实验原理两种在常温时为液态的物质混合起来而组成的二组分体系成为双液系。
两种液体若能按任意比例互相溶解,成为完全互溶的双液系;若只能在一定比例范围内互相溶解,则称部分双液系。
双液系的气相平衡相图可分为三类。
这些图的纵轴是温度(沸点),横轴是代表液体B的摩尔分数。
在图中有两条曲线:上面的曲线是气相线,表示在不同溶液的沸点与溶液成平衡时的气相组成,下面的曲线表示液相线,代表平衡时液相的组成。
三、实验仪器和药品1.实验仪器仪器名称数量仪器名称数量玻璃沸点仪一套阿贝折光仪一台WLS系列可调式恒流电源一台SWJ型精密数字温度计一台SYC超级恒温槽一台2.药品异丙醇环己烷四、实验步骤1.按要求连接好实验装置。
注意:感温杆勿与电热丝相碰。
2.接通冷凝水,用超级恒温槽完成冷凝循环。
量取35ml异丙醇从测管加入蒸馏瓶内,并时传感器浸入溶液3㎝左右。
将加热丝接通恒流电源,将电流调定1.1安,使电热丝将液体加热至缓慢沸腾,待温度基本恒定后,再连同支架一起倾斜蒸馏瓶,使小槽中气相冷凝液倾回蒸馏瓶内,重复三次,记下乙醇的沸点及环境气压。
3.依次再加入2、6、12、20ml环己烷,同上法测定溶液的沸点和吸取气、液相并测其折射率。
4.将溶液倒入回收瓶。
5.从侧管加入35ml环己烷,测其沸点。
6.依次加入2、4、10、16ml异丙醇,按上法测其沸点和吸取气、液相并测其折射率。
7.关闭仪器和冷凝水,将溶液倒入回收瓶。
五、实验注意现象1.沸点仪中没有装入溶液之前绝对不能通电加热,如果没有溶液,通电加热丝时,沸点仪会炸裂。
2.一定要在停止通电加热之后,方可取样进行分析。
物理化学-实验六:双液系气-液平衡相图

物理化学-实验六:双液系⽓-液平衡相图实验六双液系⽓—液平衡相图的绘制⼀、实验⽬的及要求1.掌握回流冷凝法测定溶液沸点的⽅法。
2.绘制环⼄烷-异丙醇双液系的沸点-组成图,确定其恒沸组成和恒沸温度。
3.了解阿贝(Abbe)折射仪的构造原理,掌握阿贝(Abbe)折射仪的使⽤⽅法。
⼆、实验原理常温下,两种液态物质相互混合⽽形成的液态混合物,称为双液系,若两种液体能按任意⽐例相互溶解,则称为完全互溶双液系。
液体的沸点是指液体的饱和蒸⽓压和外压相等时的温度。
在⼀定的外压下,纯液体的沸点是恒定的。
但对于完全互溶双液系,沸点不仅与外压有关,⽽且还与其组成有关,并且在沸点时,平衡的⽓-液两相组成往往不同。
在⼀定的外压下,表⽰溶液的沸点与平衡时⽓-液两相组成关系的相图,称为沸点-组成图, 即T~ X。
完全互溶双液系的沸点-组成图可分为三类:(1)液体与拉乌尔定律的偏差不⼤,在T~ X图上,溶液的沸点介于⼆种纯液体沸点之间(见图1(a)),如苯-甲苯系统等。
(2)实际溶液由于两组分的相互影响,常与拉乌尔定律有较⼤的负偏差,在T~X图上溶液存在最⾼沸点(见图1(b)),如卤化氢-⽔系统等。
(3)实际溶液与拉乌尔定律有较⼤的正偏差,在T~ X图上溶液存在最低沸点(见图1(c)),如⽔-⼄醇、苯-⼄醇系统等。
2、3类溶液,在最⾼或最低沸点时的⽓-液两相组成相同,这些点称为恒沸点,此浓度的溶液称为恒沸点混合物。
相应的最⾼或最低沸点称为恒沸温度,相应的组成称为恒沸组成。
本实验所要测绘的环已烷-异丙醇系统的沸点-组成图即属于图1(c)类型,其绘制原理如下:图1 完全互溶双液系的沸点-组成图当系统总组成为x的溶液加热时,系统的温度沿虚线上升,当溶液开始沸腾时,组成为y的⽓相开始⽣成,继续加热,则系统的温度继续上升,同时⽓-液两相的组成分别沿⽓相线和液相线上箭头指⽰⽅向变化,两相的相对量遵守杠杆规则⽽同时发⽣变化。
显然,若设法保持⽓-液两相的相对量⼀定,就可使得系统的温度恒定不变。
双液系气液平衡相图的绘制

五、 实验结果讨论 1.对于二组分,自由度f=2-Φ+2(T,P), Φ=1,f=3(T,P,X B ),为三维相图,不便于作图。 若固定P,则f*=3-Φ, Φ=1 时f=2(T,X B ),即可得到T-X平面图。相当于立体图在一个平面 上的投影。 由所得相图可看到气相线、 液相线。 它们将相图分为三个部分, 气相区 (气 相线上方) 、液相区(液相线下方) 、气液共存区(区域Ⅰ和Ⅱ) 。同一温度下,区域 Ⅰ中B组分的气相组成总是大于液相组成,区域Ⅱ中液相组成大于气相组成。蒸气中 富集的总是能降低溶液沸点的组分。沿着直线 1 降温: ① AB 段为混合蒸气,Φ=1,f=2,温度与组成可在此区域自由变化 ② B 点开始出现液相,开始进入 BC 段气液共存区,Φ=2,f=1,温度与组成只 有一个可自由变化 ③ 到 C 点气相消失,继续降温,进入液相区,Φ=1,f=2,温度与组成可在此区 域自由变化。 图中存在一个最低共沸点M(42.05,69.6)。在M处,自由度f=0,即T,X B 均不能任意改变。 此处气液相组成相同,共沸点温度t=69.6℃,x B =y B =42.05%。若由过M点的直线 2 降 温,则系统由气相区,经过共沸点直接进入液相区。 2.最低共沸点的出现,是由于对 Raoult 定律产生正偏差造成的(体系的总蒸气压和蒸气 分压的实验值均大于拉乌尔定律 P=P*x 的计算值)。产生偏差的可能原因很多,分子 环境发生变化,使得 分子间作用力改变而引起挥发性的改变。当同类分子间引力大于 异类分子间引力时,混合后作用力降低,挥发性增强,产生正偏差。若混合后分子发 生缔合或解离现象引起挥发性改变。若离解度增加或缔合度减少,蒸气压增大,产生
1.3990 1.3947 1.3819
1.3840 1.3795 1.3757
双液系的气液平衡相图(物理化学实验)

双液系的气液平衡相图实验者:林澄昱生04 2010030007 同组者:张弯弯实验日期:2012-03-10 提交日期:2012-03-16实验指导:刘晓惠1引言两种蒸气压不同的挥发性液体在混合之后,其溶液组成与与其平衡气相的组成不同。
在恒外压下,二组分系统达到气液平衡时,表示液态混合物的沸点与平衡时气液两相组成关系的相图,称为沸点和组成(T-x)图。
大致分为三大类,包括:(1)理想液体混合物或接近理想液体混合物的双液系,其混合物沸点介于两纯物质沸点之间。
见图1(a);(2)各组分蒸气压对拉乌尔定律产生很大的负偏差,有最高恒沸点。
见图1(b);(3)各组分蒸汽压对拉乌尔定律产生很大的正偏差,有最低恒沸点。
见图2(c)1。
图1 三类沸点组成(T-x)图本实验为了绘制常压下环己烷-乙醇的气液平衡相图,先利用阿贝折射仪测定一系列已知组成混合溶液及纯液体的折射率,绘制标准曲线,再通过沸点仪测定一系列混合溶液的沸点,收集少量气相冷凝液以及溶液,测定其各自折射率,反查标准曲线得到气液两相的组成,绘得双液系的气液平衡相图。
2实验操作2.1实验药品、仪器及测试装置示意图2.1.1实验药品环己烷,无水乙醇;2.1.2实验仪器沸点仪,调压器,温度传感器,锥形瓶,分析天平(AR2140),阿贝折射仪(型号不明,为靠近恒温箱的一台),恒温箱,胶头滴管,10ml吸量管,洗耳球;2.1.3装置示意图1. 冷却水入口2. 气相冷凝液贮存小泡3. 温度传感器4. 喷嘴5. 电热丝6. 调压器2图2 沸点仪2.2实验条件恒温槽温度:26 ℃室温:未测气压:未测2.3实验操作步骤及方法要点2.3.1标准曲线的测定及绘制2.3.1.1标准溶液的配制取5个干燥、洁净的锥形瓶,编号为1~5,分别称量空瓶质量并记录;依照表1分别量取并加入相应体积的环己烷和无水乙醇,每加入一种溶液以后称量其质量并记录;得到5份已知组分的标准溶液。
表1 标准溶液的配制方案通过称量得到的质量,可以计算得到每锥形瓶中液体含有的环己烷质量分数,通过测定其折射率,可以确定特定环己烷质量分数与折射率的关系;同时,直接量取纯的无水乙醇和环己烷,测定其折射率,可以绘制在环己烷质量分数在0~1之间的无水乙醇混合溶液与折射率的关系曲线。
双液系气液平衡相图的绘制实验报告

双液系沸点-组成图测绘实验报告实验时间:2015年4月15日学号:1120132970 一、目的要求1.测定相应组成时的沸点并制作常压下环已烷—无水乙醇双液系的平衡相图。
2.从沸点组成图了解分馏原理。
3.了解沸点的测定技术,掌握两组分液体沸点的测定方法。
4.掌握折光率与组成的关系及阿贝折光仪的测量原理和使用方法。
二.实验原理1、由液态物质混合而成的二组分系统称为双液系统。
若两液体能以任意比例互溶,称其为完全互溶双液系,若两液体只能部分互溶,称其为部分互溶双液系。
一个完全互溶的二元体系,两个纯液体组分在所有组成范围内完全互溶。
在定压下,完全互溶的二元体系的沸点—组成图可分为三类,如图C7.1所示。
a.溶液的沸点介于两纯组分沸点之间,如苯一甲苯体系;b.溶液有最低恒沸点,如环己烷-乙醇体系;c.溶液有最高恒沸点,如丙酮—氯仿体系。
下面以a为例,简单说明绘制沸点-组成图的原理。
加热总组成为x1的溶液,体系的温度上升,达液相线上1点时溶液开始沸腾,组成为x2的气相开始生成,但气相量很少,趋于0,x1、x2二点代表达到平衡时液、气两相组成。
继续加热,气相量逐渐增多,沸点继续上升,气、液二相组成分别在气相线和液相线上变化,当达某温度(如2点)并维持温度不变时,则x3、x4为该温度下液、气两相组成,气相、液相的量之比按杠杆规则确定。
从相律f = c - p +2可知:当外压恒定时,在气、液两相共存区域自由度等于1;当温度一定时,则气、液两相的组成也就确定,总组成一定,由杠杆规则可知两相的量之比也已确定。
因此,在一定的实验装置中,全回流的加热溶液,在总组成、总量不变时,当气相的量与液相的量之比也不变时(达气-液平衡),则体系的温度也就恒定。
分别取出气、液两相的样品,分析其组成,得到该温度下气、液两相平衡时各相的组成。
改变溶液总组成,得到另一温度下气、液两相平衡时各相的组成。
测得溶液若干总组成下的气液平衡温度及气、液相组成,分别将气相点用线连接即为气相线,将液相点用线连接即为液相线,得到沸点-组成图。
实验五 双液系气液平衡相图

实验五双液系气液平衡相图一、实验目的1. 绘制在p0下环已烷—异丙醇双液系的气液平衡相图,了解相图和相律的基本概念;2. 掌握回流冷凝法测定双组分液体的沸点及正常沸点的方法;3. 了解阿贝折光仪的构造原理,熟悉掌握用折光率确定二元液体组成的方法。
二、实验原理1、气—液相图图根据相律f=C-Φ+2,对于一个气—液共存的二组分体系,其自由度f=2,若再确定一个变量,整个体系的存在状态就可以用二维图形来描述。
通常测定一系列不同配比溶液的沸点及气液两相的组成,就可绘制气—液相图。
压力不同时,双液系的相图将略有差异。
本实验要求将外压校正到101325kPa。
完全互溶双液系恒定压力下的沸点-组成图可以分成三类:⑴溶液沸点介于两纯组分沸点之间(图5.1);⑵溶液存在最低沸点(图5.2);⑶溶液存在最高沸点(图5.3)。
t/ ℃ p=常数 t/ ℃ p=常数 t/ ℃ p=常数g g gl l lA x B→B A x B→ B A x B→ B图5.1 图5.2 图5.3 图5.2、图5.3有时被称为具有恒沸点的双液系。
和图5.1根本的区别在于,系统处于恒沸点时气、液两相的组成相同。
因而不能象第一类那样通过反复蒸馏而使两种组分完全分离。
如果进行简单的反复蒸馏只能得到某一纯组分和组成为恒沸点相应组成的混合物。
如果要获得两纯组分需要采用其它的方法。
系统的最高或最低恒沸点即为恒沸温度,恒沸温度对应的组成为恒沸组成。
异丙醇-环己烷双液系属于具有最低恒沸点一类的系统。
2、沸点测定仪本实验所用沸点仪如图5.4所示的。
本实验是利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成沸点图5.4沸点仪精密温度计;2.磨口塞;3.电加热丝;4.冷凝管;5.气相凝聚液。
数据可直接由温度计获得,气、液相组成可通过测定其折光率,然后由组成-折光率曲线中最后确定。
三、仪器试剂沸点仪1套;恒温槽1台;阿贝折射仪1台;移液管(1mL)2支;量筒3只;小试管9支;异丙醇(分析纯);环已烷(分析纯)。
物化实验报告 双液系的气液平衡相图

USTC 3 系 摘要:水和正丙醇的完全互溶溶液,当组成不同时其沸点和气相、液相的成分也不同。本实 验通过测量不同组成下的水和正丙醇的溶液在沸点时气相和液相的折射率, 由正丙醇-水溶 液折光率与组成工作曲线可查出对应折射率的组分。 由于温度测量存在误差, 实验中对测量 温度计进行露茎校正和压力校正。由实验结果便可作出水-正丙醇的气液平衡相图。 关键词 :沸点 折射率 温度校正 气液平衡相图。
沸点仪的设计虽各有异,但其设计思想都集中在 如何正确地测定沸点和气液相的组成,以及防止过热 和避免分馏等方面。我们所使用的沸点仪如图 5-4 所 示: 这是一只带有回流冷凝管的长颈圆底烧瓶,冷凝 管底部有一球形小室 D,用以收集冷凝下来的汽相样 品。液相样品则通过烧瓶上的支管 L 抽取,图中 E 是 一根用 300W 的电炉丝截制而成的电加热丝,直接浸 入溶液中加热,以减少溶液沸腾时的过热暴沸现象。 温度计安装时须注意使水银球一半浸在液面下,一半 露在蒸气中,并在水银球外围套一小玻璃管 C,这样, 溶液沸腾时,在气泡的带动下,使气液不断喷向水银 球而自玻璃管上端溢出;小玻璃管 C 还可减少沸点周 围环境(如空气流动或其它热源的辐射)对温度计读 数可能引起的波动,因此这样测得的温度就能较好地 代表气液两相的平衡温度。 分析平衡时气相和液相的组成,须正确取得气相 和液相样品。沸点仪中蒸气的分馏作用会影响气相的 图 5-4 沸点仪 平衡组成,使取得的气相样品的组成与气液平衡时的 A-盛液容器; B-测量温度计; 组成产生偏差,因此要减少气相的分馏作用。本实验 C-小玻管; D-小球; E-电热丝 中所用沸点仪是将平衡时的蒸气凝聚在小球 D 内,在 F-冷凝管; G-温度计; L-支管 容器 A 中的溶液不会溅入小球 D 的前提下,尽量缩短 小球 D 与大球 A 的距离,为防止分馏,尽量减少小球 D 的体积即可达此目的。为了加速达 到体系的平衡,可把 D 球中最初冷凝的液体倾回到容器 A 中。 沸点的测定 用玻璃水银温度计测量溶液的沸点,如图 5-5,固定在沸点仪上的水银温度计是全浸式 的,使用时除了要对温度计的零点和刻度误差等因素进行校正外,还应作露茎校正。这是由 于温度计未能完全置于被测体系中而引起的。 根据玻璃与水银膨胀系数的差异, 校正值的计 算式为: t 露/℃=1.610-4·n·(t 观-t 环) 校正的方法是在测量沸点的温度计 B 旁再固定一支同样精度的温度计 G, G 的水银球底 部应置于测量温度计沸点稳定值至固定温度计橡皮塞露出那一段水银柱的中部。 读沸点时同 时读取温度计 G 上的读数,得到温度 t 观和 t 环。在测量过程中,由于组成的变动,t 观也在变 动,因此温度计 G 的位置也应随着沸点稳定值而进行调整,始终让其置于温度计 B 露出水 银柱的中部。式中的 n 是露出那段水银柱的长。1.610-4 是水银对玻璃的相对膨胀系数。 沸点除了要进行露茎校正外,还需要进行压力校正。标准大气压下( P=760mmHg 或 101325Pa)测得的沸点为正常沸点。实际测量时,压力一般都不恰好为标准大气压。应用特 鲁顿规则及克劳修斯-克拉贝龙公式,可得溶液沸点随大气压变动而变动的近似值:
双液系气液平衡相图的绘制(华南师范大学物化实验)

双液系气—液平衡相图的绘制一、实验目的(1)用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图.找出恒沸点混合物的组成及恒沸点的温度.(2)掌握测定双组分液体的沸点及正常沸点的测定方法.(3)了解阿贝折射计的构造原理,熟悉掌握阿贝折射计的使用方法。
二、实验原理2。
1液体的沸点液体的沸点是液体饱和蒸汽压和外压相等时的温度,在外压一定时,纯液体的沸点有一个确定值。
2。
2双液系的沸点双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关.理想的二组分体系在全部浓度范围内符合拉乌尔定律。
结构相似、性质相近的组分间可以形成近似的理想体系,这样可以形成简单的T —x (y )图。
大多数情况下,曲线将出现或正或负的偏差.当这一偏差足够大时,在T —x(y )曲线上将出现极大点(负偏差)或极小点(正偏差)。
这种最高和最低沸点称为恒沸点,所对应的溶液称为恒沸混合物.恒定压力下,真实的完全互溶双液系的气-液平衡相图(T -x ),根据体系对拉乌尔定律的偏差情况,可分为3类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a )所示。
(2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸—水体系,如图1(b )所示。
(3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合物存在着最低沸点,如水-乙醇体系,如图1(c ))所示。
图1. 二组分真实液态混合物气-液平衡相图(T —x 图)考虑综合因素,实验选择具有最低恒沸点的乙醇—乙酸乙酯双液系。
根据相平衡原理,对二组分体系,当压力恒定时,在气液平衡两相区,体系的自由度为1.若温度一定时,则气液亮相的组成也随之而定。
当溶液组成一定时,根据杠杆原t AtAt At Bt B t Bt / o Ct / o t / o x Bx Bx B ABAABB(a)(b)(c)x 'x '理,两相的相对量也一定。
双液系的气液平衡相图-物化实验报告
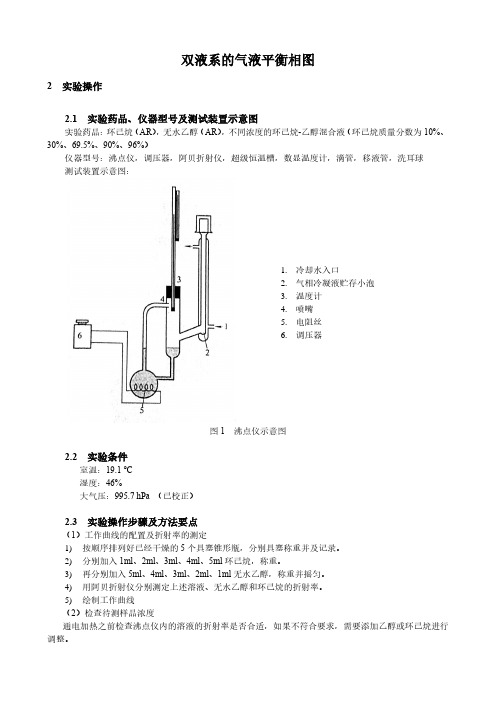
双液系的气液平衡相图2 实验操作2.1 实验药品、仪器型号及测试装置示意图实验药品:环己烷(AR),无水乙醇(AR),不同浓度的环己烷-乙醇混合液(环己烷质量分数为10%、30%、69.5%、90%、96%)仪器型号:沸点仪,调压器,阿贝折射仪,超级恒温槽,数显温度计,滴管,移液管,洗耳球测试装置示意图:1.冷却水入口2.气相冷凝液贮存小泡3.温度计4.喷嘴5.电阻丝6.调压器图1 沸点仪示意图2.2 实验条件室温:19.1 ℃湿度:46%大气压:995.7 hPa (已校正)2.3 实验操作步骤及方法要点(1)工作曲线的配置及折射率的测定1)按顺序排列好已经干燥的5个具塞锥形瓶,分别具塞称重并及记录。
2)分别加入1ml、2ml、3ml、4ml、5ml环己烷,称重。
3)再分别加入5ml、4ml、3ml、2ml、1ml无水乙醇,称重并摇匀。
4)用阿贝折射仪分别测定上述溶液、无水乙醇和环己烷的折射率。
5)绘制工作曲线(2)检查待测样品浓度通电加热之前检查沸点仪内的溶液的折射率是否合适,如果不符合要求,需要添加乙醇或环己烷进行调整。
(3)测定各溶液达到汽液平衡时的气相和液相组成打开冷却水,接通电源,慢慢调节调压器电压进行加热,直到溶液沸腾或者出现小气泡,再将电压调到33V。
待温度恒定后,记下该温度值,关电压,停止加热,同时用长滴管从冷凝管上口在小泡中取气相冷凝液,迅速测定折射率,液相溶液稍冷后,从温度计口取液相溶液测定折射率(沸腾过程已经使液相混合比较均匀了,类似“鼓泡法”;而且实际上也没有地方伸入滴管进行搅拌)。
如果沸点仪圆底烧瓶内液体快要蒸干了、电阻丝没有浸泡在液体中,就要及时补充溶液,否则体系内温度会急剧上升。
如果液面低于烧瓶侧面支管口,应及时补充液体,否则无法取液相溶液。
补充溶液时,要等到体系冷却下来。
3 结果与讨论3.1 原始实验数据表1 环己烷-乙醇混合液(标准液)的折射率序号空瓶质量/g瓶+乙醇质量/g瓶+混合液质量/g折射率129.932130.624634.4739 1.3701231.016832.487935.5774 1.3810331.169233.423335.6596 1.3926427.875530.927732.4152 1.4040528.387232.241132.9446 1.41696无水乙醇 1.36387纯环己烷 1.4284表2 环己烷-乙醇混合液(待测液)沸点及气相、液相的折射率序号环己烷质量分数温度/℃气相冷凝液折射率液相折射率1077.56 1.3638 1.3634210%75.63 1.3704 1.3654330%73.16 1.3825 1.3668469.50%64.42 1.3978 1.3817590%64.65 1.4072 1.4162696%67.26 1.4108 1.42417100%80.13 1.4278 1.4272 3.2计算的数据、结果(1)绘制折射率-组成工作曲线根据表1数据计算出各个标准溶液对应的环己烷质量分数,如表3。
双液系气液平衡相图-物理化学实验
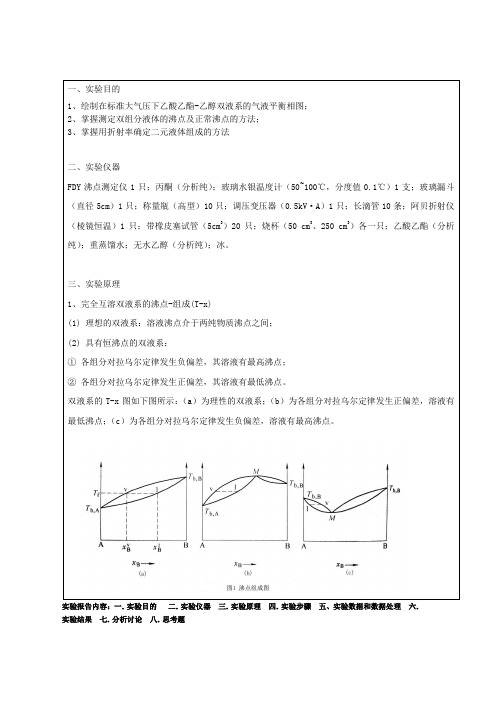
一、实验目的1、绘制在标准大气压下乙酸乙酯-乙醇双液系的气液平衡相图;2、掌握测定双组分液体的沸点及正常沸点的方法;3、掌握用折射率确定二元液体组成的方法二、实验仪器FDY沸点测定仪1只;丙酮(分析纯);玻璃水银温度计(50~100℃,分度值0.1℃)1支;玻璃漏斗(直径5cm)1只;称量瓶(高型)10只;调压变压器(0.5kV·A)1只;长滴管10条;阿贝折射仪(棱镜恒温)1只;带橡皮塞试管(5cm3)20只;烧杯(50 cm3、250 cm3)各一只;乙酸乙酯(分析纯);重蒸馏水;无水乙醇(分析纯);冰。
三、实验原理1、完全互溶双液系的沸点-组成(T-x)(1) 理想的双液系:溶液沸点介于两纯物质沸点之间;(2) 具有恒沸点的双液系:①各组分对拉乌尔定律发生负偏差,其溶液有最高沸点;②各组分对拉乌尔定律发生正偏差,其溶液有最低沸点。
双液系的T-x图如下图所示:(a)为理性的双液系;(b)为各组分对拉乌尔定律发生正偏差,溶液有最低沸点;(c)为各组分对拉乌尔定律发生负偏差,溶液有最高沸点。
实验报告内容:一实验目的二实验仪器三实验原理四实验步骤五、实验数据和数据处理六实验结果七.分析讨论八.思考题2、沸点测定仪本实验所用沸点仪是一只带回流冷凝管的长颈圆底烧。
冷凝管底部有一半球形小室,用以收集冷凝下来的气相样品。
电热丝直接加热液体以减少溶液沸腾时的过热现象及防止瓶暴沸。
小玻璃管有利于降低周围环境对温度计读数可能造成的波动。
3.组成分析本实验选用的乙酸乙酯和乙醇两者折射率相差颇大,而折射率测定又只需要少量样品,所以可用折射率-组成工作曲线来测得平衡体系的两相组成。
4、相图的绘制为了绘制二元双液系的T-x图,需在气液相达平衡后,同时测定气相组成、液相组成和溶液沸点。
实验装置图如图所示:四、实验步骤(1) 安装沸点仪并接通冷凝水;(2) 将乙醇加入沸点仪内,加热至缓慢沸腾(3) 记录乙醇的沸点(4) 测定乙醇的折射率(5) 加入不同摩尔分数的乙酸乙酯-乙醇溶液(6) 记录沸点(7) 吸取气相冷凝液、液相冷凝液测定折射率(8) 将溶液倒入回收瓶(9) 绘制曲线五、实验数据和数据处理室温:25℃大气压:100kPa M无水乙醇=46.07g/mol、M乙酸乙酯=88.11g/mol ρ无水乙醇=0.79g·mol-1ρ乙酸乙酯=0.902g·mol-1无水乙醇体积(ml) 乙酸乙酯体积(ml) 乙酸乙酯浓度(mol%)折射率n90 10 0.063 1.36380 20 0.131 1.36470 30 0.206 1.36560 40 0.287 1.36650 50 0.377 1.36740 60 0.476 1.36830 70 0.585 1.36920 80 0.707 1.37010 90 0.845 1.371 根据乙酸乙酯浓度与折射率,作图如下:添加直线拟合线及拟合方程,由拟合方程式可知:x=(y-1.3626)/0.0104室温:25℃大气压:100kPa混合体系沸点气相冷凝液折射率n 液相冷凝液折射率n 气相组成液相组成78 -- --0 076.8 1.3635 1.3626 0.0865 0.000076.2 1.3642 1.3629 0.1538 0.028875.5 1.3648 1.3632 0.2115 0.057774.7 1.3655 1.3635 0.2788 0.086574 1.3663 1.3642 0.3558 0.153873.3 1.3668 1.3651 0.4038 0.240472.6 1.3673 1.3659 0.4519 0.317372 1.368 1.3672 0.5192 0.442372.7 1.3695 1.3701 0.6635 0.721273.4 1.3697 1.3703 0.6827 0.740474.8 1.3703 1.3709 0.7404 0.798175.5 1.3708 1.3712 0.7885 0.826976.2 1.3713 1.3715 0.8365 0.855876.7 1.3716 1.3717 0.8654 0.875077 -- -- 1 1 查询数据可知:无水乙醇沸点:78℃乙酸乙酯沸点:77℃;由图可知在液相组成时,混合体系沸点76.8℃对应的值为0.0000;此数值属于误差,应当剔除。
完全互溶双液系气液平衡相图的绘制。实验报告

完全互溶双液系气液平衡相图的绘制一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3.掌握阿贝折射仪的使用方法。
二.实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-x),根据体系对拉乌尔定律的偏差情况,可分为3类:(1)一在工作曲线上找出未知溶液的组成。
三.仪器与试剂沸点仪,阿贝折射仪,调压变压器,超级恒温水浴,温度测定仪,长短取样管。
环己烷物质的量分数x环己烷为0、0.2、0.4、0.6、0.8、1.0的环己烷-乙醇标准溶液,已知101.325kPa下,纯环己烷的沸点为80.1℃,乙醇的沸点为78.4℃。
25℃时,纯环己烷的折光率为1.4264,乙醇的折光率为1.3593。
四.实验步骤:1.环己烷-乙醇溶液折光率与组成工作曲线的测定调节恒温槽温度并使其稳定,阿贝折射仪上的温度稳定在某一定值,测量环己烷-乙醇标准溶液的折光率。
为了适应季节的变化,可选择若干温度测量,一般可选25℃、30℃、35℃三个温度。
2. 无水乙醇沸点的测定将干燥的沸点仪安装好。
从侧管加入约20mL无水乙醇于蒸馏瓶内,并使传感器(温度计)浸入液体内。
冷凝管接通冷凝水。
按恒流源操作使用说明,将稳流电源调至1.8-2.0A,使加热丝将液体加热至缓慢沸腾。
液体沸腾后,待测温温度计的读数稳定后应再维持3~5min以使体系达到平衡。
在这过程中,不时将小球中凝聚的液体倾入烧瓶。
记下温度计的读数,即为无水乙醇的沸点,同时记录大气压力。
3. 环己烷沸点的测定同2步操作,测定环己烷的沸点。
大学物化实验报告--双液系的气—双液系的气—液平衡相图(精编文档).doc

【最新整理,下载后即可编辑】实验目的与要求:1. 绘制常压下环己烷-乙醇双液系的气液平衡相图(T—X图),了解相图和相律的基本概念;2. 掌握测定双组分液体的沸点及正常沸点的方法;3. 掌握用折光率确定二元液体组成的方法。
实验原理:常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
恒压下将完全互溶双液体系蒸馏,测定馏出物(气相)和蒸馏液(液相)的组成,就能找出平衡时气、液两相的成分并绘出T—X图。
通常,如果液体与拉乌尔定律的偏差不大,在T—X图上溶液的沸点介于A、B二纯液体的沸点之间见图1 (a)。
而实际溶液由于A、B二组分的相互影响,常与拉乌尔定律有较大偏差,在T—X图上就会有最高或最低点出现,这些点称为恒沸点,其相应的溶液称为恒沸点混合物,如图1(b),(c)所示。
恒沸点混合物蒸馏时,所得的气相与液相组成相同,因此通过蒸馏无法改变其组成。
图1 完全互溶双液系的相图图2 沸点仪 1.温度计;2.加料口;3.加热丝;4.气相冷凝液取样口;5.气相冷凝液本实验采用回流冷凝的方法绘制环己烷-乙醇体系的T —X 图。
其方法是用阿贝折射仪测定不同组分的体系在沸点温度时气相、液相的折射率,再从折射率—组成工作曲线上查得相应的组成,然后绘制T —X 图 仪器与试剂:沸点仪1套 超级恒温槽1台WZS -I 型阿贝折光仪25ml 量筒、小漏斗、滴管、大烧杯无水乙醇 , 环己烷,x 环己烷 各为0.1,0.3,0.5,0.7,0.95的乙醇溶液。
(250mL 试剂瓶盛装)注:x 环己烷 为环己烷的物质的量分数浓度,定义为乙醇环己烷环己烷环己烷n n n x +=个人实验图乙醇/环己烷平衡相图温度/℃908070600.000.200.400.600.80 1.00 1.20环己烷%最低恒沸物的沸点64.9℃。
双液系气液平衡相图的测绘实验流程

为二进制系统绘制气体—液体平衡相图的实验涉及多个步骤。
一,实验设置必须做好准备。
这包括装配必要的设备,如高压反应堆、供气系统和温度控制系统。
反应堆在使用前应小心清洗和干燥,以确保实验的准确性。
一旦设置完成,下一步就是准备样本解决方案。
这涉及按预期比例衡量和混合二进制的两个组成部分。
必须注意确保解决办法完全混合,避免任何可能影响实验结果的杂质。
在样品溶液制备后,它们被引入高压反应堆,然后用期望的气体密封并加压。
随后反应堆被置于温度控制系统中,其中温度逐渐上升或下降,以探索系统在一系列温度中的相位行为。
在实验中,气体和液体相的样品是在不同的温度和压力下采集的。
然后利用气相色谱或光谱测量等技术对这些样品进行分析,以确定每个阶段的构成。
这些数据对构建相位图至关重要。
实验数据被绘制在一个图表上,为二进制系统构建气体—液体平衡相图。
本图显示了气温,气压,气相和液相的构成之间的关系。
通过分析相位图,可以得到关于二进制系统的相位行为和热力学性质的宝贵信息。
为二进制系统绘制气体—液态平衡相图的过程是一项复杂而复杂的实
验,需要仔细准备、精确测量和严格分析。
然而,从这一实验中获得的结果可以为系统在不同条件下的行为提供有价值的洞察力,这对于各种工业工艺和应用都是至关重要的。
完全互溶双液系气液平衡相图的绘制

完全互溶双液系气液平衡相图的绘制一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3.掌握阿贝折射仪的使用方法及原理。
4.了解和掌握沸点仪的测定原理及方法。
5.加深对完全互溶双液系气液平衡相图的理解和增强个人动手能力。
二.实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-x图),根据体系对拉乌尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。
(2)最大负偏差:存在一个最小蒸气压值,比两个纯液体的蒸气压都小,混合物存在着最高沸点,如盐酸-水体系,如图1 (b)所示。
(3)最大正偏差:存在一个最大蒸气压值,比两个纯液体的蒸气压都大,混合物存在图1 二组分真实液态混合物气-液平衡相图(T-x图)着最低沸点,如正丙醇—水体系,如图1(c))所示。
对于后两种情况,为具有恒沸点的双液系相图。
它们在最低或最高恒沸点时的气相和液相组成相同,因而不能象第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。
为了绘制双液系的T -x 相图,需测定几组原始组成不同的双液系在气-液两相平衡后的沸点和液相、气相的平衡组成。
本实验以环己烷-乙醇为体系,该体系属于上述第三种类型。
在沸点仪(如图2所示)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T -x 相图。
本实验中气液两相的组成均采用折光率法测定。
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
正后:t 沸=t 观+Δt 露茎。
编号
1 2 3 4 5 6 7 8 9 10
乙醇体积分数
/% 100 90 70 50 38 22 15 10
5 0
h/℃
t 观/℃
t 环/℃
表 1.露茎校正数据记录
Δt 露茎/℃ t 沸/℃
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-x),根据体 系对拉乌尔定律的偏差情况,可分为 3 类:
(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如 图 1(a)所示。
(2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小, 混合物存在着最高沸点,如盐酸—水体系,如图 1(b)所示。
双液系气液平衡相图的绘 制华南师范大学物化实验
The Standardization Office was revised on the afternoon of December 13, 2020
双液系气-液平衡相图的绘制 一、实验目的
(1)用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图。找出恒沸 点混合物的组成及恒沸点的温度。 (2)掌握测定双组分液体的沸点及正常沸点的测定方法。 (3)了解阿贝折射计的构造原理,熟悉掌握阿贝折射计的使用方法。
四、数据处理
溶液沸点的校正 (1)由于温度计的水银未全部浸入待测温度的区域内而需进行露茎校正。
Δt 露茎=Kh(t 观-t 环)
式中,K=,是水银对玻璃的相对膨胀系数;h 为露出于被测体系之外的水
银柱长度,称露茎高度,以温度差值表示;t 观为测量温度计上的读数;t 环为环
境温度,可用辅助温度计读出,其水银球置于测量温度计露茎的中部。露茎校
平衡,可以等小槽中气相冷凝液体收集满后,调节冷凝管的三通阀门,使冷凝
液体流回圆底烧瓶,重复三次,直到温度计上的读数稳定数分钟,记录温度计
的读数,同时读出环境的温度;算出露茎温度,以便进行温度校正,并读出室 内大气压力。 取样
切断电源,停止加热,在冷凝管三通小槽处放置一个标有相应浓度记号的 尾接小试管,并调节冷凝管的三通阀门,使冷凝液体不再流回至圆底烧瓶,而 是流入尾接小试管中,并立即塞紧,防止其挥发;再用另一支干燥胶头滴管, 从侧管处吸取容器中的溶液约 1~2mL,转移到另一个小试管,也立即塞紧,两 支小试管置于盛有冷水的小烧杯中保持待测,以防组分改变。在样品的转移过 程中动作要迅速而仔细。并应尽早测定样品的折射率,不宜久藏。当沸点仪内 液体冷却后,将该溶液自侧管倒入到指定的回收瓶中,再换另一浓度的双液体 系溶液测定。 折射率的测定
分别测定上面取的气相和液相样品的折射率。每次加样要测读两次,若读 得的两个数值很接近,则取其平均值。每次加样前测量之前,必须先将折光仪 的棱镜面洗净,方法是用数滴挥发性溶剂(如丙酮)淋洗,再用擦镜纸轻轻擦 去残留在镜面上的溶剂,阿贝折射计在使用完毕后也必须将镜面处理干净。 平衡气相和液相组成的测定
根据气相折射率的数据,在工作曲线 n-x 上分别查出平衡气相和液相的组 成(x)。按上述步骤,本别测定乙醇和乙酸乙酯的沸点,以及各溶液的沸点和 平衡时气相和液相的组成。
相点连成气相线和液相线,即得 T-x 平衡图。
三、实验步骤
乙醇-乙酸乙酯溶液的折射率组成工作曲线的测绘 折射率-体积分数工作曲线。
对于乙醇-乙酸乙酯等部分有机液体混合体系,当使用体积分数(φ)表示
时,能得到直线的工作曲线,故只要分别准确测出 25℃时纯乙醇、乙酸乙酯的
折射率,将其连成直线,就得到 折射率-摩尔分数工作曲线。
沸点测定仪
沸点测定仪利用回流的方法保持气液两相相对量一定,测量体系温度不发
生改变时,即两相平衡后,取出两相的样品,用阿贝折射计测定气液平衡气
相、液相的折射率,再通过预先测定的折射率-组成工作曲线来确定平衡时气
相、液相的组成(即该温度下气液两相平衡成分的坐标点)。改变体系总成
分,再如上法找出另一对坐标点。这样得若干对坐标点后,分别按气相点和液
粗略配制乙醇体积分数为 5%、10%、15%、22%、38%、50%、70%、90%
组成的乙醇-乙酸乙酯溶液。 沸点的测定
自侧管假如索要测定的溶液(约 20mL),其页面应在水银球的中部。打
开冷凝水,接上电源,用调压变压器调节电压(约 12V),将液体缓慢加热使
液体沸腾,最初在冷凝管下端内的液体不能代表平衡气相的组成,为加速达到
二、实验原理
液体的沸点 液体的沸点是液体饱和蒸汽压和外压相等时的温度,在外压一定时,纯液
体的沸点有一个确定值。 双液系的沸点
双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。理想 的二组分体系在全部浓度范围内符合拉乌尔定律。结构相似、性质相近的组分 间可以形成近似的理想体系,这样可以形成简单的 T-x(y)图。大多数情况 下,曲线将出现或正或负的偏差。当这一偏差足够大时,在 T-x(y)曲线上将 出现极大点(负偏差)或极小点(正偏差)。这种最高和最低沸点称为恒沸 点,所对应的溶液称为恒沸混合物。
工作曲线(n-V)。
在
线上取 8 个点,利用乙醇、乙酸乙酯的密度合量比(%)等
条件将以上点对应体积分数换算成摩尔分数,按对应的折射率重新绘
点,再将点连成平滑曲线,即为 工作曲线(n-x)。 沸点仪的安装
将沸点仪洗净、烘干。检查带温度计的软木塞是否塞紧、电热丝是否靠近
容器底部的中心,温度计的水银球位置是否合适。 样品的测定 溶液的配制
考虑综合因素,实验选择具有最低恒沸点的乙醇-乙酸乙酯双液系。根据相
平衡原理,对二组分体系,当压力恒定时,在气液平衡两相区,体系的自由度
为 1。若温度一定时,则气液亮相的组成也随之而定。当溶液组成一定时,根
据杠杆原理,两相的相对量也一定。反之,实验中利用回流的方法保持气液两
相的相对量一定,则体系的温度也随之而定。
(3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大, 混合物存在着最低沸点,如水-乙醇体系,如图 1(c))所示。
t / oC t / oC
t / oC
tB
tB tA
tA
tA
tB
A
x B
(a)
B
A
x B
x'
B
(c)
图 1. 二组分真实液态混合物气—液平衡相图(T-x 图)
