大学有机化学醛和酮56页PPT
合集下载
第十一章醛和酮--精品PPT课件

NaBH4还原的特点: ①选择性强(只还原醛、酮、酰卤中的羰基,不还原其它基团。
②稳定(不受水、醇的影响,可在水或醇中使用)。
3. Meerwein-Ponndorf-Verley还原法
R
OH Al(OPr-i)3
R
O
O+
OH +
(H)R'
(H)R'
(二)还原为烃 1.吉尔聂尔-沃尔夫-黄鸣龙还原法
§11-1 结构、分类、同分异构和命名
一、结构
CO sp2 杂化
π键 σ键 CO
121.8。 H 116.5。 C O
H
近平面三角形结构
CO 电负性 C < O
π CO
π 电子云偏向氧原子
δδ CO 极性双键
二、分类
CH3CH2CH2CHO 脂肪醛
CHO
脂环醛
CHO
芳香醛
CH3CH=CHCHO 不饱和醛
R CH2 H(R') ① Kishner-Wolff-Huang Minlon 法 ② 硫代缩醛-脱硫加氢 ③ Clemmensen 法
(一)还原成醇
1.催化氢化
H
+
H2
O H + H2
O
Ni 压力
Ni
OH
H O
2. 用还原剂(金属氢化物)还原
(1)LiAlH4还原
CH3CH=CHCH2CHO
① LiAlH 4 干乙醚
O CH3 C CH2I
O
I2 快
CH3 C CHI2
O
I2 快
CH3 C CI3
O
OH-
CH3 C O- + CHI3
大学有机化学重点知识总结第十一章 醛、酮
—制备增加2个C原子的伯醇:
+
H2C CH2
-+
RM gBr
O -
(C2H5)2O
R C H 2 C H 2 O M g B r
H 3O + H O C H 2C H 2R
精选可编辑ppt
42
33.
CH3 ( NBS )
CH2Br
Mg
(
干醚
CH2MgBr )
① O / 干醚
(
② H3O+
CH2CH2CH2OH )
R C O R '+H 2 O H +
R CO +2 R 'O H
(R '')HO R '
(R '')H
精选可编辑ppt
33
H +
O O C H 3
( )+ ( )
O
CH2CH2CH2CH CH3OH
HO
O
O
O
C OCH3 H
O O
C OCH3
H OC H2CH 2OH
精选可编辑ppt
34
(3)活性:醛>酮 酮一般用原甲酸三乙酯形成缩酮
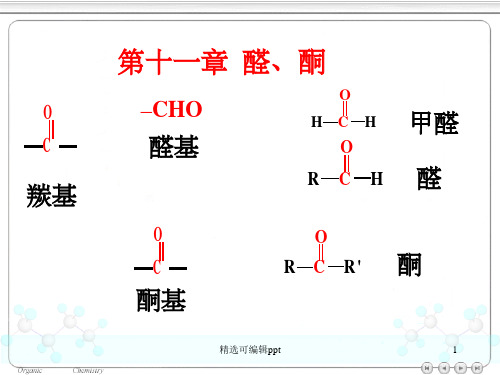
O C
羰基
第十一章 醛、酮
–CHO
醛基
O HCH
O
RCH
甲醛 醛
O
C
酮基
O
R C R' 酮
精选可编辑ppt
1
烃基
脂肪族醛和酮 芳香族醛和酮
醛和酮
饱和醛和酮
的分类 烃基是否饱和 不饱和醛和酮
一元醛和酮
羰基个数 二元醛和酮
多元醛和酮
醛和酮幻灯片.pptx

R
R C O + NH2 OH 羟胺 OH
[R C NH OH] -H2O R C N OH
R
R
肟
R R C O + NH2 NH2
肼
R C N NH2
R
腙
第28页/共81页
R R C O + NH2 NHC6H5
苯肼
R C N NHC6H5
R
苯腙
R R C O + NH2 NHCONH2
氨基脲
R C N NHCONH2
3-甲基丁醛 3-methylbutanal
CH3CH2CCH2CH3 O
3-戊酮 3-pentanone
第6页/共81页
CH3CHCHO
CHO
2-苯基丙醛 2-phenylpropanal
COOH
对甲酰基苯甲酸 4-formylbenzoic acid
CH3CHCH2CHO OH
3-羟基丁醛 3-hydroxylbutanal
CHO
第41页/共81页
❖用金属氢化物加氢:LiAlH4或NaBH4,可以把羰基还原为醇羟基,反 应机理是提供负氢离子对羰基进行亲核加成。
-
O
-
OAlH3
OH
H AlH3
C
C
H2O
C
H
H
LiAlH4
CH3CH CHCH2CHO orNaBH4 CH3CH CHCH2CH2OH
第42页/共81页
❖Meerwein-Ponndorf-Verley还原法:在异丙醇铝的存在下,以异丙醇 为还原剂,反应中只还原醛或酮的羰基,而不影响分子中的其他基团。
CH CHO CH2O HOCH2 CH2OH
有机化学 醛和酮PPT课件

CHO
RCH CH2
CO + H2
[Co(CO)4]2
+ RCH2CH2CHO
R CH CH3
此反应又称氢的甲酰化反应,反应相当于氢的甲酰基(-CHO)按反马氏规
则加成到双键上,得到以直链为主的产物。如:
+ H2C CH2 CO
H2 [Co(CO)4]2
120℃,10~20MPa
CH3CH2CHO
有机化学
CN
R OH
+ H+
C
(R')H
CN
应用:
氧负离子中间体
合成羟基腈,增长碳链。
有机化学
23
第23页/共73页
(2)与饱和NaHSO3的加成
R C
H3C(H)
O NaHSO3
R ONa
C
H3C(H)
SO3H
稀酸或稀碱
羟基磺酸钠
R
OH
C
H3C(H)
SO3Na
特点:
——鉴别醛、部分酮
①反应可逆;
② 只 有 醛 、 脂 肪 族 甲 基 酮 和—少 于—8 个分C 的离环 酮、才提可 以纯反羰应 。基化合物
本章主要内容
一、醛酮的结构、分类和命名 二、醛酮的制法 三、醛酮的物理性质 四、醛酮的化学性质 五、重要的醛酮
有机化学
1
第1页/共73页
一、醛酮的结构、分类和命名
1、醛酮的结构 羰基的结构
CO
羰基中的O原子没有发生杂 化,其2个2s电子与成键无关。
羰基的碳氧双键是由一个
键和一个键组成的。
2p
羰基是平面三角形。
饱和醛酮 不饱和醛酮 O
CHO
醛和酮PPT演示课件

(2)羰基化合物是极性化合物。
13
(二)醛、酮的物理性质
1、状:常温下,甲醛是气体,低、中级醛、酮是液体, 高级醛、酮是固体。
2、味:低级醛有强烈的刺激气味,低级酮有特殊气味, 中级醛、酮有果香味。
3、沸点:醛、酮的沸点比分子量相近的烷烃和醚高,而 比分子量相近的醇低。
4、溶解性:低级脂肪醛、酮易溶于水,其他醛、酮的 水溶性随分子量的增加而减弱,高级醛、酮和 芳香族醛、酮不溶于水。醛、酮能溶于乙醇、 乙醚等有机溶剂。
且垂直于σ键所在的平面。
12
问题:
碳氧双键和碳碳双键都是由一个σ键和一个π键 组成,它们在极性方面会有区别吗?
由于氧原子的电负性较碳原子大,羰基中π键的电 子云偏向于氧原子方面,使得羰基发生极化,羰基碳原 子就带有部分正电荷,而氧原子则带有部分负电荷。
羰基极化的情形:
δ+
δ—
CO
结论: (1)碳氧双键是一个极性不饱和键。
R—C—H + HCN O
H2O/HOH
α—羟基腈
α—羟基酸
18
(2)与亚硫酸氢钠的加成
醛、脂肪族甲基酮 、低级环酮 + 过量NaHSO3饱和 溶液作用,生成α—羟基磺酸钠。
R—C—H + HSO3Na O
R—CH—SO3Na
OH
α—羟基磺酸钠
α—羟基磺酸钠不溶于饱和NaHSO3溶液而呈白色结晶析出。
CH2 + N2
但该还原法是在碱性条件下进行的,所以当分 子中含有对碱敏感的基团时,不能使用这种还原法。
36
5、 歧化反应——Cannizzaro反应
不含α-H 的醛在浓碱作用下,一分子醛被氧化成羧酸, 一分子醛被还原成醇,该反应称为Cannizzaro反应。
13
(二)醛、酮的物理性质
1、状:常温下,甲醛是气体,低、中级醛、酮是液体, 高级醛、酮是固体。
2、味:低级醛有强烈的刺激气味,低级酮有特殊气味, 中级醛、酮有果香味。
3、沸点:醛、酮的沸点比分子量相近的烷烃和醚高,而 比分子量相近的醇低。
4、溶解性:低级脂肪醛、酮易溶于水,其他醛、酮的 水溶性随分子量的增加而减弱,高级醛、酮和 芳香族醛、酮不溶于水。醛、酮能溶于乙醇、 乙醚等有机溶剂。
且垂直于σ键所在的平面。
12
问题:
碳氧双键和碳碳双键都是由一个σ键和一个π键 组成,它们在极性方面会有区别吗?
由于氧原子的电负性较碳原子大,羰基中π键的电 子云偏向于氧原子方面,使得羰基发生极化,羰基碳原 子就带有部分正电荷,而氧原子则带有部分负电荷。
羰基极化的情形:
δ+
δ—
CO
结论: (1)碳氧双键是一个极性不饱和键。
R—C—H + HCN O
H2O/HOH
α—羟基腈
α—羟基酸
18
(2)与亚硫酸氢钠的加成
醛、脂肪族甲基酮 、低级环酮 + 过量NaHSO3饱和 溶液作用,生成α—羟基磺酸钠。
R—C—H + HSO3Na O
R—CH—SO3Na
OH
α—羟基磺酸钠
α—羟基磺酸钠不溶于饱和NaHSO3溶液而呈白色结晶析出。
CH2 + N2
但该还原法是在碱性条件下进行的,所以当分 子中含有对碱敏感的基团时,不能使用这种还原法。
36
5、 歧化反应——Cannizzaro反应
不含α-H 的醛在浓碱作用下,一分子醛被氧化成羧酸, 一分子醛被还原成醇,该反应称为Cannizzaro反应。
《醛和酮的》PPT课件

通式
此方法用于制备醇
1o醇 2o醇
甲醛
醛 3o醇
酮
精选ppt
39
与有机金属锂试剂的反应
O
O H
+ (C H 3 )2 C H C C H (C H 3 )2 (C H 3 )2 C H L i H 3 O +(C H 3 )2 C H C C H (C H 3 )2
H O O H
例二:
转化
O
COC2H5 O
CH2OH
O
II: 还原C=O生成CH2
精选ppt
33
(3) 与氢氰酸加成 RHC O HCN
R OH
C H
CN
α -氰醇
(α -羟基腈)
H2O H+
H
R C COOH OH
α -羟基酸
A: 反应在酸性条件下难以进行,在碱性条件下易进行
B: α-羟基腈多官能团中间体
26
(1) 水合反应
H 3C C O + H 2O
H
H 3C O H C
H O H
平衡偏向左边
机理:
精选ppt
27
(2)与醇的缩合
A. 反应通式:
半缩醛羟基
R H C=O
HOR/
干HCl
R OH H C OR/
R/OH,H+
R OR/ H C OR/
+
H2O
半缩醛
缩酮
(不稳定)
I:
II: 反应为平衡反应,除水可使平衡向右移动
(2)乙烯催化氧化 ➢乙酸、乙酸乙酯的原料
精选ppt
15
3、丙酮
➢无色液体 ➢工业制备
❖丙烯水化 ❖异丙苯制苯酚的付产物 ❖丙烯催化氧化
有机化学第十章醛酮PPT课件

注意事项
在醇氧化制备醛的过程中,应控制反应条件,如温度、浓度、催化剂 等,以避免过度氧化或其它副反应的发生。
通过醇的氧化制备酮
总结词
醇氧化是制备酮的一种常用方法,常用的氧化剂有高锰酸 钾、硝酸、铬酸等。
详细描述
醇氧化制备酮的反应机理是醇分子中的羟基被氧化成羰基, 同时生成氢离子,常用的氧化剂可以将醇氧化成相应的酮, 同时生成水或其它相应的产物。
醛酮还可以用于合成生物活性分子,如激素、维生素等,对生命过程具有重要影响。
05 醛酮的制备方法
通过醇的氧化制备醛
总结词
醇氧化是制备醛的一种常用方法,常用的氧化剂有高锰酸钾、硝酸、 铬酸等。
详细描述
醇氧化制备醛的反应机理是醇分子中的羟基被氧化成羰基,常用的 氧化剂可以将醇氧化成相应的醛,同时生成水或其它相应的产物。
亲核加成反应
与氢氰酸加成
酮在氢氰酸的作用下,可以发生亲核加成反应, 生成相应的羟基腈。
与水加成
酮在水的作用下,可以发生亲核加成反应,生成 相应的醇。
与醇加成
酮在醇的作用下,可以发生亲核加成反应,生成 相应的酯。
亲电加成反应
与溴加成
01
酮在溴的作用下,可以发生亲电加成反应,生成相应的溴代酮。
与硫酸加成
02 醛的化学性质
还原反应
还原成醇
还原成醇和烃的混合物
在催化剂存在下,醛基可被还原成醇, 如用氢化铝锂(LiAlH4)作为还原剂。
在某些条件下,醛基可被还原成醇和 烃的混合物,如用氢气作为还原剂。
还原成烃
在酸性条件下,醛基可被还原成烃, 如用硫酸铜和亚硫酸氢钠作为还原剂。
氧化反应
氧化成酸
在强氧化剂存在下,醛基可被氧化成羧基,如用高锰酸钾 (KMnO4)作为氧化剂。
在醇氧化制备醛的过程中,应控制反应条件,如温度、浓度、催化剂 等,以避免过度氧化或其它副反应的发生。
通过醇的氧化制备酮
总结词
醇氧化是制备酮的一种常用方法,常用的氧化剂有高锰酸 钾、硝酸、铬酸等。
详细描述
醇氧化制备酮的反应机理是醇分子中的羟基被氧化成羰基, 同时生成氢离子,常用的氧化剂可以将醇氧化成相应的酮, 同时生成水或其它相应的产物。
醛酮还可以用于合成生物活性分子,如激素、维生素等,对生命过程具有重要影响。
05 醛酮的制备方法
通过醇的氧化制备醛
总结词
醇氧化是制备醛的一种常用方法,常用的氧化剂有高锰酸钾、硝酸、 铬酸等。
详细描述
醇氧化制备醛的反应机理是醇分子中的羟基被氧化成羰基,常用的 氧化剂可以将醇氧化成相应的醛,同时生成水或其它相应的产物。
亲核加成反应
与氢氰酸加成
酮在氢氰酸的作用下,可以发生亲核加成反应, 生成相应的羟基腈。
与水加成
酮在水的作用下,可以发生亲核加成反应,生成 相应的醇。
与醇加成
酮在醇的作用下,可以发生亲核加成反应,生成 相应的酯。
亲电加成反应
与溴加成
01
酮在溴的作用下,可以发生亲电加成反应,生成相应的溴代酮。
与硫酸加成
02 醛的化学性质
还原反应
还原成醇
还原成醇和烃的混合物
在催化剂存在下,醛基可被还原成醇, 如用氢化铝锂(LiAlH4)作为还原剂。
在某些条件下,醛基可被还原成醇和 烃的混合物,如用氢气作为还原剂。
还原成烃
在酸性条件下,醛基可被还原成烃, 如用硫酸铜和亚硫酸氢钠作为还原剂。
氧化反应
氧化成酸
在强氧化剂存在下,醛基可被氧化成羧基,如用高锰酸钾 (KMnO4)作为氧化剂。
醛和酮—醛和酮(药学有机化学课件)

+ COCH3
Br2
COCH2Br + HBr
卤仿反应
卤仿反应:如果醛、酮α-碳上有三个氢,三个氢被卤素原子
取代,使得碳碳键极性增大,发生碳碳键的断裂,生成三卤
甲烷和羧酸盐的反应。
O
O
CH3C-R(H)+ 3X2
NaOH
OH CX3-C-R(H)
O
CHX3 + R(H)-C-O
O
O
CH3 C CH3 I2 + NaOH CI3 C CH3 NaOH CH3COONa + CHI3
有机化学/ 醛和酮
醛的特征反应
醛基上氢原子由于受羰基 的影响变得比较活泼,因此醛 具有不同于酮的特殊的反应。 醛能被弱氧化剂——托伦试剂、 斐林试剂氧化为羧酸。
一、托伦反应
托伦(Tollens)试剂是AgNO3与氨水生成的一种无色的 银氨配合物溶液,其中Ag+ 起着氧化剂作用,当它与醛共热时, 醛被氧化为羧酸,而它则被还原为金属银,附着在试管内壁上, 形成光亮的银镜,因此该反应也称为银镜反应。
或浓H2SO4
H
或浓H2SO4 H
半缩醛
缩醛
➢ 半缩醛不稳定,很难分离。 ➢ 缩醛具有双醚的结构,对碱、氧化剂、还原剂稳定,可
以分离出来。
➢ 缩醛在稀酸中易水解转变为原来的醛,合成中可利用此 反应来保护醛基。
一、加成反应
与醇加成 分子内也能形成半缩醛、缩醛。
CH O
干 HCl
OH
H OH O
环状半缩醛(稳定) 在糖类化合物中多见
O
C5 H3C4 H2C3 C2 HC1 H3
CH3 2-甲基-3-戊酮
C H3
醛和酮中文PPT课件

羟醛缩合反应历程
3-羟基丁醛 50%
第一步:在碱作用下,生成烯醇负离子
第二步:负离子作为亲核试剂与另一分子乙醛发生亲核加成,生成烷氧负离子
第32页/共65页
33
-羟基醛受热时容易失去一分子水,生成,-不饱和醛
巴豆醛 • 凡碳上有氢原子的-羟基醛都容易失去一分子水,生成——烯醛。 • 含有氢原子的酮也能起类似反应,生成,-不饱和酮
例1 例2
• 一卤代醛、酮往往可以继续卤化成二卤代、三卤代产物
第35页/共65页
36
• -卤代醛、酮反应的历程 碱催化(不易控制,直至同碳三卤代物,易被碱分解):
烯醇负离子
• 卤代物继续反应:
第36页/共65页
37
(B) 酸催化历程
酸催化可停 留在一卤代
• 由于卤原子是吸电子的, 碳上的氢原子在碱作用下容易离去,因此第二个 氢原子更易被取代.
• 氨衍生物对羰基的加成一般可在弱酸催化下进行,其历程和醇对羰基的加成 相类似。
• 醛酮与氨衍生物的反应,也常用来对羰基化合物的鉴定和分离: (1)生成物为具有一定熔点的固体,可利用来鉴别醛酮; (2)它们在稀酸作用下可水解成原来的醛酮,因此可利用来分离、提纯醛 酮。
第25页/共65页
鉴定和分离 m.p. 126℃
23
第23页/共65页
24
(5)与氨的衍生物反应 • 与氨的衍生物,例如:羟胺(NH2OH),肼(NH2NH2),
2,4-二硝基苯肼和氨基脲等反应.
例1:
例2:
例3: 例4:
第24页/共65页
25
• 醛酮与氨衍生物的反应历程:
第一步:羰基的亲核加成,生成不稳定的加成产物;
第二步:失去一分子水.
醛和酮PPT课件

醛的氧化: 醛容易被氧化为羧酸。
[O] RCHO
RCO2H
氧化剂:KMnO4, K2Cr2O7 , H2Cr2O7 , H2CrO4 RCO3H , Ag2O , H2O2, Br2-H2O ,
07:07:19
第13页/共58页
被Tollens 试剂氧化(银镜反应)
RCHO + Ag(NH3)2+OH
§9-1 醛、酮的分类和命名
一、分类
CH3CH2CH2CHO 脂肪醛
CHO
脂环醛
CHO
芳香醛
CH3CH=CHCHO 不饱和醛
CH2CHO CH2CHO
二元醛
O CH3CH2-C-CH3
脂肪酮
O O C-CH3
O CH3CH=CH-C-CH3
O
脂环酮 芳香酮
不饱和酮
OO CH3-C-CH2-C-CH3
CH2OH + HCOONa
07:07:19
O CHO
第17页/共58页
醛和酮的还原: 利用不同的条件,可将醛、酮还原成醇、
烃
: 1.2.1 用金属氢化物还原成醇
氢化锂铝或硼氢化钠还原醛得到伯醇,还原酮得到仲醇 (1)LiAlH4还原 LiAlH4是强还原剂,但①选择性差,除不还原C=C、C≡C外,其它不饱和 键都可被其还原;②不稳定,遇水剧烈反应,通常只能在无水醚或THF 中 使用 。
该反应在有机合成上有重要用途
O
RCH2MgX
无水乙醚
OMgX C
R
H2O
OH C
R
07:07:19
第26页/共58页
此反应是制备结构复杂的醇的重要方法
CH3
CH3
C OH
[O] RCHO
RCO2H
氧化剂:KMnO4, K2Cr2O7 , H2Cr2O7 , H2CrO4 RCO3H , Ag2O , H2O2, Br2-H2O ,
07:07:19
第13页/共58页
被Tollens 试剂氧化(银镜反应)
RCHO + Ag(NH3)2+OH
§9-1 醛、酮的分类和命名
一、分类
CH3CH2CH2CHO 脂肪醛
CHO
脂环醛
CHO
芳香醛
CH3CH=CHCHO 不饱和醛
CH2CHO CH2CHO
二元醛
O CH3CH2-C-CH3
脂肪酮
O O C-CH3
O CH3CH=CH-C-CH3
O
脂环酮 芳香酮
不饱和酮
OO CH3-C-CH2-C-CH3
CH2OH + HCOONa
07:07:19
O CHO
第17页/共58页
醛和酮的还原: 利用不同的条件,可将醛、酮还原成醇、
烃
: 1.2.1 用金属氢化物还原成醇
氢化锂铝或硼氢化钠还原醛得到伯醇,还原酮得到仲醇 (1)LiAlH4还原 LiAlH4是强还原剂,但①选择性差,除不还原C=C、C≡C外,其它不饱和 键都可被其还原;②不稳定,遇水剧烈反应,通常只能在无水醚或THF 中 使用 。
该反应在有机合成上有重要用途
O
RCH2MgX
无水乙醚
OMgX C
R
H2O
OH C
R
07:07:19
第26页/共58页
此反应是制备结构复杂的醇的重要方法
CH3
CH3
C OH
大学有机化学 醛和酮56页PPT

大学有机化学 醛和酮
•
6、黄金时代是在我们的前面,而不在 我们的 后面。
•Байду номын сангаас
7、心急吃不了热汤圆。
•
8、你可以很有个性,但某些时候请收 敛。
•
9、只为成功找方法,不为失败找借口 (蹩脚 的工人 总是说 工具不 好)。
•
10、只要下定决心克服恐惧,便几乎 能克服 任何恐 惧。因 为,请 记住, 除了在 脑海中 ,恐惧 无处藏 身。-- 戴尔. 卡耐基 。
Thank you
6、最大的骄傲于最大的自卑都表示心灵的最软弱无力。——斯宾诺莎 7、自知之明是最难得的知识。——西班牙 8、勇气通往天堂,怯懦通往地狱。——塞内加 9、有时候读书是一种巧妙地避开思考的方法。——赫尔普斯 10、阅读一切好书如同和过去最杰出的人谈话。——笛卡儿
•
6、黄金时代是在我们的前面,而不在 我们的 后面。
•Байду номын сангаас
7、心急吃不了热汤圆。
•
8、你可以很有个性,但某些时候请收 敛。
•
9、只为成功找方法,不为失败找借口 (蹩脚 的工人 总是说 工具不 好)。
•
10、只要下定决心克服恐惧,便几乎 能克服 任何恐 惧。因 为,请 记住, 除了在 脑海中 ,恐惧 无处藏 身。-- 戴尔. 卡耐基 。
Thank you
6、最大的骄傲于最大的自卑都表示心灵的最软弱无力。——斯宾诺莎 7、自知之明是最难得的知识。——西班牙 8、勇气通往天堂,怯懦通往地狱。——塞内加 9、有时候读书是一种巧妙地避开思考的方法。——赫尔普斯 10、阅读一切好书如同和过去最杰出的人谈话。——笛卡儿
有机化学全套PPT课件第十章 醛和酮

C=N
OH
t-Bu
H
H2SO4 乙醚
O
Et t-Bu
C-NH-CCH3
H
*3E 贝克曼重排反应的应用
应用1:制备酰胺、羧酸、胺。 应用2:测定酮肟的几何构型(根据反式迁移)。
NH2
反式
HO OC
NO2
顺式
O2N
OH C=N
应用3:合成(如制备尼龙6)
H+ O +H2N OH
OH N
H+
+OH2 N
*4 反应的立体化学
*4a 醛、酮与HCN的加成也符合克莱姆规则一。
O M
S
O
较
稳
L
定
-CN
L
较 不 稳 定
S
M
R
R
*4b 当醛、酮的-C上有-OH、-NH时,由于这些基团能与 羰基形成氢键,所以形成如下构象(见图),若发生加成, 亲核试剂主要从S基团一侧进攻,这称为克莱姆规则二。
H OO
L
R
S
O
H
C 2H 5
P hH
X
Mg
O
R
M
S
Mg X
R
LR
PhOຫໍສະໝຸດ HH C 2 H 5
H
O
P hH
C 2H 5 1 RMgX 2 H2O
R
H
C2H 5
+
H
OH
Ph
OH
H
C2H 5
H
R
Ph
Ph
H
C 2H 5
HO
H
R
主要产物
Ph
H
C 2H 5
