(完整版)2018年器械分类目录(新)
解读2018新版《医疗器械分类目录》

解读2018新版《医疗器械分类目录》新版《医疗器械分类目录》是我国医疗器械管理领域的重要文件,对医疗器械的分类和管理起着关键作用。
本文将对该目录的主要内容和意义进行解读。
2018年新版《医疗器械分类目录》是国家药品监督管理局、国家卫生健康委员会联合发布的,自2019年1月1日起正式实施。
目录中包含了对医疗器械的分类、产品范围、管理要求等方面的规定,全面梳理了我国医疗器械市场现状,为医疗器械的生产、流通和使用提供了明确的指导。
一、目录的分类体系《医疗器械分类目录》按照医疗器械的功能和用途进行分类,分为17个大类,共计100个小类。
这种分类体系既考虑了医疗器械的技术特点,又体现了医疗器械的临床应用需求。
通过分类,可以更好地统一和规范不同类型医疗器械的管理,方便企业和医疗机构的运营和使用。
二、目录的主要内容《医疗器械分类目录》对医疗器械的定义、分类和管理要求进行了具体规定。
其中,针对高风险型医疗器械,目录明确规定了准入要求,按照产品的等级,从注册、审评到监管都有相应的要求和流程。
这对于提高我国医疗器械的质量和安全水平非常重要。
此外,在医疗器械分类和编码方面,《医疗器械分类目录》也进行了细化和完善。
新版目录对于有争议的医疗器械分类问题进行了解决,明确了分类标准,降低了因分类不明确而产生的交叉管理问题。
同时,目录还对医疗器械的命名和编码进行了规范,提高了信息交流和管理的效率。
此外,新版目录还增加了一些新的、符合临床需求的医疗器械,如微创手术器械、家庭医疗器械等。
这些器械的添加,使得新版《医疗器械分类目录》更贴合医疗实践,更加全面地覆盖了医疗器械市场的需求。
三、目录的意义与影响新版《医疗器械分类目录》的发布和实施,对于医疗器械行业具有重要意义。
首先,目录的出台进一步规范了医疗器械市场,促进了医疗器械的良性发展。
其次,目录的分类和命名规范,使得医疗器械的信息管理更加便捷高效,提高了监管部门的工作效率。
最后,通过修改完善目录,提高了医疗器械的准入门槛,加强了产品安全性和质量可控性的管理,保护了消费者的合法权益。
新医疗器械分类目录

新医疗器械分类目录新医疗器械分类目录是国家药品监督管理局根据《医疗器械监督管理条例》制定的医疗器械分类标准。
新分类目录于2024年1月1日起正式实施,与之前的旧分类相比,新分类目录系统更为细化和科学。
下面是旧分类对应新分类的完整版:1.未分类设备:无对应的新分类。
2.心电诊断设备:新分类为电生理和心电设备。
3.医用超声诊断设备:新分类为超声和电子医疗设备。
4.射线诊断设备:新分类为射线类、超声和电子医疗设备。
5.医用核素诊断体内摄取设备:新分类为核医学设备。
6.核医学设备:新分类为核医学设备。
7.内窥镜设备:新分类为内窥镜设备。
8.医用光学设备:新分类为光学设备。
9.医用电子设备:新分类为电子医疗设备。
10.医用手术设备:新分类为外科、眼科和牙科设备。
11.医用手术室、成像设备和治疗设备:新分类为外科、眼科和牙科设备。
12.医用麻醉和复苏设备:新分类为麻醉和体外循环设备。
13.附件:新分类为其他。
14.体外循环设备:新分类为麻醉和体外循环设备。
15.医用口腔科设备:新分类为外科、眼科和牙科设备。
16.耳鼻喉科设备:新分类为耳鼻喉科设备。
17.眼科设备:新分类为外科、眼科和牙科设备。
18.口腔科设备:新分类为外科、眼科和牙科设备。
19.物理治疗和康复设备:新分类为物理治疗、康复和护理设备。
20.电子治疗和诊断设备:新分类为电子医疗设备。
21.医用成像设备:新分类为超声和电子医疗设备。
22.医用实验室设备和试剂:新分类为实验室设备、试剂和监测设备。
23.眼科医用光学设备:新分类为光学设备。
24.医用口腔诊断设备:新分类为外科、眼科和牙科设备。
25.医用康复辅助设备:新分类为物理治疗、康复和护理设备。
26.检验设备、试剂和试剂盒:新分类为实验室设备、试剂和监测设备。
27.医用实验室设备:新分类为实验室设备、试剂和监测设备。
28.现场快速诊断设备和试剂:新分类为实验室设备、试剂和监测设备。
29.医用消毒和灭菌设备:新分类为消毒器械和灭菌器械。
(word完整版)医疗器械分类目录(分类)

医疗器械分类目录
关于指定《医疗器械分类目录》的说明
一、《医疗器械分类目录》制定的依据
《医疗器械监督管理条例》及《医疗器械分类规则》(第15号局长令)。
二、《医疗器械分类目录》与《医疗器械分类规则》的关系
《医疗器械分类规则》用于指导《医疗器械分类目录》的制定和确定新的产品注册类别。
我国实行的医疗器械分类方法是分类规则指导下的目录分类制,分类规则和分类目录并存。
一旦分类目录已实施,应执行分类目录。
三、制定分类目录的原则
执行分类规则指导下的目录分类制。
参照国际通行的分类,从严掌握。
使用风险是制定产品分类目录的基础。
分类目录尽可能适应管理的需要,有利于理顺监督管理,做到科学合理.
四、符合医疗器械定义的含药医疗器械为III类医疗器械.
五、由于各种手术包内组件不确定,所以本目录不包含该类产品。
凡手术包内含有III类医疗器械的,作为III类产品管理;只含有II类和I类医疗器械的,作为II类产品管理;只含有I类医疗器械的,作为I类产品管理。
六、依据《医疗器械分类目录》不能确定医疗器械分类时,由省级药品监督管理局根据分类规则进行预先分类,并报我局核定。
医疗器械分类目录6801基础外科手术器械。
2018医疗器械法律法规目录(最全)

医疗器械法律法规、部门规章制度汇总(2018版)医疗器械重点法律法规解读1.《医疗器械监督管理条例》已经2014年2月12日国务院第39次常务会议修订通过,现将修订后的《医疗器械监督管理条例》(以下简称“《条例》”)公布,自2014年6月1日起施行。
2.《医疗器械标准管理办法》已于2017年2月21日经国家食品药品监督管理总局局务会议审议通过,现予公布,自2017年7月1日起施行。
医疗器械标准,是指由国家食品药品监督管理总局依据职责组织制定、修订,依法定程序发布,在医疗器械研制、生产、经营、使用、监督管理等活动中遵循的统一的技术要求。
在中华人民共和国境内从事医疗器械标准的制定、修订、实施及监督管理,应当遵守法律、行政法规及本办法的规定。
医疗器械标准按照其效力分为强制性标准和推荐性标准。
3.《大型医用设备配置与使用管理办法》卫生部、国家发展和改革委员会、财政部联合制定并下发(卫规财发〔2004〕474号)。
大型医用设备是指列入国务院卫生行政部门管理品目的医用设备以及尚未列入管理品目、省级区域内首次配置的整套单价在500万元人民币以上的医用设备。
大型医用设备的管理实行配置规划和配置证制度。
甲类大型医用设备的配置许可证由国务院卫生行政部门颁发;乙类大型医用设备的配置许可证由省级卫生行政部门颁发。
医疗器械安全使用指南疗机构要加强大型医用设备使用管理,严格操作规范, 保证设备使用安全、有效。
4.《体外诊断试剂注册管理办法修正案》已于2017年1月5日经国家食品药品监督管理总局局务会议审议通过,现予公布,自公布之日起施行。
本办法所称的体外诊断试剂,是指按医疗器械管理的体外诊断试剂,包括在疾病的预测、预防、诊断、治疗监测、预后观察和健康状态评价的过程中,用于人体样本体外检测的试剂、试剂盒、校准品、质控品等产品。
可以单独使用,也可以与仪器、器具、设备或者系统组合使用。
按照药品管理的用于血源筛查的体外诊断试剂和采用放射性核素标记的体外诊断试剂,不属于本办法管理范围。
2018医疗器械法律法规目录(最全)

2018医疗器械法律法规目录(最全)【】2018医疗器械法律法规目录(最全)【目录】一、中华人民共和国法律1.《中华人民共和国医疗器械管理法》2.《中华人民共和国药品管理法》3.《中华人民共和国卫生法》4.《中华人民共和国广告法》5.《中华人民共和国产品质量法》二、配套规章1.《医疗器械注册与备案管理办法》2.《医疗器械监督管理办法》3.《医疗器械不良事件报告管理办法》4.《医疗器械广告审核标准》5.《医疗器械生产监督管理办法》三、行业标准1.《医疗器械质量管理体系要求》2.《医用电气设备安全》3.《医疗器械包装》4.《手术室净化空调系统》5.《医疗器械标签与说明》四、法院判例1.【案例1】医疗器械质量纠纷案2.【案例2】医疗器械广告虚假宣传案3.【案例3】医疗器械专利侵权案4.【案例4】医疗器械违规经营案5.【案例5】医疗器械不良事件案五、政策文件1.《医疗器械生产许可证管理办法》2.《医疗器械分销许可证管理办法》3.《医疗器械进口许可证管理办法》4.《医疗器械售后服务管理办法》5.《医疗器械网络销售管理办法》【附件】所涉及附件如下:1. 医疗器械注册申请表格2. 医疗器械不良事件报告表格3. 医疗器械广告审查申请表格4. 医疗器械生产企业许可证样本5. 医疗器械经营企业许可证样本【法律名词及注释】所涉及的法律名词及注释如下:1. 医疗器械管理法:指中华人民共和国颁布的管理医疗器械的法律法规。
2. 医疗器械注册与备案管理办法:指用于管理医疗器械注册和备案的相关规章。
3. 医疗器械质量管理体系要求:规定了医疗器械质量管理体系的基本要求。
4. 医用电气设备安全:指医疗器械中涉及到电气设备的安全管理规范。
5. 医疗器械不良事件报告管理办法:规定了医疗器械不良事件报告的要求和管理办法。
【困难及解决办法】在实际执行过程中,可能遇到的困难及解决办法如下:困难:1. 医疗器械注册和备案流程繁琐,需要大量的时间和精力。
(完整版)新医疗器械分类目录(旧分类对应新分类)

16眼科器械
6823-1超声诊断设备-眼科专用超声脉冲回波设;
6823-3超声治疗设备-超声手术设备
17口腔科器械
6823-3超声治疗设备中的超声洁牙设备(2012版)
18妇产科、辅助生殖和避孕器械
6823-2超声监护设备中的超声多普勒胎儿监护仪(2012版);
6821-8电声诊断仪器(2002版);
6821-3有创医用传感器(2002版);
6821-3无创医用传感器(2002版);
6821-18心电电极(2002版);
6821-19心电导联线(2002版)
08呼吸、麻醉和急救器械
6821-1用于心脏的治疗、急救装置中的心脏除颤器(2002版)
09物理治疗器械
6823-1超声诊断设备中的超声脉冲多普勒成像设备(2012版)
6824医用激光仪器设备
01有源手术器械
6824-1激光手术和治疗设备(除眼科激光光凝机、眼晶体激光乳化设备外)(2002版)(包含医用激光光纤)
06医用成像器械
6824-2激光诊断仪器(2002版);
6824-2激光诊断仪器(2002版)
6807-6胸腔心血管外科用其他器械中的双头剥离匙、内膜剥离器;
6807-6胸腔心血管外科用其他器械中的血管扩张器、血管牵开器;
6807-6胸腔心血管外科用其他器械中的血管打洞钳(器)、心房打洞器、胸骨手钻;
6807-7胸心血管外科用吸引器除静脉撑开器
6808腹部外科手术器械
02无源手术器械
6808-2腹部外科用剪;
6809-5泌尿肛肠科用针、钩;
6809-6泌尿肛肠科用其他器械中的尿道扩张器
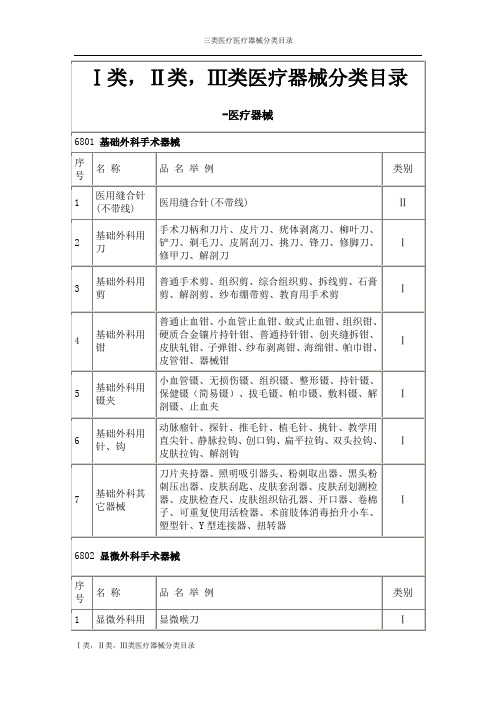
Ⅰ类,Ⅱ类,Ⅲ类医疗器械分类目录
Ⅰ
3
泌尿肛肠科用钳
血管阻断钳、骼血管阻断钳、骼静脉侧壁钳
Ⅱ
肾蒂钳、肠钳、直肠活体取样钳、膀胱肿瘤匙钳、膀胱颈钳、痔核钳
Ⅰ
5
泌尿肛肠科用钩、针
膀胱拉钩、前列腺拉钩、肛门探针
Ⅰ
6
泌尿肛肠科用其他器械
尿道扩张器、肛门镜、阴茎夹、排便清肠器
Ⅰ
J型导尿管、肛肠手术用多功能小针刀、弯头负压吸力式套扎枪
Ⅱ
血管扩张器、血管牵开器、胸骨手钻、双头剥离匙、肋骨骨膜剥离子、内膜剥离器
Ⅰ
心血管吻合器
Ⅲ
7
胸腔心血管外科用吸引器
心内吸引器(头)、左房引流管、冠状动脉吸引器、冠状动脉灌注器、大隐静脉冲洗管、静脉撑开器、短柄吸引器(头)
Ⅱ
6808腹部外科手术器械
序号
名 称
品 名 举 例
类别
2
腹部外科用剪
胃内手术剪、直角剪
Ⅱ
6810矫形外科(骨科)手术器械
序号
名 称
品 名 举 例
类别
1
矫形(骨科)外科用刀、锥
椎管铲刀、椎管锉刀、手锥
Ⅱ
丝锥、髓腔铰刀、加压螺纹钉铰刀、截断刀、截骨刀、胫骨切刀、石膏刀、胫骨切割器、髋关节成型凹凸钻、钻头、铰孔钻、手枪式手摇骨钻
Ⅰ
2
矫形(骨科)外科用剪
双关节棘突骨剪、双关节咬骨剪、骨剪、膝关节韧带手术剪、石膏剪、钢丝剪
Ⅰ
6812妇产科用手术器械
序号
名 称
品 名 举 例
类别
1
妇产科用刀
碎胎刀
Ⅰ
2
妇产科用剪
一次性使用脐带剪
Ⅱ
子宫剪、剖腹产剪、脐带剪、会阴剪
2018医疗器械法律法规目录(最全)

2018医疗器械法律法规目录(最全) 2018医疗器械法律法规目录目录:一、医疗器械法律法规概述1.《医疗器械管理条例》2.《医疗器械分类目录》3.《医疗器械注册管理办法》4.《医疗器械生产企业许可管理办法》5.《医疗器械经营企业许可管理办法》6.《医疗器械广告审查管理办法》7.《医疗器械生产企业质量管理规范》8.《医疗器械经营企业质量管理规范》9.《医疗器械不良事件管理暂行规定》10.《医疗器械不良事件报告与处理管理规定》二、医疗器械注册与备案1.《医疗器械注册与备案办法》2.《医疗器械注册申请技术审评操作规范》3.《医疗器械注册证书管理规定》4.《医疗器械备案管理办法》5.《医疗器械备案结果发布管理办法》6.《医疗器械注册与备案信息发布管理办法》三、医疗器械生产许可1.《医疗器械生产许可申请与管理办法》2.《医疗器械生产许可证管理办法》3.《医疗器械生产许可信息发布管理办法》四、医疗器械经营许可1.《医疗器械经营许可申请与管理办法》2.《医疗器械经营许可证管理办法》3.《医疗器械经营许可信息发布管理办法》五、医疗器械广告审查1.《医疗器械广告审查申报技术指南》2.《医疗器械广告审查规范》3.《医疗器械广告审查费收费标准》六、医疗器械质量管理1.《医疗器械质量管理体系规范》2.《医疗器械不良事件管理规程》3.《医疗器械风险管理指南》4.《医疗器械临床试验技术指南》七、附件1.《医疗器械申报注册申请表格》2.《医疗器械备案申请表格》3.《医疗器械生产许可申请表格》4.《医疗器械经营许可申请表格》5.《医疗器械广告审查申请表格》6.《医疗器械质量监督抽查申请表格》法律名词及注释:1.医疗器械管理条例: 国家卫生健康委员会发布的对医疗器械监督管理的法规。
2.医疗器械分类目录: 医疗器械分门别类的目录,用于对不同类别医疗器械的管理。
3.医疗器械注册管理办法: 对医疗器械注册及相关管理流程的规定。
4.医疗器械生产企业许可管理办法: 对医疗器械生产企业许可及相关管理流程的规定。
2018医疗器械法律法规目录(最全)

2018医疗器械法律法规目录(最全)【一:简洁风格】本文档为2018年医疗器械法律法规目录,详细了医疗器械领域内的法律法规内容。
为保证文档的准确性和完整性,请大家参考使用,并注意附带的附件内容。
一:医疗器械注册管理1.医疗器械注册管理办法2.医疗器械注册申请与节点管理办法3.医疗器械注册评审指南4.医疗器械注册分类管理目录5.医疗器械注册技术资料要求二:医疗器械生产许可管理1.医疗器械生产许可管理暂行办法2.医疗器械生产许可监督检查操作规范3.医疗器械生产许可代理销售监督管理办法4.医疗器械生产许可分类管理目录三:医疗器械经营许可管理1.医疗器械经营许可管理办法2.医疗器械经营许可监督检查操作规范3.医疗器械经营许可分类管理目录4.医疗器械经营许可变更管理办法四:医疗器械生产监督管理1.医疗器械生产许可监督管理办法2.医疗器械生产质量管理规范3.医疗器械生产质量管理体系规范4.医疗器械生产质量检验规范五:医疗器械经营监督管理1.医疗器械经营质量管理规范2.医疗器械经营质量管理体系规范3.医疗器械经营质量监督抽查规范【附件】1.医疗器械注册申请表格样板2.医疗器械生产许可申请表格样板3.医疗器械经营许可申请表格样板【法律名词及注释】1.医疗器械:指人体直接或间接应用于预防、诊断、治疗、矫形或替代人体生理功能而对人体具有主要作用的器具、设备、物质和其他物品。
2.注册管理:对医疗器械的上市销售进行审批和监管管理的制度。
3.生产许可管理:对医疗器械的生产企业进行许可和监督管理的制度。
4.经营许可管理:对医疗器械的经营企业进行许可和监督管理的制度。
5.生产监督管理:对医疗器械的生产质量进行监督和管理的制度。
6.经营监督管理:对医疗器械的经营质量进行监督和管理的制度。
【二:详细风格】本文档为2018年医疗器械法律法规目录,详细了医疗器械领域内的法律法规内容,以供参考使用。
请注意附带的附件内容。
一:医疗器械注册管理1.医疗器械注册管理办法:规定了医疗器械注册的程序、审核要求和监督管理措施等。
医疗器械分类目录(20180801)解读

医疗器械分类目录(20180801)解读一、主要变化新版目录与2002版目录相比,是有很大变化的:将43个子目录精简为22个;增加了产品预期用途和产品描述;产品名称举例则从原有的1008个,扩充到了66609个。
对业内企业来说,焦点核心的还有:几十种医疗器械的管理类别降了,有从三类降为二类的,也有从二类降为一类的。
也有部分产品是升类了的。
还有的产品将不再作为医疗器械管理。
产品类别上的变化是要直接影响医疗器械生产经营企业的,比如生产企业,原本自家产品是三类,降为二类管理之后,企业将无需再跑到北京、到药监总局来进行产品注册,只需在本省药监局注册即可。
从二类降为一类管理的,生产企业则更省事,产品无需注册,只需备案即可。
降类之后,在注册更省事之外,节省的还有注册费用。
以三类降为二类为例,原有境内三类产品首次注册要收费15.36万元,而转到地方注册后,目前收费最便宜的宁夏仅有3.13万元,还有十多个省份则还没开始收费呢。
当然,反过来,对升类产品而言,注册要比现在麻烦一些了,由二类升为三类的,风险级别大增,也将面临药监更为严格和密集的监管举措。
总体上而言,此次新版目录调整还是比较大的。
为此,药监总局也给了医疗器械监管人员和生产、经营、使用单位一定的消化过渡期。
如何个过渡法?过渡期内企业注册申请怎么办?请详细参阅《总局关于实施《医疗器械分类目录》有关事项的通告(2017年第143号)》,该文在CFDA官网上可以查到。
二、降类产品清单1、射频消融设备用灌注泵,管理类别由第三类降为第二类。
2、发光二极管(LED)手术照明灯,由第二类降为第一类。
3、“全自动免疫分析仪”,包括“全自动酶联免疫分析仪”、“全自动化学发光免疫分析仪”、“全自动荧光免疫分析仪”,由第三类降为第二类。
4、微生物鉴定药敏分析仪器、微生物药敏培养监测仪器,由第三类降为第二类。
5、洗板机,由第二类降为第一类。
6、2002版分类目录的“6870-2诊断图象处理软件”中的X射线影像处理系统、核医学成像、医用磁共振成像系统等,统一降为第二类。
(完整版)新版第三类医疗器械分类目录

(完整版)新版第三类医疗器械分类目录新版第三类医疗器械分类目录是中国国家药品监督管理局于2018年发布的医疗器械分类标准,根据医疗器械的功能、适用范围和风险等级进行分类。
该目录的发布对于规范和管理医疗器械市场具有重要意义。
第三类医疗器械是指用于医疗、治疗、预防疾病的非活性物品、设备、仪器或其他物品,其中包括了辅助诊断、治疗、监测、护理、康复和其他相关用途的器械。
根据新版目录,第三类医疗器械被细分为26个类别,这些类别包括:一、骨科器械:用于治疗骨骼系统疾病的器械,如骨钉、骨板、植骨材料等。
二、创伤源止血器械:用于止血的器械,如止血钳、止血带等。
三、血管介入器械:用于血管介入治疗的器械,如导管、支架等。
四、心血管器械:用于心血管疾病治疗的器械,如心脏起搏器、血压计等。
五、介入性诊疗器械:用于介入性诊疗操作的器械,如导丝、导管等。
六、放射治疗器械:用于放射治疗的器械,如放射治疗机、放射保护器械等。
七、超声诊断和治疗器械:用于超声诊断和治疗的器械,如超声探头、超声治疗仪等。
八、临床检验器械:用于临床检验的器械,如血液分析仪、生化分析仪等。
九、医用光学器械:用于眼科和其他医学光学检查的器械,如眼镜、眼镜架等。
十、病理和解剖器械:用于病理和解剖学研究的器械,如显微镜、切片机等。
十一、消毒和灭菌器械:用于消毒和灭菌的器械,如高压蒸汽灭菌器、紫外线消毒器等。
十二、医用敷料器械:用于医用敷料操作的器械,如敷料剪、敷料包装机等。
十三、家庭和个人护理器械:用于家庭和个人护理的器械,如口腔护理器械、物理治疗仪器等。
十四、康复辅助器械:用于康复辅助治疗的器械,如矫形器、假肢等。
十五、消耗性卫生材料和敷料:用于一次性使用的卫生材料和敷料,如手术刀片、纱布等。
十六、体外诊断器械:用于体外诊断的器械,如试纸、血糖仪等。
十七、口腔科器械:用于口腔科治疗的器械,如牙科钻、牙科喷砂机等。
十八、眼科器械:用于眼科治疗的器械,如验光架、角膜刀等。
完整版2018年器械分类目录新
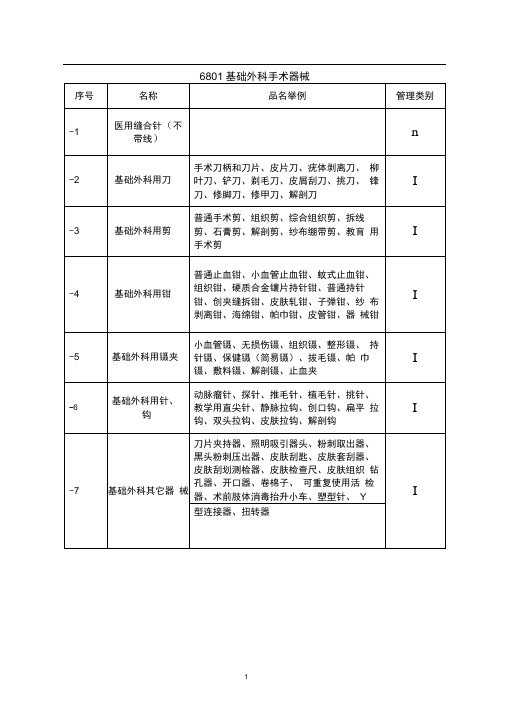
-6
显微外科用
其他器械
显微合拢器
I
6803神经外科手术器械
序号
名称
品名举例
管理类别
-1
神经外科脑 内用刀
脑神经刀、可拆卸式脑膜刀、脑神经刀、 脑膜刀
n
-2
神经外科脑 内用钳
肿瘤摘除钳、脑组织咬除钳
n
银夹钳、U型夹钳、动脉瘤夹钳
i
-3
神经外科脑 内用镊
脑膜镊、垂体瘤镊、肿瘤夹持镊
n
-4
神经外科脑 内用钩、刮
I
-4
基础外科用钳
普通止血钳、小血管止血钳、蚊式止血钳、 组织钳、硬质合金镶片持针钳、普通持针 钳、创夹缝拆钳、皮肤轧钳、子弹钳、纱 布剥离钳、海绵钳、帕巾钳、皮管钳、器 械钳
I
-5
基础外科用镊夹
小血管镊、无损伤镊、组织镊、整形镊、 持针镊、保健镊(简易镊)、拔毛镊、帕 巾镊、敷料镊、解剖镊、止血夹
I
-2
口腔用剪
牙龈剪、全冠剪
I
-3
口腔用钳
拔牙钳、切断牙钳、牙槽咬骨钳、舌钳、
扩大钳
I
-4
口腔用镊、夹
残根镊、牙用镊、长镊、成形片夹
I
-5
口腔用钩、针
牙探针、脓肿探针、牙周袋探针
I
-6
口腔用其它 器械
牙挺、丁字形牙挺、牙根尖挺、牙用锉、 牙骨锤、牙刮匙、根管充填器、牙骨膜分 离器、牙龈分离器、洁治器、刮治器、易9挖器、研光器、粘固粉充填器、银汞合金 充填器、去冠器、口镜、拔髓针柄、水枪 头、热气枪头、吹火管、咬合器、印模托 盘、汞合金输送器、磨牙带环就位器、结 扎杆、带环推子、弓丝成型器、测量器、 牙龈炎冲洗器
2018医疗器械分类目录(最新版)

医疗器械分类目录目录01有源手术器械 (1)02无源手术器械 (6)03神经和心血管手术器械 (16)04骨科手术器械 (23)05放射治疗器械 (33)06医用成像器械 (37)07医用诊察和监护器械 (48)08呼吸、麻醉和急救器械 (56)09物理治疗器械 (62)10输血、透析和体外循环器械 (69)11医疗器械消毒灭菌器械 (75)12有源植入器械 (78)13无源植入器械 (81)14注输、护理和防护器械 (88)15患者承载器械 (102)16眼科器械 (105)17口腔科器械 (116)18妇产科、辅助生殖和避孕器械 (128)19医用康复器械 (136)20中医器械 (139)21医用软件 (143)22临床检验器械 (147)编制说明 (155)01 有源手术器械说明一、范围本子目录包括以手术治疗为目的与有源相关的医疗器械,包括超声、激光、高频/射频、微波、冷冻、冲击波、手术导航及控制系统、手术照明设备、内窥镜手术用有源设备等医疗器械。
二、框架结构本子目录按照产品预期用途和专业技术及功能特点进行层级排序,共划分为10个一级产品类别,在一级产品类别的基础上根据先设备后附件的形式设立二级产品类别共25个,列举120个品名举例。
本子目录包括2002版医疗器械分类目录中《6821医用电子仪器设备》《6822医用光学器具仪器及内窥镜设备》《6824医用激光仪器设备》《6825医用高频仪器设备》《6854手术室急救室诊疗室设备及器具》《6858医用冷疗低温冷藏设备及器具》和三、其他说明(一)医用激光光纤与激光治疗仪配套应用,传输激光器产生的能量,用于激光手术治疗。
依据《关于一次性前列腺治疗套件等产品分类界定的通知》(国食药监械〔2008〕587号)和《国家食品药品监督管理局关于超声肿瘤治疗系统等17个产品分类界定的通知》(国食药监械〔2012〕36号)分类界定文件规定管理类别为二类,分类编码6824。
(医疗药品管理)医疗器械分类目录(食品药品监督局网站)最全版

(医疗药品管理)医疗器械分类目录(食品药品监督局网站)医疗器械分类目录1.无创监护仪器2.呼吸功能及气体分析测定装置3.医用刺激器4.医用刺激器5.血流量、容量测定装置6.电子压力测定装置7.生理研究实验仪器8.耳鼻喉科用镊、夹9.耳鼻喉科用钩、针10.耳鼻喉科用其他器械11.口腔用刀、凿12.口腔用剪13.口腔用钳14.口腔用镊、夹15.口腔用钩、针16.口腔用其它器械17.胸腔心血管外科用刀18.胸腔心血管外科用剪19.胸腔心血管外科用钳胸腔心血管外科用钳20.21.胸腔心血管外科用镊、夹22.胸腔心血管外科用镊、夹23.胸腔心血管外科用钩、针24.胸腔心血管外科用其他器械25.胸腔心血管外科用其他器械26.胸腔心血管外科用吸引器27.腹部外科用剪28.腹部外科用钳29.腹部外科用钩、针30.腹部外科用其他器械31.泌尿肛肠科用剪32.泌尿肛肠科用钳33.泌尿肛肠科用钳34.泌尿肛肠科用钩、针35.泌尿肛肠科用其他器械36.金属、陶瓷类义齿材料37.齿科预防保健材料38.充填辅助材料39.正畸材料40.印模材料41.铸造包埋材料42.模型材料43.矫形(骨科)外科用刀、锥44.矫形(骨科)外科用刀、锥45.矫形(骨科)外科用剪46.矫形(骨科)外科用钳47.矫形(骨科)外科用钳48.矫形(骨科)外科用锯、凿、锉49.矫形(骨科)外科用锯、凿、锉50.矫形(骨科)外科用钩、针51.矫形(骨科)外科用刮52.矫形(骨科)外科用有源器械53.矫形(骨科)外科用有源器械54.矫形(骨科)外科用其它器械55.矫形(骨科)外科用其它器械56.妇产科用刀57.妇产科用剪58.妇产科用钳59.妇产科用镊、夹60.妇产科用钩、针61.妇产科用其他器械62.计划生育用钳63.计划生育用其他器械64.注射穿刺器械65.注射穿刺器械66.烧伤(整形)用刀、凿67.烧伤(整形)用钳68.烧伤(整形)用镊、夹69.烧伤(整形)用其他器械70.体温计71.血压计72.肺量计73.听诊器(无电能)74.叩诊锤(无电能)75.反光器具76.视力诊察器具77.用于心脏的治疗、急救装置78.有创式电生理仪器及创新电生理仪器79.有创医用传感器80.无创医用传感器81.心电诊断仪器82.脑电诊断仪器83.肌电诊断仪器84.其他生物电诊断仪器85.电声诊断仪器86.无创监护仪器87.透析粉、透析液88.植入器材89.植入性人工器官90.接触式人工器官91.支架92.器官辅助装置93.器官辅助装置94.手术及急救装置95.手术及急救装置96.呼吸设备97.呼吸麻醉设备及附件98.呼吸麻醉设备及附件99.婴儿保育设备100.输液辅助装置101.输液辅助装置102.负压吸引装置103.呼吸设备配件104.呼吸设备配件105.医用制气设备106.医用高能射线治疗设备107.高能射线治疗定位设备108.放射性核素治疗设备109.放射性核素诊断设备110.放射性核素诊断设备111.核素标本测定装置112.核素设备用准直装置113.医用射线防护用品114.医用射线防护装置116.血液分析系统117.生化分析系统119.免疫分析系统120.细菌分析系统121.细菌分析系统122.尿液分析系统123.生物分离系统124.血气分析系统125.基因和生命科学仪器126.基因和生命科学仪器127.临床医学检验辅助设备128.医用培养箱129.医用离心机130.病理分析前处理设备131.血液化验设备和器具132.血液化验设备和器具133.人工心肺设备134.氧合器135.人工心肺设备辅助装置136.人工心肺设备辅助装置137.血液净化设备和血液净化器具138.血液净化设备辅助装置139.体液处理设备140.体液处理设备141.彩色超声成像设备及超声介入/腔内诊断设备142.超声母婴监护设备143.超声换能器144.便携式超声诊断设备145.超声理疗设备146.超声辅助材料147.激光手术和治疗设备148.激光诊断仪器149.激光诊断仪器150.介入式激光诊治仪器151.激光手术器械152.弱激光体外治疗仪器153.干色激光打印机154.医用激光仪器设备155.高频手术和电凝设备156.高频手术和电凝设备157.高频电熨设备158.微波治疗设备159.射频治疗设备160.射频治疗设备161.高频电极162.高压氧治疗设备163.电疗仪器164.电疗仪器165.光谱辐射治疗仪器。
2018最新免于进行临床试验医疗器械目录(2018年第94号):附件1+附件2
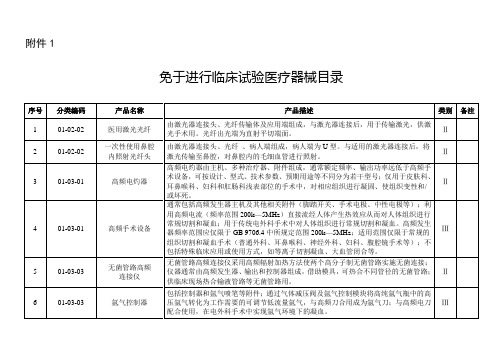
15
01-09-01
内窥镜手术动力系统
产品一般由主机、手柄、刨削刀头组成,通过电机马达带动手柄及刀头进行机械旋转,用于内窥镜手术中实现绞碎或切除组织等手术功能(鼻腔部位手术除外)。适用或参考行业标准YY/T 0955《内窥镜手术设备刨削器》。
Ⅲ
16
01-09-01
鼻窦镜手术动力系统
产品一般由主机、手柄、刨削刀头组成,通过电机马达带动手柄及刀头进行机械旋转,用于鼻窦镜手术中实现切除鼻腔部位组织等手术功能。适用或参考行业标准YY/T 0955《内窥镜手术设备刨削器》。
Ⅱ
13
01-08-02
LED手术照明灯
通常由光源、灯架等组成。用于手术辅助照明,也可单独用于小型手术。不具有无影效果。分为吊顶式、墙面式或移动式。
Ⅱ
14
01-08
一次性使用脊柱外科照明光纤
产品由光源连接头、光纤、头端组成。以无菌形式提供。与照明光源连接后,向手术部位传输光能,为脊柱微创手术提供照明。
通常外形呈直形或弧形,针尖有圆、三角、铲形状,针尾带孔。一般采用不锈钢材料制成。用于缝合组织、皮肤。产品性能指标采用下列参考标准中的适用部分,如:YY/T 0043医用缝合针。
Ⅱ
32
02-07-01
一次性使用荷包缝合针
一次性使用荷包缝合针用金属和缝线制成,由两根缝针、一根非吸收性缝线组成。产品以无菌形式提供,适用于消化道吻合手术中的荷包缝扎。产品性能指标参考YY 0877荷包缝合针标准中的适用部分。
Ⅱ
28
02-06-01
一次性止血夹
由金属、高分子聚合物或其他材料制成,用于外科手术时临时夹闭血管或组织,术后即刻取出。无菌提供,一次性使用。
Ⅱ
【中检院】2018年医疗器械产品分类界定结果汇总

【中检院】2018年医疗器械产品分类界定结果汇总2019年2⽉18⽇,中检院发布《2018年医疗器械产品分类界定结果汇总》,其中涉及573个产品共分七⼤类:⼀、按照III类医疗器械管理的产品(69个);⼆、按照II类医疗器械管理的产品(122个);三、按照I类医疗器械管理的产品(219个);四、不单独作为医疗器械管理的产品(19个);五、按药械组合管理的产品(22个);六、不作为医疗器械管理的产品(110个);七、视具体情况⽽定的产品(12个)。
全⽂具体如下:说明:1.产品分类界定结果是基于申请⼈提供的资料得出,不代表对其产品安全性和有效性的认可,仅作为医疗器械产品注册和备案的参考;结果中产品描述和预期⽤途是⽤于判定产品的管理属性和类别,不代表相关产品注册或备案内容的完整表述。
2.《医疗器械分类⽬录》中暂⽆对应⼀级产品类别的“分类编码”以“00”表⽰,如“等离⼦体治疗仪”的分类编码:09-00。
⼀、按照III类医疗器械管理的产品(69个)1.硬式⾓膜接触镜护理液:由⼄⼆胺四⼄酸⼆钠、苯甲醇、聚⼄⼆醇⾟基苯基醚、⼗⼆烷基醚硫酸钠、蒸馏⽔组成。
⽤于硬式⾓膜接触镜的清洁、消毒。
清洁、消毒后的接触镜,必须⽤清⽔或⽣理盐⽔彻底冲洗⼲净后⽅可配戴。
分类编码:16-06。
2.离体⾓膜中期保存液:由DMEM培养基、硫酸软⾻素、低分⼦右旋糖酐、地塞⽶松、妥布霉素、HEPES和注射⽤⽔组成。
⽤于供体捐献的离体⾓膜的储存、运输。
使⽤时将供体捐赠的离体⾓膜浸泡在该保存液中,通过保存液中含有的营养物质可以保持⾓膜内⽪细胞和⾓膜缘上⽪细胞的活性,从⽽延长⾓膜保存时间。
分类编码:02-15。
3.视⽹膜光疗仪:由佩戴外罩、主机、数据管理系统和附属配件(电源适配器、数据线)组成。
该治疗仪采⽤特定波长和亮度的LED连续光源,患者在睡眠期间佩戴该治疗仪照射眼底。
通过光照法减弱圆柱细胞暗适应过程,抑制⾎管内⽪⽣长因⼦过度⽣长,⽤于缓解糖尿病视⽹膜病变。
新版医疗器械分类目录就要实施!速度学习!

新版医疗器械分类目录就要实施!速度学习!还有10天,新版医疗器械分类目录就要实施啦,很多朋友还有疑问不知道如何应对。
今天医疗人咖啡就分享这篇文章供大家学习。
为贯彻实施《医疗器械监督管理条例》和《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)的要求,国家食品药品监督管理总局组织修订了《医疗器械分类目录》,现予发布,自2018年8月1日起施行。
新旧分类目录对比目录框架2017版2002版子目录数√√产品类别一级产品类别(二级目录)二级产品类别(三级目录)√产品描述√×预期用途√×品名举例√√管理类别√√目录内容2017版2002版子目录树2243产品类别206个一类产品类别1157个二类产品类别260个产品名称举例6609个1008个降低管理类别40种/产品子目录由旧版的43类精简为22类;目录中增加的“产品描述”和“预期用途”,是对一类产品共性内容的基本描述,用于指导具体产品所属类别的综合判定。
除此之外,此次还对部分医疗器械产品的管理类别进行了调整。
管理类别升高的产品序号子目录产品旧管理类别新管理类别103 神经和心血管手术器械脑压板ⅠⅡ205 放射治疗器械主动呼吸控制系统ⅡⅢ管理类别降低的产品序号子目录产品旧管理类别新管理类别101有源手术器械射频消融设备用灌注泵ⅢⅡ206医用成像器械胃肠道造影显像剂Ⅲ3胃肠超声显像粉ⅢⅡ4放射性核素扫描装置ⅢⅡ5内窥镜气囊控制器ⅢⅡ610 输血、透析和体外循环器械碘液保护帽ⅢⅡ714 注输、护理和防护器械一次性使用活检针Ⅲ8接触胸腔、腹腔、脑室、腰椎、体内创面或体表真皮深层及其以下组织创面的引流导管ⅢⅡ9髂骨穿刺针ⅢⅡ10用于非慢性创面、接触真皮深层及其以下组织且所含成分不可被人体吸收的的医用敷料ⅢⅡ1117 口腔科器械脱敏剂类产品ⅢⅡ12银汞合金Ⅱ13种植体密封材料ⅢⅡ14牙周塞治剂ⅢⅡ15洁牙粉ⅢⅡ16根管扩大液、根管清洗剂ⅢⅡ17临时冠桥树脂ⅢⅡ21 医用软件X射线影像处理系统、核医学成像、医用磁共振成像系统ⅢⅡ1922临床检验器械全自动酶联免疫分析仪、全自动化学发光免疫分析仪、全自动荧光免疫分析仪ⅢⅡ20微生物鉴定药敏分析仪器、微生物药敏培养监测仪器ⅢⅡ序号子目录产品旧管理类别新管理类别01有源手术器械发光二极管(LED)手术照明灯ⅡⅠ204骨科手术器械接触椎间隙的非无菌提供的骨科重复使用手术器械ⅡⅠ3开口用锥ⅡⅠ4可能接触中枢神经系统的非无菌提供的骨科用凿、骨科用锉、骨科用铲、脊柱外科定位/导向/测量器械、脊柱外科开孔扩孔器械、脊柱外科神经根探子、脊柱外科植骨块嵌入器、脊柱外科椎弓根钉尾部切断器、脊柱手术通道器械、脊柱外科椎体复位器、骨科剥离保护器、骨科组织保护器具Ⅰ506医用成像器械带有LED光源的医用光学放大器具ⅡⅠ614 注输、护理和防护器械足部隔离用品、隔离护罩ⅡⅠ7造口袋(含造口底盘)、造口护理用品、造口底盘、造口栓、防漏膏、造口护肤粉、造口皮肤保护剂等造口护理产品ⅡⅠ817 口腔科器械洁牙工作尖和仅用于打磨、抛光的车针ⅡⅠ9正畸弹簧ⅡⅠ10牙托梗ⅡⅠ1122临床检验器械洗板机ⅡⅠ不按照医疗器械管理序号子目录产品备注105放射治疗器械放射治疗患者床板随整机注册,不单独按医疗器械管理211医疗器械消毒灭菌器械说明医用伽玛射线灭菌器不用于医疗环境,且无注册产品,不列入目录314注输、护理和防护器械注射器用活塞不具有医疗器械的功能和目的,不按照医疗器械管理4输液瓶贴不符合医疗器械定义,不按照医疗器械管理5输注工作站不符合医疗器械定义,不按照医疗器械管理616眼科器械试镜架不符合医疗器械定义,不按照医疗器械管理718妇产科、辅助生殖和避孕器械含消毒剂(抗菌剂)阴道填塞产品不按照医疗器械管理821 医用软件医疗信息管理软件仅是医院管理工具,不按照医疗器械管理9远程医疗会诊系统软件如果不包含医学图像或者数据,则不按照医疗器械管理106870-5人体解剖学测量软件预期用途不完全符合医疗器械定义,不按照医疗器械管理1122临床检验器械与临床检验有关,但产品自身不具有医疗器械功能的产品,如:移液器、移液管,普通反应杯、反应管、反应板,普通采样杯、采样管、样本收集器,在临床实验室用于检测前/后样本传输、加/去盖、条形码识别等功能的样本管理系统等不按照医疗器械管理其他管理类别规范序号子目录产品新管理类别101 有源手术器械医用激光光纤Ⅱ203神经和心血管手术器械接触血液循环系统的心脏拉钩、心房拉钩、心室拉钩、房室拉钩、二尖瓣膜拉钩、凹凸齿止血夹Ⅰ3心血管手术或脑外科手术冲吸器Ⅱ404骨科手术器械骨髓抽吸和活检系统电钻Ⅱ5与有源设备(如电动骨钻、电动骨锯、气动骨钻)连接使用的钻头、刀头、锯片、扩髓器、刨刀、磨头等配套工具Ⅰ6髌骨爪Ⅲ7光学定位引导系统Ⅲ816眼科器械眼科用激光光纤Ⅲ917口腔科器械咬合关系记录/检查材料Ⅰ10义齿试用材料Ⅰ11金属、陶瓷材料制成的固位桩Ⅱ12替代体Ⅰ13研磨材料用于口内,Ⅱ14用于口外,Ⅰ1519医用康复器械具有矫形功能产品Ⅱ16仅具有固定支撑功能产品Ⅰ1721 医用软件诊断功能软件不直接给出诊断结论,Ⅱ18提供明确的诊断提示,Ⅲ19全自动血库系统Ⅲ在新版《分类目录》出台同时,发布了总局关于实施《医疗器械分类目录》有关事项的通告(2017年第143号)对新版《分类目录》做出相关解释过渡期要求医疗器械分类是医疗器械注册、生产、经营、使用全过程监督的基础,新版《分类目录》的出台对医疗器械的注册、生产、经营、使用等各环节都将产生影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6804眼科手术器械
6807胸腔心血管外科手术器械
6808腹部外科手术器械
6809泌尿肛肠外科手术器械
6810矫形外科(骨科)手术器械
6812妇产科用手术器械
6813计划生育手术器械
6815注射穿刺器械
6816烧伤(整形)科手术器械
6820普通诊察器械
6821
6822 医用光学器具、仪器及内窥镜设备
6823医用超声仪器及有关设备
6824医用激光仪器设备
6825医用高频仪器设备
6826物理治疗设备
6827中医器械
6831医用X射线附属设备及部件
6832医用高能射线设备
6833医用核素设备
6834医用射线防护用品、装置
6840临床检验分析仪器
6841医用化验和基础设备器具
6845体外循环及血液处理设备
6846植入材料和人工器官
6854手术室、急救室、诊疗室设备及器具
6857消毒和灭菌设备及器具
6858医用冷疗、低温、冷藏设备及器具
6863口腔科材料
6864医用卫生材料及敷料。
