医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(五)
2024年执业药师之药事管理与法规题库及精品答案

2024年执业药师之药事管理与法规题库及精品答案单选题(共40题)1、《药品经营质量管理规范》的英文缩写是()。
A.GAPB.GLPC.GCPD.GSP【答案】 D2、2015年,某省的甲药品生产企业欲对其生产的感冒药进行广告宣传,并向相关部门递交了审批申请,在审查机关审查过程中,发现该企业递交的资料中存在虚假信息,审查机关依法对该企业进行了处罚。
A.省级药品监督管理部门B.省级工商行政管理部门C.县级药品监督管理部门D.市级药品监督管理部门【答案】 A3、在境外因药品不良反应被暂停销售、使用或者撤市的,药品生产企业应当在获知后,书面报国家药品监督管理部门和国家药品不良反应监测中心,该时限为()。
A.12小时内B.24小时内C.48小时内D.72小时内4、某市药品监督管理部门在对某医药论坛监控时发现,有违法分子长期通过网络销售从非法渠道进口的贵重抗癌药品。
经查,何某从印度直接购买药品,通过其他方式将药品带到国内,再通过网店和医药论坛等将药品销往全国各地。
A.何某的行为不合法B.抗肿瘤药为处方药,不得通过网络销售给甲C.何某涉嫌销售假药D.甲购买印度产“易瑞沙”为自用,可以从轻处罚【答案】 D5、(2019年真题)根据《执业药师职业资格制度规定》,关于执业药师注册条件和要求的说法,错误的是A.取得执业药师职业资格证书并经注册方能执业B.首次注册应在取得职业资格证书后5年内申请注册C.遵纪守法,无不良信息记录D.身体健康,能坚持在执业药师岗位工作,并经执业单位考核同意【答案】 B6、经营者销售商品,违背购买者的意愿搭售商品或者附加其他不合理的条件属于A.限制竞争行为B.商业贿赂行为C.诋毁商誉行为D.混淆行为7、医疗机构要变更《医疗机构制剂许可证》许可事项,原审核、批准机关应当自收到申请之日起作出决定的期限为A.15 日B.30 日C.3 个月D.6 个月【答案】 A8、临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期,其中Ⅳ期在()阶段进行。
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(三十五)
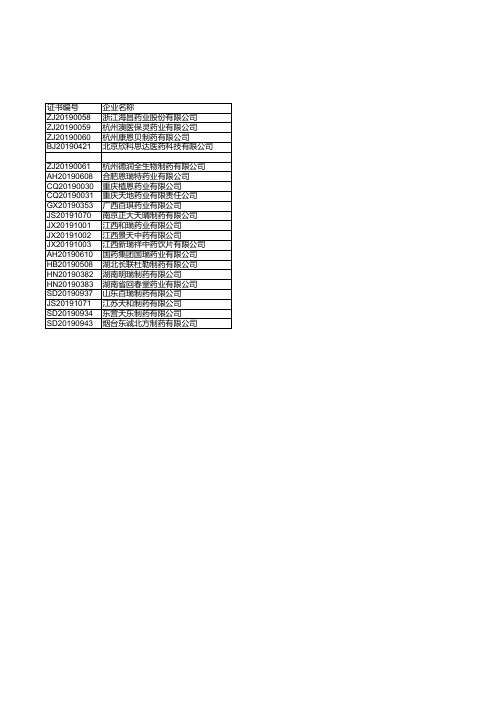
中国2018年通过《药品生产质量管理规范(2010年修订)》认证企业统计 摘编自《中国医药统计年报2018·综合册》
中国2018年通过《药品生产质量管理规范(2010年修订)》认证企业统计(三十五) 认证范围 原料药(碘海醇) 片剂(含外用).胶囊剂 片剂.胶囊剂 体内放射性药品(冻干粉针剂).注射用亚锡二巯丁二钠.注射用亚锡焦磷酸钠.注射用亚锡喷替酸.注射用亚锡亚甲基 注射用亚锡双半胱氨酸.注射用亚锡聚合白蛋白.注射用亚锡双半胱乙酯 中药饮片(净制.切制.炒制.蒸制.发酵) 硬胶囊剂 原料药(奥利司他) 无菌原料药(美罗培南.氨曲南) 片剂.硬胶囊剂.颗粒剂.糖浆剂.合剂(口服液).口服溶液剂.煎膏剂.酒剂.酊剂(内服).栓剂.乳膏剂.中药前处理及提 原料药(帕瑞昔布钠.硼替佐米) 中药饮片含直接口服中药饮片(净制.切制.炒制.炙制.煅制.蒸制) 中药饮片(净制.切制.炒制.炙制.煅制.蒸制.煮制.燀制.制炭) 中药饮片含直接口服饮片(净制.切制.炒制.炙制.煅制.蒸制) 小容量注射剂(2号生产线).冻干粉针剂(1号生产线).原料药(依达拉奉.吡嘧司特钾.唑来膦酸) 大容量注射剂(玻瓶一线.二线) 原料药(卤米松).乳膏剂(激素类) 片剂.颗粒剂.硬胶囊剂.丸剂(水蜜丸.水丸).口服液.糖浆剂(含中药提取) 无菌原料药(苯唑西林钠.氯唑西林钠.阿莫西林钠.舒巴坦钠)(101车间无菌原料药生产线) 原料药(磺胺醋酰钠) 原料药(肝素钠.依诺肝素钠) 冻干粉针剂(含激素类.注射剂一车间)
摘编自《中期 2019.06.03 2019.06.03 2019.06.03 2019.06.03
有效期至 2024.06.02 2024.06.02 2024.06.02 2024.06.02
2019.06.03 2019.06.04 2019.06.04 2019.06.04 2019.06.04 2019.06.04 2019.06.04 2019.06.04 2019.06.04 2019.06.05 2019.06.05 2019.06.05 2019.06.05 2019.06.05 2019.06.05 2019.06.05 2019.06.05
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(四十一)

认证日期 2019.07.08 2019.07.08 2019.07.08 2019.07.08 2019.07.08 2019.07.09 2019.07.11 2019.07.11 2019.07.11 2019.07.11 2019.07.12 2019.07.12 2019.07.12 2019.07.12 2019.07.12 2019.07.12 2019.07.12 2019.07.12 2019.07.15 2019.07.15 2019.07.15 2019.0管理规范(2010年修订)》认证 企业名称
北京双吉制药有限公司 北京同仁堂科技发展股份有限公司制药厂 北京北方生物技术研究所有限公司 广东罗浮山国药股份有限公司 建昌帮药业有限公司 金鸡药业股份有限公司 广西伟健药业有限公司 贵州古耕农牧业发展有限公司民族中药饮片厂 贵州泰邦生物制品有限公司 贵州圣济堂制药有限公司 天水宏康气体有限公司 甘肃众友药业中药饮片加工有限公司 江苏豪森药业集团有限公司 江苏豪森药业集团有限公司 正大天晴药业集团股份有限公司 山东益健药业有限公司 山东华鲁制药有限公司 山东科兴生物制品有限公司 广西禅方药业有限公司 广西万寿堂药业有限公司 江苏中兴药业有限公司 常州市阳光药业有限公司
有效期至 2024.07.07 2024.07.07 2024.07.07 2024.07.07 2024.07.07 2024.07.08 2024.07.10 2024.07.10 2024.07.10 2024.07.10 2025.07.11 2024.07.11 2024.07.11 2024.07.11 2024.07.11 2024.07.11 2024.07.11 2024.07.11 2024.07.14 2024.07.14 2024.07.14 2024.07.15
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(十三)

企业名称
绍兴富源气体有限公司 南京制药厂有限公司 河北药王制药集团有限公司 河北爱尔海泰制药有限公司 石药集团中诺药业(石家庄)有限公司 河北常山生化药业股份有限公司 河北旭宇金坤药业有限公司
摘编自《中国医药统计年报2018·综合册》
认证日期 2018.12.21 2018.12.24 2018.12.25 2018.12.25 2018.12.25 2018.12.25 2018.12.25
有效期至 2023.12.20 2023.12.23 2023.12.24 2023.12.24 2023.12.24 2023.12.24 2023.12.24
2018.12.25 2018.12.25 2018.12.25 2018.12.25 2018.12.25 2018.12.26 2018.12.26 2018.12.26 2018.12.26 2018.12.27 2018.12.27 2018.12.27 2018.12.24 2021.09.10 2023.12.24 2023.12.24 2021.08.02 2023.12.25 2023.12.25 2023.12.25 2023.12.26 2023.12.26 2023.12.26 2023.12.26
HE20180113 HE20180114 HE20180115M JS20180965 JS20180966 AH20160339 AH20180547 AH20180550 ZJ20190001 SC20180113 SX20180254 GD20180924 JS20180968
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(四十)

赛诺菲(北京)制药有限公司 湖北东信药业有限公司 湖北恒安芙林药业股份有限公司 连云港润众制药有限公司 南京扬子石化比欧西气体有限责任公司 北京汉典制药有限公司 江西科伦药业有限公司 江西希尔康泰制药有限公司 江西科伦药业有限公司 广东康富来药业有限公司 珠海同源药业有限公司 安徽大西北中药饮片有限公司 安徽汉枫中药饮片有限公司 合肥天麦生物科技发展有限公司 合肥天麦生物科技发展有限公司 华颐药业有限公司 宜昌东阳光长江药业股份有限公司 江苏恒瑞医药股份有限公司
摘编自《中国医药统计年报2018·综合册》
认证日期 有效期至 2019.07.01 2024.06.30 2019.07.01 2024.06.30
2019.07.01 2019.07.01 2019.07.01 2019.07.01 2019.07.01 2019.07.02 2019.07.02 2019.07.02 2019.07.02 2019.07.04 2019.07.04 2019.07.05 2019.07.05 2019.07.05 2019.07.05 2019.07.05 2019.07.05 2019.07.05
证书编号 BJ20190426 BJ20190427
企业名称 北京本草方源药业集团有限公司 北京紫云腾中药饮片有限公司
BJ20190429 HB20190514 HB20190515 JS20191092 JS20191093 BJ20190428 JX20150001 JX20160024 JX20180031 GD20191023 GD20191024 AH20190620 AH20190621 AH20190622 AH20190623 BJ20190430 HB20190516 JS20180792
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(四十二)
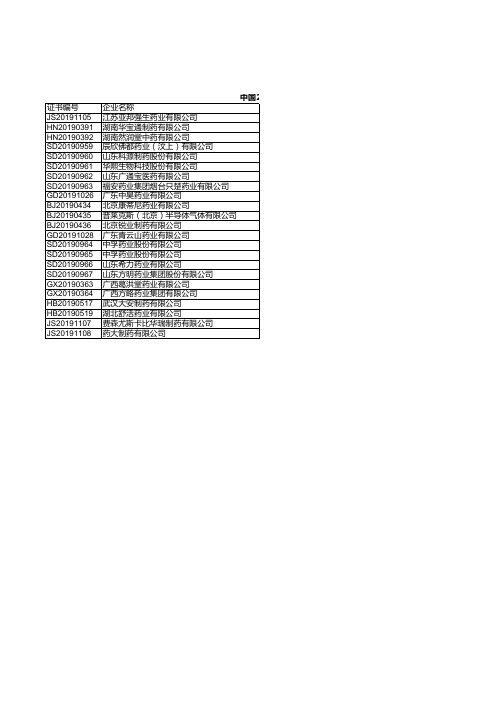
有效期至 2024.07.15 2024.07.16 2024.07.16 2024.07.16 2024.07.16 2024.07.16 2024.07.16 2024.07.16 2024.07.17 2024.07.18 2024.07.18 2024.07.18 2024.07.18 2024.07.18 2024.07.18 2024.07.18 2024.07.18 2024.07.21 2024.07.21 2024.07.21 2024.07.21 2024.07.21 2024.07.21
证书编号 JS20191105 HN20190391 HN20190392 SD20190959 SD20190960 SD20190961 SD20190962 SD20190963 GD20191026 BJ20190434 BJ20190435 BJ20190436 GD20191028 SD20190964 SD20190965 SD20190966 SD20190967 GX20190363 GX20190364 HB20190517 HB20190519 JS20191107 JS20191108
摘编自《中国医药统计年报2018·综合册》
中国医药统计年报:中国2018年中成药主要品种产量统计(二百七十五)

万瓶
10ml/支
万支
河南同源制药有限公司
万支
广州市香雪制药股份有限公司
万支
河南百年康鑫药业有限公司
万支
远大医药黄石飞云制药有限公司
万支
杭州华润老桐君药业有限公司
万支
广州花城药业有限公司
万支
哈尔滨泰华药业股份有限公司
万支
河北恒利集团制药股份有限公司
万支
江苏康缘药业股份有限公司
万支
浙江大德药业集团有限公司
万支
10ml/支
万支
正大青春宝药业有限公司
万支
产量 2029.284 1386.58 277.974 276.68 88.05 12.33 12.33 299.14 299.14 3691.381 2223.3 696.65 517.36 254.071 498.49 498.49 52.19 52 0.19
111349.416 42051.2
27231.055 15346.17 12693.08 10392.08 1911.42 776.1 597 291.308 60.003 67.92 67.92
摘编自《中国医药统计年报2018·中药生物制药分册》
产品名称 康复新液
康复新液 康复新液 康复新液
康复新液 抗扁桃腺炎合剂 抗病毒口服液
抗衰老口服液
中国2018年中成药主要品种产量统计(二百七十五)
规格
生产单位
计量单位
50ml/瓶
万瓶
四川好医生攀西药业有限责任公司
万瓶
昆明赛诺制药股份有限公司
万瓶
内蒙古京新药业有限公司
万瓶
湖南科伦制药有限公司
万瓶
60ml/瓶
药品年度报告标准管理规程

药品年度报告标准管理规程1.目的:本规程的目的是建立药品年度报告编写管理规程,指导企业对所持有药品的生产销售、上市后研究、风险管理等方面的信息和数据进行梳理总结,客观评价产品生产与批准工艺的一致性,确保产品的工艺稳定可控,产品始终如一地保持一定的质量水平,为持续改进产品质量和管理风险提供依据。
2.范围:本规程适用于本企业生产的所有产品。
3.职责:QA负责名类数据的收集、统计、分析工作,质管部起草产品年度报告。
4.内容:4.1 定义:年度报告是指持有人按自然年度收集所持有药品的生产销售、上市后研究、风险管理等方面的信息和数据,梳理总结形成的报告。
年度报告制度是指持有人编制、上报、管理年度报告的程序及要求。
4.2 每年3月底前,汇总上一年度的药品生产销售、上市后研究、风险管理等情况,编写年度报告并通过全国药品年度报告报送和管理平台完成上报。
年度报告上报前需由企业负责人审核、批准,年度报告的信息和数据应当真实、准确、完整和可追溯。
4.3 年度报告编写内容包括:4.3.1 企业基本情况,包括药品生产许可信息、生产场地信息等。
4.3.2 产品基本信息包括产品名称、规格、处方、工艺等。
4.3.3 产品全年生产销售状况及产品放行情况、市场抽检情况回顾(包括委托生产情况)。
4.3.4 原辅料及包装材料质量情况回顾(包括供应商变化及审计情况)。
4.3.5 产品稳定性考察情况、质量情况回顾,应包括各关键指标的趋势分析。
4.3.6 产品上市后研究、用户投诉、不良反应信息、产品召回情况等。
4.3.7 偏差处理情况、变更控制情况回顾;产品风险管理情况等。
4.3.8 不合格品销毁处理情况。
4.3.9 相关验证情况回顾、设备、公用系统情况回顾等。
4.3.10 产品年度质量回顾情况。
4.4 我公司指定A负责各类数据的收集、统计、分析工作,质量管理部负责起草产品年度报告。
4.5 年度报告编号格式:年度报告编号方式为:NB-yyyy-xxxx-xx,前两位为年度报告的“年报”拼音简写,中间四位为企业名称缩写,后四位为年份,最后两位为申报序号,从01开始,第一次申报为01,第二次为02,以此类推。
医药年报:中国2018年按医药工业主营业务收入企业的主要经济指标分析统计(三)

-
天津市
1523623
55362
579590 944033
-
河北省
3098059
265328
1264967 1833092
-
山西省
482246
31615
140785 341461
-
内蒙古自治区 15918
-
4807
11111
-
辽宁省
1116485
79882
475160 641325
-
吉林省
2092520
255152
1002150 1090370
-
黑龙江省
1973057
111025
907715 1065342
-
上海市
2222511
59659
1044617 1177894
-
江苏省
4111563
385974
1570590 2540973
-
浙江省
6996531
781416
2478742 4517789
-
安徽省
268021 602094
-
湖南省
708261
11125
210523 497738
-
广东省
2950703
1523006
1134392 1816311
-
广西自治区 165400
10013
64624
100776
-
海南省
264528
57095
97630
166898
-
重庆市
1453895
263553
420730 1033165
医药年报:中国2018年全部工业企业法人单位按资产总额排序统计(三)

89
注:标"※"表示该集团采用合并形式排名.其下属企业信息请参见后注
摘编自《中国医药统计年报2018·综合册》
93
※82 贵州百灵企业集团制药股份有限公司
82
※83 山东罗欣药业集团股份有限公司
92
※84 山东新华制药股份有限公司
93
※85 普洛药业股份有限公司
91
※86 深圳翰宇药业股份有限公司
96
※87 辰欣科技集团有限公司
80
※88 南京先声东元制药有限公司
90
※89 石家庄四药有限公司
96
※90 上海创诺医药集团有限公司
中国2018年全部工业企业法人单位按资产总额排序统计【前500
No. 企业名称
下属企业后注页
67 恒康医疗集团股份有限公司
/
68 贵州信邦制药股份有限公司
/
69 赛诺菲(杭州)制药有限公司
/
※70 浙江海翔药业股份有限公司
101
※71 烟台东诚药业集团股份有限公司
100
※72 费森尤斯卡比(中国)投资有限公司
81
73 阿斯利康制药有限公司
/
※74 神威药业集团有限公司
96
※75 山东鲁抗医药股份有限公司
92
76 西安杨森制药有限公司
/
※77 华兰生物工程股份有限公司
85
※78 贵州益佰制药股份有限公司
82
※79 京新控股集团有限公司
88
※80 成都地奥制药集团有限公司
80
※81 山东睿鹰制药集团有限公司
பைடு நூலகம்
93
91 浙江永太科技股份有限公司
医药年报:中国2018年通过仿制药质量和疗效一致性评价品种统计(七)

147 蒙脱石散
3g 浙江海力生制药有限公司
国药准字H19980050
148 米氮平片
15mg 哈尔滨三联药业股份有限公司
国药准字H20060702
149 米非司酮片
lOmg 华润紫竹药业有限公司
国药准字H20010633
150 米非司嗣片
25mg 华润紫竹药业有限公司
国药准字H10950003
151 奈韦拉平片
155 瑞格列奈片
lmg 江苏豪森药业集团有限公司
国药准字H20103637
156 瑞舒伐他汀钙片
5mg 浙江京新药业股份有限公司
ቤተ መጻሕፍቲ ባይዱ
国药准字H20080482
157 瑞舒伐他汀钙片
5mg 浙江海正药业股份有限公司
国药准字H20143337
158 瑞舒伐他汀钙片
5mg 鲁南贝特制药有限公司
国药准字H20080240
H20180008
167 碳酸氢钠片
0.5g 湖南汉森制药股份有限公司
国药准字H43020783
注:通过仿制药质量和疗效一致性评价品种数据截至2019年8月31日.
摘编自《中国医药统计年报2018·综合册》
种统计(七) 是否289基药目录
是 是 是 是 否 是 是 是 是 否 否 否 否 否 否 否 否 否 否 否 否 否 否 是
》
批准日期 2019.07.19 2019.07.19 2019.08.14 2019.08.30 2018.08.22 2018.12.28 2018.12.28 2018.05.14 2018.12.20 2019.01.16 2018.11.30 2018.12.13 2018.02.09 2018.07.06 2019.02.02 2019.03.05 2019.04.03 2017.12.27 2018.02.09 2018.07.06 2018.10.08 2019.02.02 2019.04.03 2019.03.21
2024年执业药师之药事管理与法规高分通关题型题库附解析答案

2024年执业药师之药事管理与法规高分通关题型题库附解析答案单选题(共40题)1、近年来,相关部门对中药材的监管力度不可谓不大,对中药材市场乱象的整治不可谓不严厉。
2012年9月,国家食药监总局曝光了安徽一批生产企业通过违法给中药饮片染色达到增重目的的情况。
其中,6家企业被收回GAP证书,并对其中12家企业立案调查。
A.真实B.优质C.可控D.安全【答案】 D2、有效期的标注自分装日期计算A.药品通用名称B.药品商品名称C.注册商标D.生物制品【答案】 D3、医疗器械召回分为三级召回的依据是A.风险程度B.安全隐患C.缺陷严重程度D.使用期限【答案】 C4、属于《药品经营许可证》许可事项的变更,应按规定重新办理《药品经营许可证》的是A.改变药品经营企业注册地址B.更换药品经营企业采购负责人C.改变药品经营方式D.改变药品经营企业组织架构【答案】 C5、下列属于劣药的认定及按劣药论处的情形是A.超过有效期的B.变质的C.被污染的D.使用依照本法必须取得批准文号而未取得批准文号的原料药生产的【答案】 A6、根据药品零售的经营行为管理要求药学服务人员应当确认个人消费者为成年人,不确定时可查验个人消费者身份证信息,不得向未成年人销售的是A.第二类精神药品B.含特殊药品复方制剂C.含兴奋剂类药品D.药品类易制毒化学品【答案】 A7、根据《药品不良反应报告和监测管理办法》使用药品后,导致显著的人体器官功能损伤的药品不良反应属于A.常见药品不良反应B.轻微药品不良反应C.新的药品不良反应D.严重药品不良反应【答案】 D8、对提供虚假材料申请药品广告审批,取得药品广告批准文号的,药品广告审查机关在发现后应当撤销该药品广告批准文号,几年内不受理该企业该品种的广告审批申请A.1年B.2年C.3年D.5年【答案】 C9、根据《处方管理办法》,医疗机构为门诊一般患者开具吗啡缓释片,每张处方的最大用量为A.一次常用量B.3日常用量C.7日常用量D.15日常用量【答案】 C10、药品经营企业的药品销售凭证应当A.保存2年以上B.保存3年以上C.保存至超过药品有效期1年,但不少于2年D.保存至超过药品有效期1年,但不少于3年【答案】 D11、(2015年真题)责令停产停业属于()A.民事责任B.刑事责任C.行政处罚D.行政处分【答案】 C12、发证机关对持证企业必须进行现场检查的情况是A.上年度销售超亿元的大型企业B.上年度被盗的零售药店C.上一年新开办的企业D.许可证即将到期的企业【答案】 C13、甲省乙市丙县的A药品生产企业近日想要发布药品广告来扩大其所生产药品的知名度,从而扩大市场,提高营业额。
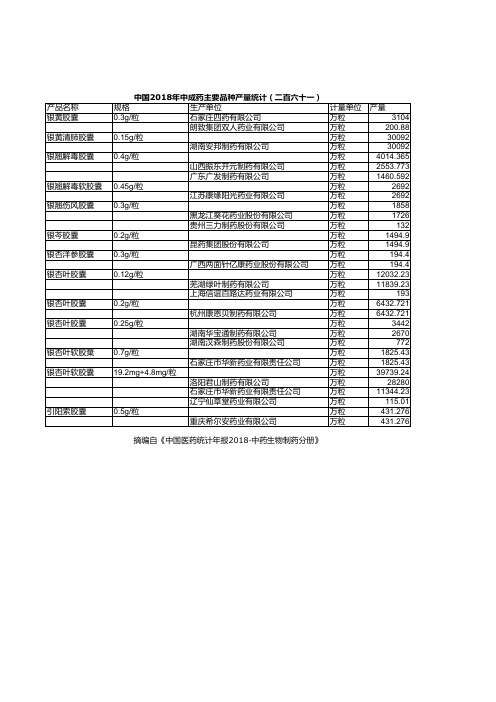
中国医药统计年报:中国2018年中成药主要品种产量统计(二百六十一)
杭州康恩贝制药有限公司
0.25g/粒
湖南华宝通制药有限公司
湖南汉森制药股份有限公司
0.7g/粒
石家庄市华新药业有限责任公司
19.2mg+4.8mg/粒
洛阳君山制药有限公司
石家庄市华新药业有限责任公司
辽宁仙草堂药业有限公司
0.5g/粒
重庆希尔安药业有限公司
计量单位
万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒
0.4g/粒
山西振东开元制药有限公司
广东广发制药有限公司
0.45g/粒
江苏康缘阳光药业有限公司
0.3g/粒
黑龙江葵花药业股份有限公司贵州三力Leabharlann 药股份有限公司0.2g/粒
昆药集团股份有限公司
0.3g/粒
广西两面针亿康药业股份有限公司
0.12g/粒
芜湖绿叶制药有限公司
上海信谊百路达药业有限公司
0.2g/粒
产品名称 银黄胶囊 银黄清肺胶囊 银翘解毒胶囊
银翘解毒软胶囊 银翘伤风胶囊
银芩胶囊 银杏洋参胶囊 银杏叶胶囊
银杏叶胶囊 银杏叶胶囊
银杏叶软胶棄 银杏叶软胶囊
引阳索胶囊
中国2018年中成药主要品种产量统计(二百六十一)
规格
生产单位
0.3g/粒
石家庄四药有限公司
朗致集团双人药业有限公司
0.15g/粒
湖南安邦制药有限公司
28280 11344.23
115.01 431.276 431.276
摘编自《中国医药统计年报2018·中药生物制药分册》
医药年报:中国2018年通过《药品生产质量管理规范》认证企业统计(七)

2018.10.11 2018.10.11 2018.10.11 2018.10.11 2018.10.12 2018.10.12 2018.10.12 2018.10.12 2018.10.14
2023.10.10 2023.10.10 2023.10.10 2023.10.10 2023.10.11 2023.10.11 2023.10.11 2023.10.11 2023.10.13
摘编自《中国医.09 2018.10.09 2018.10.09 2018.10.09 2018.10.09 2018.10.09 2018.10.09 2018.10.09 2018.10.09 2018.10.11
有效期至 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.08 2023.10.10
JX20180027 SD20180783 SD20180784 SD20180785 JS20180913 JS20180915 JS20180916 QH20180065 GS20180297
江西珍视明药业有限公司 山东方明药业集团股份有限公司 山东辰龙药业有限公司 瑞阳制药有限公司 江苏传承中药有限公司 南京正大天晴制药有限公司 南京美瑞制药有限公司 青海普兰特药业有限公司 甘肃九州天润中药产业有限公司
中国2018年通过《药品生产质量管理规范(2010年修订)》认证企 摘编自《中国医药统计年报2018·综合册》
中国2018年通过《药品生产质量管理规范(2010年修订)》认证企业统计(七) 认证范围 硬胶囊剂(含中药提取) 茶剂.片剂.硬胶囊剂.颗粒剂.中药前处理及提取车间(口服制剂) 体内放射性药品[小容量注射剂(氟[18F]脱氧葡糖注射液)] 粉针剂.冻干粉针剂(1线).小容量注射剂(最终灭菌) 大容量注射剂(A线.B线.聚丙烯输液瓶.直立式聚丙烯输液袋) 原料药(甘油磷酸钠.液状甘油磷酸钠) 大容量注射剂(112车间1线.玻璃输液瓶.抗肿瘤药).小容量注射剂(202车间1线.2线.3线.玻璃安瓿.非最终灭菌.含激 小容量注射剂(针剂车间.小容量注射剂生产线) 大容量注射剂(药品生产车间零号生产线.一号生产线) 中药饮片(净制.切制.炒制.炙制.制炭.锻制.蒸制.煮制.炖制.煨制.燀制.制霜.发酵).医疗用毒性药品中药品种(制马 钱子.马钱子粉.巴豆霜.制白附子.黑顺片.白附片.制川乌.制草乌.制南星.醋甘遂.醋狼毒.千金子霜.法半夏.清半夏.姜半 滴眼剂(A线.B线.C线.激素类).滴耳剂(B线.C线.激素类).滴鼻剂(B线).喷雾剂含中药前处理及提取(B线.C线. 小容量注射剂(108车间) 盐酸伐昔洛韦(502车间.合成3线.精制3线) 无菌原料药(盐酸丙帕他莫.盐酸甲氯芬酯.炎琥宁.硫酸头孢匹罗.头孢哌酮钠.盐酸头孢吡肟) 中药饮片(净制.切制.蒸制.煮制.炒制.煅制.炙制.燁制.制炭.煨制.粉碎).毒性饮片(净制.切制.煮制.炙制) 片剂(D106车间) 片剂 胶囊剂.搽剂.片剂.颗粒剂(含中药前处理及提取) 中药饮片(净制.切制.炙制)
GMP的前世今生

2021/5/10
2010
卫生部部务会议审 议通过《药品生产 质量管理规范 ( 2010 年 修 订 ) 》 , 自 2011 年 3 月 1 日 起 施行。
2013
中国《药品生产质 量管理规范(2010年 修 订 )》 , 即 新 版 GMP正式施行
2021/5/10
9
GMP的成效
2006年至2012年,我国医药行业实现工业总产值的年复合增
长率达到24.01%,具体情况如下
20000
18000 16000 14000
15707
18255
12000 10000
8000 6000 4000
5019
6679
8666
10048
12523
2000
0 2006年
304343
273265
200000 150000 100000
196910
188122
182636
170266
147322
50000
0 2006年
2007年
2008年
2009年
2010年
全年共查处药品案件
2011年
2012年
2013年
2021/5/10
12
CONTENTS
03 Part Three GMP的困境
2014-01-18
2021/5/10
8
GMP的成效
通过监督管理GMP,我国的医药企业的面貌发生了根本转变,取得了良好的社会效 益。
保安全
进一步保障了人民群 众的用药安全。
搞升级
促进了制药企业的结 构调整和产业升级。
中国医药统计年报:中国2018年中成药主要品种产量统计(二百二十)

藿香正气胶囊 藿香正气胶囊 藿香正气软胶囊
中国2018年中成药主要品种产量统计(二百二十)
规格
生产单位
0.25g/粒
乐普恒久远药业有限公司
山西云中制药有限责任公司
0.43g/粒
摘编自《中国医药统计年报2018·中药生物制药分册》
四川森科制药有限公司
0.25g/粒
江西百神昌诺药业有限公司
0.37g/粒
江西百神昌诺药业有限公司
0.5g/粒
江西百神昌诺药业有限公司
0.32g/粒
吉林省俊宏药业有限公司
0.45g/粒
石药集团欧意药业有限公司
0.25g/粒
四川泰华堂制药有限公司
0.3g/粒
江西新远健药业有限公司
太极集团浙江东方制药有限公司
云南白药集团股份有限公司
山西康威制药有限责任公司
山西振东开元制药有限公司
贵州三力制药股份有限公司
圣大(张家口)药业有限公司
0.5g/粒
漳州片仔癀药业股份有限公司
0.45g/粒
云南云龙制药股份有限公司 山西黄河中药有限公司
神威药业集团有限公司 天津中新药业集团股份有限公司达仁堂制药厂
计量单位
万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒 万粒
产量 3436.563 1847.343 1589.22 2976.242 2976.242 73249.18 73249.18 12966.76 12966.76 43702.76 43702.76 51950.29 51950.29 822 822 1062.642 1062.642
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
认证日期 2018.09.24 2018.09.24 2018.09.25 2018.09.25 2018.09.25 2018.09.25 2018.09.25 2018.09.26 2018.09.26 2018.09.26 2018.09.26 2018.09.26 2018.09.27 2018.09.27 2018.09.28 2018.09.28 2018.09.28 2018.09.29 2018.09.29 2018.09.29 2018.09.29 2018.09.29
中国2018பைடு நூலகம்通过《药品生产质量管理规范(2010年修订)》认证企 摘编自《中国医药统计年报2018·综合册》
中国2018年通过《药品生产质量管理规范(2010年修订)》认证企业统计(五) 认证范围 原料药(奥卡西平) 片剂.硬胶囊剂(均为固体制剂一车间.二车间).颗粒剂(固体制剂一车间.二车间.三车间).滴眼剂.软胶囊剂(含中药 医用氧(气态) 片剂(含头孢菌素类) 硬胶囊剂.片剂.颗粒剂(均为固体制剂车间).合剂.糖浆剂(均为口服液一车间).丸剂(蜜丸.水蜜丸.水丸.浓缩丸) 小容量注射剂(含中药前处理及提取) 片剂.硬胶囊剂.丸剂(蜜丸)(含中药前处理及提取.生化前处理及提取) 片剂.胶囊剂 小容量注射剂(含激素类) 合剂 中药饮片(直接口服饮片) 片剂(含青霉素类).硬胶囊剂(含头孢菌素类.青霉素类) 片剂(化学药品) 冻干粉针剂(五车间.不含生物制品) 小容量注射剂(含非最终灭菌).中药提取 医用氧(液态) 片剂 片剂 小容量注射剂(含激素类.含非最终灭菌).原料药(长春西汀) 硬胶囊剂(头孢菌素类).片剂(头孢菌素类).干混悬剂(头孢菌素类) 原料药(盐酸吡格列酮.那格列奈) 原料药[樟脑(天然).桉油.愈创蓝油烃].软膏剂
有效期至 2023.09.23 2023.09.23 2023.09.24 2030.08.24 2023.09.24 2023.09.24 2023.09.24 2023.09.25 2023.09.25 2023.09.25 2023.09.25 2023.09.25 2023.09.26 2023.09.26 2023.09.27 2023.09.27 2023.09.27 2023.09.28 2023.09.28 2023.09.28 2023.09.28 2023.09.28
企业名称
吉林汇康制药有限公司 修正药业集团长春高新制药有限公司 随州市鸿伟化工有限公司 湖南百草制药有限公司 吉林一正药业集团有限公司 通化谷红制药有限公司 吉林省长源药业有限公司 浙江普洛康裕制药有限公司 浙江瑞新药业股份有限公司 浙江惠松制药有限公司 浙江惠松制药有限公司 浙江亚太药业股份有限公司 北京海德润医药集团有限公司 杭州澳亚生物技术有限公司 南京圣和药业股份有限公司 宝金新城江都气体有限公司 南京先声东元制药有限公司 珠海同益制药有限公司 河南润弘制药股份有限公司 礼来苏州制药有限公司 江苏德源药业股份有限公司 江苏嘉福制药有限公司
证书编号 JL20180052 JL20180050 HB20180441 HN20180323 JL20180053 JL20180054 JL20180055 ZJ20180118 ZJ20180119 ZJ20180120 ZJ20180121 ZJ20180123 BJ201800370 ZJ20180124 JS20180895 JS20180898 JS20180908 GD20180873 HA20180051 JS20180899 JS20180902 JS20180903
