化工原理:精馏作业
化工原理实验—精馏

化工原理实验—精馏1. 概述精馏是一种常用的分离技术,广泛应用于化工工艺中。
它通过将混合液加热至蒸发,然后在冷凝器中冷却并凝结回液体,从而实现混合物中组分的分离。
本实验旨在通过精馏实验,掌握精馏原理、操作步骤和相关设备的使用方法。
2. 实验原理2.1 精馏原理精馏是基于液体混合物中各组分的不同沸点而进行的分离过程。
在加热的作用下,沸点较低的组分会先蒸发,经过冷凝器冷却后变为液体回流,而沸点较高的组分则会滞留在容器中。
通过收集冷凝后的液体,我们可以分离出混合物中的不同组分。
2.2 实验设备在精馏实验中,主要使用以下设备:•加热设备:电热板、油浴等;•冷凝器:通常采用水冷型冷凝器,通过循环冷却水实现液体冷凝;•分馏柱:用于增加接触面积,提高分离效果;•采样装置:用于采集样品,检测组分浓度等。
2.3 操作步骤精馏实验的基本步骤如下:1.准备实验设备:包括加热设备、冷凝器、分馏柱等;2.准备混合液:按照实验要求,将需要分离的混合液制备好;3.装配设备:将冷凝器安装在分馏柱上方,连接好相应的管道和热源;4.开始加热:逐渐加热混合液,将其中的沸点较低组分蒸发出来;5.冷却和回流:通过冷凝器使蒸发的组分冷却并凝结成液体,回流到容器中;6.收集液体:将回流液体收集,并记录途中温度和时间等相关数据;7.结束实验:实验完成后,及时关闭加热设备和冷凝器,整理实验装置。
3. 实验操作及数据记录3.1 实验设备准备首先,确保实验室环境安全,检查仪器设备是否齐全,并找到精馏实验所需的各种设备:•电热板:用来提供加热源;•分馏柱:用来增加接触面积,提高分离效果;•冷凝器:通常为水冷型冷凝器,确保冷却效果良好。
3.2 实验样品准备按照实验要求,取出需要分离的混合液样品。
注意记录样品的成分和浓度等信息。
3.3 装配设备将冷凝器安装在分馏柱上方,并连接好相应的管道和热源。
确保连接紧密,无泄漏。
3.4 开始实验1.打开电热板,设置适当的加热温度;2.将混合液置于分馏烧瓶中,放入加热设备中;3.监测温度变化:通过温度计等工具,记录样品温度的变化。
化工原理_精馏

IV I F IV I F q IV I L rm
IV - IF相当于将1kmol的原料液由20 ℃变成92.5 ℃的饱和蒸气 所需要的热量。 IV – IF= (92.5-20)CPm +rm
CPm为混合液体的平均比热;rm为混合液体的平均潜热
rm =r1 x1 + r2 x2
y2
x2
操作关系
y3
……
xm x w
提馏段理论板数=m-1
再沸器
结论: 全塔理论板数NT=(n-1)+(m-1) (不含再沸器)
其中精馏段理论板数NT1=n-1 (或注明第n块为加料板)
关于理论板数的确定注意: ∵xn是加料板浓度,而加料板属于提馏段,∴精
馏段板数在采用全凝器时为 n-1
y y1 y2
f
2
1
•a
3
4 5 6
d • e
b
xD R 1
•
8
7
•c xW
x1(xn )
xF
x2
x 1 xD
x
5.进料热状况对q线及操作线的影响 (1) 冷液进料ef1 q>1
内 容 回 顾
一、精馏原理
(1)无中间加热及冷凝器的多次部分气化和多次部分冷凝 (2)顶部回流及底部气化是保证精馏过程稳定操作的必不 可缺少的条件。 (3)精馏操作流程 (4)相邻塔板温度及浓度的关系
tn1 tn tn1 xn1 xn xn1 yn1 yn yn1
ym1
W/F=1-0.3476=0.6524
1.1123 1 0.6524 xm 0.025 1.447 xm 0.0112 1.1123 1 0.6524 1.1123 1 0.6524
化工原理精馏实验

化工原理精馏实验化工原理精馏实验是化工工程中的一项重要实验内容,它主要用于分离和提纯混合物中的组分。
本文将介绍化工原理精馏实验的基本原理、实验步骤以及实验中需要注意的事项。
1. 实验目的化工原理精馏实验的主要目的是通过温度差异,利用液体蒸汽和凝结的原理,将混合物中的组分分离并得到纯净的产品。
通过这个实验,我们可以了解精馏作为一种分离技术的原理和应用。
2. 实验原理化工原理精馏实验的基本原理是利用混合物中各组分的不同沸点,通过升温使其中具有较低沸点的组分先蒸发,然后通过冷凝使其变为液体,从而实现分离。
在实验过程中,我们需要使用精馏塔,该塔内部设置有填料,用于增加混合物和蒸汽之间的交流面积,并实现更充分的分离。
3. 实验步骤(1) 准备实验所需设备和药品,包括精馏装置、混合物、填料等。
(2) 将混合物加入精馏瓶中,并将瓶塞密封。
(3) 将冷凝管和进料管连接到精馏瓶上,确保连接牢固。
(4) 将精馏瓶放入加热设备中,逐渐升温。
(5) 观察精馏瓶内的液体是否开始蒸发,当温度上升到某一点时,开始收集冷凝液。
(6) 根据实验需要,调整加热温度和收集冷凝液的时间,以实现所需组分的分离和提纯。
4. 实验注意事项(1) 在进行化工原理精馏实验前,需先对所需设备进行检查和清洁,确保实验过程的安全性。
(2) 在实验操作中,热量的传递速度会影响分馏过程的效果,因此需要掌握合适的加热速率。
(3) 为了避免精馏烧坏填料或其他设备,需要控制温度,确保温度在安全范围内。
(4) 实验结束后,应将设备进行清洗和消毒,防止残留物对下次实验的影响。
5. 实验结果分析通过化工原理精馏实验,可以得到分离出的纯净组分,并进行定量分析。
根据实验结果,可以进一步探讨精馏的分离效果、提纯效率等指标,并对所得纯净组分进行性质分析。
总结:化工原理精馏实验是一项重要的实验内容,通过实验可以了解精馏作为一种分离技术的原理和应用。
在实验过程中,需要注意设备的清洁和安全操作,合理控制加热温度和加热速率,以达到较好的分馏效果。
化工原理实验--精馏实验
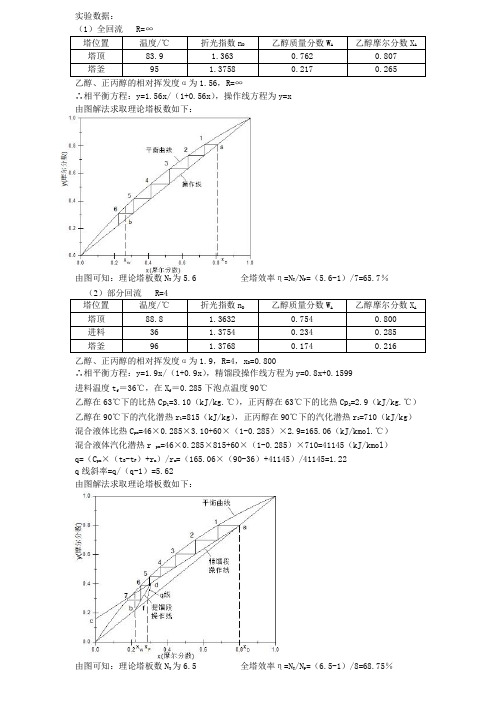
实验数据:
(1)全回流 R=∞
乙醇、正丙醇的相对挥发度α为1.56,R=∞
∴相平衡方程:y=1.56x/(1+0.56x),操作线方程为y=x
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为5.6 全塔效率η=N T/N P=(5.6-1)/7=65.7%
乙醇、正丙醇的相对挥发度α为1.9,R=4,x D=0.800
∴相平衡方程:y=1.9x/(1+0.9x),精馏段操作线方程为y=0.8x+0.1599
进料温度t f=36℃,在X f=0.285下泡点温度90℃
乙醇在63℃下的比热Cp1=3.10(kJ/kg.℃),正丙醇在63℃下的比热Cp2=2.9(kJ/kg.℃)乙醇在90℃下的汽化潜热r1=815(kJ/kg),正丙醇在90℃下的汽化潜热r2=710(kJ/kg)混合液体比热C pm=46×0.285×3.10+60×(1-0.285)×2.9=165.06(kJ/kmol.℃)
混合液体汽化潜热r pm=46×0.285×815+60×(1-0.285)×710=41145(kJ/kmol)
q=(C pm×(t B-t F)+r m)/r m=(165.06×(90-36)+41145)/41145=1.22
q线斜率=q/(q-1)=5.62
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为6.5 全塔效率η=N T/N P=(6.5-1)/8=68.75%。
化工原理精馏实验报告

化工原理精馏实验报告精馏技术在化学工程中已经得到了广泛的应用,但是如何完善其理论基础却是一个相当棘手的问题。
本文介绍了精馏实验,简要概述了精馏实验的基本原理及其应用,同时尝试深入了解精馏实验的基本操作,研究精馏实验的结果,并探讨分析其理论原理。
精馏是一种分离工艺,它的用途有两个方面。
首先,精馏是一种冷冻分离技术,可以通过利用液相与固相的分子量差异,将混合物分离出来。
其次,精馏也可以被用于提取物质,将物质从混合物中分离出来,以获得更高纯度的产品。
精馏实验的基本原理是利用溶剂的沸点级将混合液分为多个部分,然后采用吸附的方式将其中的不同组分分离出来。
精馏实验的操作步骤有:放置混合液;配置精馏塔;控制温度;给料;收集分离结果并绘制精馏曲线;分析结果。
首先,将混合液放入精馏塔中,然后控制精馏塔的温度,在进行温度控制的过程中,给料应该按预先设定的速率进行,以控制压力,这样便可以收集分离后的结果,绘制精馏曲线,根据精馏曲线的分析,可以分析出所得到的产品的有效性,并了解其分离效果。
另外,在精馏实验中,还可以采用许多其它的手段,以检验精馏实验的结果,如容量分析、比表面积测定、溶解度测定、m角测定等,从而对精馏实验的结果进行评价。
总之,精馏实验是为了让我们更好地理解和利用化学工程中的精馏技术,了解精馏实验的原理和操作,充分利用实验结果,并以此进行研究。
通过以上介绍,我们可以发现,精馏实验在化学工程中具有重要意义,可以用来分离混合液,提取物质,评价实验结果,从而为精馏技术的改进提供有力的理论支撑。
然而,在实际进行精馏实验时,需要用户掌握基本原理、进行合理操作,避免发生意外和错误,有效地利用精馏塔,从而使实验结果更好地反映出实验所需的理论结果。
综上所述,精馏技术已经在化学工程领域得到广泛应用,但是如何提高精馏技术的理论基础仍然是一个复杂的问题。
因此,精馏实验就显得十分重要,它不仅能够给我们提供更多的知识,而且可以实践中新的了解,以更加全面地把握精馏技术的理论原理,进而更好地服务于化学工程的发展。
化工原理:精馏习题答案

精馏练习题一、填空题【1】精馏操作的依据是(混合液中各组分的挥发度的差异)。
实现精馏操作的必要条件是(塔顶液相回流)和(塔底上升气流)。
【2】气液两相呈平衡状态时,气液两相温度(相同),液相组成(低于)气相组成。
【3】用相对挥发度α表达的气液平衡方程可写为( )。
根据α的大小,可用来(判断用蒸馏方法分离的难易程度),若α=1,则表示(不能用普通的蒸馏方法分离该混合液)。
【4】某两组分物系,相对挥发度3=α,在全回流条件下进行精馏操作,对第n 、n+1两层理论踏板(从塔顶往下计),若已知==+1,4.0n n y y 则()。
全回流适用于(精馏开工阶段)或(实验研究场合)。
【5】某精馏塔的精馏操作线方程为275.072.0+=x y ,则该塔的操作回流比为(),馏出液组成为()。
【6】在精馏塔设计中,若P Fx f 进料温度保持不变,若增加回流比R ,则p x (增大)w x (减小),V L (增大)。
【7】操作中的精馏塔,若进料温度FV x f 不变,若釜液量W 增加,则p x (增加),w x (增大)VL (增加)。
二、选择题(1)在用相对挥发度判别分离的难易程度时,下列哪种情况不能用普通蒸馏的方法分离(C )。
A.AB >1B. AB <1C. AB =1D. AB >10(2)在精馏的过程中,当进料为正处于泡点的饱和液体时,则(C )。
>1 <0 =1 <q <1(3)精馏塔中由塔顶向下的第n-1、n 、n+1层塔板,其气相组成的关系为(C )。
+1>y n >y n-1 B. y n+1=y n =-1 C +1<y n <y n-1 D.不确定(4)精馏塔中自上而下(C ).A.分为精馏段、加料板和提馏段三部分B.温度依次降低C.易挥发组分浓度依次降低D.蒸气量依次减少(5)某精馏塔的馏出液量是50kmo1/h ,回流比是2,则精馏段的回流液量是(A )。
h h h h(6)连续精馏中,精馏段操作线随( A )而变。
化工原理精馏作业

化工原理精馏作业精馏是一种在化工领域中常用的分离技术,通过不同组分在液相和气相之间的分配系数差异,将混合物中的各种组分进行有效分离的方法。
在精馏过程中,液体混合物首先被加热至沸点,然后通过蒸馏,将沸点低的组分蒸发出来,然后再冷凝成液体,从而实现各种组分的分离。
精馏操作常用于石油化工、化学制药、食品饮料等领域。
作为一名化工工程专业的学生,我经常接触到精馏操作,并且在实验室中也进行了一定数量的精馏操作。
在这次的作业中,我们需要对一个给定的混合物进行精馏操作,并确定各组分的塔顶和塔底流量、温度和组分浓度变化。
这将对我们的理论知识和实验操作能力提出很高的要求,下面我将详细描述这次精馏作业的过程。
首先,我们需要准备实验所需的设备和试剂。
在这次的精馏实验中,我们使用的是一座直管式精馏塔,内部填充了填料用于增加塔板数,提高分馏效率。
另外,我们还需要一个加热炉、冷凝器和采样瓶等设备,以及乙醇和水的混合物作为原料。
在实验操作之前,我们要对设备进行检查和清洁,确保设备处于良好的状态。
接下来,我们将开始进行实验操作。
首先,将混合物倒入精馏塔中,并通过加热炉将其加热至混合物的沸点。
随着加热的进行,混合物中沸点低的组分将首先蒸发出来,然后通过冷凝器冷凝成液体,从而得到塔顶产物。
而沸点高的组分则会继续停留在塔中,形成塔底产物。
在精馏过程中,我们会对塔顶和塔底的流量、温度和组分浓度进行连续监测和采样。
通过对这些参数的监测,我们可以得到混合物中不同组分的分离情况,确定精馏效果的好坏。
在实验过程中,我们需要不断调整加热功率和冷却水的流量,以确保精馏过程的顺利进行。
最后,在实验结束时,我们将收集和分析所有的数据,并绘制出流量、温度和组分浓度随时间变化的曲线图。
通过这些数据,我们可以对精馏塔的操作情况进行评估,找出操作中存在的问题并提出改进措施。
同时,我们还可以计算出各组分的分离效率和收率,对实验结果进行总结和分析。
通过这次精馏作业的实践,我对精馏操作有了更深入的了解,不仅使我对化工原理有了更深的认识,同时也提高了我的实验操作技能。
化工原理精馏实验报告

化工原理精馏实验报告
实验目的:掌握化工原理中的精馏操作,并通过实验验证理论知识的正确性。
实验原理:
精馏是一种分离液体混合物组成的常用方法。
精馏通过不同组成的液体在加热的条件下产生蒸汽,然后再在冷凝管中冷凝成液体,最后通过收集液体可以得到不同组成的馏分。
实验仪器:
1. 精馏塔:用于分离混合物。
2. 加热器:提供加热源。
3. 冷凝器:用于冷凝产生的蒸汽。
4. 温度计:用于测量温度。
实验步骤:
1. 将需要进行精馏的混合物加入精馏塔中。
2. 打开加热器,通过加热产生蒸汽。
3. 在冷凝器中冷凝产生的蒸汽,并收集液体。
4. 使用温度计测量液体的沸点。
5. 根据液体的沸点,确定得到的馏分的组成。
实验结果:
在实验过程中,我们成功地通过精馏操作将待分离的混合物分解为不同组成的馏分。
通过温度计测量得到的沸点数据,我们可以精确地确定馏分的组成。
实验结论:
通过这次实验,我们掌握了化工原理中的精馏操作,并验证了理论知识的正确性。
精馏是一种常用的分离液体混合物的方法,在工业生产中有着广泛的应用。
掌握了精馏操作,有助于我们理解和解决化工过程中的实际问题。
化工原理精馏实验报告

化工原理精馏实验报告实验目的:本实验旨在通过对乙醇和水的精馏实验,掌握精馏过程的基本原理和操作技术,了解精馏过程中的温度变化规律,并对实验结果进行分析和总结。
实验原理:精馏是利用液体混合物中各组分的沸点差异,通过加热混合物使其中某一组分先汽化,再凝结成液体,从而实现对混合物的分离的一种物理方法。
在精馏过程中,液体混合物首先被加热至其中某一组分的沸点,该组分首先汽化,然后通过冷凝器冷却凝结成液体,最终得到纯净的组分。
实验步骤:1. 将乙醇和水混合成一定比例的混合物,倒入精馏瓶中。
2. 装上加热设备和冷凝器,调节加热设备温度至混合物中乙醇的沸点。
3. 观察冷凝器出口的液体,收集不同温度下的液体样品。
4. 对收集的液体样品进行密度测定和酒精度测定。
实验结果:通过实验,我们得到了乙醇和水在不同温度下的液体样品。
经过密度测定和酒精度测定,我们得到了不同温度下乙醇和水的纯度和组成。
实验分析:根据实验结果,我们发现在不同温度下,乙醇和水的纯度和组成存在明显差异。
通过对实验数据的分析,我们可以得出精馏过程中乙醇和水的分离效果较好,且随着温度的升高,乙醇的纯度逐渐提高。
实验总结:本次实验通过对乙醇和水的精馏实验,使我们更加深入地了解了精馏过程的基本原理和操作技术。
同时,实验结果也验证了精馏过程中液体混合物的分离效果,并为我们今后在化工生产中的实际应用提供了重要参考。
结语:通过本次实验,我们不仅掌握了精馏过程的基本原理和操作技术,也对乙醇和水的混合物分离效果有了更深入的了解。
希望通过今后的实践操作和学习,能够更好地运用精馏技术解决实际生产中的问题,为化工生产贡献自己的一份力量。
精馏实验(化工原理实验)

精馏实验一、实验目的1、了解筛板式精馏塔及其附属设备的基本结构,掌握精馏操作的基本方法;2、掌握精馏过程全回流和部分回流的操作方法;3、掌握测定板式塔全塔效率。
二、实验原理1、全塔效率E T全塔效率又称总板效率,是指达到指定分离效果所需理论板数与实际板数的比值,即-1=T T P N E N (1)式中:T N -完成一定分离任务所需的理论塔板数,包括塔釜;P N -完成一定分离任务所需的实际塔板数。
全塔效率简单地反映了整个塔内塔板的平均效率,表明塔板结构、物性系数、操作状况等因素对塔板分离效果的影响。
对于双组分体系,塔内所需理论塔板数N T ,可通过实验测得塔顶组成x D 、塔釜组成x W 、进料组成x F 及进料热状况q 、回流比R等有关参数,利用相平衡关系和操作线用图解法或逐板计算法求得。
图1塔板气液流向示意图2、单板效率ME 单板效率又称莫弗里板效率,如图1所示,是指气相或液相经过一层实际塔板前后的组成变化值与经过一层理论塔板前后的组成变化值之比。
按气相组成变化表示的单板效率为1*1y =n n MV n n y E y y ++--(2)按液相组成变化表示的单板效率为1*1n n ML n n x x E x x ---=-(3)式中:y n 、1n y +-分别为离开第n 、n+1块塔板的气相组成,摩尔分数;1n x -、n x -分别为离开第n-1、n 块塔板的液相组成,摩尔分数;*ny -与x n 成平衡的气相组成,摩尔分数;*nx -与y n 成平衡的液相组成,摩尔分数。
3、图解法求理论塔板数N T图解法又称麦卡勃-蒂列(McCabe-Thiele)法,简称M-T 法,其原理与逐板计算法完全相同,只是将逐板计算过程在y-x 图上直观地表示出来。
对于恒摩尔流体系,精馏段的操作线方程为:111D n n x R y x R R +=+++(4)式中:1n y +-精馏段第n+1块塔板上升的蒸汽组成,摩尔分数;n x -精馏段第n 块塔板下流的液体组成,摩尔分数;D x -塔顶溜出液的液体组成,摩尔分数;R -回流比。
化工原理下实验精馏实验

密度 Kg/m3 971.4 969.2 967.0 964.6 962.2 959.7
四、实验操作
开机:启动四组加热丝,打开全凝器的冷却水进口阀,当 塔顶的温度快速上升时,及时关掉1、2组加热器,利用可 调加热丝将3,4组加热电流调节为12A(1#,2#板式塔) 或30A(3#,4#填料塔)
全回流:塔顶蒸汽温度达到70~80℃时,不进料也不出料 即F=0,D=0,逐渐开启回流阀,回流量的大小应注意控 制(1#、2#塔,L应小一些约为2~3l/h, 3#、4#塔回流量 可靠调节至7~8 L/h,在全回流下运行10分钟,期间当回 流流量有下降的趋势,则关小回流阀,全回流时间10分钟。
填料塔的等板高度:HETP
Z NT
等板高度(HETP)是指与一层理论塔板的传质作用相当的填料层
高度。它的大小取决于填料的类型、材质与尺寸,受系统物性、
操作条件及塔设备尺寸的影响。
Z-实际的填料层高度。
关键:如何求NT: 逐板计算法或梯级图解法
测出以下数据:
温度[℃]: tD、tf、tW 组成[mol/mol]:xD、xf、xW 流量: F、D、L
的全回流操作? (9)在本实验室的精馏实验过程,发生了液泛现象,试分析原因并提出解
决的方法。 (10)采用本实验室的流程分离乙醇和水的混合物,能否得到无水乙醇?为
什么?
精馏塔中塔板或填料是气液两相接触的场所由塔釜产生的上升蒸汽与从塔顶下降的下降液接触进行传热和传质下降液经过多次部分气化重组分含量逐渐增加上升蒸汽经多次部分冷凝轻组分含量逐渐增加从而使混合物达到一定程度的分离
精馏实验
二、实验原理简介
精馏塔中,塔板或填料是气液两相接触的场所,由塔釜产 生的上升蒸汽与从塔顶下降的下降液接触进行传热和传质, 下降液经过多次部分气化,重组分含量逐渐增加,上升蒸 汽经多次部分冷凝,轻组分含量逐渐增加,从而使混合物 达到一定程度的分离。
化工原理6.9 习题课答案(精馏)

(以上均为质量分率),原料为气液混合物,其中 蒸汽占1/3(摩尔比),苯-甲苯平均相对挥发为 2.5,设泡点回流,塔釜采用间接蒸汽加热,塔顶 采用全凝器,试求: (1)原料中气液相组成及塔顶易挥发组分的回收率;
3.998106 kJ / h 1110.6kW
(3) q 0
y xF 0.3
y 2.47x 1 1.47x
ye 0.3
xe 0.148
Rmin
xD ye ye xe
0.9 0.3 3.95 0.3 0.148
R Rmin 3.95
V' V 1 qF V F R 1D F 3.95 1 30 100 48.5koml / h
F, xF D, xD
W, xW
0.8
Dx D Fx F
xF xW xD xW
xD xF
0.2 0.3
xW xW
0.3 0.2
xW 0.0857
全塔为提馏段,且泡点加料 L F
L V
F D
1 D/F
xF
1
xW /xD
xF
1.876
W F D F 1 1.876 1 0.876 V DD
(2) q 1
Rmin
1
1
xD xF
1 xD
1 xF
1 2.47
1
0.9 0.3
2.471 0.9
1 0.3
1.80
R Rmin 1.80
V' V R 1D 1.80 1 30 84koml / h
Q' V 'r FC P ts t 84 32600 100161.5 98 20
化工原理 精馏练习题

化工原理精馏练习题一、问题描述在一个精馏塔中,对乙酸和甲醇进行分馏。
原料含有10%的乙酸和90%的甲醇。
要求设计一个塔,使得在出口处乙酸的含量为90%以上。
二、基本原理精馏是一种通过分离液体混合物中各种组分的技术。
通常使用精馏塔来实现这一过程。
精馏塔可以分为两个部分:初级分馏区和精馏区。
初级分馏区将液体混合物分为两个相,其中一个相富集乙酸,另一个相则富集甲醇。
精馏区进一步加热液体混合物,产生的蒸汽经过冷凝器后得到两个部分:富含乙酸的液体和富含甲醇的液体。
通过不断回流和再沸腾,可以实现将乙酸含量提高到所需的目标。
三、塔的设计1. 确定精馏塔的高度:- 初级分馏区的高度:根据乙酸和甲醇的相对挥发度,在塔底部设定一个管理区,用于分离液相。
在此区域温度和压力较低,适合乙酸富集。
根据经验法则,初级分馏区的高度应该是整个塔高度的1/3至1/2。
- 精馏区的高度:根据所需乙酸的含量和其他操作参数来确定此区域的高度。
通常,较高的塔设计可以提供更高的分离效果。
2. 确定进料位置:- 进料位置应该位于初级分馏区与精馏区之间的合适位置,以实现较好的分离效果。
通常情况下,进料点应该位于塔的上部,以允许较高的沸点组分从上部释放,从而改善塔的效率。
3. 选择合适的回流比:- 回流比是进入塔中再沸腾的液体与从塔顶冷凝回流的液体的质量比。
适当的回流比对提高分离效果非常重要。
较高的回流比可以提供更高的塔效率,但会增加能耗。
- 在本例中,根据乙酸和甲醇的性质和要求,选择合适的回流比是至关重要的。
四、其他操作参数除了塔的设计之外,还有一些其他操作参数需要考虑:1. 温度和压力:温度和压力的选择取决于乙酸和甲醇的性质。
通常情况下,高温和低压有利于乙酸的分离。
2. 冷凝器的设计:冷凝器用于冷却塔顶的蒸汽,并将其转变为液体。
这样,可以通过回流将纯度较高的乙酸送回塔底。
冷凝器的设计要应对不同的工艺要求和流量。
3. 分离回流液的处理:分离回流液中可能含有乙酸和甲醇。
化工原理:精馏作业
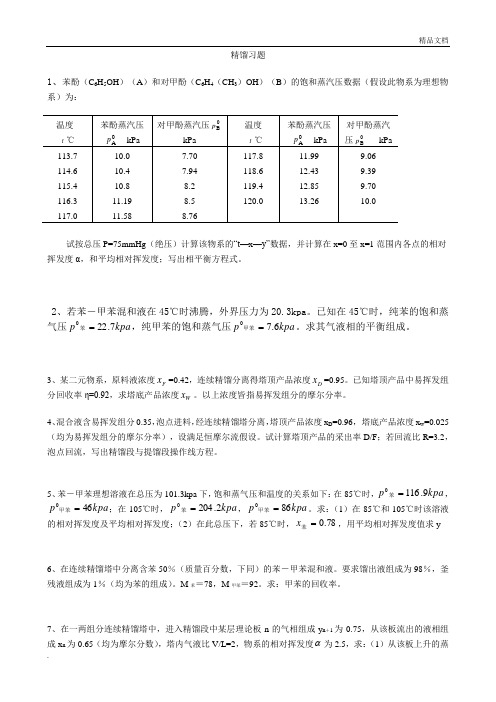
精馏习题1、苯酚(C 6H 5OH )(A )和对甲酚(C 6H 4(CH 3)OH )(B )的饱和蒸汽压数据(假设此物系为理想物系)为:试按总压P=75mmHg (绝压)计算该物系的“t—x —y”数据,并计算在x=0至x=1范围内各点的相对挥发度α,和平均相对挥发度;写出相平衡方程式。
2、若苯-甲苯混和液在45℃时沸腾,外界压力为20.3kpa 。
已知在45℃时,纯苯的饱和蒸气压kpa p 7.220=苯,纯甲苯的饱和蒸气压kpa p 6.70=甲苯。
求其气液相的平衡组成。
3、某二元物系,原料液浓度F x =0.42,连续精馏分离得塔顶产品浓度D x =0.95。
已知塔顶产品中易挥发组分回收率η=0.92,求塔底产品浓度W x 。
以上浓度皆指易挥发组分的摩尔分率。
4、混合液含易挥发组分0.35,泡点进料,经连续精馏塔分离,塔顶产品浓度x D =0.96, 塔底产品浓度x w =0.025(均为易挥发组分的摩尔分率),设满足恒摩尔流假设。
试计算塔顶产品的采出率D/F ;若回流比R=3.2,泡点回流,写出精馏段与提馏段操作线方程。
5、苯-甲苯理想溶液在总压为101.3kpa 下,饱和蒸气压和温度的关系如下:在85℃时,kpa p9.1160=苯,kpa p 460=甲苯;在105℃时,kpa p 2.2040=苯,kpa p 860=甲苯。
求:(1)在85℃和105℃时该溶液的相对挥发度及平均相对挥发度;(2)在此总压下,若85℃时,78.0=苯x ,用平均相对挥发度值求y6、在连续精馏塔中分离含苯50%(质量百分数,下同)的苯-甲苯混和液。
要求馏出液组成为98%,釜残液组成为1%(均为苯的组成)。
M 苯=78,M 甲苯=92。
求:甲苯的回收率。
7、在一两组分连续精馏塔中,进入精馏段中某层理论板n 的气相组成y n +1为0.75,从该板流出的液相组成x n 为0.65(均为摩尔分数),塔内气液比V/L=2,物系的相对挥发度α为2.5,求:(1)从该板上升的蒸气组成y n;(2)流入该板的液相组成x n-1;(3)回流比R。
化工原理课后作业(蒸馏)

5.蒸馏一、单选题1.蒸馏是分离()混合物的单元操作。
BA 气体;B 液体;C 固体;D 刚体。
2.蒸馏是利用各组分的()不同的特性实现分离的目的。
CA 溶解度;B 等规度;C 挥发度;D 调和度。
3.在二元混合液中,()的组分称为易挥发组分。
AA 沸点低;B 沸点高;C 沸点恒定;D 沸点变化。
4.在二元混合液中,沸点低的组分称为()组分。
CA 可挥发;B 不挥发;C 易挥发;D 难挥发。
5.在二元混合液中,()的组分称为难挥发组分。
BA 沸点低;B 沸点高;C 沸点恒定;D 沸点变化。
6.在二元混合液中,沸点高的组分称为()组分。
DA 可挥发;B 不挥发;C 易挥发;D 难挥发。
7.()是保证精馏过程连续稳定操作的必不可少的条件之一。
AA 液相回流;B 进料;C 侧线抽出;D 产品提纯。
8.液相回流是保证()过程连续稳定操作的必不可少的条件之一。
BA 吸收;B 精馏;C 传热;D 过滤。
9.在()中溶液部分气化而产生上升蒸气,是精馏得以连续稳定操作的一个必不可少条件。
C A 冷凝器;B 蒸发器;C 再沸器;D 换热器。
10.在再沸器中溶液()而产生上升蒸气,是精馏得以连续稳定操作的一个必不可少条件。
C A 部分冷凝;B 全部冷凝;C 部分气化;D 全部气化。
11.在再沸器中溶液部分气化而产生(),是精馏得以连续稳定操作的一个必不可少条件。
D A 上升物料;B 上升组分;C 上升产品;D 上升蒸气。
12.再沸器的作用是提供一定量的()流。
DA 上升物料;B 上升组分;C 上升产品;D 上升蒸气。
13.()的作用是提供一定量的上升蒸气流。
CA 冷凝器;B 蒸发器;C 再沸器;D 换热器。
14.()的作用是提供塔顶液相产品及保证有适宜的液相回流。
AA 冷凝器;B 蒸发器;C 再沸器;D 换热器。
15.冷凝器的作用是提供()产品及保证有适宜的液相回流。
BA 塔顶气相;B 塔顶液相;C 塔底气相;D 塔底液相。
化工原理精馏实验报告

化工原理精馏实验报告一、实验目的1.了解精馏的基本原理和操作方法。
2.掌握精馏列等常规化工装置的组装和拆卸方法。
3.学习操作精馏列进行混合物的分离。
二、实验原理精馏是利用液体混合物中组分挥发性的差异,通过升温使其分别汽化和冷凝,实现不同组分的分离。
根据原理和设备的不同,可分为常压精馏和减压精馏。
常压精馏通常采用碗状蒸馏器,其馏出液不一般含气体,供后续步骤使用。
减压精馏蒸馏器采用圆筒形设计,湿性气体排放恶劣等特点。
三、实验装置本次实验使用的精馏装置包括:碟状蒸馏器、冷凝器、接收瓶、加热器、温度传感器等。
四、实验步骤1.将碟状蒸馏器装置迅速、适当地安插在加热器上,并设置温度传感器。
2.将待测试物质加入碟状蒸馏器,并紧密封好。
3.连接冷凝器和接收瓶,确保冷凝器充分冷却。
4.使用加热器对碟状蒸馏器进行加热,并监测温度传感器。
5.在实验过程中,根据馏出液的收集情况及温度变化来调整加热器的加热功率。
6.测定不同温度下不同组分的收集量,并记录数据。
7.实验结束后,拆卸碟状蒸馏器,清洗实验装置,并做好相关记录。
五、实验结果与讨论在实验过程中,我们选择了乙醇和水的混合物进行精馏实验。
通过实验观察和数据记录,我们得到了以下结果:1.随着温度升高,乙醇的馏出量逐渐增加。
2.当温度达到78℃左右时,乙醇开始大量馏出,水的馏出量减少。
3.经过一段时间,馏出物逐渐转变为纯乙醇。
根据实验结果,我们可以得出结论:乙醇和水在常压下的沸点不同,通过精馏操作,可以将乙醇从水中分离出来,达到纯化乙醇的效果。
同时,在实验过程中,通过调节加热功率和控制温度变化,可以进一步提高乙醇的纯度。
六、实验总结本次实验通过对乙醇和水的精馏实验,掌握了精馏的基本原理和操作方法。
通过实验观察和数据记录,我们了解了温度与组分的关系,并得到了较为满意的分离效果。
同时,实验过程中我们也注意到了一些操作细节和注意事项,比如加热功率的调整和温度传感器的准确定位等。
化工原理实验—精馏

化工原理实验—精馏化工原理实验—精馏精馏是一种重要的分离技术,主要用于分离、纯化液体混合物中的各种成分。
在实际生产和科研实验中,精馏已经成为不可或缺的重要技术。
本文将就化工原理实验中的精馏实验进行详细介绍。
一、实验原理精馏的基本原理是根据不同成分在液态和气态之间的平衡关系,在加热条件下将混合物中单一成分蒸发和冷凝来实现分离、提纯目标成分。
实验中要分离的混合物首先被加热到沸腾点以上,因为各种成分的沸点不同,有些成分的沸点比另一些成分高得多,因此在离开混合物比较早的时候,一些液体成分便会压缩成气体形式,通过冷凝的方式回到液体形式,从而分离。
二、实验步骤1.实验前准备:确定实验目的,熟悉仪器使用方法和名词术语,检查实验物品是否准备充分。
2.实验流程:(1)调整设备:将水箱放在上部,并根据实验需要将装有混合物的烧瓶安装在下部。
(2)加热混合物:先在小火下加热,让混合物慢慢升温,确定加热速度以防止挥发速度过快。
随着温度的升高,由混合物挥发出来的单一成分便会通过塞子进入冷凝器,冷凝器中的水为其退回到液体形态,收集并量取所需要的物质。
3.实验结束:(1)关闭所有开关:实验完成后,将电源关闭,并将实验设备切断电源和气源。
(2)清洗设备与仪器:清洗所有已使用的材料和设备,以确保下次的实验能保证卫生和安全。
三、实验注意事项1.将水箱放置在塞子上方,仔细检查所有漏洞的位置和具有修复能力的地方,以避免机械故障与事故到来。
2.在进行实验时,必须小心谨慎地装填液体混合物,尤其是对于易燃物质,必须保持警惕,并根据实验条件和混合物来选择实验设备和材料。
3.在加热过程中,如果需要调整加热器的温度,必须慢慢调整,直到较稳定的加热水平达到。
总之,精馏实验是一项非常重要的化工原理实验,同学们在进行实验时一定要小心谨慎,严格遵守实验规范,才能保证实验的顺利进行。
化工原理实验报告-精馏

精馏实验一、实验任务和目的:1、充分利用计算机采集和控制系统具有的快速、大容量和实时处理的特点,进行精馏过程多实验方案的设计,并进行实验验证,得出实验结论。
以掌握实验研究的方法。
2、学会识别精馏塔内出现的几种操作状态,并分析这些操作状态对塔性能的影响。
3、学习精馏塔性能参数的测量方法,并掌握其影响因素。
4、测定精馏过程的动态特性,提高学生对精馏过程的认识。
二、实验原理:在板式精馏塔中,由塔釜产生的蒸汽沿塔板逐板上升与来自塔板下降的回流液,在塔板上实现多次接触,进行传热与传质,使混合液达到一定程度的分离。
回流是精馏操作得以实现的基础。
塔顶的回流量与采出量之比,称为回流比。
回流比是精馏操作的重要参数之一,其大小影响着精馏操作的分离效果和能耗。
回流比存在两种极限情况:最小回流比和全回流。
若塔在最小回流比下操作,要完成分离任务,则需要有无穷多块塔板的精馏塔。
当然,这不符合工业实际,所以最小回流比只是一个操作限度。
若操作处于全回流时,既无任何产品采出,也无原料加入,塔顶的冷凝液全部返回塔内中,这在生产中无实际意义。
但是,由于此时所需理论塔板数最少,又易于达到稳定,故常在工业装置的开停车、排除故障及科学研究时使用。
3、实验流程(简图);4、操作步骤;4.1、设置参数设置精馏段塔板数为5,设置提馏段塔板数为3,配置浓度比为0.66的乙醇/正丙醇混合液,设置进料罐的一次性进料量为2L。
4.2、精馏塔进料(1)连续点击"进料"按钮,进料罐开始进料,直到罐内液位达到70%以上。
(2)启动进料泵。
(3)设定进料泵功率,将进料流量控制器的 OP 值设为50%。
(4)设定预热器功率,将进料温度控制器的 OP 值设为60%,开始加热。
(5)打开塔釜液位控制器,控制液位在70%-80%之间。
4.3、启动再沸器(1)将塔顶冷凝器内通入冷却水。
(2)设定塔釜加热功率,将塔釜温度控制器的 OP 值设为 50%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精馏习题
1、苯酚(C 6H 5OH )(A )和对甲酚(C 6H 4(CH 3)OH )(B )的饱和蒸汽压数据(假设此物系为理想物
系)为:
试按总压P=75mmHg (绝压)计算该物系的“t—x —y”数据,并计算在x=0至x=1范围内各点的相对挥发度α,和平均相对挥发度;写出相平衡方程式。
2、若苯-甲苯混和液在45℃时沸腾,外界压力为20.3kpa 。
已知在45℃时,纯苯的饱和蒸
气压kpa p 7.220=苯,纯甲苯的饱和蒸气压kpa p 6.70=甲苯。
求其气液相的平衡组成。
3、某二元物系,原料液浓度F x =0.42,连续精馏分离得塔顶产品浓度D x =0.95。
已知塔顶产品中易挥发组分回收率η=0.92,求塔底产品浓度W x 。
以上浓度皆指易挥发组分的摩尔分率。
4、混合液含易挥发组分0.35,泡点进料,经连续精馏塔分离,塔顶产品浓度x D =0.96, 塔底产品浓度x w =0.025(均为易挥发组分的摩尔分率),设满足恒摩尔流假设。
试计算塔顶产品的采出率D/F ;若回流比R=3.2,泡点回流,写出精馏段与提馏段操作线方程。
5、苯-甲苯理想溶液在总压为101.3kpa 下,饱和蒸气压和温度的关系如下:在85℃时,kpa p 9.1160=苯,kpa p 460=甲苯;在105℃时,kpa p 2.2040=苯,kpa p 860=甲苯。
求:
(1)在85℃和105℃时该溶液的相对挥发度及平均相对挥发度;(2)在此总压下,若85℃时,78.0=苯x ,用平均相对挥发度值求y
6、在连续精馏塔中分离含苯50%(质量百分数,下同)的苯-甲苯混和液。
要求馏出液组成为98%,釜残液组成为1%(均为苯的组成)。
M 苯=78,M 甲苯=92。
求:甲苯的回收率。
7、在一两组分连续精馏塔中,进入精馏段中某层理论板n 的气相组成y n +1为0.75,从该板流出的液相组成x n 为0.65(均为摩尔分数),塔内气液比V/L=2,物系的相对挥发度α为2.5,求:(1)从该板上升的蒸气组成y n ;(2)流入该板的液相组成x n -1;(3)回流比R 。
