《含氮化合物》PPT课件
合集下载
第十七部分有机含氮化合物教学课件

NN HH
氢化偶氮苯
在化工生产中,常用 Cu 、Ni或Pt 等催化剂,
采用催化加氢的方法,还原硝基化合物。实验室
中也可采用类似的方法。
NO2
NH2
H2,Cu ,约 300 ℃
约95%
NHCOCH 3 NO 2
H 2,Pt 醇
NHCOCH 3 NH 2
2.芳环上的亲电取代反应
Br 2 Fe,140 ℃
NO2
NO 2
2.芳香族硝基化合物的物理性质
O2N
CH3 NO 2
OCH 3 C(CH 3)3
葵子麝香
O2N
CH 3 COCH 3 O2N
CH3 NO 2
(CH 3)3C
CH3 NO 2
酮麝香
(CH 3)3C
CH 3
NO 2
二甲苯麝香
3.芳香族硝基化合物的化学性质
(1). 还原 NO2
NO
NHOH
基来命名。
NH2
CH3
CH2CH2CHCH3 CH3NHCH(CH 2)4CH3
1-苯基-3-氨基丁烷 2-甲氨基丁烷 CH3CH2CH2CHNCHC3CH2H35 2-甲乙氨基戊烷
3. 当氮原子同时连有芳基和脂肪基时,命名时必 须在芳胺 名称前面加字母“ N”。
CH3 N C2H5
N-甲基-N乙基苯胺
ON
N(CH3)2
对亚硝基 -N,N二甲苯胺
NH
Hale Waihona Puke NHN,N' -二苯基 对苯二胺
O2N
NH
NO2
4,4' -二硝基二苯胺
4. 四个相同或不同的烃基与氮原子相连的化合物称 为季胺 化合物,其中 R4N+X-称为季胺盐 , R4N+OH-称为 季胺碱 。 命名胺与酸生成的盐或季胺类化合物时,用“铵” 代替“胺”,并在前面加负离子的名称。
《有机含氮化合物》课件

将硝基化合物或腈类化合物还原为 胺类。
重氮化反应
通过重氮盐与氢、醇、酚等反应, 生成相应的胺类化合物。
04
硝基化合物的合成
硝酸盐的还原
将硝酸盐通过加氢还原或电解 还原等方法得到硝基化合物。
重氮化反应
通过重氮盐与酸反应,生成相 应的硝基化合物。
氧化偶联
利用氧化剂将芳香烃或烯烃氧 化偶联成硝基化合物。
有机含氮化合物中的硝基 化合物可用作燃料添加剂 ,提高燃料的燃烧效率。
塑料和橡胶添加剂
一些有机含氮化合物可用 作塑料和橡胶的添加剂, 改善其性能。
表面活性剂
有机含氮化合物中的季铵 盐类化合物可用作表面活 性剂,如十二烷基三甲基 氯化铵等。
05
有机含氮化合物的前景 展望
新合成方法的研究
总结词
新合成方法的研究将为有机含氮化合物的制备提供更多可能性,有助于发现更高效、环保的合成路径 。
硝化反应
在浓硫酸和硝酸的混合酸中, 将有机物进行硝化反应得到硝
基化合物。
腈类化合物的合成
醛或酮的氰化
在酸性条件下,醛或酮与氰化钠或氰化钾反 应生成腈类化合物。
烯烃的氢甲酰化
在催化剂存在下,烯烃与氢氰酸反应生成相 应的腈类化合物。
重氮化反应
通过重氮盐与氰化钠或氰化钾反应,生成相 应的腈类化合物。
酯的氰解
03
颜色
有机含氮化合物的颜色多样,取决于其特定的结构。例如,含有共轭双
键的化合物可能呈现黄色或棕色,而含有苯环的化合物则可能呈现不同
的颜色。
化学性质
酸碱性
稳定性
有机含氮化合物可以表现出酸性和碱 性性质。例如,胺类化合物是碱性的 ,而许多硝基化合物和腈则是酸性的 。
重氮化反应
通过重氮盐与氢、醇、酚等反应, 生成相应的胺类化合物。
04
硝基化合物的合成
硝酸盐的还原
将硝酸盐通过加氢还原或电解 还原等方法得到硝基化合物。
重氮化反应
通过重氮盐与酸反应,生成相 应的硝基化合物。
氧化偶联
利用氧化剂将芳香烃或烯烃氧 化偶联成硝基化合物。
有机含氮化合物中的硝基 化合物可用作燃料添加剂 ,提高燃料的燃烧效率。
塑料和橡胶添加剂
一些有机含氮化合物可用 作塑料和橡胶的添加剂, 改善其性能。
表面活性剂
有机含氮化合物中的季铵 盐类化合物可用作表面活 性剂,如十二烷基三甲基 氯化铵等。
05
有机含氮化合物的前景 展望
新合成方法的研究
总结词
新合成方法的研究将为有机含氮化合物的制备提供更多可能性,有助于发现更高效、环保的合成路径 。
硝化反应
在浓硫酸和硝酸的混合酸中, 将有机物进行硝化反应得到硝
基化合物。
腈类化合物的合成
醛或酮的氰化
在酸性条件下,醛或酮与氰化钠或氰化钾反 应生成腈类化合物。
烯烃的氢甲酰化
在催化剂存在下,烯烃与氢氰酸反应生成相 应的腈类化合物。
重氮化反应
通过重氮盐与氰化钠或氰化钾反应,生成相 应的腈类化合物。
酯的氰解
03
颜色
有机含氮化合物的颜色多样,取决于其特定的结构。例如,含有共轭双
键的化合物可能呈现黄色或棕色,而含有苯环的化合物则可能呈现不同
的颜色。
化学性质
酸碱性
稳定性
有机含氮化合物可以表现出酸性和碱 性性质。例如,胺类化合物是碱性的 ,而许多硝基化合物和腈则是酸性的 。
第十二章含氮化合物ppt课件
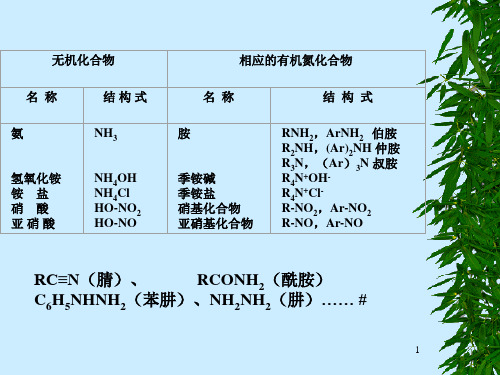
N H
CH 3
+
HNO2
CH 3
叔胺
N CH 3
+
HNO2
NO
N
CH
3
N-亚硝基甲苯胺 (棕色油状)
NMe 2
对亚硝基-N,N-二甲基苯胺 (绿色叶片状)
NO
小结: ① ② ③ ④ ⑤
0℃时,有N2↑为脂肪伯胺。 有黄色油状物或固体,则为脂肪和芳香仲胺。 无可见的反应现象为脂肪叔胺。 0℃时无N2↑,而室温有N2↑,则为芳香伯胺。 有绿色叶片状固体为芳香叔胺。 #
NH 2
Br2 Br Br + HBr
Br 白色↓
Br
Br
HNO3 Fe+HCl
H2SO4△
Br2 NaNO2H2SO4
0~5℃
H3PO2+H2O
TM
17
偶氮化合物中都含有—N=N—官能团。 偶氮化合物通式:R—N=N—R 、
Ar—N=N—R 或 Ar—N=N—
一A、r 芳香族重N盐的制备
NH2 + NaNO2+ 2HCl 0~5℃
NO 2
2-硝基丙烷
NO 2
NO 2
间二硝基苯
H3C
NO 2
对硝基甲苯
2
二、 性质
⒈ 物性
⑴ 硝基是一个强极性基,硝基化合物的偶极矩较大。 ⑵ 沸点比相应的卤代烃高。 ⑶ 多硝基化合物具有爆炸性。 ⑷ 液体硝基化合物是良好的有机溶剂。 ⑸ 有毒。 ⑹ 比重大于1。
⒉化性
⑴ 脂肪族硝基化合物
a. 互变异构和酸性
RC≡N(腈)、
RCONH2(酰胺)
C6H5NHNH2(苯肼)、NH2NH2(肼)…… #
含氮化合物ppt课件

NHCH3 CH3 CH CH3 CH CH2 CH CH3
2-甲基-4-氨基戊烷
18
也可将胺作为母体,用阿拉伯数标明氨基的位次。
CH3 CH CH CH2CH3 CH3 NH2
2-甲基-3-戊胺
CH3 CH CH2CH2CH3 NHCH3
N-甲基-2-戊胺
CH3(CH2)3OH CH3(CH2)3NH2 CH3(CH2)3CH3
分子量
74
73
72
沸点(oC)
117.7
77.8
36.1
25
1o 、2o、 3o 胺,由于H的数目不同,分子间形成氢 键能力不同,b.p.随之改变。叔胺中N原子上无活泼氢, 不能形成分子间氢键,所以其沸点最低。
CH3CH2CH2NH2 CH3CH2NHCH3 (CH3)3N
2. 据取代的烃基类型的不同,可分为:
脂肪胺
芳香胺
RCH2NH2 ArNH2
3. 根据氨基的数目还可分为:一元胺、二元胺、多元胺
14
注意:伯、仲、叔胺是按NH3中H被取代的数目来分类。而 伯、仲、叔醇以及不同级数的卤代烷是按与-OH或X
相连的碳的级数来分类的。
CH3 H3C C NH2
CH3
叔丁基胺:1o 胺
(CH3)3N+Cl- + NaOH
(CH3)3N + NaOH + NaCl
NH3+HSO4- + 2NaOH
NH2 + Na2SO4 + 2H2O
利用此性质,可从混合物中分离出并提纯胺。 也可用于胺的定性鉴别。
29
CH2NH2
OH
HCl
CH3 CH2OH
第十四部分含氮有机化合物教学课件

三、化学性质 1、还原 硝基可以被还原,特别是芳香硝基化合物的 还原有很大的实用意义。芳香硝基化合物在 不同介质中使用不同还原剂可以得到一系列 不同的还原产物。用强还原剂还原的最终产 物是伯胺,例如,在酸性介质中以铁粉还原 硝基苯则生成苯胺,这是工业上制备苯胺的 方法。
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
H
HO H -
C H 3 C H 2 C HC HC H 2
+ N (C H 3 )3
C H 3 C H 2 C H 2 C H = C H 2+(C H 3 )3 N +H 2 O
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
⑶对于芳香仲胺或叔胺,则在基前冠以“N” 字,以表示这个基团是连在氮上,而不是 连在芳香环上。
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
血红蛋白变性而引起中毒,较多地吸入它们的 蒸气或粉尘,或者长期与皮肤接触都能引起中 毒。人造香料
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
2、脂肪族硝基化合物的酸性 由于硝基的吸电子诱导效应,脂肪硝基化合
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
H
HO H -
C H 3 C H 2 C HC HC H 2
+ N (C H 3 )3
C H 3 C H 2 C H 2 C H = C H 2+(C H 3 )3 N +H 2 O
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
⑶对于芳香仲胺或叔胺,则在基前冠以“N” 字,以表示这个基团是连在氮上,而不是 连在芳香环上。
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
血红蛋白变性而引起中毒,较多地吸入它们的 蒸气或粉尘,或者长期与皮肤接触都能引起中 毒。人造香料
第九章 第十章 第十一章 第十二章 第十三章 第十四章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
第一章 第二章 第三章 第四章 第五章 第六章 第七章 第八章
2、脂肪族硝基化合物的酸性 由于硝基的吸电子诱导效应,脂肪硝基化合
含氮化合物ppt课件
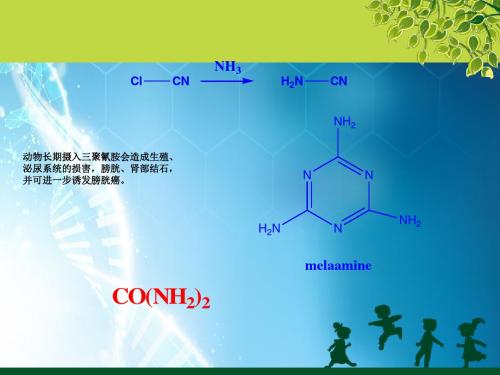
多巴胺是一种用来帮助细胞传送脉冲的化学物质,为神经递质的一种。这种递质主要负责大脑的情欲, 感觉,将兴奋及开心的信息传递,也与上瘾有关。爱情的感觉其实就是脑里产生大量多巴胺作用的结 果。所以,吸烟和吸毒都可以增加多巴胺的分泌,使上瘾者感到开心及兴奋。根据研究所得,多巴胺 能够治疗抑郁症;而多巴胺不足或失调则会令人失去控制肌肉的能力、或是导致注意力无法集中;前 者在严重时会导致手脚不自主地颤动、乃至罹患帕金森病,后者严重时会导致注意力不足过动症。 最近,有科学家研究出多巴胺可以有助进一步医治上述两种病症,主要治疗方法在于恢复脑内多巴胺 的水平。
O
H3C N O
H2C N O
O H2C N
O
生成的碳负离子可与羰基化物缩合。
CO H
CH3NO2 NaOH
CC HH
NO2
3 硝基对芳环的邻对位基团的影响
(1) 对邻对位卤素的影响
Cl
OH
O2N
NO2
Na2CO3 O2N
NO2
NO2 (2)对酚的酸性的影响
H2O
O2N
OH
NO2
OH
NO2
NO2
CH3
NH2 Br
CH3
磺化
NH2
H2SO4
硝化
NH3HSO4
H2O 180~1900C
NH2
重排
NH3
SO3H
SO3
(内盐)
N(CH3)2
HNO3 H2SO4
NH(CH3)2 NO2
NH(CH3)2
N(CH3)2
NaOH
NO2
NO2
(主产物)
N(CH3)2 NO2
多巴胺(Dopamine)
O
H3C N O
H2C N O
O H2C N
O
生成的碳负离子可与羰基化物缩合。
CO H
CH3NO2 NaOH
CC HH
NO2
3 硝基对芳环的邻对位基团的影响
(1) 对邻对位卤素的影响
Cl
OH
O2N
NO2
Na2CO3 O2N
NO2
NO2 (2)对酚的酸性的影响
H2O
O2N
OH
NO2
OH
NO2
NO2
CH3
NH2 Br
CH3
磺化
NH2
H2SO4
硝化
NH3HSO4
H2O 180~1900C
NH2
重排
NH3
SO3H
SO3
(内盐)
N(CH3)2
HNO3 H2SO4
NH(CH3)2 NO2
NH(CH3)2
N(CH3)2
NaOH
NO2
NO2
(主产物)
N(CH3)2 NO2
多巴胺(Dopamine)
《含氮、磷硫化合物》课件

03
影响因素
温度、压力、催化剂等对含氮化 合物的合成与反应机理有重要影
响。
02
反应机理
含氮化合物的合成涉及复杂的化 学反应机理,如亲核取代和亲电
加成。
04
应用前景
随着科技的发展,含氮化合物的 合成与反应机理在化工、制药等
领域的应用前景广阔。
PART 03
含磷化合物
磷的氧化物
磷的氧化物概述
介绍磷的氧化物的性质、分类和制备方法。
。硫是一种非金属元素,其化学性质不活泼,但在加热条件下可以与氧
反应生成二氧化硫。
氮、磷、硫元素在自然界中的存在形式
氮
在自然界中,氮主要以氮气的形 式存在,占大气组成的约78%。 此外,氮还存在于多种含氮化合 物中,如蛋白质、氨基酸、核酸
等。
磷
磷在地壳中的丰度较低,主要以 磷酸盐的形式存在,如磷酸钙、 磷酸钠等。此外,磷还存在于生 物体内,是构成生物体的必需元
含硫有机化合物
含硫有机化合物的概述
含硫有机化合物是指含有碳和硫两种元素的有机化合物,如磺酸 、硫醇等。
磺酸的物理和化学性质
磺酸是一类具有通式R-SO3H的有机化合物,具有强酸性,是工业 上广泛应用的重要化工原料。
硫醇的物理和化学性质
硫醇是一类具有通式R-SH的有机化合物,具有特殊的气味和毒性 ,是工业上制取各种含硫化合物的重要原料。
硫的氢化物
硫氢化物的概述
01
硫的氢化物是一类含硫和氢元素的化合物,如氢硫酸(H2S)
和硫化氢(H2S)。
氢硫酸的物理和化学性质
02
氢硫酸是一种无色、有刺激性气味的气体,有毒,易溶于水,
是工业上制取硫化物的重要原料。
含氮有机化合物ppt课件

CH3CH2CH2NH2 CH 3CH 2NHCH 2CH 3 CH3CH2-N-CH 2CH2CH3 CH 3
丙胺
二乙胺
甲乙丙胺
2.对于氮原子上连接有脂肪烃基的芳香仲胺和叔胺,常 在脂肪烃基之前冠以“N-”或“N,N-”字:
NH CH3
CH 3 N CH3
N-甲基苯胺
N,N-二甲基苯胺
3.对于比较复杂的胺,常以烃为母体,把氨基作为取代 基来命名。例如:
O
O
N+OH-
OCH3
OCH3
学 习 结 束 !
(一)尿素
尿素简称脲,白色结晶,熔点为133℃,易溶于水和乙醇。
O H2N C NH2
1.弱碱性
尿素分子中含有两个氨基,呈弱碱性,可与强酸生成盐。
硝酸脲
2.水解反应
脲在酸或碱的催化下,加热时发生水解;在脲酶作用下, 水解反应在常温下就能进行。
CO(NH2)2 + H2O 脲酶 CO2 + 2NH3
O
CH3
H3C C O CH2 CH2 N+ CH3 OH-
CH3
(四) 肾上腺素和去甲肾上腺素
肾上腺素和去甲肾上腺素是肾上腺髓质分泌的激素。人工 合成的肾上腺素为白色结晶性粉末,无臭,味苦,极微溶于 水。肾上腺素分子中有酚羟基和甲氨基,具酸碱两性;具有 邻苯二酚结构,遇光和空气易氧化变质。
HO HO
CO(NH2)2 + 2NaOH Na2CO3 + 2NH3
CO(NH2)2 + H2O + 2HCl CO2 + 2NH4Cl
3.与亚硝酸反应
脲能与亚硝酸反应,生成氮气、二氧化碳和水
CO(NH2)2 + 2HNO2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NHCH3 Cl
复杂胺(主要是脂肪胺)按系统命名法命名,烃为母体,氨基为取代基:
CH3CHCH2CHCH3 NH2 CH3
CH3CH2CHCH2CH2NHCH3 CH3
CH3CH2CH2CHCH2CH3 N(CH3)2
2-甲基-4-氨基戊烷 3-甲基-1-甲氨基戊烷 3-(二甲氨基)己烷 季铵化合物可以看作是铵的衍生物命名.例如:
NO2
OH NO2
NO2
硝基影响酚的酸性
由于硝基使苯环邻对位的电子云密度大大降低,增加了苯环上羟基中的氢离解成质子 的能力,其酸性大大增强.例如:
OH
OH
OH
OH
NO2
OH NO2NO2
OH NO2
NO2
pKa 9.98
7.15 7.23
8.40
NO2 NO2
4.0
0.38
NO2
§15.2 胺
§15.2.1 胺的分类和命名
O NO2
Na2S/H2O 95-100oC
NO2 O
NaSH- CH3OH 加热
NO2
NO2 NH2
O NH2 O
二、苯环上的亲电取代反应
间位定位基,使苯环钝化,溴代,加热至140 C;硝化用发烟硝酸和浓硫酸,并加热至 110C;磺化用发烟硫酸,并加热至110 C,硝基苯,不发生付-克反应。
NO2
(C2H5)4N+Br-
(CH3)3N+(n-C16H33)OH-
溴化四乙铵
三甲基十六烷基氢氧化铵
§15.2.2 胺的结构
胺的结构与氨类似,氨分子具角锥形结构,氮的sp3杂化轨道与三个氢原子的s轨道 重叠成键,氮上仍有一对未共享电子占据sp3杂化轨道,脂肪胺的结构与氨完全相 似,如甲胺和三甲胺.芳香胺如苯胺中的氮仍取sp3杂化,但p轨道的成分要大一些, 其H-N-H的键角更大,为113.9,氨中只有107.3
例如,氯苯与KOH煮沸数日无反应,但有硝基存在时,反应容易进行:
Cl
ONa
OH
NO2 NaOH
NO2 H+
130 oC, 0.2MPa
NO2
Cl NO2 NaOH
100 oC
ONa NO2 H+
OH NO2
NO2
NO2
NO2
NO2
Cl
NO2
NO2
Na2CO3
60 oC
NO2
2、对酚类酸性的影响
ONa NO2 H+ NO2
三、还可分为脂肪族胺与芳香族胺。
简单烃基组成的胺,把胺作母体,烃基作取代基, 常省略“基”字,取代基相同则用汉字数字表示其数目。 N上同时连苯环和脂肪烃基,苯胺为母体,以N表示烃基位置。如:
CH3NH2
CH3 NH
CH3
CH3 NCH3
CH3
N(CH3)2
甲胺 二甲胺
三甲胺 N,N-二甲基苯胺 3-氯-N-甲基苯胺
:
N
H
H H
:
N
CH3
H H
: N CH3 CH3CH3
:
NH H
氨气的结构
甲胺的结构
三甲胺的结构
苯胺的结构
在季胺盐中,氮的四个sp3杂化轨道全部用来成键,是四面体,氮原子上连有四个不同的基 团的季胺盐存在着对映体.例如,碘化甲基烯丙基苯基苄基铵,事实上能分离出右旋体和左 旋体.
CH3
HNO3,H2SO4 30 o C
CH3
CH3
NO2
+
NO2
❖结构
硝基化合物有较高的偶极矩(CH3NO2 = 4.3D),键长测定指出:两个O原子和N原子之 间的距离相等,比N=O长,比N-O短. N原子及两个O原子均是SP2杂化,杂化轨道形成三个共平面的键,N原子及两个O原 子的P轨道垂直于这个平面形成共轭键(三中心四电子键),其结构如下:
NO2
Br2,Fe 140 o C
发烟HNO3 H2SO4 110 o C
发烟H2SO4 110 o C
NO2 Br NO2
SO3H
NO2
三、苯环上的亲核取代反应
O2N
NO2
1.5 %NaOH,
100oC
季铵盐
O2N
ONa
OMe NO2
+ PhNH2
NO2
180oC
NHPh NO2
NO2
四、硝基对苯环上其它基团的影响 1、对卤原子活泼性的影响:使苯环上的亲核取代反应更容易
O2N
COOC2H5
COOC2H5
Zn/C2H5OH reflux
COOC2H5
NO2
NH2
③、金属加碱性介质 在碱性条件下, 硝基化合物被还原为偶氮化合物,例如:
NO2 Zn,NaOH/H2O
NN
NH NH
+
H
OH
50-90 oC
H2N
NH2
3、 Na2S、NaSH、(NH4)2S、Na2S2可用作还原剂,此法适用于高沸点、不溶于水的芳胺 的制备
一、按氮原子上氢原子的个数:
伯胺、仲胺、叔胺
胺是氨中的氢原子被烃基取代后的产物.氨的一个氢原子被烃基取代得伯胺,二个 氢原子被烃基取代得仲胺,三个氢原子被烃基取代得叔胺。如:
RNH2 伯胺; RR’NH 仲胺 RR’R”N 叔胺, R4N+X- 季铵盐; R4N+OH- 季铵碱 二、按分子中氨基的个数划分:一元胺,二元胺,三元胺.
.
.. O
RN
.
O
§15.1.2 芳香族硝基化合物的物理性质 ➢芳香硝基化合物多为淡黄色固体.沸点比相应的卤代烃高, 常温下为高沸点的液体或结 晶固体. ➢不溶于水,易溶于有机溶剂,多硝基化合物有爆炸性,例如:2,4,6-三硝基甲苯(TNT)为烈性 炸药. ➢ 密度大于1,多硝基化合物有香味,可作香料:二甲苯麝香;酮麝香。
§15.1.3 芳香族硝基化合物的波谱性质 N-O键的伸缩振动:1540,1350cm-1
§15.1.4 芳香族硝基化合物的化学性质 一、 还原反应 在酸性还原体系中(如Fe, Zn, Sn和盐酸)中,硝基化合物被还原 为伯胺: 催化氢化(如Ni催化加氢)也可生成伯胺
1、催化加氢,在中性条件下进行
第十五章 含氮有机化合物
§15.1 芳香族硝基化合物 §15.1.1 芳香族硝基化合物的命名、制法和结构
CH3
CH3
NO2
NO2
NO2
NO2
Cl NO2
NO2
NO2
NO2 NO2
对硝基甲苯 2,4,6-三硝基甲苯 间二硝基苯 2,4,6-三硝基氯苯
❖用硝酸和浓硫酸进行硝化,是制取芳香族硝基化合物的最简便的方法.例如:
NHCOCH3 NO2 H2, Pt C2H5OH
NHCOCH3 NH2
2、金属与给质子剂作还原剂 ①、金属加酸性介质 在酸性还原体系中(如Fe, Zn, Sn和盐酸)中,被还原为伯胺
NO2
Fe 或 Zn + HCl 乙 醇;
CHO
SnCl2 +HCl NO2
NH2
CHO NH2
②、金属加水醇等中性介质 在中性或弱酸性条件下, 硝基化合物被还原为羟胺或伯胺,例:
