决明子 检验报告模板
不同商品规格决明子的质量分析

不同商品规格决明子的质量分析杨国静;张珞琪;陈随清;王利丽【摘要】目的:对不同商品规格决明子进行质量分析,为该药的合理应用提供依据.方法:运用薄层色谱法进行定性鉴别,采用HPLC测定其中橙黄决明素、大黄酚、红镰霉素龙胆二糖苷以及决明子苷的含量.结果:决明中的4个成分均最高,其次是小决明、决明(进口),小决明(进口)含量最低,并且大部分决明(进口)、小决明(进口)含量低于药典含量标准.结论:在不同规格决明子中,决明子质量优于决明子(进口)质量,这为市场规范以及综合质量评价提供依据.【期刊名称】《中国现代中药》【年(卷),期】2018(020)008【总页数】6页(P963-967,978)【关键词】决明子;规格;橙黄决明素;大黄酚;红镰霉素龙胆二糖苷;决明子苷【作者】杨国静;张珞琪;陈随清;王利丽【作者单位】河南中医药大学药学院,河南郑州 450046;河南中医药大学药学院,河南郑州 450046;河南中医药大学药学院,河南郑州 450046;河南中医药大学药学院,河南郑州 450046【正文语种】中文决明子为豆科植物决明Cassia obtusifolia L.或小决明Cassia tora L.的干燥成熟种子。
具有清肝明目、润肠通便的作用[1]。
研究表明决明子中的含有蒽醌类、萘并吡喃酮苷类脂肪酸类以及无机元素等,主要有效成分为蒽醌类[2-3],且有研究表明萘并吡喃酮苷类的含量也不低。
现代药理研究表明决明子具有降脂、降压、抗诱变以及保肝的作用[4-5]。
近年来对决明子的质量研究日益增多,如纪亚明[6]在不同产地决明子的有效成分含量差异与品质评价中得出河南、安徽、四川区域决明子蒽醌含量较高;张毅等[7]在HPLC测定不同产地决明子中蒽醌类成分得出不同产地间的7个蒽醌类成分差异较大。
基本集中在产地之间的对比,对决明规格之间的对比却很少,并且近些年来大量进口决明子从缅甸、越南、老挝等国流入国内市场,凭借低廉价格已占领国内市场半壁江山[8],冲击国产决明市场,造成市场品种混乱,质量参差不齐。
决明子提取物

【中文名称】:决明子提取物
【供应商】:西安明泽生物科技有限公司
【提取来源】:本品为豆科植物决明Cassia obtusifolia L. 或小决明Cassia tora L. 的干燥成熟种子。
【性味归经】性味:咸苦;平凉;无毒。
归经:肝经;胆经;肾经。
【产品规格】10:1,也可按客户要求定制各种比例
【检测方法】TLC(薄层色谱法检测)
【质量标准】:
1.使用部分: 决明的干燥成熟种子。
2.色泽:棕色精细粉末。
3.目数: 100%过80目
4.气味:特殊气味
5.干燥失重:≤5%
6.灰份: <5%
7.重金属: <10PPM
8.溶剂残留:<0.05PPM
【微生物标准】
1.总细菌量: <1000CFU/gm
2.大肠杆菌:未检出
3.沙门氏菌:未检出
4.霉菌和酵母菌:<100CFU/gm
【功能主治】清热明目,润肠通便。
用于目赤涩痛,羞明多泪,头痛眩晕,目暗不明,大便秘结。
【保存】置于阴凉干燥、避光,避高温处。
【保质期】两年
【包装】内用双层塑料袋,外用铝箔袋或纸板桶(25公斤/桶)
【供应商】:西安明泽生物科技有限公司。
决明子质量标准

XXXXXXXXX有限公司
一、目的:建立决明子药材、饮片的质量标准,确保投用药材、饮片的质量。
二、范围:本规定适用于决明子药材、饮片的质量控制。
三、责任:
四、内容:
1.标准来源
2015年版《中国药典》一部
2.技术要求
2.1决明子药材:
2.2决明子饮片:
3.贮存条件:置干燥处。
4.相关标准操作规程:决明子检验操作规程(SOP-ZL-JG(YL)-024)、物料取样标准操作规程(SOP-ZL-QA-001)。
5.企业统一指定的物料名称:与2015年版《中国药典》一部一致。
6.内部使用的物料代码:1101092。
7.经批准的供应商:见合格供应商目录。
8.印刷包装材料的实样或样稿:无此项内容。
9.注意事项:无此项内容。
10.复验期:执行“物料有效期及复验期管理规程(SMP-WL-008)”相关规定。
11.文件附件:共0份。
12.修订及变更历史:。
生产企业药品检验报告模板

生产企业药品检验报告模板1. 药品基本信息- 药品名称:[药品名称]- 生产企业:[生产企业名称]- 规格:[规格]- 批号:[批号]- 有效期:[有效期]- 样品数量:[样品数量]- 检验日期:[检验日期]2. 检验项目及结果2.1. 外观检查- 外观性状:[外观性状结果]2.2. 标签标识- 标签标识是否清晰完整:[是否清晰完整结果]- 标签标识是否与药品相符:[是否与药品相符结果]2.3. 药品含量- 药品含量测定结果:[含量测定结果]2.4. 出厂日期- 药品出厂日期:[出厂日期]2.5. 贮存条件- 药品贮存条件是否符合标准:[是否符合标准结果]2.6. 微生物污染- 微生物总数:[微生物总数结果]- 大肠菌群:[大肠菌群结果]- 霉菌和酵母菌:[霉菌和酵母菌结果]2.7. 重金属含量- 铅:[铅含量结果]- 镉:[镉含量结果]- 汞:[汞含量结果]- 铜:[铜含量结果]- 镍:[镍含量结果]2.8. 其他检验项目- [项目1]:[结果1]- [项目2]:[结果2]- ...3. 检验结论根据对以上项目进行的检验,本次检验结果如下:- 外观检查:[外观检查结论]- 标签标识:[标签标识结论]- 药品含量:[药品含量结论]- 贮存条件:[贮存条件结论]- 微生物污染:[微生物污染结论]- 重金属含量:[重金属含量结论]- 其他检验项目:[其他检验项目结论]4. 检验备注- [备注信息]5. 检验人员签名与日期- 检验人员:[检验人员姓名]- 签名:[检验人员签名]- 日期:[检验日期]以上是对药品的检验结果报告,仅供参考。
如有疑问,请及时与生产企业联系。
黄酮类决明子实验报告

一、实验目的1. 了解黄酮类化合物的基本性质及其在植物中的分布;2. 掌握黄酮类化合物的提取方法;3. 学习并运用分光光度法测定黄酮类化合物的含量;4. 分析黄酮类化合物在决明子中的分布及含量。
二、实验原理黄酮类化合物是一类广泛存在于植物中的天然有机化合物,具有多种生物活性。
本实验采用超声波辅助提取法从决明子中提取黄酮类化合物,利用分光光度法测定其含量。
在特定波长下,黄酮类化合物与一定浓度的铝离子形成络合物,络合物颜色深浅与黄酮类化合物含量成正比。
三、实验材料与仪器1. 实验材料:决明子、无水乙醇、氢氧化钠、硝酸铝、三氯化铝、氢氧化钠、蒸馏水等。
2. 仪器:超声波提取仪、分光光度计、电子天平、移液器、容量瓶、试管等。
四、实验步骤1. 样品处理:称取一定量的决明子粉末,加入适量的无水乙醇,超声提取30分钟,过滤,取滤液待测。
2. 标准曲线绘制:配制一系列不同浓度的芦丁标准溶液,分别加入一定量的硝酸铝溶液,显色后,于特定波长下测定吸光度,绘制标准曲线。
3. 样品测定:取一定量的样品溶液,按照绘制标准曲线的方法进行显色,测定吸光度,根据标准曲线计算样品中黄酮类化合物的含量。
4. 结果分析:比较不同提取方法对黄酮类化合物提取效率的影响,分析黄酮类化合物在决明子中的分布及含量。
五、实验结果与分析1. 标准曲线绘制:根据实验数据绘制标准曲线,得线性回归方程为:y = 0.0488x + 0.0063,相关系数R² = 0.9987。
2. 样品测定:按照上述方法测定样品溶液的吸光度,计算样品中黄酮类化合物的含量。
结果显示,决明子中黄酮类化合物的含量为2.56mg/g。
3. 结果分析:(1)超声波辅助提取法在提取决明子中黄酮类化合物方面具有较高的效率,提取时间短,操作简便。
(2)通过分光光度法测定,得决明子中黄酮类化合物的含量为2.56mg/g,说明决明子中黄酮类化合物含量较高,具有较好的开发利用价值。
决明子质量标准及检验操作规程
XXXXXXXXXX有限公司原料质量标准及检验操作规程1品名:1.1 中文名:决明子1.2 汉语拼音:Juemingzi2 代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7 检验操作规程:7.1 试药试剂:甲醇、盐酸、乙醚、三氯甲烷、橙黄决明素对照品、大黄酚对照品、无水乙醇、乙酸乙酯、石油醚(30~60℃)、丙酮、氨试液、乙腈、磷酸。
7.2 仪器设备:显微镜、电子天平、回流装置、水浴锅、硅胶H薄层板、紫外光灯、马福炉、高效液相色谱仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:7.4.1取本品横切面制片显微镜(10×10)观察组织结构特征。
7.4.2取本品粉末1g,加甲醇10ml,浸渍1小时,滤过,滤液蒸干,残渣加水10ml使溶解,再加盐酸1ml,置水浴上加热30分钟,立即冷却,用乙醚提取2次,每次20ml,合并乙醚液,蒸干,残渣加三氯甲烷1ml使溶解,作为供试品溶液。
另取橙黄决明素对照品、大黄酚对照品,加无水乙醇-乙酸乙酯(2:1)制成每1ml各含1mg的混合溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述两种溶液各2μl,分别点于同一硅胶H薄层板上,以石油醚(30~60℃)-丙酮(2:1)为展开剂,展开,取出,晾干。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点;置氨蒸气中熏后,斑点变为亮黄色(橙黄决明素)和粉红色(大黄酚)。
7.5 检查:7.5.1水分:不得过15.0%(附录15第二法)。
7.5.2总灰分:不得过7.0%(附录17)。
7.5.3黄曲霉毒素照黄曲霉毒素测定法(附录50)测定。
取本品粉末约5g,紧密称定,加氯化钠3 g,照黄曲霉毒素测定法项下的供试品的制备方法,测定,计算,即得。
本品每1000 g含黄曲霉毒素B1不得过5μg,含黄曲霉毒素G2、黄曲霉毒素G1、黄曲霉毒素B2和黄曲霉毒素B1的总量不得过10μg。
决明子微量元素含量的分析测定

决明子微量元素含量的分析测定【摘要】目的测定分析决明子微量元素含量。
方法用电感耦合等离子发射光谱仪测定栽培决明子16种微量元素的含量。
结果栽培决明子富含镁、铁、锌、锰、铜等有重要生理活性的微量元素,是营养价值极高的中草药。
结论从微量元素角度分析,决明子是极具开发价值的药食两用中草药。
【关键词】决明子微量元素电感耦合等离子发射光谱Abstract:ObjectiveTo determine and analyze the contents of trace elements in Cassia obtusifolia L..MethodsTrace elements in Cassia obtusifolia L. were determined with inductive coupled plasma emission spectrometer. ResultsThe cultivated Cassia obtusifolia L.. contained a lot of Mg, Fe, Zn, B, Sr, Mn, Cu, and so on, which all possess important physiological activity. Conclusion Thinking over the trace elements, Cassia obtusifolia L. is a double-purpose herb for medicine and food which should be developed and explored extensively.Key words:Cassia obtusifolia L.; Trace element决明子为豆科植物草决明Cassia obtusifolia L.,或小决明Cassia tora L.的干燥成熟种子[1],因其有明目之功效而得名。
决明子饮片、标准汤剂、配方颗粒特征图谱的关联研究
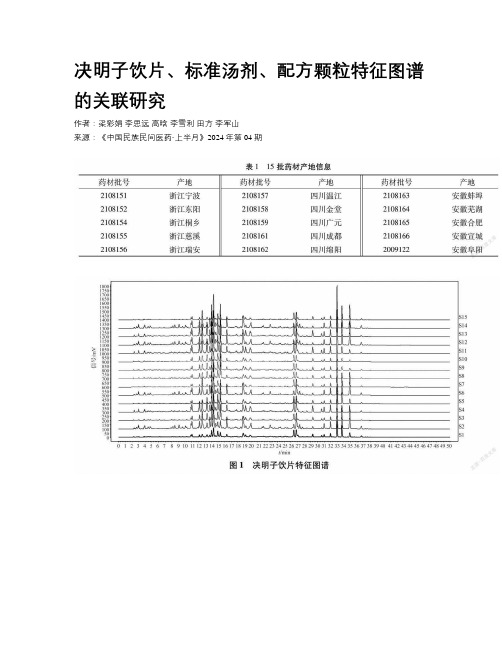
决明子饮片、标准汤剂、配方颗粒特征图谱的关联研究作者:梁彩娟李思远高晗李雪利田方李军山来源:《中国民族民间医药·上半月》2024年第04期【摘要】目的:建立高效液相色谱法测定决明子饮片、标准汤剂和配方颗粒特征图谱的方法并开展相似性研究。
方法:采用Agilent TC C18色谱柱(4.6 mm×250 mm,5 μm)进行高效液相色谱分析,本次试验流速1.0 mL/min,柱温30 ℃,检测波长为290 nm。
以乙腈(A)-0.1%乙酸溶液(B)为流动相进行梯度洗脱,进样体积10 μL。
结果:15批决明子饮片、标准汤剂、配方颗粒中均呈现7个共有特征峰,其中指认出橙黄决明素、芦荟大黄素、大黄素、大黄酚4个成分。
结论:决明子饮片、标准汤剂、配方颗粒中主要化学成分基本一致,特征图谱有较好的相似性,同时为决明子配方颗粒的质量控制提供参考依据。
【关键词】决明子;标准汤剂;特征图谱;配方颗粒;量质传递【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2024)07-0032-05DOI:10.3969/j.issn.1007-8517.2024.07.zgmzmjyyzz202407008Correlation Study on Cassiae Semen,Chinese Medicine Decoction and Formula GranulesLIANG Caijuan1 LI Siyuan1 GAO Han1 LI Xueli1 TIAN Fang1 LI Junshan1,2,3*1.Shineway Pharmaceutical Group Co. Ltd.,Shijiazhuang 051430,China;2.Yunnan Provincial Key Laboratory of Formula Granules, Chuxiong 675000,China;3.Yunnan Shineway Spirin Pharmaceutical Co. Ltd,Chuxiong 675000,ChinaAbstract:Objective A HPLC method was established for simultaneous determination of characteristic spectra of Cassiae Semen, Chinese medicine decoction, and formula granules.Methods The Agilent TC C18 column(4.6 mm×250 mm,5 μm)was used as the chromatographic column.A mixture of cetonitrile and 0.1% acetic acid solution was employed as the mobile phase for HPLC withgradient elution to determine the contents.Results There were seven characteristic peaks in the production process of formula granules.Conclusion This research was based on the correlation of Cassiae Semen, Chinese medicine decoction and formula granules.It is facilitated creating a foundation for the establishment of Cassiae Semen formula granules.Keywords:Cassiae Semen; Chinese Medicine Decoction; Characteristic Spectra; Formula Granules; Correlation Study決明子为豆科植物钝叶决明Cassia obtusifolia L.或决明(小决明)Cassia tora L.的干燥成熟种子。
决明子(大黄酚、橙黄决明素)高效液相图谱(对照和样品)

<色谱图>采集人: Admin 样品名称: 决明子 样品 ID :进样体积: 10 uL数据文件名: 决明子z023-*******对照002.lcd 方法文件名: 决明子.lcm 批处理文件名: 金银花.lcb 报告文件名: Default.lcr数据采集: 2012-6-15 10:51:02数据处理: 2012-6-15 13:07:16峰表检测器 A Ch1 284nm 峰# 1 2 总计保留时间 13.965 31.184 面积1648741 851750 2500491高度59691 60136 119827面积 % 65.937 34.063 100.000高度 % 49.814 50.186 100.000理论塔板# 5823.163 110629.9562010版药典方法,岛津LC-2010C,迪马柱子(C18\250*4.6)<色谱图>采集人: Admin 样品名称: 决明子 样品 ID :进样体积: 10 uL数据文件名: 决明子z023-*******样品002.lcd 方法文件名: 决明子.lcm 批处理文件名: 金银花.lcb 报告文件名: Default.lcr数据采集: 2012-6-15 11:47:41数据处理: 2012-6-15 13:08:02峰表检测器 A Ch1 284nm 峰# 1 2 3 4 5 总计保留时间 13.950 15.745 28.491 29.269 31.189 面积1074739 1204896 3312016 1820122 1016312 8428086高度37631 36461 214605 125204 71428 485330面积 % 12.752 14.296 39.297 21.596 12.059 100.000分离度0.000 2.274 20.578 1.982 5.081理论塔板# 5617.165 5693.975 79513.348 94356.967 110806.5912010版药典方法,岛津LC-2010C,迪马柱子(C18\250*4.6)。
决明子生药鉴定实验报告

一、实验目的本次实验旨在通过观察和分析决明子的外观性状、显微特征以及理化性质,对决明子进行生药鉴定,从而提高对中药的认识和鉴别能力。
二、实验材料1. 实验药品:决明子(钝叶决明、小决明)。
2. 实验仪器:显微镜、电子天平、水浴锅、乙醇、盐酸、碘液等。
3. 实验试剂:醋酸酐、硫酸、碘化钾、氢氧化钠等。
三、实验方法1. 外观性状鉴定(1)观察决明子的形状、大小、颜色、表面特征等。
(2)比较钝叶决明和小决明的异同。
(3)观察决明子的断面特征,包括种皮、胚乳、子叶等。
2. 显微特征鉴定(1)观察决明子的横切面和纵切面。
(2)观察决明子种皮、胚乳、子叶的细胞结构。
(3)观察决明子中的草酸钙簇晶、淀粉粒等。
3. 理化性质鉴定(1)测定决明子的水分、灰分等。
(2)进行决明子的酸碱度测定。
(3)进行决明子的浸出物测定。
四、实验结果1. 外观性状鉴定(1)钝叶决明:呈四棱性短圆柱形,一端钝圆,另一端倾斜并有尖头,长4~6mm,宽2~3mm。
表面棕绿色或暗棕色,平滑,有光泽,背腹面各有1条凸起的棱线。
棱线两侧各有1条从脐点向合点斜向的浅棕色凹纹。
质坚硬。
(2)小决明:短圆柱形,长3~5mm,宽2~2.5mm。
棱线两侧各有1条宽广的浅黄棕色带。
2. 显微特征鉴定(1)钝叶决明:最外为厚的角质层,表皮为一列栅状细胞,壁不均匀加厚,在细胞的1/2和下1/3处各有一条光辉带;以下为一列支柱细胞,略呈哑铃状,壁厚,相邻两细胞间有大的细胞间隙;内方为6~8列营养层薄壁细胞,内含草酸钙簇晶,直径3~10μm;最内一列种皮细胞排列整齐,长方形,含草酸钙棱晶。
(2)小决明:草酸钙簇晶多,直径10~19μm,部分支柱细胞外侧。
3. 理化性质鉴定(1)水分:钝叶决明为9.5%,小决明为10.2%。
(2)灰分:钝叶决明为6.2%,小决明为5.8%。
(3)酸碱度:钝叶决明为6.2,小决明为5.8。
(4)浸出物:钝叶决明为17.5%,小决明为15.2%。
成品药材决明子质量标准

杂质、灰屑检查不得过3
总灰分不得过6.0%(附录Ⅸ K )。
【含量测定】照高效液相色谱法(附录VI D)测定。
色谱条件与系统适应性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以0.1%磷酸溶液为流动相B,按下表中规定进行梯度洗脱;检测波长为284nm;理论板数按橙黄决明素峰计算应不低于3000。
测定法分别精密吸取对照品溶液与供试品溶液各10µl,注入液相色谱仪,测定,即得。
本品按干燥品计算,含大黄酚(C15H10O4)不得少于0.20%,含橙黄决明素(C17H14O7)不得少于0.080%。
炒决明子取净决明子,照清炒法(附录Ⅱ D)炒至微鼓起、有香气。用时捣碎。
略呈菱方形或短圆柱形,两端平行倾斜,微鼓起,表面绿褐色或暗棕色,偶见焦斑。微有香气。
(2) 取本品粉末1g,加甲醇10ml,浸渍1小时,滤过,滤液蒸干,残渣加水10ml使溶解,再加盐酸1ml,置水浴上加热30分钟,立即冷却,用乙醚提取2次,每次20ml,合并乙醚液,蒸干,残渣加三氯甲烷1ml使溶解,作为供试品溶液。另取橙黄决明素、大黄酚对照品,加无水乙醇-乙酸乙酯(2:1)制成每1ml各含1mg的混合溶液。照薄层色谱法(附录Ⅵ B)试验,吸取上述两种溶液各2µl,分别点于同一硅胶H薄层板上,以石油醚(30℃~60℃)-丙酮(2:1)溶液为展开剂,展开,取出,晾干。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点;置氨蒸气中熏后,斑点变为亮黄色(橙黄决明素)和粉红色(大黄酚)。
时间(分钟)
流动相A(%)
流动相B(%)
0~15
40
60
15~30
40→90
60→10
30~40
决明子 检验报告模板
重庆XX中药制药有限责任公司检验记录(首页)名称:决明子代表数量:88kg规格:药材送检数量:0.3kg批号:1504001 包装:塑料袋送检部门:生产部送检日期:2015/04/07检验依据:《中国药典》2010版报告日期:2015 /04/09【性状】菱方形或短圆柱形,两端平行倾斜。
表面绿棕色或暗棕色,平滑有光泽。
一端较平坦,另端斜尖,背腹面各有1条突起的绫线,绫线两端各有1条斜向对称而色较浅的线形凹纹。
气微,味微苦。
结论:□符合规定□不符合规定重庆XX中药制药有限责任公司检验记录(附页)检品批号:1504001【鉴别】粉末:种皮栅状细胞侧面观细胞1列,呈长方形,排列稍不平整。
种皮支持细胞表面呈类圆形。
草酸钙簇晶众多,多存在在于薄壁细胞中。
(对观察到的物质进行编号,并画出相应的图形)□具有/□不具有的显微特征结论:□符合规定□不符合规定□复试。
重庆XX中药制药有限责任公司检验记录(附页)检品批号:1504001【鉴别】照《中国药典》2010年版□一部附录Ⅵ B□二部附录Ⅴ B薄层色谱法检验。
供试品溶液的制备:取粉末1g,加甲醇10ml,浸渍1小时,滤过,滤液蒸干,残渣加水10ml使溶解,再加盐酸1ml,置水浴上加热30分钟,立即冷却,用乙醚提取2次,每次20ml,合并乙醚液,蒸干,残渣加三氯甲烷1ml使溶解,作为供试品溶液。
□标准品□对照品□对照药材溶液的制备:取连橙黄决明素对照品、大黄酚对照品,加无水乙醇-乙酸乙酯(2:1)制成每1ml各含1mg的混合溶液,作为对照品溶液。
结果:供试品色谱中,在与□标准品□对照品□对照药材色谱相应的位置上,显颜色的□荧光斑点□斑点。
结论:□符合规定□不符合规定重庆XX 中药制药有限责任公司薄层色谱检验记录检品编号:15040011 检品名称:决明子日期:2015.04.09 室温:15℃相对湿度:66% 薄层板:硅胶G 板展开剂:石油醚(30~60℃)-丙酮(2:1) 显色剂: ① ②备注:样品 点样量(微升)1 供试品 2ul2 对照品 2ul341313 · ·1212··1111 ··10 10·99 ··8 8··77 ··6 6··55 ··4 4··33 ··2 2··11··1 2 3 4 5 6重庆XX中药制药有限责任公司检验记录(附页)检品编号:1504001【水分】中国药典2010年版一部附录IX H第一法,依法检查。
药品检验报告书模板

药品检验报告书模板1. 检验目的本次检验的目的是对药品进行检测,确保其符合相关标准,以确保药品的质量和安全性。
2. 检验对象药品名称批号规格生产日期- -药品A 1234 10mg 2021/01药品B 5678 20mg 2020/12药品C 9012 5mg 2021/023. 检验项目本次检验主要围绕以下项目进行:1. 外观检查2. 可溶性残留物检查3. 化学成分检测4. 微生物检验4. 检验结果4.1 外观检查药品A、B、C的外观均符合规定要求,无明显可见的异物、颜色异常等问题。
4.2 可溶性残留物检查药品A、B、C经可溶性残留物检查,结果如下:- 药品A:检测结果为0.02mg/ml,符合规定要求。
- 药品B:检测结果为0.01mg/ml,符合规定要求。
- 药品C:检测结果为0.03mg/ml,符合规定要求。
4.3 化学成分检测本次化学成分检测主要关注以下几个指标:1. 含量测定:检测各药品中的主要活性成分含量。
2. 原料成分检测:检测药品中是否含有禁用成分或添加其他未声明的成分。
具体的化学成分检测结果如下:药品名称活性成分含量(%)原料成分检测结果药品A 99.8% 合格药品B 98.5% 合格药品C 99.9% 合格4.4 微生物检验微生物检验主要针对药品中是否存在细菌、霉菌等微生物污染。
经过检测,药品A、B、C的微生物检验结果如下:- 药品A:无细菌、霉菌污染。
- 药品B:无细菌、霉菌污染。
- 药品C:无细菌、霉菌污染。
5. 检验结论根据以上检验结果,药品A、B、C均符合相关标准要求,合格通过检验。
药品质量可靠,可以正常投放市场和使用。
6. 检验结论有效期本次检验结论的有效期为一年,即从报告发出之日起的一年内有效。
7.备注(这里可以记录检验过程中的任何异常情况、备注、建议等内容)该药品检验报告书为虚构内容,仅用于参考示例。
实际药品检验报告会根据不同药品的特性、检验要求进行定制。
不同商品规格决明子的质量分析

tora and imported Cassia, imported Cassia tora is the lowest.Most of imported Cassia tora and imported Cassia are not up to the standards of pharmacopoeia.Conclusion: Among the different specif ications of Cassia. the quality of Cassia is better than Cas— sia imported. which provides a basis for market regulation and comprehensive quality evaluation.
Quality Evaluation of Cassia with Different Specif icat ions YANG Guoding,ZHANG Luo—qi,CHEN Sui—qing ,WANG Li—li (Pharmacy school,Henan Unwemity of Traditional Chinese Med&ine,Zhengzhou 450046,China)
[Keywords] Cassia;specif ication;aurantio—obtusin;ehrysophanol;rubrofusarin gentiobioside;casside doi:10.13313/j.issn.1673-4890.20171l15004
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重庆XX中药制药有限责任公司
检验记录(首页)
名称:决明子代表数量:88kg
规格:药材送检数量:0.3kg
批号:1504001 包装:塑料袋
送检部门:生产部送检日期:2015/04/07
检验依据:《中国药典》2010版报告日期:2015 /04/09
【性状】
菱方形或短圆柱形,两端平行倾斜。
表面绿棕色或暗棕色,平滑有光泽。
一端较平坦,另端斜尖,背腹面各有1条突起的绫线,绫线两端各有1条斜向对称而色较浅的线形凹纹。
气微,味微苦。
结论:□符合规定□不符合规定
重庆XX中药制药有限责任公司
检验记录(附页)
检品批号:1504001
【鉴别】粉末:种皮栅状细胞侧面观细胞1列,呈长方形,排列稍不平整。
种皮支持细胞表面呈类圆形。
草酸钙簇晶众多,多存在在于薄壁细胞中。
(对观察到的物质进行编号,并画出相应的图形)
□具有/□不具有的显微特征
结论:□符合规定□不符合规定□复试。
重庆XX中药制药有限责任公司
检验记录(附页)
检品批号:1504001
【鉴别】照《中国药典》2010年版□一部附录Ⅵ B□二部附录Ⅴ B薄层色谱法检验。
供试品溶液的制备:
取粉末1g,加甲醇10ml,浸渍1小时,滤过,滤液蒸干,残渣加水10ml使溶解,再加盐酸1ml,置水浴上加热30分钟,立即冷却,用乙醚提取2次,每次20ml,合并乙醚液,蒸干,残渣加三氯甲烷1ml使溶解,作为供试品溶液。
□标准品□对照品□对照药材溶液的制备:
取连橙黄决明素对照品、大黄酚对照品,加无水乙醇-乙酸乙酯(2:1)制成每1ml各含1mg的混合溶液,作为对照品溶液。
结果:供试品色谱中,在与□标准品□对照品□对照药材色谱相应的位置上,显颜色的□荧光斑点□斑点。
结论:□符合规定□不符合规定
重庆XX 中药制药有限责任公司
薄层色谱检验记录
检品编号:15040011 检品名称:决明子
日期:2015.04.09 室温:15℃
相对湿度:66% 薄层板:硅胶G 板
展开剂:
石油醚(30~60℃)-丙酮(2:1) 显色剂: ① ②
备注:
样品 点样量(微升)
1 供试品 2ul
2 对照品 2ul
3
4
13
13 · ·
12
12
·
·
11
11 ·
·
10 10
·
9
9 ·
·
8 8
·
·
7
7 ·
·
6 6
·
·
5
5 ·
·
4 4
·
·
3
3 ·
·
2 2
·
·
1
1
·
·
1 2 3 4 5 6
重庆XX中药制药有限责任公司
检验记录(附页)
检品编号:1504001
【水分】中国药典2010年版一部附录IX H第一法,依法检查。
天平型号:FZ604A 编号:ZGB01-017
干燥箱型号:101-1A 编号:ZGB01-008 干燥温度:105℃ 1号 2号
称量瓶恒重W1 (g)
一次(g):
二次(g):
样品重W2 (g):
样加瓶重W3五小时(g)
再一小时(g):
计算公式:
W2-(W3-W1)
×100%
W2
⑴
⑵
平均值:
标准规定:不得过15.0%
结论:□符合规定□不符合规定
重庆XX 中药制药有限责任公司
检验记录(附页)
检品批号:1504001
灰分 照《中国药典》2010年版一部附录Ⅸ K □总灰分□酸不溶性灰分测定法检查 天平型号:FZ604A 编号:ZGB01-017 仪器型号:SX2-2.5-10A 编号:ZGB01-009 温度:550℃ 实验结果:
坩埚瓶恒重W 1 : 1# 2# 一 次(g ) 二 次(g )
样 品 重W 2: (g ) 样品+坩埚恒重W 3: 一 次(g ) 二 次(g )
计算公式:灰分% = %1002
13⨯-W W
W ①
②
平均值:
标准规定:不得过5.0%
结论:□符合规定 □不符合规定
重庆X X中药制药有限责任公司
检验记录(附页)
检品批号:1504001
【含量测定】《中国药典》2010年版□一部ⅥD□二部附录ⅤD高效液相色谱法
色谱条件与系统适用性试验:
仪器型号:LC210 编号:ZGB01-010
天平型号:FZ604A 编号:ZGB01-017
柱温:35℃检测器:□紫外
检测波长:284 nm 流动相:乙腈流速:3 ml/min
供试品溶液的配制:
取粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,加热回流2小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液25ml,蒸干,加稀盐酸30ml,置水浴中加热1小时,立即冷却,用三氯甲烷振摇提取4次,每次30ml,合并三氯甲烷液,回收溶剂至干,残渣用无水乙醇-乙酸乙酯(2:1)混合溶液使溶解,转移至25ml量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
□对照品□标准品溶液的配制:
取大黄酚对照品适量,精密称定,加无水乙醇-乙酸乙酯(2:1)混合溶液制成每1ml含大黄酚30ug的混合溶液,即得。
精密量取供试品溶液10 μl与对照品溶液10 μl,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,
重庆X X中药制药有限责任公司
检验记录(附页)
检品批号:1504001
计算:
f值计算公式: F=C/A
对照品取样量(单位:g)
对照品浓度(mg/ml)
峰面积A
f值
f平均值
RSD
样品计算公式:
样品取样量(单位:g )
峰面积A
含量(单位:)
含量平均值
RSD
示例:
标准规定:不得少于0.20%
结论:□符合规定□不符合规定
重庆X X中药制药有限责任公司
检验记录(附页)
检品批号:1504001
【含量测定】《中国药典》2010年版□一部ⅥD□二部附录ⅤD高效液相色谱法
色谱条件与系统适用性试验:
温度:湿度:
仪器型号:LC210 编号:ZGB01-010
天平型号:FZ604A 编号:ZGB01-017
柱温:35℃检测器:□紫外
检测波长:284 nm 流动相:0.1%磷酸溶液流速:3 ml/min
供试品溶液的配制:
取粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,加热回流2小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液25ml,蒸干,加稀盐酸30ml,置水浴中加热1小时,立即冷却,用三氯甲烷振摇提取4次,每次30ml,合并三氯甲烷液,回收溶剂至干,残渣用无水乙醇-乙酸乙酯(2:1)混合溶液使溶解,转移至25ml量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
□对照品□标准品溶液的配制:
取橙黄决明素对照品适量,精密称定,加无水乙醇-乙酸乙酯(2:1)混合溶液制成每1ml 含橙黄决明素20ug的混合溶液,即得。
精密量取供试品溶液10 μl与对照品溶液10 μl,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,
重庆X X中药制药有限责任公司
检验记录(附页)
检品批号:1504001
计算:
f值计算公式: F=C/A
对照品取样量(单位:g)
对照品浓度(mg/ml)
峰面积A
f值
f平均值
RSD
样品计算公式:
样品取样量(单位:g )
峰面积A
含量(单位:)
含量平均值
RSD
示例:
标准规定:不得少于0.080%
结论:□符合规定□不符合规定。
