第四章环烃(10-11(1)讲解
合集下载
汪小兰有机化学课件第四版第四章-环烃

第三节 环烷烃的结构 与稳定性
一、环丙烷的结构 二、环丁烷和环戊烷的构 象 第四节 环己烷的构象 一、环己烷的构象 二、取代环己烷的椅式
构象稳定性分析
总目录
第一节 脂环烃的分类和命名
一、分类
总目录
二、命名
1. 单环烃 (1)母体 以相应的开链烃名称前加“环(
cyclo)”字。如环某烷、环某烯、环某炔 (2)编号
总目录
2. 弯曲键的概念
总目录
C—C原子间不连成直线,而是弯曲重叠,比
σ 键弱,又有别于π 键,介于两者之间,更 接近π 键。
电子云分布在C—C外侧,易被亲电试剂进 攻,有一定的烯烃性质。
3. 燃烧热和非平面结构
燃烧热是指1 mol化合物完全燃烧生成二氧化碳和水时所放出的热 量。它反映了分子的内能大小。
3. 苯的共振式
五、苯分子结构的表示方法
圆圈式 (全球通用,当心少圈)
凯库勒式 (名不符实,但较为常用)
杜瓦苯 (此“苯”非“苯”)
闲话“江湖”野史: 1.1989年化学史坛地震:1861年洛斯密德提出芳香化合物的环状符号——1865年凯库勒沽 名钓誉?(《大学化学》) 2.擅长“大综合”的鲍林(1901—1994),因共振论等两次荣获诺贝尔奖。
短桥。使不饱和键或取代基位次尽可能小。
7
9
1 6
2
5
4 3
85
6
4
7 123
总目录
B.注明环数
环数:使桥环化合物成为开链烃所需的切割次数
C.书写顺序
取代基位次和名称→某环[a .b .c]某烷(烯或炔) a:长桥的碳原子数(不包括桥头碳); b:次长桥的碳原子数(不包括桥头碳) ; c:最短桥的碳原子数(不包括桥头碳) ;
S004 第四章 环烃有机化学 教学课件
❖在室温下就能迅速转环,在转环的过程中,原来的a键 全都变成e键,原来的e键全都变成a键。
❖当环烷烃的两个碳原子上连有不同的基团时,就存在 顺反异构现象。
H CH3
CH3 H
反-1,4-二甲基环己烷
HH
CH3
CH3 CH3
顺-1,4-二甲基环己烷
CH3
CH3 CH3
4-4 脂环烃的性质
❖脂环烃不溶于水,相对密度小于1,环烷烃的沸点比碳 原子数相同的烷烃高。 ❖三元、四元环烷烃分子中存在张力,化学性质比较活 泼,容易发生开环加成,五元以上环烷烃较稳定,性质 和烷烃相似,容易发生取代反应。
2 直立键和平伏键
❖椅式构象中的碳氢键可以分为两类,6个碳氢键与分 子的对称轴平行,叫做直立键或a键。
❖另外6个碳氢键指向环外,与直立键成109°28′的角, 平伏着向环外伸展,叫做平伏键或e键。
❖一个椅式构象的环己烷,可以通过碳碳单键的旋转变成 另一种椅式构象,叫做转环作用。
X
X
❖当环己烷上的氢原子被其它基团取代后,由于其它基团 都比氢原子大,所以取代基以e键和环相连占优势。
HH
船式构象
分子模型:
椅式构象
船式构象
❖椅式构象较稳定的原因:
①船式构象中相邻碳上的碳氢键全部为重叠式构象,存 在扭转张力,而椅式构象中相邻碳上的碳氢键全部为交 叉式构象,没有扭转张力。
②船式构象中船头碳原子C1和C4上的氢原子距离较近, 斥力较大。而椅式构象中C1和C4上的氢原子距离较远, 斥力较小。
1,2-二甲苯 邻二甲苯
CH3
CH3
1,3-二甲苯 间二甲苯
CH3
CH3
1,4-二甲苯 对二甲苯
2 多环芳香烃
第四章 环 烃

CH2
强调:在室温时用 强调:在室温时用Br2-H2O或Br2-CCl4溶 或 不能将环丙烷及其衍生物与烯烃、 液不能将环丙烷及其衍生物与烯烃、炔烃 等区分开来。 等区分开来。
环丙烷对氧化剂较稳定,它不与KMnO4水溶液 环丙烷对氧化剂较稳定,它不与 或臭氧作用,故可用KMnO4溶液来区别环丙烷及其 溶液来区别环丙烷及其 或臭氧作用,故可用 衍生物和烯烃、炔烃等化合物 等化合物。 衍生物和烯烃、炔烃等化合物。
H3C CH3
顺-1,4-二甲基环己烷 , 二甲基环己烷
反-1,4-二甲基环己烷 , 二甲基环己烷
2. 螺环烃 脂环烃分子中两个碳环共有一个碳原子 脂环烃分子中两个碳环共有一个碳原子。
单螺环的命名:根据成环碳原子的总数称为螺某烷,在螺字后面的方括号 螺原子不计算在内) 将小 中,用阿拉伯数字标出两个碳环碳原子数目(螺原子不计算在内),将小 的数字排在前面, 隔开, 的数字排在前面,数字之间用下角圆点隔开,编号是从较小环中与螺原子相
第四章 环 烃
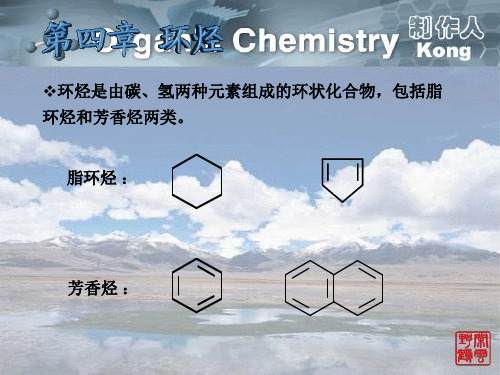
环烃是由碳 环烃是由碳和氢两种元素组成的环状化合物。根据它 是由 两种元素组成的环状化合物。 环状化合物 们的结构 性质,又可分为脂环烃 芳香烃。 结构或 脂环烃和 们的结构或性质,又可分为脂环烃和芳香烃。
§ 4~1 脂环烃
一、脂环烃的分类
碳原子的 饱和程度 饱和脂环烃 不饱和脂环烃 环炔烃 环烷烃 环烯烃
4.稠环烃 稠环烃
三、环烷的结构
说明: 说明:环烯烃 、环炔烃分子中的碳碳双键和碳碳 三键的电子结构与烯、炔烃相同, 三键的电子结构与烯、炔烃相同,故具有一般不 饱和键的通性。 饱和键的通性。
环烷烃的结构: 环烷中的碳原子为sp3杂化 环烷烃的结构: 环烷中的碳原子为 杂化。 杂化。
第四章环烃教学讲义

CH3
CH2Cl
光
Cl2 130-140℃
苯氯甲烷(氯化苄)
(2)硝化
浓H2SO4 HNO3 50-60℃
CH3
浓H2SO4
HNO3 10-30℃
NO2 H2O
硝基苯
CH3 NO2
CH3
Байду номын сангаас邻硝基甲苯
NO2 对硝基甲苯
解释:1、这是实验和工业上制备硝基化合物的方法之一; 2、甲苯比苯易硝化
(3)磺化
3.桥环的编号,从一个桥头开始,
循的最长桥编到另一个桥头,
再循余下的次长的桥编到桥头, 最短的桥最后编号。
二环壬烷
螺环烃:一个共用碳原子,两个碳环 共用的碳原子称为螺原子。
螺环(单螺环)命名原则:
1.螺作词头,成环碳原子的 总数作为母体烃的名称;
2.两个碳环(除螺原子外),
用阿拉伯数字由小到大表示;
CH3 115℃
H2SO4 5-15h
CH3
CH3
SO3H
10%-20%
邻甲苯磺酸
SO3H
75%-85%
邻甲苯磺酸
(4)付氏反应(付列德尔-克拉夫茨)
(A)烷基化反应(引入烷基的反应)
无 水 AlCl3
C H 3C H 2B r 80℃
C H 2C H 3H B r
乙 苯
常用催化剂:AlCl3、FeCl3、SnCl4、SbCl3、ZnCl2等 路易斯酸和HF、H2SO4、H3PO4等质子酸
休克尔规则:π电子数=4n+2 (n=0,1,2,3…)
电 子 数 2 6 1 0
1 4
思考题:下列哪些是芳香性化合物?
1、
2、
有机化学 第4章 环烃(原版)

II.芳香烃
芳香烃的含义:不再仅指“含有苯环且有香 味”的物质,而是指“在结构上有某些特点 并具有芳香性的许多化合物”本节主要讨论 含有苯环的碳氢化合物。
分类:
单环芳烃 根据含苯环的数目苯
多环芳烃
命名:
1、单环芳香烃
(1)一元取代苯:简单的以苯为母体,复杂的苯 为取代基;
(2)多元取代苯:用邻、间、对或数字编号; (3)IUPAC规定:甲苯、邻二甲苯、异丙苯、
简写为
5、但凯库勒不能解释:
X与
X
X
X
实际上是相同的
6、现代物理方法证明:
H
120°
H
0.1397nm
H
正六边形结构 所有的原子共平面
120°
0.1397nm CC 键长均为 0.1397nm
H
H
CH键长均为 0.110nm
0.110nm H
所有键角都为 120°
根据杂化理论:苯分子中的碳原子都是以sp2杂化 轨道成键的,故键角均为120°,所有原子均在同 一平面上。 C-C(sp2-sp2); C-H(sp2-s)。
(4)傅氏反应
在无水三氯化铝的催化下,苯与卤代烷反应, 生成烷基苯——傅氏烷基化反应。
+ CH3CH2Br 无水AlCl3
CH2CH3 + HBr
当引入的烷基为三个碳以上时,引入的烷基 会发生碳链异构现象。例如:
+ CH3CH2CH2Cl AlCl3
CH3 CH +
CH3
CH2CH2CH3
异丙苯(主 ) 正丙苯
命名:
1、简单的命名与相应的脂肪烃基本相同,在 名称前加一“环”字;
2、当环上有取代基,取代基位置数字按“最 小原则”将环编号,不同取代基顺序按“次 序规则”小的优先列出;
4环烃脂环烃-PPT精品文档

第四章 环烃 (cyclic hydrocarbon )
Ⅰ脂环烃(alicyclic hydrocarbon)
一、脂环烃分类与命名 二、脂环烃的物理化学性质 三、脂环烃的结构特征 四、环己烷及其衍生物的构象 重点掌握:环烷烃的系统命名法;
环己烷及其衍生物的构象。
一、脂环烃分类与命名
1,分类
脂环烃 (饱和程度)
环戊烷
甲基环丁烷
异基环丙烷
1,1-二甲基环丙烷
C H3
顺-1,2-二甲基环丙烷
C H3
C H3
C H3
反-1,2-二甲基环丙烷
脂环化合物由于环的限制,环上所连接的原子或基团,如同 连接在碳碳双键上一样,不能自由旋转。 如果环上有两个或两个以上的碳原子各自连有不同的原子或 基团时产生顺反异构。
二、环烷烃物理化学性质
环烷烃的张力越大,能量愈高,分子愈不稳定。
构造异构:由于原子的连接次序不同而引起的异构现象。
立体异构:由于原子在空间的排列不同而引起的异构现象。 若各异构体之间可通过键旋转转化,则为构象异构,否则 为构型异构。
环丙烷的结构
碳原子为 sp3杂化
为缓解角张力 形成弯曲键
C 105° C
C
C-C-C键角 偏离正常键 角产生角张
拜尔假定:环中碳-碳键键角的变形会产生张力。键 角变形的程度越大,张力越大。张力使环的稳定性降低,张 力越大,环的反应活性也越大。
H
H
HH
C
H
H
CC
H
H
sp3杂 化 109°28’
C
H C
H
H C
H
C-C-C=105.5 ° 弯 曲 键
109°28’ -60° =49.5° 比 正 常 的 sp3杂 化 键 角 小 49.5° 角 张 力 = 24.75°
Ⅰ脂环烃(alicyclic hydrocarbon)
一、脂环烃分类与命名 二、脂环烃的物理化学性质 三、脂环烃的结构特征 四、环己烷及其衍生物的构象 重点掌握:环烷烃的系统命名法;
环己烷及其衍生物的构象。
一、脂环烃分类与命名
1,分类
脂环烃 (饱和程度)
环戊烷
甲基环丁烷
异基环丙烷
1,1-二甲基环丙烷
C H3
顺-1,2-二甲基环丙烷
C H3
C H3
C H3
反-1,2-二甲基环丙烷
脂环化合物由于环的限制,环上所连接的原子或基团,如同 连接在碳碳双键上一样,不能自由旋转。 如果环上有两个或两个以上的碳原子各自连有不同的原子或 基团时产生顺反异构。
二、环烷烃物理化学性质
环烷烃的张力越大,能量愈高,分子愈不稳定。
构造异构:由于原子的连接次序不同而引起的异构现象。
立体异构:由于原子在空间的排列不同而引起的异构现象。 若各异构体之间可通过键旋转转化,则为构象异构,否则 为构型异构。
环丙烷的结构
碳原子为 sp3杂化
为缓解角张力 形成弯曲键
C 105° C
C
C-C-C键角 偏离正常键 角产生角张
拜尔假定:环中碳-碳键键角的变形会产生张力。键 角变形的程度越大,张力越大。张力使环的稳定性降低,张 力越大,环的反应活性也越大。
H
H
HH
C
H
H
CC
H
H
sp3杂 化 109°28’
C
H C
H
H C
H
C-C-C=105.5 ° 弯 曲 键
109°28’ -60° =49.5° 比 正 常 的 sp3杂 化 键 角 小 49.5° 角 张 力 = 24.75°
有机化学 第4章 环烃

一、芳香烃的分类 (a ) 单环芳烃:分子中含有一个苯环
CH3 苯 甲苯
(b) 多环芳烃:分子中含有两个或两个以上苯环
C H 联苯 三苯甲烷
(c) 稠环芳烃:分子中含有两个或多个苯环彼此间通过 共用两个相邻碳原子稠合而成
萘
蒽
菲
二、单环芳烃
(1)苯的结构
ቤተ መጻሕፍቲ ባይዱ
1814年法拉第发现苯
1834年米切利希提出苯这一名称
ph
甲苯基 CH3 CH3 间 CH3 邻 对
(3)单环芳烃的物理性质
苯及其同系物一般为无色液体,相对密度
小于1,但比相对分子质量相近的烷烃和 烯烃的相对密度大。不溶于水,可溶于有 机溶剂。单环芳烃具有特殊气味,有毒
(4)单环芳烃的化学性质 (4.1) 苯环上的亲电取代反应
① 卤代: 在三卤化铁等催化剂作用下,苯与卤素作用生成卤
(代)苯,此反应称为卤化反应
+ CI2 FeCI3 CI + HCI Br + HBr
CH3 + CI2 FeCI3 CI
+
+ Br2
CH3
FeBr3
CH3
CI
卤苯继续卤化,比苯难,邻对位产物为主
Cl Cl + Cl2 Cl Cl + + Cl 邻二氯苯 (39%) Cl 对二氯苯 (55%) (6%) Cl
H C2-C3 H H
H H H
H
HH
H C6-C5
重叠式
构象稳定性:椅式>船式,椅式是环己烷最稳定的构象
(1)椅式构象的画法
加竖键(a键) 加竖键(a键)
H H H H H H
CH3 苯 甲苯
(b) 多环芳烃:分子中含有两个或两个以上苯环
C H 联苯 三苯甲烷
(c) 稠环芳烃:分子中含有两个或多个苯环彼此间通过 共用两个相邻碳原子稠合而成
萘
蒽
菲
二、单环芳烃
(1)苯的结构
ቤተ መጻሕፍቲ ባይዱ
1814年法拉第发现苯
1834年米切利希提出苯这一名称
ph
甲苯基 CH3 CH3 间 CH3 邻 对
(3)单环芳烃的物理性质
苯及其同系物一般为无色液体,相对密度
小于1,但比相对分子质量相近的烷烃和 烯烃的相对密度大。不溶于水,可溶于有 机溶剂。单环芳烃具有特殊气味,有毒
(4)单环芳烃的化学性质 (4.1) 苯环上的亲电取代反应
① 卤代: 在三卤化铁等催化剂作用下,苯与卤素作用生成卤
(代)苯,此反应称为卤化反应
+ CI2 FeCI3 CI + HCI Br + HBr
CH3 + CI2 FeCI3 CI
+
+ Br2
CH3
FeBr3
CH3
CI
卤苯继续卤化,比苯难,邻对位产物为主
Cl Cl + Cl2 Cl Cl + + Cl 邻二氯苯 (39%) Cl 对二氯苯 (55%) (6%) Cl
H C2-C3 H H
H H H
H
HH
H C6-C5
重叠式
构象稳定性:椅式>船式,椅式是环己烷最稳定的构象
(1)椅式构象的画法
加竖键(a键) 加竖键(a键)
H H H H H H
大学有机化学第四章 链烃和环烃

环烷烃加氢反应的活性:环丙烷>环丁烷>环戊烷。环已烷或大环脂环烃加氢开环非常困难。
2、加卤素:环丙烷、环丁烷与烯烃相似,在常温下可以与卤素发生加成反应。
3、加卤代氢:环丙烷、环丁烷及其衍生物很容易与卤化氢发生加成反应。开环发生在含氢最多和含氢最少的两个碳原子之间,加成反应遵循马氏规则。
环戊烷以上的环烷烃,在室温下难以与卤代氢发生加成反应。
炔氢也能与重金属(Ag或Cu)作用形成不溶于水的炔化物。常用试剂为硝酸银或氯化亚铜的氨溶液。
6、聚合反应
(五)、炔烃的制备
二卤代烷在强碱性条件下脱卤化氢及金属炔化物与伯卤代烃亲核取代反应是制备炔烃的常用方法。
二、二烯烃
分子中含有两个双键的开链烃称为二烯烃(diene),其通式为CnH2n-2。
(一)、分类和命名
2、其它烷烃的氯代反应
其它烷烃在相似条件下也可以发生氯代反应,但产物更复杂。
3、烷烃和其它卤素的取代反应
4、甲烷卤代反应历程
反应历程是指由反应物至产物所经历的过程。一个反应历程是根据这一反应的许多实验事实,总结归纳作出的理论假设。这种假设必须符合并能说明已经发生的实验事实。
(1)、甲烷氯代反应机制
甲烷的卤代反应历程是自由基取代反应历程。
烯烃在一定条件下,发生自身加成反应生成分子量很大的聚合物,这种反应称为聚合反应,参加反应的烯烃称为单体。
六、烯烃的制备
1、醇的脱水
2、卤代烷脱卤化氢
卤代烷与强碱(如氢氧化钾、乙醇钠)的醇溶液共热时,脱去一分子卤化氢生成烯烃。
3、邻二卤代烷脱卤化氢
邻二卤代烷与锌粉一起共热,可脱去一分子卤素生成烯烃。
第三节炔烃和二烯烃
三、烷烃的结构
根据杂化理论认为碳原子在形成甲烷分子时发生了sp3杂化,所以甲烷分子是正四面体结构。烷烃分子中的碳原子是正四面体结构,因此除乙烷外烷烃分子中的碳原子并不排布在一条直线上,而是以锯齿形或其他可能的形式存在。所以“直链烷烃”仅指不带支链的烷烃。
2、加卤素:环丙烷、环丁烷与烯烃相似,在常温下可以与卤素发生加成反应。
3、加卤代氢:环丙烷、环丁烷及其衍生物很容易与卤化氢发生加成反应。开环发生在含氢最多和含氢最少的两个碳原子之间,加成反应遵循马氏规则。
环戊烷以上的环烷烃,在室温下难以与卤代氢发生加成反应。
炔氢也能与重金属(Ag或Cu)作用形成不溶于水的炔化物。常用试剂为硝酸银或氯化亚铜的氨溶液。
6、聚合反应
(五)、炔烃的制备
二卤代烷在强碱性条件下脱卤化氢及金属炔化物与伯卤代烃亲核取代反应是制备炔烃的常用方法。
二、二烯烃
分子中含有两个双键的开链烃称为二烯烃(diene),其通式为CnH2n-2。
(一)、分类和命名
2、其它烷烃的氯代反应
其它烷烃在相似条件下也可以发生氯代反应,但产物更复杂。
3、烷烃和其它卤素的取代反应
4、甲烷卤代反应历程
反应历程是指由反应物至产物所经历的过程。一个反应历程是根据这一反应的许多实验事实,总结归纳作出的理论假设。这种假设必须符合并能说明已经发生的实验事实。
(1)、甲烷氯代反应机制
甲烷的卤代反应历程是自由基取代反应历程。
烯烃在一定条件下,发生自身加成反应生成分子量很大的聚合物,这种反应称为聚合反应,参加反应的烯烃称为单体。
六、烯烃的制备
1、醇的脱水
2、卤代烷脱卤化氢
卤代烷与强碱(如氢氧化钾、乙醇钠)的醇溶液共热时,脱去一分子卤化氢生成烯烃。
3、邻二卤代烷脱卤化氢
邻二卤代烷与锌粉一起共热,可脱去一分子卤素生成烯烃。
第三节炔烃和二烯烃
三、烷烃的结构
根据杂化理论认为碳原子在形成甲烷分子时发生了sp3杂化,所以甲烷分子是正四面体结构。烷烃分子中的碳原子是正四面体结构,因此除乙烷外烷烃分子中的碳原子并不排布在一条直线上,而是以锯齿形或其他可能的形式存在。所以“直链烷烃”仅指不带支链的烷烃。
环烃专题教育课件

芳香烃旳定义:P62
但凡具有环状离域旳π电子云(平面环状共 轭体系),且该电子云旳p电子数符合 4n+2规则旳化合物就叫做芳香族化合物。
4n+2规则又叫做休克尔规则
三、苯旳构造表达法:
历史的原因
仍被采用
现实的——
越来越多被采用。
H
H
CC
H C 120o C
120o C C
H
H
140pm
H
108pm
苯衍生物旳命名法
CH3
Cl
甲苯
H CH3
6
顺反异构(5和6, 5和7)因成环碳原 子单键不能自由旋 转而引起旳。
H3C H
7
旋光异构 (6和7)
2、单环烃旳命名
(1)在相应烷烃名称前加“环”字,称为 “环某烷”
(2) 使全部取代基编号尽量小;
(3)有不饱和键时, 以不饱和键旳编号最小
CH3
5 6 1 CH3 4 3 2 CH3
因为角张力作用,使得环丙烷分子稳定性下降, 轻易发生加成反应使环打开
环丙烷旳构造
104o HH
C
HC H
CH H
角张力(angle strain):
环旳角度与sp3轨道夹 角差别引起旳张力
H3 H
H
2
H
H
1
H
C1-C2
H3 H
2
H H
1 HH
Newman投影式
全部C-H 键均为重叠式构 象,有扭转张力p19
4、环烃旳化学性质
(一)大环,中环化合物旳化学性质与链烷烃相同。 (二)特殊旳性质:小环不稳定,轻易开环发生加 成反应,五元环和六元环则较稳定。
小环和一般环化合物旳性质对例如下:
有机化学陈洪超编第四章环烃

4
椅式
交叉式,优势构象
3
1
5
2
4
6
船式 重叠式
2.椅式构象中的直立键和平伏键
在椅式构象中的12个C-H键可分为两种类型, 一类是垂直于环平面,称为直立键或a键 (axial bond); 另一类大致于环平面平行,称为平伏键或e键 (equatorial bond)。 每个碳上有1个a键和1个e键,6个a键上下交 替排列,同样,6个e键也是上下交替排列, 注意画法(板书)。
定,常温下即便是三元环也不与高锰酸钾 反应。
+ KMnO4
不反应
可与烯烃或炔烃区别开来。
应用: 鉴别不饱和烃和小环
四、环烷烃的稳定性
环的稳定性顺序:
,
•现代价键理论指出:当两原子轨道(电子 云)重叠成键时,要求键角与其轨道的角 度相匹配。匹配越好(接近正常键角), 重叠程度越大,键越牢固。
•σ键是原子的轨道沿键轴方向“头碰头” 重叠,重叠程度最大,最稳定;π键是 “肩并肩”重叠,重叠程度最小,最不稳 定。
CH3
1,2-二甲苯 邻-二甲苯 O-二甲苯
CH3
1,3-二甲苯 间-二甲苯 m-二甲苯
4-氯甲苯 对-氯甲苯 p-氯甲苯
CH3 CH(CH3)2
C(CH3)3
CH3CHCH2CHCH3 CH3
1-甲基-2-异丙基-3-叔丁基苯 2-甲基-4-苯基戊烷
C CH
苯乙炔
CH3
CHCH=CH2
CH3
3-(间-甲苯基)-1-丁烯
H H
H
H H
H
Benzene
Electron Density
Kekule`
Summary:
有机化学课件-第四章环烃

1,7-二甲基双环[3.2.2]壬烷
例6:
8,8-二甲基双环[3.2.1]辛烷
例7: 双环[2.2.2]-2,5,7-辛三烯
4.1.3 环烷烃的性质
(一) 物理性质 • 环烷烃的熔点和沸点都比相应的烷烃要高一些. • 相对密度也比相应的烷烃高,但比水轻. (二) 化学性质 • 脂环烃的化学性质与相应的脂肪烃类似. • 具有环状结构的特性
•顺式异构体--不稳定.
• --环下方几个 a 键上的氢原子比较靠拢,有些拥 挤,故分子能量较高,比较不稳定.
4.2 芳香烃
4.2.1 芳香烃的分类
• 大多数芳香烃含有苯的六碳环结构 , 少数称非苯 芳烃的都具有结构、性质与苯环相似的芳环. • 芳环上 (1)不易发生加成反应,
(2)不易氧化, (3)而容易起取代反应.
有机化学 Organic Chemistry
教材:有机化学(第二版) 赵建庄 张金桐主编 高等教育出版社
第四章 环烃
广东海洋大学应用化学系
4.1 脂环烃 4.1.1 脂环烃的定义 脂环烃-结构上具有环状碳骨架,而性质上与脂 肪烃相似的烃类,总称脂环烃.
环烷烃 CnH2n 环碳原子的饱和程度 环烯烃 脂环烃 单环 (上) 环炔烃 碳环 数目 双环 多环 CnH2n-2 CnH2n-4
桥头碳
双环[2.2.1]庚烷
例2:
二环[2.1.0]戊烷
例3:
二环[3.1.1]庚烷
(d) 环上碳原子编号:从一个桥头碳原子(含)开始,先编 最长的桥至第二个桥头,再编余下的较长的桥,回到 第一个桥头;最后编最短的桥. (e) 编号的顺序以取代基位置号码加和数为较小.
例4: 例5:
6-甲基双环[3.2.2]壬烷
第四章环烃(共68张PPT)

(aa型)
e键取代基多的构象稳定
(ee型)优
1.4 脂环烃的化学性质
催化加氢
1.4.2 与溴的作用
四元环需加热 不与KMnO4反应
鉴别环烷烃(三、四元环)
1.4.2 与氢卤酸的作用 不对称环丙烷符合马氏规则
1.4.3 取代反应
第二节 芳香烃
(aromatic hydrocarbon)
COC3H
CH3COCl AlC3l
CH3 难以进行
b. 烷基化反应,当R≥3时易发生重排;而酰基化反应则不发生重排。
CH(C 3)2H CH 2CH 2CH 3
+ CH 3CH 2CH 2Cl AlC 3 l
+
( 主)
( 次)
+ CH 3CH 2COClAlC 3 l
COC2CHH 3 Zn-Hg
(3) 稠环烃:两个或两个以上苯环共用两个相邻的碳原子。
2.1.3 非苯芳烃:不含苯环,但具有苯的特性“芳香性”的碳环化合物。
2.1.3 非苯芳烃:不含苯环,但具有苯的特性“芳香性”的
碳环化合物。
2.2 苯的结构
2.2.1 苯的分子构型
苯分子六个C和六个H都在同一平面内六个C组成一个正六边
形,碳-碳键长完全相等,所有键角都是120°。 2.2.2 苯分子结构的价键观点
+发烟 HNO3
CH3 浓 H 2SO 4 O 2N
+ HNO3
NO2
NO2
NO3 CH3
NO2
TNT NO2
(2) 卤化反应
注意:第二个卤素原子进入第一个卤素原子的邻、对位。
(3) 磺化
苯磺酸
注意:磺化反应可逆!
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
环丁烷的构象
2.环戊烷的构象
环戊烷分子中,C-C-C夹角为108°,接近sp3杂化轨道间夹 角109.5°,环张力甚微,是比较稳定的环。但若环为平面结构, 则其C-H键都相互重叠,会有较大的扭转张力,所以,环戊烷是 以折叠式构象存在的,为非 平面结构,见右图,其中有 四个碳原子在同一平面,另 外一个碳原子在这个平面之 外,成信封式构象。 环戊烷的构象
环丁烷总张力能为108KJ/mol,环丁烷比环丙烷要稳定些, 。 环戊烷总张力能25KJ/mol,扭转张力在2.5KJ/mol以下,因此, 环戊烷比环丁烷要稳定,环戊烷的化学性质稳定。
二、环丁烷和环戊烷的构象
1.环丁烷的构象 与环丙烷相似,环丁烷分子中存在着张力,但比环丙烷的 小,因在环丁烷分子中四个碳原子不在同一平面上,见右图: 根据结晶学和光谱学的证明, 环丁烷是以折叠壮构象存在的, 这种非平面型结构可以减少C-H 的重叠,使扭转张力减小。环丁 烷分子中 C-C-C键角为 111.5°, 角张力也比环丙烷的小,所以环 丁烷比环丙烷要稳定些,总张力 能为108KJ/mol。
第四章 环 烃
环 烃的分类
环烷烃 脂环烃 环烃 单环烷烃 桥环烷烃 螺环烷烃 集合环烷烃
环烯烃
环炔烃 单环芳烃
芳 烃
多环芳烃
非苯芳烃
ห้องสมุดไป่ตู้
Ⅰ 脂 环 烃
第一节 脂环烃的分类命名和异构现象 一、分类
1.饱和脂环烃 环烷烃 如:( )
不饱和脂环烃 环烯烃 如:( 环炔烃
)
2.环的大小:小环(3~4元);普通环(5~7元); 中环(8~12元)和大环(十二碳以上)。 3. 环的多少:单环;多环(桥环,螺环)。
通式:环烷烃与开链单烯烃相同.环单烯与单炔、二烯烃相同.
二、命名
1.环烷烃的命名 (1)根据分子中成环碳原子数目,称为环某烷。 (2)把取代基的名称写在环烷烃的前面。 (3)取代基位次按“最低系列”原则列出,基团顺序按“次 序规则”小的优先列出。 例如:
2.环烯烃的命名
(1)根据分子中成环碳原子数目,称为环某烯。
这种构象的张力很小,总张力能25KJ/mol,扭转张力在2.5KJ/mol 以下,因此,环戊烷的化学性质稳定。
三、环己烷的构象
在环己烷分子中,六个碳原子不在同一平面内,碳碳键 之间的夹角可以保持109.5°因此环很稳定。 1.两种极限构象——椅式和船式
椅式构象稳定的原因:
船式构象不稳定的原因:
例如:
(2)螺环烃
两个环共用一个碳原子的环烷烃称为螺环烃。 编号原则:从较小环中与螺原子相邻的一个 碳原子开始,徒经小环到螺原子,再沿大环 致所有环碳原子。 命名:根据成环碳原子的总数称为环某烷, 在方括号中标出各碳环中除螺碳原子以外的 碳原子数目(小的数目排前,大的排后),其 它同烷烃的命名。
现代物理方法测定,环丙烷分子中:键角 C-C-C = 105.5°; H-C-H =114°。 所以环丙烷分子中碳原子之间的sp3杂化轨道是以弯曲键(香 蕉键)相互交盖的。
由图可见,环丙烷分子中存在着较 大的张力(角张力和扭转张力), 是一个有张力环,所以易开环,发生 加成反应。 环丙烷的结构图
2.张力学说
在环丙烷分子中,电子云的重叠不能沿着sp3轨道轴对 称重叠,只能偏离键轴一定的角度以弯曲键侧面重叠,形 成弯曲键(香蕉键),其键角为 105.5°,因键角要从 109.5°压缩到105.5°,故环有一定的张力(角张力)。 另外环丙烷分子中还存在着另一种张力——扭转张力 (由于环中三个碳位于同一平面,相邻的C-H键互相处于 重叠式构象,有旋转成交叉式的趋向,这样的张力称为扭 转张力)。 环丙烷的总张力能为114KJ/mol。
2.平伏键(e键)与直立键(a键)
在椅式构象中C-H键分为两类。 第一类六个C-H键与分子的对称轴平行,叫做直立键或a键(其 中三个向环平面上方伸展,另外三个向环平面下方伸展); 第二类六个C-H键与直立键形成接近109.5°的夹角,平伏着向 环外伸展,叫做平伏键或e键。 如下图:
在室温时,环己烷的椅式构象可通过C-C键的转动(而不经 过碳碳键的断裂),由一种椅式构象变为另一种椅式构象,在 互相转变中,原来的a键变成了e键,而原来的e键变成了a键。
当六个碳原子上连的都是氢时,两种构象是同一构象。连有不同 基团时,则构象不同。
3.取代环己烷的构象
一、一元取代环己烷的构象 一元取代环己烷中,取代基可占据a键,也可占据e键,但占 据e键的构象更稳定。例如:
第二节 脂环烃的性质
一 、普通环的性质
普通脂环烃具有开链烃的通性 环烷烃主要是起自由基取代反应,难被氧化。
环烯烃具有烯烃的通性:
二、小环烷烃的特性反应
1.加成反应 (1) 加氢
(2) 加卤素
(3)加H X, H2SO4
2.氧化反应
环丙烷对氧化剂稳定,不被高猛酸钾、臭氧等氧化剂氧化。 例如:
(2)以双键的位次和取代基的位置最小为原则。 当环上有取代基及不饱和键时,不饱和键以最小的号数表示。 例如:
3.多环烃的命名
(1)桥环烃(二环、三环等) 分之中含有两个或多个碳环的多环化合 物中,其中两个环共用两个或多个碳原 子的化合物称为桥环化合物。 编号原则:从桥的一端开始,沿最长桥 编致桥的另一端,再沿次长桥致始桥头, 最短的桥最后编号。 命名:根据成环碳原子总数目称为环某 烷,在环字后面的方括号中标出除桥头 碳原子外的桥碳原子数(大的数目排前, 7,7-二甲基二环[2,2,1]庚烷 小的排后),(如左图)。其它同环烷 烃的命名。
故可用高猛酸钾溶液来区别烯烃与环丙烷衍生物。 环烃性质小结: (1)小环烷烃(3,4元环)易加成,难氧化,似烷似烯。 普通环以上难加成,难氧化,似烷。 (2)环烯烃、共轭二烯烃,各自具有其相应烯烃的通性。
第三节 脂环烃的结构
从环烷烃的化学性质可以看出,环丙烷最不稳定,环丁 烷次之,环戊烷比较稳定,环己烷以上的大环都稳定,这反 映了环的稳定性与环的结构有着密切的联系。 一、 环丙烷的结构与张力学说 1.环丙烷的结构 理论上: 1° 饱和烃,C为sp3杂化,键角为109.5° 2° 三碳环,成环碳原子应共平面,内角为60° (两者自相矛盾 ) 故三元环的结构特殊。
