L天冬氨酸
L-天冬氨酸-α-脱羧酶的分子改造中期报告

L-天冬氨酸-α-脱羧酶的分子改造中期报告L-天冬氨酸-α-脱羧酶是一种重要的生物催化剂,广泛应用于食品、化学、制药等领域。
然而,传统的L-天冬氨酸-α-脱羧酶在使用过程中存在天然来源不足、稳定性差、工业化生产成本高等问题。
因此,对L-天冬氨酸-α-脱羧酶进行分子改造具有重要意义。
本报告共分为三个部分:1)文献综述;2)研究进展;3)研究计划。
1)文献综述目前,对L-天冬氨酸-α-脱羧酶的分子改造主要采用以下几种方法:突变、重组、化学修饰和蛋白质工程。
其中突变和重组是常用的方法。
通过突变法,可以改变酶分子内的氨基酸结构,增强酶的催化效率和稳定性。
常见的突变方法包括随机突变、定点突变和基于理性设计的突变。
重组技术可以获得更具优良特性的L-天冬氨酸-α-脱羧酶,例如,在通量、活性、特异性和特异之间寻找平衡。
2)研究进展目前,对L-天冬氨酸-α-脱羧酶的分子改造主要集中在以下几个方面:1. 提高L-天冬氨酸-α-脱羧酶空间构象的稳定性和松弛度,增强其催化特性;2. 通过基因工程打造新型L-天冬氨酸-α-脱羧酶以改进特定应用特性,例如,快速碳裂解蛋白酶和变性酶;3. 通过分子对接技术预测突变位点的稳定性和活性,加强基因突变技术的预测性;4. 通过蛋白结构研究深入解析L-天冬氨酸-α-脱羧酶的结构的不同层面,例如酶动力学、稳定性等,以获得更好的酶特性。
3)研究计划我们将继续研究基于理性设计的新型L-天冬氨酸-α-脱羧酶。
首先,通过分子对接和动力学模拟技术,筛选出使酶分子更加稳定,提高催化效率的突变位点;其次,通过重组技术,设计出适用于特定应用场景的L-天冬氨酸-α-脱羧酶,如:高温、低温反应条件下的酶等。
最后,在应用研究中,将对酶催化特性进行实验分析,并对其应用进行优化和验证。
总之,这项研究将为提高L-天冬氨酸-α-脱羧酶的催化效率、增强L-天冬氨酸-α-脱羧酶的稳定性以及应用于工业化生产提供新的思路和方法。
氨基酸英文缩写记忆方法

氨基酸英文缩写记忆方法
记忆氨基酸英文缩写时,可以采用以下方法:
理性记忆法:借助关键字汉语拼音,瞬间记住5个氨基酸。
例如,天冬氨酸或天门冬氨酸,就记成冬氨酸即可,D 亮 L,脯 (就念成pú吧) P,丝 S,甘 G,暂且记下,属于易混缩写,下一步记住。
死记法:剩下的全部可以借助英语发音,只是英语首字母的缩写而已。
例如,甘氨酸—Gly—G、丙氨酸—Ala—A、缬氨酸—Val—V、亮氨酸—Leu—L、异亮氨酸—Ile—I、脯氨酸—Pro—P、丝氨酸—Ser—S、苏氨酸—Thr—T、半胱氨酸—Cys—C、蛋氨酸/甲硫氨酸—Met—M、组氨酸—His—H、天冬氨酸—Asp—D、天冬酰胺—Asn—N、谷氨酰胺—Gln—Q、谷氨酸—Glu—E、赖氨酸—Lys—K、精氨酸—Arg—R、苯丙氨酸—Phe—F、色氨酸—Trp—W、酪氨酸—Tyr—Y。
以上方法仅供参考,可以查阅生物书籍或询问专业人士,以获取更多氨基酸英文缩写记忆方法。
L-天冬氨酸对肾上腺素电子转移性能的影响

文章编号:1673-2103(2008)03-0001-04L -天冬氨酸对肾上腺素电子转移性能的影响3赵春晓1,李运输1,郁章玉2(1.曲阜师范大学化学科学学院,山东曲阜273165; 2.菏泽学院,山东菏泽274015) 摘 要:采用循环伏安法研究了肾上腺素在不同pH 的盐酸溶液中,铂电极表面上天冬氨酸与肾上腺素相互作用的电化学行为.实验结果表明,随溶液pH 值的变化和天冬氨酸加入比例的改变,肾上腺素的电化学参数呈现一定的变化规律.关键词:肾上腺素;L -天冬氨酸;循环伏安法;电化学中图分类号:O 646 文献标识码:A 氨基酸是构建生物机体的众多生物活性大分子之一,是构建细胞、修复组织的基础材料.肾上腺素是哺乳动物和人类的一种重要的儿茶酚胺类神经传递物质[1],它控制着神经系统进行一系列生物反应及神经化学过程.研究氨基酸分子与肾上腺素的相互作用,对于推动生命科学、药物化学、物理化学等学科的发展能起到一定的积极作用.本文采用循环伏安法在不同pH 值条件下研究L -天冬氨酸对肾上腺素电子转移性质的影响.1 实验部分1.1 试剂和仪器CH I 650电化学工作站(上海辰华仪器公司产品),DELT A320pH 计(梅特勒-托利多(上海)有限公司产品),K Q -100B 型超声波清洗器(昆山超声仪器有限公司产品),肾上腺素(瑞士Fluka 试剂,质量分数�97%),L -天冬氨酸,盐酸溶液,所用试剂均为分析纯.1.2 实验测试系统本实验采用三电极体系,铂电极为工作电极,铂片为对电极,饱和甘汞电极作为参比电极.本文所有的电位数据均相对于该参比电极,参比部分与研究部分用盐桥隔开.盐酸溶液作为研究介质,由于溶液的离子强度对肾上腺素的电氧化反应有较大影响,因此在配制不同pH 值的盐酸溶液时均用氯化钠恒定离子强度为0.5.因为肾上腺素容易被氧化,所以在配制溶液前先用高纯氮气去除底液中的溶解氧,并在测试前通氮气10m in .整个过程均在氮气氛中完成.每次循环伏安扫描前,铂电极依次在4#、6#金相砂纸上打磨,再用二次蒸馏水冲洗电极表面.实验用水为二次蒸馏水,实验温度为室温.2 结果与讨论2.1 肾上腺素在不同pH 的盐酸溶液中的电化学性质肾上腺素在电化学活化铂电极(即预处理铂电极[2])上不同pH 的中的循环伏安曲线见图1.由图1 I =0.5的HCl -NaCl 溶液中2.0×10-3mol/L肾上腺素在不同pH 值下铂电极上的循环伏安图F i g .1 C yc li c voltamm ogram s of 2.0×10-3m ol/La dr ena li n e i n hydr och l or i c a c id an d sod i um ch lor i deof d iffer en t pH a nd I 0.5a t pl a ti num electr ode pH:(a )0.3;(b)0.9;(c)1.5;(d)1.8;(e)2.0v:50m V /s56第30卷第2期Vol .30 No .2 菏泽学院学报Journal of H eze University 2008年3月Ma r . 20083收稿日期:2008-02-20基金项目山东省博士后创新项目();菏泽学院博士基金资助项目()作者简介赵春晓(),女,山东淄博人,在读硕士研究生,研究方向生物电化学郁章玉(6),男,山东临沂人,教授,博士,硕士研究生导师,研究方向功能性物质的电子转移性质:200702020200701:1979-:.190-:.图1可见,出现了2个峰.峰1对应的反应为肾上腺素电氧化为肾上腺素醌的的反应,峰2对应着其逆反应.随着pH 值的增大,峰1电位正移,峰2电位负移,峰电位差变大,其可逆程度降低.2.2 L -天冬氨酸对肾上腺素电化学性质的影响肾上腺素在不同比例L -天冬氨酸条件下的循环伏安曲线见图2.由图2可知,L -天冬氨酸的加入仅是对肾上腺素电氧化还原反应的伏安参数的大小有影响,但对反应特征没有影响.循环伏安曲线上没有出现新的氧化还原峰,只是随天冬氨酸的加入峰电位差逐渐增大,峰电流逐渐减小.这表明L -天冬氨酸没有改变肾上腺素电极反应的机理,其反应仍是一对准可逆的氧化还原反应,但使肾上腺素电化学反应能力降低.图2 pH =1.5,I =0.5的HCl -NaCl 溶液中2.0×10-3mol/L 肾上腺素与天冬氨酸不同比例下在铂电极上的循环伏安图F i g .2 C yclic voltamm ogr am s of 2.0×10-3m ol/La drena li ne and a s pa r t i c a c i d with d iffer en tconcen tra ti on i n hydrochlor ic a c i d an d sod iu mch lor i de of pH 1.5a nd I 0.5a t p l a t i num e lectr odec A :(a )0;(b)2.0×10-3;(c)4.0×10-3;(d)6.0×10-3;(e)8.0×10-3m ol/L v:50m V/s为了进一步明确pH 变化和加入天冬氨酸比例的变化对肾上腺素电子转移性能的影响,故做pH -i p a 图、pH -ΔE 图,如图3、图4所示.由图可知,在相同的pH 值条件下,随着加入的天冬氨酸比例的增大,氧化峰电位E pa 正移,还原峰电位E p c 负移,电位差ΔE =E pa -E pc 增大,氧化峰电流i p a,还原峰电流i p c 均逐渐减小.究其原因,这可能是由于肾上腺素含有醇羟基、酚羟基、氨基等功能基团,其性能容易受到微环境的影响[2],且由于肾上腺素含有这些官能团,比较容易与含有氧、氮的物质形成氢键复合物,从而对肾上腺素的电化学性能产生影响L 天冬氨酸为含有N 、O 原子共轭体系的杂环化合物,由此可以推测,天冬氨酸加入到体系图3 铂电极上肾上腺素电氧化峰1的i pa -pH 图F i g3 D ependen ce of i pa o n pH for a drena li nee lectr ooxida ti on c A :(■)0;(●)2.0×10-3;(▲)4.0×10-3;(★)6.0×10-3;(◆)8.0×10-3m ol/Lv:50m V /s图4 ΔE -pH 的关系曲线F i g4 D ependen ce of ΔE on pH for a dr ena li n ee letr oox i da ti onc A :(■)0;(●)2.0×10-3;(▲)4.0×10-3;(★)6.0×10-3;(◆)8.0×10-3m ol/L v:50m V /s中,与肾上腺素发生了相互作用,形成了超分子体系[3],对肾上腺素的羟基起到了一定的保护作用,使其难以游离出H +发生氧化反应.由图还可看出,加入天冬氨酸后,随着pH 值的增大,电位差逐渐增大,峰电流逐渐减小.这是因为随着pH 值的增大溶液中天冬氨酸H 3N +—R —CO OH 的形式逐渐减少,而H 3N +—R —COO -的形式逐渐增多[4],肾上腺素在酸性溶液中以质子化的形式存在,相对于中性的氨基酸偶极离子来说,对酸性离子的排斥作用更大,所以随着pH 值的增大,肾上腺素更易于与天冬氨酸结合生成超分子化合物.而肾上腺素在不同酸度的盐酸溶液中,随着pH 值的增大,电位差增大,峰电流减小,这与王磊的研究结果一致[5],表明肾上腺素电氧化还原反应能力与介质的值相关,这662008年 菏泽学院学报 第2期.-pH可能是由于酸性越高,肾上腺素质子化程度越强,使得肾上腺素上的酚羟基更有利于接近电极表面发生电子转移反应.3 结论 随着pH 值的增大,肾上腺素电氧化还原反应能力降低.在溶液中,L -天冬氨酸能与肾上腺素生成氢键超分子化合物,抑制肾上腺素的电氧化,并且随着pH 值的增大,肾上腺素更易于与天冬氨酸结合生成超分子化合物,其抑制作用更强.参考文献:[1] 张占军,李经建,吴锡尊,等.肾上腺素电氧化过程的快速扫描循环伏安研究[J ].物理化学学报,2001,17:542-546.[2] 郁章玉.肾上腺素电子转移性能及微环境效应的研究[D ].北京:中国科学院研究生院,2004.[3] Little C M ,Ange l osM G,Pa radis N pared t o an 2gi otensin II,epinephri ne is ass oc iated with high myocar 2di a l bl ood fl ow foll o wing re turn of s pontaneous c ircula ti on aft e r ca rdiac arrest [J ].Re s usc itati on,2003,59(3):353-359.[4] 赵殊,刘本才,廖蓉苏.氨基酸在水溶液中的行为[J ].东北林业大学学报,2004,32(4):105-107.[5] 王磊.生物小分子与肾上腺素相互作用的伏安特性及理论研究[D ].曲阜:曲阜师范大学,2006.The I nfluence of Aspar ti c Aci d on Electr on Tran s ferProper ti es of Adr ena li nZHAO Chun -xiao 1,L I Yun -shu 1,Y U Zhang -yu2(1.Depart ment of Che m istry ,Qufu Nor m al Univeisity,Qufu Shandong 273165,China;2.Heze Un i ve rsity,Heze Shandong 274015,China )Abstra ct:The influence of as pa rtic acid on electr on transfer pr ope rties of adr enaline wa s investigated by cyclicvolta mm etr y in hydr ochl oric ac id soluti on of vari ous pH a t a p latinum elec tr ode.The cyclic volta mmogra m s exhibit different potential diff e r ence and diff e r ent peak currents in serie s of various pH hydr oche m ical ac id s olution.A s the pH of the solution incr eased,the f or m of a s partic ac id changed,the ani on reduced,the di polar ion increased .The reacti on of adr enaline with aspa rtic ac id ani on was easier than its dipolar i on.A s a result,the changes of peak po 2tential and peak current were diff e r ent.Key wor ds:adrena line;a s partic ac id;cyclic v oltamm etr y;electr oche m istry(上接第39页)The Ag ile D evelopm en t of the D e m on stra te Systemof A lgor ithm Ba sed on Scr iptHUANG Fu -xian(Co mputer and Informati on Enginee ring Depa rt m ent,Heze Uni ve rsit y,Heze Shandong 274015,China )Abstra ct:Thr ough the analysis on principle of the demonstrate syste m t o the a lgorithm ,this paper designs a kind of si mp le scri pt ,p r ovides the design syste m based on script ,and the course and m ethod on agile devel op 2m ent is discussed.K y ;;y ;62008年 赵春晓,等:L -天冬氨酸对肾上腺素电子转移性能的影响 第2期e wor ds:de monstr a te scri p t data structure a lg orith m de monstrate s ste m agile dev e l ope ment7。
天门冬氨酸

天门冬氨酸百科名片分子式天冬氨酸又称天门冬氨酸,是一种α-氨基酸,天冬氨酸的L-异构物是20种蛋白胺基酸之一,即蛋白质的构造单位。
它的密码子是GAU和GAC。
它与谷氨酸同为酸性氨基酸。
天冬氨酸普遍存在于生物合成作用中。
它是生物体内赖氨酸、苏氨酸、异亮氨酸、蛋氨酸等氨基酸及嘌呤、嘧啶碱基的合成前体。
它可作为K+、Mg+离子的载体向心肌输送电解质,从而改善心肌收缩功能,同时降低氧消耗,在冠状动脉循环障碍缺氧时,对心肌有保护作用。
它参与鸟氨酸循环,促进氧和二氧化碳生成尿素,降低血液中氮和二氧化碳的量,增强肝脏功能,消除疲劳。
目录一般信息基本性质主要用途一般信息天门冬氨(aspaitic acid ,三字母缩写为Asp,一字母缩写为D)酸化学名称为L-(+)-氨基丁二酸,分子式为C4H7NO4分子量为133.10,本品为白色结晶或白色结晶性粉末;味微酸;在热水中溶解,在水中微溶,在乙醇中不溶,在稀天门冬氨酸盐酸及氢氧化钠溶液中易溶。
L-天门冬氨酸为酸性氨基酸之一,属非必需氨基酸,在体内由谷氨酸转氨给草酰乙酸而得,分解则通过脱氨基生成草酰乙酸或经天冬氨酸酶的作用脱氨生成丁烯二酸CTA循环。
它是生物体内赖氨酸、苏氨酸、异亮氨酸、蛋氨酸等氨基酸及嘌呤、嘧啶碱基的合成前体。
它可作为K+、Mg+离子的载体向心肌输送电解质,从而改善心肌收缩功能,同时降低氧消耗,在冠状动脉循环障碍缺氧时,对心肌有保护作用。
它参与鸟氨酸循环,促进氧和二氧化碳生成尿素,降低血液中氮和二氧化碳的量,增强肝脏功能,消除疲劳基本性质作为一类化学物质,天冬氨酸的通式决定了它们具有一些共有的基本性质。
首先,天冬氨酸是小分子物质,分子量没有超过1000。
另外,天冬氨酸熔点在230℃以上,没有确切的熔点,熔融时分解并放出CO2;都能溶于强酸和强碱溶液中;天冬氨酸均溶于水,难溶于乙醇和乙醚。
能与酸结合成盐,也能与碱结合成盐。
从天冬氨酸的结构可以看出,由于天冬氨酸的分子中有不对称的碳原子,所以具有旋光性。
天冬氨酸的功能

天冬氨酸(Aspartic acid)是一种重要的氨基酸,在人体内具有多种功能,包括:
1. 改善心肌缺血和心功能:天冬氨酸能够促进心肌细胞的代谢,增加心肌细胞对葡萄糖的利用,从而改善心肌缺血和心功能。
2. 调节血糖:天冬氨酸能够促进肝脏的糖代谢,增加肝脏对葡萄糖的利用,从而调节血糖。
3. 改善肝功能:天冬氨酸参与鸟氨酸循环,促进氨和二氧化碳生成尿素,降低血液中氮和二氧化碳的量,增强肝脏功能,消除疲劳。
4. 促进蛋白质的合成:天冬氨酸是蛋白质合成的重要前体,能够促进蛋白质的合成。
5. 维持神经系统的正常生理活动:天冬氨酸能够维持神经系统的正常生理活动,起到调节神经系统的作用。
此外,天冬氨酸还是一种重要的营养添加剂和食品添加剂,常用于制作氨基酸输液、甜味剂等。
然而,过量摄入天冬氨酸可能会引起腹泻等副作用,因此在使用时应适量控制。
如果有任何健康问题或疑虑,建议咨询专业医生或营养师的建议。
n-乙酰-l-天冬氨酸分子式c5h9no3s

乙酰-L-天冬氨酸(N-acetyl-L-aspartate)是一种天然存在的化合物,分子式为C5H9NO3S。
它在人体中具有重要的生物学功能,广泛存在于中枢神经系统和外周组织中。
乙酰-L-天冬氨酸作为一种代谢产物,对于神经元的代谢活动和神经保护具有重要意义。
以下是有关乙酰-L-天冬氨酸的一些相关内容。
一、乙酰-L-天冬氨酸的结构特征乙酰-L-天冬氨酸是一种天然存在的氨基酸衍生物,其结构特征如下:1. 分子式:C5H9NO3S2. 分子量:175.19 g/mol3. 结构:乙酰-L-天冬氨酸由L-天冬氨酸和乙酰CoA经催化作用形成,含有一个乙酰基团。
二、乙酰-L-天冬氨酸在中枢神经系统中的作用乙酰-L-天冬氨酸在中枢神经系统中起着重要的代谢和信号传导作用,具体表现在以下几个方面:1. 能量代谢:乙酰-L-天冬氨酸参与神经元的能量代谢过程,对神经元的正常功能和存活起着重要作用。
2. 代谢标志物:乙酰-L-天冬氨酸的水平变化与许多神经系统疾病和损伤有关,因此被认为是一种重要的神经代谢标志物。
3. 神经保护:乙酰-L-天冬氨酸可通过多种途径对神经元的保护起到作用,具有一定的神经保护作用。
三、乙酰-L-天冬氨酸与神经系统疾病的关系乙酰-L-天冬氨酸在许多神经系统疾病的发生发展过程中起着重要作用,下面以几种常见的神经系统疾病为例,说明其与乙酰-L-天冬氨酸的关系:1. 脑卒中:研究表明,脑卒中患者乙酰-L-天冬氨酸的代谢水平明显下降,与脑损伤程度密切相关。
2. 癫痫:癫痫发作时乙酰-L-天冬氨酸水平显著升高,成为癫痫发作的生物标志。
3. 脑肿瘤:乙酰-L-天冬氨酸在脑肿瘤的诊断和生物学监测中具有重要意义,可作为肿瘤生长的生物标志。
四、乙酰-L-天冬氨酸的检测方法为了更好地研究和了解乙酰-L-天冬氨酸在生物体内的作用和意义,科学家们发展了多种检测乙酰-L-天冬氨酸的方法,主要包括:1. 液质联用技术(LC-MS):利用液相色谱联用质谱技术,可以对乙酰-L-天冬氨酸进行高效准确的检测。
l-天冬氨酸的化学合成法

l-天冬氨酸的化学合成法
天冬氨酸是一种非必需氨基酸,可以通过化学合成的方式来制备。
天冬氨酸的化学合成法主要有以下几种方法:
1. Strecker合成法,这是一种经典的合成方法,通过氨基酸、醛和氰化物的反应来合成天冬氨酸。
首先,氰化物和醛反应形成氨
基酰亚胺,然后氨基酸对氨基酰亚胺进行水解得到天冬氨酸。
2. Enantioselective合成法,利用手性催化剂或手性试剂来
实现对映选择性合成。
这种方法可以得到具有特定立体构型的天冬
氨酸。
3. 氨基酸衍生物合成法,利用氨基酸的衍生物进行化学反应来
合成天冬氨酸。
例如,可以利用苯甲醛和亚硝酸钠反应制备对硝基
苯甲醛,再经过一系列反应合成天冬氨酸。
4. 巯基合成法,通过巯基反应合成天冬氨酸。
巯基化合物与醛
类化合物反应生成巯基醇,再通过氧化反应得到天冬氨酸。
总的来说,天冬氨酸的化学合成法有多种途径,可以根据具体
需要选择合适的方法进行合成。
这些方法都需要在严格的实验条件下进行,并且需要对反应物和产物进行精确的分析和纯化,以确保合成产物的纯度和产率。
希望这些信息能够满足你的需求。
L 天冬氨酸

英文同义词
ASP;ASPARTIC(L-);ASPARTIC ACID;ASPARTIC ACID, L-;H-ASP-OH;FEMA 3656;H-L-ASP-OH;L-ALPHAAMINOSUCCINIC ACID
物化性质
呈白色结晶或结晶性粉末,味微酸。溶于沸水,25℃时微溶于水 (0.5%),易溶于稀酸和氢氧化钠溶液中, 不溶于乙醇、乙醚、加热至270℃分解,等电点2.77,其比旋度与所溶的溶剂有关。在酸溶液中为右旋,碱溶液 中为左旋,水溶液中为右旋 。
L 天冬酸
化学品
目录
01 英文同义词
03 产品用途
02 物化性质 04 生产方法
L-天冬氨酸是一种有机化合物,化学式为C4H7NO4。白色结晶或结晶性粉末,味微酸。溶于沸水,25℃时微 溶于水 (0.5%),易溶于稀酸和氢氧化钠溶液中,不溶于乙醇、乙醚、加热至270℃分解,等电点2.77,其比旋度 与所溶的溶剂有关。在酸溶液中为右旋,碱溶液中为左旋,水溶液中为右旋。
三、用于合成甜味剂,医药上用于治疗心脏病,用作肝功能促进剂、氨解毒剂、疲劳消除剂和氨基酸输液成 分等。
四、营养增补剂、调昧增香剂。添加于各种清凉饮料。医药上用作氨解毒剂、肝功能促进剂、疲劳恢复剂。
五、用于生化研究,用作疲劳恢复剂、氨解毒剂、临床诊断药。
生产方法
左旋天冬氨酸的制法有合成法和发酵法。1.合成法主要是以马来酸或富马酸或它们的酯为原料,在加压下用 氨处理,然后水解。较容易合成得到外消旋天冬氨酸,但至今还没有理想的拆分外消旋体的方法。2.发酵法在酶 作用下,将富马酸与氨加成,可高收率地得到产品。采用这种方法只生成左旋体,收率高,因此是工业生产的主 要方法。
感谢观看
产品用途
L天冬氨酸
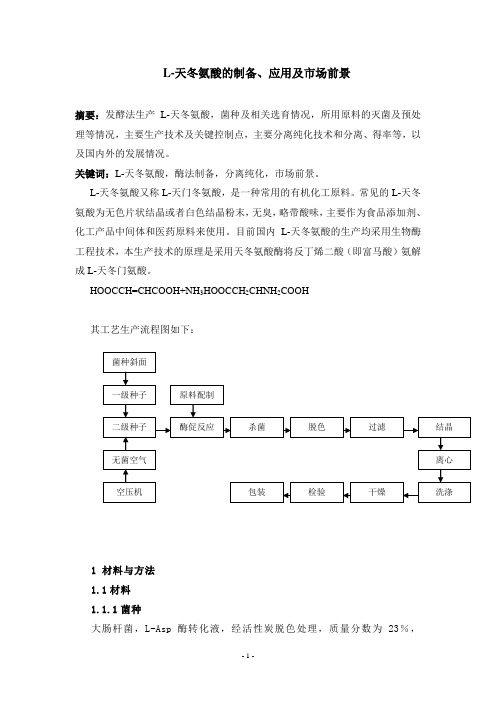
L-天冬氨酸的制备、应用及市场前景摘要:发酵法生产L-天冬氨酸,菌种及相关选育情况,所用原料的灭菌及预处理等情况,主要生产技术及关键控制点,主要分离纯化技术和分离、得率等,以及国内外的发展情况。
关键词:L-天冬氨酸,酶法制备,分离纯化,市场前景。
L-天冬氨酸又称L-天门冬氨酸,是一种常用的有机化工原料。
常见的L-天冬氨酸为无色片状结晶或者白色结晶粉末,无臭,略带酸味,主要作为食品添加剂、化工产品中间体和医药原料来使用。
目前国内L-天冬氨酸的生产均采用生物酶工程技术,本生产技术的原理是采用天冬氨酸酶将反丁烯二酸(即富马酸)氨解成L-天冬门氨酸。
HOOCCH=CHCOOH+NH 3HOOCCH 2CHNH 2COOH其工艺生产流程图如下:1 材料与方法1.1材料1.1.1菌种大肠杆菌,L-Asp 酶转化液,经活性炭脱色处理,质量分数为23%,二级种子 一级种子 杀菌 脱色 酶促反应 原料配制无菌空气 菌种斜面空压机 干燥 洗涤过滤 结晶 离心 检验 包装pH=8.87。
大肠杆菌分离纯化:配置牛肉膏蛋白胨培养基,配置后高压蒸汽灭菌并倒平板,将培养皿放入37℃的恒温培养箱中培养24-48小时,以检查是否灭菌彻底。
确定灭菌完全的培养皿可用平板划线法或稀释涂布平板法接种微生物。
大肠杆菌可从河道污水或者家禽、家畜生活附近的土壤中分离培养获得。
1.1.2培养基斜面养基:蛋白胨6g/L,牛肉膏2g/L氯化钠10g/L,琼脂20g/L,pH7.0。
种子培养基:碳源和氮源成分以及浓度按照实验设定值,硫酸镁0.5g/L,硫酸二氢钾2g/L,氯化钠3.5g/L,pH7.0。
原始种子培养基:富马酸15g/L,玉米浆20g/L,硫酸镁0.5g/L,硫酸二氢钾2g/L,氯化钠3.5g/L,pH7.0。
转化培养基:富马酸氨溶液,pH8.5。
1.1.3仪器与试剂分光光度计,恒温振荡器,阳离子交换树脂,自动旋光仪,数字熔点仪,离心机。
我国L天冬氨酸生产方法分析

我国L天冬氨酸生产方法分析提示:我国L-天冬氨酸生产方法分析,首先利用少根根霉(RhizopusarrhizusA.Fisch)发酵产生反丁烯二酸,再接种普通变形杆菌(ProteusvulgarisHauser)发酵生产L-天冬氨酸。
发酵法是早期工业化生产L-天冬氨酸的主要方法,其生产周期长,副产物多,生产成本较高且技术风险大,限制了当时的L-天冬氨酸产品仅应用于医药领域。
导读:我国L-天冬氨酸生产方法分析,首先利用少根根霉(RhizopusarrhizusA.Fisch)发酵产生反丁烯二酸,再接种普通变形杆菌(ProteusvulgarisHauser)发酵生产L-天冬氨酸。
发酵法是早期工业化生产L-天冬氨酸的主要方法,其生产周期长,副产物多,生产成本较高且技术风险大,限制了当时的L-天冬氨酸产品仅应用于医药领域。
L-天冬氨酸生产始于20世纪60年代,日本田边制药公司利用反丁烯二酸发酵技术率先实现了工业化生产,之后,又在固定化技术的基础上研发出固定化大肠杆菌细胞法连续生产L-天冬氨酸。
1973年,Chibata 等从大肠杆菌中提取天门冬氨酸酶,包埋在交联聚丙烯酰胺中制成固定化酶,催化富马酸和氨合成L-天冬氨酸。
1985年,日本三菱石油化学公司利用黄色短杆菌(BrevibacteriumflavumOkumuraetal.)游离细胞将富马酸转化为L-天冬氨酸。
20世纪80年代初,我国开始研制生产L-天冬氨酸,80年代中期采用固定化细胞法进行了生产中试,随后进行了工业化生产。
由于固定化细胞法工艺设备投入多,技术要求高,产品的生产成本相对较高。
随着市场竞争的日趋激烈,2000年,王雪根等研制出游离整体细胞法替代固定化细胞法工业化生产L-天冬氨酸,简化了工艺流程,降低了生产成本,而且减少了对环境的污染。
到目前为止,工业化生产L-天冬氨酸的主要方法包括:传统发酵法、固定化酶或固定化细胞法和游离整体细胞法。
L-天冬氨酸α-脱羧酶基因的功能鉴定及酶学性质研究

L-天冬氨酸α-脱羧酶基因的功能鉴定及酶学性质研究L-天冬氨酸α-脱羧酶(PanD)作为泛酸合成途径中的重要调控酶,可以特异性催化L-天冬氨酸脱掉α羧基,生成具有高价值的β-丙氨酸,由L-天冬氨酸生物法生产β-丙氨酸极具工业化潜能。
目前对PanD的研究存在着PanD重组酶基因来源有限、自剪切机制不清晰等问题,此外已发现的PanD普遍存在底物依赖性失活现象,限制了其工业化应用。
本文选择不同来源的panD基因在大肠杆菌(Escherichia coli)中异源表达,并考察了纯化后的PanD的自剪切情况、酶学性质以及底物失活速率。
选择NCBI panD基因库中42种尚未有研究报道的panD基因和2种已发现具有酶制剂开发潜力的panD基因(谷氨酸棒杆菌Corynebacterium glutamicum、枯草芽孢杆菌Bacillus subtilis),按照E.coli的密码子偏好性优化后,连接到pET28a(+)载体上,然后在E.coli BL21(DE3)中重组表达,构建了44株重组菌。
利用亲和层析纯化获得相应的重组酶并比较其活力,发现有6种PanD与C.glutamicum PanD、B.subtilis PanD一样具有较高的比酶活。
不同来源panD 基因转录翻译后自剪切情况可以分为几乎未裂解、部分裂解和基本完全裂解三类。
自剪切程度直接影响到酶的活力,孵育可以促进酶裂解成熟,但对酶活的提高并不显著。
氨基酸序列亲缘性越近,其自剪切情况也基本相似。
研究表明底物L-天冬氨酸对Pan D具有抑制作用,底物浓度越高,抑制作用越强。
在底物浓度固定的情况下,剩余酶活与时间呈一级反应关系。
测定重组酶的失活速率发现,通常情况下,重组酶的酶活越高,底物失活速率越大。
其中杰氏棒杆菌(Corynebacterium jeikeium)来源的PanD的比酶活可达11.8 U·mg-1,是目前报道的最高水平;单核增生李斯特菌(Listeriamonocytogenes)来源的PanD不仅酶活较高(8.9 U·mg-1),而且底物失活速率较小,为2.071×10-3 min-1,故对这两种来源的重组酶的酶学性质、底物转化能力进行了比较分析。
天冬氨酸的等电点

天冬氨酸的等电点
答案:天冬氨酸的等电点是2.77
分析:天冬氨酸(Aspartic Acid)又称天门冬氨酸,是一种α-氨基酸,其化学式为HOOCCH2CH(NH2)COOH。
天冬氨酸的L-异构物是20种蛋白胺基酸之一,即蛋白质的构造单位。
它的密码子是GAU和GAC。
天门冬氨酸,它与谷氨酸同为酸性氨基酸。
天冬氨酸普遍存在于生物合成作用中。
天门冬氨酸化学名称为L-(+)-氨基丁二酸,分子式为C4H7NO4分子量为133.10,本品为白色结晶或白色结晶性粉末;味微酸;在热水中溶解,在水中微溶,在乙醇中不溶,在稀盐酸及氢氧化钠溶液中易溶。
L-天门冬氨酸为酸性氨基酸之一,属非必需氨基酸,在体内由谷氨酸转氨给草酰乙酸而得,分解则通过脱氨基生成草酰乙酸或经天冬氨酸酶的作用脱氨生成丁烯二酸CTA循环。
它是生物体内赖氨酸、苏氨酸、异亮氨酸、蛋氨酸等氨基酸及嘌呤、嘧啶碱基的合成前体。
它可作为K+、Mg+离子的载体向心肌输送电解质,从而改善心肌收缩功能,同时降低氧消耗,在冠状动脉循环障碍缺氧时,对心肌有保护作用。
它参与鸟氨酸循环,促进氧和二氧化碳生成尿素,降低血液中氮和二氧化碳的量,增强肝脏功能,消除疲劳。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
L-天冬氨酸的制备、应用及市场前景摘要:发酵法生产L-天冬氨酸,菌种及相关选育情况,所用原料的灭菌及预处理等情况,主要生产技术及关键控制点,主要分离纯化技术和分离、得率等,以及国内外的发展情况。
关键词:L-天冬氨酸,酶法制备,分离纯化,市场前景。
L-天冬氨酸又称L-天门冬氨酸,是一种常用的有机化工原料。
常见的L-天冬氨酸为无色片状结晶或者白色结晶粉末,无臭,略带酸味,主要作为食品添加剂、化工产品中间体和医药原料来使用。
目前国内L-天冬氨酸的生产均采用生物酶工程技术,本生产技术的原理是采用天冬氨酸酶将反丁烯二酸(即富马酸)氨解成L-天冬门氨酸。
HOOCCH=CHCOOH+NH 3HOOCCH 2CHNH 2COOH其工艺生产流程图如下:1 材料与方法1.1材料1.1.1菌种大肠杆菌,L-Asp 酶转化液,经活性炭脱色处理,质量分数为23%,二级种子 一级种子 杀菌 脱色 酶促反应 原料配制无菌空气 菌种斜面空压机 干燥 洗涤过滤 结晶 离心 检验 包装pH=8.87。
大肠杆菌分离纯化:配置牛肉膏蛋白胨培养基,配置后高压蒸汽灭菌并倒平板,将培养皿放入37℃的恒温培养箱中培养24-48小时,以检查是否灭菌彻底。
确定灭菌完全的培养皿可用平板划线法或稀释涂布平板法接种微生物。
大肠杆菌可从河道污水或者家禽、家畜生活附近的土壤中分离培养获得。
1.1.2培养基斜面养基:蛋白胨6g/L,牛肉膏2g/L氯化钠10g/L,琼脂20g/L,pH7.0。
种子培养基:碳源和氮源成分以及浓度按照实验设定值,硫酸镁0.5g/L,硫酸二氢钾2g/L,氯化钠3.5g/L,pH7.0。
原始种子培养基:富马酸15g/L,玉米浆20g/L,硫酸镁0.5g/L,硫酸二氢钾2g/L,氯化钠3.5g/L,pH7.0。
转化培养基:富马酸氨溶液,pH8.5。
1.1.3仪器与试剂分光光度计,恒温振荡器,阳离子交换树脂,自动旋光仪,数字熔点仪,离心机。
1.2方法1.2.1培养条件培养温度为37℃培养时间为26h左右1.2.2酶反应取一环生长良好的斜面种子装于有30mL种子培养液的250mL培养摇瓶中,37℃、180r/min下恒温摇床培养16h得到种子液。
取种子液10mL,在5000r/min下离心10min,用生理盐水冲洗2~3次,加入100mL富马酸氨溶液,在温度为37℃、转速为180r/min的条件下进行酶转化反应,用HPLC 测定反应液中富马酸含量,待富马酸含量降至较低值时需加底物溶液,直到转化速度较慢时结束反应。
1.2.3产物的分离因为L-谷氨酸脱羧酶能专一的催化L-谷氨酸脱羧生成γ-氨基丁酸和二氧化碳而L-天冬氨酸不被作用,可用L-谷氨酸脱羧酶分离L-谷氨酸和L-天冬氨酸。
在100mL三角瓶中加入湿菌体,0.5g,混合物0.6g,0.2mol/L醋酸缓冲液(pH=5.0)30mL吐温-80 0.01g,于35℃,170r/min震荡反应30min。
取2mL反应液,添加0.2mol/L硼酸缓冲液(pH=9.0)2mL,使酶反应终止,离心去除菌体。
以berthelot显色法测定转化液中的γ-氨基丁酸。
比活定义为在35℃,pH=5.0时1g湿菌体1h所转化产生的γ-氨基丁酸的μmol数,单位为U,1U=1.0μmol/g.h。
1.2.4测定方法菌体生物量的测定通过发酵液OD值体现菌体的生物量,即样品菌液经摇匀后吸取菌液2mL定容于50mL容量瓶中,在640nm波长处测定吸光值。
发酵液OD值与细胞干质量之间的线性关系为Y(干质量)=0.1709xX(OD 值)-0.0042,线性回归因子为0.997。
富马酸含量测定从酶反应中吸取0.4mL,定容于100mL容量瓶中,在280nm处测定吸光值。
依据标准曲线计算出浓度。
L-天冬氨酸定性检测分析(纸层析法)用30cmx28cm层析滤纸,溶剂系统为正丁醇、冰乙酸及水的质量比为4:1:2。
上行展开10~11h,展开至距顶端1~2cm处。
用pH7.5的0.05%的溴酚蓝乙醇溶液显色。
L-天冬氨酸用0.5%的茚三酮溶液显色。
转化率定义在底物富马酸溶液中,底物转化率=(底物初始浓度-底物终止浓度)/底物初始浓度。
1.2.5 L-天冬氨酸的结晶过程加酸量与pH的关系取转化液100mL,恒温于80℃,滴加40%硫酸调节pH,记录pH随加酸量的变化,作pH值变化曲线。
L-天冬氨酸的结晶操作取转化液100mL,恒温于80℃,滴加40%的硫酸调节pH至4.3左右,加入一定量的晶种,再滴加40%硫酸至pH为2.8,控温冷却至室温,过滤,干燥至恒重。
2结果与讨论2.1优化培养基成分的选定目前都是采用富马酸作为直接碳源,蛋白胨、牛肉膏蛋白胨作为直接氮源进行发酵培养L-天冬氨酸的转化菌。
菌体培养--酶形成的过程曲线从斜面上挑取一环菌苔接种到装有50mL培养基的500mL三角瓶中,37℃摇瓶培养,间隔取样,分别测定培养液的OD值、pH、基质富马酸含量及酶活,得到菌体培养。
2.2酶反应温度对富马酸转化量的影响取50mL培养液分别于37℃和50℃温度下进行酶反应。
50℃时开始酶活很高,第1、2d酶反应很快,转化富马酸的量占总量的90%,以后酶反应缓慢,说明50℃时第三天酶开始失活。
而在37℃进行酶反应,前5d反应速度基本不变,第6d酶反应缓慢。
比较底物的转化率,37℃转化率较高,考虑生产成本,选用37℃进行酶反应。
2.3酶的失活情况将50mL培养液于37℃静置放置,每隔1d测其酶活,观察酶的失活情况,见图。
由酶失活曲线可知,当酶处于静置状态时,经4d,酶活剩余40%,第5d,酶活剩30%,第6、7d后,酶活只有20%。
与处于反应状态相比较,可以看出,酶在静置状态失活更快些。
2.4酶浓度、底物浓度对反应速度的影响在50mL培养液中一次性加入底物溶液600mL,此时酶浓度恒定,为e1,定时测定富马酸浓度,计算不同富马酸浓度时的反应速率,可以绘出这一酶反应过程中不同底物浓度和反应速度的关系曲线。
随着反应进行,富马酸浓度降到1%e2时,底物浓度以下的时候再一次加入底物溶液600mL,同样测出酶浓度为e1,和反应速率之间的关系。
3 L-天冬氨酸的生产应用及市场分析3.1生产应用3.1.1作为食品添加剂由于L-天冬氨酸是酸性氨基酸,带有酸味,故可直接作为酸味调节剂。
它有两个羧基,容易生成稳定的天冬氨酸盐,可用于各种食品的营养强化和风味的调节。
如天冬氨酸钠是一种鲜味剂,也可以与呈味核苷酸等并用,且具有解除人体疲劳的特殊功效,在发达国家如日本等正在逐步代替味精。
3.1.2用于合成甜味剂由L-天冬氨酸为主要原料合成的甜味剂阿巴斯甜其作为蔗糖的替代品,用量持续增长。
鉴于阿巴斯甜专利权已到期,使生产成本降低,作为代替蔗糖的首选甜味剂,欧美国家需求劲强。
3.1.3 合成聚天冬氨酸由L-天冬氨酸为主要原料合成的聚天冬氨酸(PASP),属于生物高分子材料,具有很好的生物相容性和降解性,近年来主要应用于水处理剂、化妆品、分散剂、螯合剂、医药、水凝胶、农用化肥等领域。
研究表明,PASP进入环境中可以完全生物降解,属于环境友好型绿色化学品。
尤其从20世纪90年代开始,随着环保意识的增强,该产品逐渐受到世界上各大化学公司的关注。
3.1.4用于合成新药与临床治疗氨基酸衍生物已广泛用作抗肿瘤药物,如N-磷酸乙酰-L-天门冬氨酸是一个天冬氨酸转氨甲酚基酶的过渡状况抑制剂,利用这个抑制剂可中断嘧啶核苷酸的合成途径达到抗肿瘤目的。
以亮氨酸和酯化的天冬氨酸共聚而成的仿天然皮肤的层状伤口裹敷物,包扎伤口后可以不必再解开而成为皮肤的一部分。
天冬氨酸钾、钠在临床上主要作为心脏病治疗药物、肝功能促进剂、氨解毒剂和氨基酸输液成分。
3.2 技术进展L-天冬氨酸的工业化生产始于上世纪七十年代的日本,早期采用传统的微生物发酵法,即以糖类物质为基础原料,通过细胞的新陈代谢来积累产物,再经过适当的提取精制工艺而制成。
由于该工艺生产周期长,副产物多且技术风险大,使产品的生产成本较高,价格的高昂也限制了产品只能应用于医药领域。
随着后来生物酶技术的发展,特别是固定化酶技术研究的不断深入,该产品的生产也逐步向该领域靠近。
到了八十年代,由于采用酶法生产所需的主要原料——富马酸能得以大量廉价生产,故也使得以固定化酶法进行生产的技术被开发出来,并且逐步取代了传统的发酵工艺,成为当时主要的生产方法。
我国在20世纪八十年代中后期开始了对该产品的研制与开发,并且成功地进行了中试,随后也有了小批量的工业化生产,采用的基本上都是固定化酶法生产技术。
该工艺设备投入多,技术要求高,使产品的生产成本相对较高。
随着近年来市场竞争的日趋激烈,怎样降低生产成本,提高产品质量成为了关键;而固定化酶法由于其工艺上的限制,决定了其无法再降低成本。
3 .3市场分析3.3.1 市场需求分析由于L-天冬氨酸主要用在食品添加剂、合成阿斯巴甜、丙氨酸、聚天冬氨酸方面。
而这些产品的市场需求逐年加大,尤其是阿斯巴甜,目前全球有一百多个国家在使用,产量已增至1.8万t/a。
随着肥胖和糖尿病的高发,对低热量食品的需求在加大,加上阿斯巴甜的专利权限已到期,使生产成本降低,作为代替蔗糖的首选甜味剂,欧美国家需求强劲。
3.3.2 国内生产状况我国L-天冬氨酸的生产历史不长,规模化生产的时间在上世纪九十年代中后期,经过十多年的发展,已形成了一定的生产规模,合计年生产能力约在8~10万吨左右,但厂家也是良莠不齐,生产规模在5000吨以上的只有为数不多的几家,其余的都在2000吨以下。
近几年由于L-天冬氨酸的应用范围不断扩大,需求大幅度增长,尤其在合成阿斯巴甜和聚天冬氨酸方面,国际国内需求量的增加导致产量也在逐年增加,有些公司正是看到了其潜在的市场需求,正在积极介入这一领域。
参考文献【1】章燕,徐虹,李莎,L天冬氨酸的清洁提取工艺生物加工过程2007.11 【2】张沙冰L-天冬氨酸的生产应用及市场分析高新技术产业发展【3】吴月,范伟平,欧阳平凯,L-天冬氨酸结晶过程南京化工大学学报【4】唐芳,谭天伟,王芳,L-天冬氨酸转化菌发酵条件的优化北京化工大学学报2003.【5】乐薇,孙晓梅,李步海,大肠杆菌的培养及L-天冬酰胺酶活力的测定中南名族大学学报2003.9【6】盛晓燕,付勇前,李双,徐晴,黄和,利用富马酸发酵废液培养L-天冬氨酸转化菌策略的研究食品科技2010【7】吴晓燕,钱绍松,刘毅,陈然,刘倩,焦庆才,酶法分离制备γ-氨基丁酸和L-天冬氨酸精细化工2005.12【8】徐虹,朱建良,侯军,欧阳平凯,游离酶法生产L-天冬氨酸的工艺研究南京化工大学学报。
