初中化学除杂方法和习题
初中化学化学除杂分离和提纯解题技巧(超强)及练习题(含答案)及解析

故选:D。
6.下列除去杂质的方法,错误的是( )
A.除去H2中的少量水蒸气:通过浓硫酸
B.除去CuO中的少量碳粉:在空气中充分加热
C.除去CO2中少量的CO:通过灼热的氧化铜
D.除去ZnCl2溶液中少量的CuCl2:加入足量的铁屑充分反应后,过滤
D.除去O2中含有的少量水蒸气和CO2:将混合气体依次通过烧碱溶液和浓硫酸
【答案】D
【解析】
【详解】
A、过量的稀盐酸和氧化钙反应生成氯化钙和水,和碳酸钙反应生成氯化钙、水和二氧化碳,该选项不能达到实验目的;
B、铁不能在空气中燃烧,因此不能用铁丝代替红磷,该选项不能达到实验目的;
C、稀盐酸和氯化钠溶液不能是酚酞试液变色,氢氧化钾溶液能使酚酞试液变红色,利用酚酞试液不能区分稀盐酸和氯化钠溶液,该选项不能达到实验目的;
考点:除杂质
8.下列实验方案或结论不正确的是()
A.除去铜粉中含有的少量铁粉:将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥
B.不用其它任何试剂就能将CuSO4溶液、稀H2SO4、NaCl溶液、NaOH溶液鉴别出来
C.除去CO2中的少量HC1气体:先通过NaOH溶液,再通过浓硫酸
D.鉴别NaCl、Na2SO4和(NH4)2SO4三种溶液:各取少量于试管中,分别滴加Ba (OH)2溶液
【点睛】
除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
4.下表物质中含有少量杂质,其中除杂方法正确的是( )
物质
杂质
除去杂质的方法
A
CaCl2溶液
MgCl2
加入金属钙
【化学】初中化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)

【化学】初中化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)一、中考化学除杂分离和提纯1.下列除杂(括号内为杂质)的试剂选用正确的是( )A .AB .BC .CD .D【答案】B 【解析】 【分析】 【详解】A 、CaCl 2溶液(盐酸)加入过量的Na 2CO 3溶液发生反应;2322Na CO 2HCl=2NaCl CO H O ++↑+ 2323Na CO CaCl =2NaCl CaCO ++↓会生成新杂质NaCl ,Na 2CO 3,被提纯CaCl 2会减少,不符合题意; B 、NaOH 溶液(Na 2CO 3溶液)加入适量的Ca(OH)2溶液发生反应;2323Na CO Ca(OH)=CaCO 2NaOH +↓+ 可以去除Na 2CO 3,符合题意;C 、CuO(Cu) 加入足量的稀H 2SO 4,CuO 会和稀H 2SO 4反应生成硫酸铜和水CuO 减少,不符合题意;D 、KCl 溶液(K 2SO 4溶液)加入适量的Ba(NO 3)2溶液发生反应;243234K SO Ba(NO )=2KNO BaSO ++↓ 虽然去除了K 2SO 4但是会产生新杂质KNO 3不符合题意; 故选:B 。
2.下列除杂质的方法正确的是( )A.A B.B C.C D.D【答案】D【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氧化铜和盐酸反应生成氯化铜和水,把原物质除去了,故A不正确;B、硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,引入新杂质硝酸钠,故B不正确;C、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,把原物质除去了,故C不正确;D、铁和氯化铜反应生成氯化亚铁和铜,可以除去氯化亚铁溶液中的氯化铜杂质,没有引入新的杂质,故D正确。
故选D。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.下列方法不能达到除杂目的的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、CO能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
中考化学溶液的除杂分离和提纯综合练习题含答案解析
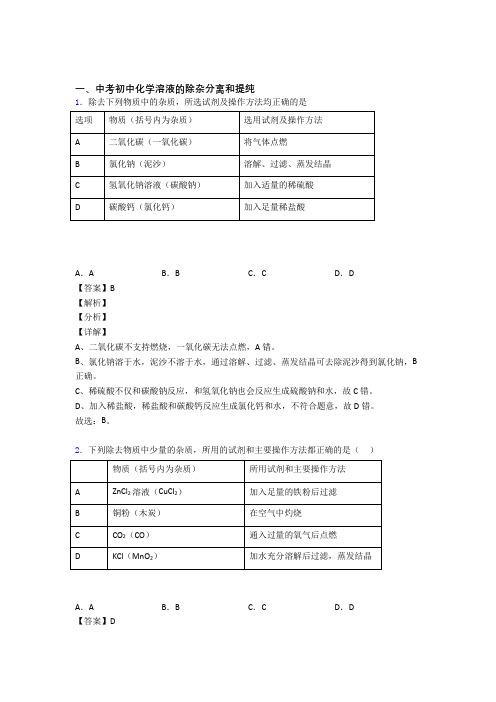
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中的杂质,所选试剂及操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、二氧化碳不支持燃烧,一氧化碳无法点燃,A错。
B、氯化钠溶于水,泥沙不溶于水,通过溶解、过滤、蒸发结晶可去除泥沙得到氯化钠,B 正确。
C、稀硫酸不仅和碳酸钠反应,和氢氧化钠也会反应生成硫酸钠和水,故C错。
D、加入稀盐酸,稀盐酸和碳酸钙反应生成氯化钙和水,不符合题意,故D错。
故选:B。
2.下列除去物质中少量的杂质,所用的试剂和主要操作方法都正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、铁粉与氯化铜反应生成氯化亚铁,除去杂质氯化铜后会引入新杂质氯化亚铁,不符合除杂原则,选项错误;B、木炭与空气中的氧气反应生成二氧化碳,铜也能与空气中的氧气反应,反应后生成氧化铜,不符合除杂原则,选项错误;C、气体中如果一氧化碳的含量较低,则一氧化碳不会发生燃烧,选项错误;D、氯化钾易溶于水,而二氧化锰不溶于水,将固体混合物加水充分溶解后过滤,将滤液蒸发结晶得到纯净氯化钾,选项正确,故选D。
【点睛】除杂的原则:1、除杂剂只能与杂质反应,不能与欲保留的物质反应;2、不能引入新杂质;3、最佳的除杂方法是除杂剂与杂质反应生成欲保留的物质。
3.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、加入过量的CuCl2溶液和铁充分反应,得到铜和氯化亚铁溶液,过滤得到铜,洗涤、干燥得到纯净的铜,符合题意;B、KC1中的杂质MnO2,加入足量的水溶解,是KC1溶解,MnO2不能溶解,过滤、洗涤、后面应该蒸发结晶才能得到KC1,不符合题意;C、NaCl中的杂质NaNO3,加入适量的硝酸银溶液是和主要物质NaCl发生反应,没有除去杂质NaNO3,不符合题意;D、Cu中的杂质C,在空气中灼烧,Cu、C都会与氧气反应,Cu反应生成氧化铜,C反应产生二氧化碳,主要物质被反应了,不符合题意。
初中化学除杂方法

初中化学除杂方法本文由查字典化学网为您整理提供:1.CO2(CO):把气体通过灼热的氧化铜2.CO(CO2) :通过足量的NaOH溶液3.H2(水蒸气):通过浓硫酸/通过NaOH固体4.CuO(C):在空气中(在氧气流中)灼烧混合物5.出去C粉中的CuO,可加入适量的稀硫酸溶液(CuO+H2S04=CuSO4+H2O)然后过滤后取滤液渣6.Cu(Fe):加入足量的稀硫酸7.Cu(CuO):加入足量的稀硫酸,或可将混合固体加入CuSO4溶液中,(Fe+CuSO4=Cu+FeSO4),然后过滤去滤渣8.FeSO4(CuSO4):加入足量的铁粉9.NaCl(Na2CO3):加入足量的盐酸10.NaCl(Na2SO4):加入足量的氯化钡溶液11.KCl(K2S04):向溶液加入适量的BaCl2溶液(K2S04+BaCl2=2KCl+BaSO4)然后过滤去滤液12.NaCl(NaOH):加入足量的盐酸13.NaOH(Na2CO3):加入足量氢氧化钙溶液(Na2CO3+Ca(OH)2=2NaOH+CaCO3)然后过滤后去滤液14.NaCl(CuSO4)加入质量的氢氧化钡溶液(先加氢氧化钠,再加氯化钡同样可以)15.NaNO3(NaCl):加入足量的硝酸银溶液16.NaCl(KNO3):蒸发溶剂17.KNO3(NaCl):冷却热饱和溶液18.CO2(水蒸气):通过浓硫酸19.N2(O2):将混合气体通过灼热的铜网(2Cu+O2=2CuO)20.Na2SO4(NaOH):加入适量的稀硫酸溶液(2NaOH+H2S04=Na2SO4+2H20)21.NaCl(BaCl2):加入适量的Na2SO4溶液(BaCl2+Na2S04=2NaCl+BaSO4)然后过滤取滤液22.KNO3(AgNO3):加入适量的KCl溶液(AgNO3+KCl=KNO3+AgCl)然后过滤取滤液23.NaNO3(CuSO4):加入适量的Ba(OH)2溶液(CuSO4+Ba(OH)2=Cu(OH)2+BaSO4)然后过滤去滤液24.NaNO3((NH4)2O4):加入适量的Ba(OH)2溶液((NH4)2O4+Ba(OH)2=BaSO4+2NH3+2H2O)然后过滤后去滤液25.Na2SO4(Na2CO3)加入适量的稀H2SO4溶液(Na2CO3+H2SO4=Na2S04+2H2O+CO2)26.CaO(CaCO3):加热混合固体(CaCO3==(高温)==Ca0+CO2)。
初中化学化学除杂分离和提纯的基本方法技巧及练习题及练习题(含答案)

初中化学化学除杂分离和提纯的基本方法技巧及练习题及练习题(含答案)一、中考化学除杂分离和提纯1.下列各组除杂质(括号内表示少量杂质)的试剂或方法错误的一组是A.NaCl溶液(MgCl2);适量NaOH溶液,过滤B.CaO(CaCO3);稀盐酸C.铜粉(铁粉);足量硫酸铜溶液,过滤D.O2(水蒸气);固体NaOH【答案】B【解析】【分析】【详解】A、MgCl2能与适量NaOH溶液反应生成氢氧化镁沉淀和氯化钠,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
B、CaO和CaCO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
C、铁粉能与硫酸铜溶液反应生成硫酸亚铁和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、氢氧化钠具有吸水性,且不与氧气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
故选:B。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.按照加水溶解、过滤、蒸发的顺序进行操作,可以分离的一组混合物是。
A.木炭粉和MnO2B.Fe粉和CuOC.KMnO4和K2MnO4D.MnO2和NaCl【答案】D【解析】【分析】【详解】A、木炭粉和二氧化锰均不能溶于水,不能用加水溶解、过滤、蒸发分离,不符合题意;B、铁粉和氧化铜均不溶于水,不能用加水溶解、过滤、蒸发分离,不符合题意;C、高锰酸钾和锰酸钾均溶于水,不能用加水溶解、过滤、蒸发分离,不符合题意;D、二氧化锰不溶于水,氯化钠溶于水,加水溶解、过滤,可得二氧化锰,蒸发可得氯化钠,可以用加水溶解、过滤、蒸发将它们分离,符合题意。
故选D。
3.除去下列物质中的杂质(括号内物质为杂质)的方法错误的是 ( )A.N2(O2)——通过灼热的铜网B.Fe(Fe2O3)——过量稀盐酸、过滤C.H2(水蒸气)——通过浓硫酸的洗气瓶D.NaOH溶液(Na2CO3)——适量Ca(OH)2溶液,过滤【答案】B【解析】【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
初中化学除杂质的方法归纳

初中化学除杂质的方法归纳
常见的初中化学除杂质的方法有以下几种:
1. 沉淀法:利用溶液中不溶于水的固体沉淀下来的特点,将混合物中的杂质与主要物质分离。
比如,通过加入适当的化学试剂使得混合物中的某种离子产生沉淀而分离出来。
2. 蒸馏法:利用混合物中成分的沸点差异,将混合物中的杂质与主要物质分离。
比如,将混合物加热至其中某个组分沸点时,蒸发的气体可以通过冷凝器冷却并收集,从而将主要物质与其他杂质分离。
3. 萃取法:利用混合物中不同成分在不同溶剂中的溶解度差异,将混合物中的杂质与主要物质分离。
比如,通过在混合物中加入一种合适的溶剂,使得其中的某个组分只溶于该溶剂而被分离出来。
4. 结晶法:利用混合物中不同成分在溶液中的溶解度差异,将混合物中的杂质与主要物质分离。
比如,在混合物中加入一种化学试剂,使得主要物质溶解度下降,从而分离出杂质。
然后再通过慢慢降温等方法,让主要物质逐渐结晶出来。
初中化学《物质的净化与除杂应用》复习题

初中化学《物质的净化与除杂应用》复习题1. 用括号中的试剂除去下列物质中的杂质,所用试剂错误的是()A.除去CO2中的CO(灼热的CuO)B.除去O2中的H2O蒸汽(CaO)C.除去NaCl溶液中的Na2CO3(CaCl2溶液)D.除去C粉中的Cu粉(稀硫酸)2. 下列除去杂质所选择的试剂或方法中(括号里为杂质),正确的是()A.CO2(CO):点燃B.CO2(HCl):NaOH溶液C.NaCl(Na2CO3):H2SO4D.N2(O2):通过灼热的铜3. 除去下列物质中的杂质(括号内为杂质),所选用的试剂与方法正确的是()A.NaOH(Na2CO3):加入稀盐酸至不再产生气泡B.Cu粉(C):在空气中充分灼烧C.CuSO4溶液(FeSO4):加足量铜粉,过滤D.CaCl2溶液(HCl):加过量CaCO3粉末,过滤4. 下列除去杂质(括号内为杂质),选用的试剂正确的是()A.NH3(水蒸气)--浓硫酸B.CaO(CaCO3)−−稀盐酸C.Cu(CuO)−−蒸馏水D.NaOH(Na2SO4)−−Ba(OH)2溶液5. 除去下列各物质中混有的少量杂质(括号内为杂质),所用试剂及操作方法均正确的是()A.铁粉(Fe2O3)加入足量的稀盐酸,过滤B.NaCl溶液(MgCl2)加入适量的NaOH溶液、过滤C.CO气体(CO2)通过灼热的氧化铁粉末D.K2SO4溶液(K2CO3)加入足量的稀硫酸6. 用括号中的试剂除去下列物质中所含杂质,所用的药品错误的是()A.Na2SO4溶液中混有Na2CO3(稀硫酸)B.NaCl溶液中混有Na2SO4(BaCl2溶液)C.KCl溶液中混有K2CO3(稀盐酸)D.CO2中混有CO(NaOH溶液)7. 以下除杂方法(括号内为杂质)正确的是()A.AB.BC.CD.D8. 下列除去杂质(在括号内)选用的方法(在箭头右侧)正确的是()A.CO2气体(CO)→点燃B.KCl固体(MnO2)→加水、过滤、蒸发C.CO2气体(HCl)→通入NaOH溶液中D.KCl溶液(K2CO3)→加稀H2SO4B C.C D.DA.AB.11. 下列除去杂质的方法,错误的是()A.除去H2中的少量水蒸气:通过浓硫酸B.除去CO2中的少量HCl:通入足量的饱和NaHCO3溶液,干燥C.除去NaCl溶液中少量的CaCl2:加入适量Na2CO3溶液,过滤D.除去FeCl3溶液中少量的CuCl2:加入足量的铁屑充分反应后,过滤12. 除去下列物质中混有的少量杂质(括号内为杂质)拟定的实验方案不可行的是()A.N2气体(O2);通过灼热的铜网B.CuO(木炭粉);在空气中灼烧C.CO2(CO);通过灼热的木炭层D.CO(CO2);通过足量的澄清石灰水13. 除去下列物质中的少量杂质,所用括号内的方法不正确的是()A.氦气中的少量氧气(灼热的铜网)B.二氧化碳气体中的少量一氧化碳(点燃)C.硫酸亚铁溶液中少量的硫酸铜溶液(足量的铁粉,过滤)D.氧化钙中少量的碳酸钙(高温)A.AB.BC.CD.D15. 下列关于物质鉴别、除杂实验方案不能达到目的的是()A.鉴别HCl、NaOH、Na2CO3三种无色溶液:滴加紫色石蕊溶液,观察颜色变化B.鉴别硬水和软水:加肥皂水,搅拌,观察泡沫和浮渣情况C.除去氯化钾溶液中硫酸钾:加适量氯化钡溶液,过滤D.除去硝酸钾固体中少量氯化钠:冷却热饱和溶液结晶,过滤16. 除去下列物质中混有的少量杂质(括号内为杂质),所选用的操作方法正确的是()A.炭粉(铁粉)----将固体粉末在空气中灼烧B.CaO (CaCO3)−−−−加水,过滤C.CO2 (CO)−−−−将气体点燃D.HNO3[Ba (NO3) 2]−−−−加入适量的H2SO4溶液,过滤17. 下列除去杂质的方法,错误的是()A.除去H2中的少量水蒸气:通过浓硫酸B.除去CuO中的少量碳粉:在空气中充分加热C.除去CO2中少量的CO:通过灼热的氧化铜D.除去ZnCl2溶液中少量的CuCl2:加入足量的铁屑充分反应后,过滤18. 下列实验方案不能达到实验目的的是()A.NaCl固体、NaOH固体和NH4NO3固体,可以用水鉴别B.稀盐酸、NaOH溶液、CuSO4溶液、NaCl溶液,不加任何试剂就可以鉴别C.除去铜粉中的Fe2O3,加入过量的稀盐酸,充分反应后过滤D.除去Na2SO4溶液中的CuSO4,加入适量的Ba(OH)2溶液,充分反应后过滤19. 下列实验方案中,能达到预期目的是()A.用NaOH溶液除去CO2中混有的HCl气体B.用点燃的方法除去CO中混有的少量CO2C.用稀盐酸除去热水瓶胆壁上的水垢(主要成分是碳酸钙和氢氧化镁)D.用BaCl2溶液除去KNO3溶液中混入的少量K2SO4,得到纯净的KNO3溶液20. 除去下列物质中的杂质(括号内为杂质),所选用的试剂与方法正确的是()A.H2(水蒸气):通过浓硫酸B.CO(CO2):通过NaOH溶液C.NaCl溶液(CaCl2):加入过量Na2CO3溶液,过滤D.铁粉(锌粉):加入稀硫酸,过滤21. 下列方法中,能除去生石灰中混有的少量碳酸钙的是()A.加强热B.加盐酸C.加氢氧化钠D.加水22. 不需要加任何指示剂,就能除去CaCl2溶液中少量的HCl,得到纯净的CaCl2溶液,可选用下列物质中的()A.生石灰B.熟石灰C.碳酸钙D.碳酸钠23. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是()A.Zn粉(Fe):用ZnCl2溶液浸泡,过滤B.碳粉(MnO2):滴入H2O2溶液,过滤C.NaCl溶液(Na2SO4):加入适量MgCl2溶液,过滤D.CO2 (H2O):通过盛有浓硫酸的洗气瓶24. 要除去下列物质中的少量杂质(括号内物质为杂质),所选试剂不正确的是()A.NaOH(Na2CO3):盐酸B.CO2(O2):灼热的铜粉C.CO(CO2):氢氧化钠溶液D.O2(H2O):浓硫酸25. 要除去下列四种物质中的少量杂质(括号内的物质为杂质)甲:CaCO3(Na2CO3)乙:NaOH(Na2CO3)丙:KCl(KHCO3)丁:炭粉(CuO)可选用的试剂及操作方法有:①加适量盐酸,搅拌,过滤;②加适量水,搅拌,过滤;③加适量盐酸,蒸发;④溶解,加适量石灰水,过滤,蒸发。
初中化学除杂专项
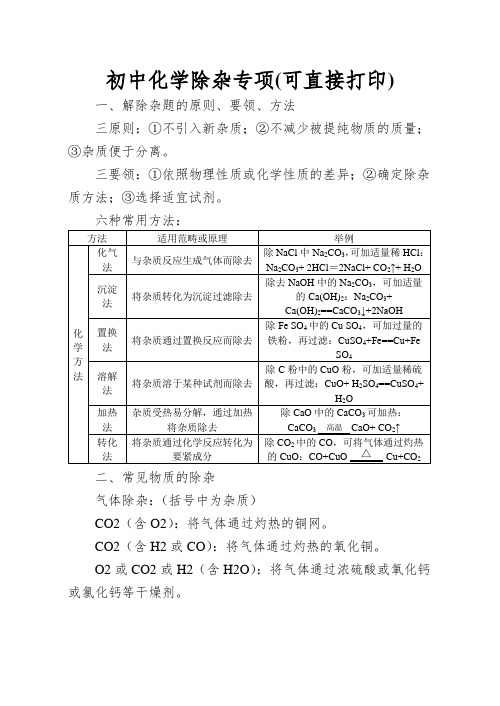
初中化学除杂专项(可直接打印)一、解除杂题的原则、要领、方法三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①依照物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
六种常用方法:二、常见物质的除杂气体除杂:(括号中为杂质)CO2(含O2):将气体通过灼热的铜网。
CO2(含H2或CO):将气体通过灼热的氧化铜。
O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂。
O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中固体除杂:Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤。
(将爽朗金属用酸溶解)Fe(含Cu):用磁铁将铁粉吸引出来。
Cu(含CuO)、Fe(含Fe2O3):高温下与H2或CO反应。
(将金属氧化物还原成金属)CuO(含Cu或C):在空气中灼烧。
CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)CaCO3(含CaO):加足量水溶解,过滤,取滤渣。
(CaO 与水反应溶于水)CaCO3(含CaCl2):加足量水溶解,过滤,取滤渣。
(Ca Cl2溶于水,CaCO3不溶于水)CaCl2(含CaCO3):加足量水溶解,过滤,取滤液蒸发。
Ca(OH)2(含CaO):加足量水。
(CaO与水反应生成氢氧化钙)溶液除杂:FeSO4溶液(含H2SO4或CuSO4)、FeCl2溶液(含盐酸或CuCl2):过量铁粉,过滤,取滤液。
有关反应:Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=Cu+ Fe SO4Fe+2HCl=FeCl2+H2↑;Fe+CuCl2=Cu+ FeC l2NaCl溶液(含Na2CO3):加适量稀盐酸。
Na2CO3+2HCl =2NaCl+H2O+CO2↑Na2SO4溶液(含CuSO4):加适量NaOH溶液。
CuSO4+ 2NaOH=Cu(OH)2↓+Na2SO4三、经典例题( )例1. (07昆明)除去KCl溶液中混有的少量K2CO3,选用的试剂是A.H2SO4溶液B.稀盐酸C.K2SO4溶液D. Ag NO3溶液( )例2. (08哈尔滨)除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )例3. (08黄石)下列除杂方法正确的是A.用NaOH除去CO2中混有的HClB.用点燃的方法除去CO2中混有少量的COC.用水除去MnO2中混有的KClD.用硝酸除去NaCl 中混有的Na2CO3( )例4. (08盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是( )例5. (08南通)除去下列物质中所含少量杂质的方法正确的是(四、中考链接( )1.(08大庆)下表中,除去物质所含杂质的方法正确的是( )2.(07雅安)除去下列各组物质中的杂质,所用试剂和方法均正确的是()3.(11扬州)下列除杂选用试剂正确的是A.用过量的O2除去CO2中CO B.用过量的FeSO4溶液除去Zn中的FeC.用过量的NaOH除去CaCl2溶液中HCl D.用过量HCl溶液除去Cu中CuO()4.(11无锡)除去下表所列物质中含有的杂质,所用试剂和操作方法均正确的是()5.(11泰州)除去下列物质中括号内少量杂质的方法,合理的是A. CaO(CaCO3):加入足量的稀盐酸B. CO2(CO):在氧气中点燃C. H2 (HCl、H2O):把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管D. KNO3(K2SO4):溶解,加入过量的硝酸钡溶液、过滤()6.(09南通)下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)A. NaCl( Na2CO3 ):加入足量稀盐酸、蒸发、结晶B. CaCl2 ( CaCO3 ) :加入足量稀硫酸、蒸发、结晶C. Fe (Cu) :加入足量稀盐酸、过滤、洗涤、干燥D. MnO2 (KCl):加入足量的水溶解、过滤、洗涤、干燥()7.(09扬州)下列除杂试剂选用正确的是()8.(09连云港)除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是()9.(09淮安)除去下列物质中少量的杂质,所用方法错误的是()10.(09盐城)下表中,除去物质中所含少量杂质的方法错误的是选项物质所含杂质除去杂质的方法A N2气体O2将气体慢慢通过灼热的铜网B MnO2粉末KCl 加水溶解、过滤、洗涤、烘干C FeCl2溶液CuCl2加入过量的铁粉,充分反应后过滤D KCl溶液CaCl2加入适量碳酸钠,充分反应后过滤()11.(09泰州)为了除去括号内的杂质),所选用试剂和操作方法都正确的是选项物质选用试剂(过量)操作方法A CO2(CO)O2点燃B Cu(Fe)稀盐酸加入稀盐酸充分反应后过滤、洗涤C CuSO4溶液(H2SO4)氧化铜加入氧化铜粉末充分反应后过滤D 盐酸(H2SO4)硝酸钡溶液加入硝酸钡溶液充分反应后过滤()12.(11.淄博市)除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是序号物质杂质(少量)试剂和操作方法A O2 H2O蒸汽通过浓H2SO4B 稀盐酸稀硫酸加入适量BaCl2溶液,过滤C Na2CO3粉末NaHCO3粉末加热D KNO3溶液Ba(NO3)2溶液加入适量的Na2SO4溶液,过滤()13. (11.湛江市)下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)选项物质除杂试剂(足量)操作方法A[CO2(HCl)氢氧化钠溶液气体通过盛有氢氧化钠溶液的洗气瓶B NaCl(Na2CO3)盐酸加入足量盐酸、蒸发、结晶C MnO2(NaCl)水加入足量水溶解、过滤、洗涤、干燥D Cu(CuO)氧气通入足量氧气并加热()14.(11.雅安市)下表中,除去物质所含杂质的方法正确的是选项物质所含杂质除去杂质的方法()15.(11.襄阳市)下列除去杂质所选择牟试剂错误的是:选项物质杂质所选试剂A CO2水蒸气浓硫酸B CaCl2溶液盐酸CaCO3C Cu CuO 稀盐酸D NaCl溶液NaOH溶液BaCl2溶液()16.(11达州市)下列各组括号内除杂技的方法或试剂错误的是A.CO2中混有CO(点燃)B.Cu粉中混有CuO(稀硫酸)C.CO中混有CO2 (氢氧化钠溶液)D.Cu粉中混有Fe粉(用磁铁吸引)()17.(11.德州市)除去下列物质中的少量杂质,所选用的试剂及反应类型均正确的是()18.(11.无锡市)除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是选项物质杂质除去杂质所选试剂操作方法A 二氧化碳一氧化碳氧气点燃B 氯化钾碳酸钾稀盐酸蒸发C 锌铁稀硫酸过滤D 氧化钙碳酸钙稀盐酸蒸发()19.(11.烟台市)除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是物质杂质除杂质选用的试剂和操作方法A CO2CO 通入O2,点燃B 二氧化碳氯化氢气体通过氢氧化钠溶液C Cu(NO3)2溶液AgNO3溶液加入过量的铜粉,过滤D 碳酸钙氯化钙加入足量的水溶解,过滤、洗涤、干燥()20.(11.宜宾市)除去下列物质中的杂质所选用试剂或操作方法不正确的一组是物质所含杂质除去杂质的试剂或方法A CaO CaCO3HClB CuO Cu灼烧C NaOH溶液Na2CO3适量Ca(OH)2溶液、过滤D O2 H2O 干燥()22.(11.滨州市)除去下列物质中的少量杂质,所用试剂或方法不正确的是()23.(11.鸡西市)除去下列物质中所含的少量杂质,所选试剂正确的是。
初中化学常见物质的除杂总结(可编辑修改word版)

初中化学常见物质的除杂总结概念理解首先明白物质除杂是干什么,物质除杂又叫物质提纯,即把混合物中少量的杂质出去,得到较纯净物质的过程。
初中化学除杂、提纯方法及例题将混合物中的几种物质分开而分别得到较纯净的物质,这种方法叫做混合物的分离。
将物质中混有的杂质除去而获得纯净物质,叫提纯或除杂。
1 物理方法1.l 过滤法.原理:把不溶于液体的固体与液体通过过滤而分开的方法称为过滤法。
如:氯化钙(CaCl2)中含有少量碳酸钙(CaCO3)杂质,先将混合物加水(H2O)溶解,由于氯化钙(CaCl2)溶于水,而碳酸钙(CaCO3)难溶于水,过滤除去杂质碳酸钙(CaCO3),然后蒸发滤液,得到固体氯化钙(CaCl2)。
如果要获得杂质碳酸钙(CaCO3),可洗涤烘干。
练习1 下列混合物可以用溶解、过滤、蒸发操作来分离的是:()A.CaCO3CaO B.NaCl KNO3C.NaNO3BaSO4D.KCl KClO31.2 结晶法.原理:几种可溶性固态物质的混合物,根据它们在同一溶剂中的溶解度或溶解度随温度的变化趋势不同,可用结晶的方法分离。
eg:除去固体硝酸钾(KNO3)中混有的氯化钠(NaCl)杂质,先在较高温度下制成硝酸钾的饱和溶液,然后逐步冷却,由于硝酸钾(KNO3)的溶解度随温度的升高而显著增大,温度降低,大部分硝酸钾成为晶体析出,而氯化钠的溶解度随温度的升高而增大得不显著,所以大部分氯化钠仍留在母液中,通过过滤把硝酸钾和氨化钠溶液分开。
为进一步提纯硝酸钾,可再重复操作一次,叫重结晶或再结晶。
练习2 下列混合物适宜用结晶法分离的是:()A.NaNO3 Na2CO3B.NaNO3 NaCl C.NaOH Mg(OH)2D.NaCl BaSO42 化学方法:原理(一)、加入的试剂只与杂质反应,不与原物反应。
(二)、反应后不能带入新的杂质。
(三)、反应后恢复原物状态。
(四)、操作方法简便易行。
初中常用化学除杂方法有以下几种:2.1 沉淀法:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
中考化学溶液的除杂分离和提纯(大题培优 易错 难题)附答案

一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、加入过量的CuCl2溶液和铁充分反应,得到铜和氯化亚铁溶液,过滤得到铜,洗涤、干燥得到纯净的铜,符合题意;B、KC1中的杂质MnO2,加入足量的水溶解,是KC1溶解,MnO2不能溶解,过滤、洗涤、后面应该蒸发结晶才能得到KC1,不符合题意;C、NaCl中的杂质NaNO3,加入适量的硝酸银溶液是和主要物质NaCl发生反应,没有除去杂质NaNO3,不符合题意;D、Cu中的杂质C,在空气中灼烧,Cu、C都会与氧气反应,Cu反应生成氧化铜,C反应产生二氧化碳,主要物质被反应了,不符合题意。
故选A。
2.下列除杂所选用试制与操作方法均正确的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,过滤可除去碳酸钙,但是也把原物质除去了,不符合除杂原则,不符合题意;B、碳酸钠能与过量稀盐酸反应生成氯化钠、水和二氧化碳,盐酸具有挥发性,再蒸发除去盐酸,能除去杂质且没有引入新的杂质,符合除杂原则,符合题意;C、硫酸钠能与过量氯化钡溶液反应生成硫酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质(过量的)氯化钡,不符合除杂原则,不符合题意;D、CO和氢气均能与灼热的CuO反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,不符合题意。
故选B。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.下表列出了除去物质中所含少量杂质的方法,其中错误的是A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、氢氧化钠溶液能与HCl气体反应,不与H2反应,将混合气体通入足量的氢氧化钠溶液,再干燥,可得到H2,此选项不符合题意;B、稀盐酸将碳酸钠溶液除去的同时,也将氢氧化钠溶液除去了,此选项符合题意;C、NaCl易溶于水,泥沙难溶于水,加入足量的水溶解、过滤,可滤出泥沙,然后蒸发水,得到氯化钠,此选项不符合题意;D、氧化铜与氧气不反应,碳粉能与氧气反应,生成的气体逸出。
初中化学除杂题解法指导与专项训练(附答案)
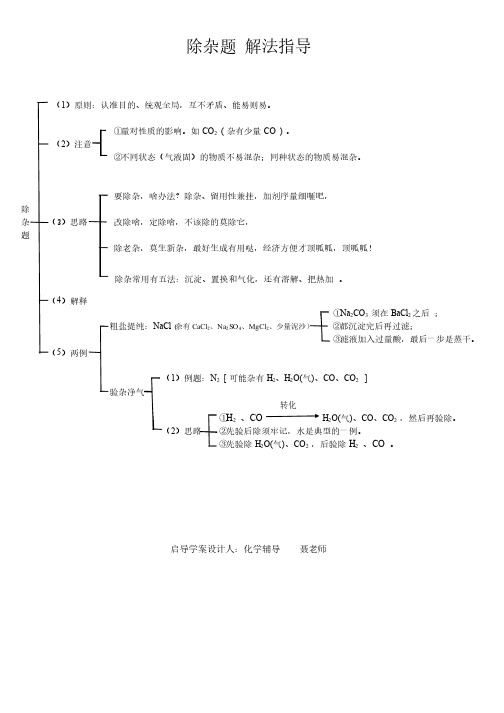
除杂题除杂题 解法指导(1)原则:认准目的、统观全局,互不矛盾、能易则易。
)原则:认准目的、统观全局,互不矛盾、能易则易。
①量对性质的影响。
如CO 2 ( 杂有少量CO ) 。
(2)注意)注意②不同状态(气液固)的物质不易混杂;同种状态的物质易混杂。
不同状态(气液固)的物质不易混杂;同种状态的物质易混杂。
要除杂,啥办法?除杂、留用性兼挂,加剂序量细咂吧,要除杂,啥办法?除杂、留用性兼挂,加剂序量细咂吧, 除 杂 (3)思路)思路 改除啥,定除啥,不该除的莫除它,改除啥,定除啥,不该除的莫除它,改除啥,定除啥,不该除的莫除它,题除老杂,莫生新杂,最好生成有用哒,经济方便才顶呱呱,顶呱呱!除老杂,莫生新杂,最好生成有用哒,经济方便才顶呱呱,顶呱呱!除杂常用有五法:沉淀、置换和气化,还有溶解、把热加除杂常用有五法:沉淀、置换和气化,还有溶解、把热加 。
(4)解释)解释①Na 2CO 3 须在BaCl 2之后之后 ; 粗盐提纯:NaCl (杂有杂有CaCl 2、Na 2SO 4、MgCl 2、少量泥沙) ②都沉淀完后再过滤;都沉淀完后再过滤; ③滤液加入过量酸,最后一步是蒸干。
(5)两例)两例(1)例题:N 2 [ 可能杂有H 2、H 2O(气)、CO 、CO 2 ] 验杂净气验杂净气转化①H 2 、CO H 2O(气)、CO 、CO 2 ,然后再验除。
,然后再验除。
(2)思路)思路 ②先验后除须牢记,水是典型的一例。
先验后除须牢记,水是典型的一例。
③先验除H 2O(气)、CO 2 ,后验除H 2 、CO 。
启导学案设计人:化学辅导启导学案设计人:化学辅导 聂老师聂老师除杂题 专项训练1.下列除去混合物中少量杂质的方法或加入试剂合理的是.下列除去混合物中少量杂质的方法或加入试剂合理的是 ( )选项选项 物质物质 所含杂质所含杂质 除去杂质的方法或加入试剂除去杂质的方法或加入试剂 A KCl K 2SO 4 Ba(NO 3) 2 B CuO Cu 空气中灼烧空气中灼烧 C CO 2 N 2 澄清石灰水澄清石灰水 D Ca(OH)2CaCO 3盐酸盐酸2.下列实验操作中,不能达到实验目的是(下列实验操作中,不能达到实验目的是( )3.除去下列物质中含有的杂质所选用试剂或操作方法不正确...的一组是的一组是 物 质 所含杂质所含杂质 除去杂质的试剂或方法除去杂质的试剂或方法 A NaCl 溶液 Na 2CO 3 过量盐酸,加热过量盐酸,加热 B CuO Cu 灼烧灼烧 C KCl KClO 3 MnO 2,加热,加热 D O 2 H 2O 浓硫酸,干燥浓硫酸,干燥4.为提纯下列物质,所选用的除杂试剂和分离方法都正确的是为提纯下列物质,所选用的除杂试剂和分离方法都正确的是 ( ) 序号序号 物质(括号内为杂质)物质(括号内为杂质) 除杂试剂除杂试剂 分离方法分离方法 A 氯化钠固体(碳酸钠)氯化钠固体(碳酸钠) 稀盐酸稀盐酸 蒸发结晶蒸发结晶 B 氯化铜溶液(氯化锌)氯化铜溶液(氯化锌) 金属铜金属铜 过滤过滤 C 二氧化碳(一氧化碳)二氧化碳(一氧化碳)氢氧化钠溶液氢氧化钠溶液洗气洗气D 二氧化锰粉末(碳粉)二氧化锰粉末(碳粉) 水 过滤过滤5.下列选项中括号内物质为杂质,右边为除杂试剂,其中不合理...的是的是 A .氯化钠固体(碳酸钙).氯化钠固体(碳酸钙) 水 B .氧气(水蒸气).氧气(水蒸气) 浓硫酸浓硫酸 C .硫酸亚铁溶液(硫酸铜).硫酸亚铁溶液(硫酸铜) 铁粉铁粉实验目的实验目的实验操作实验操作A 鉴别涤纶和羊毛面料鉴别涤纶和羊毛面料 分别取样灼烧、闻气味分别取样灼烧、闻气味B 提纯粗盐(含少量泥沙)提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶将粗盐加适量水溶解、过滤、蒸发结晶 C 除去氯化钙溶液中少量盐酸除去氯化钙溶液中少量盐酸加入过量的碳酸钙粉末、充分反应后过滤加入过量的碳酸钙粉末、充分反应后过滤D 分离硫酸钠和硫酸铜的混合溶液分离硫酸钠和硫酸铜的混合溶液 加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸6.为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是,所选试剂及操作方法均正确的是 ( )序号序号样品成分样品成分所选试剂所选试剂操作方法操作方法A KCl (MnO 2)水溶解、过滤、洗涤干燥溶解、过滤、洗涤干燥B Na 2CO 3(NH 4HCO 3)加热至质量不再减少加热至质量不再减少 C NaCl (KNO 3) 水溶解、降温结晶、过滤溶解、降温结晶、过滤D NaCl (MgCl 2)过量NaOH 溶液溶液过滤、蒸发结晶过滤、蒸发结晶7.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是(,下列操作方法正确的是( ) 选项选项 物质物质 操作方法操作方法A Fe (Fe 2O 3)加入过量稀盐酸,充分反应后过滤加入过量稀盐酸,充分反应后过滤 B CaO 粉末(CaCO 3粉末)粉末) 加足量的水,充分搅拌后过滤加足量的水,充分搅拌后过滤 C NaOH 溶液[Ca(OH)2溶液] 通入过量CO 2气体,充分反应后过滤气体,充分反应后过滤 D CuSO 4溶液(硫酸)溶液(硫酸)加入过量CuO 粉末,加热,充分反应后过滤粉末,加热,充分反应后过滤8.除去下列物质中的少量杂质(括号内为杂质)的方法错误的是(.除去下列物质中的少量杂质(括号内为杂质)的方法错误的是( ) A .O 2(H 2O )﹣用生石灰)﹣用生石灰 B .NaCl 溶液(KNO 3)﹣降温结晶)﹣降温结晶 C .CaCO 3粉末(Na 2CO 3)﹣加水过滤)﹣加水过滤D .KCl 溶液(K 2CO 3)﹣加适量盐酸)﹣加适量盐酸 9. 除去下列物质中的杂质,选用试剂或操作方法不正确是( ) 物质物质所含杂质所含杂质除去杂质的试剂或方法除去杂质的试剂或方法A Na 2CO 3固体固体NaHCO 3固体固体加热加热 B Cu Fe 加过量稀盐酸后过滤、洗涤、干燥加过量稀盐酸后过滤、洗涤、干燥 C O 2 H 2O 通人盛有过量浓H 2SO 4的洗气瓶的洗气瓶 D CO 2HC1 通入盛有NaOH 溶液的洗气瓶,然后干燥溶液的洗气瓶,然后干燥10.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是,所选试剂(过量)及操作方法均正确的是 ( ) 物质物质 选用试剂选用试剂 操作方法操作方法 A Cu(CuO) 氧气氧气 通入氧气并加热通入氧气并加热B CO 2(HCl) 氢氧化钠溶液氢氧化钠溶液 通过盛有氢氧化钠溶液的洗气瓶通过盛有氢氧化钠溶液的洗气瓶 C CaCl 2溶液(盐酸)溶液(盐酸) 碳酸钙粉末碳酸钙粉末 加入碳酸钙粉末充分反应后过滤加入碳酸钙粉末充分反应后过滤 D KCl 溶液(K 2CO 3) 氯化钙溶液氯化钙溶液加入氯化钙溶液充分反应后过滤加入氯化钙溶液充分反应后过滤11.除去下列物质中所含的少量杂质,下表中除杂方法正确的是除去下列物质中所含的少量杂质,下表中除杂方法正确的是 选项选项 物 质 所含杂质所含杂质 除杂质的方法除杂质的方法 A 氧化铜氧化铜 氯化钠氯化钠 加水溶解、过滤、蒸发结晶加水溶解、过滤、蒸发结晶 B 氧气氧气 水蒸气水蒸气 通过盛有浓硫酸的洗气瓶通过盛有浓硫酸的洗气瓶 C 硫酸钠溶液硫酸钠溶液 稀硫酸稀硫酸 加入过量碳酸钠溶液,过滤过滤D 二氧化碳二氧化碳一氧化碳一氧化碳点燃点燃12.除去下列各组物质中的少量杂质,所用方法不正确...的是的是 ( ) 选项选项 物质物质 杂质杂质 除去杂质的方法除去杂质的方法 A NaCl 泥沙泥沙 加入水溶解,过滤,蒸发加入水溶解,过滤,蒸发B O 2 水蒸气水蒸气 通过足量的浓硫酸通过足量的浓硫酸C NaOH 溶液溶液Na 2CO 3 滴入足量稀盐酸至不再产生气体滴入足量稀盐酸至不再产生气体 D H 2HCl 气体气体先通过NaOH 溶液,再通过浓硫酸溶液,再通过浓硫酸13. 下列除去杂质的方法中正确的是下列除去杂质的方法中正确的是 ( ) 选项选项 物质物质 杂质杂质 除杂质的方法除杂质的方法 A CaCl 2溶液溶液 稀盐酸稀盐酸 过量碳酸钙、过滤过量碳酸钙、过滤B KOH 溶液溶液 KCl 适量稀盐酸适量稀盐酸 C NaCl 溶液溶液Na 2CO 3 适量硝酸钙溶液、过滤适量硝酸钙溶液、过滤 D O 2CO 通过灼热的氧化铜通过灼热的氧化铜14.除去下列物质中的杂质(括号中的为杂质),所用试剂错误..的是的是 ( ) 选项选项 A B C D 物质物质 CO 2(CO) CO 2(HCl) Cu(CuO) KCl(MnO 2) 除杂试剂除杂试剂CuO NaOH 溶液溶液稀盐酸稀盐酸H 2O 15.下表列出了除去物质中所含少量杂质的方法,其中错误的是下表列出了除去物质中所含少量杂质的方法,其中错误的是 ( ) 选项选项 物质物质 杂质杂质 除杂方法除杂方法 A CO 2 CO 点燃B Cu 粉 Fe 粉 磁铁吸引磁铁吸引 C CaO CaCO 3 高温高温D CaCl 2溶液溶液稀盐酸稀盐酸加入足量的CaCO 3 ,过滤,过滤16.除去下列物质中的少量杂质所选用的试剂或方法正确的是(除去下列物质中的少量杂质所选用的试剂或方法正确的是( ) 选项选项 物质物质 所含杂质所含杂质 所选用试剂或方法所选用试剂或方法A NaOH 溶液溶液Na 2CO 3 溶液溶液 稀盐酸稀盐酸 B CaO CaCO 3高温灼烧高温灼烧C CO 2 CO 点燃点燃D 稀盐酸稀盐酸稀硫酸稀硫酸加适量Ba(NO 3)2溶液,再过滤溶液,再过滤17.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是,所用方法正确的是 ( )A .CO 2气体(CO 气体)——通入氧气通入氧气B .CaO 固体(CaCO 3固体)——加水充分溶解,过滤加水充分溶解,过滤C .KCl 固体(MnO 2固体)——加水充分溶解,过滤,蒸发结晶加水充分溶解,过滤,蒸发结晶D .NaCl 溶液(CaCl 2溶液)——滴加碳酸钾溶液至恰好完全反应,过滤滴加碳酸钾溶液至恰好完全反应,过滤 18.除去下列物质中混有的少量杂质(括号内为杂质)所用方法正确的是除去下列物质中混有的少量杂质(括号内为杂质)所用方法正确的是 ( ) A.CO 2( CO )──通入氧气点燃通入氧气点燃B.SO 2( HCl )──通过足量的氢氧化钠溶液通过足量的氢氧化钠溶液C.KCl 固体(固体( KClO 3 )── 加少量二氧化锰固体并加热加少量二氧化锰固体并加热D.NaCl 溶液( NaHCO 3 )──滴加稀盐酸至恰好完全反应滴加稀盐酸至恰好完全反应 19.下列鉴别物质的方法错误..的是的是 ( ) A.用水鉴别无水硫酸铜和氯化钠晶体用水鉴别无水硫酸铜和氯化钠晶体 B.用熟石灰鉴别硫酸铵和氯化铵用熟石灰鉴别硫酸铵和氯化铵C.用燃烧的木条鉴别氧气和二氧化碳用燃烧的木条鉴别氧气和二氧化碳D.用小木条鉴别浓硫酸和稀硫酸用小木条鉴别浓硫酸和稀硫酸20、下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的是( ) 混合物混合物 思路方法思路方法 选用物质选用物质 A .CO 2(CO) 点燃点燃 空气空气B .NaOH(Na 2CO 3) 沉淀、过滤沉淀、过滤 石灰乳[Ca(OH)2] C .FeCl 2(CuCl 2) 置换、过滤置换、过滤 铁粉铁粉D .NaCl(MgCl 2) 沉淀、过滤沉淀、过滤 NaOH 21、除去下列物质中的少量杂质,所用试剂或方法不正确的是( ) 选项选项 物质物质 杂质杂质 试剂或方法试剂或方法A NaCl 固体固体 泥沙泥沙 加水溶解、过滤、蒸发加水溶解、过滤、蒸发 B NaCl 溶液溶液 Na 2CO 3 滴加硫酸溶液至不再产生气泡滴加硫酸溶液至不再产生气泡 C KNO 3 溶液溶液 Ba(NO 3)2 滴加适量K 2SO 4溶液、过滤溶液、过滤 D N 2O 2通过红热的铜丝通过红热的铜丝22、除去下列物质中的杂质所选用的试剂或操作方法不正确的一组是(、除去下列物质中的杂质所选用的试剂或操作方法不正确的一组是( ) 物质物质 所含杂质所含杂质 除去杂质的试剂或方法除去杂质的试剂或方法 A CaO CaCO3 HCl B CuO Cu 灼烧灼烧C NaOH 溶液溶液 Na 2CO 3 适量Ca(OH)2溶液、过滤过滤 D O 2H 2O 干燥干燥23、(2011济南)济南) 除去下列各物质中混有的少量杂质,所用试剂和操作方法均正确的是( ) 序号序号 物质物质 杂质杂质 所用试剂和操作方法所用试剂和操作方法A H 2HCl 通过足量的NaOH 溶液、干燥溶液、干燥 B Na 2CO 3溶液溶液 Na 2SO 4溶液溶液 加入过量的Ba(NO 3)2溶液,过滤溶液,过滤 C NaCl 固体固体 细沙细沙 加入足量的水溶解,过滤加入足量的水溶解,过滤 D 铁粉铁粉Fe 2O 3加入适量的稀盐酸,过滤加入适量的稀盐酸,过滤24、下列做法正确的是(、下列做法正确的是( )A .加入适量的氢氧化钡溶液以除去NaCl 溶液中的少量Na 2SO 4B .加入适量的碳酸钙粉末以除去盐酸溶液中的少量CaCl 2C .用点燃的方法除去CO 2中混有的少量CO D .用氢氧化钠溶液处理硫在氧气中燃烧产生的气体.用氢氧化钠溶液处理硫在氧气中燃烧产生的气体25、除去下列物质中括号内少量杂质的方法,合理的是(、除去下列物质中括号内少量杂质的方法,合理的是( )A .CaO(CaCO 3):加入足量的稀盐酸B .CO 2(CO):在氧气中点燃:在氧气中点燃C .H 2 (HCl 、H 2O):把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管D .KNO 3(K 2SO 4):溶解,加入过量的硝酸钡溶液,过滤:溶解,加入过量的硝酸钡溶液,过滤26、除去下列各物质中的少量杂质(括号内为杂质),其中方法错误的是(,其中方法错误的是( ) A .Cu 粉(Fe 粉):用磁铁吸:用磁铁吸 B .NaOH (NaNO 3):加稀盐酸:加稀盐酸 C. NaCl (泥沙)(泥沙):溶解、过滤、蒸发:溶解、过滤、蒸发 D. O 2(水蒸气):用浓H 2SO 4干燥干燥 27、除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是(、除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是( ) 选项选项 物质物质 杂质杂质 除去杂质所选试剂除去杂质所选试剂 操作方法操作方法 A 二氧化碳二氧化碳 一氧化碳一氧化碳 氧气氧气 点燃点燃 B 氯化钾氯化钾 碳酸钾碳酸钾 稀盐酸稀盐酸 蒸发蒸发 C 锌 铁 稀硫酸稀硫酸 过滤过滤 D 氧化钙氧化钙碳酸钙碳酸钙稀盐酸稀盐酸蒸发蒸发28、下列除去杂质所选择的试剂错误的是(、下列除去杂质所选择的试剂错误的是( )29、除去下列物质中混有的少量杂质(括号中的物质为杂质)所设计的试验方案或操作中,合理的是(、除去下列物质中混有的少量杂质(括号中的物质为杂质)所设计的试验方案或操作中,合理的是( ) A、KNO 3晶体(NaCl ):将固体溶于水,配置成热的饱和溶液,采用降温结晶的方法 B、CO 2气体(HCl ):将气体通过装有NaOH 溶液的洗气瓶溶液的洗气瓶 C、BaCl 2溶液(Ba(OH)2):加入适量得稀硫酸,过滤加入适量得稀硫酸,过滤 D、O 2 ( N 2):将混合气体通过炽热得铜网。
【化学】化学溶液的除杂分离和提纯的专项培优练习题及答案
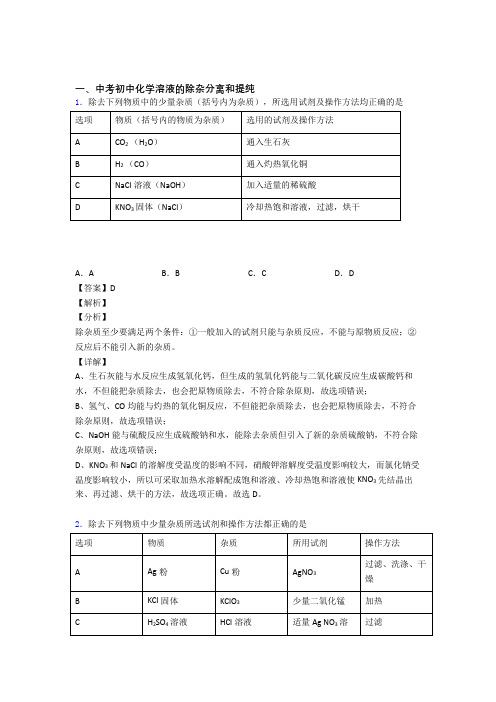
一、中考初中化学溶液的除杂分离和提纯1.除去下列物质中的少量杂质(括号内为杂质),所选用试剂及操作方法均正确的是A.A B.B C.C D.D【答案】D【解析】【分析】除杂质至少要满足两个条件:①一般加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】A、生石灰能与水反应生成氢氧化钙,但生成的氢氧化钙能与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;B、氢气、CO均能与灼热的氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项错误;C、NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项错误;D、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤、烘干的方法,故选项正确。
故选D。
2.除去下列物质中少量杂质所选试剂和操作方法都正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、Cu的活动性强于Ag,可以将Cu从其盐溶液中置换出来,故加入AgNO3可以与Cu反应,再过滤、洗涤、干燥即可除去,符合题意;B、KClO3在二氧化锰催化下可生成KCl和O2,但反应产物中有固体二氧化锰,不符合题意;C、HCl可与Ag NO3反应生成AgCl沉淀和HNO3,引入了新的杂质,不符合题意;D、NH3属碱性气体,可与酸反应,故不可用浓硫酸干燥,不符合题意。
故选A。
3.除去下列物质中的少量杂质,所选用的试剂及操作方法不正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、浓硫酸具有吸水性,可以去除氧气中水蒸气,正确。
B、稀硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,过滤后只剩下盐酸,即除去杂质又未引入新杂质,正确。
C、氢氧化钠和二氧化碳反应生成碳酸钠和水,一氧化碳不能与氢氧化钠反应,又未引入新的杂质,正确。
初中常用化学除杂的几种方法-教育文档

初中常用化学除杂的几种方法2.1沉淀法:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
练习3下列混合物可用沉淀法除去杂质(括号内的物质是杂质)的是()A.KNO3〔Ba(NO3)2〕B.NaCl〔KNO3〕C.NaNO3[NaCl]D.Ca(NO3)2[AgCl]2.2化气法:将混合物中的杂质与适当试剂反应变成气体而除去。
如:硝酸钠固体中含有少量碳酸钠杂质,可将混合物加水溶解,再加入适量稀硝酸溶液,硝酸与碳酸钠反应生成硝酸钠、水和二氧化碳,再蒸发滤液,获得硝酸钠固体。
练习4下列混合物中的杂质(括号内的物质是杂质)适宜用气体法除去的是:()A.NaNO3〔Ba(NO3)2〕B.NaCl[Mg(OH)2]C.KNO3〔K2CO3〕D.Na2SO4〔MgSO4〕2.3置换法:将混合物中的杂质与适量试剂通过发生置换反应而除去。
如:硫酸锌固体中含有少量硫酸铜杂质,可将混合物溶解之后,加人适量锌粉,再过滤除去被置换出来的铜,蒸发滤液获得硫酸铜固体。
练习5加入下列哪些物质可以除去硫酸亚铁溶液中混有的少量杂质硫酸铜()A.ZnB.FeC.CuD.Mg练习6将混有少量铁粉和锌份的硫酸铜晶体溶于适量水,充分净置过滤,结果是A.滤出了混杂在其中的铁粉B.滤出了混杂在其中的锌粉C.滤出了一些铜粉D.什么也没滤出2.4吸收法:两种以上混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
如:一氧化碳中含有二氧化碳时,可将混合气体通过盛有氢氧化钠的溶液。
2.5其它法:将混合物中的杂质用化学方法转化成其它物质。
如:氧化钙中含有碳酸钙,可采用高温燃烧的方法,使碳酸钙高温分解成氧化钙和二氧化碳,二氧化碳扩散到空气中,除去杂质。
也可以归纳:1、液体中除去液体:物理结晶法,如氯化钠中混硝酸钠;沉淀法:KNO3〔Ba(NO3)2〕(加Na2SO4);化气法,氯化钠溶液中混碳酸钠(加稀盐酸);置换法,FeCl2(加Fe)。
初中化学除杂试题及答案

初中化学除杂试题及答案1. 在实验室中,为了除去氯化钠溶液中的少量碳酸钠,可以采取的方法是:A. 加入盐酸B. 加热C. 加入氯化钙D. 加入水答案:A2. 某学生在进行实验时,不小心将硫酸铜溶液与硫酸亚铁溶液混合,为了分离出纯净的硫酸铜溶液,应该采取的措施是:A. 加入铁粉B. 加入铜粉C. 加入氢氧化钠D. 加入硫酸答案:A3. 为了除去铜粉中的少量铁粉,可以采取以下哪种方法?A. 加入盐酸B. 加入硫酸铜溶液C. 加入硫酸D. 加入水答案:B4. 在实验室中,为了除去氢氧化钠溶液中的少量碳酸钠,可以采取的方法是:A. 加入氢氧化钙B. 加入氢氧化钠C. 加入二氧化碳D. 加入盐酸答案:A5. 实验室中,为了除去铜片表面的氧化铜,可以采取的方法是:A. 加热B. 加入稀硫酸C. 加入盐酸D. 加入水答案:B6. 为了除去硝酸钾溶液中的少量氯化钠,可以采取的方法是:A. 蒸发结晶B. 加热C. 加入硝酸D. 加入水答案:A7. 在实验室中,为了除去酒精中的少量水,可以采取的方法是:A. 加入生石灰B. 加热蒸馏C. 加入硫酸铜D. 加入水答案:B8. 为了除去铁粉中的少量铜粉,可以采取以下哪种方法?A. 加入盐酸B. 加入硫酸铜溶液C. 加入硫酸D. 加入水答案:A9. 在实验室中,为了除去硝酸银溶液中的少量氯化银,可以采取的方法是:A. 加入硝酸B. 加热C. 加入水D. 加入盐酸答案:A10. 实验室中,为了除去硫酸铜溶液中的少量硫酸,可以采取的方法是:A. 加入铜粉B. 加入氧化铜C. 加入氢氧化铜D. 加入水答案:A。
除杂题化学初中

选择题:要除去氯化钠溶液中的少量碳酸钠,下列方法中最适宜的是?A. 加入过量稀硫酸B. 加入过量氯化钙溶液(正确答案)C. 加入过量硝酸银溶液D. 加入过量氢氧化钙溶液欲除去铜粉中的少量铁粉,下列方法中最适宜的是?A. 加入过量稀盐酸(正确答案)B. 加入过量硫酸铜溶液C. 加入过量水D. 加入过量氢氧化钠溶液要除去二氧化碳气体中的少量一氧化碳,下列方法中最适宜的是?A. 通过灼热的氧化铜(正确答案)B. 通过灼热的碳层C. 通过澄清石灰水D. 通过氢氧化钠溶液欲除去生石灰中的少量石灰石,下列方法中最适宜的是?A. 加水溶解后过滤B. 加强热至高温(正确答案)C. 加入过量稀盐酸D. 加入过量碳酸钠溶液要除去硝酸钾溶液中的少量硫酸钾,下列方法中最适宜的是?A. 加入过量硝酸钡溶液(正确答案)B. 加入过量氢氧化钠溶液C. 加入过量氯化钾溶液D. 加入过量硝酸银溶液欲除去锌粉中的少量镁粉,下列方法中最适宜的是?A. 加入过量稀硫酸B. 加入过量氢氧化钠溶液(正确答案)C. 加入过量氯化锌溶液D. 加入过量碳酸锌溶液要除去氢气中的少量氯化氢气体,下列方法中最适宜的是?A. 通过氢氧化钠溶液(正确答案)B. 通过浓硫酸C. 通过澄清石灰水D. 通过饱和食盐水欲除去氯化钙溶液中的少量盐酸,下列方法中最适宜的是?A. 加入过量硝酸银溶液B. 加入过量碳酸钙粉末(正确答案)C. 加入过量氢氧化钙溶液D. 加入过量氯化钡溶液要除去铁粉中的少量铝粉,下列方法中最适宜的是?A. 加入过量稀硫酸B. 加入过量氢氧化钠溶液(正确答案)C. 加入过量氯化铁溶液D. 加入过量碳酸钠溶液。
(完整word)初中化学常见物质的除杂总结,推荐文档

初中化学常见物质的除杂总结概念理解首先明白物质除杂是干什么,物质除杂又叫物质提纯,即把混合物中少量的杂质出去,得到较纯净物质的过程。
初中化学除杂、提纯方法及例题将混合物中的几种物质分开而分别得到较纯净的物质,这种方法叫做混合物的分离。
将物质中混有的杂质除去而获得纯净物质,叫提纯或除杂。
1 物理方法1.l 过滤法.原理:把不溶于液体的固体与液体通过过滤而分开的方法称为过滤法。
如:氯化钙(CaCl2)中含有少量碳酸钙(CaCO3)杂质,先将混合物加水(H2O)溶解,由于氯化钙(CaCl2)溶于水,而碳酸钙(CaCO3)难溶于水,过滤除去杂质碳酸钙(CaCO3),然后蒸发滤液,得到固体氯化钙(CaCl2)。
如果要获得杂质碳酸钙(CaCO3),可洗涤烘干。
练习1 下列混合物可以用溶解、过滤、蒸发操作来分离的是:()A.CaCO3 CaO B.NaCl KNO3C.NaNO3 BaSO4D.KCl KClO31.2 结晶法.原理:几种可溶性固态物质的混合物,根据它们在同一溶剂中的溶解度或溶解度随温度的变化趋势不同,可用结晶的方法分离。
eg:除去固体硝酸钾(KNO3)中混有的氯化钠(NaCl)杂质,先在较高温度下制成硝酸钾的饱和溶液,然后逐步冷却,由于硝酸钾(KNO3)的溶解度随温度的升高而显著增大,温度降低,大部分硝酸钾成为晶体析出,而氯化钠的溶解度随温度的升高而增大得不显著,所以大部分氯化钠仍留在母液中,通过过滤把硝酸钾和氨化钠溶液分开。
为进一步提纯硝酸钾,可再重复操作一次,叫重结晶或再结晶。
练习2 下列混合物适宜用结晶法分离的是:()A.NaNO3 Na2CO3B.NaNO3 NaCl C.NaOH Mg(OH)2D.NaCl BaSO42 化学方法:原理(一)、加入的试剂只与杂质反应,不与原物反应。
(二)、反应后不能带入新的杂质。
(三)、反应后恢复原物状态。
(四)、操作方法简便易行。
初中常用化学除杂方法有以下几种:2.1 沉淀法:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
【化学】化学 分离和提纯除杂的专项 培优练习题含详细答案

一、中考初中化学除杂分离和提纯1.下列实验方案能达到实验目的的是()A.A B.B C.C D.D【答案】D【解析】【详解】A、除去KCl溶液中的K2CO3,加入适量的硝酸钙溶液,硝酸钙与碳酸钾反应生成硝酸钾和碳酸钙沉淀,过滤可除去碳酸钙,但引入了新的杂质硝酸钾,故A不正确;B、除去BaCl2溶液中的HCl,加入过量Ba(OH)2溶液,除去了杂质但引入了新杂质Ba(OH)2(过量的),故B不正确;C、稀盐酸和稀硫酸都属于强酸,不能通过比较溶液的pH来区分,故C不正确;D、氢氧化钠固体加水溶解会放出大量的热,溶液温度升高;硝酸铵固体加水溶解会吸收热量,溶液温度降低,可鉴别二者,故D正确。
故选D。
2.要除去氯化钠溶液中含有的少量碳酸钠,可采用的方法是①通入适量的二氧化碳②加入适量的氯化钡溶液③加入适量的稀盐酸④加入适量的石灰水()A.①或③B.②或③C.②或④D.③或④【答案】B【解析】【分析】【详解】①二氧化碳不和碳酸钠溶液反应,不能除去杂质,此项错误;②氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,反应时不会带入新的杂质,故此项正确;③盐酸能和碳酸钠反应,且生成氯化钠,不会带入新的杂质,此项正确;④氢氧化钙溶液能和碳酸钠反应,但反应时会生成氢氧化钠,带入新的杂质,此项错误,故选B。
3.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是( )物质杂质试剂操作方法A K2CO3溶液K2SO4BaCO3加适量BaCO3,粉末,充分反应后,过滤B MgCl2溶液HCl过量Mg(OH)2过滤C CO2水蒸气足量NaOH固体干燥D CaCO3CaO无高温煅烧A.A B.BC.C D.D【答案】B【解析】【分析】除杂条件是不引入新的杂质,加入的物质不和原物质反应。
【详解】A、碳酸钡为沉淀,不能与硫酸钾发生反应,故A不正确;B、加入过量氢氧化镁,氢氧化镁能与盐酸反应生成氯化镁和水,再过滤掉剩余氢氧化镁得到氯化镁溶液,故B正确;C、氢氧化钠与原物质二氧化碳能发生反应,故C不正确;D、高温燃烧时原物质碳酸钙发生分解反应,故D不正确。
初中化学物质除杂(提纯)专题完整版

初中化学物质除杂(提纯)专题完整版除杂(提纯)的原则是保留原物质,不引入新杂质,不减少被提纯物质的质量,以及杂质便于分离。
为了实现这些原则,需要遵循三个原则:①把杂质除掉,保留原物质;②不减少被提纯物质的质量;③杂质便于分离。
除杂的四个要领是:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂,注意加入的试剂不能与原物质反应;④在具体操作中应注意所加试剂的量和操作语言的描述。
一、物理方法1.过滤法:用于除去可溶物和不溶物。
常见的不溶于水的沉淀包括:AgCl、BaCO3、BaSO4、大多数的碳酸盐、以及Cu(OH)2、Fe(OH)3、Al(OH)3等氢氧化物、MnO2等。
2.结晶法:大多数固体物质的溶解度随温度升高而增大,曲线为"陡升型",如KNO3.少数固体物质的溶解度受湿度的影响很小,曲线为"缓升型",如NaCl。
极少数固体物质的溶解度随湿度的升高而减小,曲线为"下降型",如Ca(OH)2.下列混合物适宜用结晶法分离的是:A。
NaNO3 Na2CO3 B。
NaNO3 NaCl C。
NaOH Mg(OH)2 D。
NaCl BaSO4.3.磁铁吸引:用于分离有磁性和无磁性的物质,如铁粉和硫粉、铜粉和铁粉。
4.洗气法:用于分离气体和液体,如H2(H2O)、CO2(H2O)。
二、化学方法1.沉淀法:通过使混合物中的杂质与适当试剂反应生成沉淀,然后通过过滤除去沉淀。
例如,如何除去下列物质中的杂质(括号内为杂质),用化学方程式表示:NaCl( Na2SO4)、HCl ( H2SO4)、HNO3(HCl)、NaCl(MgCl2)。
2.气体法:将混合物中的杂质与适当试剂反应变成气体而除去。
一般规律为:CO32+强酸= CO2;NH4++ OH-= NH3.例如,如何除去下列物质中的杂质(括号内为杂质),用化学方程式表示:NaCl( Na2CO3)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学除杂常用的方法一、物理方法物理方法是根据被提纯物质和杂质之间物理性的差异而除去杂质的方法,初中化学有过滤和结晶两种。
1. 过滤法:是把难溶性物质跟易溶性物质分离的一种方法。
例1. 如何除去食盐中混有的少量泥沙。
简析:将含有泥沙的食盐溶于水,利用食盐溶于水而泥沙不溶,通过过滤,把泥沙从食盐中除去,再把滤液蒸干即得纯净的食盐。
2. 结晶法:是根据几种固体物质的溶解度受温度变化影响的不同,通过冷却或升温的方法使其中的一种物质先结晶出来,然后过滤使结晶出来的晶体与母液分离的一种方法。
例2. 如何除去KNO中混有的少量NaCl。
3配成热的饱和溶液,利用简析:将含有少量NaCl的KNO3的溶解度受温度变化影响大的性质,采用降温冷却的方KNO3法,使KNO结晶析出,而NaCl则留在母液里,再过滤即可得3晶体。
纯净的KNO3二、化学方法采用化学方法,必须遵循以下几个原则:(一).加入的试剂只与杂质反应,不与原物反应。
例如:氢氧化钠中混入碳酸钠。
如果用盐酸来除的话,确实可以把碳酸钠除去,但同时也把氢氧化钠除去了。
(二).反应后不能带入新的杂质。
例如:氢氧化钠中混入碳酸钠。
如果用氯化钙来除的话,确实可以把碳酸钠除去,但同时引进了新的杂质——氯化钠。
(三).反应后恢复原物状态。
对于所要提纯的物质,原来是什么状态,提纯后还应该是什么状态。
一般情况下,我们主要考虑怎样把杂质除掉,对恢复原物状态不做考虑。
(四).操作方法简便易行。
除杂的时候尽力用简单易行的方法进行,尽量避免用高温,电解等方法。
化学方法是根据被提纯物质和杂质之间的化学性质差异,选择不与被提纯物反应而与杂质反应的试剂把杂质除杂的同时,不能给被提纯物带来新的杂质。
常用的方法有以下几种:1. 沉淀法:即将杂质转变为沉淀而除去。
常用的沉淀剂为:Mg Fe Cu 232+++、、等阳离子,一般用可溶性碱,Cl -用Ag +,SO 42-用Ba CO 232+-,用Ca2+。
例3. 如何除去NaCl 中混有的少量Na SO 24。
简析:把混合物溶于水,得到含Na Cl SO +--、、42的溶液,其中SO 42-为杂质离子,可加Ba 2+使SO 42-转变为BaSO 4沉淀而除去,加入的试剂不能带来新的杂质,故试剂的阴离子为Cl -,即向混合溶液中加入BaCl 2溶液至不再产生沉淀为止,过滤、蒸发滤液即得纯净的氯化钠。
Na SO BaCl BaSO NaCl 24242+=↓+2. 气化法:即将杂质转变为气体而除去 例4. 如何除去Na SO 24中混有的少量Na CO 23简析:把混合物溶于水,得到含Na SO CO +--、、4232的溶液,其中CO 32-为杂质离子。
可加酸使CO 32-转变为CO 2气体而除去,加入的试剂不能带来新的杂质,故试剂的阴离子为SO 42-,即加入适量H SO 24后将溶液蒸干即得纯净的Na SO 24。
Na CO H SO Na SO CO H O 23242422+=+↑+3. 转化法:即将杂质转变为被提纯物而除去。
例5. 如何除去CO 2中混有的少量CO 。
简析:把混合气体通过灼热CuO 充分发生反应即可把CO 转变为CO 2而除去。
CO CuOCu CO ++∆24. 置换法:类似于转化法,它是采用合适的置换剂将杂质置换出来而除去。
例6. 如何除去FeSO 4中混有的少量CuSO 4。
简析:把混合物溶于水,得到含Cu Fe SO 2242++-、、的溶液,其中Cu 2+为杂质离子,向混合溶液中加入过量铁粉,铁粉与Cu 2+发生置换反应而除去,然后过滤、蒸发结晶即得纯净的FeSO 4。
Fe CuSO FeSO Cu +=+445.吸收法:两种以上混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
如:一氧化碳中含有二氧化碳时,可将混合气体通过盛有氢氧化钠的溶液。
练习:下列气体中的杂质(括号内的物质是杂质)用吸收法除去,所选试剂正确的是A O 2(H 2O) 用浓H 2SO 4 除水 B CO 2(HCl 用NaOH 溶液除HClC NH 3(H 2O)用浓H2SO4除水 D CO2 (HCl )用Na2CO3溶液除HCl 答案:A C 小结:气体的吸收剂可考虑:浓硫酸吸收水蒸气、氨气;氢氧化钠溶液吸收二氧化碳、二氧化硫、氯化氢气体等;水吸收氨气、氯化氢气体等,氯化钙溶液吸收氨气。
6.其它法:将混合物中的杂质用化学方法转化成其它物质。
如:氧化钙中含有碳酸钙,可采用高温燃烧的方法,使碳酸钙高温分解成氧化钙和二氧化碳,二氧化碳扩散到空气中,除去杂质。
还有如碳酸钠中含有碳酸氢钠,可采用加热的方法专题练习——除杂题1、下列各组离子在水溶液中能大量共存的是()A. H+、Ba2+、NO3-、OH-B. H+、K+、Cl-、CO32-C. Na+、Ag+、NO3-、CO32-D. Na+、K+、OH-、SO42-2、某NaNO3溶液中混有少量NaCl,Na2SO4和Na2CO3杂质,为除去这些杂质,仅提供3种药品:AgNO3溶液、BaCl2溶液和稀HCl。
请设计合理的顺序将杂质逐一除去,并填写下面实验报告。
(简要回答)Ba+ OH-3、在分开盛放的A、B两溶液中,共含有Na+、Cu2+、Ba2+、Mg2+、OH-、NO3-、SO42-七种离子两溶液中所含离子各不相同,已知A溶液里含三种阳离子和两种阴离子,其余在B溶液里,则B溶液里所含离子应该是。
5、分离NaCl、FeCl3和BaSO4的混合物,应选用的一组试剂是()A. H2O、AgNO3、HNO3B. H2O、NaOH、HNO3C. H2O、NaOH、HClD. H2O、KOH、HNO36、欲除去下列各物质中的少量杂质(括号内的物质为杂质),同时,又不能引入新的杂质,分别写出所加试剂和发生反应的化学方程(A ))CO NaCl(Na 32(B )(HCl)HNO 3(C ))CO (Na SO Na 3242 (D ))SO HCl(H 42 7、除去NaOH 中混有的少量32CO Na 杂质,可加入试剂( ) A. 盐酸 B. 石灰水 C. 2CO D. 2CaCl 溶液 8、下列试管内壁的物质能用括号内所给试剂除去的是( )A. 盛石灰水后留下的固体(氢氧化钠溶液)B. 用足量2H 还原CuO 后留下的光亮红色固体(稀盐酸)C. 盛过植物油的试管(热碱液)D. 氯化铁溶液和氢氧化钠溶液反应后留下的固体(水) 9、下列物质中,不能与32CO Na 溶液发生反应的是( )A. 稀3HNOB. KOH 溶液C. 2BaCl 溶液D. 3AgNO 溶液 10、下列各组物质的溶液,两两混合都能发生反应的一组是( )A. 2BaCl 、NaCl 、42SO NaB. 3AgNO 、HCl 、23)(NO CuC. 2)(OH Ca 、32CO K 、HClD. NaOH 、42SO H 、23)(NO Ba 11、硫酸钠溶液中有少量碳酸钠杂质,除去该杂质可加入适量( )A. 稀42SO HB. HClC. 硝酸D. 石灰水 12、为了除去KCl 溶液中含有的少量3FeCl 和42SO K 杂质,应依次加入的试剂是( )A. 先加入适量3AgNO 溶液,再加入适量2BaCl 溶液。
B. 先加入适量2BaCl 溶液,再加入适量3AgNO 溶液。
C. 先加入适量KOH 溶液,再加入适量23)(NO Ba 溶液。
D. 先加入适量KOH 溶液,再加入适量2BaCl 溶液。
13、某溶液中大量含有+Ag ,+2Cu ,+2Ba ,三种阳离子中的两种离子和离子-3NO ,-Cl ,-OH ,-23CO 四种阴离子中的两种离子溶液中大量含有的四种离子应该是( )A. +Ag 、+2Cu 、-3NO 、-ClB. +Ag 、+2Ba 、-Cl 、-OHC. +2Cu 、+2Ba 、-3NO 、-ClD. +2Cu 、+Ag 、-3NO 、-23CO 14、除去硝酸中混有的少量盐酸,可加入的试剂是( ) A. 2BaCl 溶液 B. NaOH 溶液 C. 3AgNO 溶液 D. 23)(NO Ba 溶液 15、除去铜粉中混有的少量氧化铜,其主要操作过程是( ) A.加入过量稀42SO H 微热后,过滤,洗涤 B. 加强热或在空气中灼热。
C.加适量水,加热,过滤,洗涤D.加适量稀42SO H 微热,过滤,洗涤。
16、有CuO 、Fe 、CO 、2)(OH Ba 溶液、32CO Na 溶液、NaOH 溶液和稀42SO H 等7种物质,常温下每两种物质间能发生的化学反应有( )A. 7个B. 6个C. 5个D. 4个17、工业上食盐水的精制是为了除去粗盐中的+2Ca ,+2Mg ,-24SO 及泥沙,可将粗盐溶于水,然后进行下列五项操作:① 过滤 ②加过量的NaOH 溶液 ③加适量的HCl ④ 加过量的32CO Na 溶液 ⑤ 加过量的2BaCl 溶液。
正确操作顺序是( )A. ①④②⑤③B. ④①②⑤③C. ②⑤④①③D. ⑤④①②③ 18、某溶液中仅含+K ,+2Mg ,-24SO ,-Cl 四种离子,其中离子个数比为::2++Mg K 8:5:4=-Cl ,若+K 为8m 个,则-24SO 离子个数可能是( ) A. 1m B. 2m C. 4m D. 6m19、将下列试剂分别滴入硝酸铜溶液,碳酸钠溶液和稀盐酸中,能观察到三种不同现象的是( )A. 氢氧化钾溶液B.氯化钡溶液C. 氢氧化钙溶液D. 氯化钾溶液 20、在不用指示剂的条件下,欲将含有盐酸的氯化钡溶液由酸性变为中性,应选用的最佳试剂是( )A. 氢氧化钡溶液B. 硝酸银溶液C. 碳酸钡粉末D. 生石灰粉末 21、 某工厂的废渣中混有少量的锌粒和氧化铜(其它成分不跟酸反应),与大量废盐酸接触能形成污水,产生公害,若向污水中撒入铁粉,且反应后铁粉有剩余,此时污水中一定含有金属离子是( )A. +2Fe ,+2CuB. +2Cu ,+HC. +2Zn ,+2FeD. +2Zn ,+H22、当土壤的pH 值为4时,农作物不能生长,现要改良它,应撒施的物质是( )A. 食盐B. 石灰石C. 熟石灰D. 胆矾 23、某溶液中存在+2Mg 、+Ag 、+2Ba 三种阳离子,现用NaOH ,32CO Na 和NaCl 三种溶液使它们转化为沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,则所加溶液的顺序正确的是( )A. NaCl 、NaOH 、32CO NaB. 32CO Na 、NaCl 、NaOHC. NaOH 、NaCl 、32CO NaD. NaCl 、32CO Na 、NaOH 24、某溶液中滴加2BaCl 溶液,产生不溶于稀3HNO 的白色沉淀,则该溶液中可能含有的离子是( )A. +AgB. -24SOC. +Ag 或-24SOD. -3NO 25、下列反应能够一步实现的是( )A. 32CaCO CaCl →B. 3FeCl Fe →C. 2)(OH Cu CuO →D. NaCl NaNO →326、在23)(NO Hg 、23)(NO Cu 和23)(NO Zn 的混合溶液中,加入足量的铁粉,充分反应后,溶液中存在的溶质是( )A. 23)(NO Zn 和23)(NO FeB. 23)(NO Cu 和23)(NO ZnC. 只有23)(NO ZnD. 只有23)(NO Fe27、NaCl 溶液中混有少量4MgSO ,若加一种试剂除去,该试剂是 。
