高一化学方程式总结
高一化学方程式大全总结

高一化学方程式大全总结化学方程式大全包括了化学反应中的所有反应方程式。
化学方程式由反应物、生成物和反应条件组成,用化学符号表示。
下面是一些高一化学常见的反应方程式的总结:1.酸碱中和反应方程式:酸+碱→盐+水例如:HCl + NaOH → NaCl + H2O2.金属与酸反应的方程式:金属+酸→盐+氢气例如:2HCl + Mg → MgCl2 + H23.金属与非金属氧化物反应方程式:金属+氧化物→相应的金属氧化物例如:Ca + O2 → CaO4.金属与水反应方程式:金属+水→金属氢氧化物+氢气例如:2Na + 2H2O → 2NaOH + H25.金属与非金属氧化物的反应方程式:金属+非金属氧化物→相应的金属氧化物例如:2Al + 3Cl2O → Al2O3 + 3Cl26.金属与酸性氧化物反应方程式:金属+酸性氧化物→相应的金属氧化物+气体例如:Mg + CO2 → MgO + C7.金属与金属氧化物反应方程式:金属+金属氧化物→相应的金属+氧化物例如:2K + Fe2O3 → 2Fe + K2O8.单质在氧气中燃烧方程式:非金属+氧气→氧化物例如:C + O2 → CO29.碱金属与水反应方程式:碱金属+水→碱式氢氧化物+氢气例如:2Na + 2H2O → 2NaOH + H210.烧碱与酸反应方程式:烧碱+酸→盐+水例如:NaOH + HCl → NaCl + H2O11.过滤反应方程式:固体/悬浊液+溶液→溶液+沉淀例如:AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq) 12.沉淀反应方程式:离子交换反应:阳离子+阴离子→沉淀例如:BaCl2(aq) + Na2SO4(aq) → BaSO4(s) + 2NaCl(aq) 13.气体生成反应方程式:反应物→生成物+气体例如:2H2O2(aq) → 2H2O(l) + O2(g)14.氧化还原反应方程式:氧化剂+还原剂→氧化物+还原物例如:2Na + Cl2 → 2NaCl15.高温分解反应方程式:反应物→生成物例如:2H2O(g) → 2H2(g) + O2(g)这些只是化学方程式的一小部分,还有许多其他类型的化学方程式,例如植物光合作用方程式、电解反应方程式、酸雨反应方程式等等。
高一化学方程式总结大全

高一化学方程式总结大全一、碱金属:1. 新切的钠有银白色光泽,但很快发暗;方程式:4Na+O2=2Na2O;该产物不稳固。
钠在空气中燃烧时,发出黄色的火焰;同时生成淡黄色的固体,方程式:2Na+O2点燃==== Na2O2。
锂燃烧方程式:4Li+O2点燃==== 2Li2O;钾燃烧方程式:K+O2点燃==== KO2。
2. 钠与氧气在不点火时安稳反应,硫的化学性质不如氧气活泼,将钠粒与硫粉混合时爆炸,方程式:2Na+S=Na2S3. 钠与水剧烈反应后滴有酚酞的水变成红色,方程式:2Na+2H2O=2NaOH+H2↑;钾与水反应更剧烈,乃至爆炸,为了安全,常在小烧杯上盖一块小玻璃片。
4. 过氧化钠粉末用脱脂棉包住,①滴几滴水,脱脂棉燃烧;方程式:2Na2O2+2H2O=4NaOH+O2↑;②用玻璃管吹气,脱脂棉也燃烧;有关的方程式:2Na2O2+2CO2=2Na2CO3+O2↑;这两个反应都是放热反应,使脱脂棉到达着火点。
在过氧化钠与水或CO2反应生成O2的两个反应中,为生成1mol O2,需要的Na2O2的物质的量都为2mol,同时需要的H2O或CO2的物质的量都为2mol。
5. 纯碱的化学式是Na2CO3 ,它不带结晶水,又俗名苏打。
碳酸钠晶体化学式是Na2CO3?10H2O,在空气中不稳固,容易失去结晶水,风化,最后的产物是粉末状,叫无水碳酸钠。
钠、氧化钠、过氧化钠、氢氧化钠等在空气中露置的最后产物都是无水碳酸钠。
6. 碳酸钠和碳酸氢钠两种固体物质都可以与盐酸反应放出气体,有关离子方程式分别为:CO32-+2H+=H2O+CO2↑;HCO3-+H+=H2O+CO2↑;其中,以碳酸氢钠与盐酸的反应速度更快;如果碳酸钠和碳酸氢钠的质量相同,当它们完全反应时消耗的盐酸以碳酸钠为多。
7. 碳酸钠和碳酸氢钠的热稳固性较差的是碳酸氢钠,其加热时产生分解,方程式是:2NaHCO3=Na2CO3+H2O+CO2↑。
(完整版)高一化学必修一化学方程式大全

高一化学必修一化学方程式大全1、钠在空气中燃烧(黄色的火焰)2Na +O2==【点燃】Na2O2钠块在空气中变暗4Na+O2=2Na2ONa2O在空气中加热(变黄)2Na2O+O2=2Na2O22、钠与水反应(浮、熔、游、响、红)2Na +2H2O =2H2O +H2 ↑2Na +2H2O =2Na+ +2OH- +H2↑3、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白)2Na2O2 +2H2O =4NaOH +O2 ↑2Na2O2 +2H2O =4Na+ +4OH -+O2↑碱性氧化物Na2O与水的反应Na2O+H2O=2NaOH4、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是:2Na2O2 +2CO2 =2Na2CO3 +O25、苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶液Na2CO3 +2HCl =2NaCl +H2O+CO2↑CO32- +2H+=H2O +CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3 +HCl =NaHCO3 +NaClCO32- +H+ =HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+ =H2O +CO2↑6、小苏打受热分解2NaHCO3==【加热】Na2CO3 +H2O +CO2 ↑7、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 +NaOH==【加热】Na2CO3 +H2OHCO3-+OH - =H2O +CO32-(若是溶液中反应有离子方程式)8、金属锂在空气中燃烧4Li +O2==【加热】2Li2O9、氯气的性质铜丝在氯气中剧烈燃烧(棕色烟)Cu +Cl2==【点燃】CuCl2之后加水,可由绿色溶液(浓)得到蓝色溶液(稀)Cl2 +2FeCl2 =2FeCl32Cl2+2NaBr=2NaCl+Br2Cl2 +2NaI =2NaCl+I2Cl2+SO2 +2H2O=H2SO4 +2HCl2Na +Cl2 ==【点燃】2NaCl10、铁在氯气中剧烈燃烧2Fe +3Cl2==【点燃】3FeCl311、氢气在氯气中燃烧(苍白色火焰)H2 +Cl2==【点燃】2HCl氟气与氢气反应(黑暗处即可爆炸)H2+F2=2HF12、氯气溶于水(新制氯水中含H+、Cl-、ClO-、OH-、Cl2、HClO、H2O)Cl2 +H2O =HCl +HClOCl2 +H2O =H++Cl- +HClO13、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)2HClO==【光照】2HCl +O2↑14、工业制漂白粉的原理及漂白粉的失效2Ca(OH)2 +2Cl2 =Ca(ClO)2 +CaCl2 +2H2O2Ca(OH)2 +2Cl2 =2Ca2++2ClO-+2Cl-+2H2OCa(ClO)2+CO2+H2O=CaCO3↓+2HClO2HClO==【光照】2HCl +O2↑Ca2-+2ClO-+CO2 +H2O =CaCO3↓+2HClO15、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶)MnO2 +4HCl(浓)==【加热】MnCl2+Cl2↑+2H2OMnO2 +4H++2Cl-==【加热】Mn2++Cl2↑+2H2O16、新制氯水注入盛溴化钠溶液的试管中Cl2 +2NaBr =Br2 +2NaClCl2 +2Br- =Br2 +2Cl-17、铁与硫加热反应Fe +S==【加热】FeS铁与氧气加热反应3Fe+2O2==【加热】Fe3O4铁在氯气中加热反应2Fe+3Cl2==【加热】2FeCl318、铜与浓硫酸反应:Cu+2H2SO4 (浓) ==【加热】CuSO4 +2H2O+SO2 ↑19、碳与浓硫酸反应:C+2H2SO4(浓)==【加热】2H2O+CO2↑+2SO2↑20、工业制单质硅(碳在高温下还原二氧化硅)SiO2 +2C=(高温)Si +2CO↑21、二氧化硅与氢氧化钠反应SiO2 +2NaOH =Na2SiO3 +H2OSiO2 +2OH+ =SiO32- +H2O22、氮气和氢气反应(工业合成氨)N2 +3H2→【催化剂】2NH32NH3→【高温高压】N2 +3H223、氮气和氧气放电下反应(雷雨发庄稼)N2 +O2=(放电)2NO2NO +O2=2NO2二氧化氮溶于水3NO2 +H2O =2HNO3 +NO3NO2 +H2O =2H++2NO3-+NO24、HNO3与Fe的反应Al、Fe遇浓HNO3、浓硫酸钝化(常温)Fe与浓HNO3加热Fe+6HNO3==【加热】Fe(NO3)3+3NO2↑+3H2OFe与稀HNO3反应Fe+4HNO3=Fe(NO3)3+NO↑+2H2O3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O25、NO2 、O2 的混合气通入水中无剩余气体4NO2 +O2 +2H2O = 4 HNO326、NO 、O2 的混合气通入水中无剩余气体4NO +3O2 +2H2O = 4 HNO327. 氨的催化氧化4NH3 +5O2 ==【催化剂、加热】4NO +6H2O28. 碳酸氢铵受热分解NH4HCO3==【加热】NH3 ↑+H2O↑+CO2↑29. 用浓盐酸检验氨气(白烟生成)HCl +NH3 =NH4Cl30. 硫酸铵溶液与氢氧化钠溶液混合加(NH4)2SO4 +2NaOH==【加热】2NH3↑+Na2SO2 +2H2O NH4++OH-==【加热】NH3 ↑+H2O31. 硝酸铵溶液与氢氧化钠溶液混合(不加热)NH4NO3 +NaOH =NH3·H2O +NaNO3NH4++OH-=NH3·H2O32. 铝箔在氧气中剧烈燃烧4Al +3O2 ==2Al2O333. 铝片与稀盐酸反应2Al +6HCl =2AlCl3 +3H2↑2Al +6H+=2Al3++3H2↑34. 铝与氢氧化钠溶液反应2Al+2NaOH +2H2O =2NaAlO2 +3H2↑2Al +2OH-+2H2O =2AlO2-+3H2↑35. 铝与三氧化二铁高温下反应(铝热反应)2Al +Fe2O3==【高温】2Fe +Al2O336. 镁在二氧化碳中燃烧2Mg +CO2 ==【点燃】2MgO + C37. 氧化铝溶于氢氧化钠溶液Al2O3 +2NaOH = 2NaAlO2 +H2OAl2O3 +2OH-=2AlO2-+H2O38. 硫酸铝溶液中滴过量氨水Al2(SO4)3 +6NH3·H2O=2Al(OH)3↓+(NH4)2SO4Al3++ 3 NH3·H2O =Al(OH)3↓+3NH4+39. ①氢氧化铝溶液中加盐酸Al(OH)3 +3HCl =AlCl3 +3H2OAl(OH)3 +3H+=Al3++3H2O②Al(OH)3与NaOH溶液反应Al(OH)3 +NaOH =NaAlO2 +2 H2OAl(OH)3 +OH-=AlO2-+2 H2O40. 高温下铁与水反应3Fe +4H2O(g)==【高温】Fe3O4 +4H241. 铁与盐酸反应Fe +2HCl =FeCl2 +H2↑Fe +2H+=Fe2++H2↑42. 氧化铁溶于盐酸中Fe2O3 +6HCl =2FeCl3 +3H2OFe2O3 +6H+=2Fe3++3H2O43. 氯化铁中滴入氢氧化钠溶液(红褐色沉淀)FeCl3 +3NaOH =Fe(OH)3 ↓+3NaClFe3++3OH-=Fe(OH)3 ↓44. 氢氧化亚铁在空气中被氧化(白色沉淀变为红褐色沉淀)4Fe (OH)2 +O2 +2H2O =4Fe (OH)345. 氯化亚铁溶液中通入氯气2FeCl2 +Cl2 =2FeCl32 Fe2++Cl2 = 2 Fe3++2Cl-46. 氯化铁溶液中加入铁粉2FeCl3 +Fe =3FeCl22Fe3++Fe =3Fe2+47. 用KSCN检验的存在离子方程式Fe3++3SCN-= Fe(SCN)3。
高一化学必修一知识点总结化学方程式

高一化学必修一知识点总结化学方程式高一化学必修一化学方程式(一)钠1、钠在空气中燃烧(黄色的火焰):2Na + O2 Na2O22、钠块在空气中变暗:4Na+O2=2Na2O3、Na2O在空气中加热(变黄):2Na2O+O22Na2O24、金属锂在空气中燃烧:4Li + O2 2Li2O5、钠与水反响(浮、熔、游、响、红)2Na + 2H2O = 2NaOH+ H2 ↑2Na + 2H2O = 2Na+ + 2OH - + H2 ↑Na2O 、Na2O2的相关反响:1、碱性氧化物Na2O与水的反响:Na2O+H2O=2NaOH2、过氧化钠与水的反响(放热反响、Na2O2是强氧化剂,可用于漂白)2Na2O2 + 2H2O = 4NaOH + O2 ↑2Na2O2 + 2H2O = 4Na++4OH -+O2↑3、碱性氧化物Na2O与CO2的反响Na2O + CO2 = Na2CO34、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源(供氧剂),原因是: 2Na2O2 + 2CO2 = 2Na2CO3 + O25、 Na2O + SO2 = Na2SO3 Na2O2 + SO2 = Na2SO46、Na2O +2HCl = 2NaCl + H2O7、2Na2O2 +4 HCl = 4 NaCl + 2 H2O + O2 ↑NaHCO3与Na2CO31、小苏打受热分解: 2NaHCO3 Na2CO3 + H2O +CO2 ↑2、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 + NaOH Na2CO3 + H2O3、假设是氢氧化钠和碳酸氢钠溶液中反响有离子方程式:NaHCO3 + NaOH = Na2CO3 + H2O HCO3-+ OH - = H2O + CO32-4、向NaOH溶液中通入少量CO2 :2NaOH + CO2 = Na2CO3 + H2O5、继续通入过量CO2 :Na2CO3 + CO2 + H2O = 2 NaHCO3总反响方程式:NaOH + CO2 = NaHCO36、苏打(纯碱)与盐酸反响:①盐酸中滴加纯碱溶液Na2CO3 + 2HCl = 2NaCl + H2O +CO2↑ CO32- + 2H+ = H2O + CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3 + HCl =NaHCO3 + NaCl CO32- + H+ = HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑ HCO3-+H+ = H2O +CO2↑7、(1)Na2CO3溶液、NaHCO3溶液与Ca(OH)2反响:Na2CO3 +Ca(OH)2 = CaCO3↓+2 NaOHNaHCO3 +Ca(OH)2(多)= CaCO3↓+ NaOH +H2O2NaHCO3 +Ca(OH)2(少)= CaCO3↓+ Na2CO3 +2H2O8、 Na2CO3溶液、NaHCO3溶液与CaCl2反响:Na2CO3 +CaCl2 = CaCO3↓+2 Na ClNaHCO3溶液与CaCl2 不反响;高一化学必修一化学方程式(二)Fe1、铁与硫加热反响 Fe + S FeS2、铁与氧气加热反响 3Fe+2O2 Fe3O43. 铁在氯气中加热反响 2Fe+3Cl2 2FeCl34、高温下铁与水蒸气反响: 3Fe + 4H2O(g) Fe3O4 + 4H25、铁与盐酸反响:Fe + 2HCl = FeCl2 + H2↑ Fe + 2H+ = Fe2+ + H2↑6.铁的氧化物FeO 、Fe2O3 、Fe3O4溶于盐酸中:1)FeO + 2HCl = FeCl2 + H2OFeO + 2H+ = Fe2+ + H2O2)Fe2O3 + 6HCl = 2FeCl3 + 3H2OFe2O3 + 6H+ = 2Fe3+ + 3H2O3) Fe3O4 + 8HCl = FeCl2 +2FeCl3 +4H2OFe3O4 + 8H+ =Fe2+ +2Fe3+ +4 H2O7.Fe(OH)2 、Fe(OH)3 的制备:1) FeSO4 + 2NaOH = Fe(OH)2 ↓+Na2SO4Fe2+ + 2OH - = Fe(OH)2 ↓氯化铁中滴入氢氧化钠溶液(红褐色沉淀)2)FeCl3 + 3NaOH = Fe(OH)3 ↓+3NaClFe3+ + 3OH - = Fe(OH)3 ↓氢氧化亚铁在空气中被氧化(白色絮状沉淀迅速变成灰绿色,最后变为红褐色沉淀)3)4Fe (OH)2 + O2 + 2H2O = 4Fe (OH)34)不稳定性:2Fe(OH)3 Fe2O3 + 3H2O8.Fe2+ 、Fe3+ 之间的转化:1)氯化亚铁溶液中通入氯气(或者加氯水)2FeCl2 + Cl2 = 2FeCl32 Fe2+ + Cl2 = 2 Fe3+ + 2Cl-2)氯化铁溶液中参加铁粉:2FeCl3 + Fe = 3FeCl22Fe3+ + Fe = 3Fe2+3)用KSCN检验Fe3+的存在:离子方程式:Fe3++3SCN-= Fe (SCN)3 (血红色)4)印刷电路板:2FeCl3 + Cu = 2FeCl2 +CuCl2高一化学必修一化学方程式(三)(1)硫与非金属:S + O2 SO2 H2+ S H2S(2)硫与金属:Fe + S FeS 2Cu + S Cu2S(3)二氧化硫与水反响:SO2 + H2O H2SO3(4)二氧化硫与碱性氧化物反响:SO2 + CaO = CaSO3(5)二氧化硫与碱反响:SO2 + 2NaOH = Na2SO3 + H2O SO2 + Ca(OH)2 =CaSO3↓ + H2O(6)二氧化硫与硫化氢气体反响:2H2S +SO2 = 3S↓ + 2H2O(7)二氧化硫通入氯水中:SO2 + Cl2 + 2H2O = 2HCl + H2SO4(Cl2可换作Br2、I2) (8)二氧化硫被O2氧化:2SO2 + O2 2SO3(9)三氧化硫与水反响:SO3 + H2O = H2SO4(10)三氧化硫与碱反响:SO3 + Ca(OH)2 = CaSO4↓ + H2O(12)工业合成氨:N2 + 3H2 2NH3(13)氨的催化氧化:4NH3 +5O2 4NO + 6H2O(14)NH3在水中的反响:NH3 + H2O NH3• H2O NH4+ + OH-(15)氨水受热分解:NH3•H2O NH3↑ + H2O(16)实验室制取氨气:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2H2O(17)碳酸氢铵受热分解:NH3 ↑+ H2O↑ + CO2↑(18)用浓盐酸检验氨气(白烟生成): HCl + NH3 = NH4Cl(19)氯化铵受热分解:NH4Cl NH3↑ + HCl↑(20)硫酸铵溶液与氢氧化钠溶液混合加(NH4)2SO4 +2NaOH2NH3↑+Na2SO4 +2H2O NH4+ + OH - NH3 ↑+ H2O(21)硝酸铵溶液与氢氧化钠溶液混合(不加热)(检验NH4+的方法)NH4NO3 + NaOH = NH3↑+H2O + NaNO3 NH4+ + OH- = NH3↑+H2O(22)氮气和氧气放电下反响(雷雨发庄稼)N2 + O2 2NO 2NO + O2 2NO2(23)二氧化氮溶于水:3NO2 + H2O 2HNO3 + NO3NO2 + H2O 2H++ 2NO3-+NO(24)NO2 、O2 的混合气通入水中无剩余气体: 4NO2 + O2 + 2H2O = 4 HNO3(25)NO 、O2 的混合气通入水中无剩余气体: 4NO + 3O2 + 2H2O = 4 HNO3(26)NO、NO2的回收:NO2 + NO + 2NaOH = 2Na NO2+ H2O5、浓硫酸、HNO3与Cu反响:Al、Fe遇浓HNO3、浓硫酸钝化(常温)(27)Cu与浓HNO3加热:Cu+4HNO3 (浓)= Cu(NO3)2 +2NO2↑+ 2H2O(28)Cu与稀HNO3反响:3Cu+8HNO3 (稀)= 3Cu(NO3)2 +2NO↑+ 4H2O(29)铜与浓硫酸反响:Cu+2H2SO4 (浓) CuSO4 +2H2O+SO2 ↑(30)浓硫酸与木炭反响:C+2H2SO4(浓) 2H2O+CO2↑+2SO2↑(31)浓硝酸与木炭反响:C+4HNO3(浓) 2H2O+CO2↑+4NO2↑。
高一化学方程式总结归纳

高一化学方程式总结归纳化学方程式是根据化学反应得出来的公式,如果反应有特定的条件,书写的时候一律标注该特定条件。
今天小编在这给大家整理了高一化学方程式总结归纳_高一化学方程式有哪些,接下来随着小编一起来看看吧!高一化学必修一离子反应知识点高一化学必修1氧化还原反应知识高中化学学习方法与技巧生活中的化学现象大全高一化学方程式(一)Cl2+Cu==CuCl2(点燃条件)、3Cl2+2Fe==2FeCl3Cl2+2Na==2NaCl、Cl2 + H2==2HCl3Cl2 +2P==2PCl3、Cl2 + PCl3==PCl5Cl2+H2O==HCl+HClO Cl2+2NaOH===NaCl+NaClO+H2O 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2OCl2+2FeCl2===2FeCl3Ca(ClO)2+H2O+ CO2(少量)== Ca CO3↓+2 HClOCa(ClO)2+2H2O+ 2CO2(多量)== Ca(HCO3)2↓+2 HClOCa(ClO)2+2 HCl == Ca Cl2+2 HClO(强酸制弱酸) 2HClO 2HCl+O2↑F2 + H2 === 2HF 2F2 +2H2O===4HF+O2Br2 + H2 === 2H Br(500oC) I2 + H2 2HI2Cl2+2NaBr===2NaCl+Br2 Cl2 +2 K I ===2 K Cl+I2HCl + AgNO3 === AgCl↓+ HNO3 Br2 +2 K I ===2 K Br+I2 4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2OHCl + AgNO3 === AgCl↓ + HNO3 HCl + AgNO3 =AgCl↓(白色)+HNO3NaBr+AgNO3 = AgBr↓(浅黄色)+NaNO3 NaI + AgNO3 === AgI↓(黄色)+ Na NO32AgBr 2Ag+Br2(AgCl、AgI类似) Na2SO3+ H2O +Cl2== Na2SO4 +2HCl高一化学方程式(二)歧化反应Cl2+H2O==HCl+HClO(加碱或光照促进歧化:(Cl2+H2O H++Cl+HClO)Cl2+2NaOH==NaCl+NaClO+H2O(Cl2+2OH=Cl+ClO+H2O) Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O(Cl2+2OH=Cl+ClO +H2O)3Cl2+6KOH(浓)5KCl+KClO3+3H2O(3Cl2+6OH 5Cl+ClO3+3H2O)3S+6NaOH 2Na2S+Na2SO3+3H2O(3S+6OH 2S2+SO32+3H2O)4P+3KOH(浓)+3H2O==PH3+3KH2PO2(4P+3OH+3H2O==P H3+3H2PO2)11P+15CuSO4+24H2O==5Cu3P+6H3PO4+15H2SO43C+CaO CaC2+CO3C+SiO2 SiC+2CO1.镁与盐酸响应:Mg + 2H+ = Mg2+ + H22.铝与盐酸响应2Al + 6H+ = 2Al3+ +3H23.锌与盐酸响应Zn + 2H+ = Zn2+ + H24.铁与稀硫酸响应Fe + 2H+ = Fe2+ + H25.氧化镁与稀硫酸响应MgO + 2H+ = Mg2+ + H2O6.氧化铁与稀盐酸响应Fe2O3 + 6H+ = 2Fe3+ + 3H2O7.氢氧化钠与稀硫酸响应OH- + H+ = H2O8.氢氧化镁与稀盐酸响应Mg(OH)2 + 2H+ = Mg2+ + 2H2O9.硝酸银与稀盐酸响应Ag+ + Cl-= AgCl10.氯化钡与稀硫酸响应Ba2+ + SO42- = BaSO411.氢氧化钡与稀硫酸响应Ba2++2OH-+2H++SO42-= BaSO4+2H2O 12.氯化镁与氢氧化钠溶液响应Mg2+ +2OH-= Mg(OH)213.二氧化碳与氢氧化钠溶液响应CO2 + 2OH- == CO32-+ H2O14.过量的二氧化碳与氢氧化钠溶液响应CO2 + OH-== HCO3-15.二氧化硫与氢氧化钠溶液响应SO2 + 2OH- == SO32- + H2O16.过量的二氧化硫与氢氧化钠溶液响应SO2 + OH-== HSO3-17.二氧化碳与澄清的石灰水响应CO2 + Ca2+ +2OH-== CaCO3+ H2O 18.氢氧化钙溶液与纯碱溶液响应Ca2+ + CO32-== CaCO319.氢氧化钡溶液与碳酸钠溶液响应Ba2+ + CO32-== BaCO320.硫酸铜溶液与氢氧化钾溶液响应Cu2+ + 2OH-== Cu(OH)2高一化学方程式(三)还原性 S+4H++6==6NO2+2H2O+3S+4HNO3(稀)=3SO2+4NO+2H2O3S+4H++4=3SO2+4NO+2H2ON2+O2=2NO4P+5O2=P4O10(常写成P2O5)2P+3X2=2PX3(X表示F2,Cl2,Br2) PX3+X2 PX5P4+20HNO3(浓) 4H3PO4+20NO2+4H2OC+2F2 CF4 C+2Cl2 CCl4C+O2(足量) CO2 2C+O2(少量) 2COC+CO2 2CO C+H2O CO+H2(生成水煤气)2C+SiO2 Si+2CO(制得粗硅)Si(粗)+2Cl2 SiCl4 (SiCl4+2H2===Si(纯)+4HCl)Si(粉)+O2 SiO2 Si+C SiC(金刚砂)Si+2NaOH+H2O==Na2SiO3+2H2(Si+2OH +H2O= +2H2)高一化学方程式(四)高一必修一必修二化学方程式(1) 4Na+O2=2Na2O (2) Na2O+O2 2Na2O2(3) 2Na+O2 Na2O2 (注:反应条件不同;生成物也不同。
高一必修一化学方程式总结(全)

...高一化学方程式总结〔1〕.Fe与O2:3Fe+2O2Fe3O4 一.钠:〔2〕.Al2O3电解:2Al2O34Al+3O2↑〔1〕.Na在空气中与O2:4Na+O2=2Na2O〔白色〕〔2〕.Na在O2中燃烧:2Na+O2Na2O2〔淡黄色〕〔3〕.Na与S:2Na+S=Na2S〔研磨即爆炸〕〔4〕.Na与Cl2:2Na+C2l2NaCl〔5〕.Na与H2O:2Na+2H2O=2NaOH+H2↑〔2Na+2H2O +-=2Na+2OH+H2↑〕+〔6〕.Na与HCl:2Na+2HCl=2NaCl+H2↑〔2Na+2H +=2Na+H2↑〕〔7〕.Na与CuSO4溶液:2Na+2H2O+CuSO4=Na2SO4+ Cu(OH)2↓+H2↑〔8〕.Na与FeC3l溶液:6Na+6H2O+2FeC3l=6NaCl+ 〔3〕.Fe与H2O〔g〕高温:3Fe+4H2O〔g〕Fe3O4+4H23+2+〕〔4〕.FeCl3+Fe:2FeCl3+Fe=3FeC2l〔2Fe+Fe=3Fe2+3+〔5〕.FeCl2+Cl2:2FeCl2+Cl2=2FeCl3〔2Fe+Cl2=2Fe -+2Cl〕〔6〕.FeCl3与Cu:2FeCl3+Cu=2FeC2l+CuC2l(用于雕刻3+2+2+〕铜线路板)〔2Fe+Cu=2Fe+Cu〔7〕.FeO与HCl:FeO+2HCl=FeC2l+H2O〔同H2SO4〕+2+〔FeO+2H=Fe+H2O〕〔8〕.Fe2O3与HCl:Fe2O3+6HCl=2FeC3l+3H2O〔同+=2Fe3++3H2O〕H2SO4〕〔Fe2O3+6H〔9〕.Fe3O4与HCl:Fe3O4+8HCl=2FeC3l+FeC2l+4H2O +2+3+〔同H2SO4〕〔Fe3O4+8H=Fe+2Fe+4H2O〕〔10〕.FeSO4与NaOH:FeSO4+2NaOH=Fe(OH)2↓+2Fe(OH)3↓+3H2↑〔9〕.Na2O与H2O:Na2O+H2O=2NaOH 〔10〕.Na2O与CO2:Na2O+CO2=Na2CO32+-=Fe(OH)2↓〕Na2SO4〔Fe+2OH〔11〕.FeCl3与NaOH:FeCl3+3NaOH=Fe(OH)3↓+3NaCl〔11〕.Na2O2与H2O:2Na2O2+2H2O=4NaOH+O2↑+-〔2Na2O2+2H2O=4Na+4OH+O2↑〕〔12〕.Na2O2与CO2:2Na2O2+2CO2=2Na2CO3+O2〔供氧〕〔13〕.Na2CO3与HCl:Na2CO3+2HCl=2NaCl+H2O+2-+CO2↑〔互滴鉴别〕〔CO3+2H=H2O+CO2↑〕〔14〕.NaHCO3与HCl:NaHCO3+HCl=NaCl+H2O+CO2 -+↑〔HCO3+H=H2O+CO2↑〕〔15〕.NaHCO3与NaOH:NaHCO3+NaOH=Na2CO3+H2O --2-〔HCO3+OH=CO3+H2O〕〔16〕.Na2CO3与H2O与CO2:Na2CO3+H2O+CO2=2--〕2NaHCO3〔鉴别、除杂〕〔CO3+H2O+CO2=2HCO33+-=Fe(OH)+3OH3↓〕+〔Fe(OH)3+3H3+=Fe〔Fe〔12〕.Fe(OH)2与H2O与O2:4Fe(OH)2+2H2O+O2=4Fe(OH)3〔白色沉淀→灰绿色沉淀→红褐色沉淀〕〔13〕.Fe(OH)2与HCl.Fe(OH)2+2HCl==FeC2l+2H2O+2+〔Fe(OH)2+2H=Fe+2H2O〕〔14〕.Fe(OH)3与HCl:Fe(OH)3+3HCl==FeC3l+3H2O+3H2O〕〔15〕.Fe(OH)3加热:2Fe(OH)3Fe2O3+3H2O 〔16〕.FeCl3与KSCN F:eCl3+3KSCN==Fe(SCN3+)3KCl 3+-3+〔Fe=Fe(SCN3)〕(红色溶液,用于鉴别Fe +3SCN)〔17〕.NaHCO3分解:2NaHCO3Na2CO3+H2O+CO2↑〔18〕.NaOH与CO2(少量):2NaOH+CO2(少量)=Na2CO3 -2-+H2O〔2OH+CO2(少量)=CO3 +H2O〕〔17〕.FeCl3与H2S(少量):2FeCl3+H2S(少量)=2FeC2l+2HCl+S↓〔18〕.FeCl3与KI:2FeCl3+2KI=2FeC2l+2KCl+2I↓〔19〕.FeCl3与H2O:FeCl3+3H2OFe(OH)3(胶体)+3HCl〔19〕.NaOH与CO2〔过量〕:NaOH+CO2〔过量〕=NaHCO3〔OH --〕+CO2〔过量〕=HCO3二.铝:〔20〕.C与H2O:C+H2OCO+H2(生成水煤气) 四.硅:〔1〕Si与NaOH与H2O:Si+2NaOH+H2O=Na2SiO3+-2-2H2↑〔Si+2OH+H2O=SiO3+2H2↑〕...〔1〕.Al与6HCl:2Al+6HCl=2AlC3l+3H2↑〔同H2SO4〕〔2Al+6H+=2Al3++3H2↑〕〔2〕Si与HF:Si+4HF=SiF4+2H2↑〔3〕Si与F2:Si+2F2=SiF4〔2〕.Al与NaOH与H2O:2Al+2NaOH+2H2O=2--NaAlO2+3H2↑〔2Al+2OH+2H2O=2AlO2+3H2↑〕〔3〕.Al2O3与HCl:Al2O3+6HCl=2AlC3l+3H2O+3+〔Al2O3+6H=2Al+3H2O〕〔4〕.Al2O3与NaOH:Al2O3+2NaOH=2NaAlO2+H2O--〔Al2O3+2OH=2AlO2+H2O〕〔5〕.Al(OH)3与HCl:Al(OH)3+3HCl=AlC3l+3H2O+3+〔Al(OH)3+3H=Al+3H2O〕〔6〕.Al(OH)3与NaOH:Al(OH)3+NaOH=NaAlO2+2H2O--〔Al(OH)3+OH=AlO2+2H2O〕〔7〕.2Al(OH)3Al2O3+3H2O〔8〕.AlCl3与NH3·H2O:AlCl3+3NH3·H2O=Al(OH)3↓+3++3NH4Cl〔Al+3NH3·H2O=Al(OH)3↓+3NH4〕〔9〕.NaAlO2与HCl与H2O:-+NaAlO2+HCl+H2O=NaCl+Al(OH)3↓〔AlO2+H+H2O=Al(OH)3↓〕〔4〕Si与O2:Si+O2SiO2〔研细的硅与纯氧〕〔5〕Si与C:Si+CSiC〔6〕C与SiO2:2C+SiO22CO↑+Si〔工业制粗硅〕〔7〕Cl2:与Si:2Cl2+Si=SiC4l〔8〕SiC4l与H2:SiCl4+2H2=Si+4HC〔l粗硅提纯〕〔9〕SiO2与NaOH:SiO2+2NaOH=Na2SiO3+H2O-2-〔SiO2+2OH=SiO3+H2O〕〔10〕CaO与SiO2::CaO+SiO2CaSiO3〔11〕SiO2与HF:SiO2+4HF=SiF4+2H2O〔12〕Na2SiO3与HCl:Na2SiO3+2HCl=2NaCl+H2SiO3↓〔13〕Na2SiO3与H2O与CO2:Na2SiO3+H2O+CO2=NaCO+HSiO↓〔强酸制弱酸〕2323〔14NaH〕SiOOCO()NaSiO+HO+2CO与23222322与过量:()=2NaHCO+HSiO过量↓323〔10〕.NaAlO2与CO2(少量)与H2O:2NaAlO2+CO2(少量)+3H2O=2Al(OH)3↓+Na2CO3-2-〕〔12〕.AlO2+CO2(少量)+3H2O=2Al(OH)3↓+CO3〔11〕.NaAlO2与CO2(过量)与2H2O:NaAlO2+CO2(过量)+2H2O=Al(OH)3↓+NaHCO3--〕〔AlO2+CO2(过量)+2H2O=Al(OH)3↓+HCO3〔12〕.Al与O2:4Al+3O2=2Al2O3〔15〕SiO2与Na2CO3:SiO2+Na2CO3Na2SiO3+CO2↑〔16〕SiO2与CaCO3:SiO2+CaCO3CaSiO3+CO2↑〔工业制玻璃〕〔17〕H2SiO3与NaOH:H2SiO3+2NaOH==Na2SiO3+ 2H2O〔18〕H2SiO3分解:H2SiO3SiO2+H2O五.氯:三.铁:〔1〕Cu与Cl2:Cu+Cl2CuCl2(棕黄色烟) CaSO3↓+H2O〔11〕Ca(OH)2与SO2(过量):Ca(OH)2+SO2(过量)〔2〕Cl2与Fe:3Cl2+2Fe2FeCl3(棕黄色烟)〔高价产物〕=Ca(HSO3)2〔12〕CaO与SO2:CaO+SO2=CaSO3〔13〕SO2与O2:2SO2+O22SO3〔3〕Na与Cl2:2Na+Cl22NaCl(白烟) 〔14〕Cl2与SO2:Cl2+SO2+2H2O=H2SO4+2HCl(同Br2、+2--I2)〔Cl2+SO2+2H2O=4H+SO4+2Cl)〔15〕H2S与SO2:2H2S+SO2=2H2O+3S↓〔4〕Cl2与H2:Cl2+H22HCl(燃烧苍白色火焰,光照〔16〕SO3与H2O:SO3+H2O=H2SO4〔17〕CaO与SO3:CaO+SO3=CaSO4会爆炸)〔5〕Cl2与P:3Cl2+2P2PCl3(液体) 〔18〕H2S与O2(少量):2H2S+O2(少量)2H2O+2S〔6〕Cl2与P:5Cl2+2P2PCl5(固体)〔白色烟雾〕〔7〕Cl2与H2O:Cl2+H2OHCl+HClO(新制氯水成分+,Cl-,ClO-,OH-)三分子H2O,C2l,HClO四离子H〔8〕Cl2与2NaOH:Cl2+2NaOH=NaCl+NaClO+H2O〔9〕Cl2与Ca(OH)2:2Cl2+2Ca(OH)2=CaC2l+Ca(ClO)2+2H2O 〔19〕H2S+O2(足量):2H2S+3O2(足量)2H2O+2SO2 〔20〕FeS与HCl:FeS+2HCl=H2S↑+FeC2l(同H2SO4,实验室制备H2S)〔21FeSO4FeS〕与:+11O2FeO+8SO2222232〔22SOH〕与O SO+HO=HSO〔工业制硫酸〕:323224〔工业制漂白粉〕〔10〕漂白粉的漂白原理Ca(ClO)2与H2O与CO2(少量):七.氮Ca(ClO)2+H2O+CO2(少量)=CaCO3↓+2HClO〔强酸制弱酸〕〔1〕N2与H2:N2+3H22NH3〔工业合成氨〕〔11〕漂白粉的失效原理Ca(ClO)2与H2O与CO2(少量):〔2〕N2与O2:N2+O22NOCa(ClO)+HO+CO()=CaCO+2HClO少量↓22232HClO2HCl+O2↑〔12〕FeCl2与Cl2:2FeCl2+C2l=2FeC3lN2与Mg:N2+3MgMg3N2〔3〕〔4〕NO与O2:2NO+O2=2NO2〔13〕NaBr与Cl2:2NaBr+Cl2==2NaCl+Br2〔2Br -+C2l〔5〕2NO2N2O4-==2Cl+Br2〕- 〔14〕KI+C2l:2KI+C2l==2KCl+2I〔2I -+Cl2==2Cl + 〔6〕NO2与H2O:3NO2+H2O=2HNO3+NO〔7〕NO与3O2与2H2O:NO+3O2+2H2O=4HNO3〔8〕NO2与O2与H2O:4NO2+O2+2H2O=4HNO3I2〕〔15〕实验室制备氯气MnO2与HCl(浓):MnO2+4HCl(浓)+-MnCl2+Cl2↑+2H2O〔MnO2+4H+2Cl 〔9〕Na2SO3与H2SO4:Na2SO3+H2SO4=Na2SO4+SO2+H2O〔实验室制备SO2〕〔10〕Na2SO3+O2:2Na2SO3+O2=2Na2SO4 〔11〕SO2(少量)与NH3与H2O:SO2(少量)+2NH3+H2O=2+Mn+Cl2↑+2H2O〕〔16〕NaX与AgNO3:NaX+AgNO3=AgX↓+NaNO3〔X=Cl,Br,I〕(沉淀不溶于HNO3,根据沉淀颜色鉴别卤离子) (NH4)2SO3++OH-〔12〕NH3+H2ONH3·H2ONH4〔13〕NH3与HCl:NH3+HCl=NH4Cl(白烟) 〔14〕NH3与HNO3:NH3+HNO3=NH4NO3(白烟)〔17〕NaCl与AgNO3:NaCl+AgNO3=AgCl↓+NaN3O 〔15〕NH3与H2SO4:2NH3+H2SO4=(NH4)2SO4(白色沉淀)〔18〕NaBr与AgNO3:NaBr+AgNO3=AgBr↓+NaN3O (浅黄色沉淀) 〔16〕NH3与O2:4NH3+5O24NO+6H2O〔17〕NO+O2:2NO+O2=2NO2〔18〕NO2+H2O:3NO2+H2O=2HNO3+NO〔工业制硝酸〕〔19〕KI与AgNO3:KI+AgNO3=AgI↓+KN3O(黄色沉淀)〔19〕NH4Cl受热分解:NH4ClNH3↑+HCl↑〔20〕NH4HCO3六.硫:受热分解:NH4HCO3NH3↑+H2O+CO2↑〔1〕Na与S加热:2Na+SNa2S〔2〕Fe与S:Fe+SFeS 〔21〕(NH4)2SO4与NaOH:(NH4)2SO4+2NaOH〔3〕Cu与S:2Cu+SCu2S〔低价产物〕+ Na2SO4+2NH3↑+2H2O(用于检验NH4)〔4〕H2与S:H2+SH2S 〔22〕NH4Cl与Ca(OH)2:2NH4Cl+Ca(OH2)CaCl2+2NH3↑+2H2O〔实验室制氨气〕〔5〕S与O2:S+O2SO2八.硫酸〔6〕S与NaOH:3S+6NaOH2Na2S+Na2SO3+ 〔1〕H2SO4(浓)与Cu:2H2SO4(浓)+CuCuSO4+-2-2-3H2O〔3S+6OH2S+SO3+3H2O〕〔7〕SO2:与H2O:SO2+H2OH2SO3〔注意“可逆反响〞的定义〕〔8〕NaOH与SO2(少量):2NaOH+SO2(少量)=Na2SO3+ 2H2O+SO2↑〔2〕HSO2↑2SO4(浓)与Zn:2H2SO4(浓)+Zn=ZnSO4+2H2O+〔3〕H2SO4(浓)与Fe〔少量〕:6H2SO4(浓)+2FeFe2(SO4)3+6H2O+3SO2↑(Fe少量)H2O 〔4〕H2SO4(浓)与C:2H2SO4(浓)+CCO2↑+2H2O〔9〕NaOH与SO2〔过量〕:NaOH+SO2〔过量〕=NaHSO3+2SO2↑〔10〕Ca(OH)2与SO2(少量):Ca(OH)2+SO2(少量)= 〔5〕H2SO4(浓)与S:2H2SO4(浓)+S2H2O+3SO2↑〔6〕H2S+H2SO4(浓):H2S+H2SO4(浓)=S↓+SO2↑+2+SO2↑+2H2O〔7〕HBr+H2SO4(浓):2HBr+H2SO4(浓)=Br2H2O〔8〕HNO3遇光分解:4HNO34NO2↑+O2↑+2H2O〔硝酸显黄色的原因〕〔9〕Cu与HNO3(浓)Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O +-2+〔Cu+4H+2NO3=Cu+2NO2↑+2H2O〕(10)HNO3(稀)与Cu:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O+-2+〔3Cu+8H+2NO3=3Cu+2NO↑+4H2O〕〔11〕HNO3(浓)与Fe:6HNO3(浓)+FeFe(NO3)3+3H2O+3NO2↑〔12〕HNO3(稀)与Fe(足量):8HNO3(稀)+3Fe(足量)= 3Fe(NO3)2+2NO↑+4H2O〔13〕HNO3(稀)与Fe(少量):4HNO3(稀)+Fe(少量)= Fe(NO3)3+NO↑+2H2O〔14〕C与HNO3(浓):C+4HNO3(浓)CO2↑+4NO2↑+2H2O。
高一化学方程式总结通用7篇

高一化学方程式总结通用7篇高一化学方程式总结篇一化合反应1、镁在空气中燃烧:2Mg + O2点燃2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43、铝在空气中燃烧:4Al + 3O2 点燃2Al2O34、氢气在空气中燃烧:2H2 + O2 点燃2H2O5、红磷在空气中燃烧:4P + 5O2 点燃2P2O56、硫粉在空气中燃烧:S + O2 点燃SO27、碳在氧气中充分燃烧:C + O2 点燃CO28、碳在氧气中不充分燃烧:2C + O2 点燃2CO9、二氧化碳通过灼热碳层:C + CO2 高温2CO10、一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO312、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2O14、钠在氯气中燃烧:2Na + Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温CaO + CO2↑苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶液Na2CO3 + 2HCl = 2NaCl + H2O+CO2↑CO32- + 2H+ = H2O + CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3 + HCl =NaHCO3 + NaClCO32- + H+ = HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+ = H2O +CO2↑小苏打受热分解2NaHCO3==【加热】Na2CO3 + H2O +CO2 ↑氧化还原反应:1. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O2. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑3. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑4. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑5. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO26.一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO27.一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2氧化性:2FeCl3 + Fe === 3FeCl22FeCl3 + Cu === 2FeCl2 + CuCl2 (用于雕刻铜线路版)2FeCl3 + Zn === 2FeCl2 + ZnCl2FeCl3 + Ag === FeCl2 + AgCFe2(SO4)3 + 2Ag === FeSO4 + Ag2SO4(较难反应)Fe(NO3)3 + Ag 不反应2FeCl3 + H2S === 2FeCl2 + 2HCl + S2FeCl3 + 2I === 2FeCl2 + 2Cl + I2FeCl2 + Mg === Fe + MgCl2还原性:2FeCl2 + Cl2 === 2FeCl33Na2S + 8HNO3(稀) === 6NaNO3 + 2NO + 3S + 4H2O3Na2SO3 + 2HNO3(稀) === 3Na2SO4 + 2NO + H2O2Na2SO3 + O2 === 2Na2SO4硫和硫的化合物1、硫和钠反应的方程式:2Na+S=Na2S (条件:研磨) 现象:轻微爆炸2、硫和铁反应的方程式:Fe+S=FeS(条件加热)3、硫和浓硫酸反应的化学方程式:S+2H2SO4 =SO2↑ +2 H2O (条件:加热)4、硫和氢氧化钠溶液反应的化学方程式:3S+6NaOH=2Na2S+Na2SO3 + 3H2O(除硫的`化学方法)5、SO2与水反应的方程式:SO2 + H2O =H2SO3 (可逆反应要用可逆符号)6、少量的SO2与NaOH溶液反应的化学方程式:SO2 +2NaOH=Na2SO3 + H2O7、过量的SO2与NaOH溶液反应的化学方程式:SO2 + NaOH=NaHSO38、少量的SO2与澄清石灰水反应的化学方程式:SO2 + Ca(OH)2= CaSO3↓ + H2O9、少量的SO2与饱和的碳酸氢钠溶液反应的化学方程式:SO2 +2NaHCO3= Na2SO3 +2CO2 +H2O10、SO2与Na2SO3溶液反应的化学方程式:SO2 + Na2SO3 +H2O =2NaHSO311、SO2与氢硫酸反应的化学方程式:SO2 + 2H2S=3S↓+2H2O高一化学方程式总结篇二钠及其化合物的性质1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2点燃====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
高一化学方程式总结(精选17篇)

高一化学方程式总结(精选17篇)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如工作报告、合同协议、心得体会、条据书信、规章制度、礼仪常识、自我介绍、教学资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of classic sample essays, such as work reports, contract agreements, personal experiences, normative letters, rules and regulations, etiquette knowledge, self introduction, teaching materials, complete essays, and other sample essays. If you want to learn about different sample formats and writing methods, please pay attention!高一化学方程式总结(精选17篇)高一化学方程式总结(精选17篇)高一化学方程式总结篇1二氧化碳溶解于水:CO2+H2O===H2CO3生石灰溶于水:CaO+H2O===Ca(OH)2氧化钠溶于水:Na2O+H2O====2NaOH三氧化硫溶于水:SO3+H2O====H2SO4硫酸铜晶体受热分解:CuSO4·5H2O加热CuSO4+5H2O 无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO4·5H2O 高一化学方程式总结篇2钠及其化合物的性质1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2点燃====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
(完整版)高一必修一化学方程式总结(全)

高一化学方程式总结一.钠:(1).Na在空气中与O2:4Na + O2 = 2Na2O(白色)(2).Na在O2中燃烧:2Na + O2Na2O2(淡黄色)(3).Na与S:2Na + S = Na2S(研磨即爆炸)(4).Na与Cl2:2Na + Cl22NaCl(5).Na与H2O:2Na + 2H2O = 2NaOH + H2↑ (2Na + 2H2O = 2Na+ + 2OH- + H2↑)(6).Na与HCl:2Na + 2HCl = 2NaCl + H2↑ (2Na + 2H+ =2Na+ + H2↑ )(7).Na与CuSO4溶液:2Na + 2H2O + CuSO4 = Na2SO4+ Cu(OH)2↓ + H2↑(8).Na与FeCl3溶液:6Na + 6H2O + 2FeCl3 = 6NaCl + 2Fe(OH)3↓ + 3H2↑(9).Na2O与H2O:Na2O + H2O = 2NaOH(10).Na2O与CO2:Na2O + CO2= Na2CO3(11).Na2O2与H2O:2Na2O2 + 2H2O = 4NaOH + O2↑(2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑)(12).Na2O2与CO2:2Na2O2 + 2CO2 = 2Na2CO3 + O2(供氧)(13).Na2CO3与HCl:Na2CO3 +2HCl = 2NaCl + H2O +CO2↑(互滴鉴别)(CO32- + 2H+ = H2O + CO2↑)(14).NaHCO3与HCl:NaHCO3 + HCl = NaCl + H2O + CO2↑(HCO3- + H+ = H2O + CO2↑)(15).NaHCO3与NaOH:NaHCO3 +NaOH=Na2CO3 + H2O (HCO3- + OH- = CO32- + H2O)(16).Na2CO3与H2O 与CO2 :Na2CO3 + H2O + CO2 =2NaHCO3(鉴别、除杂)(CO32- + H2O + CO2 = 2HCO3-)(17).NaHCO3 分解:2NaHCO3Na2CO3+H2O+ CO2↑(18).NaOH与CO2 (少量):2NaOH + CO2 (少量) = Na2CO3 + H2O (2OH-+ CO2 (少量) = CO32- + H2O)(19).NaOH 与CO2(过量):NaOH + CO2(过量)= NaHCO3(OH -+ CO2(过量)= HCO3-)二.铝:(1).Al与6HCl:2Al+6HCl=2AlCl3+3H2↑(同H2SO4)(2Al+6H+ =2Al3+ + 3H2↑ )(2).Al 与NaOH 与H2O:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑(2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑)(3).Al2O3与HCl:Al2O3 + 6HCl = 2AlCl3 + 3H2O(Al2O3 + 6H+ =2Al3+ + 3H2O)(4).Al2O3与NaOH:Al2O3+2NaOH=2NaAlO2+H2O(Al2O3 + 2OH- = 2AlO2- + H2O )(5).Al(OH)3与HCl:Al(OH)3 + 3HCl = AlCl3 + 3H2O(Al(OH)3 + 3H+ = Al3+ + 3H2O)(6).Al(OH)3与NaOH:Al(OH)3+NaOH=NaAlO2+2H2O (Al(OH)3 + OH- = AlO2- + 2H2O)(7).2Al(OH)3Al2O3 + 3H2O(8).AlCl3与NH3·H2O:AlCl3 + 3NH3·H2O = Al(OH)3↓ + 3NH4Cl (Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+)(9).NaAlO2与HCl与H2O:NaAlO2+HCl+H2O=NaCl+Al(OH)3↓ (AlO2- + H+ +H2O = Al(OH)3↓ )(10).NaAlO2 与CO2(少量)与H2O:2NaAlO2 + CO2(少量)+3H2O=2Al(OH)3↓+Na2CO3(12).AlO2- + CO2(少量)+ 3H2O = 2Al(OH)3↓ + CO32-)(11).NaAlO2与CO2(过量)与2H2O:NaAlO2+CO2(过量)+2H2O=Al(OH)3↓+NaHCO3(AlO2- + CO2(过量) + 2H2O = Al(OH)3↓ + HCO3-)(12).Al 与O2 :4Al + 3O2 = 2Al2O3三.铁:(1).Fe与O2:3Fe+2O2Fe3O4(2).Al2O3电解:2Al2O34Al+3O2↑(3).Fe与H2O(g)高温:3Fe+4H2O(g)Fe3O4+4H2(4).FeCl3 + Fe :2FeCl3 + Fe = 3FeCl2(2Fe3+ + Fe = 3Fe2+)(5).FeCl2+Cl2:2FeCl2+Cl2=2FeCl3(2Fe2+ + Cl2 = 2Fe3++2Cl-)(6).FeCl3与Cu:2FeCl3 + Cu = 2FeCl2 + CuCl2(用于雕刻铜线路板) (2Fe3+ + Cu = 2Fe2++ Cu2+)(7).FeO与HCl:FeO+ 2HCl = FeCl2 + H2O(同H2SO4)(FeO+2H+=Fe2+ +H2O )(8).Fe2O3 与HCl :Fe2O3 + 6HCl = 2FeCl3 + 3H2O(同H2SO4)(Fe2O3 + 6H+=2Fe3+ + 3H2O)(9).Fe3O4 与HCl:Fe3O4 + 8HCl = 2FeCl3 + FeCl2 +4H2O(同H2SO4)(Fe3O4 + 8H+=Fe2+ +2Fe3+ +4H2O)(10).FeSO4与NaOH:FeSO4 + 2NaOH=Fe(OH)2↓ +Na2SO4(Fe2+ + 2OH-=Fe(OH)2↓)(11).FeCl3与NaOH:FeCl3 + 3NaOH=Fe(OH)3 ↓+ 3NaCl (Fe3+ + 3OH-=Fe(OH)3 ↓)(12).Fe(OH)2 与H2O 与O2:4Fe(OH)2 + 2H2O + O2 =4Fe(OH)3 (白色沉淀→灰绿色沉淀→红褐色沉淀)(13).Fe(OH)2与HCl.Fe(OH)2+2HCl==FeCl2+2H2O(Fe(OH)2 + 2H+=Fe2+ + 2H2O)(14).Fe(OH)3与HCl:Fe(OH)3+3HCl==FeCl3+3H2O(Fe(OH)3 + 3H+ = Fe3+ + 3H2O)(15).Fe(OH)3加热:2Fe(OH)3Fe2O3 + 3H2O(16).FeCl3与KSCN:FeCl3+3KSCN==Fe(SCN)3+3KCl(Fe3++ 3SCN- = Fe(SCN)3)(红色溶液,用于鉴别Fe3+) (17).FeCl3与H2S(少量):2FeCl3 + H2S(少量) = 2FeCl2 + 2HCl + S↓ (18).FeCl3与KI:2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2↓(19).FeCl3与H2O:FeCl3+3H2O Fe(OH)3(胶体)+3HCl (20).C与H2O:C+H2O CO+H2 (生成水煤气)四.硅:(1)Si与NaOH与H2O:Si + 2NaOH + H2O = Na2SiO3 +2H2↑ (Si+2OH-+H2O= SiO32- + 2H2↑)(2)Si与HF:Si+ 4HF = SiF4 + 2H2↑(3)Si与F2:Si+ 2F2 = SiF4(4)Si与O2:Si+O2SiO2 (研细的硅与纯氧)(5)Si 与C:Si + C SiC(6)C与SiO2:2C+ SiO22CO↑+Si(工业制粗硅)(7)Cl2:与Si:2Cl2+Si= SiCl4(8)SiCl4 与H2:SiCl4 +2H2=Si+4HCl(粗硅提纯)(9)SiO2 与NaOH:SiO2 + 2NaOH = Na2SiO3 + H2O(SiO2 + 2OH- = SiO32-+ H2O )(10)CaO与SiO2::CaO+SiO2CaSiO3(11)SiO2 与HF:SiO2 + 4HF = SiF4 + 2H2O(12)Na2SiO3 与HCl:Na2SiO3 +2HCl=2NaCl+H2SiO3↓(13)Na2SiO3 与H2O与CO2:Na2SiO3 + H2O+CO2 =Na2CO3 + H2SiO3↓(强酸制弱酸)(14)Na2SiO3与H2O与CO2 (过量):Na2SiO3 + H2O+ 2CO2 (过量) = 2NaHCO3+H2SiO3↓(15)SiO2与Na2CO3:SiO2 + Na2CO3Na2SiO3+ CO2↑ (16)SiO2 与CaCO3:SiO2 + CaCO3CaSiO3+ CO2↑(工业制玻璃)(17)H2SiO3与NaOH:H2SiO3 + 2NaOH == Na2SiO3 +2H2O(18)H2SiO3分解:H2SiO3 SiO2 + H2O五.氯:(1)Cu与Cl2:Cu+Cl2CuCl2 (棕黄色烟)(2)Cl2与Fe:3Cl2+2Fe2FeCl3(棕黄色烟) (高价产物)(3)Na 与Cl2 :2Na + Cl2 2NaCl (白烟)(4)Cl2 与H2:Cl2 +H22HCl (燃烧苍白色火焰,光照会爆炸)(5)Cl2 与P:3Cl2 + 2P 2PCl3 (液体)(6)Cl2 与P:5Cl2 + 2P 2PCl5(固体) (白色烟雾)(7)Cl2与H2O:Cl2+H2O HCl+HClO (新制氯水成分三分子H2O,Cl2,HClO四离子H+,Cl-,ClO-,OH-)(8)Cl2 与2NaOH:Cl2 + 2NaOH = NaCl + NaClO + H2O(9)Cl2与Ca(OH)2:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O (工业制漂白粉)(10)漂白粉的漂白原理Ca(ClO)2与H2O与CO2(少量) :Ca(ClO)2+H2O+ CO2(少量) = CaCO3↓+2HClO (强酸制弱酸)(11)漂白粉的失效原理Ca(ClO)2与H2O与CO2(少量):Ca(ClO)2+H2O+CO2(少量) = CaCO3↓+ 2HClO2HClO2HCl+O2↑(12)FeCl2与Cl2:2FeCl2 + Cl2 = 2FeCl3(13)NaBr 与Cl2:2NaBr + Cl2 == 2NaCl + Br2(2Br - + Cl2 == 2Cl- + Br2)(14)KI + Cl2:2KI + Cl2 == 2KCl + I2(2I- + Cl2 == 2Cl- + I2)(15)实验室制备氯气MnO2与HCl(浓):MnO2 + 4HCl(浓) MnCl2+Cl2↑+2H2O (MnO2+ 4H+ + 2Cl-Mn2+ + Cl2↑ + 2H2O)(16)NaX与AgNO3:NaX+AgNO3=AgX↓+NaNO3(X=Cl,Br,I)(沉淀不溶于HNO3,根据沉淀颜色鉴别卤离子)(17)NaCl 与AgNO3:NaCl + AgNO3 = AgCl↓ + NaNO3 (白色沉淀)(18)NaBr 与AgNO3:NaBr + AgNO3 = AgBr↓ + NaNO3 (浅黄色沉淀)(19)KI 与AgNO3:KI +AgNO3 = AgI↓ + KNO3 (黄色沉淀)六.硫:(1)Na 与S加热:2Na + S Na2S(2)Fe与S:Fe+S FeS(3)Cu与S:2Cu+S Cu2S (低价产物)(4)H2与S:H2 + S H2S(5)S 与O2:S + O2 SO2(6)S 与NaOH:3S + 6NaOH 2Na2S + Na2SO3 + 3H2O (3S + 6OH-2S2- + SO32- + 3H2O)(7)SO2:与H2O:SO2+H2O H2SO3(注意“可逆反应”的定义)(8)NaOH与SO2 (少量):2NaOH+ SO2 (少量) = Na2SO3 + H2O(9)NaOH与SO2(过量):NaOH+ SO2(过量)= NaHSO3(10)Ca(OH)2 与SO2 (少量) :Ca(OH)2 + SO2 (少量) =CaSO3↓+ H2O(11)Ca(OH)2 与SO2(过量):Ca(OH)2 + SO2(过量)=Ca(HSO3)2(12)CaO与SO2:CaO+ SO2 = CaSO3(13)SO2与O2:2SO2+O2 2SO3(14)Cl2与SO2:Cl2+SO2 +2H2O=H2SO4+2HCl (同Br2、I2) (Cl2+SO2 +2H2O= 4H+ + SO42- + 2Cl-)(15)H2S 与SO2:2H2S + SO2= 2H2O + 3S↓(16)SO3与H2O:SO3+H2O=H2SO4(17)CaO与SO3:CaO+ SO3 = CaSO4(18)H2S 与O2(少量):2H2S + O2(少量) 2H2O+2S (19)H2S + O2(足量):2H2S + 3O2(足量) 2H2O + 2SO2(20)FeS 与HCl:FeS + 2HCl = H2S↑ + FeCl2(同H2SO4,实验室制备H2S)(21)FeS2与O2:4FeS2+11O22Fe2O3 + 8SO2(22)SO3与H2O:SO3+H2O=H2SO4(工业制硫酸)七.氮(1)N2与H2:N2+3H22NH3(工业合成氨)(2)N2与O2:N2+O22NO(3)N2 与Mg:N2 + 3Mg Mg3N2(4)NO 与O2:2NO + O2 = 2NO2(5)2NO 2 N2O4(6)NO2与H2O:3NO2+H2O = 2HNO3+NO(7)NO与3O2与2H2O:NO+3O2+2H2O=4HNO3(8)NO2与O2与H2O:4NO2+O2+2H2O=4HNO3(9)Na2SO3与H2SO4:Na2SO3+H2SO4=Na2SO4+SO2 +H2O (实验室制备SO2)(10)Na2SO3 + O2:2Na2SO3 + O2 = 2Na2SO4(11)SO2(少量) 与NH3 与H2O: SO2(少量) + 2NH3 + H2O = (NH4)2SO3(12)NH3+H2O NH3·H2O NH4++OH-(13)NH3 与HCl :NH3 + HCl = NH4Cl(白烟)(14)NH3 与HNO3:NH3 + HNO3 = NH4NO3(白烟)(15)NH3 与H2SO4:2NH3 + H2SO4 = (NH4)2SO4(16)NH3与O2:4NH3+5O2 4NO+6H2O(17)NO + O2:2NO + O2 = 2NO2(18)NO2+H2O:3NO2+H2O=2HNO3+NO(工业制硝酸)(19)NH4Cl受热分解:NH4Cl NH3↑+HCl↑(20)NH4HCO3受热分解:NH4HCO3NH3↑+ H2O +CO2↑(21)(NH4)2SO4与NaOH:(NH4)2SO4 + 2NaOHNa2SO4 + 2NH3↑+ 2H2O (用于检验NH4+)(22)NH4Cl 与Ca(OH)2:2NH4Cl + Ca(OH)2CaCl2 + 2NH3↑+2H2O(实验室制氨气)八.硫酸(1)H2SO4(浓) 与Cu:2H2SO4(浓) + Cu CuSO4 + 2H2O + SO2↑(2)H2SO4(浓) 与Zn:2H2SO4(浓) +Zn = ZnSO4 + 2H2O + SO2↑(3)H2SO4(浓) 与Fe(少量):6H2SO4(浓) + 2FeFe2(SO4)3 + 6H2O + 3SO2↑ (Fe少量)(4)H2SO4(浓) 与C:2H2SO4(浓) + C CO2↑ + 2H2O + 2SO2↑(5)H2SO4(浓) 与S:2H2SO4(浓) + S 2H2O + 3SO2↑(6)H2S + H2SO4(浓):H2S + H2SO4(浓)= S↓+ SO2↑+ 2H2O(7)HBr + H2SO4(浓):2HBr + H2SO4(浓)= Br2 + SO2↑+ 2H2O(8)HNO3遇光分解:4HNO3 4NO2↑+ O2↑+ 2H2O(硝酸显黄色的原因)(9)Cu与HNO3(浓)Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O(Cu + 4H+ + 2NO3- = Cu2+ + 2NO2↑+ 2H2O)(10)HNO3(稀)与Cu:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O(3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑+ 4H2O)(11)HNO3(浓)与Fe:6HNO3(浓) + Fe Fe(NO3 )3+ 3H2O + 3NO2↑(12)HNO3(稀)与Fe(足量):8HNO3(稀) + 3Fe(足量)= 3Fe(NO3)2+2NO↑+4H2O(13)HNO3(稀)与Fe(少量):4HNO3(稀) + Fe(少量)= Fe(NO3)3 + NO↑ + 2H2O(14)C与HNO3(浓):C + 4HNO3(浓) CO2↑+ 4NO2↑+ 2H2O。
高一必修化学方程式大全

高一必修化学方程式大全
化学方程式是化学教学中一个重要的组成部分,在深入研究和探索化学律下实验过程中具有至关重要的意义。
以下是高一必修化学方程式大全:
一、酸和碱的中和反应
HCl(aq)+NaOH(aq)→NaCl(aq)+H2O(l)
二、气体反应
CO2(g)+2H2(g)→CH3OH(l)+H2O(g)
三、金属与稀盐溶液反应
2Fe(s)+2HCl(aq)→2FeCl2(aq)+H2(g)
四、无机化合物反应
2KOH(aq)+H2(g)→K2O(s)+2H2O(l)
五、乙醇燃烧反应
C2H5OH(l)+3O2(g)→2CO2(g)+3H2O(g)
六、水素氧化反应
H2(g)+1/2O2(g)→H2O(l)
七、氧化还原反应
3MnO4(aq)+8H+(aq)+5Fe2(aq)→3Mn2+(aq)+5Fe3+(aq)+4H2O(l)
八、醇中容积反应
C2H5OH(l)+3O2(g)→2CO2(g)+3H2O(g)
九、焦硫水解反应
C6H14(l)+7O2(g)→6CO2(g)+7H2O(g)+2SO2(g)
以上就是高一必修化学方程式大全,虽然少数反应式可能会比较复杂,但他们都被不失时机地应该和掌握,以便于在学习的过程中能够更加有效地运用。
关于化学方程式,除了熟练掌握一些基础反应式外,还要经常总结练习,培养化学的“合成性思维”,以便于解决实际问题。
同时,在日常学习中,要深刻理解化学本质,掌握反应原理,加深对基础知识的理解,让单纯的记忆变成深入洞察的思维过程。
高中化学必修1化学方程式总结
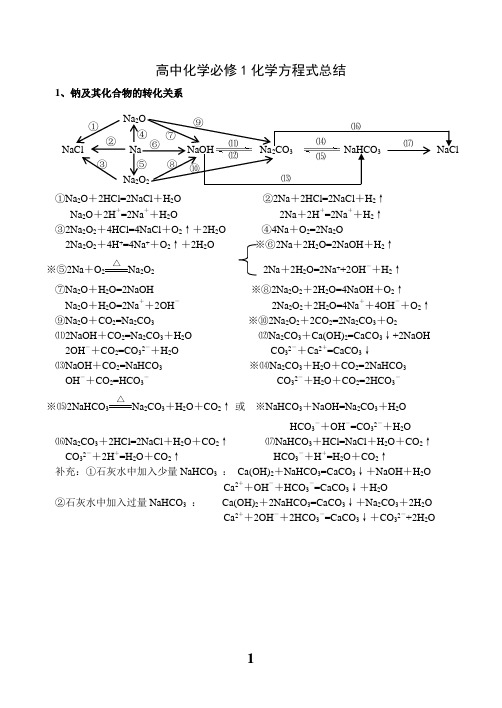
高中化学必修1化学方程式总结1、钠及其化合物的转化关系①Na 2O +2HCl=2NaCl +H 2O ②2Na +2HCl=2NaCl +H 2↑Na 2O +2H +=2Na ++H 2O 2Na +2H +=2Na ++H 2↑ ③2Na 2O 2+4HCl=4NaCl +O 2↑+2H 2O ④4Na +O 2=2Na 2O2Na 2O 2+4H +=4Na ++O 2↑+2H 2O ※⑥2Na +2H 2O=2NaOH +H 2↑ ※⑤2Na +O 2△Na 2O 2 2Na +2H 2O=2Na ++2OH -+H 2↑⑦Na 2O +H 2O=2NaOH ※⑧2Na 2O 2+2H 2O=4NaOH +O 2↑Na 2O +H 2O=2Na ++2OH - 2Na 2O 2+2H 2O=4Na ++4OH -+O 2↑ ⑨Na 2O +CO 2=Na 2CO 3 ※⑩2Na 2O 2+2CO 2=2Na 2CO 3+O 2⑾2NaOH +CO 2=Na 2CO 3+H 2O ⑿Na 2CO 3+Ca(OH)2=CaCO 3↓+2NaOH2OH -+CO 2=CO 32-+H 2O CO 32-+Ca 2+=CaCO 3↓⒀NaOH +CO 2=NaHCO 3 ※⒁Na 2CO 3+H 2O +CO 2=2NaHCO 3OH -+CO 2=HCO 3- CO 32-+H 2O +CO 2=2HCO 3-※⒂2NaHCO 3△Na 2CO 3+H 2O +CO 2↑ 或 ※NaHCO 3+NaOH=Na 2CO 3+H 2OHCO 3-+OH -=CO 32-+H 2O⒃Na 2CO 3+2HCl=2NaCl +H 2O +CO 2↑ ⒄NaHCO 3+HCl=NaCl +H 2O +CO 2↑CO 32-+2H +=H 2O +CO 2↑ HCO 3-+H +=H 2O +CO 2↑补充:①石灰水中加入少量NaHCO 3 : Ca(OH)2+NaHCO 3=CaCO 3↓+NaOH +H 2OCa 2++OH -+HCO 3-=CaCO 3↓+H 2O②石灰水中加入过量NaHCO 3 : Ca(OH)2+2NaHCO 3=CaCO 3↓+Na 2CO 3+2H 2OCa 2++2OH -+2HCO 3-=CaCO 3↓+CO 32-+2H 2ONaCl Na NaOH Na 2CO 3 NaHCO 3 NaCl Na 2O Na 2O 2 ① ② ③ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ⑾ ⑿ ⒀ ⒁ ⒂⒃ ⒄ ④2、铝及其化合物的转化关系①2Al +6HCl=2AlCl 3+3H 2↑ ②4Al +3O 2 △2Al 2O 32Al +6H +=2Al 3++3H 2↑※③2Al +2NaOH +2H 2O=2NaAlO 2+3H 2↑ ④Al 2O 3+6HCl=2AlCl 3+3H 2O2Al +2OH -+2H 2O=2AlO 2-+3H 2↑ Al 2O 3+6H +=2Al 3++3H 2O ※⑤Al 2O 3+2NaOH=2NaAlO 2+H 2O ⑥AlCl 3+3NH 3·H 2O=Al(OH)3↓+3NH 4ClAl 2O 3+2OH -=2AlO 2-+H 2O Al 3++3NH 3·H 2O = Al(OH)3↓+3NH 4+⑦Al(OH)3+3HCl=AlCl 3+3H 2O ⑧2Al(OH)3△Al 2O 3+3H 2OAl(OH)3+3H +=Al 3++3H 2O☆⑨NaAlO 2+HCl +H 2O =Al(OH)3↓+NaCl 或NaAlO 2+2H 2O +CO 2=Al(OH)3↓+NaHCO 3AlO 2-+H ++H 2O=Al(OH)3↓ AlO 2-+2H 2O +CO 2=Al(OH)3↓+HCO 3-※⑩Al(OH)3+NaOH = NaAlO 2+2H 2O ☆⑾Al 3++3H 2O Al(OH)3胶体+3H +Al(OH)3+OH -= AlO 2-+2H 2O 明矾净水⑿AlCl 3+4NaOH = NaAlO 2+3NaCl +2H 2O Al 3++4OH -= AlO 2-+2H 2OAl Al 2O 3 A l (O H )3 KAl(SO 4)2NaAlO 2AlCl 3 ① ② ③ ④ ⑤ ⑥⑦⑧ ⑨⑩⑾⑿①Fe 3O 4+4CO△3Fe +4CO 2 ※② 3Fe +4H 2O(g)高温Fe 3O 4+4H 2 ③ Fe +2HCl=FeCl 2+H 2↑ 或3Fe +2O 2点燃Fe 3O 4Fe +2H +=Fe 2++H 2↑ ④2Fe +3Cl 2点燃2FeCl 3※⑤2FeCl 2+Cl 2 = 2FeCl 3 ※⑥Fe +2FeCl 3 = 3FeCl 22Fe 2++Cl 2 = 2Fe 3++2Cl - Fe +2Fe 3+= 3Fe 2+⑦FeCl 2+2NaOH = Fe(OH)2↓+2NaCl ⑧Fe(OH)2+2HCl = FeCl 2+2H 2OFe 2++2OH -= Fe(OH)2↓ Fe(OH)2+2H += Fe 2++2H 2O※⑨4Fe(OH)2+O 2+2H 2O = 4Fe(OH)3 ⑩FeCl 3+3NaOH = Fe(OH)3↓+3NaCl白色沉淀迅速变成灰绿色,最后变成红褐色 Fe 3++3OH -= Fe(OH)3↓⑾Fe(OH)3+3HCl = FeCl 3+3H 2O Fe 3++3H 2O Fe(OH)3胶体+3H +(净水) Fe(OH)3+3H += Fe 3++3H 2O ⑿2Fe(OH)3△Fe 2O 3+3H 2O⒀Fe 2O 3+6HCl = 2FeCl 3+3H 2O ※⒁FeCl 3+3KSCN = Fe(SCN)3+3KClFe 2O 3+6H += 2Fe 3++3H 2O Fe 3++3SCN -= Fe(SCN)3Fe 3O 4 Fe FeCl 2 Fe(OH)2 Fe(SCN)3 FeCl 3 Fe(OH)3 Fe O 3 ①② ③ ④⑤ ⑥ ⑦ ⑧ ⑨⑩ ⑾⑿ ⒁ ⒀①Si +O 2△SiO 2②SiO 2+2C 高温 Si +2CO ↑※③SiO 2+4HF = SiF 4↑+2H 2O (刻蚀玻璃)④Si +4HF = SiF 4↑+2H 2↑ ⑤SiO 2+CaO高温CaSiO 3※⑥SiO 2+2NaOH = Na 2SiO 3+H 2O SiO 2+CaCO 3高温CaSiO 3+CO 2↑SiO 2+2OH -= SiO 32-+H 2O ※⑦Na 2SiO 3+2HCl = H 2SiO 3↓+2NaCl SiO 2+Na 2CO 3高温Na 2SiO 3+CO 2↑ SiO 32-+2H += H 2SiO 3↓※⑦Na 2SiO 3+H 2O +CO 2=H 2SiO 3↓+Na 2CO 3或Na 2SiO 3+2H 2O +2CO 2=H 2SiO 3↓+2NaHCO 3SiO 32-+H 2O +CO 2=H 2SiO 3↓+CO 32-或SiO 32-+2H 2O +2CO 2=H 2SiO 3↓+2HCO 3-⑧H 2SiO 3+2NaOH = Na 2SiO 3+2H 2O ⑨H 2SiO 3 △H 2O +SiO 2H 2SiO 3+2OH -= SiO 32-+2H 2O 5、氯及其化合物的转化关系①2Fe +3Cl 2 点燃2FeCl 3 ②Cu +Cl 2 点燃CuCl 2 ③2FeCl 3+Cu = 2FeCl 2+CuCl 22Fe 3++Cu = 2Fe 2++Cu 2+④H 2+Cl 2 2HCl※⑤MnO 2+4HCl(浓) △MnCl 2+Cl 2↑+2H 2OMnO 2+4H ++2Cl - △ Mn 2++Cl 2↑+2H 2O ※⑥Cl 2+H 2O = HCl +HClO ※⑦2HClO 2HCl +O 2↑Cl 2+H 2O = H ++Cl -+HClO 2HClO 2H ++2Cl -+O 2↑※⑧Cl 2+2NaOH = NaCl +NaClO +H 2O ※⑨2Cl 2+2Ca(OH)2 = CaCl 2+Ca(ClO)2+2H 2OCl 2+2OH -= Cl -+ClO -+H 2O 工业制漂白粉※⑩Ca(ClO)2+H 2O +CO 2 = CaCO 3↓+2HClO 或Ca(ClO)2+2HCl = CaCl 2+2HClOCa 2++2ClO -+H 2O +CO 2= CaCO 3↓+2HClO 或ClO -+H += HClO 漂白粉的漂白原理向漂白粉溶液中通入过量的CO 2:Ca(ClO)2+2H 2O +2CO 2 = Ca(HCO 3)2+2HClOClO -+H 2O +CO 2 = HCO 3-+HClONa 2SiO 3 SiF 4 Si SiO 2 H 2SiO 3 CaSiO 3 ①②③ ④ ⑤⑥ ⑦ ⑧⑨ CuCl 2 HClO HCl Cl 2 FeCl 3NaClO Ca(ClO)2① ② ③ ④⑤ ⑥ ⑦ ⑧ ⑨ ⑩ 点燃或光照 光照光照①S +O 2 点燃SO 2②2H 2S +SO 2=3S +2H 2O※③SO 2+O 2 催化剂加热 2SO 3 ④SO 3+H 2O = H 2SO 4 ⑤SO 2+CaO△CaSO 3 或 SO 2+Ca(OH)2 = CaSO 3↓+H 2O⑥SO 3+CaO = CaSO 4 SO 2+Ca 2++2OH -=CaSO 3↓+H 2O SO 3+Ca(OH)2 = CaSO 4+H 2O ⑦2CaSO 3+O 2△2CaSO 4※⑧SO 2+Cl 2+2H 2O = H 2SO 4+2HCl ※⑨Cu +2H 2SO 4(浓) △CuSO 4+SO 2↑+2H 2OSO 2+Cl 2+2H 2O = 4H ++SO 42-+2Cl -Cu +2H 2SO 4(浓) △Cu 2++SO 42-+SO 2↑+2H 2O※⑩C +2H 2SO 4(浓)△CO 2↑+2SO 2↑+2H 2O7、氮及其化合物的转化关系 ※①N 2+O 22NO※②2NO +O 2 = 2NO 2※③3NO 2+H 2O = 2HNO 3+NO 3NO 2+H 2O =2H ++2NO 3-+NO以上三个反应为“雷雨发庄稼”原理 扩展反应有:4NO 2+O 2+2H 2O = 4HNO 3 4NO +3O 2+2H 2O = 4HNO 3 ※④Cu +4HNO 3(浓) = Cu(NO 3)2+2NO 2↑+2H 2O 上面两个反应主要用于气体溶于水时的计算Cu +4H ++2NO 3-=Cu 2++2NO 2↑+2H 2O 或 4HNO 3 4NO 2↑+ O 2↑+ 2H 2OC +4HNO 3(浓)△CO 2↑+2NO 2↑+2H 2O 浓硝酸见光易变黄的原因※⑤3Cu +8HNO 3(稀) = 3Cu(NO 3)2+2NO ↑+4H 2O ⑥N 2+3H 2催化剂 高温高压2NH 33Cu +8H ++2NO 3-=3Cu 2++2NO ↑+4H 2O 合成氨反应是人工固氮的主要途径 ⑦NH 3+HCl = NH 4Cl ⑧NH 4Cl△NH 3↑+HCl ↑NH 3+H += NH 4+(水溶液中) 补充:NH 4HCO 3 △NH 3↑+H 2O+CO 2↑氨气与酸均能反应生成铵盐,且与挥发性酸 铵盐受热都易分解,但并不是所有的铵盐 (如浓HCl 、浓HNO 3)相遇时空气中有白烟 都分解出氨气,如NH 4NO 3、(NH 4)2SO 4※⑧NH 4Cl +NaOH△NaCl +NH 3↑+H 2O NH 4++OH-△NH 3↑+H 2O所有的铵盐都能与碱作用放出氨气,可利用此反应鉴别铵离子。
高一化学必修一化学方程式总结

高一化学必修一化学方程式总结在高一化学必修一中,我们学习了众多重要的化学方程式,这些方程式是理解化学知识的关键。
下面就为大家详细总结一下。
一、金属及其化合物相关的化学方程式1、钠及其化合物(1)钠在空气中燃烧:2Na + O₂=点燃= Na₂O₂(2)钠与水反应:2Na + 2H₂O = 2NaOH + H₂↑(3)过氧化钠与水反应:2Na₂O₂+ 2H₂O = 4NaOH + O₂↑(4)过氧化钠与二氧化碳反应:2Na₂O₂+ 2CO₂= 2Na₂CO₃+ O₂2、铝及其化合物(1)铝与氧气反应:4Al + 3O₂= 2Al₂O₃(2)铝与盐酸反应:2Al + 6HCl = 2AlCl₃+ 3H₂↑(3)铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H₂O =2NaAlO₂+ 3H₂↑(4)氧化铝与盐酸反应:Al₂O₃+ 6HCl = 2AlCl₃+ 3H₂O+ H₂O(6)氢氧化铝与盐酸反应:Al(OH)₃+ 3HCl = AlCl₃+ 3H₂O (7)氢氧化铝与氢氧化钠溶液反应:Al(OH)₃+ NaOH =NaAlO₂+ 2H₂O3、铁及其化合物(1)铁与氧气反应:3Fe + 2O₂=点燃= Fe₃O₄(2)铁与盐酸反应:Fe + 2HCl = FeCl₂+ H₂↑(3)铁与硫酸铜溶液反应:Fe + CuSO₄= FeSO₄+ Cu(4)氧化亚铁与盐酸反应:FeO + 2HCl = FeCl₂+ H₂O(5)氧化铁与盐酸反应:Fe₂O₃+ 6HCl = 2FeCl₃+ 3H₂O (6)四氧化三铁与盐酸反应:Fe₃O₄+ 8HCl = FeCl₂+2FeCl₃+ 4H₂O(7)氢氧化亚铁与氧气、水反应:4Fe(OH)₂+ O₂+ 2H₂O =4Fe(OH)₃二、非金属及其化合物相关的化学方程式1、硅及其化合物(1)硅与氧气反应:Si + O₂=高温= SiO₂(2)二氧化硅与氢氟酸反应:SiO₂+ 4HF = SiF₄↑ + 2H₂O+ H₂O(4)硅酸钠溶液与盐酸反应:Na₂SiO₃+ 2HCl = 2NaCl +H₂SiO₃↓2、氯及其化合物(1)氯气与金属钠反应:2Na + Cl₂=点燃= 2NaCl(2)氯气与金属铁反应:2Fe + 3Cl₂=点燃= 2FeCl₃(3)氯气与氢气反应:H₂+ Cl₂=点燃= 2HCl(4)氯气与水反应:Cl₂+ H₂O = HCl + HClO(5)次氯酸光照分解:2HClO =光照= 2HCl + O₂↑(6)氯气与氢氧化钠溶液反应:Cl₂+ 2NaOH = NaCl + NaClO + H₂O3、硫及其化合物(1)硫在氧气中燃烧:S + O₂=点燃= SO₂(2)二氧化硫与水反应:SO₂+ H₂O ⇌ H₂SO₃(3)二氧化硫与氧气反应:2SO₂+ O₂⇌ 2SO₃(4)三氧化硫与水反应:SO₃+ H₂O = H₂SO₄(5)铜与浓硫酸反应:Cu + 2H₂SO₄(浓) =△= CuSO₄+SO₂↑ + 2H₂O(6)碳与浓硫酸反应:C + 2H₂SO₄(浓) =△= CO₂↑ + 2SO₂↑ + 2H₂O4、氮及其化合物(1)氮气与氧气反应:N₂+ O₂=放电= 2NO(2)一氧化氮与氧气反应:2NO + O₂= 2NO₂(3)二氧化氮与水反应:3NO₂+ H₂O = 2HNO₃+ NO(4)氨气与水反应:NH₃+ H₂O ⇌ NH₃·H₂O(5)氨气与盐酸反应:NH₃+ HCl = NH₄Cl(6)氯化铵受热分解:NH₄Cl =△= NH₃↑ +HCl↑(7)碳酸氢铵受热分解:NH₄HCO₃=△= NH₃↑ + CO₂↑ +H₂O(8)硝酸铵与氢氧化钠反应:NH₄NO₃+ NaOH =△= NH₃↑ + NaNO₃+ H₂O(9)铜与浓硝酸反应:Cu + 4HNO₃(浓) = Cu(NO₃)₂+ 2NO₂↑ + 2H₂O(10)铜与稀硝酸反应:3Cu + 8HNO₃(稀) = 3Cu(NO₃)₂+2NO↑ + 4H₂O这些化学方程式在高一化学学习中非常重要,同学们一定要牢记并理解其反应原理,通过多做练习来熟练掌握,为后续的化学学习打下坚实的基础。
高一化学方程式总结5篇

高一化学方程式总结5篇高中化学是理科中偏文科的一门学科,学习化学不仅需要一定的逻辑思维能力,还要有一定的记忆能力,来背诵化学方程式。
下面就是我给大家带来的高一化学方程式总结,希望能帮助到大家!高一化学方程式总结11、硫酸根离子的检验:BaCl2+Na2SO4=BaSO4↓+2NaCl2、碳酸根离子的检验:CaCl2+Na2CO3=CaCO3↓+2NaCl3、碳酸钠与盐酸反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑4、木炭还原氧化铜:2CuO+C高温2Cu+CO2↑5、铁片与硫酸铜溶液反应:Fe+CuSO4=FeSO4+Cu6、氯化钙与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl7、钠在空气中燃烧:2Na+O2△Na2O2钠与氧气反应:4Na+O2=2Na2O8、过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑9、过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O210、钠与水反应:2Na+2H2O=2NaOH+H2↑11、铁与水蒸气反应:3Fe+4H2O(g)=F3O4+4H2↑12、铝与氢氧化钠溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑13、氧化钙与水反应:CaO+H2O=Ca(OH)214、氧化铁与盐酸反应:Fe2O3+6HCl=2FeCl3+3H2O15、氧化铝与盐酸反应:Al2O3+6HCl=2AlCl3+3H2O16、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH=2NaAlO2+H2O17、氯化铁与氢氧化钠溶液反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl18、硫酸亚铁与氢氧化钠溶液反应:FeSO4+2NaOH=Fe(OH)2↓+Na2SO419、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2+2H2O+O2=4Fe(OH)320、氢氧化铁加热分解:2Fe(OH)3△Fe2O3+3H2O↑高一化学方程式总结2单质与氧气的反应:1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧:4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分燃烧:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O高一化学方程式总结3钠及其化合物的性质1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2点燃====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
高一必背化学方程式总结

高一必背化学方程式总结高一化学方程式是学好高中化学知识的基础,下面是给大家带来的高一化学方程式知识点,希望能帮助到大家!高一化学方程式知识点总结1Cu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3NaOH + H3PO4=3H2O + Na3PO43NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+ H2O 吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成CuSO4+5H2O= CuSO4·H2O 蓝色晶体变为白色粉末CuSO4·H2OΔ CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl = A gCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)高一化学方程式知识点总结2化合反应1、镁在空气中燃烧:2Mg + O2 点燃2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43、铝在空气中燃烧:4Al + 3O2 点燃2Al2O34、氢气在空气中燃烧:2H2 + O2 点燃2H2O5、红磷在空气中燃烧:4P + 5O2 点燃2P2O56、硫粉在空气中燃烧:S + O2 点燃SO27、碳在氧气中充分燃烧:C + O2 点燃CO28、碳在氧气中不充分燃烧:2C + O2 点燃2CO9、二氧化碳通过灼热碳层:C + CO2 高温2CO10、一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO312、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4??5H2O14、钠在氯气中燃烧:2Na + Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温CaO + CO2↑高一化学方程式知识点总结3非金属单质(F2,Cl2,O2,S,N2,P,C,Si,H)氧化性:F2+H2===2HF (阴暗处爆炸)F2+Xe(过量)==XeF22F2(过量)+Xe==XeF4 (XeF4是强氧化剂,能将Mn2+氧化为MnO4–)nF2+2M===2MFn(M表示大部分金属)2F2+2H2O===4HF+O2 (水是还原剂)2F2+2NaOH===2NaF+OF2+H2OF2+2NaCl===2NaF+Cl2F2+2NaBr===2NaF+Br2F2+2NaI===2NaF+I27F2(过量)+I2===2IF7F2+Cl2(等体积)===2ClF (ClF属于类卤素:ClF+H2O==HF+HClO )3F2(过量)+Cl2===2ClF3 (ClF3+3H2O==3HF+HClO3 )Cl2+H2 2HCl (将H2在Cl2点燃;混合点燃、加热、光照发生爆炸)3Cl2+2P 2PCl3 Cl2+PCl3 PCl5 Cl2+2Na 2NaCl3Cl2+2Fe 2FeCl3 Cl2+Cu CuCl2Cl2+2FeCl2===2FeCl3 (在水溶液中:Cl2+2Fe2+===2Fe3++3Cl )Cl2+2NaBr===2NaCl+Br2 Cl2+2Br =2Cl +Br2Cl2+2KI===2KCl+I2 Cl2+2I =2Cl +I23Cl2(过量)+2KI+3H2O===6HCl+KIO33Cl2+I–+3H2O=6H++6Cl–+IO3–5Cl2+I2+6H2O===2HIO3+10HCl5Cl2+I2+6H2O=10Cl–+IO3–+12H+Cl2+Na2S===2NaCl+S↓ Cl2+S2–=2Cl–+S↓Cl2+H2S===2HCl+S↓ (水溶液中:Cl2+H2S=2H++2Cl–+S↓Cl2+SO2+2H2O===H2SO4+2HClCl2+SO2+2H2O=4H++SO42–+2Cl–Cl2+H2O2===2HCl+O2 Cl2+H2O2=2H++Cl–+O22O2+3Fe Fe3O4 O2+K===KO2S+H2 H2S 2S+C CS2 S+Zn ZnSS+Fe FeS (既能由单质制取,又能由离子制取)S+2Cu Cu2S (只能由单质制取,不能由离子制取)3S+2Al Al2S3 (只能由单质制取,不能由离子制取)N2+3H2 2NH3 N2+3Mg Mg3N2 N2+3Ca Ca3N2N2+3Ba Ba3N2 N2+6Na 2Na3N N2+6K 2K3NN2+6Rb 2Rb3N N2+2Al 2AlNP4+6H2 4PH3 P+3Na Na3P 2P+3Zn Zn3P2H2+2Li 2LiH高一必背化学方程式总结。
高一上化学方程式整理

高一上化学方程式整理如下:(1) 氢氧化钡溶液与稀H2SO4 反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2OBa(OH)2 + H2SO4 == BaSO4 + 2H2O(2) 硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2OH2SO4+Ba(OH)2=BaSO4+2H2O(3) 硫酸氢钠溶液中加入氢氧化钡溶液至硫酸根沉淀完全:H++SO42-+Ba2++2OH-=BaSO4↓+2H2ONaHSO4+ Ba(OH)2=BaSO4↓+NaOH+H2O(4) 碳酸氢钠溶液和氢氧化钠溶液混合HCO3-+OHˉ=CO32-+H2ONaHCO3+ NaOH=Na2CO3+H2O(5) 氢氧化钠溶液中加入过量碳酸氢钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2ONaOH+CaHCO3=CaCO3↓+ Na2CO3+H2O(6) 氢氧化钠溶液中加入少量碳酸氢钙溶液:Ca2++2HCO3-+2OH-=CaCO3↓+H2O+ CO32-NaOH+CaHCO3=CaCO3↓+Na2CO3+H2O(7) 向AlCl3溶液中加入少量的NaOH溶液:Al3+ + 3OH-=Al(OH)3↓AlCl3+3NaOH=Al(OH)3+3NaCl(8) 向AlCl3溶液中加入过量的NaOH溶液:Al3+ +4OH-=AlO2-+2H2OAlCl3+3NaOH=Al(OH)3+3NaCl Al(OH)3+NaOH=NaAlO4+2H2O AlCl3+4NaOH= NaAlO4+3NaCl(9) 氯化铁溶液中加过量氨水:Fe 3++3NH3·H2O= Fe (OH)3↓+3NH4+FeCl3+3NH3·H2O= Fe (OH)3↓+3NH4Cl(10) 氯化铝溶液中加入过量的氨水A13++3NH3·H2O= Al(OH)3↓+3NH4+A1Cl3+3NH3·H2O= Al(OH)3↓+3NH4Cl(11) 氯化铝溶液中加入少量的氨水(同上) A13++3NH3·H2O= Al(OH)3↓+3NH4+A1Cl3+3NH3·H2O= Al(OH)3↓+3NH4Cl(12) 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-= CaCO3↓+H2OCa(OH)2+NaHCO3-= CaCO3↓+NaOH+H2O(13) 澄清石灰水与过量小苏打溶液混合:Ca2++2OH-+2HCO3-= CaCO3↓+2H2O+ CO32-Ca(OH)2+NaHCO3= CaCO3↓+NaOH+H2O NaOH+ NaHCO3= Na2CO3↓+ H2OCa(OH)2+2NaHCO3= CaCO3↓+2H2O+ NA2CO3(14) 铝片溶于苛性钠溶液:2Al+2OH-+2H2O =2AlO2-+3H2↑2Al+2NaOH=2NaAlO2+3H2↑(15) 金属铜与稀硝酸反应:3Cu + 8H+ + 2NO3-= 3Cu2+ +4H2O+ 2NO↑3Cu+8HNO3(稀)△3Cu(NO3)2 + 4H2O + 2NO↑(16) 金属铜与浓硝酸反应:Cu + 4H+ + 2NO3-= Cu2+ + 2NO2↑+2H2 OCu + 4HNO3 (浓)= Cu(NO3)2 + 2NO2↑+2H2 O(17) 稀硝酸与过量的铁屑反应Fe+4H++2NO3-= Fe2++2NO↑+2 H2OFe+HNO3(稀)= Fe(NO3)2+2NO↑+2 H2O(18) 稀硝酸与少量的铁屑反应2Fe+8H++2NO3-= 2Fe3++2NO↑+4 H2O 2Fe+8HNO3(稀)= 2Fe(NO3)3+2NO↑+4H2O(19) 氢氧化亚铁溶于稀盐酸Fe (OH)2+2H+ = Fe2++2H2O(20) 氢氧化亚铁溶于稀硝酸3Fe (OH)2+10H+ + NO3-= 3Fe3++8H2O+ NO↑(21) 向次氯酸钙溶液中通人过量的二氧化碳C1O一+CO2+H2O= HCO3-+HClO(22) 向次氯酸钙溶液中通人少量的二氧化碳:Ca2++2C1O一+CO2+H2O=Ca CO3↓+2HClO(23) 氯化铁溶液中加过量氨水:A13++3NH3·H2O= Al(OH)3↓+3NH4+(24) ¬¬Na2CO3溶液与少量硝酸溶液:H+ + CO32-=HCO3-(25) CaCO3溶液与硝酸溶液:2H+ + CaCO3 =CO2↑+ H2O+ Ca2+(26) CaCO3溶液与醋酸溶液:2CH¬¬3COOH+ CaCO3 =Ca2++2CH3COO-+CO2↑+ H2O(27) 硫酸铜溶液和氢氧化钡溶液混合:Cu2+ + SO42-+Ba2+ + 2OH-= Cu(OH)2↓+ BaSO4↓(28) 硫酸镁溶液和氢氧化钡溶液混合Mg2++SO42-+Ba2+ + 2OH -= Mg (OH)2↓+ BaSO4↓(29) 等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合Ba2++2OH一+ NH4++HCO3一=BaCO3↓+H2O+ NH3·H2O (30) 在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合HSO3-+OH -==SO32-+H2O(31) 在稀溶液中亚硫酸氢铵与过量氢氧化钠混合:NH4++HSO3-+2OH-==SO32-+H2O+ NH3·H2O(32) 铜片插入硝酸银溶液中:Cu + 2Ag+ = Cu2+ + 2Ag(33) Cl2通入NaOH溶液::Cl2 + 2OH-== Cl-+ ClO-+ H2O(34) 氯化铁和铜反应::2Fe3++Cu=2Fe2++Cu2+(35) FeCl2溶液中通入Cl2::2Fe2++Cl2 = 2Fe3++2 Cl-(36) 溴化亚铁溶液中通入过量氯气::2Fe2++4Br-+3Cl2==2Fe3++2Br2+6 Cl-(37) 溴化亚铁溶液中通入少量氯气::2Fe2++Cl2 = 2Fe3++2 Cl -(38) 在碘化亚铁溶液中通入足量氯气:2Fe2++4I-+3Cl2==2Fe3++2I2+6Cl-(39) 在碘化亚铁溶液中通入少量氯气2Fe2++Cl2 = 2Fe3++2 Cl -(40) 实验室用MnO2和浓盐酸制取Cl2::MnO2+4 H+¬¬+2 Cl-Mn2++Cl2↑+2H2O(41) 足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓(42) 少量的CO2通入澄清石灰水中::CO2+ Ca2++2OH-=CaCO3↓+H2O(43) 足量的CO2通入澄清石灰水中:CO2+ OH-=2HCO3-(44) 少量的SO2通入澄清石灰水中::SO2+ Ca2++2OH-=CaSO3↓+H2O(45) 足量的SO2通入澄清石灰水中:SO2+ OH-=2HSO3-(46) AgNO3溶液中滴入过量氨水::Ag++ 2 NH3·H2O = Ag(NH3)2+ + 2H2O(47) 向氯化铁溶液中加入铁粉:2Fe3++ Fe =3Fe2+(48) 钠和冷水反应:2Na+2H2O=2Na++2OH-+H2↑(49) 铁粉和稀硫酸::Fe + 2H+ == Fe2+ + H2↑(50) FeSO4酸性溶液中加过量双氧水:2Fe2++H2O2+2H+=2Fe3++2H2O(51) 二氧化硅与氢氧化钠溶液反应:SiO2+2 OH-=SiO32-+ H2O(52) Na与CuSO4溶液反应:2Na+2H2O+ Cu2+=2Na++Cu(OH)2↓+H2↑(53) Na与FeCl3溶液反应:6Na+6H2O+ 2Fe3+=6Na++2Fe (OH)3↓+3H2↑(54) O与H2O反应:Na2O+2H2O=2Na++2OH-(55) Na2O2与H2O反应:2Na2O2+2H2O=4Na++4OH-+O2↑(56) Al2O3与盐酸反应:Al2O3 + 6H+ ==2 Al3++ 3H2O(57) Al2O3与NaOH溶液反应:Al2O3+ 2OH-==2 AlO2-+H2O(58) Al(OH)3与HCl反应:Al(OH)3 + 3H+== Al3++ 3H2O(59) Al(OH)3与NaOH溶液反应:Al(OH)3 +OH-=AlO2-+2H2O(60) Na2SiO3溶液与稀盐酸反应:SiO32-+ 2H+ H2SiO3↓。
高一化学方程式大全

必修一化学方程式总结一、钠及其化合物1、钠与氧气:常温:4Na + O2 == 2Na2O 点燃:2Na + O2Na2O22、钠与水反应:2Na + 2H2O == 2NaOH + H2↑离子方程式:2Na + 2H2O == 2Na++ 2OH-+ H2↑3、钠与硫酸反应:2Na + H2SO4 == Na2SO4+ H2↑4、氧化钠与水反应:Na2O+H2O == 2NaOH5、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 == 2Na2CO3+ O26、过氧化钠与水反应:2Na2O2 +2H2O == 4NaOH + O2↑离子方程式:2Na2O2 +2H2O == 4Na+ + 4OH-+ O2↑7、NaOH溶液通入少量CO2:2NaOH +CO2 == Na2CO3 +H2O 离子方程式:2OH-+CO2 == CO3 2-+H2ONaOH溶液通入过量CO2:NaOH +CO2 == NaHCO3 离子方程式:OH-+CO2 == HCO3-8、①向碳酸钠溶液滴入少量稀盐酸:Na2CO3+ HCl == NaHCO3 + NaCl向稀盐酸溶液滴入少量碳酸钠:Na2CO3+ 2HCl == 2NaCl +CO2↑+H2O②除去碳酸氢钠中混有的碳酸钠:Na2CO3 + CO2 + H2O == 2NaHCO3③碳酸钠与氢氧化钙:Na2CO3 +Ca(OH)2 == CaCO3 ↓+2NaOH④碳酸氢钠与盐酸:NaHCO3 + HCl == NaCl +CO2↑+H2O⑤少量碳酸氢钠溶液滴入氢氧化钙溶液中:NaHCO3 +Ca(OH)2 ==NaOH+CaCO3 ↓+H2O少量氢氧化钙溶液滴入碳酸氢钠溶液中:2NaHCO3 +Ca(OH)2 == Na2CO3 +CaCO3 ↓+2H2O⑥除去碳酸钠溶液中的碳酸氢钠:NaHCO3 + NaOH == Na2CO3 +H2O⑦除去碳酸钠固体中的碳酸氢钠:2NaHCO3Na2CO3 +CO2↑+H2O⑧鉴别碳酸钠和碳酸氢钠溶液:Na2CO3 +CaCl2 == CaCO3 ↓+2NaCl二、铝及其化合物1、铝与氧气的反应:4Al + 3O2 2Al2O32、铝与氧化铁反应(铝热反应):2Al + Fe2O3 2Fe + Al2O33、铝和稀盐酸:2Al +6HCl == 2AlCl3 +3H2↑离子方程式:2Al+ 6H+ ==2Al3+ +3H2↑4、铝和NaOH溶液:2Al +2NaOH +2H2O == 2NaAlO2 +3H2↑离子方程式:2Al +2OH-+2H2O == 2AlO2-+3H2↑5、氧化铝和稀硫酸:Al2O3 +3H2SO4 == Al2(SO4)3 +3H2O 离子方程式:Al2O3 + 6H+ == 2Al3+ + 3H2O6、氧化铝和NaOH溶液:Al2O3 + 2NaOH == 2NaAlO2 +H2O 离子方程式:Al2O3 + 2OH-== 2AlO2-+ H2O7、氢氧化铝和稀盐酸:Al(OH)3 +3HCl == AlCl3 +3H2O 离子方程式:Al(OH)3 +3H+ == Al3+ + 3H2O8、氢氧化铝和NaOH溶液:Al(OH)3 + NaOH == NaAlO2 +2H2O 离子方程式:Al(OH)3 +OH-==AlO2-+ 2H2O9、氢氧化铝受热分解:2Al(OH)3Al2O3 +3H2O10、硫酸铝与氨水反应:Al2(SO4)3 +6NH3•H2O == 2Al(OH)3↓+3(NH4)2SO4离子方程式:Al3+ + 3NH3•H2O == Al(OH)3↓+3NH4+11、AlCl3溶液中加入少量NaOH溶液:AlCl3 + 3NaOH ==Al(OH)3↓+3NaClAlCl3溶液中加入过量NaOH溶液:AlCl3 + 4NaOH == NaAlO2+3NaCl+ 2H2O12、往NaAlO2溶液中通入少量CO2:2NaAlO2 +CO2 + 3H2O == 2Al(OH)3↓+ Na2CO3往NaAlO2溶液中通入过量CO2:NaAlO2 +CO2 + 2H2O == Al(OH)3↓+ NaHCO313、电解氧化铝:2Al2O3(熔融)4Al+3O2↑三、铁及其化合物1、铁与氧气反应:3Fe + 2O2Fe3O4铁与硫反应:Fe + S FeS2、铁与盐酸反应:Fe + 2HCl == FeCl2 +H2↑离子方程式:Fe + 2H+ == Fe2++H2↑铁与CuSO4溶液:Fe +CuSO4 == FeSO4 + Cu 离子方程式:Fe +Cu2+== Fe2++ Cu3、铁和水蒸气:3Fe +4H2O(g)Fe3O4 + 4H24、氧化亚铁与盐酸反应:FeO + 2HCl == FeCl2 +H2O 离子方程式:FeO + 2H+ == Fe2++H2O5、氧化铁与盐酸反应:Fe2O3 + 6HCl == 2FeCl3 +3H2O 离子方程式:Fe2O3 + 6H+ == 2Fe3++3H2O6、CO还原氧化铁:3CO+Fe2O33CO2 + 2Fe7、氯化铁与NaOH溶液:FeCl3 +3NaOH == Fe(OH)3 ↓+3NaCl 离子方程式:Fe3+ +3OH-== Fe(OH)3 ↓8、硫酸亚铁与NaOH溶液:FeSO4 + 2NaOH == Fe(OH)2 ↓+ Na2SO4 离子方程式:Fe2+ +2OH-== Fe(OH)2 ↓9、氢氧化铁加热分解:2Fe(OH)3 Fe2O3 +3H2O10、氢氧化亚铁被氧化为氢氧化铁:4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3(白色沉淀迅速变灰绿色,最后变为红褐色)11、除去FeCl2中的FeCl3:Fe +2FeCl3 == 3FeCl2 离子方程式:Fe +2Fe3+ == 3Fe2+12、FeCl2与Cl2反应:2FeCl2 + Cl2 == 2FeCl3 离子方程式:2Fe2+ +Cl2 == 2Fe3+ +2Cl-13、FeCl3与Cu反应:Cu +2FeCl3 == 2FeCl2 +CuCl2 离子方程式:Cu +2Fe3+ == 2Fe2++Cu2+14、氯化铁与硫氰化钾反应:FeCl 3 + 3KSCN Fe(SCN)3 + 3KCl(溶液变红)四、硅及其化合物1、硅与氧气加热:Si + O2 SiO2硅与氟气:Si + 2F2 == SiF42、硅单质与氢氟酸:Si + 4HF== SiF4↑+2H2↑3、硅与NaOH溶液反应:Si + 2NaOH+ H2O == Na2SiO3 + 2H2↑4、二氧化硅与氢氟酸反应:SiO2 + 4HF== SiF4↑+2H2O5、二氧化硅与氧化钙高温反应:SiO2 + CaO CaSiO36、二氧化硅与NaOH溶液反应:SiO2 + 2NaOH == Na2SiO3 +H2O7、二氧化硅与碳反应:SiO2 + 2C2CO + Si8、硅酸钠与与盐酸反应:Na2SiO3 + 2HCl == 2NaCl +H2SiO3↓离子方程式:SiO32-+ 2H+ ==H2SiO3↓9、往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO2 +H2O == Na2CO3 +H2SiO3↓10、二氧化硅与纯碱反应:SiO2 +Na2CO3Na2SiO3 + CO2↑11、二氧化硅与石灰石反应:SiO2 +CaCO3CaSiO3 + CO2↑12、加热硅酸:H2SiO3SiO2 +H2O五、氯及其化合物1、实验室制氯气:MnO2 +4HCl(浓)MnCl2 +Cl2↑+2H2O 离子方程式:MnO2 +4H++2Cl-Mn2++Cl2↑+2H2O2、钠在氯气中燃烧:2Na +Cl22NaCl(产生大量白烟)铁在氯气中燃烧:2Fe +3Cl22FeCl3 (产生大量棕黄色的烟)铜在氯气中燃烧:Cu +Cl2CuCl2 (产生大量棕黄色的烟)氢气在氯气中燃烧:H2 +Cl22HCl(苍白色火焰,瓶口出现白雾)3、氯气和水反应:Cl 2 + H2O HCl+ HClO 离子方程式:Cl2 + H2O H++Cl-+ HClO4、次氯酸光照分解:2HClO2HCl+O2↑5、氯水中通入SO2:Cl2 +SO2 +2H2O==2HCl+H2SO4 离子方程式:Cl2 +SO2 +2H2O==4H++2Cl-+SO42-6、氯气与NaOH溶液:Cl2+2NaOH ==NaCl +NaClO +H2O 离子方程式:Cl2+2OH-==Cl-+ClO-+H2O7、工业生产漂白粉:2Cl2+2Ca(OH)2 ==CaCl2+Ca(ClO)2+2H2O8、漂白粉漂白原理:Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO9、向漂白粉溶液中加入稀盐酸:Ca(ClO)2+2HCl==CaCl2+2HClO10、氯气通入溴化钾溶液:Cl2 + 2KBr ==2KCl +Br2 离子方程式:Cl2 + 2Br-==2Cl-+Br2氯气通入碘化钾溶液:Cl2 + 2KI ==2KCl +I2 离子方程式:Cl2 + 2I-==2Cl-+I2溴水和碘化钾溶液:Br2 + 2KI ==2KBr +I2 离子方程式:Br2 + 2I-==2Br-+I211、氯化钠和硝酸银溶液:NaCl +AgNO3 ==AgCl ↓+Na NO3 离子方程式:Cl-+Ag+==AgCl ↓六、硫及其化合物1、硫在空气中燃烧:S + O2 SO2 硫与氢气加热:H2 + S H2S2、二氧化硫与水:SO 2 + H2O H2SO3二氧化硫与氧化钙:SO2 +CaO ==CaSO3少量SO2与NaOH溶液:SO2+2NaOH==Na2SO3 +H2O 离子方程式:SO2+2OH-==SO32-+H2O过量SO2与NaOH溶液:SO2+NaOH==NaHSO3 离子方程式:SO2+OH-==HSO3-3、SO2通入过量的澄清石灰水:SO2+Ca(OH)2 ==CaSO3↓+H2O 离子方程式:SO2+Ca2++2OH-==CaSO3↓+H2O过量的SO2通入澄清石灰水:2SO2+Ca(OH)2 ==Ca(HSO3)2 离子方程式:SO2+OH-==HSO3-4、二氧化硫与硫化氢:SO2 + 2H2S == 3S↓+ 2H2O5、二氧化硫催化氧化:2SO2+O22SO36、亚硫酸钠和硫酸反应:Na2SO3 +H2SO4 == Na2SO4+SO2↑+H2O7、Na2SO3 与氧气反应:2Na2SO3+O2==2Na2SO48、三氧化硫与水反应:SO3 + H2O==H2SO49、三氧化硫与氧化钙:SO3 +CaO ==CaSO410、三氧化硫与氢氧化钙:SO3 +Ca(OH)2==CaSO4↓+H2O11、铜与浓硫酸反应:Cu +2H2SO4(浓)CuSO4+SO2↑+2H2O12、碳与浓硫酸反应:C +2H2SO4(浓)CO2↑+2SO2↑+2H2O13、二氧化硫与过氧化氢反应:SO2+H2O2=H2SO4七、氮及其化合物1、氮气和氧气反应:N2+O22NO2、工业合成氨:N2+3H22NH33、一氧化氮与氧气反应:2NO+O2==2NO24、NO2溶于水:3NO2+H2O==2HNO3+NO5、氨气溶于水:NH 3+H2O NH3•H2O 氨水显弱碱性(电离方程式):NH3•H2O NH4++OH-6、浓氨水受热分解:NH3•H2O NH3↑+H2O7、氨气和氯化氢:NH3+HCl==NH4Cl(产生白烟)8、氨的催化氧化:4NH3+5O24NO+6H2O9、氯化铵受热分解:NH4Cl NH3↑+HCl↑10、碳酸氢铵受热分解:NH4HCO3NH3↑+CO2↑+H2O11、硝酸铵和NaOH:NH4NO3+NaOH NaNO3+NH3↑+H2O离子方程式:NH4++OH-NH3↑+H2O12、实验室制氨气:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O13、浓硝酸与铜反应:Cu +4HNO3==Cu(NO3)2+2NO2↑+2H2O 离子方程式:Cu +4H++2NO3-==Cu2++2NO2↑+2H2O14、稀硝酸与铜反应:3Cu +8HNO3==3Cu(NO3)2+2NO↑+4H2O离子方程式:3Cu +8H++2NO3-==3Cu2++2NO↑+4H2O15、硝酸见光分解:4HNO3==4NO2↑+O2↑+2H2O16、NH4+检验的离子方程式:NH4++OH-NH3↑+H2O17、NO2、O2混合气通入水中无剩余气体:4NO2+O2+2H2O==4HNO318、NO、O2混合气通入水中无剩余气体:4NO+3O2+2H2O==4HNO319、少量氨气与氯气2NH3+3Cl2 = N2+6HCl20、过量氨气与氯气8NH3+3Cl2 = N2+6NH4Cl。
高一化学必修一化学方程式大全

化学⼀门历史悠久⽽⼜富有活⼒的学科,它的成就是社会⽂明的重要标志。
其中化学⽅程式是很重要的化学⽤语,如果想要学好化学,就⼀定要背好化学⽅程式。
下⾯店铺总结了⾼⼀化学必修⼀化学⽅程式⼤全,希望能都帮到⼤家! 1、⾦属钠投到硫酸铜溶液中的化学⽅程式: 2Na+2H2O=2NaOH+H2↑ CuSO4+2NaOH=Cu(OH) 2↓+ Na2SO4 (先冒⽓泡再蓝⾊沉淀) 2、⾦属钠与盐酸的化学⽅程式:2Na+2HCl=2NaCl+H2↑ 3、氢氧化钠⽅在空⽓中变质的化学⽅程式: 2NaOH+CO2=Na2CO3+H2O Na2CO3+10H2O=Na2CO3·10H2O 4、⾦属钠放在空⽓的氧化:4Na+O2=2Na2O (银⽩⾊变暗) 5、⾦属钠在空⽓燃烧:2Na+O2=Na2O2 Δ (⽣成淡黄⾊粉末) 6、过氧化钠在空⽓中变质: 2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2 7、过氧化钠与酸反应:2Na2O2+4HCl=4NaCl+2H2O+O2↑ 8、氧化钠在空⽓中变质: Na2O+H2O=2NaOH Na2O+CO2=Na2CO3 9、氧化钠与酸反应:Na2O+2HCl=2NaCl+H2O 10、氧化钠在空⽓中燃烧:2Na2O+O2=2Na2O2 11、氯⽓与铁的反应⽅程式:2Fe+3Cl2=2FeCl3 点燃(红棕⾊的烟) 12、氯⽓与铜的反应⽅程式:Cu+Cl2=CuCl2 点燃(棕黄⾊的烟) 13、氯⽓与氢⽓的反应⽅程式:Cl2+H2=2HCl 点燃(苍⽩⾊⽕焰,⽣成⽩雾) 14、氯⽓与钠单质的反应⽅程式:2Na+Cl2=2NaCl 点燃(淡黄⾊的烟) 15、⼯业制漂⽩: 2Cl2+2Ca(OH) 2=CaCl2+Ca(ClO) 2+2H2O (为Ca(OH) 2⽯灰乳) 16、氯⽓与⽔的⽅程式:Cl2+H2O=HCl+HClO 17、消毒、处理多余的氯⽓、制84消毒液: Cl2+2NaOH=NaClO+NaCl+H2O 18、次氯酸钠在空⽓中变质: 2NaClO+CO2+H2O=2HClO+Na2CO3 NaClO+CO2+H2O=HClO+NaHCO3 19、漂⽩在空⽓中变质:Ca(ClO) 2+CO2+H2O=CaCO3↓+2HClO 20、次氯酸见光分解:2HClO=2HCl+O2↑光照 21、氯化铁通⼊沸⽔中制氢氧化铁胶体: FeCl3+3H2O=Fe(OH) 3 (胶体)+3HCl Δ 22、碳酸钠与盐酸的反应⽅程式: Na2CO3+2HCl(过)=2NaCl+CO2↑+H2O Na2CO3+HCl(少)=NaHCO3+NaCl 23、碳酸氢钠与盐酸的反应⽅程式:NaHCO3+HCl=NaCl+H2O+CO2↑ 24、碳酸氢钠与碱反应⽅程式: NaHCO3+NaOH=Na2CO3+H2O NaHCO3+Ca(OH) 2=2H2O+Na2CO3+CaCO3↓ 25、碳酸氢钠受热易分解:2NaHCO3=Na2CO3+CO2↑+H2O Δ 26、⼆氧化碳通⼊碳酸钠溶液中:Na2CO3+CO2+H2O=2NaHCO3 27、浑浊⽯灰⽔变澄清:CO2+CaCO3+H2O=Ca(HCO3) 2 28、碳酸氢钙受热分解:Ca(HCO3) 2= CO2↑+CaCO3+H2O Δ 29、氢氧化亚铁在空⽓中变质: 4Fe(OH) 2+O2+2H2O=4Fe(OH) 3(由⽩⾊沉淀变成灰绿⾊再变成红褐⾊沉淀) 30、保存氯化亚铁溶液: 2FeCl3+Fe=3FeCl2 2Fe3++Fe=3Fe2+ 31、制造印刷线路板: 2FeCl3+Cu=2FeCl2+CuCl2 2Fe3++Cu=2Fe2++Cu2+ 32、2FeCl2+Cl2=2FeCl3 2Fe2++Cl2=2Fe3++2Cl- 33、Fe2O3+3CO = 2Fe+3CO2 ⾼温 34、Ba2++SO42+=BaSO4↓ Ag++Cl-= AgCl↓ 35、Zn+Cu2+= Zn2++Cu Zn+Fe2+= Zn2++Fe 36、溶洞的形成: CO2+CaCO3+H2O=Ca(HCO3)2 Ca(HCO3)2=CO2↑+CaCO3+H2O Δ 37、NaHCO3+BaCl2 ?不反应(⼀般情况下,强酸才能制弱酸) 38、⼯业上制取⽔煤⽓:C+H2O(g)=CO+H2 ⾼温 39、⾃然界通过放电把氮⽓转化为⼀氧化氮:N2+O22NO 放电(NO⽆⾊、难溶于⽔) 40、⼯业上制备氨⽓:N2+3H22NH3 ⾼温、⾼压、催化剂 41、⼀氧化氮在常温下被氧化:2NO+O2=2NO2(NO2红棕⾊、有刺激性⽓味的有毒⽓体、易溶于⽔) 42、⼯业上制取硝酸、⼆氧化氮溶于⽔⽣成硝酸和⼀氧化氮: 3NO2+H2O=2HNO3+NO 43、氨溶解于⽔:NH3+H2ONH3·H2O(⼀⽔合氨、弱碱性、能使酚酞溶液变红) 44、⼀⽔合氨的电离:NH3·H2ONH4++OH- 45、氨与盐酸的反应:NH3+HCl=NH4Cl 46、⼯业上制备硝酸需要的⼀氧化氮的⽅程式:4NH3+5O2=4NO+6H2O ⾼温催化剂 47、碳酸氢铵受热分解:NH4HCO3=NH3↑+CO2↑+H2O Δ (密封保存在阴凉处、施肥时埋在⼟下) 48、氯化铵受热分解:NH4Cl=NH3↑+HCl↑ Δ 49、铵态氮肥不能与碱(如草⽊灰)混合施⽤:NH4++OH-=NH3↑+H2O Δ 50、实验室制氨⽓:2NH4Cl+Ca(OH)2=2NH3↑+CaCl2+2H2O Δ(向上排空⽓法收集、湿润的红⾊⽯蕊试纸) 51、硝酸受热分解:4HNO3=4NO2↑+O2↑+2H2O 受热或见光(应保存在棕⾊试剂瓶中、阴凉处) 52、铜与硝酸的反应: Cu +4HNO3(浓) =Cu(NO3)2+2NO2↑+2H2O (遇浓硝酸⽣成⼆氧化氮) 3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O (遇稀硝酸⽣成⼀氧化氮) 53、浓硝酸与⽊炭的反应:4HNO3(浓)+C=CO2↑+4NO2↑+2H2O Δ 54、硫单质铁的反应:Fe+S=FeS Δ (硫单质的氧化性、S黄⾊或淡黄⾊固体,不溶⽔、微溶酒精、易溶CS2) 55、硫单质与氧⽓的反应:S+O2=SO2 点燃 (硫单质的.还原性、SO2有刺激性⽓味的有毒⽓体、易溶于⽔) 56、硫粉遇碱发⽣歧化反应:3S+6NaOH=2Na2S+Na2SO3+3H2O Δ 57、⿊⽕药爆炸的化学⽅程式:S+2KNO3+3C=K2S+3CO2↑+N2↑ 58、⼆氧化硫被氧⽓氧化:2SO2+O22SO3 催化剂 Δ 59、⼆氧化硫与硫化氢发⽣归中反应:SO2+2H2S=3S↓+2H2O (H2S臭鸡蛋⽓味) 60、浓硫酸与铜加热发⽣反应:2H2SO4(浓)+Cu=CuSO4+SO2↑+2H2O Δ 61、浓硫酸与⽊炭加热发⽣反应:2H2SO4(浓)+C=2SO2↑+CO2↑+2H2O Δ 62、⼆氧化硫能使澄清⽯灰⽔变浑浊:SO2+Ca(OH)2=CaSO3↓+H2O 63、⼆氧化硫与氯⽓发⽣氧化还原反应:SO2+Cl2+2H2O=H2SO4+2HCl 64、酸⾬的形成:2SO2+O22SO3 粉尘等催化 SO3+H2O=H2SO4 SO2+H2OH2SO3 2H2SO3+O2=2H2SO4 65、海⽔提镁第⼀步:Mg+2H+=Mg2++H2↑ (盐酸、稀硫酸) 66、镁与氮⽓的反应:3Mg+N2=Mg3N2 点燃 67、镁与⼆氧化碳反应:2Mg+CO2=2MgO+C 点燃(镁着⽕不能⽤⼆氧化碳扑灭) 68、海⽔提溴单质:2Br-+Cl2=Br2+2Cl- 69、半导体硅与氧⽓的反应:Si+O2=SiO2 Δ(⾃然界没有游离态的硅) 70、⼯业上制粗硅:SiO2+2C=Si+2CO↑⾼温(光导纤维、沙⼦和⽯英的主要成分是SiO2) 71、硅与氟⽓的反应:Si+2F2=SiF4 72、硅与氢氟酸的反应:Si+4HF=SiF4+2H2 73、制作黏合剂:Si+2NaOH+H2O=Na2SiO3+2H2↑ 74、玻璃与烧碱反应:SiO2+2NaOH=Na2SiO3+H2O (Na2SiO3的⽔溶液称为⽔玻璃) 75、⼆氧化硅与碱性氧化物的反应:SiO2+CaO=CaSiO3 ⾼温 76、刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O 77、⼯业制玻璃: CaCO3+SiO2=CaSiO3+CO2↑⾼温 Na2CO3+SiO2=Na2SiO3+CO2↑⾼温 78、⾦属铝在氧⽓中燃烧:4Al+3O2=2Al2O3 点燃 79、铝热反应:2Al+Fe2O3=Al2O3+2Fe⾼温 (铝粉与氧化铁粉的混合物称为铝热剂,⽤于焊接钢轨) 80、⾦属铝与酸的反应:2Al+6HCl=2AlCl3+3H2↑ 81、⾦属铝与碱的反应: 2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑(四羟基合铝酸钠) 82、实验室制氢氧化铝:AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl(⽩⾊沉淀) 83、氢氧化铝溶于强酸中:Al(OH)3+3H+=Al3++3H2O 84、氢氧化铝溶于强碱中: Al(OH)3+OH-=[Al(OH)4]- (四羟基合铝酸根离⼦) 85、氧化铝溶于强酸: Al2O3+6H+=2Al3++3H2O (氧化铝为两性氧化物) 86、氧化铝溶于强碱:Al2O3+2OH-+3H2O=2[Al(OH)4]- 87、碱式碳酸铜的制取:2Cu+O2+H2O+CO2=Cu2(OH)2CO3 (绿⾊) 88、铜与氧⽓的反应:Cu+O2=2CuO Δ 89、铜与硫粉的反应:2Cu+S=Cu2S Δ 90、4CuO=2Cu2O+O2↑⾼温(⿊⾊物质变为红⾊物质) 91、CuSO4·5H2O=CuSO4+5H2O↑ Δ (蓝⾊晶体变为⽩⾊粉末) 92、氯化铝与少量的氢氧化钠反应:Al3++3OH-=Al(OH)3↓ 93、氯化铝与过量的氢氧化钠反应:Al3++4OH-=[Al(OH)4]- 94、四羟基合铝酸根离⼦与酸的反应:[Al(OH)4]-+H+=H2O+Al(OH)3↓ 95、实验室制取氯⽓: 4HCl(浓)+MnO2 =MnCl2+Cl2↑+2H2O Δ (黄绿⾊⽓体、有毒、密度⽐空⽓⼤) 96、实验室制取⼆氧化碳: CaCO3+2HCl=CaCl2+H2O+CO2↑(⽆⾊⽆味、密度⽐空⽓⼤,溶于⽔)【⾼⼀化学必修⼀化学⽅程式⼤全】。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
◇+高一化学方程式总结◇+(一)
◇1Na:
1、钠与氧气反应:4Na+O2=2Na2O
钠在空气中燃烧:2Na+O2△Na2O2
2、钠与水反应:2Na+2H2O=2NaOH+H2↑
3、过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑
4、过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O2
5、金属钠与硫酸铜溶液:○12Na + 2H2O = 2NaOH + H2↑
○22NaOH + CuSO4 = Cu(OH)2↓+ Na2SO4
总方程式:2Na + CuSO4 + 2H2O = Cu(OH)2 + Na2SO4 + H2↑6、金属钠与四氯化钛:4Na + TiCl4熔融Ti + 4NaCl
◇2Cl:
7、氯气与金属铁反应:2Fe+3Cl2点燃2FeCl3
8、氯气与金属铜反应:Cu+Cl2点燃CuCl2
9、氯气与金属钠反应:2Na+Cl2点燃2NaCl
10、氯气与氢气反应:H2 + Cl2 点燃HCl
11、氯气与磷反应:P + Cl2(不足)点燃PCl3
P + Cl2(充足)点燃PCl5
12、氯气与水反应:Cl2+H2O=HCl+HClO
13、次氯酸光照分解:2HClO光照2HCl+O2↑
14、氯气与氢氧化钠溶液反应:Cl2+2NaOH=NaCl+NaClO+H2O
15、氯气与消石灰反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
16、盐酸与硝酸银溶液反应:HCl+AgNO3=AgCl↓+HNO3
17、漂白粉长期置露在空气中:Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO
◇3Fe:
18、氯化铁与氢氧化钠溶液反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl
19、硫酸亚铁与氢氧化钠溶液反应:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
20、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2+2H2O+O2=4Fe(OH)3
21、氢氧化铁加热分解:2Fe(OH)3△Fe2O3+3H2O↑
22、三氯化铁溶液与铁粉反应:2FeCl3+Fe=3FeCl2
23、氯化亚铁中通入氯气:2FeCl2+Cl2=2FeCl3
24、铁与水蒸气反应:3Fe+4H2O(g)=Fe3O4+4H2↑
25、氧化铁与盐酸反应:Fe2O3+6HCl=2FeCl3+3H2O
◇4N:
26、氮气与氧气在放电下反应:N2+O2放电2NO
27、一氧化氮与氧气反应:2NO+O2=2NO2
28、二氧化氮与水反应:3NO2+H2O=2HNO3+NO
29、NO、NO2的回收:NO2+NO+2NaOH=2NaNO2+H2O
30、浓硝酸与铜反应:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑
31、稀硝酸与铜反应:3Cu+8HNO3(稀)△3Cu(NO3)2+4H2O+2NO↑
32、氨气的实验室制取:2NH4Cl+Ca(OH)2△CaCl2+2H2O+2NH3↑
33、氨水受热分解:NH3•H2O△NH3↑+H2O
34、氨气与氯化氢反应:NH3+HCl=NH4Cl
35、氯化铵受热分解:NH4Cl△NH3↑+HCl↑
36、碳酸氢氨受热分解:NH4HCO3△NH3↑+H2O↑+CO2↑
37、硝酸铵与氢氧化钠反应:NH4NO3+NaOH△NH3↑+NaNO3+H2O
38、硫酸铵与氢氧化钠反应:(NH4)2SO4+2NaOH△2NH3↑+Na2SO4+2H2O ◇4S:
39、S + Fe△FeS
40、S + Cu△Cu2S
41、S + Na =Na2S
42、S + O2点燃SO2
43、S + H2△H2S
H2S + SO2 =S↓+ H2O
H2S + H2SO4(浓) = S↓+ SO2 + 2H2O [不能用浓硫酸干燥硫化氢]
44、二氧化硫与水反应:SO2+H2O≈H2SO3
45、二氧化硫与氧气在催化剂的作用下反应:2SO2+O2催化剂2SO3
46、三氧化硫与水反应:SO3+H2O=H2SO4
47、SO2+CaO=CaSO3
48、SO2尾气处理:SO2+2NaOH=Na2SO3+H2O
49、SO2+Ca(OH)2=CaSO3↓+H2O
50、SO2+Cl2+2H2O=2HCl+H2SO4
51、SO2 + CaO = CaSO3
52、实验室制取SO2: Na2SO3 + H2SO4(浓) △SO2↑+ H2O + Na2SO4
实验室制取H2S: Na2S + H2SO4△H2S + Na2SO4
53、浓硫酸与铜反应:Cu+2H2SO4(浓)△CuSO4+2H2O+SO2↑
54、浓硫酸与木炭反应:C+2H2SO4(浓)△CO2↑+2SO2↑+2H2O
◇5Mg
55、Mg的制取:○1CaCO3高温、煅烧CaO + CO2↑
○2CaO + H2O = Ca(OH)2
○3Mg2+ + Ca(OH)2 = Mg(OH)2 + Ca2+
○4Mg(OH)2 + 2HCl =MgCl2 + 2H2O
○5MgCl2电解、熔融Mg + Cl2↑
◇6Si
56、Si + O2△SiO2
57、Si+2F2=SiF4
58、二氧化硅与氢氟酸反应:SiO2+4HF=SiF4+2H2O
硅单质与氢氟酸反应:Si+4HF=SiF4+2H2↑
59、二氧化硅与氧化钙高温反应:SiO2+CaO高温CaSiO3
60、二氧化硅与氢氧化钠溶液反应:SiO2+2NaOH=Na2SiO3+H2O
硅单质与氢氧化钠溶液反应: Si+2NaOH+H2O=Na2SiO3+2H2↑
61、SiO2 + Na2CO3高温Na2SiO3 + CO2↑
62、往硅酸钠溶液中通入二氧化碳:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓
63、硅酸钠与盐酸反应:Na2SiO3+2HCl=2NaCl+H2SiO3↓
64、硅单质的实验室制法:粗硅的制取:SiO2+2C高温电炉Si+2CO
粗硅转变为纯硅:○1Si(粗)+2Cl2△SiCl4
○2SiCl4+2H2高温Si(纯)+4HCl
◇7Al
65、铝与氢氧化钠溶液反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
66、氧化铝与盐酸反应:Al2O3+6HCl=2AlCl3+3H2O
67、氯化铝与一水合氨反应:AlCl3 + 3NH3•H2O = Al(OH)3↓+ 3NH4Cl
68、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH + 3H2O=2Na[Al(OH)4]
四羟基合铝酸钠溶液通入二氧化碳:CO2(过量) + Na[Al(OH)4] = NaHCO3 + Al(OH)3↓
CO2(少量) + 2Na[Al(OH)4] = Na2CO3+ 2Al(OH)3↓+
H2O
69、实验室制取氢氧化铝:Al2(SO4)3+6NH3•H2O=2Al(OH)3↓+3(NH3)2SO4
70、氢氧化铝与盐酸反应:Al(OH)3+3HCl=AlCl3+3H2O
71、氢氧化铝与氢氧化钠溶液反应:Al(OH)3+NaOH=Na[Al(OH)4]
72、氢氧化铝加热分解:2Al(OH)3△Al2O3+3H2O
73、Al3+ + 3Al(OH)4-= 4Al(OH)3↓。
