化学仿制药参比制剂目录(第三十六批)(征求意见稿)
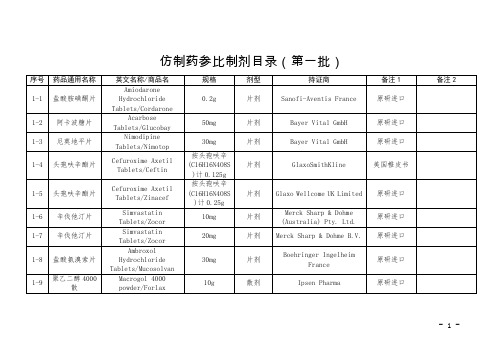
仿制药参比制剂目录(CFDA)
1-44
米索前列醇片
Misoprostol Tablets/Cytotec
0.2mg
片剂
Pharmacia Limited
原研进口
1-45
马来酸依那普利片
Enalapril Maleate Tablets/Renitec
5mg
片剂
Merck Sharp & Dohme(Australia)Pty. Ltd.
10mg
片剂
Merck Sharp & Dohme (Australia) Pty. Ltd.
原研进口
1-7
辛伐他汀片
Simvastatin Tablets/Zocor
20mg
片剂
Merck Sharp & Dohme B.V.
原研进口
1-8
盐酸氨溴索片
Ambroxol Hydrochloride Tablets/Mucosolvan
50mg
片剂
Bayer Vital GmbH
原研进口
1-3
尼莫地平片
Nimodipine Tablets/Nimotop
30mg
片剂
Bayer Vital GmbH
原研进口
1-4
头孢呋辛酯片
Cefuroxime Axetil Tablets/Ceftin
按头孢呋辛(C16H16N4O8S)计0.125g
片剂
GlaxoSmithKline
美国橙皮书
1-5
头孢呋辛酯片
Cefuroxime Axetil Tablets/Zinacef
按头孢呋辛(C16H16N4O8S)计0.25g
片剂
国家药监局关于发布仿制药参比制剂目录(第三十六批)的通告-国家药品监督管理局通告2021年第7号

制定机关
国家药品监督管理局
公布日期
2021.01.21
施行日期
2021.01.21
文号
国家药品监督管理局通告2021年第7号
主题类别
药政管理
效力等级
部门规范性文件
时效性
现行有效
正文:
----------------------------------------------------------------------------------------------------------------------------------------------------
国家药品监督管理局通告
2021年第7号
国家药监局关于Байду номын сангаас布仿制药参比制剂目录(第三十六批)的通告
经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第三十六批)。
特此通告。
附件:仿制药参比制剂目录(第三十六批)
国家药监局
2021年1月21日
——结束——
化学仿制药参比制剂目录(第二十四批)(公示征求意见稿)

化学仿制药参比制剂目录(第二十四批)(公示征求意见稿)
序号
药品通用名称
英文名称/商品名
规格
剂型
持证商
备注1
备注2
24-1
阿莫西林胶囊
Amoxicillin Capsules/Sawacillin
250mg
胶囊剂
Astellas Pharma Inc.
未进口原研药品
日本橙皮书
24-2
阿莫西林胶囊
Amoxicillin Capsules/PASETOCIN
CARDIZEMCD
120mg
控ቤተ መጻሕፍቲ ባይዱ胶囊剂
BAUSCH HEALTH US LLC
国际公认的同种药品
美国橙皮书
24-9
盐酸地尔硫卓控释胶囊
Diltiazem Hydrochloride Extended-release Capsules/CARDIZEMCD
180mg
控释胶囊剂
BAUSCH HEALTH US LLC
10mg
注射剂
Mitsubishi Tanabe Pharma Corporation
国内上市的原研药品
原研进口
24-35
注射用盐酸地尔硫䓬
Diltiazem Hydrochloride for Injection/HERBESSER(合贝爽)
50mg
注射剂
Mitsubishi Tanabe Pharma Corporation
美国橙皮书
24-13
注射用丙戊酸钠
Sodium Valproate for Injection/ Depakine(德巴金)
0.4g
注射剂
Sanofi Aventis Deutschland GmbH
化学仿制药参比制剂目录(第三十批)(征求意见稿)【模板】
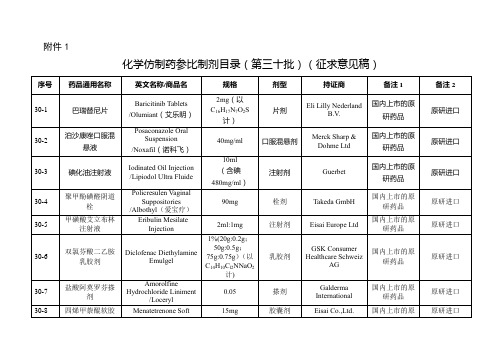
Fresenius Medical Care North America
未进口原研药品
美国橙皮书
30-29
地拉罗司片
Deferasirox Tablets/Jadenu
90mg
片剂
Novartis Pharmaceuticals Corporation
未进口原研药品
美国橙皮书
30-30
地拉罗司片
/Temodar
100mg
胶囊剂
Merck Sharp and Dohme Corp
未进口原研药品
美国橙皮书
30-45
替莫唑胺胶囊
Temozolomide Capsules
125μg
胶囊剂
IBSA Institut Biochimique SA
未进口原研药品
美国橙皮书
30-21
L-甲状腺素钠软胶囊
Levothyroxine Sodium Soft Capsules/Tirosint
137μg
胶囊剂
IBSA Institut Biochimique SA
未进口原研药品
美国橙皮书
氨氯地平5mg和阿托伐他汀40mg
片剂
Pfizer Inc
未进口原研药品
美国橙皮书
30-43
替莫唑胺胶囊
Temozolomide Capsules
/Temodar
20mg
胶囊剂
Merck Sharp and Dohme Corp
未进口原研药品
美国橙皮书
30-44
替莫唑胺胶囊
Temozolomide Capsules
30-16
L-甲状腺素钠软胶囊
国家药监局关于发布仿制药参比制剂目录(第八十批)的通告

国家药监局关于发布仿制药参比制剂目录(第八十
批)的通告
文章属性
•【制定机关】国家药品监督管理局
•【公布日期】2024.05.13
•【文号】国家药监局通告2024年第19号
•【施行日期】2024.05.13
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】药政管理
正文
国家药监局通告
2024年第19号
关于发布仿制药参比制剂目录(第八十批)的通告经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第八十批)。
特此通告。
附件:化学仿制药参比制剂目录(第八十批)
国家药监局
2024年5月13日。
《化学仿制药参比制剂目录(第四十五批)》(征求意见稿)

Indivior Europe Limited
未进口原研药品
欧盟上市
45-43
丁丙诺啡纳洛酮舌下片
Buprenorphine Hydrochloride and Naloxone Hydrochloride Sublingual Tablets
丁丙诺啡8mg/纳洛酮2mg(均以碱基计)
原研进口
45-2
恩他卡朋双多巴片(Ⅱ)
Entacapone,Levodopa and Carbidopa Tablets(Ⅱ)
左旋多巴100mg,卡比多巴25mg,恩他卡朋200mg
Orion Corporation
国内上市的原研药品
原研进口
45-3
结构脂肪乳注射液(C6~24)
Structural Fat Emulsion Injection(C6~24)/Structolipid(力文)
125mg
Actelion Pharmaceuticals Ltd
未进口原研药品
美国橙皮书
45-33
盐酸肾上腺素注射液/肾上腺素注射液
Epinephrine Injection/Epinephrine(Copackaged)
1mg/10mL(0.1mg/mL)
Hospira Inc
未进口原研药品
美国橙皮书
Indivior Europe Limited
未进口原研药品
欧盟上市
45-44
盐酸氮卓斯汀滴眼液
Azelastine Hydrochloride Eye Drops/Allergodil
0.5mg/ml(6ml)
MEDA Pharma GmbH & Co. KG
化学仿制药参比制剂目录(第四十二批)(征求意见稿)
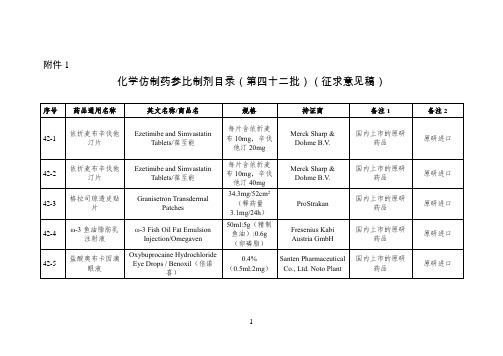
B.Braun Melsungen AG
未进口原研药品
欧盟上市
42-29
复方α-酮酸片
Compound α-Ketoacid Tablets
0.63g
Fresenius Kabi Deutschland GmbH
未进口原研药品
欧盟上市
42-30
盐酸头孢卡品酯颗粒
Cefcapene Pivoxil Hydrochloride Granules /Flomox
Idarubicin Hydrochloride Injection/Idamycin Pfs
1 mg/ml
Pfizer Inc
未进口原研
美国橙皮书
42-25
盐酸氟西汀口服溶液
Fluoxetine Hydrochloride Oral Solution/ Prozac
20mห้องสมุดไป่ตู้/5ml
Lilly France
0.146%
Glaukos Corporation
未进口原研药品
美国橙皮书
42-21
壬二酸凝胶
Azelaic Acid Gel / Finacea
15%
Leo Pharma AS
未进口原研药品
美国橙皮书
42-22
盐酸吉西他滨注射液
Gemcitabine Hydrochloride Injection
英文名称/商品名
规格
持证商
备注1
备注2
42-36
盐酸帕罗西汀片
Paroxetine Hydrochloride Tablets/赛乐特
20mg(以C19H20FNO3计)
中美天津史克制药有限公司
化学仿制药参比制剂目录(第二十九批)(征求意见稿)
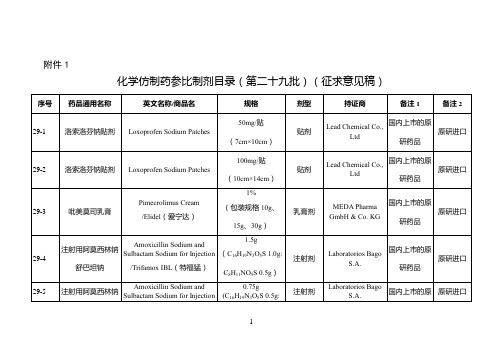
美国橙皮书
29-40
托吡酯缓释胶囊
Topiramate Extended-releaseCapsules /Trokendi XR
25mg
胶囊剂
Supernus Pharmaceuticals Inc.
未进口原研药品
美国橙皮书
29-41
托吡酯缓释胶囊
Topiramate Extended-releaseCapsules /Trokendi XR
Treprostinil Extended DiolaminereleaseTablets /Orenitram
1mg
(以曲前列尼尔计)
片剂
United Therapeutics Corporation
未进口原研药品
美国橙皮书
29-35
曲前列尼尔缓释片
Treprostinil Extended DiolaminereleaseTablets /Orenitram
/Priftin
150mg
片剂
Sanofi Aventis US LLC
未进口原研药品
美国橙皮书
29-32
曲前列尼尔缓释片
Treprostinil Diolamine Extended-releaseTablets /Orenitram
0.125mg
(以曲前列尼尔计)
片剂
United Therapeutics Corporation
胶囊剂
Purdue GMP Center LLC
未进口原研药品
美国橙皮书
29-45
布洛芬盐酸去氧肾上腺素片
美国橙皮书
29-43
托吡酯缓释胶囊
Topiramate Extended-releaseCapsules /Trokendi XR
化学仿制药参比制剂目录(第三十八批)(征求意见稿)
Indivior UK Limited
国内上市的原研药品
原研进口
38-76
羧甲基纤维素钠滴眼液
Carboxymethylcellulose Sodium Eye Drops / Refresh Celluvisc
0.4ml:2mg
Allergan Pharmaceuticals Ireland
附件1
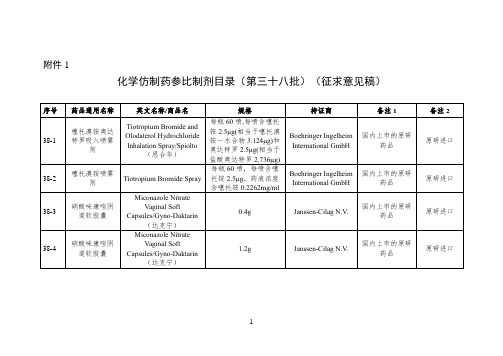
化学仿制药参比制剂目录(第三十八批)(征求意见稿)
序号
药品通用名称
英文名称/商品名
规格
持证商
备注1
备注2
38-11
噻托溴铵奥达特罗吸入喷雾剂
Tiotropium Bromide and Olodaterol Hydrochloride Inhalation Spray/Spiolto(思合华)
每瓶60喷,每喷含噻托铵2.5μg(相当于噻托溴铵一水合物3.124μg)和奥达特罗2.5μg(相当于盐酸奥达特罗2.736μg)
Boehringer Ingelheim International GmbH
国内上市的原研药品
原研进口
38-22
噻托溴铵喷雾剂
Tiotropium Bromide Spray
4.选择未进口参比制剂开展仿制药研究除满足其质量要求外,还需满足现行版《中国药典》和相关指导原则要求。
附件2
已发布化学仿制药参比制剂目录(增补)(征求意见稿)
序号
药品通用名称
英文名称/商品名
规格持证商备注1Fra bibliotek备注2
38-32
富马酸伏诺拉生片
Vonoprazan Fumarate Tablets /Vocinti(沃克)
化学仿制药参比制剂目录(第三十七批)》(征求意见稿)
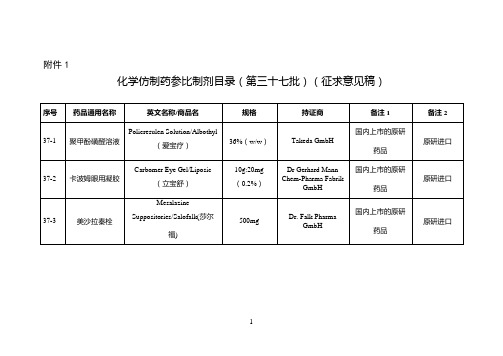
地奈德洗剂
DesonideLotion/Desowen
0.05%(120ml)
GaldermaAustralia Pty Ltd /GaldermaHong Kong Limited
国际公认的同种药品
增加持证商GaldermaHong Kong Limited
备注
1.未在国内上市品种,需参照原总局2015年第230号公告等的相关要求开展研究,通用名、剂型等经药典委核准后为准。
10g:20mg(0.2%)
DrGerhard MannChem-PharmaFabrikGmbH
国内上市的原研药品
原研进口
37-3
美沙拉秦栓
MesalazineSuppositories/Salofalk(莎尔福)
500mg
Dr. Falk Pharma GmbH
国内上市的原研药品
原研进口
37-43
GlaxosmithklineConsumer Healthcare Holdings USLlc
未进口原研药品
美国橙皮书
37-76
盐酸氯普鲁卡因注射液
ChloroprocaineHydrochloride Injection/Clorotekal
50mg/5ml(10mg/ml)
B Braun MedicalInc
未进口原研药品
日本上市
8-267
醋酸地塞米松片
Dexamethasone Acetate Tablets/Dectancyl
0.5mg
Sanofi Aventis France
欧盟上市
修订,不限上市国及产地
24-24
酮咯酸氨丁三醇注射液
Ketorolac Trometamol/Taradyl
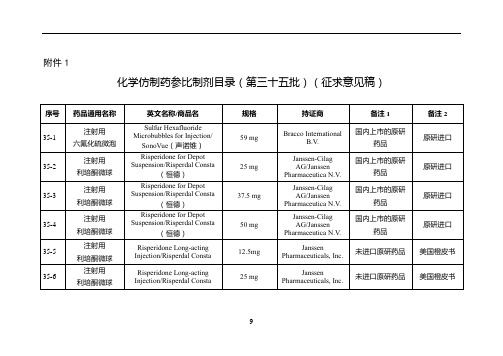
化学仿制药参比制剂目录(第三十五批)(征求意见稿)
4.选择未进口参比制剂开展仿制药研究除满足其质量要求外,还需满足现行版《中国药典》和相关指导原则要求。
附件3
未通过审议品种目录
序号
药品通用名称
英文名称/商品名
规格
持证商
备注1
备注2
遴选情况说明
35-41
氟轻松油剂
Fluocinolone Acetonide Oil/ Derma-Smoothe/FS
Baxter Healthcare
Pty Ltd
未进口原研药品
澳大利亚上市
35-19
琥珀酸
呋罗曲坦片
Frovatriptan Tablet/Isimig
2.5mg
Menarini International Operations Luxembourg SA
未进口原研药品
欧盟上市
35-20
间苯三酚
口服冻干片
甲氧苄啶16mg/ml
Roche S.p.A
未进口原研药品
欧盟上市
35-22
依托芬那酯凝胶
Etofenamate Gel/Traumon
5%(50g,100g)
MEDA Manufacturing GmbH
未进口原研药品
欧盟上市
35-23
依托芬那酯凝胶
Etofenamate Gel/Traumon
10%(50g,100g)
美国橙皮书
35-9
注射用
利培酮微球
Risperidone powder and solvent for depot suspension for Injection/Risperdal Consta
化学仿制药参比制剂目录(第二十九批)(征求意见稿)

225mg
胶囊剂
GlaxoSmithKline LLC
未进口原研药品
美国橙皮书
29-29
盐酸普罗帕酮缓释胶囊
Propafenone Hydrochloride Extended-release Capsules
/Rythmol SR
325mg
胶囊剂
GlaxoSmithKline LLC
78mg/0.5ml
(以棕榈酸帕利哌酮计)
注射剂
Jassen Pharmaceuticls Inc
未进口原研药品
美国橙皮书
29-23
棕榈酸帕利哌酮注射液
Paliperidone Palmitate Extended-releaseInjectable Suspension/Invega Sustenna
29-12
盐酸氮卓斯汀滴眼液
Azelastine Hydrochloride Eye Drops
6ml:3mg
眼用制剂
MEDA PharmaGmbH& Co. KG
国内上市的原研药品
原研进口
29-13
伊布替尼胶囊
Ibrutinib Capsules
/Imbruvica(亿珂)
140mg
胶囊剂
Pharmacyclics LLC
国内上市的原研药品
原研进口
29-6
荧光素钠注射液
Fluorescein Sodium Injection
/Fluorescite(历设得)
5ml:0.5g(10%)
(以荧光素计)
注射剂
Alcon Laboratories Inc
国内上市的原研药品
化学仿制药参比制剂目录(第三十六批)(征求意见稿)【模板】

原研进口
36-10
吡仑帕奈片
Perampanel Tablets/Fycompa(卫克泰)
4mg
Eisai Europe Limited
国内上市的原研药品
原研进口
36-11
吡仑帕奈片
Perampanel Tablets/Fycompa
2mg
Eisai Inc
未进口原研药品
美国橙皮书
附件2
已发布化学仿制药参比制剂目录(增补)(征求意见稿)
序号
药品通用名称
英文名称/商品名
规格
持证商
备注1
备注2
36-34
双氯芬酸钠缓释片
Diclofenac Sodium extended release tablet/Voltaren SR 100
0.1g
Novartis Pharma AG
国内上市的原研药品
Palbociclib Tablets/Ibrance
75mg
Pfizer Inc
未进口原研药品
美国橙皮书
36-17
哌柏西利片
Palbociclib Tablets/Ibrance
100mg
Pfizer Inc
未进口原研药品
美国橙皮书
36-18
哌柏西利片
Palbociclib Tablets/Ibrance
150mg /15mL (10mg /mL)
Nabriva Therapeutics Ireland DAC
未进口原研药品
美国橙皮书
36-15
硫酸长春新碱注射液
Vincriscristine Sulfate Injection
国家药监局关于发布仿制药参比制剂目录(第八十三批)的通告

国家药监局关于发布仿制药参比制剂目录(第八十三
批)的通告
文章属性
•【制定机关】国家药品监督管理局
•【公布日期】2024.09.27
•【文号】国家药监局通告2024年第37号
•【施行日期】2024.09.27
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】药政管理
正文
国家药监局通告
2024年第37号
关于发布仿制药参比制剂目录(第八十三批)的通告
经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第八十三批)。
特此通告。
附件:化学仿制药参比制剂目录(第八十三批)
国家药监局
2024年9月27日。
仿制药参比制剂目录(第三十一至四十批)

Guanfacine Hydrochloride Extended Release Tablets/
Intuniv Guanfacine Hydrochloride Extended Release Tablets/
Intuniv Guanfacine Hydrochloride Extended Release Tablets/
片
Tablets/Odefsey
Bimatoprost ophthalmic 31-24 贝美前列素涂剂
solution/Latisse
3ml:0.9mg
Allergan INC
31-25 奥泽沙星乳膏 Ozenoxacin Cream/Xepi 1%(10g、30g、45g)Ferrer Internacional SA
Intuniv
Lidocaine and Tetracaine Cream/Pliaglis
规格 15mg 30mg
1mg
持证商 Specgx LLC Specgx LLC
Shire Development Inc
2mg
Shire Development Inc
3mg
Shire Development Inc
Infants' Motrin
40mg:ml(15ml、 30ml)
Johnson And Johnson Consumer Inc Mcneil Consumer Healthcare
Divisioon
利巴韦林冻干粉 Ribavirin For Inhalation
31-17
6g
吸入剂
Solution/Virazole
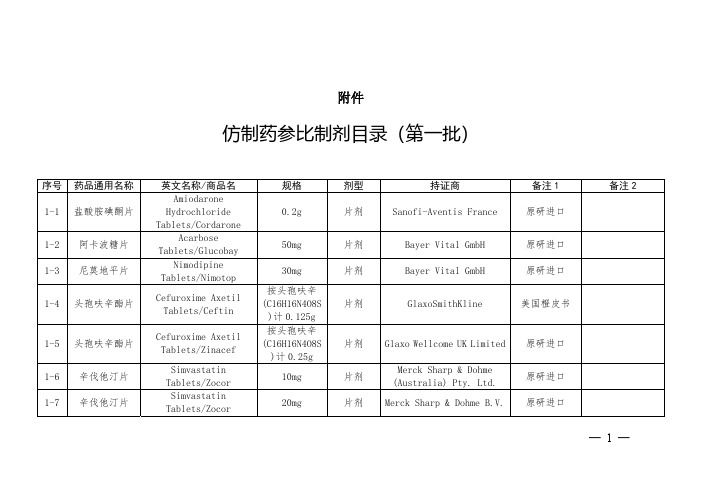
仿制药参比制剂目录1-16批

1-44
米索前列醇片
Misoprostol Tablets/Cytotec
0.2mg
片剂
Pharmacia Limited
原研进口
1-45
马来酸依那普利片
Enalapril Maleate Tablets/Renitec
5mg
片剂
Merck Sharp & Dohme(Australia)Pty. Ltd.
30mg
片剂
Boehringer Ingelheim France
原研进口
1-9
聚乙二醇4000散
Macrogol 4000 powder/Forlax
10g
散剂
Ipsen Pharma
原研进口
1-10
醋酸去氨加压素片
Desmopressin Acetate Tablets/Minirin
0.1mg
25mg
胶囊剂(软胶囊)
Novartis Pharma Schweiz AG
原研进口
1-26
环孢素软胶囊
Ciclosporin Soft Capsules/Sandimmun Neoral
50mg
胶囊剂(软胶囊)
Novartis Pharma Schweiz AG
原研进口
1-27
甲巯咪唑片
Thiamazole Tablets/Thyrozol
片剂
GlaxoSmithKline
美国橙皮书
1-5
头孢呋辛酯片
Cefuroxime Axetil Tablets/Zinacef
按头孢呋辛(C16H16N4O8S)计0.25g
片剂
Glaxo Wellcome UK Limited
食品药品监管总局办公厅公开征求仿制药质量和疗效一致性评价参比制剂备案与推荐程序的意见

食品药品监管总局办公厅公开征求仿制药质量和疗效一致性评价参比制剂备案与推荐程序的意见文章属性•【公布机关】国家食品药品监督管理总局•【公布日期】2016.04.11•【分类】征求意见稿正文食品药品监管总局办公厅公开征求仿制药质量和疗效一致性评价参比制剂备案与推荐程序的意见为落实《国务院办公厅关于开展仿制药质量和疗效一致性评价意见的通知》(国办发〔2016〕8号)的有关要求,食品药品监管总局组织起草了《仿制药质量和疗效一致性评价参比制剂备案与推荐程序(征求意见稿)》,现向社会公开征求意见。
请将修改意见于2016年4月30日前通过电子邮件反馈至国家食品药品监督管理总局仿制药质量一致性评价办公室。
电子邮件:*************.cn附件:仿制药质量和疗效一致性评价参比制剂备案与推荐程序(征求意见稿)食品药品监管总局办公厅2016年4月11日附件仿制药质量与疗效一致性评价参比制剂备案与推荐程序(征求意见稿)为贯彻落实国务院办公厅《关于开展仿制药质量和疗效一致性评价的意见》(国办发〔2016〕8号)的任务要求,进一步明确参比制剂的选择流程,制定本备案与推荐程序。
一、本程序所述参比制剂备案与推荐工作,是指药品生产企业、行业协会、原研药品生产企业、国际公认的同种药物生产企业等作为申请人或推荐人,参照《普通口服固体制剂参比制剂选择和确定指导原则》,通过备案、推荐、申报等方式,选择参比制剂的过程。
二、药品生产企业可通过备案的方式选择参比制剂。
生产企业填写《参比制剂备案表》(附件1);撰写《综述资料》(附件4),详述参比制剂选择理由;提交所生产品种现行有效的批准证明文件,生产产品首次批准和上市后变更等历史沿革情况的说明。
三、行业协会可组织同品种生产企业提出参比制剂的推荐意见。
行业协会填写《参比制剂推荐表》(附件2);撰写《综述资料》(附件4),详述参比制剂选择理由;提交行业协会资质证明复印件、推荐过程记录与说明、相关同品种生产企业同意推荐的证明性文件。
CFDA化学仿制药参比制目录总(精编)1-22
0.25g(按 C17H18FN3O3
计)
片剂
Bayer Vital GmbH
原研进口
进口产品现名为 环丙沙星片。
— 4 ——
1-35
盐酸环丙沙星 片
Ciprofloxacin Hydrochloride Tablets/Ciprobay
0.5g(按 C17H18FN3O3
计)
片剂
Bayer Vital GmbH
Tablets/Augmentin
Amoxicillin and Clavulanate Potassium
Tablets/Augmentin
Amoxicillin and Clavulanate Potassium
Tablets/Augmentin
Glimepiride Tablets/Amaryl
片剂
Bayer SA-NV
原研进口
胶囊剂
Bayer Healthcare LLC
美国橙皮书
附件
序号 2-1
药品通 用名称
盐酸胺 碘酮片
仿制药参比制剂目录(第二批)
英文名称/商品名
Amiodarone Hydrochloride Tablets/Ancaron
规格 0.1g
剂型 片剂
持证商 Sanofi K.K.
Nimodipine Tablets/Nimotop
Cefuroxime Axetil Tablets/Ceftin
Cefuroxime Axetil Tablets/Zinacef
Simvastatin Tablets/Zocor Simvastatin Tablets/Zocor
规格
0.2g
化学仿制药参比制剂目录(第三十批)(征求意见稿)

30-41
氨氯地平阿托伐他汀钙片
Amlodipine Besylate and Atorvastatin Calcium Tablets/Caduet
氨氯地平5mg和阿托伐他汀20mg
片剂
Pfizer Inc
未进口原研药品
美国橙皮书
30-42
氨氯地平阿托伐他汀钙片
Amlodipine Besylate and Atorvastatin Calcium Tablets/Caduet
未进口原研药品
美国橙皮书
30-38
卡格列净二甲双胍缓释片
Canagliflozin and Metformin Hydrochloride Extended Release Tables
/Invokamet XR
卡格列净50mg和盐酸二甲双胍1000mg
片剂
Janssen Pharmaceuticals Inc
醋酸钙口服溶液
Calcium Acetate Oral Solution/Phoslyra
667mg/5ml
口服溶液剂
Fresenius Medical Care North America
未进口原研药品
美国橙皮书
30-29
地拉罗司片
Deferasirox Tablets/Jadenu
90mg
片剂
Novartis Pharmaceuticals Corporation
2ml:1mg
注射剂
Eisai Europe Ltd
国内上市的原研药品
原研进口
30-6
双氯芬酸二乙胺乳胶剂
Diclofenac Diethylamine Emulgel
第1至第24批仿制药参比制剂目录(截止2019年9月)

Limited Les Laboratoires Servier
原研进口 原研进口 原研进口
进口产品现名为 环丙沙星片。
片剂(缓 释片)
Les Laboratoires Servier
原研进口
-4-
1-39
左甲状腺素钠 片
1g (C16H19N3O5 S 0.875g 与
C8H9NO5 0.125g)
1mg
2mg
10mg
25mg
50mg
5mg
75mg
片剂
片剂
片剂
片剂 胶囊剂 (软胶 囊) 胶囊剂 (软胶 囊) 胶囊剂 (软胶 囊) 片剂
片剂
Beecham Group Plc
Beecham Group Plc
Sanofi-Aventis Deutschland GmbH Sanofi-Aventis Deutschland GmbH Novartis Pharma Schweiz
10g
剂型 片剂 片剂 片剂 片剂
片剂 片剂 片剂 片剂 散剂
持证商 Sanofi-Aventis France
备注 1 原研进口
Bayer Vital GmbH Bayer Vital GmbH
原研进口 原研进口
GlaxoSmithKline
美国橙皮书
Glaxo Wellcome UK Limited 原研进口
Amoxicillin and Clavulanate Potassium
Tablets/Augmentin
Glimepiride Tablets/Amaryl
Glimepiride Tablets/Amaryl Ciclosporin Soft Capsules/Sandimmun
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
MSD SHARP & DOHME GMBH/MSD France/MSD ItaliaS.r.l./Merck Sharp &DohmeBV
未进口原研药品
NabrivaTherapeutics Ireland DAC
未进口原研药品
美国橙皮书
36-15
硫酸长春新碱注射液
VincriscristineSulfate Injection
1mg/ml
Hospira,Inc
国际公认同种药品
美国橙皮书
36-16
哌柏西利片
PalbociclibTablets/Ibrance
50mg
G.D. Searle LLC
未进口原研药品
美国橙皮书
36-39
舒更葡糖钠注射液
SugammadexSodium Injection/Bridion
200mg/2ml
OrganonUS aIncA Sub Of Merck And CoInc
未进口原研药品
美国橙皮书
36-40
盐酸帕罗西汀肠溶缓释片
75mg
PfizerInc
未进口原研药品
美国橙皮书
36-17
哌柏西利片
PalbociclibTablets/Ibrance
100mg
PfizerInc
未进口原研药品
美国橙皮书
36-18
哌柏西利片
PalbociclibTablets/Ibrance
125mg
Pfizerinc
未进口原研药品
美国橙皮书
36-19
Paroxetine Hydrochloride Enteric-Coated Sustained-Release Tablets/Paxil Cr
37.5mg
ApotexTechnologiesInc
未进口原研药品
美国橙皮书
36-41
注射用硫酸艾莎康唑
IsavuconazoniumSulfate for Injection/Cresemba
0.1g
Novartis Pharma AG
国内上市的原研药品
原研进口
36-35
他克莫司缓释胶囊
Tacrolimus Sustained-release Capsules/新普乐可复
0.5mg
AstellasPharma Europe B.V.
国内上市的原研药品
原研进口
36-36
他克莫司缓释胶囊
Tacrolimus Sustained-release Capsules/新普乐可复
伊布替尼片
IbrutinibTablets/Imbruvica
420mg
PharmacyclicsLLC
未进口原研药品
美国橙皮书
36-20
伊布替尼片
IbrutinibTablets/Imbruvica
280mg
PharmacyclicsLLC
未进口原研药品
美国橙皮书
36-21
伊布替尼片
IbrutinibTablets/Imbruvica
原研进口
36-8
骨化三醇注射液
Calcitriol Injection/Calcijex(溉纯)
1ml:1μg
AbbVie Pte. Ltd.
国内上市的原研药品
原研进口
36-9
吡仑帕奈片
PerampanelTablets/Fycompa(卫克泰)
2mg
Eisai Europe Limited
国内上市的原研药品
36-5
塞瑞替尼胶囊
CeritinibCapsules /Zykadia(赞可达)
150mg
NovartisEuropharmLimited
国内上市的原研药品
原研进口
36-6
吸入用伊洛前列素溶液
IloprostSolution for Inhalation/Ventavis(万他维)
2ml:20μg
1g:0.01g
TheramexIreland Limited
未进口原研药品
欧盟上市
36-30
依托孕烯炔雌醇阴道环
EtonogestrelandEthinylestradiolVaginal Ring
依托孕烯11.7mg;炔雌醇2.7mg
anon
未进口原研药品
欧盟上市
36-31
雷马曲班片
未进口原研药品
欧盟上市
36-49
普瑞巴林胶囊
PregabalinCapsules/Lyrica
25mg
Pfizer
未进口原研药品
欧盟上市
36-50
普瑞巴林胶囊
PregabalinCapsules/Lyrica
50mg
Pfizer
未进口原研药品
欧盟上市
36-51
普瑞巴林胶囊
PregabalinCapsules/Lyrica
4mg
EisaiInc
未进口原研药品
美国橙皮书
36-13
贝派度酸片
BempedoicAcid Tablets
180mg
EsperionTherapeuticsInc
未进口原研药品
美国橙皮书
36-14
来氟米林注射液
lefamulinInjection/Xenleta
150mg /15mL (10mg /mL)
未进口原研药品
欧盟上市
36-45
达沙替尼片
DasatinibTablets /Sprycel
50mg
Bristol-Myers Squibb Pharma EEIG
未进口原研药品
欧盟上市
36-46
达沙替尼片
DasatinibTablets /Sprycel
70mg
Bristol-Myers Squibb Pharma EEIG
原研进口
36-10
吡仑帕奈片
PerampanelTablets/Fycompa(卫克泰)
4mg
Eisai Europe Limited
国内上市的原研药品
原研进口
36-11
吡仑帕奈片
PerampanelTablets/Fycompa
2mg
EisaiInc
未进口原研药品
美国橙皮书
36-12
吡仑帕奈片
PerampanelTablets/Fycompa
150mg
Pfizer
未进口原研药品
欧盟上市
36-52
普瑞巴林胶囊
PregabalinCapsules/Lyrica
200mg
Pfizer
未进口原研药品
欧盟上市
36-53
普瑞巴林胶囊
PregabalinCapsules/Lyrica
225mg
Pfizer
未进口原研药品
欧盟上市
36-54
注射用醋酸卡泊芬净
372mg(按艾沙康唑计200mg)
AstellasPharma US, Inc.
未进口原研药品
美国橙皮书
36-42
骨化三醇软胶囊
Calcitriol Soft Capsules/Rocaltrol
0.25μg
ValidusPharmaceuticals LLC
未进口原研产品
美国橙皮书
36-43
琥珀酸美托洛尔缓释片
0.10%
Novartis Pharmaceuti皮书
36-24
左卡尼汀片
LevocarnitineTablets/Carnitor
330mg
LeadiantBiosciencesInc
未进口原研药品
美国橙皮书
36-25
艾拉戈克钠片
ElagolixSodium Tablets/Orilissa
1mg
AstellasPharma Europe B.V.
国内上市的原研药品
原研进口
36-37
注射用硼替佐米
BortezomibFor Injection/Velcade
3.5mg
Millennium PharmaceuticalsInc
未进口原研药品
美国橙皮书
36-38
塞来昔布胶囊
Celecoxib Capsules/Celebrex
150mg
AbbVie Inc.
未进口原研药品
美国橙皮书
36-26
艾拉戈克钠片
ElagolixSodium Tablets/Orilissa
200mg
AbbVie Inc.
未进口原研药品
美国橙皮书
36-27
注射用马来酸匹杉琼
Pixantroneinjection/Pixuvri
29mg
LesLaboratoiresServier
附件1
化学仿制药参比制剂目录(第三十六批)(征求意见稿)
序号
药品通用名称
英文名称/商品名
规格
持证商
备注1
备注2
36-1
碘普罗胺注射液
IopromideInjection/Ultravist(优维显)
100ml:76.89g
Bayer Vital GmbH
国内上市的原研药品
原研进口
36-2
利奥西呱片
RiociguatTablets/Adempas(安吉奥)
4.选择未进口参比制剂开展仿制药研究除满足其质量要求外,还需满足现行版《中国药典》和相关指导原则要求。
附件2
已发布化学仿制药参比制剂目录(增补)(征求意见稿)
