分析化学数据处理及结果计算解读
化学实验中的数据处理与结果分析

化学实验中的数据处理与结果分析在化学实验中,数据处理和结果分析是非常重要的步骤。
通过对实验数据的处理和分析,我们可以得出结论,验证假设,揭示规律,并进一步推动科学研究的发展。
本文将介绍一些常见的数据处理方法和结果分析技巧。
一、数据处理方法1. 数据整理和清洗:在进行实验前,我们首先要对实验数据进行整理和清洗,确保数据的准确性和可靠性。
包括检查实验操作是否规范、检查仪器是否校准,排除异常值等。
2. 数据平均值计算:在重复试验中,我们通常会进行多次测量,然后计算这些测量结果的平均值,以减小实验误差的影响。
平均值可以更好地代表实验结果。
3. 标准差和误差分析:标准差是衡量数据的离散程度的指标,它可以反映实验数据的稳定性和精确度。
误差分析可以帮助我们评估实验误差的来源,并优化实验方案。
4. 曲线拟合和回归分析:对于一些实验数据呈现出曲线关系的情况,我们可以通过曲线拟合和回归分析来拟合数据,得出曲线方程和相关参数,以获得更多的信息和推断。
二、结果分析技巧1. 结果的可靠性评估:在进行结果分析时,我们需要评估实验结果的可靠性。
可以考虑的因素包括实验方法的适用性、实验数据的准确性和重复性等。
2. 结果与理论比较:将实验结果与理论值进行对比,可以评估实验数据的准确性和实验方法的有效性。
如果实验结果与理论值相符,说明实验结果是可靠的。
3. 结果的趋势和规律分析:通过对实验数据的趋势和规律进行分析,可以揭示化学现象背后的科学规律。
例如,某实验结果随着时间的变化呈现出一定的规律性,我们可以通过分析这种规律性来深入了解化学反应的动力学过程。
4. 结果的讨论和解释:在结果分析中,我们也要对实验结果进行讨论和解释。
可以结合相关的理论知识和先前的研究成果,解释实验结果背后的原因和机制。
结论在化学实验中,数据处理和结果分析是确保实验结果准确性和可靠性的关键步骤。
通过合理的数据处理方法和结果分析技巧,我们可以更好地理解实验数据,揭示化学规律,并推动科学研究的进展。
分析化学中的数据处理

第7章Management of Experimental Data in AnalyticalChemistry分析化学中的数据处理7.1 统计学(statistics)中常用术语1、总体:所考察的对象的全体。
2、样本(子样):自总体中随机抽出的一组测量值。
3、样本大小(或容量):样本中所含测量值的数目。
3、值表:f t ,α体现t , f , P 之间的关系已知f , P 时,可从表中查出相应的t 值。
表中置信度就是概率P ,它表示t 值一定时,测定值落在范围内的概率。
) (s t ⋅±μ显著性水准P −=1 α自由度n n f , 1−=为测定次数双边:表示P 是从-t 到+t 积分而得的面积。
检验时的标准置信度=P%95检验步骤a. 根据题意计算t计b. 计算出α , f, 查t表c. 比较t计与t表,然后作出结论计算α , f ,05.095.011 =−=−=P α3141=−=−=n f 查表7-3,得18.33,05.0=t 因为t 计= 8>t 0.05,3所以,平均值与标准值存在显著性差异。
分析结果存在系统误差。
•由F 的定义式可计算得F值若F→1,则s1与s2 相差不大;若F 较大,则s1与s2存在显著性差异。
检验步骤a. 计算F值,b. 计算f大,f小,查F值表得F表c. 比较:若F计>F表,存在显著性差异;反之,不存在显著性差异。
(3) 查F 值表:计算自由度516=−==小大f f 由表7-4 查得F 表= 5.05(4) 由于F 计= 2.22 , 故F 计<F 表所以,该两组数据的精密度无显著性差异。
作出此判断的置信度为90%。
检验步骤:①用F检验法:检验s1与s2 之间是否存在显著性差异。
如s1与s2 之间存在显著性差异,则两组分析数据存在显著性差异。
如s1与s2 之间不存在显著性差异,则可认为s1≈s2 ,可计算合并标准偏差继续进行下述检验。
查t 值表,得t表值。
分析化学 误差与数据处理0.

二、分析结果的准确度和精密度
例题2、下列情况对分析结果产生何种影响(A.正误差;B.负误 差;C.无影响;D.降低精密度)
(1)用甲基橙作为指示剂标定HCl溶液时,使用的基准物Na2CO3 中含少量NaHCO3( 偏高 )
(2)若H2C2O4.2H2O基准物长期置于有干燥剂的干燥器中,用它 标定NaOH溶液的浓度,得到的结果将 ( 偏低 ) (2)在差减法称量中第一次称量使用了磨损的法码( ) (4)配标准溶液时,容量瓶内溶液未摇匀( ) (5)滴定分析中,用移液管取被测溶液时,未用被测溶液洗移 液管 ( )
准确且精密 不准确但精密 准确但不精密 不准确且不精密
精密度是保证准确度的先决条件; 精密度好,不一定准确度高.
二、分析结果的准确度和精密度
5、分析数据的评断
➢ 可疑数据的取舍 过失误差的判断 目的:确定某个数据是否可用; 方法: 4d 法 Q检验法 格鲁布斯(Grubbs)检验法
➢ 分析方法的准确性系统误差及偶然误差的判断
①绝对偏差 di xi x ∑di = 0
②平均偏差
d
1 n
n i 1
di
——测定次数少时(样本平均偏差)
n
xi m
i 1
n
——测定次数多时( 总体平均偏差)
③相对平均偏差
d dr x 100 %
二、分析结果的准确度和精密度
(2)偏差的表示方法
④标准偏差
n
xi x 2 ——样本标准偏差S:
பைடு நூலகம்
二、分析结果的准确度和精密度
4、影响精密度的因素 ——方法存在偶然误差 (1)偶然误差(随机误差)的概念 (2)偶然误差的特点
分析化学中的数据处理

分析化学中的数据处理
1.正态分布(高斯GAUSS分布)
它在概率统计中占有特别重要的地位,因为 许多随机变量都服从或近似服从正态分布, 分析测定中的随机误差也是这样的,P55图 3-3即为正态分布曲线,它的数学表达式为:
分析化学中的数据处理
若对某试样作若干批测定,每批又作n个 平行测定
则
S
=
X
S n
由此可见:
(2-4)
①平均值的精密度比单次测定的精密度
更次好数,的S X平方S根;成平反均比值.的②标增准加偏测差定与次测数定,
可使平均值的标准偏差减小。
作
s x
n 关系图如P59图3-5所示。
s
分析化学中的数据处理
分析化学中的数据处理
§2.1 几个概念(P52)
研究对象的某种特性值的全体叫总体; 从总体中随机取出的一组数据叫样本; 样本所含测量值的数目叫样本容量。例 如,对某矿石中Fe的含量作了无限次测 定,所得无限多个数据的集合就是总体, 其中每个数据就是个体,从中随机取出 一组数据(例如8个数据)就是样本,样 本容量为8。
3)大多数测定值集中在µ的附 近,所以µ为最可信赖值或 最佳值
分析化学中的数据处理
正态分布曲线随µ、σ值不同而不同,应
用起来不方便,为此,采用变量转换的
方法,将其化为同一分布-标准正态分
布
即
u= x-
令 代入(2-5)式得
y=f(x)=
1
- u2
e2
2
又 dx= du
第三章 分析化学中的数据处理

m
◇分析天平(称至0.1mg):12.8228g(6) , 0.2348g(4) , 0.0600g(3) ◇千分之一天平(称至0.001g): 0.235g(3) ◇1%天平(称至0.01g): 4.03g(3), 0.23g(2) ◇台秤(称至0.1g): 4.0g(2), 0.2g(1)
V
☆滴定管(量至0.01mL):26.32mL(4), 3.97mL(3) ☆容量瓶:100.0mL(4),250.0mL (4) ☆移液管:25.00mL(4); ☆量筒(量至1mL或0.1mL):25mL(2), 4.0mL(2)
如果测量数据 不断增多,组分 得越来越细,直 方图则逐渐趋于 一条平滑的曲 线—正态分布曲 线。 离散特性:各数据是分散的,波动的
s: 总体标准偏差
s
x
i 1
n
i
2
n
29
集中趋势:有向某个值集中的趋势
: 总体平均值
1 n lim x n n i 1
i
d: 总体平均偏差
3、随机误差: 由一些随机的偶然的不可避免的原因所造成的误 差。 特点:①波动性,可变性,无法避免; 例如:已知某矿石中Fe2O3 真实含量为50.36%, 测量值具波动性如下所示:50.40%, 50.30%, 50.25%, 50.37%; ②符合统计规律:正态分布规律。
4、减小随机误差
在消除系统误差的前提下,平行测定次数愈多, 平均值愈接近真实值。因此,增加测定次数,可 以提高平均值精密度而减小随机误差。在一般化 学分析中,对于同一试样,通常要求平行测定 2 ~ 4次即可。
3.2.2 有效数字修约规则 舍去多余数字的过程,称为数字修约。数字修 约遵循的规则:四舍六入五成双。例:将下列 测量值修约为三位有效数字
高三化学总结化学实验中的数据处理与结果分析方法

高三化学总结化学实验中的数据处理与结果分析方法在高三化学学习中,进行化学实验是必不可少的一环。
通过化学实验,我们可以亲自操作,观察实验现象,积累实验经验,加深对化学概念和原理的理解。
然而,仅仅进行实验是不够的,更为重要的是对实验数据进行处理和结果进行分析。
下面将对化学实验中的数据处理与结果分析方法进行总结。
一、数据处理方法1.无量纲量的计算在化学实验中,我们经常会遇到一些无量纲量的计算,如摩尔比率、pH值、溶解度积等。
对于这些无量纲量,我们可以通过直接计算或间接计算得到。
例如,在计算摩尔比率时,可以根据反应物的化学方程式写出化学计量关系,然后根据实际实验数据计算出比率。
2.浓度计算浓度计算是化学实验中常见的数据处理方法之一。
浓度可以用质量浓度、体积浓度和摩尔浓度来表示。
在计算浓度时,需要明确溶质和溶剂的质量或体积,并根据摩尔比率来计算摩尔浓度。
3.误差处理在实际实验中,由于各种因素的干扰,实验数据会存在一定的误差。
因此,对于实验数据的处理,需要进行误差处理。
常见的误差处理方法包括均值计算、相对误差计算、绝对误差计算等。
通过对实验数据的误差处理,可以更加准确地评估实验结果的可靠性。
二、结果分析方法1.图表展示在化学实验中,通过绘制图表可以有效地表达实验结果。
常见的图表有曲线图、柱状图、散点图等。
图表展示可以清晰地展示实验结果的变化趋势和规律,便于进行比较和分析。
2.结果解释与推理对于实验结果的分析,需要进行结果解释和推理。
通过对实验结果的解释,可以深入理解实验现象和化学原理。
同时,通过对实验结果的推理,可以对未知因素进行推断和猜测,为进一步的研究提供思路和方向。
3.误差分析在结果分析中,需要对实验误差进行分析。
误差分析可以帮助我们评估实验结果的可靠性,并提出改进的建议。
对于实验误差的分析,可以从实验条件、仪器设备、操作技术等方面进行分析,以减小误差并提高实验结果的准确性。
总结:通过对高三化学实验中的数据处理与结果分析方法的总结,我们可以发现,在进行化学实验时,数据处理和结果分析同样重要。
第3章-2 分析化学中的数据处理
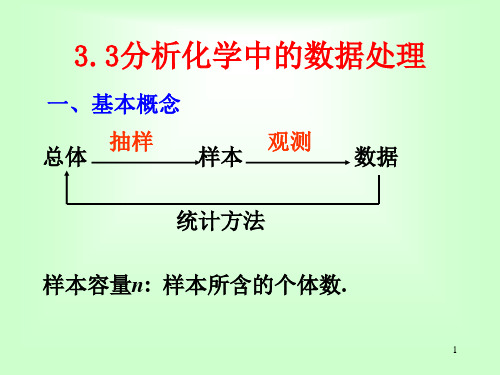
表3.2 正态分布概率积分表
随机误差出现的区间
测量值出现的区间
概率
(以σ为单位) u=±1 u=±1.96 u=±2 u=±2.58 u=±3
x=μ±1σ x=μ±1.96σ x=μ±2σ x=μ±2.58σ x=μ±3σ
68.3% 95.0% 95.5% 99.0% 99.7%
12
例1 已知某试样中质量分数的标准值为1.75%, σ=0.10%,又已知测量时没有系统误差,求分析 结果落在(1.75±0.15)%范围内的概率。 解: x x 1.75% 0.15%
(47.60 0.13)%
(47.60 0.23)%
置信度越高,置信区间就越大,所 估计的区间包括真值的可能性也就 越大,置信度定在 95%或 90%。
23
3.4 显著性检验
1. 平均值与标准值的比较-t检验法
步骤:a.将 x ,μ 和 n代入 t x n ,求t计
x 10.79%, s 0.042%
9 1.43
t
x s
n
10.79% 10.77% 0.042%
查表 ,P=0.95,f=8 时, t0.05 , 8=2.31 。 t<t0.05 , 8 ,故 x 与 μ 之间不存在显著性差异,即采用新方法后,没有 引起明显的系统误差。 25
涉及到的是测量值较少时的平均偏差;但在用统
计学处理数据时,广泛采用标准偏差来衡量数据
的分散程度。
2
总体标准偏差:
(测量次数为无限多次时)
σ
x
n
2
样本标准偏差:
(测量值不多时)
s
x x
n 1
2
高三化学总结化学实验中的数据处理与结果解读方法

高三化学总结化学实验中的数据处理与结果解读方法化学实验是高中化学教学重要的一环,通过实验可以使学生更深入地理解理论知识,并培养实验操作和数据处理能力。
然而,对于高三学生来说,他们需要更加系统地总结和掌握化学实验中的数据处理与结果解读方法,以提高实验的准确性和实验数据的可信度。
本文将从以下几个方面进行总结和讨论。
一、数据处理方法在化学实验中,数据的处理是非常关键的,它直接影响到实验结果的准确性和可靠性。
以下是几种常用的数据处理方法:1. 数据平均法:对于多次重复实验得到的数据,可以通过求平均值来获得更可靠的结果。
这需要计算所有数据的和,并除以实验次数,得到平均值。
例如,对于测量一组重量的实验数据,可以将每次实验得到的数据相加后除以实验次数,得到物质的平均重量。
2. 标准差法:标准差是对数据离散程度的度量,用于评估实验结果的可靠性和数据的精确程度。
计算标准差可以帮助我们判断实验数据是否存在偏差,以及偏差的大小。
在实验数据处理时,可以根据标准差的大小来判断数据的可靠性,并对数据进行修正。
3. 图表分析法:将实验数据以图表的形式呈现可以更直观地观察数据之间的关系和趋势。
常用的图表包括直方图、折线图和散点图等。
通过观察图表,可以发现数据的规律、异常值和趋势,进一步分析实验结果。
二、结果解读方法实验结果的解读是化学实验中非常重要的环节,它涉及到对实验数据和现象的分析和推理。
以下是几种常用的结果解读方法:1. 结果的定性分析:实验结果中有时会出现一些颜色变化、气体生成或析出物等现象,通过观察和对比,可以推测反应是否发生、发生了哪种类型的反应。
例如,实验中加入盐酸产生气泡,则可以推测产生了气体。
2. 结果的定量分析:有些实验需要通过测量现象参数来得出结论,例如实验中测定溶液的酸碱度、测量物质的浓度等。
在这种情况下,需要根据已有的数据和实验方法,计算出相应的结果。
3. 结果的比较和推断:通过对实验结果进行比较和推断,可以得出一些有关物质性质或反应机理的结论。
高三化学总结化学实验中的数据处理与结果分析

高三化学总结化学实验中的数据处理与结果分析在高三化学学习的过程中,我们不仅要理解和掌握化学实验的基础知识和操作技能,还需要学会正确地处理实验数据和分析实验结果。
本文将对化学实验中的数据处理与结果分析进行总结。
一、数据处理1. 实验数据的整理和统计在进行化学实验时,我们通常会产生一系列数据,包括质量、体积、温度、浓度等参数。
为了更好地理解实验过程和结果,我们需要对这些数据进行整理和统计。
可以将数据按照一定的规律进行排列,并计算出平均值、标准偏差等统计量,以准确反映实验数据的特征。
2. 实验数据的单位换算和精确度处理在进行数据处理时,我们还需要进行单位换算和精确度处理。
根据实验的需要,我们可能需要将数据从一种单位转换为另一种单位,确保数据的一致性和可比性。
同时,为了保证分析结果的准确性,我们还要注意数据的精确度,遵循有效数字的规则进行四舍五入和修约。
3. 实验数据的图表展示为了更直观地展示实验数据和结果,我们可以将其以图表的形式呈现。
常用的图表类型包括折线图、柱状图、散点图等。
通过图表的分析和比较,可以更清晰地揭示数据间的关系和趋势,进一步帮助我们理解实验结果的内涵。
二、结果分析1. 数据与理论的对比在分析实验结果时,我们需要将实验数据与相应的理论知识进行对比。
通过比较实验数据与理论值的差异,我们可以评估实验的准确性和可靠性,检验理论模型的适用性。
如果实验结果与理论预期相符,说明实验操作正确且理论推导合理;如果存在较大的偏差,则需要分析偏差的原因,可能是实验操作失误或者理论假设的局限性。
2. 结果的解释与探究实验结果的分析不仅要对数据进行简单的描述和比较,还应该深入解读和探究实验现象背后的原理和机制。
我们可以通过反应速率、物质转化率、能量变化等方面的分析,揭示物质的结构特点和性质变化规律,进一步提升对化学实验的理解和把握。
3. 结果的意义和应用最后,我们还应该思考实验结果的意义和应用。
化学实验不仅是为了获取实验数据和结果,更是为了揭示化学规律和解决实际问题。
分析化学实验数据处理与结果解析要点

分析化学实验数据处理与结果解析要点在分析化学实验中,数据处理和结果解析是非常重要的步骤。
通过准确处理实验数据并解析结果,我们能够得出有关样品性质和组成的重要信息。
下面将介绍分析化学实验数据处理和结果解析的要点。
一、数据处理要点1.数据收集与整理在进行分析化学实验时,首先需要收集实验所需的数据。
在收集数据时,确保数据的准确性和完整性,避免出现误差。
同时,要将数据按照一定的规则进行整理,方便后续的数据处理和结果解析。
2.数据的平均值与标准偏差在处理数据时,常常需要计算数据的平均值和标准偏差。
平均值反映了数据的集中趋势,而标准偏差则表示了数据的离散程度。
通过计算平均值和标准偏差,我们能够对实验数据进行更加准确的分析和判断。
3.误差分析误差是不可避免的,在进行数据处理时需要对误差进行合理的分析。
常见的误差包括系统误差和随机误差。
通过分析误差,我们可以评估实验数据的可靠性,并进行相应的修正和调整。
二、结果解析要点1.结果的可靠性评价在进行结果解析时,首先需要评价结果的可靠性。
可靠性的评价可以通过误差分析、实验重复性等方法进行判断。
只有在结果被认为是可靠的情况下,才能进行进一步的解析和推断。
2.结果与理论比较将实验结果与理论的预期进行比较,可以帮助我们对实验进行解释和理解。
如果实验结果与理论预期相符,那么可以认为实验结果是可靠的,并从中得出结论。
如果实验结果与理论预期存在较大差异,需要进一步分析可能的原因,并进行进一步的实验或修正。
3.结果的图表展示图表是整理和展示实验结果的重要工具。
通过绘制图表,可以更直观地观察和比较实验结果。
在制作图表时,要注明坐标轴、数据单位等重要信息,并保证图表的清晰、准确和美观。
4.结果的讨论和推断在解析实验结果时,要进行充分的讨论和推断。
分析实验结果所得到的性质和组成信息,并与已有的知识进行结合,从而得出合理的推断和结论。
在讨论和推断过程中,要注意逻辑严密、合理性和可重复性。
综上所述,分析化学实验数据处理与结果解析是十分重要的环节。
化学实验数据处理与结果分析方法总结

化学实验数据处理与结果分析方法总结在化学实验中,数据处理和结果分析是非常重要的环节,能够帮助我们理解实验结果并得出科学结论。
本文将总结一些常用的化学实验数据处理方法和结果分析方法,以帮助读者更好地理解和应用这些技巧。
一、数据处理方法1. 数据整理与筛选:在进行数据处理之前,需要对实验数据进行整理和筛选,排除异常数据和不符合实验要求的数据。
可以使用软件或者手工方法进行数据整理和筛选,确保所使用的数据是准确和可靠的。
2. 均值和标准差的计算:均值是指一组数据的平均值,可以通过将所有数据相加再除以数据的数量来计算。
标准差是用来度量数据分布的离散程度,可以帮助判断数据是否集中在均值附近。
计算均值和标准差有助于对实验结果的整体趋势进行分析。
3. 相关性分析:当进行多组实验或者多个变量的测量时,可以使用相关性分析来判断变量之间的关系。
相关性分析可以通过计算相关系数来完成,常用的相关系数有皮尔逊相关系数和斯皮尔曼等级相关系数。
4. 曲线拟合与回归分析:当实验数据呈现出一定的规律或者趋势时,可以使用曲线拟合和回归分析来建立数学模型,并预测实验结果。
曲线拟合可以通过拟合曲线上的点来找到最佳拟合线,而回归分析可以通过建立回归方程来描述变量之间的关系。
二、结果分析方法1. 数据图表:将实验数据转化为图表是直观和清晰地展示数据的一种方式。
常用的数据图表包括折线图、柱状图、散点图等,可以根据实验数据的特点选择合适的图表类型。
图表的标题、坐标轴标签、图例等元素应该清晰明确,方便读者理解和分析。
2. 比较分析:通过比较不同实验组的数据,可以发现实验之间的差异和规律。
在比较分析中,需要注意选择合适的统计方法,如方差分析(ANOVA)和学生 t 检验等,来检验实验之间的差异是否显著。
3. 趋势分析:在研究一系列时间点或者浓度变化的实验情况时,可以通过趋势分析来揭示实验数据的变化规律。
通过绘制曲线图或者计算斜率,可以判断实验数据的趋势是递增、递减还是保持稳定。
分析化学--分析结果的数据处理

§2-2 分析结果的数据处理一、可疑测定值的取舍1、可疑值:在平行测定的数据中,有时会出现一二个与其它结果相差较大的测定值,称为可疑值或异常值(离群值、极端值)2、方法㈠、Q 检验法:由迪安(Dean )和狄克逊(Dixon )在1951年提出。
步骤:1、将测定值由小至大按顺序排列:x 1,x 2,x 3,…x n-1,x n ,其中可疑值为x 1或x n 。
2、求出可疑值与其最邻近值之差x 2-x 1或x n -x n-1。
3、用上述数值除以极差,计算出QQ=11χχχχ---n n n 或Q=112χχχχ--n4、根据测定次数n 和所要求的置信度P 查Q p ,n 值。
(分析化学中通常取0.90的置信度)5、比较Q 和Q p ,n 的大小:若Q >Q p ,n ,则舍弃可疑值;若Q <Q p ,n ,则保留可疑值。
例:4次测定铁矿石中铁的质量分数(%)得40.02, 40.16,40.18和40.20。
㈡、格鲁布斯法:步骤:1、将测定值由小至大按顺序排列:x 1,x 2,x 3,…x n-1,x n ,其中可疑值为x 1或x n 。
2、计算出该组数据的平均值x 和标准偏差s 。
3、计算统计量G :若x 1为可疑值,则G==s1χχ-若x n 为可疑值,则G==s n χχ-4、根据置信度P 和测定次数n 查表得G p ,n ,比较二者大小若G >G p ,n ,说明可疑值相对平均值偏离较大,则舍去;若G <G p ,n ,则保留。
注意:置信度通常取0.90或0.95。
例1:分析石灰石铁含量4次,测定结果为:1.61%, 1.53%,1.54%和1.83%。
问上述各值中是否有应该舍弃的可疑值。
(用格鲁布斯检验法检验 P=0.95)例 2 测定碱灰中总碱量(以w Na 2O 表示),5次测定结果分别为:40.10%,40.11%,40.12%,40.12%和40.20% (1)用格鲁布斯法检验40.20%是否应该舍去;(2)报告经统计处理后的分析结果;(3)用m 的置信区间表示分析结果(P=0.95)二、显著性检验用统计的方法检验测定值之间是否存在显著性差异,以此推测它们之间是否存在系统误差,从而判断测定结果或分析方法的可靠性,这一过程称为显著性检验。
分析化学--分析结果的数据处理

1§2-2分析结果的数据处理一、可疑测定值的取舍1、 可疑值:在平行测定的数据中,有时会出现一二个与其它结果相差较大的测 定值,称为可疑值或异常值(离群值、极端值)2、 方法㈠、Q 检验法:由迪安(Dean )和狄克逊(Dixon )在1951年提出。
步骤:1、 将测定值由小至大按顺序排列:X i , X 2, X 3,…X n-1 , X n ,其中可疑值为X i 或X n o2、 求出可疑值与其最邻近值之差 X 2-X 1或X n -X n-1。
3、 用上述数值除以极差,计算出 Q4、 根据测定次数n 和所要求的置信度P 查Q, n 值。
(分析化学中通常取的置信度)5、 比较Q 和Q , n 的大小:若Q>Q ,n ,则舍弃可疑值;若Q< Q ,n ,贝M 呆留可疑值。
例:4次测定铁矿石中铁的质量分数(%得,,和。
㈡、格鲁布斯法:步骤:1、将测定值由小至大按顺序排列:X 1, X 2, X 3,…X n-1 , X n ,其中可疑值为X 1或X n 。
2、计算出该组数据的平均值X 和标准偏差s3、计算统计量 G:若X 1为可疑值,则G== s Q=n 1 或 Q= n 1若X n为可疑值,则G = = S4、根据置信度P和测定次数n查表得G, n,比较二者大小若G> G,n,说明可疑值相对平均值偏离较大,则舍去;若G< G, n,则保留。
注意:置信度通常取或。
例1:分析石灰石铁含量4次,测定结果为:%, %,%和%问上述各值中是否有应该舍弃的可疑值。
(用格鲁布斯检验法检验P=)例2测定碱灰中总碱量(以wNa t0表示),5次测定结果分别为:%,%,%,彌%(1)用格鲁布斯法检验%是否应该舍去;(2)报告经统计处理后的分析结果;(3)用m 的置信区间表示分析结果(P=二、显著性检验用统计的方法检验测定值之间是否存在显著性差异,以此推测它们之间是否存在系统误差,从而判断测定结果或分析方法的可靠性,这一过程称为显著性检验。
分析化学数据处理及结果计算

分析化学数据处理及结果计算分析化学数据处理及结果计算是实验数据处理过程中的重要一环,它涉及到数据的整理、计算、分析和解释,为科学研究和实验结果的合理评价提供依据。
本文将从数据整理、结果计算和分析三个方面对分析化学数据处理进行探讨。
1.数据整理数据整理是数据处理的第一步,其目的是将实验数据进行标准化和合理化处理。
在数据整理过程中,需要对原始数据进行筛选、排除异常值、填充缺失值等操作,以确保数据的准确性和可靠性。
常用的数据整理方法包括数据的去除、插补、平滑和标准化等。
数据的去除是指将实验中的异常数据和无效数据进行排除。
异常数据可能是由于仪器故障、实验操作失误等原因导致的,对实验结果的误差较大,因此需要将其从数据集中删除。
无效数据是指在实验过程中没有得到有效结果的数据,例如测量结果为0、样品溶解度过低等情况,也需要进行筛选和删除。
数据的插补是指对实验数据中出现的缺失值进行填充,以保证数据的完整性和一致性。
常用的插补方法包括线性插补、均值插补、回归插补等。
在选择插补方法时,需要考虑插补结果的准确性和合理性。
数据的平滑是指对实验数据中的噪声进行滤波处理,以减少噪声对结果的影响。
平滑方法有移动平均法、傅里叶变换法等,选择适当的平滑方法可以使数据更加平稳和可靠。
数据的标准化是指将不同维度和量纲的数据统一转化为相同的数值范围。
常用的标准化方法包括最大最小值标准化、z-score标准化等,标准化后的数据可以更好地进行比较和分析。
2.结果计算结果计算是分析化学数据处理的核心环节,根据实验数据进行计算和推导,得出实验结果和结论。
在结果计算过程中,需要根据实验目的和实验方法选择适当的计算方法,并正确运用数理统计和数值计算方法。
常用的结果计算方法包括均值计算、标准差计算、回归分析、相关分析等。
均值计算是指对数据样本进行求平均值,标准差计算是用来反映数据的离散程度和相对误差。
回归分析是用来建立预测模型和拟合实验数据,通过回归方程的参数来描述变量之间的关系。
高三化学总结化学实验数据处理与结果分析

高三化学总结化学实验数据处理与结果分析化学实验是学习化学知识中至关重要的一部分,通过实验数据的处理和结果的分析,我们可以深入了解实际化学现象和反应规律。
本文将就高三化学实验数据处理与结果分析进行总结和归纳。
一、实验数据处理1. 实验数据的记录与整理在进行化学实验的过程中,准确地记录实验数据是十分重要的。
应按照实验设备和药品的使用顺序进行记录,确保数据的完整和有序。
同时,还需注意数据的单位和精确度,以及记录时间和环境的相关信息。
2. 数据的处理与分析实验数据处理是对实验结果的定量分析和计算。
根据实验的目的和需要,我们可以采用各种数学、统计和图表方法来处理数据,例如平均值、标准差、误差计算、相关性分析等。
3. 实验误差的分析与讨论实验中难免会存在各种误差,如系统误差和偶然误差。
对于数据的误差分析是实验结果有效性的重要保证。
我们可以通过比较不同实验数据之间的差异、定量计算误差范围等方法,来评估实验误差对结果的影响程度。
二、结果分析1. 实验结果的展示方式在化学实验中,我们可以通过表格、图表和图像等方式来展示实验结果。
表格应具有清晰的结构和可读性,图表应具有准确的坐标轴和恰当的图例。
此外,还应标明数据的单位和误差范围,以便读者快速理解实验结果。
2. 结果的定性分析根据实验的目的和数据处理的结果,我们可以对实验结果进行定性分析。
将实验结果与相关的理论知识联系起来,探讨实验现象产生的原因和背后的化学原理,从而深化对化学知识的理解。
3. 结果的定量分析有些实验需要进行定量分析,通过计算和比较实验数据,得出一些数量关系和结论。
例如摩尔计算、配位数计算、电量计算等。
在进行定量分析时,需要考虑到实验条件、实验误差以及数据的可靠性,以准确地得出结论。
4. 结果的讨论与推论在实验结果分析的过程中,我们还需要对结果进行讨论和推论。
通过比较不同实验数据之间的差异、探究数据背后的规律,进一步探索化学知识的内在联系和应用价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6
2、质量
• 习惯上称为重量,用符号m表示,单位为kg,
在分析化学上常用g、mg和μg表示。
• 换算关系: • 1kg=1000g 1g=1000mg 1mg=1000μg
2020/11/13
Analytical Chemistry
7
3、体积
• 体积或容积用符号V表示,SI单位为立方米(m3),
o 分析化学中常用单位为升/摩尔(L/mol)
o Vm=V/nB
2020/11/13
Analytical Chemistry
11
6、密度
• 符号ρ,单位千克/米3(kg/m3) • 常用单位为克/厘米3(g/cm3)或克/毫升(g/mL)。 • 体积受温度影响,密度必须注明有关温度。
2020/11/13
2020/11/13
Analytical Chemistry
2
第一节 分析化学法定计量单位及计算基础
• 一、法定计量单位 • 法定计量单位:由国家以法令形式规定使用或
允许使用的计量单位。
• 我国的法定计量单位:以国际单位制单位为基
础,结合我国的实际情况制定。
• 国际单位制SI—International System of Units
2020/11/13
Analytical Chemistry
3
1971年第14届国际法定计量大会规定SI基本单位
量的名称 单位名称 符号 量的名称 单位名称 符号
长度
米
m 热力学温度 开[尔文] K
质量 千克(公斤) kg 物质的量 摩[尔] mol
时间
秒
s
光强度 坎[德拉] cd
电流
安[培]
A
2020/11/13
18
4、体积分数
o B的体积分数 = 混合前B的体积/混合物的体积
o φB表示,量纲为1。
o φ (C H OH)= 0.70 或φ (C H OH) = 70 %
Analytical Chemistry
4
二、分析化学中常用法定计量单位
o 1、物质的量
o 物质的—表示物质的基本单元多少
o 符号为nB,单位名称为摩尔,单位符号为mol, 中文符号为摩。
o 1mol—系统中物质单元B的数目与0.012kg碳12的原子数目相等。
o 注意:基本单元应予指明。例如原子、分子、 离子、电子及其他粒子等。
o 在分析化学中摩尔质量单位常用g/mol表示。
2020/11/13
Analytical Chemistry
9
常用物质的摩尔质量
名称 盐酸 硫酸 氢氧化钠 氨水 碳酸钠 氯化钠 高锰酸钾
化学式 HCl H2SO4 NaOH
NH3·H2O Na2CO3
NaCl KMnO4
式量 36.46 98.08 40.00 35.05 105.99 58.45 158.04
17
3、质量浓度
• B的质量浓度 = B的质量/混合物的体积
• ρB表示,单位为g/L或mg/L、μg/L、ng/L。
• ρB= mB/V
• 式中: • ρB—物质B的质量浓度,g/L; • mB—物质B的质量,g;
• V—混合物(溶液)的体积,L
2020/11/13
Analytical Chemistry
13
8、物质的相对分子质量
• 物质的相对分子质量—物质的分子或特定单元 平均质量与12C原子质量的1/12之比。
• 物质的相对分子质量用符号Mr表示,量纲为1, 以前称为分子量。
• 例如FeO的相对分子质量为71.84
2020/11/13
Analytical Chemistry
14
三、溶液浓度表示方法
基本单元 HCl
1/2H2SO4 NaOH
NH3·H2O 1/2Na2CO3
NaCl 1/5KMnO4
2020/11/13
Analytical Chemistry
MB 36.46 49.04 40.00 35.05 53.00 58.45 31.61
10
5、摩尔体积
o 摩尔体积=体积/物质的量
o 摩尔体积的符号为Vm,国际单位为立方米/摩 尔(m3/mol)
在分析化学上常用L、mL 和μL表示。
• 换算关系: • 1 m3 =1000L 1L=1000mL 1mg=1000μL
2020/11/13
Analytical Chemistry
8
4、摩尔质量
o 摩尔质量=质量/物质的量
o 摩尔质量的符号MB,单位为千克/摩尔 (kg/mol)
o MB=m/nB
• 物质的量浓度 • 质量分数 • 质量浓度 • 体积分数 • 比例浓度 • 滴定度
2020/11/13
Analytical Chemistry
15
1、物质的量浓度
o 物质的量浓度 = 物质的量/混合物的体积
o cB=nB/V
o 式中: o cB—物质B的物质的量浓度,mol/L; o nB—物质B的物质的量,mol; o V—混合物(溶液)的体积,L o B—基本单元
2020/11/13
Analytical Chemistry
5
例题
• 以H2SO4为基本单元,98.08g的H2SO4 • 以1/2 H2SO4为基本单元,98.08g的H2SO4 • 1mol H • 1mol H2 • 1mol(1/2Na2CO3 )
2020/11/13
Analytical Chemistry
Analytical Chemistry
12
7、元素的相对原子质量
• 元素的相对原子质量—元素的平均原子质量与 12C原子质量的1/12之比。
• 元素的相对原子质量用符号Ar表示,量纲为1, 以前称为原子量。
• 例如Fe的相对原子质量为55.85。
2020/11/13
Analytical Chemistry
2020/11/13
Analytical Chemistry
16
2、质量分数
• B的质量分数 = B的质量/混合物的质量 • ωB表示,量纲为1。 • ω(HCl)=0.38 或ω(HCl)=38 % • 质量分数表示mg/g、μg/g、ng/g
2020/11/13
Analytical Chemistry
化验分析数据处理及 结果计算
2020/11/13
Analytical Chemistry
1
教学指导:
• 分析化学常用法定计量单位及计算基础 • 化学分析中常用的溶液浓度及其滴定度的表示
方法
• 滴定分析法计算 • 分析结果的判断及分析数据的取舍方法(4d法、
Q检验法、Grubbs法)
• 平均值精密度的表示方法及平均值的置信区间
