完全互溶双液系的气-液平衡相图
二组分完全互溶双液系气-液平衡相图

课程名称:大学化学实验(P)指导老师:成绩:_______________实验名称:二组分完全互溶双液系气-液平衡相图实验类型:物性测试同组学生姓名:【实验目的】1.学习测定气-液平衡数据及绘制二组分系统相图的方法,加深理解相律和相图等概念。
2.掌握正确测量纯液体和液体混合物沸点的方法。
3.熟悉阿贝折光仪的原理及操作,熟练掌握超级恒温超的使用和液体折射率的测定。
4.了解运用物理化学性质确定混合物组成的方法。
【实验原理】两种液态物质若能以任意比例混合,则称为二组分完全互溶液态混合物系统。
当纯液体或液态混合物的蒸气压与外压相等时就会沸腾,此时的温度就是沸点。
在一定外压下,纯液体的沸点有确定值,通常说的液体沸点指101.3kPa下的沸点。
对于完全互溶的混合物系统,沸点不仅与外压有关,还与系统的组成有关。
在一定压力下,二组分完全互溶液态混合物系统的沸点与组成的关系可分为三类:(1)液态混合物的沸点介于两纯组分的沸点之间,如苯-甲苯系统;(2)液态混合物有沸点极大值,如丙酮-氯仿系统;(3)液态混合物有沸点极小值,如水-乙醇系统、苯-乙醇系统。
对于第(1)类,在系统处于沸点时,气液两相的组成不相同,可以通过精馏使系统的两个组分完全分离。
第(2)、(3)类是由实际系统与拉乌尔定律产生严重偏差导致。
正偏差很大的系统,如第(3)类,在T-x图上呈现极小值,负偏差很大时,如第(2)类,则会出现极大值。
相图中出现极致的那一点,称为恒沸点,恒沸点温度和组成都是非常重要的平衡数据。
具有恒沸点组成的二组分混合物,在蒸馏时的气相组成和液相组成完全一样,整个蒸馏过程中沸点恒定不变,因此称为恒沸混合物,如要获得两纯组分,则需采取其他方法。
液态混合物组成的分析是相平衡实验的关键。
组分分析常采用折射率法、密度法等物理方法和色谱分析法等。
本实验采用折射率法。
在一定温度下的折射率是物质的一个特征参数,液态混合物的折射率与组成有关,一般呈简单的函数关系。
双液系相图实验报告

双液系相图实验报告二组分完全互溶双液系气-液平衡相图实验报课程名称:大学化学实验(P)指导老师:成绩:_______________实验名称:二组分完全互溶双液系气-液平衡相图实验类型:物性测试同组学生姓名:【实验目的】1. 学习测定气-液平衡数据及绘制二组分系统相图的方法,加深理解相律和相图等概念。
2. 掌握正确测量纯液体和液体混合物沸点的方法。
3. 熟悉阿贝折光仪的原理及操作,熟练掌握超级恒温超的使用和液体折射率的测定。
4. 了解运用物理化学性质确定混合物组成的方法。
【实验原理】两种液态物质若能以任意比例混合,则称为二组分完全互溶液态混合物系统。
当纯液体或液态混合物的蒸气压与外压相等时就会沸腾,此时的温度就是沸点。
在一定外压下,纯液体的沸点有确定值,通常说的液体沸点指101.3kPa下的沸点。
对于完全互溶的混合物系统,沸点不仅与外压有关,还与系统的组成有关。
在一定压力下,二组分完全互溶液态混合物系统的沸点与组成的关系可分为三类:(1)液态混合物的沸点介于两纯组分的沸点之间,如苯-甲苯系统;(2)液态混合物有沸点极大值,如丙酮-氯仿系统;(3)液态混合物有沸点极小值,如水-乙醇系统、苯-乙醇系统。
对于第(1)类,在系统处于沸点时,气液两相的组成不相同,可以通过精馏使系统的两个组分完全分离。
第(2)、(3)类是由实际系统与拉乌尔定律产生严重偏差导致。
正偏差很大的系统,如第(3)类,在T-x图上呈现极小值,负偏差很大时,如第(2)类,则会出现极大值。
相图中出现极致的那一点,称为恒沸点,恒沸点温度和组成都是非常重要的平衡数据。
具有恒沸点组成的二组分混合物,在蒸馏时的气相组成和液相组成完全一样,整个蒸馏过程中沸点恒定不变,因此称为恒沸混合物,如要获得两纯组分,则需采取其他方法。
液态混合物组成的分析是相平衡实验的关键。
组分分析常采用折射率法、密度法等物理方法和色谱分析法等。
本实验采用折射率法。
在一定温度下的折射率是物质的一个特征参数,液态混合物的折射率与组成有关,一般呈简单的函数关系。
双液系的气—液平衡相图

实验五双液系的气—液平衡相图一、实验目的1、绘制在标准压力下乙醇-正丙醇体系的沸点组成图,并确定其恒沸点及恒沸组成;2、熟练掌握测定双组分液体沸点的方法及用折光率确定二组分物系组成的方法;3、掌握超级恒温槽、阿贝折射仪、气压计等仪器的使用方法。
二、实验原理1、相图任意两个在常温时为液态的物质混合起来组成的体系称为双液系。
两种溶液若能按任意比例进行溶解,称为完全互溶双液系,如环已烷-乙醇、正丙醇-乙醇体系都是完全互溶体系。
若只能在一定比例范围内溶解,称为部分互溶双液系,例苯-水体系。
在完全互溶双液系中,有一部分能形成理想液态混合物,如苯-甲苯系统,二者的行为均符合拉乌尔定律,但大部分双液系是非理想液态混合物,其行为与拉乌尔定律有偏差。
液体的沸点是指液体的蒸气压与外界压力相等时的温度。
在一定外压下,纯液体的沸点有其确定值,但双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。
双液系两相平衡时的气相组成和液相组成并不相同。
通常用几何作图的方法将双液系的沸点对其气相和液相的组成作图,所得图形叫双液系的沸点T(或t)-组成(x)图,即T(或t)—x图。
它表明了沸点与液相组成和与之平衡的气相组成之间的关系。
在恒定压力下,二组分系统气液达到平衡时,其沸点-组成(t-x)图分三类:(1)混合液的沸点介于A、B二纯组分沸点之间。
这类双液系可用分馏法从溶液中分离出两个纯组分。
如苯-甲苯系统,此时混合物的行为符合拉乌尔定律或对拉乌尔定律的偏差不大。
如图5-1(a)所示。
(2)有最低恒沸点体系,如环已烷-乙醇体系,t—x图上有一个最低点,此点称最低恒沸点,在此点相互平衡的液相和气相具有相同的组成,此时混合物的行为对拉乌尔定律产生最大正偏差,如图5-1(b)所示。
对于这类的双液系,用分馏法不能从溶液中同时分离出两个纯组分。
(3)有最高恒沸点体系,如氯仿-丙酮体系,t—x图上有一个最高点,此点称最高恒沸点,在此点相互平衡的液相和气相具有相同的组成,此时混合物的行为对拉乌尔定律产生最大负偏差,如图5-1(c)所示。
徐州工程学院完全互溶双液系气液平衡相图的绘制

徐州工程学院完全互溶双液系气液平衡相图的绘制绘制完全混溶双液体体系的气液平衡相图1。
实验目的1。
测定常压下环己烷-乙醇双液体系的T-x图,找出恒沸点混合物的组成和最低恒沸点2.掌握阿贝折射仪的使用方法2。
实验原理由两种液体物质组成的双组分系统称为双液体系统。
根据两种组分溶解度的不同,可分为三种情况:完全混溶、部分混溶和完全不混溶当两种挥发性液体混合形成完全可混溶的体系时,如果两种组分的蒸汽压不同,则混合物的组成与平衡时的气相组成不同。
当压力保持恒定时,混合物的沸点与两种组分的相对含量有关。
在恒压下,完全混溶的双液体体系的真实气液平衡相图(t-x)可根据体系与拉乌尔定律的偏差分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图2.7(a)所示(2)最大负偏差:存在一个最小蒸汽压值,该值小于两种纯液体的蒸汽压。
混合物具有最高沸点,如盐酸-水体系,如图2.7(b)所示(3)最大正偏差:存在最大蒸汽压值,该值大于两种纯液体的蒸汽压。
混合物的沸点最低,如图2.7(c)所示t/oct/oct Bt/oct bttatbxb(b)ATA XB(a)bax ‘ bax bx ‘(c)b图2.7双组分真实液体混合物的气液平衡相图(T-x图)后两种情况是具有恒定沸点的双液相图它们在最低或最高恒定沸点下具有相同的气相和液相组成,因此它们不能像第一种类型那样通过重复蒸馏将双液体系统的两种组分彼此分离,并且只能通过蒸馏和其他方法将一种纯物质和另一种恒定沸点混合物分离。
为了确定双液体系统的T-X相图,在气液平衡后,应同时确定双液体系统的沸点以及液相和气相的平衡组成。
本实验采用环己烷-乙醇体系,属于上述第三类。
t-x相图可以通过在沸点仪中蒸馏不同组成的混合物(如图2.8所示)并测量其沸点以及相应的气相和液相组成来绘制。
本实验中两相的成分分析用折射率法测定。
折射率是物质的特征值,与物质的浓度和温度有关,所以测量物质的折射率时需要恒温。
完全互溶双液系气液均衡相图的绘制
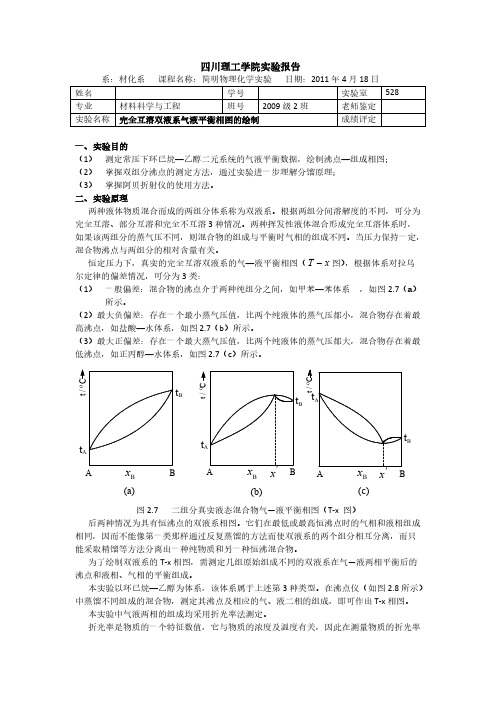
温度稳定后,记下温度计的读数,即为溶液的沸点。
切断电源,停止加热,先用吸管从小槽中取出气相冷凝液,迅速测定各自的折光率。用
烧杯盛水冷却液相,再从侧管处吸出少许液相,迅速测定各自的折光率。剩余溶液倒入回
收瓶。
按 1 号溶液的操作,依次测定 2,3,4,5,6,7,8 号溶液的沸点和气—液平衡时的
气、液相折光率。
图 2.8 构
使传感器(温度计)浸入液体内。冷凝管接通冷凝水。将稳流温度计的读数稳定后再
维持 3~5min,以使体系达到平衡。记下温度计的读数,即为无水乙醇的
沸点,同时记录大气压力。
3. 环乙烷沸点的测定
同第 2 步操作测定环乙烷的沸点。测定前应注意,必须将沸点仪清洗干净并干燥。
四、 实验步骤
1. 环已烷—乙醇溶液折光率与组成工作曲线的测定
调节恒温槽温度并使其稳定,恒温水使阿贝折射仪上的温度稳定在某一
定值,测量系列环已烷—乙醇标准溶液在此温度下的折光率。为了适应季
节的变化,可选择若干温度测量,一般可选 25℃,30℃,35℃三个温度。
2. 无水乙醇沸点的测定
将干燥的沸点仪安装好。从侧管加入约 20mL 无水乙醇于蒸馏瓶内,并
4. 测定系列浓度待测溶液的沸点和折光率
同第 2 步操作,从侧管加入约 20mL 预先配制好的 1 号环乙烷—乙醇溶液于蒸馏瓶内,
并使传感器(温度计)浸入溶液内,将液体加热至缓慢沸腾。因最初在冷凝管下端小槽内
的液体不能代表平衡气相的组成,为加速达到平衡,须连同支架一起倾斜蒸馏瓶,使小槽
中的气相冷凝液倾回蒸馏瓶内,重复 3 次(注意:加热时间不宜太长,以免物质挥发),待
t / oC
x'
B
tB tA
完全互溶双液系的平衡相图

7-目镜;
8-望远镜筒;
9-示值调节螺钉;
10-阿米西棱镜手轮;
11-色散值刻度圈;
12-棱镜锁紧扳手;
13-棱镜组;
14-温度计座;
15-恒温器接头;
16-保护罩;
17-主轴;
18-反光镜
阿贝折射仪是一种精密的
光学仪器,使用时注意以下几点:
☻使用时要注意保护棱镜,清洗时只能用擦镜纸而不 能用滤纸等。加 试样时不能将滴管口触及镜面。对于酸碱等腐蚀性液体不得用阿贝折射 仪。 ☻每次测定时,试样不可加地太多,一般加需加2-3滴即可。
在每一份样品的蒸馏过程中,正常回流1~2min后,即可 取样测定,不宜等待时间过长。
每次取样量不宜过多,取样时毛细滴管一定要干燥,不能 留有上次的残液,并且气相部分的样品要取干净。
使用阿贝折光仪时,棱镜上不能触及硬物(如滴管)。
六 数据处理
1. 将测得的折射率-组成数据列表,并绘 制成工作曲线。
恒温槽1台;阿贝折射仪1台;沸点仪1 套; 移液管(1mL2支、10mL1支);具塞小 试管9支。 环己烷(A.R.);无水乙醇(A.R.)
沸点仪原理图
1-温度计; 2-进样口; 3-加热丝; 4-气相冷凝液取样口 5-气相冷凝液
四 实验步骤
1. 调节恒温槽温度比室温高5℃,通恒温水于阿贝折射仪中。 2. 测定折射率与组成的关系,绘制工作曲线。
大学物化实验报告__双液系的气_双液系的气_液平衡相图
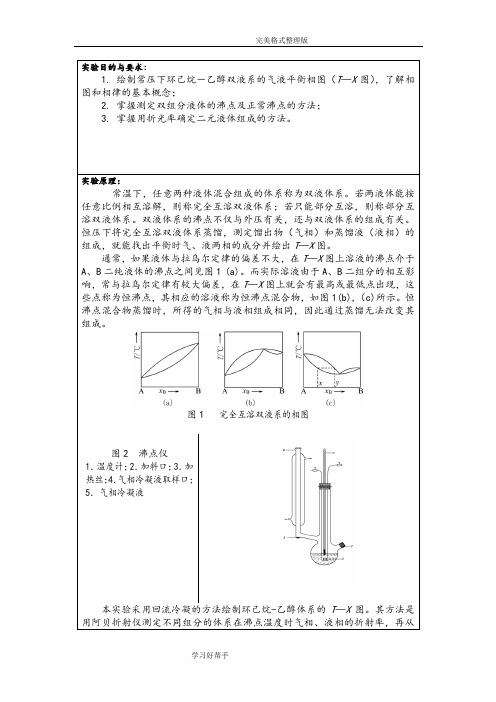
图1 完全互溶双液系的相图
2 沸点仪
温度计;2.加料口;3.加
方程:y=-0.0266x²+0.0893x+1.3599
数据分析:
实验所得图可以看出液相的混合物中随着环己烷含量的升高沸点先逐渐下降到一个恒沸点然后迅逐渐上升,而气相的混合物随着环己烷的升高是迅速到一点然后保持一个稳定的波动,而且液相和气相的交点是恒沸点,混合物组分的改变导致沸点的改变。
注:1、报告内的项目或内容设置,可根据实际情况加以调整和补充。
2、教师批改学生实验报告时间应在学生提交实验报告时间后10日内。
实验七双液系气液平衡相图的测定

数据处理
1. 将实验中测得的折射率—组成数据列表,并绘制成 工作曲线。
2. 将实验中测得的沸点—折射率数据列表,并从工作 曲线上查得相应的组成,从而获得沸点与组成的关 系。
3. 绘制沸点—组成图,并标明最低恒沸点和组成。 4. 在精确的测定中,还要对温度计的外露水银柱进行
仪器操作
使用方法
3. 调光: 转动镜筒使之垂直,调节反射镜使入射光进入棱镜,
同时调节目镜的焦距,使目镜中十字线清晰明亮。调节消 色散补偿器使目镜中彩色光带消失。再调节读数螺旋,使 明暗的界面恰好同十字线交叉点处重合。这时镜筒的轴与 掠射光线平行。 4. 读数:
从读数望远镜中读出刻度盘上的折射率数值。常用的 阿贝折射仪可读至小数点后的第四位,为了使读数准确, 一般应将试样重复测量三次,每次相差不能超过0.0002, 然后取平均值。
仪器操作
注意事项
1.使用时要注意保护棱镜,清洗时只能用擦镜纸而不能用滤纸 等。加试样时不能将滴管口触及镜面。对于酸碱等腐蚀性液 体不得使用阿贝折射仪。
2.每次测定时,试样不可加得太多,一般只需加2~3滴即可。 3.要注意保持仪器清洁,保护刻度盘。每次实验完毕,要在镜
面上加几滴丙酮,并用擦镜纸擦干。最后用两层擦镜纸夹在 两棱镜镜面之间,以免镜面损坏。 4.读数时,有时在目镜中观察不到清晰的明暗分界线,而是畸 形的,这是由于棱镜间未充满液体;若出现弧形光环,则可 能是由于光线未经过棱镜而直接照射到聚光透镜上。
0.200mL、…、0.900mL的环己烷,再依次移入 0.900mL、0.800mL、…、0.100mL的异丙醇,轻 轻摇动,混合均匀,配成9份已知浓度的溶液(按 纯样品的密度,换算成质量百分浓度)。用阿贝 折射仪测定每份溶液的折射率及纯环己烷和异丙 醇的折射率。以折射率对浓度作图,即可绘制工 作曲线。
完全互溶双液系统气 液均衡相图的绘制2 误差分析

对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料电试力卷保相护互装作置用调与试相技互术关,通系电1,力过根保管据护线生高0不产中仅工资2艺料22高试2可中卷以资配解料置决试技吊卷术顶要是层求指配,机置对组不电在规气进范设行高备继中进电资行保料空护试载高卷与中问带资题负料2荷试2,下卷而高总且中体可资配保料置障试时2卷,32调需3各控要类试在管验最路;大习对限题设度到备内位进来。行确在调保管整机路使组敷其高设在中过正资程常料1工试中况卷,下安要与全加过,强度并看工且25作尽52下可22都能护可地1关以缩于正小管常故路工障高作高中;中资对资料于料试继试卷电卷连保破接护坏管进范口行围处整,理核或高对者中定对资值某料,些试审异卷核常弯与高扁校中度对资固图料定纸试盒,卷位编工置写况.复进保杂行护设自层备动防与处腐装理跨置,接高尤地中其线资要弯料避曲试免半卷错径调误标试高方中等案资,,料要编试求5写、卷技重电保术要气护交设设装底备备置。4高调、动管中试电作线资高气,敷料中课并设3试资件且、技卷料中拒管术试试调绝路中验卷试动敷包方技作设含案术,技线以来术槽及避、系免管统不架启必等动要多方高项案中方;资式对料,整试为套卷解启突决动然高过停中程机语中。文高因电中此气资,课料电件试力中卷高管电中壁气资薄设料、备试接进卷口行保不调护严试装等工置问作调题并试,且技合进术理行,利过要用关求管运电线行力敷高保设中护技资装术料置。试做线卷到缆技准敷术确设指灵原导活则。。:对对在于于分调差线试动盒过保处程护,中装当高置不中高同资中电料资压试料回卷试路技卷交术调叉问试时题技,,术应作是采为指用调发金试电属人机隔员一板,变进需压行要器隔在组开事在处前发理掌生;握内同图部一纸故线资障槽料时内、,设需强备要电制进回造行路厂外须家部同出电时具源切高高断中中习资资题料料电试试源卷卷,试切线验除缆报从敷告而设与采完相用毕关高,技中要术资进资料行料试检,卷查并主和且要检了保测解护处现装理场置。设。备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。
双液系的气-液平衡相图

双液系的⽓-液平衡相图双液系的⽓-液平衡相图⼀、实验⽬的1. 掌握采⽤阿贝折光率仪确定⼆元液体组成的⽅法;2. 掌握测定双组份液体的沸点及正常沸点的⽅法;3. 绘制在恒压下环⼰烷-⼄醇双液系的⽓-液平衡相图。
⼆、实验原理两种液态的物质混合⽽成的⼆组分体系称为双液系。
它可以分为完全互溶和部分互溶的双液系。
体系的沸点不仅与外压有关,⽽且与双液系的组成有关。
在恒压下做温度T对组成x的关系图即为T-x图。
由相律可知,对于双液系在恒压下⽓-液两相共存区域中,⾃由度为1。
当温度⼀定时,⽓-液两相的相对组成也就有了确定值。
根据杠杆原理,两相的相对量也确定了。
因此实验测定⼀系列不同组成的双液系溶液的⽓-液相平衡时的沸点及此时⽓相和液相的组成,即可得T-x图。
因此双液系⽓-液平衡相图实验主体上包括⼀系列混合体系的沸点测定和⽓-液相组成分析两个主要内容。
体系的沸点可⽤沸点仪测定的,其构造如图7.2所⽰。
采⽤电热丝直接加热溶液,以防⽌过热现象,同时该沸点仪⽤平衡蒸馏法分离⽓液两相,具有可便于取样分析及避免分馏等优点。
体系的⽓液相组成的分析是相图绘制的另⼀核⼼,可以根据待测体系的理化性质寻找多种合适的分析⽅法。
以完全互溶双液系环⼰烷-⼄醇体系为例。
由于环⼰烷和⼄醇两者的折光率相差较⼤,因此本实验可采⽤测定溶液折光率⽅法来确定两组分的组成,⽤阿贝折光仪测定两组分组成的折光率,可以测出折光率对组成的⼯作曲线,根据测得液体样品的折光率,从⼯作曲线上可查得两相的组成。
三、仪器与药品FDY双液系沸点测定仪,阿贝折光仪,超级恒温槽,长滴管,烧杯(50 ml,250 ml),具塞锥形瓶(10ml),刻度移液管(5ml)丙酮(AR级);环⼰烷(AR级);⼄醇(AR级)图7-1 FDY双液系沸点测定仪前⾯板⽰意图图7-1是沸点仪加热控制器的前⾯板⽰意图,各功能键的说明如下:1、电源开关2、加热电源调节——调节所需的加热电源。
3、温度显⽰窗⼝——显⽰所测温度值。
完全互溶双液系统气-液平衡相图的绘制(2) 误差分析

大学化学实验Ⅱ实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业:环境科学091姓名:岳凡耀学号:0908100121指导教师:谭蕾实验成绩:实验编号:十四实验项目名称:完全互溶双液系统气-液平衡相图的绘制报告人:岳凡耀同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:2011年4月 28日一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X B图或沸点-组成图。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(а)所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1(b)所示。
(3)最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1(c)所示。
图1 完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
压力不同,同一双液系统的相图不同,恒沸点及恒沸组成也不同。
本实验采用回流冷凝的方法绘制乙醇-环己醇体系的T-X B图。
完全互溶双液系气液平衡相图的绘制

完全互溶双液系气液平衡相图的绘制一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3.掌握阿贝折射仪的使用方法及原理。
4.了解和掌握沸点仪的测定原理及方法。
5.加深对完全互溶双液系气液平衡相图的理解和增强个人动手能力。
二.实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-x图),根据体系对拉乌尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。
(2)最大负偏差:存在一个最小蒸气压值,比两个纯液体的蒸气压都小,混合物存在着最高沸点,如盐酸-水体系,如图1 (b)所示。
(3)最大正偏差:存在一个最大蒸气压值,比两个纯液体的蒸气压都大,混合物存在图1 二组分真实液态混合物气-液平衡相图(T-x图)着最低沸点,如正丙醇—水体系,如图1(c))所示。
对于后两种情况,为具有恒沸点的双液系相图。
它们在最低或最高恒沸点时的气相和液相组成相同,因而不能象第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。
为了绘制双液系的T -x 相图,需测定几组原始组成不同的双液系在气-液两相平衡后的沸点和液相、气相的平衡组成。
本实验以环己烷-乙醇为体系,该体系属于上述第三种类型。
在沸点仪(如图2所示)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T -x 相图。
本实验中气液两相的组成均采用折光率法测定。
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。
双液系的气-液平衡相图ppt课件

三.仪器与试剂 [注意按实际使用的记录]
四.试验步骤
1.工作曲线绘制
(1)调节超级恒温水浴温度在室温5℃以上,以适应季 节的变化,但所选温度应易于获得试样的密度数据。 环己烷和乙醇分别恒温10min,根据配制混合物所需 的体积,用移液管精确量取,配制环己烷摩尔分数为 0.10,0.20,0.30,0.40,0.50,0.60,0.70, 0.80,0.90 的环己烷-乙醇溶液各10ml。为避免样 品的挥发带来的误差,配制应尽可能迅速。 (2)用尽可能短的软管将阿贝折光仪连接在前述调好 的恒温水浴上,以保持折光仪棱镜处于恒定温度。测 量上述9个溶液以及无水乙醇和纯环己烷的折光率。
按上述相同的步骤,用第二套沸点仪测定环己 烷摩尔分数为0.90 的环己烷-乙醇溶液的沸 点以及气相和液相的折射率测定。
6.系列环己烷-乙醇溶液以及环己烷的测定 按上述第5步所述步骤,分别用第一套沸点仪从
低组成向高组成逐一测定各溶液的沸点、大气压 及两相样品的折光率,而用第二套沸点仪从高组成 向低组成逐一测定各溶液的沸点、大气压及两相 样品的折光率。直至完成所有溶液的测定。 系列溶液可回收供其它同学使用;每个试样测定 后,将沸点仪尽量倒干净即可,不必干燥。记录温度 数据时千万不要忘记注明所用温度计的编号或代 码!
2.精密数字温度温差仪温度的校正
将两套精密数字温度温差仪的探头同时放入 恒温水浴中,测定温度的差值,以其中一套的 读数为基准,对另一套精密数字温度温差仪读 数进行校正。并作燥的沸点仪安装好。检查 带有温度计的软木塞是否塞紧,电热丝要靠 近烧瓶底部的中心。温度计探头的位置应 处在支管之下,但至少要高于电热丝1 cm。 温度计套管中应加入适量的硅油或液体石 蜡,以完全浸没测温探头敏感部分(约2.5~ 3cm),便于传热。
物化实验报告 双液系的气液平衡相图

USTC 3 系 摘要:水和正丙醇的完全互溶溶液,当组成不同时其沸点和气相、液相的成分也不同。本实 验通过测量不同组成下的水和正丙醇的溶液在沸点时气相和液相的折射率, 由正丙醇-水溶 液折光率与组成工作曲线可查出对应折射率的组分。 由于温度测量存在误差, 实验中对测量 温度计进行露茎校正和压力校正。由实验结果便可作出水-正丙醇的气液平衡相图。 关键词 :沸点 折射率 温度校正 气液平衡相图。
沸点仪的设计虽各有异,但其设计思想都集中在 如何正确地测定沸点和气液相的组成,以及防止过热 和避免分馏等方面。我们所使用的沸点仪如图 5-4 所 示: 这是一只带有回流冷凝管的长颈圆底烧瓶,冷凝 管底部有一球形小室 D,用以收集冷凝下来的汽相样 品。液相样品则通过烧瓶上的支管 L 抽取,图中 E 是 一根用 300W 的电炉丝截制而成的电加热丝,直接浸 入溶液中加热,以减少溶液沸腾时的过热暴沸现象。 温度计安装时须注意使水银球一半浸在液面下,一半 露在蒸气中,并在水银球外围套一小玻璃管 C,这样, 溶液沸腾时,在气泡的带动下,使气液不断喷向水银 球而自玻璃管上端溢出;小玻璃管 C 还可减少沸点周 围环境(如空气流动或其它热源的辐射)对温度计读 数可能引起的波动,因此这样测得的温度就能较好地 代表气液两相的平衡温度。 分析平衡时气相和液相的组成,须正确取得气相 和液相样品。沸点仪中蒸气的分馏作用会影响气相的 图 5-4 沸点仪 平衡组成,使取得的气相样品的组成与气液平衡时的 A-盛液容器; B-测量温度计; 组成产生偏差,因此要减少气相的分馏作用。本实验 C-小玻管; D-小球; E-电热丝 中所用沸点仪是将平衡时的蒸气凝聚在小球 D 内,在 F-冷凝管; G-温度计; L-支管 容器 A 中的溶液不会溅入小球 D 的前提下,尽量缩短 小球 D 与大球 A 的距离,为防止分馏,尽量减少小球 D 的体积即可达此目的。为了加速达 到体系的平衡,可把 D 球中最初冷凝的液体倾回到容器 A 中。 沸点的测定 用玻璃水银温度计测量溶液的沸点,如图 5-5,固定在沸点仪上的水银温度计是全浸式 的,使用时除了要对温度计的零点和刻度误差等因素进行校正外,还应作露茎校正。这是由 于温度计未能完全置于被测体系中而引起的。 根据玻璃与水银膨胀系数的差异, 校正值的计 算式为: t 露/℃=1.610-4·n·(t 观-t 环) 校正的方法是在测量沸点的温度计 B 旁再固定一支同样精度的温度计 G, G 的水银球底 部应置于测量温度计沸点稳定值至固定温度计橡皮塞露出那一段水银柱的中部。 读沸点时同 时读取温度计 G 上的读数,得到温度 t 观和 t 环。在测量过程中,由于组成的变动,t 观也在变 动,因此温度计 G 的位置也应随着沸点稳定值而进行调整,始终让其置于温度计 B 露出水 银柱的中部。式中的 n 是露出那段水银柱的长。1.610-4 是水银对玻璃的相对膨胀系数。 沸点除了要进行露茎校正外,还需要进行压力校正。标准大气压下( P=760mmHg 或 101325Pa)测得的沸点为正常沸点。实际测量时,压力一般都不恰好为标准大气压。应用特 鲁顿规则及克劳修斯-克拉贝龙公式,可得溶液沸点随大气压变动而变动的近似值:
完全互溶双液系统气 液平衡相图的绘制2误差分析

大学化学实验□实验报告(物理化学部分)(贵州大学化学与化工学院——大学化学教学与示范中心)班级专业:_________ 环境科学091姓名:__________ 岳凡耀学号:_________ 0908100121指导教师:_____________ 谭蕾实验成绩:_____________________________实验编号:十四实验项目名称:完全互溶双液系统气-液平衡相图的绘制报告人:岳凡耀同组人:赵安娜、赵芳、吴红、陈彦霖、孙腾实验时间:2011年4月28日一、实验目的:1.掌握阿贝折射仪的使用方法通过测定混合物的折射率确定其组成。
2.学习常压下完全互溶双液系统气-液平衡相图的测绘方法,加深对相律、恒沸点的理解。
二、实验原理:相图是描述相平衡系统温度、压力、组成之间关系的图形,可以通过实验测定相平衡系统的组成来绘制。
两种液体物质混合而成的两组分体系称为双液系。
若两液体能以任意比例互溶,称其为完全互溶双液系统;若两液体只能部分互溶,称其为部分互溶双液系统。
当纯液体或液态混合物的蒸气压与外压相等时,液体就会沸腾,此时气-液两相呈平衡,所对应的温度就是沸点。
双液系统的沸点不仅取决于压力,还与液体的组成有关。
表示定压下双液系统气-液两相平衡时温度与组成关系的图称为T-X B图或沸点-组成图。
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T-X),根据体系对乌拉尔定律的偏差情况,可分为三类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1 ( a ) 所示。
(2)最大负偏差:混合物存在着最高沸点,如盐酸-水体系,如图1 ( b)所示。
(3 )最大正偏差:混合物存在着最低沸点,如正丙醇-水体系,如图1 (c)所示。
图1完全互溶双液系统的气-液平衡相图在最高沸点和最低沸点处,气相线与液相线相交,对应于此点组成的溶液,达到气-液两相平衡时,气相与液相组成相同,沸腾的结果只使气相量增加、液相量减少,沸腾过程中温度保持不变,这时的温度叫恒沸点,相应的组成叫恒沸组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验三完全互溶双液系的气-液平衡相图
一、实验目的
1.绘制常压下环己烷-乙醇双液系的T—X图,并找出最低恒沸点和最低恒沸混合物的组成。
2.学会阿贝折射仪的使用。
二、实验原理
在大气压下,完全互溶双液系的沸点-组成相图有理想溶液及无恒沸点、最低恒沸点和最高恒沸点实际溶液四种:
环己烷-乙醇体系沸点—组成图与乙醇-水体系沸点—组成图相似,同属实际溶液中第二类有最低恒沸点的。
其相图可通过阿贝折射仪测定不同组成样品体系在沸点温度时气-液相的折射率、查“折射率—组成工作曲线得相应的组成”来绘制的。
三、仪器药品
1、仪器
阿贝折射仪1台; 沸点仪1套; 恒温槽1台;0.1刻度水银温度计(0-100℃)2支;带磨口塞子的小样品管(2mL)16支;移液管(2mL)2支;胶头滴管2个; 50mL 烧杯10只(公用);50mL量筒10只(公用)。
2、药品
(1)无水乙醇(AR);环己烷(AR); 二次蒸馏水。
(2)在样品瓶中依次加入环己烷10mL、20mL、30mL、40mL、50mL、60mL、70mL、80mL、90mL和乙醇90mL、80mL、70mL、60mL、50mL、40mL、30mL、20mL、20mL已知浓度的标准溶液(按纯样品的密度,换算成物质的量分数)9份。
(3)环己烷物质的量分数约为0.05、0.15、0.30、0.45、0.55、0.65、0.80、0.95的环己烷-乙醇溶液样品。
四、实验步骤
1、测已知浓度的标准的折射率,作环己烷-乙醇的折射率-组成工作曲线
(1)调节超级恒温槽水浴温度,使阿贝折射仪上的温度为250.1
±℃左右。
(2)依次测已知浓度的标准溶液及纯乙醇和环己烷的的折射率(棱镜不能触及硬物如滴管,擦拭棱镜用擦镜纸)。
2、按图安装好沸点仪
-
沸点仪
将一干燥、洁净的磁子放入已洗涤、干燥的沸点仪内,按图安装在实验室特制的磁力加热电热套内(250mL、只可覆盖圆底烧瓶底部1/5);一支温度计离圆底烧瓶约0.5cm,另一支温度计水银球上沿与支管口下沿相齐。
3、测定纯乙醇和环己烷的沸点
(1)在圆底烧瓶中加入约40mL无水乙醇,打开并调节冷凝水和电热套加热开关或旋钮(加热速率控制在“3-5”档),使蒸汽在冷凝管中回流的高度保持在1.5 cm 左右。
待3-5min下、上温度计示数趋于稳定后,测得该溶液沸点。
(2)回收无水乙醇,洗涤并干燥圆底烧瓶后,同法测纯环己烷的沸点。
4、测定环己烷-乙醇系列样品溶液的沸点和相互平衡的气、液相折射率
(1)按浓度由低到高顺序取40mL事先配好的样品溶液加入沸点仪中,打开并调节冷凝水和电热套加热开关或旋钮,使蒸汽在冷凝管中回流的高度保持在1.5 cm左右。
待3-5min,下、上温度计示数趋于稳定后、读取沸点温度,旋上支管活塞、收集约1mL冷凝液,停止加热;取移液管取约1mL的气、液相液体分别储存在带磨口塞子的小样品管中;最后用滴管取尽沸点仪中的测定液,放回原试剂瓶中供下组其他同学使用。
(2)在沸点仪中再加入40mL新待测液,用上述同样方法依次测定(更换溶液时,务必用滴管取尽沸点仪中的测定液,以免带来误差)。
(3)待全部样品溶液沸点及其对应的气、液相样品取完后,集中分别测定其折射率。
五、数据处理
1、以将实验中测得的折射率—组成数据列表,并绘制成工作曲线。
2、将实验中测得的沸点—折射率数据列表,从工作曲线上查得相应的组成,从而获得沸点与组成的关系。
室温______℃;大气压_______Pa;纯乙醇沸点_____℃; 纯环己烷沸点_____℃
液相汽相序号沸点/℃
n D x环己烷n D y环己烷1
2
3
4
5
6
7
8
3、绘制沸点—组成图,并标明最低恒沸点和组成。
【思考问题】
1、在该实验中,测定工作曲线时折射仪的恒温温度与测定样品时折射仪的恒温温度是否需要保持一致?为什么?
2、过热现象对实验产生什么影响?如何在实验中尽可能避免?
3、试估计哪些因素是本实验的误差主要来源?
参考文献
[1 ]丛欢. 介绍改进的恒沸点仪.大学化学,2007,22(2),45-48
[2] 复旦大学.物理化学实验(3th),北京:高等教育出版社,2004,39-45
[3 ]钟爱国. 沸点仪加热装置的改进.大学化学,2003,18(4),54
[4] 刘一品.双液系的气液平衡相图实验装置的改进.大学化学,2003,18(6),
46
[5] 石秋之.对双液系相图体系选择的改进.大学化学,1996,11(4),36。
