新九年级上册化学必须记住的化学式和化学方程式化合价
人教版九年级化学上册必记的化学式和化学方程式(基础,必须掌握)

1、气态非金属单质: 氧气O 2 、氮气N 2 、氢气H 2 、氯气Cl 22、固态非金属单质: 碳C 、磷P 、硫S 、硅Si3、稀有气体单质: 氦He 、氖Ne 、氩Ar4、金属单质:铁Fe 、铜Cu 、锌Zn 、铝Al 、银Ag 、镁Mg 、钡Ba 、铂Pt 、金Au 、汞Hg 、钾K 、钙Ca 、锰Mn、钠Na1、氧化物:水H 2O 、 二氧化碳CO 2、 过氧化氢H 2O 2、 二氧化锰MnO 2、 一氧化碳CO 、 二氧化硫SO 2二氧化氮NO 2、 氧化铜CuO 、 氧化铁Fe 2O 3、四氧化三铁Fe 3O 4、 氧化镁MgO 、 氧化钙CaO 、 一氧化碳CO 、 五氧化二磷P 2O 5、 氧化铝Al 2O 3、 二氧化硅SiO 2、 氧化汞HgO 、 氧化亚铜Cu 2O 、 氨气NH 3 2、酸:硫酸H 2SO 4、碳酸H 2CO 3、盐酸HCl 、硝酸HNO 3 3、碱:氢氧化钠NaOH 、氢氧化钙Ca(OH)2、氢氧化钾KOH4、盐:氯化钠NaCl 、 氯化钾KCl 、 硫酸铜CuSO 4 、 碳酸钠Na 2CO 3、 氯酸钾KClO 3、 高锰酸钾KMnO 4、锰酸钾K 2MnO 4、 碳酸钙CaCO 3、 硫酸亚铁FeSO 4、 硫酸铁Fe 2(SO4)3 5、有机物:甲烷CH4、乙醇(俗名酒精)C 2H 5OH九年级上册必须记住的化学方程式(34个)1、镁燃烧:2Mg+O 2 2MgO2、铁燃烧:3Fe+2O 2 Fe 3O 43、铝燃烧:4Al+3O 2 2Al 2O 34、氢气燃烧:2H 2+O 2 2H 2O (淡蓝色火焰)5、红磷燃烧:4P+5O 2 2P 2O 56、硫粉燃烧: S+O 2SO 27、碳充分燃烧:C+O 2CO 28、碳不充分燃烧:2C+O 22CO9、二氧化碳通过灼热碳层: C+CO 22CO10、一氧化碳燃烧:2CO+O 2 2CO 211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO 2+H 2O==H 2CO 3(溶液变红)12、生石灰溶于水:CaO+H 2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO 4+5H 2O==CuSO 4·5H 2O 14、实验室用双氧水制氧气:2H 2O 22H 2O+O 2↑15、加热高锰酸钾:2KMnO 4 K 2MnO 4+MnO 2+O 2↑16、水在直流电的作用下分解:2H 2O 2H 2↑+O 2↑17、碳酸不稳定而分解:H 2CO 3==H 2O+CO 2↑18、高温煅烧石灰石(二氧化碳工业制法):CaCO 3CaO+CO 2↑19、铁和硫酸铜溶液反应:Fe+CuSO 4==FeSO 4+Cu (湿法炼铜的反应原理)20、锌和稀硫酸反应(实验室制氢气):Zn+H 2SO 4==ZnSO 4+H 2↑21、镁和稀盐酸反应:Mg+2HCl==MgCl 2+H 2↑ 22、氢气还原氧化铜:H 2+CuOCu+H 2O23、木炭还原氧化铜:C+2CuO 2Cu+CO 2↑ 24、水蒸气通过灼热碳层:H2O+C H 2+CO (水煤气)25、焦炭还原氧化铁:3C+2Fe 2O 3 4Fe+3CO 2↑ 26、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4(蓝色沉淀) 27、甲烷在空气中燃烧:CH 4+2O2CO 2+2H 2O (蓝色火焰) 28、酒精在空气中燃烧:C 2H 5OH+3O 22CO 2+3H 2O29、一氧化碳还原氧化铜:CO+CuO Cu+CO 230、一氧化碳还原氧化铁:3CO+Fe 2O 3 2Fe+3CO 2 31、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO 2==CaCO 3↓+H 2O (变浑浊)32、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO 2==Na 2CO 3+H 2O33、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑34、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑人教版九年级化学上册必记的化学式和化学方程式(基础,必须掌握)。
(完整word版)初中常见化合价、化学式、化学方程式

初中常见化学式和化学方程式一、常见元素原子团化合价口诀元素化合价口诀:钾钠氢银正一价,氟氯溴碘负一价,钙镁钡锌正二价,通常氧是负二价,铜有正一、正二价,铁有正二、正三价,铝是正三价,硅是正四价,碳是正二、正四价,单质元素化合价为零!原子团化合价口诀:NH4+(铵根离子)、NO3-(硝酸根离子)、OH-(氢氧根离子)、CO32-(碳酸根离子)、HCO3-(碳酸氢根离子)、MnO4-(高锰酸根离子)、MnO42-(锰酸根离子)、ClO3-(氯酸根离子)、SO42-(硫酸根离子)、SO32-(亚硫酸根离子)、PO43-(磷酸根离子)初中常见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P + 5O2 2P2O52、氢气在空气中燃烧生成水:2H2 + O22H2O3、硫磺在空气(或氧气)中燃烧:S + O2 SO24、镁条在空气(或氧气)中燃烧:2Mg + O22MgO5、铁丝在氧气中燃烧:3Fe + 2O2 Fe3O46、木炭在空气(或氧气)中完全燃烧:C + O2 CO27、木炭不充分燃烧:2C + O22CO8、一氧化碳燃烧:2CO + O2 2CO29、二氧化碳和水反应生成碳酸:CO2 + H2O == H2CO310、二氧化碳通过灼热的炭层:CO2 + C 2CO点燃点燃点燃点燃点燃点燃点燃高温点燃11、生石灰作为干燥剂:CaO + H2O == Ca(OH)2二、分解反应11、高锰酸钾制氧气:2KMnO4 K2MnO4+ MnO2+ O2↑12、氯酸钾制氧气:2KClO3 2KCl + 3O2↑13、双氧水制氧气:2H2O22H2O + O2↑14、电解水:2H2O 2H2↑+ O2↑15、碳酸分解:H2CO3H2O + CO2↑16、高温煅烧石灰石(工业制取二氧化碳):CaCO3 CaO +CO2↑三、置换反应17、铜和硝酸银溶液反应:Cu + 2AgNO3 == 2Ag + Cu(NO3)218、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO419、锌和硫酸反应制取氢气:Zn + H2SO4== ZnSO4+ H2↑20、铝和稀硫酸反应:2Al + 3H2SO4== Al2(SO4)3+ 3H2↑21、木炭还原氧化铁:3C + 2Fe2O34Fe + 3CO2↑木炭还原氧化铜:C + 2CuO 2Cu + CO2↑木炭还原四氧化三铁:2C + Fe3O43Fe +2CO2↑氢气还原氧化铜:H2 + CuO Cu + H2O四、复分解反应(一)酸 + 碱→盐 + 水22、氢氧化钠与盐酸反应:NaOH + HCl == NaCl + H2O23、氢氧化钠与硫酸反应:2NaOH + H2SO4== Na2SO4+ 2H2O24、氢氧化铝治疗胃酸过多:Al(OH)3 + 3HCl == AlCl3+ 3H2O25、氢氧化镁与硫酸反应:Mg(OH)2 + H2SO4== MgSO4+ 2H2O(二)酸 + 盐→新酸 + 新盐26、盐酸与硝酸银溶液反应:HCl + AgNO3 == AgCl↓+ HNO3△MnO2△MnO2通电高温高温高温高温高温27、氯化钡溶液与硫酸溶液反应:BaCl2 + H2SO4== BaSO4↓+ 2HCl28、碳酸钠与稀盐酸:Na2CO3+ 2HCl == 2NaCl+ H2O + CO2↑碳酸氢钠与稀盐酸:NaHCO3 + HCl == NaCl+ H2O + CO2↑29、石灰石与稀盐酸反应(实验室)制取二氧化碳:CaCO3+2HCl = CaCl2+H2O+CO2↑(三)碱 + 盐→另一种碱 + 另一种盐30、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓31、氯化铁溶液和氢氧化钠溶液反应:FeCl3+3NaOH==Fe(OH)3↓+3NaCl(四)盐 + 盐→两种新盐32、硝酸银溶液与氯化钠溶液反应:AgNO3 + NaCl == AgCl↓+ NaNO333、氯化钡溶液与碳酸钠溶液反应:BaCl2+ Na2CO3= BaCO3↓+ 2NaCl(五)金属氧化物 + 酸→盐 + 水34、稀盐酸清洗铁锈:6HCl + Fe2O3== 2FeCl3+ 3H2O35、氧化铜与稀硫酸反应:CuO + H2SO4== CuSO4+ H2O五、非金属氧化物 + 碱→盐 + 水36、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O37、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O38、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O39、氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH==Na2SO4+ H2O六、其他反应类型40、一氧化碳还原氧化铜:CO + CuO Cu + CO241、一氧化碳还原氧化铁:3CO + Fe2O32Fe + 3CO2↑42、一氧化碳还原四氧化三铁:4CO + Fe3O43Fe + 4CO2↑43、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O44、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃高温高温。
初中常见化合价、化学式、化学方程式
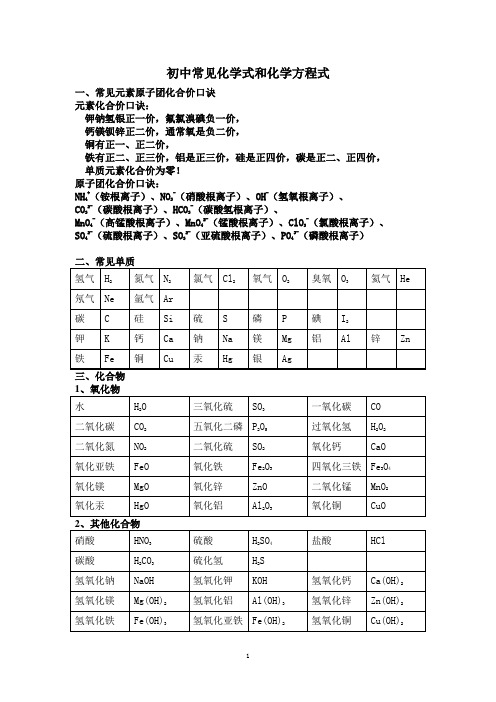
初中常见化学式和化学方程式一、常见元素原子团化合价口诀元素化合价口诀:钾钠氢银正一价,氟氯溴碘负一价,钙镁钡锌正二价,通常氧是负二价,铜有正一、正二价,铁有正二、正三价,铝是正三价,硅是正四价,碳是正二、正四价,单质元素化合价为零!原子团化合价口诀:NH4+(铵根离子)、NO3-(硝酸根离子)、OH-(氢氧根离子)、CO32-(碳酸根离子)、HCO3-(碳酸氢根离子)、MnO4-(高锰酸根离子)、MnO42-(锰酸根离子)、ClO3-(氯酸根离子)、SO42-(硫酸根离子)、SO32-(亚硫酸根离子)、PO43-(磷酸根离子)初中常见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P + 5O2 2P2O52、氢气在空气中燃烧生成水:2H2 + O22H2O3、硫磺在空气(或氧气)中燃烧:S + O2 SO24、镁条在空气(或氧气)中燃烧:2Mg + O22MgO5、铁丝在氧气中燃烧:3Fe + 2O2 Fe3O46、木炭在空气(或氧气)中完全燃烧:C + O2 CO27、木炭不充分燃烧:2C + O22CO8、一氧化碳燃烧:2CO + O2 2CO29、二氧化碳和水反应生成碳酸:CO2 + H2O == H2CO310、二氧化碳通过灼热的炭层:CO2 + C 2CO点燃点燃点燃点燃点燃点燃点燃高温点燃11、生石灰作为干燥剂:CaO + H2O == Ca(OH)2二、分解反应11、高锰酸钾制氧气:2KMnO4 K2MnO4+ MnO2+ O2↑12、氯酸钾制氧气:2KClO3 2KCl + 3O2↑13、双氧水制氧气:2H2O22H2O + O2↑14、电解水:2H2O 2H2↑+ O2↑15、碳酸分解:H2CO3H2O + CO2↑16、高温煅烧石灰石(工业制取二氧化碳):CaCO3 CaO +CO2↑三、置换反应17、铜和硝酸银溶液反应:Cu + 2AgNO3 == 2Ag + Cu(NO3)218、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO419、锌和硫酸反应制取氢气:Zn + H2SO4== ZnSO4+ H2↑20、铝和稀硫酸反应:2Al + 3H2SO4== Al2(SO4)3+ 3H2↑21、木炭还原氧化铁:3C + 2Fe2O34Fe + 3CO2↑木炭还原氧化铜:C + 2CuO 2Cu + CO2↑木炭还原四氧化三铁:2C + Fe3O43Fe +2CO2↑氢气还原氧化铜:H2 + CuO Cu + H2O四、复分解反应(一)酸 + 碱→盐 + 水22、氢氧化钠与盐酸反应:NaOH + HCl == NaCl + H2O23、氢氧化钠与硫酸反应:2NaOH + H2SO4== Na2SO4+ 2H2O24、氢氧化铝治疗胃酸过多:Al(OH)3 + 3HCl == AlCl3+ 3H2O25、氢氧化镁与硫酸反应:Mg(OH)2 + H2SO4== MgSO4+ 2H2O(二)酸 + 盐→新酸 + 新盐26、盐酸与硝酸银溶液反应:HCl + AgNO3 == AgCl↓+ HNO3△MnO2△MnO2通电高温高温高温高温高温27、氯化钡溶液与硫酸溶液反应:BaCl2 + H2SO4== BaSO4↓+ 2HCl28、碳酸钠与稀盐酸:Na2CO3+ 2HCl == 2NaCl+ H2O + CO2↑碳酸氢钠与稀盐酸:NaHCO3 + HCl == NaCl+ H2O + CO2↑29、石灰石与稀盐酸反应(实验室)制取二氧化碳:CaCO3+2HCl = CaCl2+H2O+CO2↑(三)碱 + 盐→另一种碱 + 另一种盐30、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓31、氯化铁溶液和氢氧化钠溶液反应:FeCl3+3NaOH==Fe(OH)3↓+3NaCl(四)盐 + 盐→两种新盐32、硝酸银溶液与氯化钠溶液反应:AgNO3 + NaCl == AgCl↓+ NaNO333、氯化钡溶液与碳酸钠溶液反应:BaCl2+ Na2CO3= BaCO3↓+ 2NaCl(五)金属氧化物 + 酸→盐 + 水34、稀盐酸清洗铁锈:6HCl + Fe2O3== 2FeCl3+ 3H2O35、氧化铜与稀硫酸反应:CuO + H2SO4== CuSO4+ H2O五、非金属氧化物 + 碱→盐 + 水36、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O37、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O38、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O39、氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH==Na2SO4+ H2O六、其他反应类型40、一氧化碳还原氧化铜:CO + CuO Cu + CO241、一氧化碳还原氧化铁:3CO + Fe2O32Fe + 3CO2↑42、一氧化碳还原四氧化三铁:4CO + Fe3O43Fe + 4CO2↑43、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O44、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃高温高温。
初三化学式与化合价知识点归纳

初三化学式与化合价知识点归纳初三化学式与化合价知识点归纳在我们平凡无奇的学生时代,很多人都经常追着老师们要知识点吧,知识点就是一些常考的内容,或者考试经常出题的地方。
掌握知识点有助于大家更好的学习。
以下是店铺为大家收集的初三化学式与化合价知识点归纳,仅供参考,大家一起来看看吧。
初三化合价知识化合价口诀化合价一:一价氟氯溴碘氢,还有金属钾钠银。
二价氧钡钙镁锌,铝三硅四都固定。
氯氮变价要注意,一二铜汞一三金。
二四碳铅二三铁,二四六硫三五磷。
常见元素的主要化合价二:氟氯溴碘负一价;正一氢银与钾钠。
氧的负二先记清;正二镁钙钡和锌。
正三是铝正四硅;下面再把变价归。
全部金属是正价;一二铜来二三铁。
锰正二四与六七;碳的二四要牢记。
非金属负主正不齐;氯的负一正一五七。
氮磷负三与正五;不同磷三氮二四。
硫有负二正四六;边记边用就会熟。
化合价口诀三:一价氢氯钾钠银;二价氧钙钡镁锌,三铝四硅五氮磷;二三铁二四碳,二四六硫全都齐;铜以二价最常见。
化合价口诀四:一价氢氯钾钠银二价氧钙钡镁锌三铝四硅五价磷二三铁二四碳二四六硫都齐全铜汞二价最常见负一硝酸氢氧根负二硫酸碳酸根负三记住磷酸根正一价的是铵根初三化学式知识单质:氢气H2、氮气N2、氧气O2、氯气Cl2、氦He、碳C、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。
非金属氧化物:水H2O、二氧化碳CO2、一氧化碳CO、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3、过氧化氢(双氧水)H2O2、二氧化氮NO2。
金属氧化物:氧化铁Fe2O3(赤铁矿,铁锈的主要成分)、四氧化三铁Fe3O4(磁铁矿的主要成分)、氧化铝Al2O3(铝土矿的主要成分)、氧化铜CuO、氧化钙CaO、二氧化锰MnO2、氧化镁MgO。
酸:盐酸HCl(胃酸的主要成分)、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、乙酸CH3COOH(俗称醋酸)。
初中化学必背化学式大全修改后

九年级化学必背化学式及常见元素化合价1.元素符号:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷H He Li Be B ,C N O F Ne, Na Mg Al Si P,硫氯氩钾钙锰铁铜锌银钡铂金汞碘S Cl Ar K Ca, Mn Fe Cu Zn Ag, Ba Pt Au Hg I2.常见离子氢离子H+ 钠离子Na+钾离子K+银离子Ag+铵根离子NH4+钙离子Ca2+镁离子Mg2+铜离子Cu2+ 钡离子Ba2+,锌离子Zn2+亚铁离子Fe2+铁离子Fe3+铝离子Al3+氯离子Cl-氢氧根离子OH-硝酸根离子NO3-氧离子O2-硫酸根离子SO42-碳酸根离子CO32-3.常见物质的化学式与名称:单质:由一种元素组成的纯净物。
C:碳 S:硫 P:磷 Fe:铁Mg:镁 Al:铝 Hg:汞 Zn:锌Cu:铜 Ag:银 O2:氧气 H2:氢气 N2:氮气 O3:臭氧氧化物:由两种元素组成,其中有一种是氧元素的化合物。
CO:一氧化碳 CO2:二氧化碳 SO2:二氧化硫 MnO2:二氧化锰SO3:三氧化硫 H2O2:过氧化氢CuO:氧化铜 CaO:氧化钙MgO:氧化镁 HgO:氧化汞 Fe2O3:氧化铁 Al2O3:氧化铝H2O:水(相对分子质量最小的氧化物) P2O5:五氧化二磷 Fe3O4:四氧化三铁酸:HCl:盐酸 H2SO4:硫酸 HNO3:硝酸 H2CO3:碳酸H2SO3亚硫酸 CH3COOH:醋酸碱:NaOH:氢氧化钠 Ca(OH)2:氢氧化钙 KOH:氢氧化钾 Mg(OH)2:氢氧化镁Cu(OH)2:氢氧化铜 NH3.H2O氨水 Fe(OH)3:氢氧化铁 Al(OH)3:氢氧化铝盐酸盐/氯化物:KCl:氯化钾 NaCl:氯化钠 KCl:氯化钾 AgCl:氯化银CuCl2:氯化铜 CaCl2:氯化钙 MgCl2:氯化镁 ZnCl2:氯化锌BaCl2:氯化钡 FeCl2:氯化亚铁 AlCl3:氯化铝 FeCl3:氯化铁碳酸盐:CaCO3:碳酸钙 Na2CO3:碳酸钠 NaHCO3:碳酸氢钠BaCO3:碳酸钡 K2CO3:碳酸钾 NH4HCO3:碳酸氢铵硫酸盐:Na2SO4:硫酸钠 ZnSO4:硫酸锌 MgSO4:硫酸镁CaSO4:硫酸钙 CuSO4:硫酸铜 BaSO4:硫酸钡FeSO4:硫酸亚铁 Fe2(SO4)3:硫酸铁 Al2(SO4)3:硫酸铝(NH4)2SO4:硫酸铵 Na2SO3:亚硫酸钠硝酸盐:AgNO3:硝酸银 NaNO3:硝酸钠 Cu(NO3)2:硝酸铜KNO3:硝酸钾 NH4NO3:硝酸铵 NaNO2:亚硝酸钠钾盐:KMnO4:高锰酸钾 K2MnO4:锰酸钾 KClO3:氯酸钾有机化合物:C 2H5OH:乙醇 C6H12O6:葡萄糖 CH4:甲烷4、常见元素及常见的根价:常见元素化合价记忆口决:一价氢氟钾钠银;二价氧钙钡镁锌;三铝四硅五价磷;二三铁二四碳;二四六硫都齐全;铜汞二价最常见。
九年级上册化学必须记住的化学式和化学方程式

九年级上册化学必须记住的化学式一、单质的化学式:25个1、气态非金属单质:氧气O2、氮气N2、氢气H2、氯气Cl22、固态非金属单质:碳C 、磷P、硫S、硅Si3、稀有气体单质:氦He、氖Ne、氩Ar4、金属单质:铁Fe、铜Cu、锌Zn、铝Al、银Ag、镁Mg、钡Ba、铂Pt、金Au、汞Hg、钾K、钙Ca、锰Mn、钠Na 二、化合物的化学式:37个1、氧化物:水H2O、二氧化碳CO2、过氧化氢H2O2、二氧化锰MnO2、一氧化碳CO、二氧化硫SO2、二氧化氮NO2、氧化铜CuO、氧化铁Fe2O3、四氧化三铁Fe3O4、氧化镁MgO、氧化钙CaO、一氧化碳CO、五氧化二磷P2O5、氧化铝Al2O3、二氧化硅SiO2、氧化汞HgO、氧化亚铜Cu2O、氨气NH32、酸:硫酸H2SO4、碳酸H2CO3、盐酸HCl、硝酸HNO33、碱:氢氧化钠NaOH、氢氧化钙CaOH2、氢氧化钾KOH4、盐:氯化钠NaCl、氯化钾KCl、硫酸铜CuSO4、碳酸钠Na2CO3、氯酸钾KClO3、高锰酸钾KMnO4、锰酸钾K2MnO4、碳酸钙CaCO3、硫酸亚铁FeSO4、硫酸铁Fe2SO435、有机物:甲烷CH4、乙醇俗名酒精C2H5OH九年级上册化学必须记住的化学方程式34个1、镁燃烧:2Mg+O 2 2MgO2、铁燃烧:3Fe+2O 2Fe 3O 43、铝燃烧:4Al+3O 22Al 2O 34、氢气燃烧:2H 2+O 22H 2O 淡蓝色火焰5、红磷燃烧:4P+5O 22P 2O 56、硫粉燃烧: S+O 2SO 27、碳充分燃烧:C+O 2CO 2 8、碳不充分燃烧:2C+O 22CO9、二氧化碳通过灼热碳层: C+CO 22CO 10、一氧化碳燃烧:2CO+O 22CO 211、二氧化碳和水反应二氧化碳通入紫色石蕊试液:CO 2+H 2O==H 2CO 3溶液变红 12、生石灰溶于水:CaO+H 2O==CaOH 2 13、无水硫酸铜作干燥剂:CuSO 4+5H 2O==CuSO 4·5H 2O 14、实验室用双氧水制氧气:2H 2O 22H 2O+O 2↑15、加热高锰酸钾:2KMnO 4 K 2MnO 4+MnO 2+O 2↑ 16、水在直流电的作用下分解:2H 2O2H 2↑+O 2↑ 17、碳酸不稳定而分解:H 2CO 3==H 2O+CO 2↑ 18、高温煅烧石灰石二氧化碳工业制法:CaCO 3CaO+CO 2↑ 19、铁和硫酸铜溶液反应:Fe+CuSO 4==FeSO 4+Cu 湿法炼铜的反应原理 20、锌和稀硫酸反应实验室制氢气:Zn+H 2SO 4==ZnSO 4+H 2↑ 21、镁和稀盐酸反应:Mg+2HCl==MgCl 2+H 2↑ 22、氢气还原氧化铜:H 2+CuO Cu+H 2O 23、木炭还原氧化铜:C+2CuO2Cu+CO 2↑ 24、水蒸气通过灼热碳层:H 2O+CH 2+CO 水煤气 25、焦炭还原氧化铁:3C+2Fe 2O 34Fe+3CO 2↑26、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO 4==CuOH 2↓+Na 2SO 4蓝色沉淀 27、甲烷在空气中燃烧:CH 4+2O 2CO 2+2H 2O 蓝色火焰 28、酒精在空气中燃烧:C 2H 5OH+3O 2 2CO 2+3H 2O 29、一氧化碳还原氧化铜:CO+CuOCu+CO 230、一氧化碳还原氧化铁:3CO+Fe 2O 3 2Fe+3CO 231、二氧化碳通过澄清石灰水检验二氧化碳:CaOH 2+CO 2==CaCO 3↓+H 2O 变浑浊 32、氢氧化钠和二氧化碳反应除去二氧化碳:2NaOH+CO 2==Na 2CO 3+H 2O 33、石灰石或大理石与稀盐酸反应二氧化碳的实验室制法:CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑34、碳酸钠与浓盐酸反应泡沫灭火器的原理: Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑。
九年级上化学常见化学式、必背化学方程式
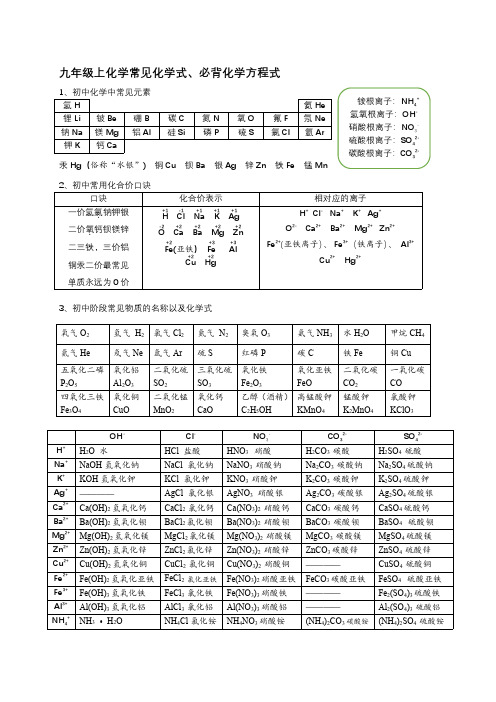
九年级上化学常见化学式、必背化学方程式1、初中化学中常见元素氢H 氦He 锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne 钠Na 镁Mg 铝Al硅Si磷P硫S氯Cl氩Ar钾K钙Ca汞Hg(俗称“水银”)铜Cu钡Ba银Ag锌Zn铁Fe锰Mn2、初中常用化合价口诀口诀化合价表示相对应的离子一价氢氯.钠钾银二价氧.钙钡镁锌二三铁,三价铝铜汞二价最常见单质永远为0价+1H -1Cl +1Na +1K+1Ag -2O+2Ca+2Ba +2Mg+2Zn +2Fe(亚铁)+3Fe+3Al+2Cu+2HgH +Cl -Na +K +Ag +O 2-Ca 2+Ba 2+Mg 2+Zn 2+Fe 2+(亚铁离子)、Fe 3+(铁离子)、Al 3+Cu 2+Hg 2+3、初中阶段常见物质的名称以及化学式氧气O 2氢气H 2氯气Cl 2氮气N 2臭氧O 3氨气NH 3水H 2O 甲烷CH 4氦气He 氖气Ne 氩气Ar 硫S 红磷P 碳C 铁Fe 铜Cu 五氧化二磷P 2O 5氧化铝Al 2O 3二氧化硫SO 2三氧化硫SO 3氧化铁Fe 2O 3氧化亚铁FeO二氧化碳CO 2一氧化碳CO 四氧化三铁Fe 3O 4氧化铜CuO 二氧化锰MnO 2氧化钙CaO乙醇(酒精)C 2H 5OH 高锰酸钾KMnO 4锰酸钾K 2MnO 4氯酸钾KClO 3OH -Cl -NO 3-CO 32-SO 42-H +H 2O 水HCl 盐酸HNO 3硝酸H 2CO 3碳酸H 2SO 4硫酸Na +NaOH 氢氧化钠NaCl 氯化钠NaNO 3硝酸钠Na 2CO 3碳酸钠Na 2SO 4硫酸钠K +KOH 氢氧化钾KCl 氯化钾KNO 3硝酸钾K 2CO 3碳酸钾K 2SO 4硫酸钾Ag +————AgCl 氯化银AgNO 3硝酸银Ag 2CO 3碳酸银Ag 2SO 4硫酸银Ca 2+Ca(OH)2氢氧化钙CaCl 2氯化钙Ca(NO 3)2硝酸钙CaCO 3碳酸钙CaSO 4硫酸钙Ba 2+Ba(OH)2氢氧化钡BaCl 2氯化钡Ba(NO 3)2硝酸钡BaCO 3碳酸钡BaSO 4硫酸钡Mg 2+Mg(OH)2氢氧化镁MgCl 2氯化镁Mg(NO 3)2硝酸镁MgCO 3碳酸镁MgSO 4硫酸镁Zn 2+Zn(OH)2氢氧化锌ZnCl 2氯化锌Zn(NO 3)2硝酸锌ZnCO 3碳酸锌ZnSO 4硫酸锌Cu 2+Cu(OH)2氢氧化铜CuCl 2氯化铜Cu(NO 3)2硝酸铜————CuSO 4硫酸铜Fe 2+Fe(OH)2氢氧化亚铁FeCl 2氯化亚铁Fe(NO 3)2硝酸亚铁FeCO 3碳酸亚铁FeSO 4硫酸亚铁Fe 3+Fe(OH)3氢氧化铁FeCl 3氯化铁Fe(NO 3)3硝酸铁————Fe 2(SO 4)3硫酸铁Al 3+Al(OH)3氢氧化铝AlCl 3氯化铝Al(NO 3)3硝酸铝————Al 2(SO 4)3硫酸铝NH 4+NH 3•H 2ONH 4Cl 氯化铵NH 4NO 3硝酸铵(NH 4)2CO 3碳酸铵(NH 4)2SO 4硫酸铵铵根离子:NH 4+氢氧根离子:OH -硝酸根离子:NO 3-硫酸根离子:SO 42-碳酸根离子:CO 32-4、写出下列反应的化学方程式(★必须全部掌握★):(1)红磷在空气中燃烧:522O P 2O 5P 4点燃+(2)硫在氧气中燃烧:22O S 点燃+(3)铁丝在氧气中燃烧:432O Fe O 2Fe 3点燃+(4)碳在氧气中充分燃烧:22CO O C 点燃+;(5)碳不充分燃烧:CO 2O C 22点燃+(6)氢气在空气中燃烧:O H 2O H 2222点燃+(7)镁条在空气中燃烧:MgO2O Mg 22点燃+(8)电解水反应:↑+↑222O H 2OH 2通电(9)实验室高锰酸钾制取氧气:↑++∆22424O MnO MnO K KMnO 2(10)实验室氯酸钾制取氧气:↑+∆2MnO 3O 3KCl 2KClO 22(11)实验室过氧化氢溶液(俗称双氧水)制取氧气:↑+22MnO 22O O H 2O H 22(12)铁与硫酸铜溶液反应:44FeSO Cu CuSO Fe ++(13)氧化铜与氢气在加热的条件下反应生成铜单质和水:OH Cu H CuO 22++∆(14)硫酸铜溶液与氢氧化钠溶液反应生成硫酸钠溶液和氢氧化铜沉淀:4224SO Na )OH (Cu OHNa 2CuSO +↓+(15)高温煅烧石灰石(主要成分CaCO 3):↑+23CO CaO CaCO 高温(16)木炭与氧化铜反应生成铜和二氧化碳:↑++2CO Cu 2CuO2C 高温(17)焦炭把铁从它的氧化物矿石里还原出来:↑++232CO 3Fe 4O Fe 2C 3高温(18)高温条件下,碳能使二氧化碳转变成一氧化碳;CO2O C C 2高温+(19)用稀盐酸和大理石(或石灰石)制取二氧化碳:↑+++2223CO O H CaCl HCl 2CaCO (20)二氧化碳使澄清石灰水变浑浊:OH CaCO )OH (Ca CO 2322+↓+(21)二氧化碳溶于水:3222CO H O H O C +,(22)碳酸不稳定,易分解:OH O C CO H 2232+↑(23)一氧化碳燃烧:22CO 2O CO 2点燃+(24)一氧化碳还原氧化铜:2CO Cu CuO CO ++∆(25)氧化钙溶于水:22)OH (Ca OH O Ca +(26)甲烷在空气中燃烧:OH 2CO O 2CH 2224++点燃(27)乙醇在空气中燃烧:OH 3CO 2O 3OH H C 22252++点燃(28)实验室用锌粒和稀硫酸制取氢气:↑++2442H ZnSO SO H Zn。
必过10个“难关”:化学式、化合价---2024-2025学年九年级化学人教版(2024)上册

初三化学上学期必过10个“难关”化学式、化合价【必练】1、化合价口诀:一价氢氯钾钠银二价氧钙钡镁锌三铝四硅五价磷二三铁、二四碳二四六硫都齐全铜汞二价最常见氢一氧二为标准单质为零要记准负一氢氧硝酸根负二硫酸碳酸根负三记住磷酸根正一价的是铵根2.初中必背元素及其符号(1)前二十号元素原子序数12345678910元素名称氢氦锂铍硼碳氮氧氟氖元素符号原子序数11121314151617181920元素名称钠镁铝硅磷硫氯氩钾钙元素符号(2)其他重要常见元素元素名称铁铜锌银汞碘元素符号Mn Ba Pb Sn 3.初中常见物质的名称及化学式名称氧化铁五氧化二磷二氧化硫三氧化硫一氧化碳二氧化碳化学式名称氧化铜氧化镁四氧化三铁二氧化锰氯化钾氯化钠化学式名称氯化钙氯化镁氯化铝氯化亚铁氯化铁氯化铜化学式名称氯化银氯化铵硫酸钾硫酸钙硫酸钠硫酸钡化学式名称硫酸镁硫酸铝硫酸锌硫酸亚铁硫酸铁硫酸铜化学式名称硫酸铵碳酸钠碳酸钾碳酸钙硝酸钾硝酸钠化学式名称硝酸铜硝酸银硝酸铵氢氧化钾氢氧化钙氢氧化钠化学式名称氢氧化铁氢氧化铜盐酸硫酸过氧化氢氧化汞化学式名称甲烷乙醇氨气氯酸钾高锰酸钾锰酸钾化学式4.化学符号周围数字的含义(1)元素符号前面的数字,表示 。
如:2O 表示 。
(2)化学式前面的数字,表示该物质的粒子个数。
如:2O 2中前面的数字“2”表示 。
(3)元素符号右下角的数字表示每个粒子中某元素的原子个数。
如: O 2中的“2”表示 。
(4)离子符号右上角的数字表示 。
如:O 2-。
(5)离子符号前的数字表示 。
如: 2O 2-前面的数字“2”。
(6)元素符号正上方的数字表示元素的 。
如:O -2。
元素符号和化学式前加上数字以后, 就失去了宏观意义,只有 意义。
5、单质的写法1)、金属、固体非金属(碘除外)、稀有气体等化学式的写法: (1)铁 (2)硫 (3)氖气 (4)铜 (5)铝 (6)氦气 (7)红磷 (8)银 (9)木炭 2)、气体非金属化学式的写法:(1)氧气 (2)氢气 (3)氯气 (4)氮气 (5)硫 (6)氖气 6、化合物化学式的书写和命名在化合物中正三价的铁一般读作铁,正二价的铁读作亚铁。
九年级化学上册-必背知识点讲解-人教新课标版

化学上册必背知识点一、化学用语1、常见元素及原子团的名称和符号非金属: O氧 H氢 N氮 Cl氯 C碳 P磷 S硫金属: K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag银 Mn锰 Ba钡原子团(根):氢氧根硝酸根碳酸根硫酸根磷酸根铵根OH- NO3- CO32- SO4 2- PO43- NH4+2、化合价口诀(1) 常见元素化合价口诀:一价氢氯钾钠银;二价氧钙钡镁锌;三五氮磷三价铝;铜汞一二铁二三;二、四、六硫四价碳;许多元素有变价,条件不同价不同。
(2) 常见原子团(根)化学价口诀:一价硝酸氢氧根;二价硫酸碳酸根;三价常见磷酸根;通常负价除铵根。
4、必须熟记的制取物质的化学方程式(1)实验室制取氧气一: 2KMnO4===K2MnO4+MnO2+O2↑(2)实验室制取氧气二: 2H2O2 ===2H2O+O2↑(3) 实验室制取氧气三: 2KClO3===2KCl+3O2↑(4)实验室制法CO2: CaCO3+2HCl==CaCl2+H2O+CO2↑(5)实验室制取氢气: Zn+H2SO4==ZnSO4+H2↑(6)电解水制取氢气: 2H2O===2H2↑+O2↑(7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu(8)炼铁原理: 3CO+Fe2O3===2Fe+3CO2(9)生灰水[Ca(OH)2 ]的制取方法:CaO+H2O==Ca(OH)2(10)生石灰(氧化钙)制取方法:CaCO3 ===CaO+CO2↑二.金属活动性顺序:金属活动性由强至弱:K Ca Na Mg Al , Zn Fe Sn Pb (H) ,Cu Hg Ag Pt Au。
(按5个一句顺序背诵)钾钙钠镁铝,锌铁锡铅(氢),铜汞银铂金。
三、常见物质的颜色、状态1、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态),除了有颜色的固体,其他固体一般为白色。
初中化学“化合价口诀+方程式”

初中化学“化合价口诀+全部方程式”化合价口诀 (熟记)(正价)氢钠钾银正一价,钙镁钡锌正二价,铝三硅四氮磷五,二四六硫二四碳,铜汞二一,铁二三(负价), 氟氯溴碘负一价,氧硫常显负二价;氮磷均有负三价;单质化合价为零。
• 一价钾钠氯氢银:钾(K )钠(Na )在化合物中通常显 +1 价;氯(Cl )在氯化物中一般显 -1 价(如氯化钠 NaCl );氢(H )在化合物中常为 +1 价;银(Ag )在化合物中通常显 +1 价。
• 二价氧钙钡镁锌:氧(O )在化合物中一般显 -2 价(除过氧化物等特殊情况);钙(Ca )、钡(Ba )、镁(Mg )、锌(Zn )在化合物中常显 +2 价。
• 三铝四硅五价磷:铝(Al )在化合物中通常显 +3 价;硅(Si )常见化合价为 +4 价; 磷(P )有 +5 价等多种化合价,这里主要强调常见的 +5 价。
• 二三铁,二四碳:铁(Fe )有 +2 价(亚铁离子)和 +3 价(铁离子);碳(C )有 +2 价(如一氧化碳 CO )和 +4 价(如二氧化碳 CO₂)。
• 二四六硫都齐全:硫(S )有 -2 价(如硫化氢 H₂S )、+4 价(如二氧化硫 SO₂)和 +6 价(如三氧化硫 SO₃)。
• 铜汞二价最常见:铜(Cu )和汞(Hg )在化合物中通常显 +2 价,但铜也有 +1 价(如氧化亚铜 Cu₂O )。
• 氢一氧二要记清:再次强调氢一般为 +1 价,氧一般为 -2 价。
• 单质元素价为零:任何单质中元素的化合价都为 0 价,比如氧气(O₂)、铁(Fe )等单质中 氧元素和铁元素化合价均为 0 。
常见原子团的化合价负一硝酸NO 3-氢氧根 OH -负二碳酸 CO 32- 硫酸 SO 42-锰酸根 MnO 42-负三只有磷酸根 PO 43-,正一价的是氨根 NH 4+可溶物与不溶物的记忆口诀 口诀一钾钠铵盐均可溶;硝盐入水影无踪 硫酸盐中钡不溶;氯化盐中银不溶 碳酸盐中只溶钾、钠、铵; 碱只溶钾、钠、钙、钡、铵 口诀二钾钠铵盐硝酸盐,完全溶解不困难。
九年级化学表达式及符号

九年级化学表达式及符号一、常见元素符号1. 氢:H2. 氦:He3. 锂:Li4. 铍:Be5. 硼:B6. 碳:C7. 氮:N8. 氧:O9. 氟:F10. 氖:Ne11. 钠:Na12. 镁:Mg13. 铝:Al14. 硅:Si15. 磷:P16. 硫:S17. 氯:Cl18. 氩:Ar19. 钾:K20. 钙:Ca二、常见原子团符号及化合价1. 氢氧根离子- 符号:OH⁻- 化合价:-1价2. 硝酸根离子- 符号:NO₃⁻- 化合价:-1价3. 碳酸根离子- 符号:CO₃²⁻- 化合价:-2价4. 硫酸根离子- 符号:SO₄²⁻- 化合价:-2价5. 铵根离子- 符号:NH₄⁺- 化合价:+1价三、化学方程式(表达式)1. 氧气的制取- 过氧化氢分解制取氧气- 文字表达式:过氧化氢→水 + 氧气- 化学方程式:2H₂O₂MnO₂__2H₂O+O₂↑- 氯酸钾分解制取氧气(用二氧化锰作催化剂)- 文字表达式:氯酸钾→氯化钾+氧气(反应条件:二氧化锰作催化剂,加热)- 化学方程式:2KClO₃MnO₂、Δ__2KCl + 3O₂↑- 高锰酸钾分解制取氧气- 文字表达式:高锰酸钾→锰酸钾+二氧化锰+氧气(反应条件:加热) - 化学方程式:2KMnO₄Δ__K₂MnO₄+MnO₂+O₂↑2. 氢气的制取(锌和稀硫酸反应)- 文字表达式:锌+稀硫酸→硫酸锌+氢气- 化学方程式:Zn + H₂SO₄=ZnSO₄+H₂↑3. 二氧化碳的制取(大理石或石灰石与稀盐酸反应)- 文字表达式:碳酸钙+稀盐酸→氯化钙+水+二氧化碳- 化学方程式:CaCO₃+2HCl = CaCl₂+H₂O+CO₂↑。
九年级上册化学必须记住的化学式和化学方程式

九年级上册化教必须记着的化教式之阳早格格创做一、单量的化教式:(25个)1、气态非金属单量:氧气O2、氮气N2、氢气H2、氯气Cl22、固态非金属单量:碳C、磷P、硫S、硅Si3、密有气体单量:氦He、氖Ne、氩Ar4、金属单量:铁Fe、铜Cu、锌Zn、铝Al、银Ag、镁Mg、钡Ba、铂Pt、金Au、汞Hg、钾K、钙Ca、锰Mn、钠Na两、化合物的化教式:(37个)1、氧化物:火H2O、两氧化碳CO2、过氧化氢H2O2、两氧化锰MnO 2、一氧化碳CO、两氧化硫SO2、两氧化氮NO2、氧化铜CuO、氧化铁Fe2O 3、四氧化三铁Fe3O4、氧化镁MgO、氧化钙CaO、一氧化碳CO、五氧化两磷P2O5、氧化铝Al2O3、两氧化硅SiO2、氧化汞HgO、氧化亚铜Cu2O、氨气NH32、酸:硫酸H2SO4、碳酸H2CO3、盐酸HCl、硝酸HNO33、碱:氢氧化钠NaOH、氢氧化钙Ca(OH)2、氢氧化钾KOH4、盐:氯化钠NaCl、氯化钾KCl、硫酸铜CuSO4、碳酸钠Na2CO3、氯酸钾KClO3、下锰酸钾KMnO4、锰酸钾K2MnO4、碳酸钙CaCO3、硫酸亚铁FeSO4、硫酸铁Fe2(SO4)35、有机物:甲烷CH4、乙醇(雅名酒粗)C2H5OH九年级上册化教必须记着的化教圆程式(34个)1、镁焚烧:2Mg+O22MgO2、铁焚烧:3Fe+2O2 Fe3O43、铝焚烧:4Al+3O2 2Al2O34、氢气焚烧:2H2+O2 2H2O(浓蓝色火焰)5、白磷焚烧:4P+5O2 2P2O56、硫粉焚烧: S+O2SO27、碳充分焚烧:C+O2CO28、碳没有充分焚烧:2C+O22CO 9、两氧化碳通过灼热碳层:C+CO2 2CO10、一氧化碳焚烧:2CO+O2 2CO211、两氧化碳战火反应(两氧化碳通进紫色石蕊试液):CO2+H2O==H2CO3(溶液变白)12、死石灰溶于火:CaO+H2O==Ca(OH)213、无火硫酸铜做搞燥剂:CuSO4+5H2O==CuSO4·5H2O14、真验室用单氧火造氧气:2H2O22H2O+O2↑15、加热下锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑16、火正在曲流电的效率下领会:2H2O 2H2↑+O2↑ 17、碳酸没有宁静而领会:H2CO3==H2O+CO2↑18、下温煅烧石灰石(两氧化碳工业造法):CaCO3 CaO+CO2↑19、铁战硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu(干法炼铜的反应本理)20、锌战密硫酸反应(真验室造氢气):Zn+H2SO4==ZnSO4+H2↑21、镁战密盐酸反应:Mg+2HCl==MgCl2+H2↑22、氢气还本氧化铜:H2+CuO Cu+H2O23、木冰还本氧化铜:C+2CuO 2Cu+CO2↑24、火蒸气通过灼热碳层:H2O+C H2+CO(火煤气)25、焦冰还本氧化铁:3C+2Fe2O34Fe+3CO2↑26、氢氧化钠溶液取硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4(蓝色重淀)27、甲烷正在气氛中焚烧:CH4+2O2 CO2+2H2O(蓝色火焰) 28、酒粗正在气氛中焚烧:C2H5OH+3O2 2CO2+3H2O29、一氧化碳还本氧化铜:CO+CuO Cu+CO230、一氧化碳还本氧化铁:3CO+Fe2O3 2Fe+3CO231、两氧化碳通过澄浑石灰火(考验两氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O(变浑浊)32、氢氧化钠战两氧化碳反应(取消两氧化碳):2NaOH+CO2==Na2CO3+H2O33、石灰石(或者大理石)取密盐酸反应(两氧化碳的真验室造法):CaCO3+2HCl==CaCl2+H2O+CO2↑34、碳酸钠取浓盐酸反应(泡沫灭火器的本理): Na2CO3+2HCl==2NaCl+H2O+CO2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
九年级上册化学必须记住的化学式
一、单质的化学式:(24个)
1、气态非金属单质:氧气O2、氮气N2、氢气H2、氯气Cl2
2、固态非金属单质:碳C、磷P、硫S、硅Si
3、稀有气体单质:氦He、氖Ne、氩Ar
4、金属单质:铁Fe、铜Cu、锌Zn、铝Al、银Ag、镁Mg、
钡Ba、金Au、汞Hg、钾K、钙Ca、锰Mn、钠Na
二、化合物的化学式:(37个)
1、氧化物:水H2O、二氧化碳CO2、过氧化氢H2O2、二氧化锰MnO2、
一氧化碳CO、二氧化硫SO2、二氧化氮NO2、氧化铜CuO、氧化铁Fe2O3、
四氧化三铁Fe3O4、氧化镁MgO、氧化钙CaO、一氧化碳CO、五氧化二磷P2O5、氧化铝Al2O3、二氧化硅SiO2、氧化汞HgO、特殊:氨气NH3
2、酸:硫酸H2SO4、碳酸H2CO3、盐酸HCl、硝酸HNO3
3、碱:氢氧化钠NaOH、氢氧化钙Ca(OH)2、氢氧化钾KOH
4、盐:氯化钠NaCl、氯化钾KCl、硫酸铜CuSO4、碳酸钠Na2CO3、
氯酸钾KClO3、高锰酸钾KMnO4、锰酸钾K2MnO4、碳酸钙CaCO3、
硫酸亚铁FeSO4、硫酸铁Fe2(SO4)3
5、有机物:甲烷CH4、乙醇(俗名酒精)C2H5OH
九年级上册化学必须记住的化学方程式(34个)
1、镁燃烧:2Mg+O22MgO
2、铁燃烧:3Fe+2O2Fe3O4
3、铝燃烧:4Al+3O22Al2O3
4、氢气燃烧:2H2+O22H2O(淡蓝色火焰)
5、红磷燃烧:4P+5O22P2O5
6、硫粉燃烧:S+O2SO2
7、碳充分燃烧:C+O2CO28、碳不充分燃烧:2C+O22CO
9、二氧化碳通过灼热碳层:C+CO22CO
10、一氧化碳燃烧:2CO+O22CO2
11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO3(溶液变红)
12、生石灰溶于水:CaO+H2O==Ca(OH)2
13、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4·5H2O
14、实验室用双氧水制氧气:2H2O22H2O+O2↑
15、加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑
16、水在直流电的作用下分解:2H2O2H2↑+O2↑
17、碳酸不稳定而分解:H2CO3==H2O+CO2↑
18、高温煅烧石灰石(二氧化碳工业制法):CaCO3CaO+CO2↑19、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu(湿法炼铜的反应原理)20、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑
21、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑22、氢气还原氧化铜:H2+CuO Cu+H2O
23、木炭还原氧化铜:C+2CuO2Cu+CO2↑
24、水蒸气通过灼热碳层:H2O+C H2+CO(水煤气)
25、焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑
26、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4(蓝色沉淀)
27、甲烷在空气中燃烧:CH4+2O2CO2+2H2O(蓝色火焰)
28、酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O
29、一氧化碳还原氧化铜:CO+CuO Cu+CO2
30、一氧化碳还原氧化铁:3CO+Fe2O32Fe+3CO2
31、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O(变浑浊)
32、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O
33、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):
CaCO3+2HCl==CaCl2+H2O+CO2
34、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2↑
化合价
正一钾钠和氢银,正二钙铜镁钡锌,
铝三硅四氧负二,铁变二三碳二四,
氟氯溴碘负一价,单质零价永不变。
谈变价,也不难。
正二亚铁,正三铁。
原子团,化合价
负一氢氧硝酸根,硝酸根NO3:-1氢氧根OH:-1
负二硫酸碳酸根,硫酸根SO4:-2碳酸根CO3:-2
负三记住磷酸根,磷酸根PO4:-3
正一价的是铵根。
铵根NH4:+1。
