大学有机化学第三章不饱和脂肪烃
不饱和脂肪烃—烯烃氧化(有机化学课件)

O RCOOH(过氧酸)
催化氧化
R
R"
C O+ O C
R'
OH
R
R"
CO+OC
R'
H
R R" R' C C H
OH OH
R
R"
CC
R'
H
O
酮、酸 邻二醇 酮、醛 环氧化物 环氧乙烷 酮、醛
学后释疑
产生乙烯
放置吸有某种成分的的H2
+
1 2
O2
PdCl 2-CuCl2 120~130 C °
O CH3C H —CH3
用 途 合成:工业上在氯化钯–氯化铜的作用下,生产乙醛、丙酮
小结
R C
R'
R" C
H
注意双键和H的变化
KMnO4(浓,热), OH 或 K2Cr2O7, H (1) O3
(2) H2O, Zn
被中性或碱性的高锰酸钾氧化——缓慢氧化
邻二醇
OH OH
KMnO4(稀,冷)
或
OsO4
反应的立体化学——顺式产物
HO OH
用 途 鉴别:紫红色褪去,常温下鉴别烯烃 合成:制备顺式邻二醇
烯烃的氧化反应 1. 与高锰酸钾反应
被酸性高锰酸钾氧化——剧烈氧化
浓,热 或
CH2= RCH= R R C=
产物特点 CO2 + H2O RCOOH R R C=O
酸性KMnO4溶液
HH
OO RRCCOOOOOHHH
RR
RR""
有机化学合成总结

有机化学合成总结1.饱和脂肪烃(1).偶联反应(2).醛、酮还原(3).烯烃、炔烃还原2. 不饱和脂肪烃 一、烯烃合成 (1).醇脱水(2).卤代烷脱卤化氢(3).邻二卤化合物脱卤化氢(4).炔的还原RORR-XR-R RCCRRCH 2-CH 2RRCH=CHR RCH 2-CH 2RCH=CH 2R RCH2-CH 2-OHR-CH 2CH2XR-CH=CH 2R-CHX-CH 2XR -CH=CH 2(5).Wittig 反应二、炔烃合成 (1)从其它炔烃(2)通过二卤消除反应3.卤代烃(1)烷烃的卤代(2)不饱和烃和卤化氢或卤素加成(3)从醇制备C CR1R2RHCOR1R2R-CH=P(Ph)3R-C C-R 1R-CR1XCH R-C CR 1R-C-C-R 1X H H XRX RHX 2R-CH-CH 2XR-CH=CH 2R-CH=CH 2R-CH CH 2X X X 2RXROHX-G(4)卤素的置换 4.醇(1) 烯烃水合C-CH 2OH H RHR-CH=CH 2OH 2(2)硼氢化-氧化(3).醛,酮,羧酸及其酯还原(4) 从格利雅试剂RCl NaIRI R-CH 2CH 2OHR-CH=CH 2(BH 3)2C-CH 2OHH RHR-CH=CH 2R-CH 2OHRCHOR-COOH RCOOR 1RROR ROHR-CH 2-OHRMgXCH 2O RH R1ORMgX R 1CHOR 1MgX RCHORR2R1ORMgX R 1R 2CO R 1MgXRR2CO(5)卤烃水解5.醚(1)从醇去水(2)威廉森合成法6.酚的合成(1)从芳卤衍生物(2)从芳磺酸(3)重氮盐水解7.醛酮(1).醇的氧化和脱氢(2).炔烃的水合R-CH2OH R-CH2XOHR-O-RR-O-R1RXRONa OHNO2NO2ClNO2NO2SO3Na OHNH2OHR-C-R'OHHR-C-R'OR-C C-R R-C-CH2RO(3).同碳二卤化合物水解CH 3OCX 2CH 3(4).傅-克酰基化反应(5).芳烃侧链的氧化(6).β-二羰基化合物8.醌(1)二元酚氧化(2).苯胺氧化9.羧酸及其衍生物和取代酸R(Ar)OR(Ar)COClCHOCH 3OHOHOOOO NH 2CH 3O CH 2R CH 3O CH 2O OC 2H 5RXCH 3O CHR 1R 2CH 3OCH 2OOC 2H 5R 1XR 2X一、酸(1).从伯醇或醛制备(2).从烃氧化(3).从格利雅试剂制备(4).腈水解(5).苯甲酸制备6.β-二羰基化合物二、羟基酸(1).从羟(基)腈水解R C O HR-CH 2OH R C OOHCOOHRR-MgX R-COOH CO2R-CN R-COOH CH 3CCl3COOH RCHO HCN R C COOHOHHHO O CH 2R C 2H 5O O CH 2O OC 2H 5RX O H O CHR 1R 2C 2H 5O O CH 2O OC2H5R 1X R 2X(2).从卤代酸水解(3).雷福尔马茨基反应ZnBrCH 2COOC 2H 5R-CHORCHCH 2COOHOH9. 含氮化合物一、硝基化合物 (1)芳烃和硝酸反应:二、胺类化合物(1).从硝基化合物还原(2).氨的烷基化(3).腈和酰胺的还原(4).醛酮的还原胺化(5).霍夫曼酰胺降级反应(6).盖布瑞尔合成法Cl-CH 2COOHCH 2-COOHOHNO 2NO2NH 2RNH 2RXR 2NHR-CNR-CH 2NH 2R-CH 2-NH-R 1R-CHONH 2-R 1R 1CONH 2RNH 2NHORNH 2RX。
有机化学-第三章不饱和烃:烯烃和炔烃

a
18
分子的结构包括分子的构造、构型和构象。
同分异构
构造异构
碳架异构 官能团位次异构 官能团异构
互变异构
立体异构
构型异构
顺反异构 对映异构
构象异构
a
19
当两个双键碳原子均连接不同的原子或基团时,即产 生顺反异构现象。如下列三种形式的烯烃都有顺反异构 体,而其它形式的烯烃则没有顺反异构体。
a
20
3.3 烯烃和炔烃的命名
构 型 异 构 体 : ( I) 和 ( Ⅱ ) 是 由 于 构 型 不 同 而 产 生 的 异 构 体 , 称 为 构 型 异 构 体 (configurational isomers)。构型异构体具有不同的物理性质。
a
17
顺反异构体:像(I)和(Ⅱ)这种构型异构体通常用顺、反 来区别,称为顺反异构体(cis and trans ismers),也称几 何异构体(geometric ismers)。
对于碳原子数相同的烯烃顺反异构体,顺式异构 体的沸点比反式异构体略高,而熔点则是反式异构体 比顺式异构体略高。
a
44
与烷烃相似,折射率也可用于液态烯烃和炔烃的鉴 定和纯度的检验。在分子体系中,由于电子越容易极化, 折射率越高,因此,烯烃和炔烃的折射率一般比烷烃大。
a
45
3.5 烯烃和炔烃的化学性质
不饱和链烃分子中同时含有碳碳双键和三键的化合物 称为烯炔。在系统命名法中,选择含有双键和三键在内的 最长碳链作为主链,一般称为“某烯炔”(“烯”在前、 “炔”在后),碳链的编号遵循“最低系列”原则,使双 键、三键具有尽可能低的位次号,其它与烯烃和炔烃命名 法相似。
a
37
但主链编号若双键、三键处于相同的位次供选择时,优 先给双键以最低编号。例如:
有机化学农科习题答案
习题2
(4)可有物种一溴代产物: CH3CHCH2CH2CH3
CH3
8.用化学方法区别下列各组化合物: (1)丙烷和环丙烷:丙烷 溴水 无现象 褪色 环丙烷 (2)环戊烷和1,2-二甲基环丙烷: 环戊烷 溴水 无现象 开环,褪色 1,2-二甲基环丙烷 9.用纽曼投影式表示1-氯丙烷绕C1-C2旋转的四种代表 性构象,并比较其稳定性。
(8)二环[4,4,0] 癸烷:
习题2
3.下列化合物的系统命名如有错误请改正。 (1) C2H5 2-乙基丁烷;3-甲基戊烷。 CH3CHCH2CH3 (2) (CH3)3CCH2CH2CH3 1,1,1-三甲基丁烷;2,2-二甲基戊烷。 (3) CH3CHCH2CH2CH3 2-异丙基戊烷;2,3-二甲基己烷。 CHCH3 CH3 (4) CH3 CH3CH2CCH2CH3 3-二甲基戊烷;3,3-二甲基戊烷。 CH3 (5) CH3 CH2C-CH2CHCH2CH3 2,2,3-三甲基己烷; 2,2,4-三甲基己烷。 CH CH 3 3 习题2
Cl
4.经元素分析,某化合物的实验式为CH,分子量测定 得78,请写出该化合物的分子式。 解:实验式量为13;则可得到分子式与实验式之比: 78/13=6。 因此,得到该化合物的分子式为:C6H6。 5.指出下列化合物哪些可以通过氢键缔合?那些虽不能 缔合,但能与水形成氢键?哪些既不能缔合又不能与水 形成氢键? (1)、(5)、(8)属于1;(2)、(3)、(7)属于2;(4)、(6)属于3
习题1
习题1
6.比较下列各组化合物的沸点高低(不查表)。 (1)C7H16<C8H18;(2)C2H5Cl<C2H5Br; (3)C6H5-CH2CH3<C6H5-CHO;(4)CH3OCH3<CH3CH2OH; (5)CH3CH2CH2CH2CH2CH3>(CH3)2CHCH(CH3)CH2CH3。 7.比较下列各组化合物的水溶性大小。 (1)C2H5OH>C6H5OH;(2)C4H9OH>C4H9Cl; (3)CH3OCH3>CH3CH3;(4)C17H35COOH<C17H35COO+Na-; (5)C6H6(OH)6>C6H11OH。 8.CH2=CH2+H2 Ni CH3-CH3;Δ H=? 解:根据C=Cπ键和H-H键的断裂所需能量与生成两个C-H 键所释放出的能量进行计算。 9.指出下列酸碱反应中的共轭酸碱对,说明每个反应的 平衡方向。 (1) CH3COOH+NaHCO3=CH3COONa+H2CO3;→向右 A1 B2 B1 A2 (2) CH3COOH+H2O=CH3COO-+H3O;→向右 A1 B2 B1 A2
大学有机化学二课后题答案

第二章 饱和脂肪烃2.1 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
a.CH 3(CH 2)3CH(CH 2)3CH 3C(CH 3)22CH(CH 3)2 b.C H C H CH H C H HC H CHHc.CH 322CH 3)2CH 23d.CH 3CH 2CHCH 2CH 3CHCH CH 2CH 2CH 3CH 3CH 3e.C CH 3H 3C CH 3Hf.(CH 3)4Cg.CH 3CHCH 2CH 32H 5h.(CH 3)2CHCH 2CH 2CH(C 2H 5)21。
答案:a. 2,4,4-三甲基-5-正丁基壬烷 5-butyl -2,4,4-trimethylnonane b. 正己 烷 hexane c. 3,3-二乙基戊烷 3,3-diethylpentane d. 3-甲基-5-异丙基辛烷 5-isopropyl -3-methyloctane e. 2-甲基丙烷(异丁烷)2-methylpropane (iso-butane) f. 2,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane (neopentane) g. 3-甲基戊烷 3-methylpentane h. 2-甲基-5-乙基庚烷 5-ethyl -2-methylheptane 2.2 下列各结构式共代表几种化合物?用系统命名法命名。
a.CH 3CHCH 32CH3CH 3CH 3 b.CH 3CH3CH 2CHCH 3CH CH 3CH 3c.CH 3CH 3CH CH 3CH 3CH CH 3CH 3d.CH 3CHCH 2CHCH 3CH 3CH H 3CCH 3e.CH 3CH CH CH 2CH CH 3CH 333f.CH 3CH CH 3CH CH3CH 3CHCH 33答案:a =b = d = e 为2,3,5-三甲基己烷c = f为2,3,4,5-四甲基己烷2.3 写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
有机化学不饱和脂肪烃
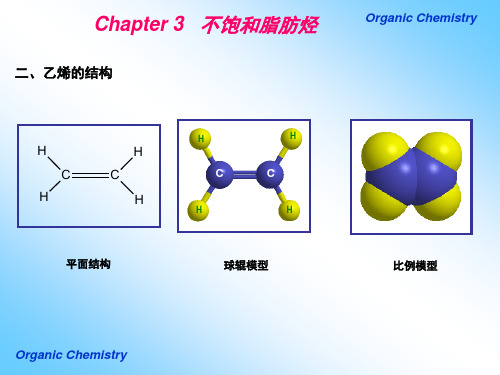
的 sp2杂化轨道。三个sp2 杂化轨道的轴在一个平面上,键角
120°,剩余的一个 p 轨道保持原状,垂直于sp2 杂化轨道平面
2p — — — 2p — — —
能
量 2s —
2s —
1s —
1s —
基态
激发态
—
———
sp2杂化态
Organic Chemistry
a C
b
a C
b
a C
b
a C
d
a C
b
d C
e
a C
a
b C
d
存在几何异构现象
Organic Chemistry
无几何异构现象
Chapter 3 不饱和脂肪烃
Organic Chemistry
④ 顺反异构的表示: 当两个双键碳上没有共同基团时,以顺反表示构型有困难,则用 Z(同)、E(对)来表示,即分别将双键碳原子上的两个原子或 基团按次序规则定出较优基团,如果较优基团在同侧,则以“ Z ” 表示;在异侧则以“ E ”表示
3
H
H3C1 C
2
H
Cl
C
2
C1 H3
(Z)—2—氯—2—戊烯
H
C
4
C
3
H
C6 H3 C
5
H
(2Z,4E)—2,4—己二烯
Organic Chemistry
Chapter 3 不饱和脂肪烃
⑤ 顺反异构体的数目
Organic Chemistry
Organic Chemistry
Chapter 3 不饱和脂肪烃
Chapter 3 不饱和脂肪烃
烃基饱和和不饱和

烃基饱和和不饱和
烃基饱和和不饱和是有机化学中的两个常见概念。
烃是指仅由碳氢元素构成的化合物,其中碳氢键是主要的键类型。
烃可以分为两类:饱和烃和不饱和烃。
饱和烃,也称为脂肪烃,是指分子中所有碳原子都与最大数量的氢原子相连。
这意味着它们没有任何双键或环状结构。
最常见的饱和烃是烷烃,其中所有碳原子都是以单键链接的。
例如,甲烷(CH4)、乙烷(C2H6)和丙烷(C3H8)都是饱和烃。
饱和烃通常是液体或固体,在常温下很少存在气态。
不饱和烃是指分子中存在一个或多个碳-碳双键或环状结构。
不饱和烃分为两类:烯烃和炔烃。
烯烃是指分子中至少有一个碳-碳双键,而炔烃则是指分子中至少有一个碳-碳三键。
例如,乙烯(C2H4)和丙烯(C3H6)是烯烃,而乙炔(C2H2)是炔烃。
不饱和烃通常是气态,在常温下很少存在液态或固态。
在化学反应中,烃基的饱和或不饱和性质会对反应的类型和速率产生影响。
例如,饱和烃更难被氧化,因此烷烃的燃烧反应需要更高的温度和氧气浓度。
另一方面,不饱和烃的双键或三键更容易参与化学反应,如加成反应和聚合反应。
总之,烃基的饱和和不饱和性质对于有机化学的研究和实际应用都具有重要意义。
了解这些概念可以帮助我们更好地理解烃化合物的性质和反应行为。
- 1 -。
脂肪烃基化学式

脂肪烃基化学式
脂肪烃是一类重要的有机化合物,由碳和氢元素组成,具有一定的结构特征和化学性质。
脂肪烃可以分为饱和脂肪烃和不饱和脂肪烃两大类。
饱和脂肪烃的化学式一般为CnH2n+2,其中n为大于等于1的整数。
饱和脂肪烃中的碳原子通过单键连接,每个碳原子周围都被饱和地包围着氢原子。
这种结构使得饱和脂肪烃具有较高的稳定性和惰性,不易与其他物质发生反应。
常见的饱和脂肪烃有甲烷、乙烷、丙烷等。
不饱和脂肪烃的化学式一般为CnH2n,其中n为大于等于2的整数。
不饱和脂肪烃中的碳原子之间存在双键或者三键连接,使得分子结构具有较大的活性。
不饱和脂肪烃可以进一步分为单不饱和脂肪烃和多不饱和脂肪烃两类。
单不饱和脂肪烃中只有一个碳碳双键,如乙烯;而多不饱和脂肪烃中则存在多个碳碳双键或者三键,如丙烯酸。
脂肪烃在自然界中广泛存在,是很多生物体的主要组成部分。
比如,动物脂肪中主要含有饱和脂肪烃,而植物脂肪中则主要含有不饱和脂肪烃。
脂肪烃在生物体中具有重要的生理功能,既能提供能量,又能作为体内重要物质的合成原料。
脂肪烃还具有广泛的应用价值。
饱和脂肪烃常用作燃料或润滑剂,
如石油和天然气中的烷烃类化合物。
不饱和脂肪烃则常用于化工领域,如合成树脂、塑料和橡胶等。
此外,脂肪烃还可以用于制备表面活性剂、染料和医药中间体等。
脂肪烃的化学式揭示了其分子结构和元素组成,但真正了解脂肪烃的性质和应用需要深入研究和实践。
通过不断的科学探索和创新,人类可以更好地利用脂肪烃这一宝贵的化学资源,为社会和人类的发展做出更大的贡献。
有机化学第三章不饱和脂肪烃

Br + CH2 CH CH=CH2
+ BrCH2 CH CH=CH2
BrCH2 CH
+ CH CH2
49
2、Diels-Alder反应(双烯合成反应) 共轭二烯与乙烯或取代乙烯反应生成环状化 合物:
CN + CN
D-A反应的特点: *机理:协同反应,没有中间体; *参与反应的取代烯烃双键上有吸电子基时 有利于反应;
第三章
不饱和脂肪烃(6学时)
本章要点 • 不饱和脂肪烃包括烯烃、炔烃等; • 基本反应有加成反应、氧化反应、聚合反应等; • 亲电加成反应机理; • 键上的诱导效应、共轭效应; • 共轭二烯烃的结构特征与加成反应;
1
第一节 烯烃
• 定义:含碳-碳双键的烃;属不饱和烃 • 单烯烃的通式: CnH2n
RCOOH + R/COOH RCOOH + CO2 + H2O
– 中性、碱性介质或较低温度下:控制的氧化条件,只断 开键;
RCH CHR
/
KMnO4
RCH OH
CHR/ OH
26
⑵ 臭氧化
R1 R2
R3 H
O3
R1 R2 O
O O
R3 H
O H2O R1 O R2
+
O R3 O R2
+
OH
Zn/H2O
C
杂化
5
p轨道与p轨道
重叠形成键
键:p-p
键:sp2-sp2 键的特点:1)垂直于分子平面 2)使双键无法自由旋转
6
C
C
双键碳原子绕键轴旋转将破坏键, 因此室温下不能绕键轴旋转
7
二、 命名和异构
有机习题
6. 合成下列化合物:
COOH
(1)
OH
;
O
(2)CH2 =CH2
CH3CH2 C
CH3
11
有机化学精品课程 /kech/yjhx/专业班级
学号
姓名
第九章 羧酸、羧酸衍生物和取代羧酸
1. 给下列化合物命名或根据名称写结构式:
CH3C O O
H 5C 2 C C Cl COCl ;
Cl3C CH
OH OH
(3)
(5) (Z)-乙醛肟; (6)2-丁烯醛-2,4-二硝基苯腙
( 4)
C2H5
H
H
CHO
3. 完成下列化学反应式:
(1) CHO + CH3CHO 稀NaOH 加热
CHO + HCHO
浓NaOH
(2) (3)
(CH3)3 CMgBr C2 H5CHO
1) NaBH4 2) H3O+
学号
姓名
第五章 旋光异构
1. 命名下列化合物或根据名称写出结构式:
(1)
H C2H5
CH2OH CHO H OH OH
COOH CH3
(2)
(3) (S)—2—羟基丙醛
H
2. 下列说法是否正确: (1) D 或 R 型化合物一定是右旋体,L 或 S 化合物一定是左旋体; (2) 分子中有无手性碳原子,是判断分子有无旋光性的标准; (3) 有手性的分子一定有旋光性,一定有对映体; (4) 同一物质的内消旋体和外消旋体是对映异构体。 3. 判断下列化合物相互间的关系(对映体,非对映体,或相同物) :
(1) CH2NH2 CH2NH
CH3
CH2N
CH3 CH3
有机化学第四版课后答案 精品

第一章 绪论1.1 答案:离子键化合物 共价键化合物熔沸点 高 低 溶解度 溶于强极性溶剂 溶于弱或非极性溶剂 硬度 高 低1.2 答案: NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na + , K + , Br -, Cl -离子各1mol 。
由于CH 4 与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3 答案:C+624H+11CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化HHH HC 1s 2s 2p 2p 2p y zx 2p yx yz2p zxyz2p xxyz 2sH1.4答案:a.C C H H H HCC HH HH或 b.H C H H Clc.H N HHd.H S He.H O NOO f.O C H Hg.O P OO O H H Hh.H C C HHH H HO P O O OH HH或i.H C C Hj.OS O HH OOO S O OOHH或1.5答案:b.ClCClH Hc.HBrd.HCClClCl e.H 3COHH 3COCH 3f.1.6答案:电负性 O > S , H 2O 与H 2S 相比,H 2O 有较强的偶极作用及氢键。
2.2答案:a. 2,4,4-三甲基-5-正丁基壬烷 5-butyl -2,4,4-trimethylnonaneb. 正己 烷 hexanec. 3,3-二乙基戊烷 3,3-diethylpentaned. 3-甲基-5-异丙基辛烷 5-isopropyl -3-methyloctanee. 2-甲基丙烷(异丁烷)2-methylpropane (iso-butane)f. 2,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane (neopentane)g. 3-甲基戊烷 3-methylpentaneh. 2-甲基-5-乙基庚烷 5-ethyl -2-methylheptane 2.3答案:a =b = d = e 为2,3,5-三甲基己烷c = f 为2,3,4,5-四甲基己烷 2.4答案:a.错,应为2,2-二甲基丁烷Cb. c.d.e.f.错,应为2,3,3-三甲基戊烷错,应为2,3,5-三甲基庚烷g.h.2.5答案:c > b > e > a >d 2.6答案:3 种123ClClCl2.12答案: a 是共同的 2.13答案:Br H HBrHH ABHH Br BrHHCBr H HH BrH DBr H H BrHH2.15答案:这个化合物为2.16 答案: 稳定性 c > a > b3.1答案:a. 2-乙基-1-丁烯2-ethyl-1-buteneb. 2-丙基-1-己烯2-propyl-1-hexenec. 3,5-二甲基-3-庚烯3,5-dimethyl-3-heptened. 2,5-二甲基-2-己烯2,5-dimethyl-2-hexene3.2 答案:a. b.错,应为1-丁烯 c.d.e. f.错,应为2,3-二甲基-1-戊烯g.h.错,应为2-甲基-3-乙基-2-己烯3.4答案:c , d , e ,f 有顺反异构c.C2H5CHCCH2IH( Z )-1-碘-2-戊烯( E )-1-碘-2-戊烯CC2H5CCH2IHH d.CHCCH(CH3)2H( Z )-4-甲基-2-戊烯H3CCHCHCH(CH3)2H3C( E )-4-甲基-2-戊烯e.CH3CCHCH( Z )-1,3-戊二烯HCH2CHCHCH( E )-1,3-戊二烯H3CCH2f.CH3CCHC( 2Z,4Z )-2,4-庚二烯HCH HC2H5CH3CCHCHCH C2H5H( 2Z,4E )-2,4-庚二烯CHCHCH3CCH C2H5H( 2E,4E )-2,4-庚二烯CHCHC( 2E,4Z )-2,4-庚二烯H3CCH HC2H53.11 答案:a.CH3CH2CH=CH2H2SO4CH3CH2CH CH3OSO2OHb.(CH3)2C=CHCH3HBr(CH3)2C-CH2CH3Brc.CH3CH2CH=CH2BH3H2O2OH-CH3CH2CH2CH2OHd.CH3CH2CH=CH2H2O / H+CH3CH2CH-CH3OHe.(CH3)2C=CHCH2CH3O3Zn H2O,,CH3COCH3+CH3CH2CHOf.CH2=CHCH2OHCl2 / H2O ClCH2CH-CH2OHOH1).2).1).2).3.12答案:1-己烯正己烷Br2 / CCl4or KMnO4无反应褪色正己烷1-己烯CH3CH=CHCH3CH2=CHCH2CH3或3.14答案:稳定性:CCH3H3C CH CH3CH3++>C CH3H3C CH CH3CH3>CCH3H3C CH2CH2CH3+3.15答案:C=CHCH2CH2CH2CH=CH3CH3CH+CH3CH3C-CH2CH2CH2CH2CH=CH3CH3CCH3CH3++H+H_3.16答案:or3.17答案:a. 4-甲基-2-己炔4-methyl-2-hexyneb. 2,2,7,7-四甲基-3,5-辛二炔2,2,7,7-tetramethyl-3,5-octadiyneCH Cd.c.3.19答案:a.HC CH LindlarcatH2C CH2 b.HC CHNi / H2CH3CH3c.HC CH+H2OHgSO4H2SO4CH3CHO d.HC CH+HClHgCl2CH2=CHCle.H3CC CHHgBr2HBrCH3C=CH2BrHBrCH3-CBrBrCH3f.H3CC CH+Br2CH3C=CHBrBrg.H3CC CH+H2OHgSO4H2SO4CH3COCH3+ H2LindlarcatH3CC CH+H2h.H3CC CH+HBr HgBr2CH3C=CH2Bri.CH3CH=CH2HBr(CH3)2CHBr正庚烷1,4-庚二烯1-庚炔Ag(NH 3)2+灰白色无反应1-庚炔正庚烷1,4-庚二烯Br 2 / CCl 4褪色无反应正庚烷1,4-庚二烯a.b.2-甲基戊烷2-己炔1-己炔Ag(NH 3)2+灰白色无反应1-己炔2-己炔Br 2 / CCl 4褪色无反应2-己炔2-甲基戊烷2-甲基戊烷3.21答案:a.CH 3CH 2CH 2C CHHCl (过量)CH 3CH 2CH 2CClClCH 3b.CH 3CH 2C CCH 3+KMnO 4H+CH 3CH 2COOH+CH 3COOHHgSO 4H 2SO 4c.CH 3CH 2C CCH 3+H 2OCH 3CH 2CH 2COCH 3+CH 3CH 2COCH 2CH 3d.CH 2=CHCH=CH 2+CH 2=CHCHO CHOe.CH 3CH 2C CH+HCNCH 3CH 2C=CH 2CN3.22答案:CH 3CHCH 2C CH H 3C3.23答案:AH 3CCH 2CH 2CH 2C CHBCH 3CH=CHCH=CHCH 33.24答案:CH 2=CHCH=CH 2HBrCH 3CH CH=CH 2Br+CH 3CH=CHCH 2BrCH 2=CHCH=CH 22HBrCH 3CHCH BrCH 3Br+CH 3CHCH 2BrCH 2BrCH 2=CHCH 2CH=CH 2HBr CH 3CHCH 2CH=CH 2Br CH 2=CHCH 2CH=CH 22HBrCH 3CHBrCH 2CH BrCH 3第四章 环烃4.1答案:C 5H 10 不饱和度Π=1a.环戊烷b.c.d.e.1-甲基环丁烷顺-1,2-二甲基环丙烷反-1,2-二甲基环丙烷1,1-二甲基环丙烷cyclopentane1-methylcyclobutanecis -1,2-dimethylcyclopropanetrans -1,2-dimethyllcyclopropane1,1-dimethylcyclopropanef.乙基环丙烷ethylcyclopropane4.3 答案:a. 1,1-二氯环庚烷 1,1-dichlorocycloheptaneb. 2,6-二甲基萘 2,6-dimethylnaphthalene c. 1-甲基-4-异丙基-1,4-环己二烯 1-isopropyl ―4-methyl -1,4-cyclohexadiene d. 对异丙基甲苯 p -isopropyltoluene e. 2-氯苯磺酸 2-chlorobenzenesulfonic acidf.CH 3NO 2Clg.CH 3CH 3h.2-chloro -4-nitrotoluene 2,3-dimethyl -1-phenyl -1-pentene cis -1,3-dimethylcyclopentane4.5答案:a.b.c.d.e.OOO Hor4.7答案:a.CH 3HBrCH 3Brb.+Cl 2高温Cl c.+Cl 2ClClClCl+d.CH 2CH 3+Br 2FeBr 3C 2H 5Br+BrC 2H 5e.CH(CH 3)2+Cl 2高温C(CH 3)2Clf.CH 3O 3Zn -powder ,H 2OCHOOg.CH 3H 2SO 4H 2O ,CH 3OHh.+CH 2Cl 2AlCl 3CH 2i.CH 3+HNO 3CH 3NO 2+CH 3NO 2j.+KMnO 4H +COOH k.CH=CH 2+Cl 2CH CH 2ClCl4.8答案:1.24.9答案:CH 3CH 3CH 3CH 3+Br 2FeBr 3CH 3CH 3CH 3CH 3+BrBr +Br 2FeBr 3CH 3CH 3CH 3CH 3+BrBrCH 3CH 3+Br 2FeBr 3CH 3CH 3Br4.10答案: b , d 有芳香性 4.11答案:a.A B C1,3-环己二烯苯1-己炔Ag(NH 3)2+C灰白色无反应A BBr 2 / CCl 4无反应褪色B Ab.A B环丙烷丙烯KMnO 4无反应褪色A B4.12答案:a.b.c.d.e.f.ClCOOHNHCOCH 3CH 3NO 2COCH 3OCH 34.13答案:a.Br 2FeBr 3BrNO 2HNO 3H 2SO 4Brb.HNO 3H 2SO 4NO 2Br 2FeBr 3BrO 2Nc.CH 32 Cl 2FeCl 3CH 3ClCld.CH 3+Cl 2FeCl 3CH 3Cl KMnO 4COOHCle.CH 3KMnO 4COOHCl 2FeCl 3COOHClf.HNO3H2SO4NO2CH3H3C 2Br2FeBr3BrCH3BrNO2g.Br2FeBr3CH3CH3Br KMnO4COOHBrHNO3H2SO4COOHBrNO24.14答案:可能为or or or oror or……即环辛烯及环烯双键碳上含非支链取代基的分子式为C8H14O2的各种异构体,例如以上各种异构体。
大学有机化学第三章不饱和脂肪烃

01
绿色合成
发展绿色合成方法,减少不饱和脂肪烃 合成过程中的环境污染和资源浪费,是 可持续发展的重要方向。
02
03
循环经济
通过循环利用不饱和脂肪烃,实现资 源的最大化利用,同时降低对环境的 负面影响。
跨学科研究的趋势与展望
化学与其他学科的交叉
不饱和脂肪烃的研究涉及到化学、生物学、医学、材料科学等多个学科领域,跨学科合作将有助于推动不饱和脂肪烃 的深入研究和发展。
烯烃的化学性质主要取决于碳碳双键,可以发生 加成、氧化、聚合等反应。
炔烃
01
炔烃的通式为CnH2n-2,其中含有两个碳碳三键。
02
炔烃的稳定性比烯烃更低,因为碳碳三键更容易受到亲电攻 击。
03
炔烃的化学性质与烯烃相似,但三键的反应活性更高,可以 发生加成、氧化、聚合等反应。
共轭二烯烃
01
02
03
烯烃的合成与转化
烷烃的热裂
在加热条件下,烷烃可以发生热裂反 应,生成烯烃和氢气。
醇的脱水
在酸催化下,醇可以发生脱水反应, 生成烯烃和水。
烯烃的合成与转化
• 炔烃的还原:通过还原炔烃的碳碳三键, 可以得到相应的烯烃。
烯烃的合成与转化
加氢反应
烯烃可以与氢气在催化剂的作用下发生加氢反应,生 成相应的烷烃。
烯烃的1,2-加成反应:在催化剂的作用 下,两个烯烃分子可以发生1,2-加成反 应,生成共轭二烯烃。
共轭二烯烃的转化
04 不饱和脂肪烃在工业和生 活中的应用
工业应用
01 02
塑料和合成橡胶生产
不饱和脂肪烃,如乙烯和丙烯,是塑料和合成橡胶的主要原料。它们通 过聚合反应形成高分子聚合物,广泛应用于包装、建筑材料、汽车部件 等领域。
有机化学课后答案

有机化学课后答案集团标准化工作小组 #Q8QGGQT-GX8G08Q8-GNQGJ8-MHHGN#第一章 绪论扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2CH 4 及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同为什么答案: NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na + , K + , Br -,Cl -离子各1mol 。
由于CH 4 与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
碳原子核外及氢原子核外各有几个电子它们是怎样分布的画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的画出它们的轨道形状及甲烷分子的形状。
答案:写出下列化合物的Lewis 电子式。
a. C 2H 2b. CH 3Clc. NH 3d. H 2Se. HNO 3f. HCHOg. H 3PO 4h. C 2H 6i. C 2H 2j. H 2SO 4答案:下列各化合物哪个有偶极矩画出其方向。
a. I 2b. CH 2Cl 23 e. CH 3OH f. CH 3OCH 3 答案: 1.6 根据S 与O 的电负性差别,H 2O 与H 2S 相比,哪个有较强的偶极-偶极作用力或氢键 答案:电负性 O > S , H 2O 与H 2S 相比,H 2O 有较强的偶极作用及氢键。
第二章 饱和脂肪烃2.2 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
a.CH 3(CH 2)3CH(CH 2)3CH 3C(CH 3)22CH(CH 3)2 b.C H C H C H H C HH C H H C H H H c.CH 322CH 3)2CH 23d.CH 3CH 2CH CH 2CH 3CH CH 2CH 2CH 3CH 3CH 3e.C CH 3H 3C 3H f.(CH 3)4Cg.CH 3CHCH 2CH 3C 2H 5h.(CH 3)2CHCH 2CH 2CH(C 2H 5)21。
有机化学第三章不饱和烃
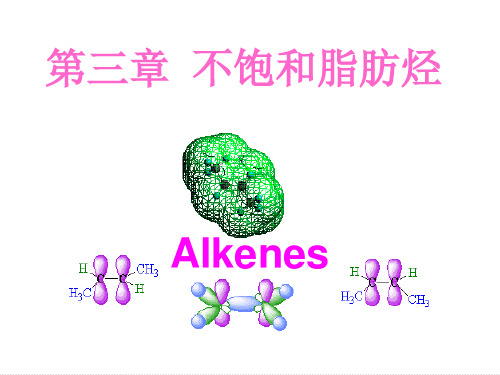
CH3
H
CC
H
CH3
反式(trans)
(顺)—2—丁烯(沸点3.7 0C)
08:38
(反)—2—丁烯(沸点0. 9 0C)
第三章 不饱和烃 16
The E, Z Designation
Z, E异构—— 根据次序规则,较 大基团在同侧为 Z–型,不同侧为 E–型
08:38
H3C
Cl
H
C2H5
Z-型
H3C
2-乙基-1-戊烯
H3C CH C CH2 H3C CH2 CH2 CH2 CH3
3-甲基-2-乙基-1-己烯
08:38
第三章 不饱和烃 10
一、 系统命名法 (续)
(2)主链编号,使双键的编号尽可能小;
12345 6
H3C CH CH2 C CH CH3
65 4 3 2 1
CH3
CH3
1
H3C
6
+ CH3—CH CH2
HX
3
2
1
CH3—CH—CH3
(Ⅰ ) (主 )
X CH3—CH2—CH2—X (Ⅱ )
马氏规则的另一表述方法:带正电的部分加到含氢较多的碳上
08:38
第三章 不饱和烃 35
原因:
1. 烷基排斥电子,H+进攻电子云密度大的碳原子,(这种由于 电子云密度分布对性质产生的影响叫电子效应)
08:38
第三章 不饱和烃 34
3. 与卤化氢加成:氢电加成,历程为:H+首先与双键中的 p电子对结合是另一碳原子形成碳正离子,碳正离子再与X-结 合成卤代烷。
CH2=CH2 + HX [CH3—+CH2] + X-
有机化学习题1(学习资料)

授课典型习题解析 第一章 绪论[例1] 解释下列术语:(1)均裂 (2)异裂 (3)活性中间体 (4)路易斯酸 (5)路易斯碱 解:(1)共价键断裂时,成键的一对电子平均分给成键的两个原子或基团,生成带有单电子的原子或基团,此共价键断裂的方式称为均裂。
(2)共价键断裂时,成键的一对电子被成键原子或基团中的一个全部占有成负离子,另一个原子或基团则缺一个电子而成正离子,此共价键断裂的方式称为异裂。
(3)在有机反应中生成的活性高、但又比活化络合物(过渡态)相对稳定的中间物种称为活性中间体,又叫反应中间体。
(4)路易斯酸:具有空轨道并具有接受电子对能力的分子或正离子。
(5)路易斯碱:至少含有一对未共用电子对,具有给予电子对能力的分子或负离子。
[例2] 排列C-H 键的极性大小次序:A .CH 3F B. CH 3Cl C. CH 3Br D. CH 3 I解:极性大小次序为: A>B>C>D 。
以上四种化合物分别为含不同卤原子的一卤代甲烷。
卤素的电负性越大, C-H 键的极性越大,其化合物的极性越大。
由于卤素的电负性大小次序为:F>Cl>Br>I ,所以,极性大小次序为: A>B>C>D 。
[例3] 下列物质中哪些是路易斯酸?哪些是路易斯碱?BF 3,NH 3,(C 2H 5)2O ,+NO 2,R -CH 2,R +CH 2,AlCl 3,F -,H 2O ,HOR解:路易斯酸:BF 3,+NO 2,R +CH 2,AlCl 3 路易斯碱:NH 3,(C 2H 5)2O ,,R -CH 2,F -H 2O 和HOR 既是路易斯酸,又是路易斯碱。
例如:在水形成的氢键中,氧原子是路易斯碱,而氢原子是路易斯酸。
醇也可形成氢键。
[例4]下列各化合物哪些属于极性溶剂?哪些属于质子性极性溶剂?A.B.C.D.E.G.H.H 2OHCO 2HCH 3OHS OCH 3H 3CF.OHCCl 3CO N(CH 3)2H解:极性溶剂为分子有极性的溶剂。
有机化学课后习题参考答案(农科)

有机化学(第二版) 赵建庄 张金桐 主编习 题 参 考 答 案第二章 饱和脂肪烃1.用系统命名法命名下列化合物,并指出(1)中碳原子的类型(1)2,4-二甲基-4-乙基己烷 (2)3-甲基戊烷(3)2,4-二甲基-3-乙基戊烷 (4)2,2,3-三甲基丁烷 (5)2,3,4-三甲基己烷 (6)2,2,5-三甲基-6-异丙基-壬烷 2.写出下列化合物的结构式,如有错误请予以更正。
(1)2,3,4-三甲基3-乙基戊烷 (2)2,3,3-三甲基丁烷 (3)2,4-二乙基-4-异丙基己烷 (4)2,4-二甲基-3-丙基戊烷 其结构式如下:CH 3CHCH 2CCH 2CH 3CH 2CH CH 2CH 3CH 3CH 3CH 3CH 3CHCH 2CH CH 3CH 3CH 3H 2CCH 3CH 3CH 3CH CHCHCH 3CH 3CH H 2CCH 2CH 3CH 3C CHCH 3CH 3CH 3CH 3⑴⑵⑶⑷(1)正确。
(2)错误。
应为:2,2,3-三甲基丁烷。
(3)错误。
应为:2,5-二甲基-3,3-二乙基庚烷。
(4)错误。
应为:2-甲基-3-异丙基己烷。
3.某烃与Cl 2反应只能生成一种一氯代物,该烃的分子式是( 3 ) (1)C 3H 8 (2)C 4H 10 (3)C 5H 12 (4)C 6H 144.将下列化合物的沸点由高到低排列成序 (2)>(4)>(3)>(5)>(1)解题思路:分子量不同的化合物,分子量越大,沸点越高,分子相同的化合物,其分子中支链越多,沸点越低。
5.下列哪对结构式表示的化合物是等同的(假定式中所表示的C-C 单键可以自由旋转)(1),(2)均等同。
解题思路:将各个结构式均用纽曼投影式表示,然后旋转某一个碳原子进行比较。
6.用纽曼投影式画出下列结构式中围绕指出键旋转所产生的典型构象,命名并指出优势构构象。
(1)BrCH 2-CH 2BrC H 3CHCH 2C CH 2CH 3CH 3CH 3H 2CCH 31。
有机化学 1-4 习题解答

答案:
3.15完成下列反应式:
答案:
3.16分子式为C6H10的化合物A,经催化氢化得2-甲基戊烷。A与硝酸银的氨溶液作用能生成灰白色沉淀。A在汞盐催化下与水作用得到 。推测A的结构式,并用反应式加简要说明表示推断过程。
答案:
3.17分子式为C6H10的A及B,均能使溴的四氯化碳溶液褪色,并且经催化氢化得到相同的产物正己烷。A可与氯化亚铜的氨溶液作用产生红棕色沉淀,而B不发生这种反应。B经臭氧化后再还原水解,得到CH3CHO及HCOCOH(乙二醛)。推断A及B的结构,并用反应式加简要说明表示推断过程。
答案:稳定性:
3.9写出下列反应的转化过程:
答案:
3.10分子式为C5H10的化合物A,与1分子氢作用得到C5H12的化合物。A在酸性溶液中与高锰酸钾作用得到一个含有4个碳原子的羧酸。A经臭氧化并还原水解,得到两种不同的醛。推测A的可能结构,用反应式加简要说明表示推断过程。
答案:
3.11命名下列化合物或写出它们的结构式:
a. 1,3-环己二烯,苯和1-己炔b.环丙烷和丙烯
答案:
4.9写出下列化合物进行一元卤代的主要产物:
答案:
4.10由苯或甲Biblioteka 及其它无机试剂制备:答案:
4.11分子式为C8H14的A,能被高锰酸钾氧化,并能使溴的四氯化碳溶液褪色,但在汞盐催化下不与稀硫酸作用。A经臭氧化,再还原水解只得到一种分子式为C8H14O2的不带支链的开链化合物。推测A的结构,并用反应式加简要说明表示推断过程。
c. 2-甲基-1,3,5-己三烯d.乙烯基乙炔
答案:
a. 4-甲基-2-己炔4-methyl-2-hexyneb. 2,2,7,7-四甲基-3,5-辛二炔2,2,7,7-tetramethyl-3,5-octadiyne
有机化学不饱和脂肪烃详解演示文稿
第一节 烯 烃
一、双键的结构 1.实验现象
① 现代物理手段测得所有原子在同一平面,每个碳原子只和
三个原子相连。键角120°
② 测键能:C—C 345.6 KJ/mol; C = C 610 KJ/mol
双键的键能不是两个单键键能之和:345.6 * 2 = 691.2
KJ/mol
R2C=CR2 > R2C=CHR >
R C
H
H C
R
R
>
C
H
R
C H
> RHC=CH2 > H2C=CH2
第25页,共89页。
总结:
◆双键碳上烷基越多越稳定 ◆反式比顺式稳定。
氢化热的大小反映烯烃的相对稳定性。 双键碳原子上的烷基越多,烯烃越稳定。
R2C=CR2>R2C=CHR>RCH=CHR>RCH=CH2>CH2=CH22-甲基
CH3
CH3 C CH2 OH Cl
不对称烯烃与极性试剂加成时,试剂中带有部分正 电荷的原子或基团总是加到带有部分负电荷的双键碳原
子上,而试剂中带有部分负电荷的原子或基团总是加到
带有部分正电荷的双键碳原子上。
第40页,共89页。
B.由碳正离子反应历程解释
按反应历程,反应的第一步要生成碳正离子。
以丙烯为例,则有两种可能:
丙烯>反-2-丁烯>顺-2-丁烯>1-丁烯。
第26页,共89页。
(二)亲电加成反应
(Electrophilic Addition Rxn)
亲电加成:亲电试剂进攻引起的加成反应为 亲电加成反应。
亲电试剂:带部分正电荷或缺电子的试剂为 亲电试剂,具有亲电子性质。
有机化学作业本答案全

CH3 Br
CH3 MgBr
CH3
CH2Br
CH2MgBr
三. 下述情况属于SN1的是( B,C,D ) ,属于SN2的是(A,E.F ).
第13页/共20页
四、按要求排列下列化合物
1、D>A>B>C 3、A>C>D>B
2、A>C>D>B 4、D>C>B>A
五. 推断结构
1、 A. H2C CH CH2Br B. H2C CH CH2 CH2 CH CH2
第8页/共20页
2、加入KMnO4/H2SO4溶液,使之褪色者为甲苯、 环己烯,不能使之褪色的为苯;在甲苯、环己烯中分
别加入Br2/CCl4溶液,能使之褪色的为环己烯、不能使 之褪色的为甲苯
七.用苯合成对硝基苯甲酸
CH3Cl AlCl 3
CH3
HNO3 H2SO4
CH3
KMnO4 H2SO4
NO2
CH3 E. CH3CHCHCH3
Br
C. H2C
CHCHCH3 CH3
CH3 F. CH3CCH2CH3
Br
1、在四种物质中分别加入Br2/CCl4溶液,能使之褪色的为苯 乙烯、苯乙炔,不能使之褪色的为乙苯、苯;在苯乙烯、苯乙炔 溶液中加入[Ag(NH3)2]+,能产生银白色沉淀者为苯乙炔;在乙 苯、苯的溶液中加入KMnO4/H2SO4溶液,使之褪色者为乙苯.
第三章 不饱和脂肪烃
一.命名或写出结构式
1. Z-3-甲基-1-氯-3-庚烯 2、顺-3-甲基-3-戊烯-1-炔
H2C CH
H
3.
CC
H
CH3
H
4.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
激发
2PX 2PY 2PZ
2S
激发态
SP2杂 化
2PZ SP2 SP2 SP2
2)炔烃
C—C σ SP—SP
C≡C
C—C π1 Py —Py
C—C π2 PZ —Pz
键长 0.120nm;键能 835KJ/mol
π 1⊥ π2
乙炔键角 1800
SP杂化
2PX 2PY 2PZ 2S 基态
激发
2PX 2PY 2PZ
CH3—CH2—C=CH2
2—甲基—1—丁烯 CH3
CH3—CH—CH =CH2 CH3
3—甲基—1—丁烯
2 顺反异构体
若d>c>b>a,当双键C1 上的较优基团与C2上的 较优基团处于碳碳双键 同侧时(以双键方向为 中心轴),这种结构称 为Z式;反之,较优基 团处于碳碳双键异侧的 称为E式。
a C
80%
马氏规律:不对称烯烃与卤化氢加成时,试
剂中的氢原子(或带正电荷部分)主要是加到
含氢较多的烯碳原子上,试剂中的卤原子(或
带负电荷的部分)加到含氢较少的烯碳上。
HI>HBr>HCl>HF
过氧化物条件下与HBr的反马氏加成
在过氧化物(如H2O2、R—O—O—R)存在下, 不对称烯烃与HBr加成不遵守马氏规则。
第 三 章 烯烃、炔烃、二烯烃
• 烯烃、炔烃 • 烯烃、炔烃的结构 • 同分异构、命名 • 性质 • 二烯烃 • 概念及分类、命名、结构 • 性质 • 萜类化合物
第一节 烯、炔烃
一 烯、炔烃的结构
1)烯烃
C=C SP2杂化
C—C σ SP2—SP2 C—C π PZ —Pz
sp2杂化
2PX 2PY 2PZ 2S 基态
C H 3 C H 2C H 3
C H 3C C C HC H 2C HC H C H C H 3
6-甲基-4-乙基-2-壬烯-7-炔
CH3—CH=CH—C ≡CH 3-戊烯-1-炔
2)对于环烯 以双键的位置为最小,若取代基处于第1、2 位,照顾较小取代基为最小编号。
CH3
3 2
1
3-甲基环己烯
2 C2H5 1 CH3
b
a C
b
c C
d
d C
c
“Z、E”和“顺反”标记的关系——没有必然联 系
Z、E法:适用于所有的顺反异构体(较优基团)
顺反法:适用于两个双键碳上连有相同的基团
Cl
H
C=C
顺- 2-氯-2-丁烯
CH3
CH3 E- 2-氯-2-丁烯
Cl
H
C=C
Z-1-氯-1-溴- 1-丁烯
Br
CH2 CH3
3 烯炔的命名
(一)命名的步骤
1)选含C =C或C ≡ C的最长碳键作为主链,母体名 称为相应的某烯、炔。
2)从距离不饱和键的最近一端进行编号,根据它们所 处的位置称为某烯或某炔。 3) 如有顺反异构,在名称前加上顺或反, Z或E。 4)正确书写
(二)常用的不饱和烃基
CH2 =CH— CH3CH =CH—
乙烯基
Байду номын сангаас
+ C H 3C H C H 2 H B r有 过 日 氧 光 化 或 物 C H 3 C H 2C H 2 B r
+ C H 3 C HC H 2 H B r
C H 3 C HC H 3 B r
1)链的引发 R O O R
2 R O H B r R O H B r
2)链的增长
R C H C H 2 B r
四 烯烃和炔烃化学性质
(一 )亲电加成反应
1 卤化
CC
X2
XX
溴的四氯化碳
CC
溶液或溴水
XX
CC
X2
CC
XX
C H 2 = C H C H 2CC H B r2 C H 2 C HC H 2CC H B r B r
2与卤化氢反应
CH3CH CHCH3+HBr
CH3CH CHCH3 H Br
20%
C3HC2HCH C2H +B2r H2O C3HC2HCH C2H
OH Br
C3HC2HCH C2H +HOBr
C3HC2HCH C2H OH Br
5、与水加成(H+)
C H 3 C HC H 2 H 2 OH C H 3 C HC H 3
HC
CH
H2OHgSO4 H2SO4
CH2
O H
CH
CH3
R C H C H 2B r R C H 2B rC H 2
H B r R C H 2C H 2B r B r R C H 2B rC H 3
主
次
3)链的终止
B r B r
B r2
2RCHCH2Br
RCHCH2Br
RCHCH2Br
RCHCH2Br Br
RCH CH2Br
Br
3、与硫酸的加成
4、与HOX加成
CH
OH
O
烯醇式与酮式的互变异构
O
C C OH
CC
H
C CH+ H2O HH2gSSO44O
O
C CH 3
6 催化氢化
CH2
CH2+
H2
Ni T.P
CH CH+ H2 TN.iPCH2
CH3CH3 Ni
CH2 T.P
OH
CH
CH2
CH3CH3
(二)亲电加成反应历程
1、常见的亲电试剂: H+、X+ 、NO2+ 、R+ 、ZnCl2、FeCl3 常见的亲核试剂:
2S
激发态
SP杂化
SP SP
2Py2PZ
二、烯、炔的异构现象及命名 1.构造异构、官能团位置异构 戊炔 HC≡C—CH2—CH2CH3
HC≡C—CH—CH3 CH3
HC—C≡C—CH2— CH3
CH3—CH2—CH=CH2 1—丁烯 CH3—CH=CH—CH3 2—丁烯 CH3—CH2—CH2—CH=CH2 1—戊烯
C
CH3
CH3
(2E,4Z)-3-甲基-2,4-己二烯
(三)特殊的烯烃命名
• 1)烯炔命名 • 选含“C=C” 和“C≡C”最长链为主链,若分子中
“C=C” 和“C≡C”的位置对称,以双键编号最小, 以炔为母体;若“C=C” 和“C≡C”的位置不对称, 从官能团距链端最近一端开始编号。
CH2=CH—C≡CH 1-丁烯-3-炔
丙烯基(烯碳上去掉一个H)
CH2 =CH—CH2—
烯丙基
CH3 CH3 CH3CH CH CH C CH3
CH2CH3
4,5,5—三甲基—2—庚烯
E-3-甲基-4-异丙基-3-庚烯
H
C Br
CH3
C Cl
Z—2—氯—1—溴丙烯
Z—1-bromo-2-chloropropene
H
H
H C
CH3
CC
1-甲基-2-乙基环己烯
CH3
3-甲基-5-氯环戊烯
Cl
3)炔烃的衍生物命名 乙烯基乙炔 CH2=CH—C ≡CH
CH3 CH3—C—2 C≡CH1
CH3 叔丁基乙炔
CH3CHC≡CH
CH3 异丙基乙炔 3-甲基-1-丁炔
三 烯烃和炔烃物理性质
物理性质与烷烃相似
在烯烃的顺反构体中,顺式的沸点比反式的大,而 反式的熔点比顺式的大。(?) 烯烃(炔烃)同分异构体的沸点比较。
