2016年最新乳腺癌辅助化疗诊断及治疗标准流程
乳腺癌的新辅助化疗与手术效果评估

乳腺癌的新辅助化疗与手术效果评估乳腺癌是女性常见的恶性肿瘤之一,其治疗方法多样化,包括手术切除、放射治疗、化疗等。
随着医学科技的进步,新辅助化疗成为乳腺癌治疗中的重要一环。
本文将探讨乳腺癌的新辅助化疗以及手术治疗的效果评估。
一、乳腺癌的新辅助化疗介绍新辅助化疗是指在手术治疗之前,通过化疗药物来缩小肿瘤的体积,减少转移的风险,提高手术的可行性和疗效。
该治疗方法可以减少手术切除的范围,降低乳房切除及外科手术的风险,同时在术前明确种植和淋巴结转移情况。
此外,新辅助化疗有助于个体化治疗方案的制定,提高治疗的准确性和针对性。
二、乳腺癌的新辅助化疗药物针对乳腺癌的新辅助化疗方案包括多种不同种类的药物,主要包括化疗药物、靶向治疗和内分泌治疗。
化疗药物如环磷酰胺、多柔比星等常用于减少肿瘤体积,抑制癌细胞增殖。
靶向治疗药物如曲妥珠单抗、赫赛汀等则通过针对癌细胞上的特定靶点,阻断其生长和扩散。
对于雌激素受体阳性的乳腺癌,内分泌治疗药物如阿曲莫司汀可有效抑制肿瘤的生长。
三、乳腺癌的新辅助化疗与手术的协同作用新辅助化疗可以有效地缩小肿瘤体积,降低术中出血量,提高手术的切除率和局部控制效果。
化疗药物可以预处理乳腺癌细胞和微转移灶,减少淋巴结转移的风险,提高乳腺癌的根治性手术成功率。
此外,新辅助化疗还可以为手术提供更准确的术前分期,帮助医生制定更合理的手术方案。
四、乳腺癌的手术效果评估手术治疗是乳腺癌的首选治疗方法,包括乳腺切除术、乳房保留手术和腋窝淋巴结清扫术等。
通过手术可以彻底切除肿瘤组织,提供更详细的病理学信息。
手术后,医生可以对术中病理学结果进行评估,确定患者的肿瘤分期和分子分型,从而为后续治疗方案的制定提供有效依据。
此外,手术后的生存率和无瘤生存率也是评估手术效果的重要指标。
五、乳腺癌的新辅助化疗与手术效果评估方法评估乳腺癌新辅助化疗与手术的效果可以通过多种方法,如放射学影像学评估、病理学评估、化疗反应评估和术后远期随访等。
乳腺癌化疗操作规程

乳腺癌化疗操作规程乳腺癌化疗是目前治疗乳腺癌的重要手段之一,通过使用化学药物来杀死癌细胞或抑制其生长和分裂。
下面是针对乳腺癌化疗的操作规程。
一、化疗前准备1. 检查患者的基本情况,包括年龄、身体状况、乳腺癌的分期等。
2. 给予患者必要的解释和教育,让患者了解化疗的目的、疗程和可能出现的不良反应。
3. 完善患者的体格检查、血液学、肝功能、肾功能等常规检查。
4. 评估患者的心理状态,提供必要的心理支持。
二、化疗药物的选择1. 根据患者的病情和分期,以及可能的预后情况,考虑选择适当的化疗药物。
2. 考虑患者的年龄、身体状况、生殖功能等因素,尽量减少毒副作用。
3. 结合药物的使用方式和疗程,制定化疗方案。
三、给药途径和剂量1. 综合考虑药物的药代动力学特点和患者的生理状况,选择合适的给药途径,包括口服、静脉注射、皮下注射等。
2. 根据患者情况和化疗药物的推荐剂量,确定剂量和给药频次。
3. 仔细计算药物的总量,避免出现过量或不足的情况。
四、化疗监测和评价1. 在化疗开始前,评估患者的病情和身体状况,包括肿瘤大小、淋巴结转移情况等。
2. 在化疗期间,定期检查患者的血常规、肝功能、肾功能和心脏功能等指标,及时发现并处理不良反应。
3. 根据化疗效果和不良反应的程度,及时调整药物剂量和给药方案。
4. 定期进行影像学检查,如超声检查、乳腺核磁共振或CT扫描,评估肿瘤的缩小程度。
五、不良反应的处理1. 根据不同化疗药物的不良反应特点,预先做好不良反应的预防和处理工作。
2. 如恶心、呕吐、腹泻等胃肠道反应,可以给予相应的抗恶心药物、止泻药物等。
3. 如骨髓抑制引起的血细胞减少,可以监测血象,及时采取相应的处理措施,如输注血小板、使用白细胞生长因子等。
六、化疗后的护理1. 化疗结束后,对患者进行综合评估,包括疗效评价、药物副作用的监测和处理等。
2. 监测患者的复发情况,定期进行影像学检查和肿瘤标志物的检测。
3. 提供必要的心理支持和康复指导,帮助患者应对化疗的不良反应和生活质量的改善。
乳腺癌辅助化疗方案

乳腺癌辅助化疗方案一、研究背景乳腺癌是女性常见的恶性肿瘤之一,辅助化疗作为乳腺癌综合治疗的重要组成部分,可以显著提高患者的生存率和生活质量。
本文档旨在介绍乳腺癌辅助化疗的常用方案及相关注意事项,供参考使用。
二、辅助化疗适应症⒈早期乳腺癌患者:根据肿瘤分期、分子分型、患者年龄、全身情况等因素,确定是否需要进行辅助化疗,并选择合适的化疗方案。
⒉晚期乳腺癌患者:辅助化疗可用于提高手术效果、缩小肿瘤体积、减少转移风险、控制病情等。
三、化疗方案选择⒈化疗药物选择:根据患者具体情况,可选择单药或联合应用多种化疗药物,如顺铂、环磷酰胺、氟尿嘧啶等。
⒉方案剂量和周期:根据患者的耐受性和治疗效果,调整化疗剂量和给药周期,一般为3-4周为一个周期,连续进行若干个周期。
⒊联合其他治疗:辅助化疗可与手术、放疗、靶向治疗等进行联合应用,以提高治疗效果。
四、化疗的不良反应及处理⒈恶心、呕吐:可使用有效的止吐药物,如多潘立酮。
⒉骨髓抑制:定期监测血常规指标,必要时进行升支或减药。
⒊头发脱落:建议患者采取合适的头皮护理措施,如低温头皮敷料等。
⒋其他不良反应:根据患者的具体情况,针对性给予相应的支持性治疗。
五、注意事项⒈疗程监测:定期进行影像学检查和肿瘤标志物检测,评估治疗效果。
⒉患者体力恢复:化疗结束后应进行适当的康复训练,提高患者的体力和生活质量。
⒊心理支持:提供积极的心理支持和鼓励,帮助患者积极面对治疗和康复过程。
【附件】:⒈辅助化疗药物清单。
⒉化疗方案详细信息表。
⒊相关疗效评估指标解释。
⒋不良反应处理指南。
【法律名词及注释】:⒈辅助化疗:指在手术、放疗等综合治疗之前或之后应用的化学药物治疗,既可控制原发病灶,又可消灭肿瘤微转移灶的治疗方式。
⒉综合治疗:指根据肿瘤性质和患者具体情况,采用手术、化疗、放疗、靶向治疗等多种治疗手段进行综合治疗的方法。
⒊靶向治疗:指通过靶向特定分子、信号通路等来干预肿瘤生长和发展的治疗方式。
⒋转移风险:指乳腺癌在局部治疗后可能出现的淋巴结转移或远处转移的概率。
乳腺癌化疗方案ec t

简介乳腺癌是女性最常见的恶性肿瘤之一,也可罹患于男性。
乳腺癌的治疗方法多种多样,其中化疗是常用的治疗手段之一。
EC-T方案是一种常用于乳腺癌患者的化疗方案,本文将详细介绍EC-T方案的治疗流程、药物选择、副作用管理以及疗效评估等方面的内容。
一、EC-T方案治疗流程乳腺癌的治疗流程是一个系统化的过程,包括化疗、手术、放疗、内分泌治疗等多个阶段。
EC-T方案通常用于乳腺癌手术前的化疗,其治疗流程如下:1.第一周期化疗:使用Epirubicin和Cyclophosphamide两种化疗药物进行联合化疗。
通常每21天为一个周期,每个周期内患者需要接受一次静脉注射。
2.第二周期化疗:在第一个周期化疗后,患者会进行T(Docetaxel)单药治疗。
同样,每21天为一个周期,每个周期需要进行一次静脉注射。
3.疗程的重复:EC-T方案的化疗周期需要重复多个疗程,具体疗程次数的确定需要根据患者的具体情况和医生的建议。
4.手术治疗:在完成EC-T方案的化疗后,患者通常会接受手术治疗,包括乳房保留手术或乳房切除手术。
二、EC-T方案药物选择EC-T方案主要使用以下几种化疗药物进行治疗:1.Epirubicin:属于蒽环类抗肿瘤药物,作用于肿瘤细胞DNA,抑制肿瘤细胞的分裂和增殖。
2.Cyclophosphamide:一种碱化剂,能够通过干扰DNA的正常复制过程,造成肿瘤细胞的死亡。
3.Docetaxel:属于紫杉醇类抗肿瘤药物,通过干扰细胞的微管组织结构,阻断细胞有丝分裂的进行,从而抑制肿瘤细胞的增殖。
这些药物在EC-T方案中的组合使用,可以充分发挥它们的抗肿瘤作用,提高治疗效果。
三、EC-T方案的副作用管理化疗是一种强有力的治疗手段,但同时也会伴随一系列的副作用。
针对EC-T 方案的副作用,我们可以采取以下措施进行管理:1.恶心和呕吐:化疗会刺激患者的胃肠道,造成恶心和呕吐。
医生可以根据患者的具体情况,开具相关药物进行抗恶心和呕吐的治疗。
乳腺癌辅助化疗方案

乳腺癌辅助化疗方案乳腺癌辅助化疗方案1、介绍乳腺癌是女性最常见的恶性肿瘤之一,在早期发现并进行合适的治疗可以提高患者的生存率。
乳腺癌的辅助化疗方案是目前一种常用的治疗方法,可有效减少肿瘤复发和转移的风险。
2、检查和评估2.1 乳腺癌分期乳腺癌的分期是根据肿瘤的大小、淋巴结是否受累以及是否存在远处转移来决定的。
常用的分期系统包括TNM分期系统和分子分型系统。
2.2 评估患者的全身状况在确定辅助化疗方案之前,需要评估患者的身体状况、心脏功能、肝肾功能以及其他重要的生理指标。
3、辅助化疗药物3.1 化疗药物辅助化疗常用的药物包括阿霉素、环磷酰胺、氟尿嘧啶等。
根据患者的具体情况,可以选择单药或联合药物治疗。
3.2 靶向治疗药物针对乳腺癌特定的分子靶点,靶向治疗药物可以提高治疗效果,并减少副作用。
常用的靶向治疗药物包括曲妥珠单抗、帕博利珠单抗等。
4、辅助化疗方案4.1 理想化方案理想化的辅助化疗方案是根据患者的病理类型、分期和身体状况来定制的。
通常包括多个疗程,每个疗程之间有一定的间隔时间。
4.2 方案示例(示例:AC-T方案)第1疗程:A环磷酰胺+C多柔比星第2疗程:C多柔比星第3疗程:T紫杉醇第4疗程:T紫杉醇4.3 副作用管理辅助化疗会伴随一系列的副作用,包括恶心、呕吐、脱发等。
在治疗过程中,需要对副作用进行有效管理,以提高患者的生活质量。
5、随访和监测辅助化疗结束后,需要对患者进行定期的随访和监测,以及进一步评估治疗效果。
附件:1、相关研究资料和临床试验报告2、医疗器械使用说明书3、患者自我管理手册法律名词及注释:1、辅助化疗:在手术、放疗等治疗之前或之后进行的化疗,用于减少肿瘤复发和转移的风险。
2、肿瘤分期:根据肿瘤的大小、淋巴结是否受累以及是否存在远处转移来划分肿瘤的严重程度。
3、靶向治疗:针对肿瘤特定的分子靶点进行的治疗,可以提高治疗效果并减少副作用。
乳腺癌辅助化疗方案

乳腺癌辅助化疗方案1、TAC方案多西她赛 75mg /M2 d1阿霉素50 /M2 d1环磷酰胺 500 /M2 d1 共6个周期,21天为1周期多西她赛预处理:地塞米松8mg Bid连续3天(-1,1,2) 适用于高度复发危险得病例。
该方案中多柔比星得不良反应主要为心脏毒性,心肌毒性与剂量累计密切相关,辅酶Q10,维生素C,维生素E可清除自由基,可能会降低心脏毒性。
该方案得剂量限制性毒性就是造血系统毒性,白细胞,尤其就是粒细胞下降,易引起发热性粒细胞下降与感染、而且粒细胞下降发生早,最早发生在用药后3~4天,降至最低点得时间就是第8天,通常再降至最低点1周左右能完全恢复、,预防使用G-CSF可有效地预防严重得骨髓抑制得发生。
如出现发热性粒细胞下降应注意以下几点:拍摄胸片,查血常规;尽量避免有创操作,仔细检查并尽可能发现感染病灶及感染;常规进行血、尿培养、中心静脉置管或可疑感染部位得培养;经验性应用广谱抗生素,根据药敏试验结果更换抗生素等。
本方案致吐性为中等程度,应用5-HT3拮抗剂。
2、AC—P方案阿霉素 60mg/M2 d1第1-4周期环磷酰胺600mg /M2 d1 第1—4周期紫杉醇 175mg /M2d1 第5-8周期 21天为1周期紫杉醇预处理:地塞米松20mg 口服(用药前12h、前6h)苯海拉明40mg肌注、西咪替丁400mg静脉注射(用药前30min) 适用于高度复发危险得病例注意事项:紫杉醇用药需测量血压(化疗前30min、0min、后15min、后30min、后60min、后2h、后3h),静滴时间:3h; 紫杉醇在滴注得最初几分钟内,有可能发生过敏反应、如发生过敏反应症状较轻微,如脸红或局部皮肤反应,则不需终止治疗。
如果发生严重过敏反应,如血压下降超过20mmHg、支气管痉挛或全身皮疹或红斑,则需立即停止滴注,并进行对症治疗。
紫杉醇用药2-3天后会感到关节与肌肉疼痛,在给予G—CSF治疗得病人肌肉疼痛会加重。
乳腺癌辅助化疗方案

乳腺癌辅助化疗方案【乳腺癌辅助化疗方案】一、背景介绍:乳腺癌是一种常见的恶性肿瘤,在女性中发病率较高。
辅助化疗是乳腺癌治疗中的一种重要手段,可在手术前或手术后减小肿瘤体积,降低进一步转移的风险。
本文档旨在提供乳腺癌辅助化疗的方案,供参考使用。
二、辅助化疗的指征:1.早期乳腺癌患者,手术后病理显示淋巴结转移的情况;2.大型肿瘤(直径大于5cm)患者,手术前辅助化疗可减小肿瘤体积,有助于手术的进行;3.年轻患者、高分化程度差、高HR(雌激素受体)阳性的乳腺癌患者,辅助化疗可减小肿瘤复发的风险;4.患者存在HER2(人表皮生长因子受体-2)过表达,辅助化疗可降低复发风险。
三、辅助化疗的药物选择:1.化疗药物:a.蒽环类药物:如阿霉素;b.铂类药物:如顺铂;c.抗代谢药物:如环磷酰胺;d.紫杉醇类药物:如紫杉醇;e.氟尿嘧啶类药物:如卡培他滨。
2.靶向治疗药物:a.靶向HER2的药物:如曲妥珠单抗;b.靶向HR的药物:如阿那曲唑。
四、辅助化疗方案的制定:根据患者的具体情况和病理分型,制定个体化的辅助化疗方案。
一般包括以下几个方面:1.药物选择:根据患者的病理类型、肿瘤分期、受体状态等因素,选择合适的化疗药物和靶向治疗药物。
2.剂量和使用周期:根据患者的身体状况和治疗效果评估,合理确定药物剂量和使用周期。
3.联合治疗:可考虑辅助化疗和放疗、手术等方法的联合治疗,以取得更好的治疗效果。
4.不良反应和处理:对于辅助化疗可能出现的不良反应,应及时处理和预防,并给予适当的支持治疗。
五、附件:本文档附件部分包括患者的病历资料,包括病理报告、影像学检查结果、化验数据等,为制定个体化辅助化疗方案提供参考依据。
六、法律名词及注释:1.阿霉素:一种抗肿瘤化疗药物,主要用于乳腺癌等肿瘤的治疗。
2.顺铂:一种铂类抗肿瘤药物,可用于多种恶性肿瘤的治疗。
3.环磷酰胺:一种抗代谢药物,用于治疗多种恶性肿瘤。
4.紫杉醇:一种抗肿瘤药物,主要用于乳腺癌和卵巢癌等的治疗。
乳腺癌新辅助化疗后病理诊断与评估标准

乳腺癌新辅助化疗后病理诊断与评估标准乳腺癌新辅助化疗后的病理评估可帮助判断疗效、评估预后,客观、准确、详实的病理诊断报告对于优化患者诊疗,具有非常重要的意义。
2015年4月,由复旦大学肿瘤医院病理科杨文涛教授与四川大学华西医院病理科步宏教授牵头,全国50余位乳腺病理和临床专家共同制定了《乳腺新辅助化疗后的病理诊断专家共识》。
本文以此为蓝本,总结概括了相关内容,与广大同道及患者分享。
新辅助治疗的目的在于对某些局部晚期乳腺癌患者采用全身治疗,使肿瘤体积缩小、分期降低,从而使不可手术的乳腺癌患者获得手术治疗的机会,或是让原本不适合保乳手术的患者获得保乳机会。
新辅助治疗包括新辅助化疗、新辅助内分泌治疗和靶向治疗,以新辅助化疗应用最为广泛。
新辅助化疗于术前进行,可直接观察化疗后肿瘤的变化。
对新辅助化疗后乳腺标本的病理评估非常重要,可借此判断疗效,并预测患者的预后。
新辅助化疗后乳腺癌的病理诊断能够为临床治疗提供可靠依据,并能更准确地评估乳腺癌患者的预后。
一、新辅助化疗后乳腺标本的取材1.新辅助化疗前的肿块定位:建议新辅助化疗前行粗针穿刺活检时放置标志物,如金属夹、金属圈等,以免化疗后肿瘤退缩难以辨认瘤床。
若无条件放置标志物,可在新辅助化疗前根据肿块大小和影像学,对肿瘤表面皮肤进行标记(如纹身定位),这对于化疗后瘤床定位及范围判断有一定帮助。
2.新辅助化疗后的标本取材:瘤床的正确辨认需要结合对化疗前肿块位置和大小的描述,还需要在巨检时仔细观察和触摸。
影像学技术可有助于判断瘤床情况。
目前国际上尚缺乏公认的取材规范,建议参照新辅助化疗前肿瘤的部位及范围,先按每1cm取1块的原则进行取材,如果切片中未见残余肿瘤,则需要对瘤床进行补充广泛取材。
在初次取材镜下未见肿瘤的情况下,如果大体有明确的病变或瘤床,建议将其完全取材;如大体标本中缺乏明确的病变或瘤床,则应尽可能多取材,必要时需将整个象限或整个标本(指肿块切除标本)全部取材。
2016年最新乳腺癌诊断及治疗标准流程

乳腺癌 (2016年版)一、乳腺癌标准住院流程(一)适用对象。
第一诊断为乳腺癌(C50.900)拟行乳腺癌根治术(保乳、改良根治、根治术)(二)诊断依据。
1.病史:乳腺肿块、乳头溢液、无痛;2.体征:肿块质硬、边界不清、活动度差,与皮肤粘连;3.桔皮征、血性乳头溢液等;4.辅助检查:彩超、钼靶、MRI等;5.病理:穿刺或活检诊断。
(三)治疗方案的选择及依据。
1.改良根治术:明确乳腺癌患者;2.保乳手术:有保乳意愿、适宜行保乳手术的乳腺癌患者;3.其他术式:不适合上述术式的乳腺癌患者;4.可行前哨淋巴结活检等。
(四)标准住院日为≤18天。
(五)进入路径标准。
1第一诊断必须符合ICD10:C50.900乳腺癌疾病编码;2.当患者合并其他疾病,但住院期间无需特殊处理也不影响第一诊断时,可以进入路径。
(六)术前准备(术前评估)3-5天。
1.血常规、尿常规、粪常规、凝血实验、血糖、肝功能、肾功能、电解质、血脂、传染病四项、甲状腺功能、性激素六项;2.胸片、肝胆胰脾彩超、甲状腺彩超、盆腔彩超、心电图、心脏彩超、双肾输尿管膀胱彩超;3.乳腺彩超、钼靶,必要时行双乳MRI检查等;4.根据临床需要选做:肿瘤标志物全套、血气分析、肺功能、24小时动态心电图、头、胸、上腹部CT、MRI、ECT等。
(七)预防性抗菌药物选择与使用时机。
预防性抗菌药物应用应按《抗菌药物临床应用指导原则(2015年版)》(国卫办医发〔2015〕43号)1.预防性用药时间为术前30分钟;2.手术超过3小时加用1次抗菌药物;3.术后24小时内停止使用抗菌药物。
(八)手术日为入院第≤4天。
1.麻醉方式:全麻;2.手术方式:乳房单纯切除术、乳癌改良根治术、乳癌保乳术、乳癌根治及扩大根治术,必要时行前哨淋巴结活检术及乳房重建术;3.手术内固定物:皮肤钉合器的应用、切缘银夹标志等;4.输血:视术中情况而定;5.病理:冰冻、石蜡切片,免疫组化检查,必要时行FISH基因检测;6.其他:必要时术中使用可吸收缝线、双极电凝、术后应用镇痛泵。
2016年最新乳腺癌辅助化疗诊断及治疗标准流程图

乳腺癌辅助化疗(2016年版)一、乳腺癌辅助化疗标准住院流程(一)适用对象。
第一诊断为乳腺腺癌(ICD-10:C50.801,C50.802 C50.803,C50.804伴C50.900),符合以下条件:1.腋窝淋巴结阳性。
2.腋窝淋巴结阴性但伴有高危复发因素者:如①年龄<35岁②肿瘤直径>2.0cm③核分级为Ⅲ级④有脉管癌栓⑤Her-2阳性(指免疫组化3+或/和荧光原位杂交有扩增)。
注:对于Her-2阳性,同时LN阳性或淋巴结阴性的T 大于0.5cm的患者,建议曲妥珠单抗辅助治疗。
(二)诊断依据。
根据卫生部《乳腺癌诊疗规(2011年)》和NCCN《乳腺癌临床实践指南中国版》1.症状:发现乳房肿块。
2.体格检查:乳房触诊及腋下淋巴结触诊,全身浅表淋巴结肿大情况。
3.一般情况评估:体力状态评估。
4.实验室检查:乳腺B超;血清肿瘤标志物检查如:CEA、CA125及CA153等。
5.病理诊断为乳腺癌。
(三)进入路径标准。
1.第一诊断必须符合(ICD-10:C50.801,C50.802 C50.803,C50.804伴C50.900),乳腺癌疾病编码。
2.原发灶根治术后,无远处转移或准备入院检查排除远处转移。
3.符合化疗适应证,无化疗禁忌。
4.当患者合并其他疾病,但住院期间不需要特殊处理也不影响第一诊断的临床路径流程实施时,可以进入路径。
(四)标准住院日。
2-4天。
(五)住院期间的检查项目。
1.必需的检查项目1).基线及每3月复查时检查项目:Her2检测(基线);肿瘤标记物如CEA、CA125、CA153;胸片或胸部CT、腹部或/及盆腔超声或增强CT/MRI、乳腺及腋下锁骨上淋巴结超声和心脏超声、乳腺钼靶或MRI(每年一次)。
2).每周期化疗前检查项目:(1)血常规、尿常规、大便常规。
(2)肝肾功能、电解质、血糖、凝血功能。
(3)心电图。
2.根据患者病情进行的检查项目1)提示肿瘤有复发时,可进行相关部位CT或MRI;2)骨扫描;3)合并其他疾病相关检查。
2016年最新乳腺癌辅助化疗诊断及治疗标准流程

2016年最新乳腺癌辅助化疗诊断及治疗标准流程乳腺癌是常见的女性恶性肿瘤之一,对于患者的健康和生命安全具有重要影响。
随着医学技术的不断发展,乳腺癌的辅助化疗诊断及治疗标准也在不断更新和完善。
本文将介绍2016年最新的乳腺癌辅助化疗诊断及治疗标准流程,帮助患者更好地了解和应对这一疾病。
一、乳腺癌的辅助化疗诊断乳腺癌的辅助化疗诊断主要包括病理学检测和分子生物学检测。
病理学检测通过乳腺癌的组织学形态和生化特性来判断乳腺癌的类型和分期。
分子生物学检测则通过基因和蛋白质的表达水平变化来判断乳腺癌的分子亚型和预后。
在2016年的最新辅助化疗诊断标准中,病理学检测提供了对乳腺癌组织形态和生化特性的详细描述,包括乳头状癌、导管内癌、小叶内癌等不同类型。
同时,还可以通过淋巴结转移情况和肿瘤分期来判断乳腺癌的病情。
分子生物学检测则通过乳腺癌相关基因的表达水平来判断乳腺癌的分子亚型。
最新的研究表明,乳腺癌可以分为雌激素受体(ER)阳性、人类表皮生长因子受体2(HER2)阳性和三阴性乳腺癌等不同亚型。
这一新的分类方法对乳腺癌的治疗决策和预后判断具有重要意义。
二、乳腺癌的辅助化疗治疗标准流程乳腺癌的辅助化疗治疗标准流程主要包括化疗方案的选择、手术治疗和放疗的辅助。
化疗方案的选择是根据乳腺癌患者的具体情况和病理学检测结果来决定的。
根据最新的研究和经验,化疗方案可分为单药治疗和联合药物治疗。
对于ER阳性的乳腺癌患者,内分泌治疗是首选,可以通过使用雌激素受体调节剂来阻断雌激素对肿瘤生长的刺激。
对于HER2阳性的乳腺癌患者,可以通过使用人工合成的抗HER2单克隆抗体来阻断HER2对肿瘤生长的刺激。
对于三阴性乳腺癌患者,目前尚缺乏特异性的靶向治疗方法,化疗仍然是主要的治疗手段之一。
手术治疗是乳腺癌治疗的关键环节之一。
根据乳腺癌的分期和个体差异,手术治疗可分为乳房保留手术和乳房切除手术。
对于早期乳腺癌患者,乳房保留手术是首选。
对于晚期乳腺癌患者,乳房切除手术则是必要的。
乳腺癌新辅助化疗疗效及其判断方法

乳腺癌新辅助化疗疗效及其判断方法[摘要] 越来越多乳腺癌患者选择进行术前新辅助化疗,与传统辅助化疗相比,新辅助化疗有其独特的优势。
作者综述了新辅助化疗疗效,包括疗效评价系统、化疗前后的变化和化疗反应的评估。
[关键词]乳腺癌; 新辅助化疗; 化疗反应; 腋窝淋巴结转移;综述乳腺癌新辅助化疗(neoadjuvant chemotherapy, NACT),指的是彻底切除肿瘤前先进行系统性药物治疗,最初作为标准治疗方案用于炎性乳腺癌和无法手术的局部进展期乳腺癌[1-2]。
乳腺癌术前主要通过细针抽吸确诊,因此肿瘤病理信息很有限,如肿瘤的分类、分期。
现在,术前乳腺肿块活检,前哨淋巴结活检和影像学检查(如磁共振成像)越来越普及,显著提高了术前肿瘤分类分期的准确性;因此,对越来越多乳腺癌患者采取了术前化疗[3-5]。
1 乳腺癌新辅助化疗疗效乳腺癌新辅助化疗有助于提高化疗疗效:乳腺癌发生发展过程中病灶周围发生血管重塑,大量微小血管增生;术前进行NACT,肿瘤局部丰富血供尚未受到手术破坏,可提高化疗局部疗效。
另外,除了治疗大体可见病变,NACT还为微小转移灶提供早期治疗机会,防止因局部治疗而延误系统治疗的时间。
所以,目前NACT 已经是局部进展期乳腺癌(locally advanced breast cancer,LABC)和炎性乳腺癌(inflammatory breast cancer,IBC)的标准治疗方案。
NACT对存活率的影响目前尚无明确的定论。
有研究表明:新辅助化疗和辅助化疗相比对患者的存活率没有明显改善。
最近一项比较术前新辅助化疗与术后辅助化疗的研究表明:(1) 50岁以下乳腺癌患者无病生存率(disease-free survival,DFS)(HR 0.85,P=0.09)和总生存率(overall survival,OS)(HR 0.81,P=0.06)均上升;(2) 16年随访期间,术前新辅助化疗组的DFS(44%)和OS(61%)都高于术后辅助化疗组(DFS 38%,OS 55%);(3) 无论年龄大小,所有5年无事件的患者中,接受术前新辅助化疗者DFS(HR 0.85,P=0.09)高于接受术后辅助化疗者(HR 0.81,P=0.053)。
乳腺癌化疗临床路径

乳腺癌化疗临床路径一、乳腺癌临床路径标准住院流程(一)适用对象。
第一诊断为乳腺癌(ICD10:C50)行乳腺癌新辅助化疗、术后辅助化疗及姑息性化疗。
(二)诊断依据。
根据《临床诊疗指南-肿瘤学分册》(中华医学会编著,人民卫生出版社)《临床诊疗指南-肿瘤分册》(中华医学会编著,人民卫生出版社)1. 病史:乳腺肿块、乳头溢液、无痛;2.体征:肿块、边界不清、与皮肤粘连、桔皮样症、血性乳头溢液等;3. 辅助检查:彩超和钼靶和/或MRI、乳管镜等;4. 病理:细针穿刺、Core needle等穿刺或活检诊断以及术后病理。
(三)治疗方案的选择及依据。
根据《临床诊疗指南-内科学分册》(中华医学会编著,人民卫生出版社),《临床诊疗指南-肿瘤分册》(中华医学会编著,人民卫生出版社),《NCC N乳腺癌临床实践指南》(中国版,2011年)化疗医嘱(以下方案选一)1.CMF方案---------28天为1周期环磷酰胺100 mg/m2 PO 第1-14天或环磷酰胺600 mg/m2IV 第1,8天甲氨喋呤40 mg/m2 IV 第1,8天氟尿嘧啶500 mg/m2 IV 第1,8天2.AC方案: 21天重复,共6疗程阿霉素60 mg/m2 IV 第1天环磷酰胺600 mg/m2 IV 第1天3.FAC或FEC方案-------21天为1周期氟尿嘧啶500mg/m2 IV 第1天阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV第1天环磷酰胺600 mg/m2 IV 第1天4.AT方案----------21天重复多西紫杉醇(泰索帝)75 mg/m2 IV 第1天阿霉素50 mg/m2 IV 第1天5.DOX----CMF方案阿霉素40-50 mg/m2IV或表阿霉素70-80mg/m2IV d1 q21d*4紧接4个周期后输环磷酰胺600 mg/m2 iv 1甲氨蝶呤40 mg/m2 iv 1氟尿嘧啶600 mg/m2 iv 1 q21d*86.TAC方案泰素帝75 mg/m2 iv 1预处理:地塞米松8mg Bid连续3天(-1,1,2)阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV 1环磷酰胺500 mg/m2 iv 1 q21d*67.AC-T方案阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV第1天环磷酰胺600 mg/m2 iv 1紧接4个周期后输泰素175 mg/m2 iv 3h 1 q21d*48.AC-D方案阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV第1天环磷酰胺600 mg/m2 iv 1紧接着泰素帝75 mg/m2iv 1 q21d*49.NFL方案米托蒽醌12 mg/m2iv 1氟尿嘧啶350mg/(m2.d)iv 1-3环磷酰胺300mg/d在5-Fu前用iv 1-3 q21d*6或以上10.PA方案q21d*6泰素175 mg/m2 iv3h输注d1(需用地塞米松、甲氰咪呱、本海拉明与处理)阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV111.DA方案泰素帝75 mg/m2 iv 1h输注(需用地塞米松与处理)1阿霉素50 mg/m2 iv 1q21d*612.XD 方案希罗达1250mg/(m2.d) PO Bid 1~14泰素帝75 mg/m2 iv 1 q21d13.GC方案健择1000 mg/m2 iv 1,8顺铂75 mg/m2 iv 2 q21-28d*(4~6)14.NP方案每21天重复长春瑞宾25mg/m2 IV 第1,8天顺铂75mg/m2 ivgtt 第1天或卡铂AUG 5-6 ivgtt 3h 第2天15.NX方案每21天重复长春瑞宾25mg/m2 IV 第1,8天希罗达1250 mg/m2 PO Bid 1~14 q21d16.Xeloda(希罗达)希罗达1250 mg/m2 PO Bid 1~14 q21d17.DN方案--------21天重复多西紫杉醇60-75 mg/m2IV 第1天(地塞米松8mg Bid连续3天(-1,1,2)长春瑞宾25 mg/m2 IV 第1,8天18.AC*+Trastuzumab(Herceptin)阿霉素40-50 mg/m2 IV或表阿霉素70-80mg/m2 IV第1天环磷酰胺600 mg/m2iv 1 q21d*6赫赛汀4mg/kg(首次量) iv Weekly,至PD2mg/kg(维持量) iv 19.T *+Trastuzumab(Herceptin)泰素175 mg/m2iv 3h输注1q21d*6赫赛汀4mg/kg(首次量) iv Weekly, 至PDmg/kg(维持量) iv 20.TPC方案泰素175 mg/m2iv 3h输注1q21d*6卡铂AUC 5-6iv 1q21d*6赫赛汀4mg/kg(首次量)iv Weekly, 至PD2mg/kg(维持量) iv21.三苯氧胺方案三苯氧胺10mg PO Bid或20mg Qd 每日口服连续5年22.MA或MPA单药方案甲地孕酮160mg PO或500mg PO 每日口服直到进展或不能耐受其他副作用甲孕酮每日口服直到进展或不能耐受其他副作用23.瑞宁得(Anastrozole)1mg PO 每日口服,直到疾病进展24.依西美坦25mg PO 每日口服,直到疾病进展25.来曲唑(Letrozole)2.5mg PO 每日口服,直到疾病进展26.诺雷德(Goserelin depot)3.6mg SC 每月1次27.芙仕德500mg SC 每月1次(四)标准住院日为≤12天。
乳腺癌辅助化疗方案

乳腺癌辅助化疗方案1、TAC方案多西他赛75mg/M2d1阿霉素50/M2d1环磷酰胺500/M2d1共6个周期,21天为1周期多西他赛预处理:地塞米松8mg Bid连续3天(-1,1,2)适用于高度复发危险的病例。
该方案中多柔比星的不良反应主要为心脏毒性,心肌毒性与剂量累计密切相关,辅酶Q10,维生素C,维生素E可清除自由基,可能会降低心脏毒性。
该方案的剂量限制性毒性是造血系统毒性,白细胞,尤其是粒细胞下降,易引起发热性粒细胞下降和感染。
而且粒细胞下降发生早,最早发生在用药后3~4天,降至最低点的时间是第8天,通常再降至最低点1周左右能完全恢复。
,预防使用G-CSF可有效地预防严重的骨髓抑制的发生。
如出现发热性粒细胞下降应注意以下几点:拍摄胸片,查血常规;尽量避免有创操作,仔细检查并尽可能发现感染病灶及感染;常规进行血、尿培养、中心静脉置管或可疑感染部位的培养;经验性应用广谱抗生素,根据药敏试验结果更换抗生素等。
本方案致吐性为中等程度,应用5-HT3拮抗剂。
2、AC-P方案阿霉素60mg/M2d1第1-4周期环磷酰胺600mg/M2d1第1-4周期紫杉醇175mg/M2d1第5-8周期21天为1周期紫杉醇预处理:地塞米松20mg口服(用药前12h、前6h)苯海拉明40mg肌注、西咪替丁400mg静脉注射(用药前30min)适用于高度复发危险的病例注意事项:紫杉醇用药需测量血压(化疗前30min、0min、后15min、后30min、后60min、后2h、后3h),静滴时间:3h;紫杉醇在滴注的最初几分钟内,有可能发生过敏反应。
如发生过敏反应症状较轻微,如脸红或局部皮肤反应,则不需终止治疗。
如果发生严重过敏反应,如血压下降超过20mmHg、支气管痉挛或全身皮疹或红斑,则需立即停止滴注,并进行对症治疗。
紫杉醇用药2-3天后会感到关节和肌肉疼痛,在给予G-CSF 治疗的病人肌肉疼痛会加重。
可自行缓解。
2016年最新乳腺癌放疗诊断及治疗标准流程

肿瘤科乳腺癌术后放疗(2016年版)一、标准住院流程(一)适用对象。
第一诊断为乳腺癌。
1、行乳腺癌根治术或改良根治术后,有以下指标:1)局部和区域淋巴结复发高危的患者,即T3及以上或腋窝淋巴结阳性≥4个;2)T1、T2有1-3个淋巴结阳性同时含有高危复发因素者。
2、保乳术后原则上都具有术后放疗指征。
(二)诊断依据。
病理学明确为乳腺癌。
(三)进入路径标准。
第一诊断为乳腺癌:1、行乳腺癌根治术或改良根治术后,有以下指标:1)局部和区域淋巴结复发高危的患者,即T3及以上或腋窝淋巴结阳性≥4个;2)T1、T2有1-3个淋巴结阳性同时含有高危复发因素者。
2、保乳术后原则上都具有术后放疗指征。
当患者合并其他疾病,但住院期间不需要特殊处理也不影响第一诊断的临床路径流程实施时,可以进入路径。
(四)标准住院日。
10-42天。
住院期间的检查项目。
1.必需的检查项目(1)血常规、尿常规、大便常规;(2)肝肾功、电解质;(3)乳腺及引流区淋巴结彩超、胸片或胸部CT、心电图;2.根据患者病情进行的检查项目(1)ECT全身骨扫描;(2)提示肿瘤有转移时,相关部位CT、MRI;(3)合并其他疾病需进行相关检查:如心肌酶谱、24小时动态心电图、心肺功能检查、BNP等;(五)治疗方案的选择。
1.常规放疗。
2.适形或调强放疗。
3.放疗期间可选择的治疗:必要的升血和皮肤保护剂等。
(六)出院标准。
1.放疗计划制定完成,病情稳定,生命体征平稳。
2.没有需要住院处理的并发症及合并症。
(七)变异及原因分析。
1.治疗中出现局部皮肤严重放射性皮炎、放射性肺炎等需要延长住院时间增加住院费用。
2.伴有其他基础疾病或并发症,需进一步诊断及治疗或转至其他相应科室诊治,延长住院时间,增加住院费用。
3.医师认可的变异原因分析。
4.其他患者方面的原因。
二、临床表单适用对象:第一诊断为乳腺癌(ICD-10:C30.08);患者姓名:性别:年龄:门诊号:住院号:(有条件的单位患者也可以在门诊治疗)。
乳腺癌新辅助化疗方案和具体用药完整版

乳腺癌新辅助化疗方案和具体用药完整版Luminal分型依据在luminal A型的分型依据中,ER、PR、Ki-67表达的判定值建议采用报告阳性细胞的百分比。
Ki-67增殖指数高地的判定值在不同病理实验中心可能不同,可采用20%-30%作为判断Ki-67增殖指数高低的界值;同时,以20%作为PR表达高低的判定界值,可进一步区分Luminal A样和Luminal B样(Her-2 阴性)。
在luminal B型的分型依据中,其中不满足Luminal A样条件的其他Luminal样肿瘤均可作为Luminal B样亚型。
TNM分期依据T(原发癌瘤)T0:原发癌瘤未查出Tis:原位癌(包括未探及肿块的乳头湿疹样乳腺癌)T1:癌瘤长径≤2 cmT2:癌瘤长径>2 cm,且≤5 cmT3:癌瘤长径>5cmT4:癌瘤大小不计,但侵及皮肤或胸壁(肋骨、肋间肌、前锯肌),炎性乳腺癌也包括在内。
N(区域淋巴结)N0:同侧腋窝无肿大淋巴结N1:同侧腋窝有肿大淋巴结,可推动。
N2:同侧腋窝肿大淋巴结彼此融合,或与周围组织黏连。
N3:有同侧胸骨旁淋巴结转移,有同侧锁骨上淋巴结转移。
M(远处转移)M0:不存在远处转移M1:存在远处转移病理分型1 非浸润性癌:包括癌细胞未突破末梢、乳管或腺泡基底膜的小叶原位癌、癌细胞未突破导管壁基底膜的导管内癌以及不伴发浸润性癌的乳头湿疹样癌。
此型属早期,预后较好。
2 浸润性特殊癌:包括乳头状癌、鳞状细胞癌、有大量淋巴细胞浸润的髓样癌、大汗腺样癌、小管癌(高分化腺癌)、黏液腺癌、腺样囊性癌等。
3 浸润性非特殊癌:包括浸润性小叶癌、浸润性导管癌、硬癌、髓样癌(无大量淋巴细胞浸润)、单纯癌、腺癌等。
此型是乳腺癌中最常见的类型,约占80%,但判断预后尚需结合其他因素。
4 其他罕见癌。
辅助化疗方案与具体药物Her-2 阳性乳腺癌AC(蒽环类联合环磷酰胺)-THP(紫杉类联合曲妥珠单抗、帕妥珠单抗):1.表柔比星(100mg/m2)+环磷酰胺(600mg/m2)序贯紫杉醇((80mg/m2)+曲妥珠单抗(首剂8mg/kg,之后6mg/kg)+帕妥珠单抗(首剂840mg,之后420mg)。
乳腺癌术后辅助全身治疗临床指南
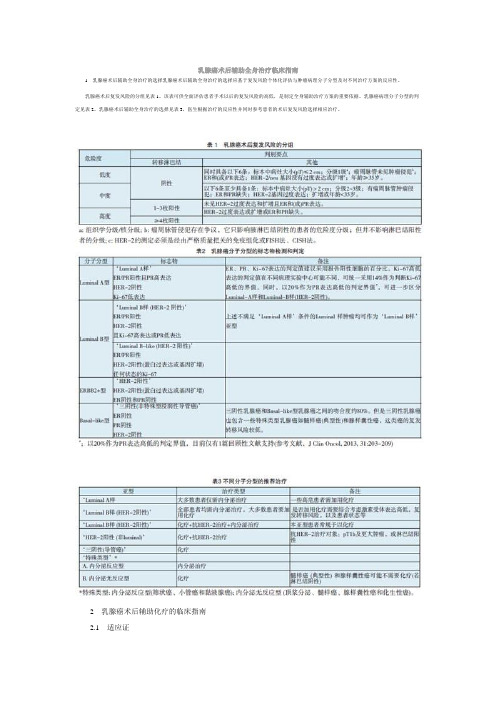
乳腺癌术后辅助全身治疗临床指南1乳腺癌术后辅助全身治疗的选择乳腺癌术后辅助全身治疗的选择应基于复发风险个体化评估与肿瘤病理分子分型及对不同治疗方案的反应性。
乳腺癌术后复发风险的分组见表1。
该表可供全面评估患者手术以后的复发风险的高低,是制定全身辅助治疗方案的重要依据。
乳腺癌病理分子分型的判定见表2。
乳腺癌术后辅助全身治疗的选择见表3,医生根据治疗的反应性并同时参考患者的术后复发风险选择相应治疗。
2乳腺癌术后辅助化疗的临床指南2.1适应证⑴肿瘤>2 cm。
⑵淋巴结阳性。
⑶激素受体阴性。
⑷HER-2阳性(对T1a以下患者目前无明确证据推荐使用辅助化疗)。
⑸组织学分级为3级。
辅助化疗方案的制定应综合考虑肿瘤的临床病理学特征、患者方面的因素和患者的意愿以及化疗可能的获益和由之带来的不良反应等。
免疫组化检测应该常规包括ER、PR、HER-2和Ki-67。
2.2禁忌证⑴妊娠期:妊娠早、中期患者,应慎重选择化疗。
⑵年老体弱且伴有严重内脏器质性病变患者。
2.3治疗前谈话⑴辅助化疗的目的是降低肿瘤复发率,提高总生存率。
⑵化疗的不良反应。
⑶年龄>70岁的患者接受化疗可能会有获益,但应慎重权衡化疗带来的利弊。
2.4治疗前准备⑴首次化疗前应充分评估患者的脏器功能,检测方法包括血常规、肝肾功能、心电图等。
以后每次化疗前应常规检测血常规和肝肾功能;使用心脏毒性药物前应常规做心电图和(或)左室射血分数(left ventricular ejectionfraction,LVEF)测定;其他检查应根据患者的具体情况和所使用的化疗方案等决定。
⑵育龄妇女应妊娠试验阴性并嘱避孕。
⑶签署化疗知情同意书。
2.5辅助化疗方案与注意事项(化疗详细方案参见附录Ⅵ、Ⅶ)⑴选择联合化疗方案,常用的有:①以蒽环类为主的方案,如CAF、A (E)C、FE100C方案(C:环磷酰胺,A:多柔比星,E:表柔比星,F:氟尿嘧啶)。
虽然吡柔比星(THP)在欧美少有大组的循证医学资料,但在我国日常临床实践中,用吡柔比星代替多柔比星也是可行的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2016年最新乳腺癌辅助化疗诊断及治疗标准流程
乳腺癌辅助化疗(2016年版)
一、乳腺癌辅助化疗标准住院流程
(一)适用对象。
第一诊断为乳腺腺癌(ICD-10:C50.801,C50.802 C50.803,C50.804伴C50.900),符合以下条件:
1.腋窝淋巴结阳性。
2.腋窝淋巴结阴性但伴有高危复发因素者:如①年龄<35岁②肿瘤直径>2.0cm③核分级为Ⅲ级④有脉管癌栓⑤Her-2阳性(指免疫组化3+或/和荧光原位杂交有扩增)。
注:对于Her-2阳性,同时LN阳性或淋巴结阴性的T 大于0.5cm的患者,建议曲妥珠单抗辅助治疗。
(二)诊断依据。
根据卫生部《乳腺癌诊疗规范(2011年)》和NCCN《乳腺癌临床实践指南中国版》
1.症状:发现乳房肿块。
2.体格检查:乳房触诊及腋下淋巴结触诊,全身浅表淋巴结肿大情况。
3.一般情况评估:体力状态评估。
4.实验室检查:乳腺B超;血清肿瘤标志物检查如:CEA、CA125及CA153等。
5.病理诊断为乳腺癌。
(三)进入路径标准。
1.第一诊断必须符合(ICD-10:C50.801,C50.802 C50.803,C50.804伴C50.900),乳腺癌疾病编码。
2.原发灶根治术后,无远处转移或准备入院检查排除远处转移。
3.符合化疗适应证,无化疗禁忌。
4.当患者合并其他疾病,但住院期间不需要特殊处理也不影响第一诊断的临床路径流程实施时,可以进入路径。
(四)标准住院日。
2-4天。
(五)住院期间的检查项目。
1.必需的检查项目
1).基线及每3月复查时检查项目:Her2检测(基线);肿瘤标记物如CEA、CA125、CA153;胸片或胸部CT、腹部或/及盆腔超声或增强CT/MRI、乳腺及腋下锁骨上淋巴结超声和心脏超声、乳腺钼靶或MRI(每年一次)。
2).每周期化疗前检查项目:
(1)血常规、尿常规、大便常规。
(2)肝肾功能、电解质、血糖、凝血功能。
(3)心电图。
2.根据患者病情进行的检查项目
1)提示肿瘤有复发时,可进行相关部位CT或MRI;
2)骨扫描;
3)合并其他疾病相关检查。
(六)化疗前准备。
1.体格检查、体能状况评分。
2.排除化疗禁忌。
3.患者、监护人或被授权人签署相关同意书。
(七)选择化疗方案
依据卫生部《乳腺癌诊疗规范(2011年)》等。
化疗方案(以下方案选一,根据患者的危险分层)
1)CEF/CAF/CTF:2周或3周方案,分别是环磷酰胺+表柔比星+氟尿嘧啶/环磷酰胺+多柔比星+氟尿嘧啶/环磷酰胺+吡柔比星+氟尿嘧啶。
2) EC/AC: 2周或3周方案,分别是环磷酰胺+表柔比星/环磷酰胺+多柔比星,可选择吡柔比星替代。
3) PTX: 单周或二周方案,为紫杉醇(Her2阳性者加用曲妥珠单抗)。
4) TXT:3周方案,为多西他赛(Her2阳性者加用曲妥珠单抗)。
5)TCbH:3周方案,为多西他赛+卡铂+曲妥珠单抗。
6)TAC:3周方案,为多西他赛+蒽环类+环磷酰胺。
7)TC(H):3周方案,为多西他赛+环磷酰胺(Her2阳
性者加用Her2阳性者加用曲妥珠单抗)。
(八)化疗后必须复查的检查项目。
1.血常规:建议每周复查1-2次。
根据具体化疗方案及血像变化,复查时间间隔可酌情增减。
2.肝肾功能:每化疗周期复查1次。
根据具体化疗方案及血像变化,复查时间间隔可酌情增减。
(九)化疗中及化疗后治疗。
化疗期间脏器功能损伤的相应防治:止吐、保肝、水化、抑酸剂、止泻药、预防过敏、升白细胞及血小板、贫血治疗。
(十)出院标准。
1.完成既定化疗流程。
2.无发热等感染表现。
3.无Ⅲ度及以上的恶心、呕吐及腹泻(NCI分级)。
4.无未控制的癌痛。
5.无需干预的异常化验结果。
6.无需干预的其他并发症。
(十一)变异及原因分析。
1.治疗前、中、后有感染、切口愈合不佳等其他合并症者,需进行相关的诊断和治疗,可能延长住院时间并致费用增加。
2.化疗后出现骨髓抑制,需要对症处理,导致治疗时间延长、费用增加。
3.药物不良反应需要特殊处理,如过敏反应、神经毒性、心脏毒性等。
4.高龄患者根据个体化情况具体实施。
5.医师认可的变异原因分析,如药物减量使用。
6.其他患者方面的原因等。
二、乳腺癌辅助化疗临床表单
适用对象:第一诊断为乳腺癌((ICD-10:
C50.801,C50.802 C50.803,C50.804
伴C50.900);
患者姓名:性别:年龄:门诊号:住院号:住院日期:年月日出院日期:年月日标准住院日:天
时
间住院第1-2天住院第2-3
天
住院第3
天
住院第4
天
(出院
日)
诊疗工作□询问病史及
体格检查
□完成病历书
写
□完善检查
□交代病情
□上级医师
查房,根
据检查结
果完善诊
疗方案
□完成化疗
前准备
□根据体
检、影像
学检查、
病理结果
等,行病
例讨论,
确定化疗
方案
□完成必要
的相关科
室会诊
□住院医师
完成上级
□化疗
□住院医
师完成
病程记
录
□上级医
师查房
□向患者
及家属
交代病
情及化
疗后注
意事项
□完成
出院
记录、
病案
首页、
出院
证明
等书
写
□向患
者交
代出
院后
的注
意事
项,重
点交
代复
诊时
间及
医师查房记录等病历书写□签署化疗知情同意书、自费用品协议书、输血同意书□向患者及家属交待化疗注意事项发生紧急情况时处理方法
重点医嘱长期医嘱:
□肿瘤内科护
理常规
□二级护理
□饮食:根据患
者情况
临时医嘱:
□胸片或胸部
CT、肝胆胰脾
B超、妇科超
声、乳腺及腋
下淋巴结超声
□病理学活组
织检查与诊断
□每周期化疗
前检查项目:
□血常规、尿常
规、大便常规
+隐血
□肝肾功能、电
解质、血糖、
凝血功能、
CEA、CA153、
CA125
□心电图
长期医嘱:
□患者既往
基础用药
⏹补液治
疗(水化、
碱化)
⏹其他医
嘱(化疗
期间一级
护理)
临时医嘱:
□化疗
□重要脏器
保护
□止吐
□其他特殊
医嘱
长期医
嘱:
□患者既
往基础
用药
⏹补液
治疗
(水
化、碱
化)
⏹其他
医嘱
(化疗
期间一
级护
理)
临时医
嘱:
□化疗
□复查血
常规、
肝肾功
能
□重要脏
器保护
□止吐、
止泻
□其他特
殊医嘱
出院医
嘱:
□出院
带药
护理工作□入院介绍
□入院评估
□指导患者进
行相关辅助
检查
□化疗前准
备
□宣教
□心理护理
□观察患
者病情
变化
□定时巡
视病房
□协助
患者
办理
出院
手续
□出院
指导,
重点
出院
后用
药方
法
变异□无□有,原
因:
□无□
有,原因:
□无□
有,原因:
□无□
有,原
因:
1.
2.
护士签名医师签名。
