原子分子离子符号写法练习
化学用语练习

化学用语练习一、写出下列元素符号:氦:___ 氢_____ 氖_____ 氟______ 氯_____ 硫____ 氧___ 磷___ 氮____ 硫____碳___ 镁____ 钠_____ 铝_____ 锰汞___ 钙_____ 金___ 钡___ 铂____锌___ 铁____ 碘____ 氩___ 硅____ 钾银____ 铜____二、写出下列离子符号:钾离子_____ 钠离子____ 氢离子_____ 镁离子_____ 钙离子_____ 银离子_____氯离子_____ 锌离子_____ 氧离子______ 铜离子_____ 铁离子_____ 亚铁离子_____ 钡离子______ 氟离子_____ 硫离子_____ 铵根离子______ 硫酸根离子_______硝酸根离子________ 碳酸根离子______ 铝离子_____ 氢氧根离子_______三、化学式的书写氮气______ 氢气______ 氧气______ 氯气______ 臭氧______ 水______ 过氧化氢_______ 二氧化碳_____ 二氧化硫_______ 二氧化锰_________ 四氧化三铁________五氧化二磷________ 氧化汞________ 汞铜____ 铁______ 锌______ 氦气______氖气_____ 氯化钠______ 氯化钾_______ 氯酸钾________ 高锰酸钾____________锰酸钾__________ 碳____ 一氧化碳_____ 氧化铝________ 氯化氢______ 碳酸钙氢氧化钙_______ 氧化铜_______ 三氧化硫_____ 碘化钾______ 硝酸钠______硝酸铵__________ 二氧化氮________ _一氧化氮_____ 氨气_____ 氯化银______硝酸______ 硫酸_______ 碳酸钠_________ 硫酸铜_______ 硫酸亚铁__________氧化镁________ 氢氧化钠_________ 氧化钙________四、物质的组成与构成1。
人教版九年级化学上册 分子、原子、离子和元素 专项提高练习(word版,含答案)

分子、原子、离子和元素专项提高练习类型一微观粒子的联系与区别1.下列对分子、原子、离子的认识,不正确的是()A.水是由水分子构成的B.分子和原子不带电,离子带电C.构成物质的粒子有分子,原子和离子D.水分子和过氧化氢分子都是由氢原子、氧原子构成,因此它们的化学性质相同2.下列事实或现象,能说明“在化学反应中,分子可以再分,而原子不能再分”的是()A.物体有热胀冷缩的现象B.走进茶叶店,可闻到茶叶的清香C.冰雪融化D.碳酸受热分解变成二氧化碳和水3.下列有关推理正确的是()A.原子是不带电的粒子,所以不带电的粒子一定是原子B.同种分子构成的物质属于纯净物,所以纯净物一定是同种分子构成的C.同种元素的不同原子中质子数相同,所以质子数相同的不同原子一定属于同种元素D.原子由核外电子、质子和中子构成,所以原子核中一定含有质子和中子4.对于构成物质的分子、原子和离子的认识,下列说法正确的是()A.构成分子的原子能保持该物质的化学性质B.原子得失电子变成离子后,元素的种类发生了变化C.离子之间存在着相互作用,分子间没有相互作用D.两种原子的质量之比等于它们的相对原子质量之比5.下列对分子、原子、离子的认识正确的是()A.同种分子排列方式不同,化学性质不同B.同种原子按不同方式结合,可以构成不同物质C.在干冰中,分子因相互作用而静止不动D.原子得失电子形成离子后,原子核发生了变化类型二物质的组成和构成6.在每个二氧化碳(CO2)、二氧化硫(SO2)、氧气(O2)分子中含有相同的()A.氧分子数B.氧离子数C.氧原子数D.元素种类7.现有下列5种物质:①二氧化碳②洁净的空气③水蒸气④液氧⑤四氧化三铁,含有氧分子的一组是()A.①②④B.②④C.②③④D.②③④⑤8.下列物质中,既含有分子又含有离子的是()A.空气B.硫酸铜溶液C.金刚石D.液态氧9.思维导图有助于建构知识网络,图为某同学建立的有关物质构成的思维导图。
常见元素的名称符号离子符号

【06】熟记并正确书写常见元素的名称、符号、离子符号。
在国际上,现在统一采用元素的拉丁文名称的第一个大写字母来表示元素,如果几种元素名称的第一个字母相同时,可再附加一个小写的字母来区别,我们称这种符号为“元素符号”。
每种元素都有各自的名称和符号。
例如,用符号O表示氧元素,用符号H表示氢元素,这种符号叫做元素符号。
元素符号既表示一种元素,还表示这种元素的一个原子。
元素的名称用汉字表示,元素的符号用英文表示。
离子符号是表示带电荷的原子或原子团的符号,符号右上角的n或n-表示带几个单位的正电荷或负电荷。
例1 BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称。
若知:①在BGO中,锗处于其最高价态,②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中铋具有最外层8电子稳定结构,③BGO可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。
请填空:1 锗和铋的元素符号分别是__________和__________。
2 BGO晶体的化学式是______________________。
3 BGO晶体中所含铋氧化物的化学式是________________。
【解析】首先根据锗位于第四主族,确定它的最高正价为4价,对应氧化物为GeO2。
根据条件②,铋位于周期表中第V A族,最外层有5个电子,形成氯化物时最外层有8个电子,因此每个铋原子与3个氯原子结合形成共价化合物,可知铋的化合价为3,对应氧化物为Bi2O3。
由条件③,BGO晶体可看成两种金属的氧化物组成的复杂氧化物,可写成Bi2O3·GeO2,且两种氧化物中所含氧的总质量相等,因此可写为2Bi2O3·3GeO2,或变形为Bi4GeO43或Bi4Ge3O12。
【答案】1 Ge;Bi。
2 Bi4Ge3O12[或2Bi2O3·3GeO2、Bi4GeO43]。
练习5 化学符号及其周围数字的意义 -初三化学 (人教版)(解析版)

练习5 化学符号及其周围数字的意义一、符号的意义 1、元素符号表示的意义宏观意义:表示某元素;微观意义:表示1个某原子。
如:H 表示:①氢元素②1个氢原子。
2H 表示:2个氢原子。
方法技巧:元素符号前的数字:几个原子2、离子符号的意义(注意区别:“离子符号的意义”与“离子符号中数字的意义”不同) 如:Al 3+表示铝离子;nAl 3+表示 n 个铝离子 。
Al 3+ 中数字“3”表示 一个氯离子带三个单位的正电荷 。
方法技巧:离子符号前的数字:几个离子3、化合价的书写:位置 正负号与数字的顺序 数字1是否省略 举例 化合价 元素符号正上方 符号在前数字在后 不能省略 Mg +2O 离子符号元素符号右上方先写数字后写号省略不写Mg 2+(1) 表示某物质(2)表示某(物质)由×元素(和×元素)组成 (3)表示1个某分子(4)表示1个某分子由几个×原子(和几个×原子)构成 二、认识元素符号或化学式周围的数字的不同意义1、左边数字:nM M 为元素符号时,表示有n 个M 原子 。
M 为化学式时,表示n 个 分子 。
yR x n ±±m系数x 表示微粒个数角码y 表示分子中的原子数±m 表示 物质中元素的化合价 n± 表示离子所带的电荷数M为离子符号时,表示n个离子。
2、右上角数字:M n+,表示1个M n+ 离子带个单位的正电荷。
3、正上方数字:M+n,表示M元素在化合物中显+n价。
4、右下角数字:M n,表示1个M分子中含有n个原子。
1.(2020·鄂州)下列说法正确的是A. 过氧化氢溶液是混合物,是因为它含有不同种分子B. 2Fe3+与3N中的“3”都表示微粒的个数C. 表示的微粒都带有电荷D. CuO中氧元素的化合价表示为:2Cu O【答案】A【解析】A.过氧化氢溶液是混合物,是因为它含有水和过氧化氢两种不同种分子;B.2Fe3+中的“3”表示一个铁离子带3个单位的正电荷,3N中的“3”表示3个氮原子;C.和表示的微粒中质子数=核外电子数,不带有电荷;表示的微粒质子数>核外电子数,微粒失去电子,带正电荷;D.CuO中氧元素的化合价为-2,表示为:-2Cu O。
初三化学基础练习

初三化学基础练习(四)班级姓名1、用化学符号表示:2个氮原子;1个氯分子;2个氢氧根离子;氢氧化铜中铜元素的化合价为+2价。
2、在“金刚石、氖气、二氧化硫、活性炭、氨气、石油”中选择适当的物质填空。
电工用的电笔中常充入;玻璃刀头上镶的是;形成酸雨的主要物质是;用于炼制汽油、煤油的原料是;防毒面具的滤毒罐中常加入的一种物质是;能使酚酞溶液变红的气体是。
3、现有C、H、O、Ca四种元素,选用一种或几种写出符合下列要求的化学式...酒精灯中盛放的液体物质是;可口可乐中含有的一种酸是;覆盖在地球表面约占3/4的液体;石灰水中的有效成分是。
4、甲、乙、丙、丁四种元素,甲的单质是空气中含量最多的气体;乙是地壳中含量最多的金属元素;丙是人体中含量最多的元素;丁元素原子核外只有一个电子。
则:甲元素的名称是;乙元素是_______;丙元素的符号是_______;丁元素形成的单质是_________;乙和丙形成的化合物的化学式是_________。
5、⑴用名称或化学用语填空:①2个氮原子,②体温计中的液态金属③3个氢离子,④硝酸根离子,⑤氯化镁中镁元素显+2价。
6、家庭厨房实际上就是一个化学世界,“柴米油盐酱醋糖”等都是化学物质。
请问:(1)加碘食盐所含碘酸钾(KIO3)中,I元素的化合价是。
(2)白糖与红塘,主要成分都是蔗糖。
利用活性炭的性,可将红塘脱色变成白糖。
(3)天然气的主要成分的化学式为。
(4)食盐中的阴离子。
7、用化学符号和数字表示:(1)3个铝离子,(2)2个氦气分子,(3)n个银原子,(4)+2价的镁元素,8、在“氧气、活性炭、二氧化碳、石墨、熟石灰”中选择适当的物质填空:(1)可供急救病人呼吸;(2)可作温室气体肥料;(3)可作电极;(4)可做冰箱的除臭剂;(5)是常用的建筑材料。
9、在H、O、C、S四种元素中,选择适当的元素,组成符合下列要求的物质,将其化学式填入空格中。
(1)能形成“酸雨”的氧化物;(2)相对分子质量最小的氧化物;(3)“雪碧”中含有的一种酸;(4)天然气的主要成分;(5)冶金工业中常用来作还原剂的氧化物。
九年级上册化学期末专练:元素符号、化合价、离子符号、化学式默写和计算

九年级上册化学期末复习专练元素符号、化合价、离子符号、化学式背写与计算➢背写部分一. 写出元素符号1.元素周期表前20个元素氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙2.常见元素:锰铁银碘钡汞铅溴铜锌金二. 背出常见元素、原子团的化合价:(用符号填写)常见元素化合价:常见原子团化合价:(一定要靠记忆来背写)练习:1. 标出下列物质中N元素的化合价,请标在N元素的正上方①N.2; ②N.O: ③N.O2: ④N.2O5; ⑤HN.O3⑥N.H4N.O32. NaSO4中S的化合价是KMnO4中Mn的化合价为三、写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子铜离子亚铁离子氢氧根离子硫酸根离子硝酸根离子碳酸根离子铵根离子碳酸氢根离子四、写出下列物质的化学式1、单质三原子:臭氧双原子:氧气氯气氢气碘溴单原子:稀有气体:氦气氩气氖气金属:铜银水银锌铁其他:磷金刚石硫碳石墨2、化合物氧化物:氧化铝水干冰氧化铜三氧化硫过氧化氢二氧化硫氧化钾氧化钙一氧化碳二氧化锰四氧化三铁五氧化二磷氯化物:氯化钠氯化铜氯化银氯化氢氯化镁氯化铁硫化物:硫化氢硫化钠硫化锌其他:氯酸钾 硫酸钾 碳酸钙 锰酸钾 高锰酸钾 硫酸 氢氧化钙 氢氧化钾 氢氧化铝 碳酸钠 碳酸铵 综合练习 1、看符号写含义O 5N 3H 2 C Al mC 2、按要求写出下列符号:①氧元素 ②两个氧原子 ③氧气 ④两个氧气分子 ⑤氧离子 ⑥两个氧离子 3、写出下列符号中数字2的意义。
2H Ca 2+ 2SO 3 Cl 2 2H 2O 、2MgO C +2u SO 42-➢ 计算部分一、根据化学式计算相对分子质量或相对分子质量之和1、A12(SO 4)3的相对分子质量=2、下列各相对分子质量的计算中,正确的是( ) A 、2MgO 的相对分子质量之和=2×24+16=64 B 、NO 2的相对分子质量=14×16×2=448C、2N的相对分子质量和=2(14+2)=32D、3O2的相对分子质量和=3×(16×2)=96二、根据化学式计算化合物中各元素的质量比(最简整数比)化合物中各元素的质量比等于各元素的相对原子质量的和之比1:计算硫酸铵【(NH4)2SO4】中各元素的原子个数比及各元素的质量比解:(NH4)2SO4中N、H、S、O原子个数比为:(NH4)2SO4中各元素的质量比:2、在H2SO4中氢、硫、氧三种元素的质量比的计算式正确的是( )A、(1×2):32:(16×4)B、1:32:16C、2:1:4D、(16×4):32:(1×2)三、计算化合物中某元素的质量分数例题:计算碳酸氢铵【NH4HCO3】中氮元素的质量分数。
九年级上册化学分子和原子知识点及练习题

分子和原子知识点及练习题分子和原子知识讲解考点1:分子和原子1、分子的特性:(1) 分子等微粒的体积和质量都________ 。
(2) 分子等微粒总在不断地____________ ,温度________ ,运动速度___________(3) 分子等微粒间有_____________ 。
2.分子的定义:分子是保持____________________ 的最小微粒。
3.原子的定义:原子是_________________ 的最小微粒。
化学反应的微观实质:___________________________________________考点 2:元素1.定义:元素就是具有相同 _________________________ 的一类原子的总称。
2.特点: ________ ,_________________________下列说法有没有错误 ?把错误的说法加以改正。
①水是由 1个氧元素和 2 个氢元素组成的。
②二氧化硫中有硫和氧 2 个元素。
①错误。
改正:水是由 ____________________________ 组成的。
② 错误。
改正:二氧化硫由 ______________________ 组成。
3. 各种元素在地壳中的含量相差很大。
(1) .地壳中含量最多的元素是 _________ ,其次是 _______ 。
(2) .地壳中含量最多的金属元素是 __________ ,其次是 ______ 。
(3) .氢、碳、氮等元素在地壳中的含量相对较少。
4. 原子和元素的区别:[提问 ] 前面我们学过物质的构成可用原子表示, 现在又知道元素可以表示物质的组成。
用原子 表示物质的构成和用元素表示物质的组成有什么区别呢 ?[讲解 ] 原子表示的是物质的微观结构, 而元素表示的是物质的宏观组成。
用原子时只能对应微 观粒子,而用元素时只能对应宏观物质。
请看下列表格:元素原子概念 联系 具有相同 ____________________________ 的一类 原子的总称_______________ 中的最小粒子区分_______________ ,不表示个数,即表示 ________ ,又讲 _________ ,有 数量多少的含义使用 范围 举例 应用于描述物质的宏观组成,例如可以说, “水里含有氢元素和氧元素 ”或 “水里由氢元 素和氧元素组成的 ”,但不能说 “水是由二个 氢元素和一个氧元素所组成的 ”应用于描述物质的微观结构。
(完整)分子原子离子的综合练习题集

分子原子离子的综合练习题一.选择题1.某微粒R m—的核电荷数为n,你认为不可能据此推测出的是( )A.该微粒的质子数 B.该微粒所属元素种类 C.该微粒的电子数 D.该微粒的相对粒子质量2.元素X核电荷数为a,它的阳离子X m+与Y的阴离子Y n—的电子层结构相同,则元素Y的核电荷数( ) A.m+n+a B.m—n—a C.m+n-a D.a-m-n3.据中央电视台对云南澄江抚仙湖湖底古城考古的现场报道,科学家曾通过测定古生物遗骸中的碳14原子含量来推断古城年代。
碳14原子结构示意图为其相对原子的质量为14。
下列关于碳14的说法中不正确的是()。
A.质子数为6 B.核外由两个电子层,第一层有4个电子C.核外电子数为6 D.核电荷数等于核外电子数4.某粒子由12个质子、12个中子和10个电子构成,该粒子是()。
A.分子 B.原子 C.阴离子 D.阳离子5.关于钠离子和钠原子的认识不正确的是( ).A.他们的质子数相同 B.它们的电子层数相同C.Na比Na+少一个电子 D.Na+的最外层是相对稳定结构6.X、Y、Z、Q四种元素的核电荷数分别为a、b、c、d(均小于18),若它们的离子X m+、Y n+、Z m—、Q n-的电子层数相同,则下列关系中,正确的是().A.a—b=n-m B.b—d=2n C.c—d=m+n D.a-c=03.原子核外第三电子层与第一电子层的电子数相等的原子,其质子数为()A.20 B.14 C.12 D.107.某元素的阳离子A3+的核外有23个电子,核内有30个中子,则该元素原子的核电荷数和原子量分别为( ) A.23,53 B.26,30 C.26,56 D.23,468.下列各组数字代表了元素的核电荷数,其中能组成AB2型离子化合物的一组是()A.11和7 B.12和17 C.8和12 D.11和169.M元素的离子为M2+,其核外电子数为a,核内中子数为b,则M的相对原子质量为( ) A.a+b+2 B.a+b—2 C.a+b D.b+210.下列微粒中,与Na+的质子数和电子数都相同的是( )A.F- B.H2O C.NH4+ D.OH-11.有关钠原子结构示意图,其说法错误的是( )A.表示钠的原子核核内有11个质子B.弧线表示电子层,其共有3个电子层C.数字“1"表示第一层的电子层上有一个电子D.数字“2”表示第一电子层上有2个电子12.某R2+离子中有23个电子,R元素的相对原子质量为55,则R原子核内的中子数为( ) A.25 B.28 C.30 D.3212.下列各组分子中,核外电子总数相等的一组是()A.CO和NO B.NH3和CH4 C.SO2和H2S D.CO2和NH3·H2O13.牙膏中的含氟化合物对牙齿有保护作用.一种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为( )A.7 B.9 C.10 D.1914.近日,某省发现部分大米镉超标,镉超标易引起镉中毒.镉元素的核电荷数为48,相对原子质量为112,则镉原子的核外电子数是( )A.48 B.64 C.112 D.16015.钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性能好等优良性能,因此被广泛用于火箭、航天飞机、船舶和化工等.已知钛原子的质子数为22,中子数为26,则钛原子的核外电子数为()A.48 B.26 C.4 D.2216、2012年4月,媒体曝光某不法企业用皮革废料熬制成工业明胶,再制成药用胶囊流向市场.皮革废料中重金属铬超标,危害人体健康.铬(Cr)原子的核电荷数为24,相对原子质量为52,铬原子的核外电子数为()A.24 B.28 C.52 D.7617.根据右图提供的信息,下列说法正确的是( )A.钠原子最外层有11个电子B.钠的相对原子质量是22。
原子分子离子符号写法练习

化学符号的书写专题练习 1(4分)用符号和数字填空①2个硫酸根离子;②3个氮气分子;③+3价的铁元素;2.用化学用语填空:(1)2个铵根离子;(3)写出氯化铁的化学式并标出该化合物中铁元素的化合价(1)请写出相应的化学符号或名称:①2个硫原子;②+2价的镁元素;③2C1-;④H 2O 2:。
②3O 2。
(1)2个氢原子;(2)3个氢氧根离子;(1)镁元素;2)两个过氧化氢分子;(3)硫酸溶液中的阴离子;3..用适当的化学符号和数字填空(1)三个铁原子;(3)水中氢元素的化合价;(4)四个二氧化碳分子。
4)现有H 、O 、N 、C 、Na 五种元素,请选用其中的元素写出符合下列要求的物质各一个(用化学式表示):(1)空气中含量最多的气体;(2)人体中含量最多的物质;5.化学用语是学习化学的重要工具,请用数字和符号表示下列粒子:①3个氢分子,②5个硫酸根离子。
6.按要求填空:⑴用化学符号表示:2个硝酸根离子氢氧化铁中铁元素的化合价。
⑶地壳中含量最多的元素与最多的金属元素形成的化合物的化学式。
7.用微粒的观点回答下列问题:(1)保持水的化学性质的微粒是。
(2)水通电分解过程中,不变的微粒是。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是8.用化学符号或者化学式填写(1)2个氢原子2)五氧化二氮分子4)地壳中含量最高的金属元素。
9.正确读写化学符号是学好化学的基础,下列读法或写法正确的是()A .3H —3个氢分子B.2Mg 2+—2个镁离子C .硫酸钾—KSO 4 D.氧化铁—FeO10.下列化学用语表示正确的是()A .两个氯原2Cl 2B .镁离子C .二氧化硫分子SO 2D .碳酸钠NaCO 311.下列化学用语书写正确的是()A .1个氖原子NaB .+2价的铁元素Fe +2C .4个氢分子4HD .3个硝酸根离子3NO 3—12..物质的化学式和相应的名称均正确的是()A.O 3氧气B.MgCl 2氯化镁C. O 4Fe 3氧化铁D.Fe(OH)2氢氧化铁13.“2H”表示的意义是()A.2个氢元素B.2个氢原子C.氢分子D.氢离子14.下列化学用语与含义不相符的是()A.AlCl 3—氯化铝B.钙离子—Ca 2+C.2个氧元素—2OD.2个水分子—2H 2O 43.下列物质的化学符号书写正确的是()A.氧化镁MgO 2B.氧化铝AL 2O 3C.水银AgD.二氧化硫SO 215.在化学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。
答案元素符号原子团及化学式的书写及练习

答案元素符号原子团及化学式的书写及练习Final revision on November 26, 2020+2Mg_表示镁元素的化合价是正2价+2MgO表示氧化镁中镁元素的化合价是正2价元素符号、原子团及化学式的书写及练习(参考答案)班级_______姓名_______________一、写出各元素的元素符号或名称及部分常见原子团离子的符号。
常见元素化合价口诀:_______(答案略)______________、_________________________________________________________、________________________________________________________、___________________________________________________________、_____________________________常见原子团化合价口诀:________(答案略)________、___________________________________________________________、_____________________________三、理解各种符号或数字的意义:1、写出下列各种符号所表示的意义:“Cu”表示①表示铜元素②表示一个铜原子(表示铜这种物质)“H2O”表示①表示水这种物质②表示水是由氢元素和氧元素组成的③表示一个水分子④表示一个水分子由二个氢原子和一个氧原子构成的。
“5H”表示①表示5个氢原子“2CO2”表示①表示2个二氧化碳分子2、写出下列各种符号或指出符号中的“2”的意义:三个铁原子3Fe五个五氧化二磷分子5P2O5液态氮N2铝离子Al3+氯离子Cl-二个铵根离子2NH4+2Mg_表示2个镁原子Mg2+_表示一个镁离子带2个单位的正电荷SO2_表示一个二氧化硫分子中含有2个氧原子四、熟练书写化学式:(写出下列各种物质的化学式)1、单质:氢气H2氯气Cl2氮气N2氦气He氖气Ne氩气Ar铜Cu锰Mn镁Mg金刚石C固态磷P硫磺S臭氧气体O3 2、化合物:氧化物:一氧化碳CO水H2O二氧化硫SO2氧化镁MgO氧化铁Fe2O3氧化亚铁FeO 氧化铜CuO 氧化铝Al 2O 3氧化锌ZnO 氧化亚铜Cu 2O硫化物:(硫元素显示-2价)硫化镁MgS 硫化锌ZnS 硫化铁Fe 2S 3硫化亚铁FeS 硫化钠Na 2S 氯化物(又称盐酸盐)氯元素显示-1价氯化镁MgCl 2氯化锌ZnCl 2氯化铁FeCl 3氯化亚铁FeCl 2 氯化钠NaCl 氯化铜CuCl 2氯化铵NH 4Cl 氯化氢(盐酸)HCl 氢氧化物(含OH )氢氧化镁Mg(OH)2氢氧化锌Zn(OH)2氢氧化铁Fe(OH)3氢氧化铝Al(OH)3氢氧化钠Na OH 氢氧化铜Cu(OH)2氢氧化钾K OH 氢氧化钡Ba(OH)2硝酸盐(含硝酸根NO 3)硝酸镁Mg(NO 3)2硝酸锌Zn(NO 3)2硝酸铁Fe(NO 3)3硝酸钾K NO 3硝酸钠Na NO 3硝酸铜Cu(NO 3)2硝酸铵NH 4NO 3硝酸银Ag NO 3硝酸钙Ca(NO 3)2硝酸铝Al(NO 3)3硝酸钡Ba(NO 3)2硝酸亚铁Fe(NO 3)2硫酸盐(含SO 4)硫酸镁MgSO 4硫酸锌ZnSO 4硫酸铜CuSO 4硫酸铁Fe 2(SO 4)3 硫酸钠Na 2SO 4硫酸钾K 2SO 4硫酸铵(NH 4)2SO 4硫酸钡BaSO 4 碳酸盐或碳酸氢盐(含CO 3或HCO 3)碳酸镁MgCO 3碳酸锌ZnCO 3碳酸钙CaCO 3碳酸钡BaCO 3碳酸钠Na 2CO 3碳酸钾K 2CO 3碳酸氢钠NaHCO 3碳酸氢铵NH 4HCO 3 酸类(H +与某些阴离子结合而成的化合物)盐酸(氯化氢)HCl 氢硫酸(硫化氢)H 2S 氢氟酸(氟化氢)HF 硫酸H 2SO 4硝酸HNO 3碳酸H 2CO 3亚硫酸H 2SO 3磷酸H 3PO 4 五、其它练习1、写出下列物质化学式中,加点元素的化合价( 已知氧的化合价-2,氢+1)-1-2+5+4+(n+4)00HF .H 2SP ..2O 5H 2C .O 3H n R .O n+2 H 2 Cu2、A 原子和B 原子在形成化合物时,每个A 原子得到2个电子,形成A 离子,每个B 原子失去3个电子,成为B 离子。
化学式及离子符号书写练习
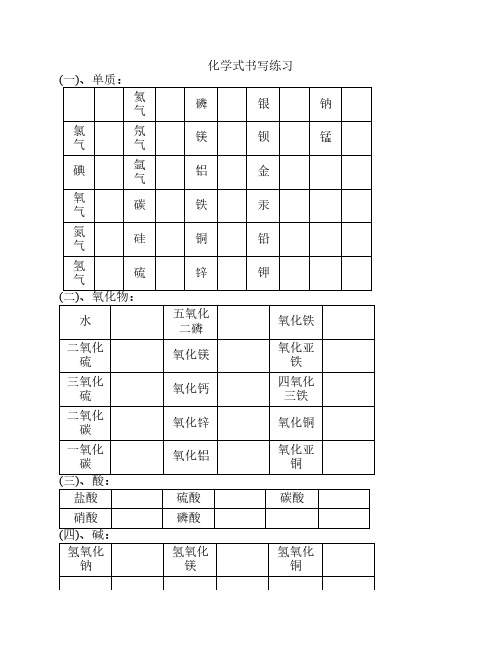
碳酸
氢氧化 铜
氢氧化 钾
氢氧化 钙
氢氧化 钡
(五)、盐: 硝酸钾 硝酸钠 硝酸钡 硝酸钙 硝酸镁 硝酸铝 硝酸锌 硝酸铁 硝酸亚 铁 硝酸铜 硝酸银 硝酸铵 碳酸钾
碳酸钠
碳酸钡
碳酸钙
碳酸镁
碳酸铝
氢氧化 铝
氢氧化 铁
氢氧化 亚铁
氯化钾 氯化钠 氯化钡 氯化钙 氯化镁 氯化铝 氯化锌 氯化铁
氯化亚铁
5、人体含量最多的金属元素__________
6、地壳中含量最多的非金属元素与含量最高的金属元素组成的化合
物___
7、KClO3中氯元素的化合价是_______ 3ClO2表示
8、O3中氧元素的化合价是______2Hg表示
9、Fe2+中“2”表示__________
Ca2+和S2-中“2”表示__________
硝酸根离子 m个碳酸根离子 高锰酸根离子 氢氧根离子
13、空气中含量最多的元素_____ 空气中含量最多的气体
二、按要求填空
1、FeSO4的名称__________
NaNO2的名称
2、构成氯化钠的微粒是________氯酸钾中的阴离子
3、右图表示的微粒是______ 画出氧原子的结构示意图
4、相对分子质量最小的氧化物________
10、过氧化氢中氧元素的化合价是__________
6、两个氦原子_________氖气
氩原子
7、氧化钾的化学式__________
8、硫酸铁的化学式________常温下一种液态金属的化学式
9、 硅元素______铅元素
铂元素
金元素
10、3个亚铁离子_______ 铁离子
3个碳酸分子
分子 原子 离子练习题

原子、分子、离子中考针对练习题(二)1.下列叙述中不正确的是( )A 、钠原子失去电子后变成钠离子B 、氯离子失去电子后变成氯原子C 、原子的质量主要集中在原子核上D 、化学变化中分子不能再分2.下列关于原子的叙述正确的是( )A.原子是不能再分的粒子B.一切物质都是由原子直接构成的C.一切原子的原子核由质子和中子构成D.原子核内质子数必等于核外电子数3.根据钠原子结构示意图,判断下列说法错误的是( )A.钠原子核外有3个电子层B.钠原子在化学反应中容易得到电子C.钠原子最外层只有一个电子D.钠原子的核电荷数为114.朝核问题引发了国际关注,核问题的关键是核能的如何利用。
已知某种核原料的原子核中含有1个质子和2个中子,那么( )A.该原子是一种氢原子B.该元素是金属元素C.该原子核外有3个电子D.该原子核带2个单位的正电荷5.如右图是某原子结构示意图,有关它的说法错误的是A.它的核内有12个质子B.它属于非金属元素C 它有3个电子层 D.它的最外层有2个电子6.下列四种粒子的结构示意图中,属于稀有气体元素的原子是 ( )7.下列对分子、原子、离子的认识,正确的是 ( )A .分子是保持物质性质的最小粒子B .原子是最小的粒子,不可再分C .原子得到或失去电子后形成D.CO 2和CO 性质的差异主要是由于分子间的间隔不同8.化学反应前后可能发生变化的是 ( )A .物质的总质量B .元素种类C .原子数目D .分子数目11.原子失去最外层电子后,会改变的是( )A.元素种类B.相对原子质量C.中子数D.化学性质12.关于钠离子和钠原子的认识不正确的是( )A.它们的质子数相同B.它们的电子层数不同C.Na比Na+少一个电子D.Na+的最外层是稳定结构13.Ca2+右上角的数字表示的意义是()A.钙原子最外层上有2个电子B.钙原子有2个电子层C.钙离子带两个单位正电荷D.2个钙离子14.下列物质中可能由原子构成的是( )A. 纯净物B.水银C.氧化汞 D.酒精15.下列说法中正确的是( )A. 纯净物一定是由分子构成的B.由同种分子构成的物质一定是纯净物C. 分子是保持物质性质的唯一粒子D.在化学变化中原子和分子都发生了变化16.下列关于氧分子与氧原子的说法,错误的是( )A. 氧分子大,氧原子小B.氧气既由氧分子构成,也由氧原子构成C氧气的化学性质由氧分子保持 D. 在化学反应中,氧分子能再分,氧原子不能17. 20世纪20年代,就有人预言可能存在由4个氧原子构成的氧分子(O4),但一直没有得到证实。
浙教版科学八年级下册第二章《微粒的模型与符号》化学式练习含答案

八年级科学化学式练习一、写出下列元素符号:碳氢氧氮氯硫磷,钾钙钠镁铝铁锌,溴碘锰钡铜硅银,氦氖氩氟铍汞金二、写出下列原子团的符号及化合价:硝酸根离子? 、?? ?硫酸根离子? ?? 、 ??碳酸根离子+ 、 ? 碳酸氢根离子- 、?氢氧根离子 ? 、? 铵根离子、二、写出下列物质的化学式:1.单质的化学式:(1)铜铁汞铝 ?钙钡(2)硫黄 ? 硅 ?金刚石石墨黄磷(3)氦气氖气 ?氩气(4)碘 ?溴氢气氧气氯气氮气 ?2、根据化合价写出下列化合物的化学式:(1)氧化物:(A)金属氧化物:氧化钠氧化钾氧化钙氧化铜氧化铁氧化亚铁四氧化三铁氧化铝(B)非金属氧化物:水、二氧化碳一氧化碳二氧化硫三氧化硫五氧化二磷冰(2)酸:(某酸:H+ + 某酸根阴离子)硫酸硝酸盐酸(酸根Cl-)碳酸(3)碱:氢氧化钠氢氧化钾氢氧化钙氢氧化镁氢氧化铝氢氧化铜氢氧化钡氢氧化铁氢氧化亚铁(4)盐酸盐:氯化钠氯化钾氯化钡氯化钙氯化铜氯化铝氯化亚铁氯化铁氯化银(5)碳酸盐:碳酸钾碳酸钠碳酸钙?碳酸镁? 碳酸钡碳酸氢钠碳酸氢铵(6)硫酸盐:硫酸钾硫酸钠硫酸钙硫酸镁? 硫酸钡硫酸亚铁硫酸铵硫酸铁(7)硝酸盐:硝酸银 ?硝酸钠硝酸钙硝酸镁? 硝酸钡硝酸亚铁硝酸铵硝酸铁四、用化学符号表示:1、铁离子2、氯离子3、氢离子4、铜离子5、3个亚铁离子6、2个铜离子7、2个钠离子8、氢气 9、氢元素 10、1个氢原子11、2个氢原子 12、一个氢分子 13、2个氢分子14、2个氢离子 15、2个水分子 16、正2价的钙元素17、2个一氧化氮分子 18、2个氧离子 19、带2个单位负电荷的硫离子 20、氧化镁中镁元素的化合价为+2价五、说出下列“2”的含义1、2Cl2、3Cl2+23、2K+4、 BaCO35、2Fe3+6、SO27、2SO3 8、S042-9、Ca2+ 10、3Fe2+11、H2 12、2Cl-六、标出下列加点元素的化合价1、 H Cl..Cl..O2Cl..2K Cl..O3Ca(Cl..O)2H Cl..O3H Cl..O22、S.O3S.O2S . H2S.O4H2S. H2S.O3Na2S.O43、Mn..O2Mn..Cl2Mn.. K Mn..O4 K2 Mn.. O4Mn..O4-Mn..O42-4、N.2N.2O3N.2O5N. O N. O2H N. O3N. O3-N. H4N. O3N. H4+ Al(N. O3)3Mg(N. O3)2七、标出下列物质中各.元素的化合价1、CO2 2、CO 3、H2CO34、NaNO35、Fe(OH)3 6、K2O 7、Al2O38、FeCl29、H2O 10、SO311、P2O5、 12、BaSO4八、写出下列符号的名称或含义1、O22、FeCl33、FeO4、Cu5、3H2O 6、Cl-27、S 8、S2-九、说一说“SO2”表示的含义1、 2、3、 4、5、十、根据化学式计算(相对原子质量质量Fe-56,O-16,Cu-64,S-32)1、Fe2O3: (1)铁、氧元素质量比(2)铁、氧原子个数比(3)铁元素的质量分数(4)铁元素的化合价(5)320克Fe2O3中含铁元素的质量,含氧元素的质量2、CuSO4:(1)由、、元素组成,(2)原子个数比: =(3)元素质量比: = (4)硫元素的化合价(5)各元素的质量分数:Cu%= S%= O%=(6)160克硫酸铜中各元素的质量:Cu: S:O:八年级科学练习班级姓名二、写出下列元素符号:碳 C 氢 H 氧 O 氮 N 氯 Cl 硫 S 磷 P ,钾 K 钙 Ca 钠 Na 镁 Mg 铝 Al 铁 Fe 锌 Zn ,溴 Br 碘 I 锰 Mn 钡 Ba 铜 Cu 硅 Si 银 Ag ,氦 He 氖 Ne 氩 Ar 氟 F 铍 Be 汞 Hg 金 Au二、写出下列原子团的符号及化合价:硝酸根离子? NO3- 、?? -3 ?硫酸根离子? SO42-?? 、 ?? -2碳酸根离子+ CO32-、 ? -2 碳酸氢根离子 HCO3-、? -1 氢氧根离子 ? OH-、? -1 铵根离子 NH+、 +1 二、写出下列物质的化学式:1.单质的化学式:(1)铜 Cu 铁 Fe 汞 Hg 铝 Al ?钙 Ca 钡 Ba(2)硫黄 S ? 硅 Si ?金刚石 C 石墨 C 黄磷 P(3)氦气 He 氖气 Ne ?氩气 Ar(4)碘 I2 ?溴 Br2氢气 H2氧气 O2氯气 Cl2氮气 N2 ?2、根据化合价写出下列化合物的化学式:(1)氧化物:(A)金属氧化物:氧化钠 Na2O 氧化钾 K2O 氧化钙 CaO 氧化铜 CuO 氧化铁 Fe2O3氧化亚铁 FeO 四氧化三铁Fe3O4氧化铝 Al2O3(B)非金属氧化物:水 H20 、二氧化碳 CO2一氧化碳 CO二氧化硫 SO2三氧化硫 SO3五氧化二磷 P2O5冰 H2O(2)酸:(某酸:H+ + 某酸根阴离子)硫酸 H2SO4 硝酸 HNO3盐酸(酸根Cl-) HCl 碳酸 H2CO3(3)碱:氢氧化钠 NaOH 氢氧化钾 HOH 氢氧化钙 Ca(OH)2氢氧化镁 Mg(OH)2氢氧化铝Al(OH)3氢氧化铜 Cu(OH)2氢氧化钡 Ba(OH)2氢氧化铁 Fe(OH)3氢氧化亚铁 Fe(OH)2(4)盐酸盐:氯化钠 NaCl 氯化钾 K Cl 氯化钡 Ba Cl2 氯化钙Ca Cl2氯化铜CuCl2氯化铝 Al Cl3氯化亚铁 Fe Cl2氯化铁Fe Cl3氯化银 AgCl(5)碳酸盐:碳酸钾K2CO3 碳酸钠Na2CO3 碳酸钙? CaCO3碳酸镁? MgCO3 碳酸钡BaCO3 碳酸氢钠NaHCO3 碳酸氢铵NH4HCO3(6)硫酸盐:硫酸钾 K2SO4硫酸钠 Na2SO4硫酸钙 CaSO4硫酸镁?MgSO4硫酸钡BaSO4硫酸亚铁FeSO4硫酸铵(NH4)2SO4硫酸铁 Fe2(SO4)3(7)硝酸盐:硝酸银 AgNO3 ?硝酸钠 NaNO3硝酸钙Ca(NO3)2硝酸镁? MgNO3)2硝酸钡Ba(NO3)2硝酸亚铁Fe(NO3)2硝酸铵NH4NO3硝酸铁Fe(NO3)3四、用化学符号表示:1、铁离子 Fe3+2、氯离子 Cl-3、氢离子 H+4、铜离子 Cu2+5、3个亚铁离子 3Fe2+6、2个铜离子 2Cu2+7、2个钠离子 2Na+8、氢气 H2 9、氢元素 H 10、1个氢原子 H11、2个氢原子 2H 12、一个氢分子 H2 13、2个氢分子 2H2+214、2个氢离子 2 H+ 15、2个水分子 2 H20 16、正2价的钙元素 Ca 17、2个一氧化氮分子 2NO 18、2个氧离子 2O2- 19、带2个单+2位负电荷的硫离子 S2- 20、氧化镁中镁元素的化合价为+2价 MgO五、说出下列“2”的含义1、2Cl 2个氯原子2、3Cl2 1个氯分子中有2个氯原子+23、2K+ 2个钾离子4、 BaCO3 碳酸钡中钡元素的化合价是正2价5、2Fe3+ 2个铁离子6、SO2 1个二氧化硫分子中有2个氧原子7、2SO3 2个三氧化硫分子 8、S042- 1个硫酸根离子带2个单位的负电荷9、Ca2+ 1个钙离子带2个单位的正电荷 10、3Fe2+ 1个亚铁离子带2个单位的正电荷11、H2 1个氢分子中有2个氢原子 12、2Cl- 2个氯离子六、标出下列加点元素的化合价-1 +2 0 +5 +1 +5 +31、 H Cl..Cl..O2Cl..2K Cl..O3Ca(Cl..O)2H Cl..O3H Cl..O2+6 +4 0 +6 -2 +4 +62、S.O3S.O2S . H2S.O4H2S. H2S.O3Na2S.O4+4 +2 0 +7 +6 +7 +63、Mn..O2Mn..Cl2Mn.. K Mn..O4 K2 Mn.. O4Mn..O4-Mn..O42-0 +3 +5 +2 +4 +5 +5 -3 +54、N.2N.2O3N.2O5N. O N. O2H N. O3N. O3-N. H4N. O3-3 +5 +5N. H4+ Al(N. O3)3Mg(N. O3)2七、标出下列物质中各.元素的化合价+4 -2 +2 -2 +1 +4 2 +1 +5 -21、CO2 2、CO 3、H2CO34、NaNO3+3 -2 +1 +1 -2 +3 -2 +2 -15、Fe(OH)3 6、K2O 7、Al2O38、FeCl2+1 -2 +6 -2 +5 -2 +2 +6 -29、H2O 10、SO311、P2O5、 12、BaSO4八、写出下列符号的名称或含义1、O21个氧分子氧气2、FeCl3氯化铁(1个氯化铁分子) 3、FeO 氯化亚铁(1个氯化亚铁分子)4、Cu 铜元素 1个铜原子金属铜5、3H2O 3个水分子 6、Cl 氯元素 1个氯原子-27、S 负2价的硫元素 8、S2- 1个带2个单位负电荷的硫离子九、说一说“SO2”表示的含义1、二氧化硫这种物质2、 1个二氧化硫分子3、二氧化硫中含有硫元素和氧元素4、二氧化硫分子的相对分子质量为645、 1个二氧化硫分子由1个硫原子和2个氧原子构成十、根据化学式计算(相对原子质量质量Fe-56,O-16,Cu-64,S-32)1、Fe2O3: (1)铁、氧元素质量比 7:3 (2)铁、氧原子个数比 2:3(3)铁元素的质量分数 70% (4)铁元素的化合价 +3(5)320克Fe2O3中含铁元素的质量 224 克,含氧元素的质量 96克2、CuSO4:(1)由铜、硫、氧元素组成,(2)原子个数比:Cu:S:O = 1:1:4(3)元素质量比:Cu:S:O = 2:1:3(4)硫元素的化合价 +6(5)各元素的质量分数:Cu%= 33.3% S%= 16.7%O%= 50%(6)160克硫酸铜中各元素的质量:Cu: 53.3克 S: 26.7克O: 80克[文档可能无法思考全面,请浏览后下载,另外祝您生活愉快,工作顺利,万事如意!]。
化学式的写法 (3)

元素符号
O
氧:C 碳:Al 铝氯::Cl 钙:Ca 铜:Cu
氢:H 硫:S 汞:Hg 氮:N 氯:Cl 银:Ag 钠:Na 钾:K 锡:Sn 镁:Mg 锰:Mn 碘:I 硅:Si 锌:Zn 钡:Ba 磷:P 铁:Fe 金:Au
元素符号意义 以H为例:
1、表示氢元素 2、表示一个氢原子
需注意2H只表示2个氢 原子
-2
2-
SO4 K Ca
-2
+1
H2SO4 K
2.下列离子符号表示方法哪些是错误的?把它们改 在横线上。
Al3- Mg2+ Na+ OH1-
Al3+
OH-
化学方程式 用化学式来表示化学反应的式子
通电
2H2O ====== 2H2↑+O2 ↑
表示水通电分解生成氢气和氧气
表示每两个水分子反应生成两个 氢分子和一个氧分子
2.表示一个分子的原子构成。 一个水分子由二个氢原子和一个氧原子构成。
但在化学式前边有 数字,就只能表示 微粒个数了。
例如:2H2O表示2 个水分子。
符号Fe意义
铁元素 一个铁原子 铁这种单质
元素化合价口诀:
一价氢氯钾钠银 二价氧钙钡锌镁
三铝四硅三五磷 二三铁,二四碳,
二四六硫都齐全,
一二铜汞最常见
亚铁离子---Fe2+ 硫酸根离子---SO42-
铁离子---Fe 3+ 碳酸根离子---CO32-
钠离子---Na + 硝酸根离子---NO-3
银离子---Ag +
-
氢氧根离子---OH
锌离子---Zn2+ 铵根离子---NH4+
高中化学《元素符号、元素名称的书写》练习题(附答案解析)

高中化学《元素符号、元素名称的书写》练习题(附答案解析)学校:___________姓名:___________班级:___________一、单选题1.在饮用水中添加含钙、镁、锌、硒等的矿物质,可以改善人体营养,增强体质。
其中的“钙、镁、锌、硒”是指 ( )A .分子B .原子C .离子D .元素2.下列有关化学用语表示正确的是( )A .核内有8个中子的碳原子:B .18O 2-的结构示意图:C .羟基的电子式:D .淀粉和纤维素的结构简式:CH 2O 3.同温同压下,等体积的两容器内分别充满14N 16O 和13C 16O 气体,下列对两容器中气体的判断正确的是( )A .分子数相同B .中子数不同C .质子数相同D .气体质量相同4.在元素周期表中,有一种元素14058Ce ,它作为玻璃添加剂,能吸收紫外线与红外线,还可降低车内温度,从而节约空调用电,现已被大量应用于汽车玻璃行业。
下列对其元素说法正确的是( )A .所含的质子数为140B .所含的质量数是58C .所含的中子数是82D .核外电子数是1405.下列表示离子符号表示正确的有( )①CO 32﹣②③④⑤Mg 2+ A .①②③④⑤ B .②③④ C .②④⑤ D .③④⑤6.下列化学用语书写正确的是( )A .三个二氧化硫分子:2SO 3B .两个氧分子:2OC .Co 元素的化合价:Na 3Co +O 2D .一个铝离子:Al +3 7.下列化学用语表示正确的是( )A .镁离子符号:+2MgB .硫酸钾化学式:4KSOC .聚乙烯结构简式:[2n 2CH CH ]=D .稀硝酸电离方程式:+33HNO H +NO -=8.下列有关化学用语表示正确的是( )A.氮气的结构式:N=N B.F-的结构示意图:C.中子数为20 的氯原子:2017Cl D.NH3的电子式:9.乙炔气经CaCl2等净化后,在氮气氛中可催化聚合为聚乙炔。
【初中化学】九年级专题训练(二) 分子、原子、离子和元素(练习题)

九年级专题训练(二)分子、原子、离子和元素(223)1.对下列事实的解释,不合理的是()A.通过气味辨别氮气和氨气-——分子是运动的,不同分子的性质不同B.氧气经压缩储存在钢瓶中——压强增大,分子之间的间隔变小C.干冰升华为二氧化碳气体——状态变化,分子大小随之变化D.蔗糖在热水中溶解更快——温度越高,分子运动速率越大2.从电解水反应的微观示意图中获得的信息正确的是()A.化学反应是分子的重新组合B.化学反应前后原子数目增多C.该反应的反应类型为分解反应D.该反应说明水由氢气和氧气组成3.利用分子的知识解释,选择合适选项填空。
A.分子不断运动,温度升高时运动加快B.分子很小C.分子间有间隔,温度、气压发生变化时,间隔大小随之发生改变(1)湿衣服晾一段时间会变干,是因为。
(2)可以将大量的氧气压缩到天蓝色的钢瓶中,是因为。
(3)一滴水里的水分子个数由10亿人来数,每人每分钟数100个,昼夜不停,需3万年才能数完,是因为。
(4)水受热后变成水蒸气,体积变大,说明。
(5)食盐放入水中,整杯水都有咸味,说明。
4.如图是某化学反应的微观示意图,其中“”和“”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质。
请回答:(1)a、b物质均属于(填物质分类),从微观角度说明你的判断依据是。
(2)该反应属于(填基本反应类型)反应。
5.下列物质中,由阴、阳离子构成的是()A.二氧化碳B.氢气C.氯化钠晶体D.水银6.近年,我国科学家首次拍摄到水分子团簇图像,模型如图。
下列说法正确的是()A.氢、氧两种元素只能组成水B.团簇中的水分子不再运动C.水蒸气冷凝成水,分子间隔减小D.过氧化氢和冰都是由水分子构成的7.最近科学家发现,水在−157∘C超低温、正常压力或真空条件下仍呈液态,比蜂蜜还黏稠。
下列关于这种“高密度液态水”的说法正确的是()A.化学性质与普通水不同B.分子不再运动C.氢、氧两种原子的个数比为2∶1D.分子间的间隔比普通水的大8.从下列图片中不能获取的信息是()A.分子之间有间隔B.硅原子是由原子核和电子构成的C.水分子受热运动速率加快D.构成物质的粒子有分子、原子和离子9.图为元素周期表的一部分(X元素信息不全)。
专题2.6.2表示物质的符号——离子的符号(原卷版+解析)

2020年浙教版八年级下科学同步学习精讲精练第2章微粒的模型与符号2.6-2表示物质的符号——离子的符号目录 (1) (2) (2) (3) (5)离子符号1.离子的定义离子是带电的原子或原子团。
带正电荷的离子称为阳离子,带负电荷的离子称为阴离子。
原子得到电子形成阴离子,失去电子形成阳离子。
2.离子符号的定义离子符号是在形成该离子的原子的元素符号右上角标出该离子所带的电荷数。
3.离子符号的表示方法(难点)(1)只带一个单位电荷(正、负电荷),则把个数“1”省去,直接在元素符号右上角写“+”或“-”号。
如:Na+:表示带1个正电荷的钠离子;Cl-:表示带1个负电荷的氯离子。
(2)带多个单位电荷(正、负电荷),则在元素符号右上角先写电荷数,再写“+”或“-”号,如:Mg2+:表示带2个正电荷的镁离子;Al3+:表示带2个负电荷的铝离子;O2-:表示带2个负电荷的氧离子。
4.常见的原子团有些离子的组成不止一种元素,如OH-和SO2-4等,这种离子称为某某根离子,这些离子是带电的原子团。
常见的较复杂的离子见下表:1.物质的构成说明前面几节我们已经学到,有的物质是由原子直接构成的,如金属、金刚石、石墨等。
分子是由原子构成的,分子可以直接构成物质,如二氧化碳。
而有些物质是由阴阳离子构成,如氯化钠。
由离子直接构成的物质,化学式不再表示物质组成元素的原子个数比,而是离子个数比。
而由分子构成物质的化学式又叫分子式,如NO2。
2.离子符号的表示及意义1.多个离子的表示在离子符号的前面加上数字。
如2个镁离子(2Mg2+)、3个硝酸根离子(3NO-3)等。
2.离子中各个数字的含义归纳5SO2-4:“5”表示5个硫酸根离子,“2”表示每个硫酸根离子带有2个单位负电荷,“4”表示1个硫酸根离子中含有4个氧原子。
【说明】①在化学反应里,常作为一个整体参加反应的原子集团叫原子团,也叫根。
原子团也是离子。
原子团和原子团之间也可以形成化合物。
元素符号、原子团及化学式的书写及练习

+2 Mg__________________________ +2 MgO______________________________ 元素符号、原子团及化学式的书写及练习一、写出各元素的元素符号或名称及部分常见原子团离子的符号。
常见原子团离子符号:1、写出下列各种符号所表示的意义:“Cu” 表示①__________________ ②_________________________“H 2O” 表示① ②③ ④“5H” 表示 ①“2CO 2”表示 ①2、写出下列各种符号或指出符号中的“2”的意义:三个铁原子 五个五氧化二磷分子 液态氮铝离子 氯离子 二个铵根离子2Mg___________________________ Mg 2+______________________________SO2___________________________1、单质: 氢气 氯气 氮气 氦气 氖气 氩气 铜锰 镁 金刚石 固态磷 硫磺 臭氧气体2 、化合物:氧化物: 一氧化碳 水 二氧化硫 氧化镁 氧化铁氧化亚铁 氧化铜 氧化铝 氧化锌 氧化亚铜硫化物:(硫元素显示-2价)硫化镁 硫化锌 硫化铁 硫化亚铁 硫化钠氯化物(又称盐酸盐)氯元素显示-1价氯化镁 氯化锌 氯化铁 氯化亚铁氯化钠 氯化铜 氯化铵 氯化氢(盐酸)氢氧化物(含OH )氢氧化镁 氢氧化锌 氢氧化铁 氢氧化铝氢氧化钠 氢氧化铜 氢氧化钾 氢氧化钡硝酸盐(含硝酸根N O 3)硝酸镁 硝酸锌 硝酸铁 硝酸钾硝酸钠硝酸铜硝酸铵硝酸银硝酸钙硝酸铝硝酸钡硝酸亚铁硫酸盐(含SO4)硫酸镁硫酸锌硫酸铜硫酸铁硫酸钠硫酸钾硫酸铵硫酸钡碳酸盐(含CO3)碳酸镁碳酸锌碳酸钙碳酸钡碳酸钠碳酸钾碳酸氢钠碳酸氢铵磷酸盐(含PO4)磷酸镁磷酸锌磷酸铜磷酸铁磷酸钠磷酸钾磷酸铵磷酸钡酸类(H+与某些阴离子结合而成的化合物)盐酸(氯化氢)氢硫酸(硫化氢)氢氟酸(氟化氢)硫酸硝酸碳酸亚硫酸磷酸酸式盐(含HCO3或HSO4或HPO4)碳酸氢钠碳酸氢钙碳酸氢钡碳酸氢铵硫酸氢钠硫酸氢钙硫酸氢钡硫酸氢铵磷酸氢钠磷酸氢二钙磷酸氢钡磷酸氢铵五、其它练习1、写出下列物质化学式中,加点元素的化合价?(已知氧的化合价-2,氢+1)HF.H2S.P.2O5 H2CO3 HnROn+2H2Cu2、A原子和B原子在形成化合物时,每个A原子得到2个电子,形成A离子,每个B原子失去3个电子,成为B离子。
化学式及离子符号书写练习

化学式书写练习碳酸钠碳酸铁高锰酸钾碳酸钡碳酸亚铁锰酸钾碳酸钙碳酸铜亚硫酸钠碳酸镁碳酸银亚硝酸钠碳酸铝碳酸铵常见离子符号氢离子铵根离子钾离子钠离子钡离子钙离子镁离子铝离子锌离子亚铁离子铁离子铜离子银离子氯离子硝酸根离子硫酸根离子氢氧根离子碳酸根离子一、用化学用语填空1、2个氧原子____2个氧离子 2个氧分子 2个硫酸分子2、锌离子____ 镁离子氢离子银离子铜离子氟离子钾离子钡离子钙离子硫离子3、+2价的镁元素__________4、2个氮分子__________5、保持硫酸铜化学性质的粒子是_____构成氧化汞的微粒是6、两个氦原子_________氖气氩原子7、氧化钾的化学式__________8、硫酸铁的化学式________常温下一种液态金属的化学式9、硅元素______铅元素铂元素金元素10、3个亚铁离子_______ 铁离子 3个碳酸分子11、氧化铁中铁元素的化合价___硝酸铵中+5价的氮元素12、铵根离子________4个氨分子_____铝离子 2个硫酸根离子____硝酸根离子 m个碳酸根离子高锰酸根离子氢氧根离子13、空气中含量最多的元素_____ 空气中含量最多的气体二、按要求填空1、FeSO4的名称__________ NaNO2的名称2、构成氯化钠的微粒是________氯酸钾中的阴离子3、右图表示的微粒是______ 画出氧原子的结构示意图4、相对分子质量最小的氧化物________5、人体含量最多的金属元素__________6、地壳中含量最多的非金属元素与含量最高的金属元素组成的化合物___7、KClO3中氯元素的化合价是_______ 3ClO2表示8、O3中氧元素的化合价是______2Hg表示9、Fe2+中“2”表示__________ Ca2+和S2-中“2”表示__________10、过氧化氢中氧元素的化合价是__________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原子分子离子符号写法练
习
Prepared on 21 November 2021
化学符号的书写专题练习 1(4分)用符号和数字填空
①2个硫酸根离子;②3个氮气分子;③+3价的铁元素;
2.用化学用语填空:
(1)2个铵根离子;(3)写出氯化铁的化学式并标出该化合物中铁元素的化合价
(1)请写出相应的化学符号或名称:
①2个硫原子;②+2价的镁元素;③2C1-;④H 2O 2:。
②3O 2。
(1)2个氢原子;(2)3个氢氧根离子;
(1)镁元素;2)两个过氧化氢分子;(3)硫酸溶液中的阴离子;
3..用适当的化学符号和数字填空
(1)三个铁原子;
(3)水中氢元素的化合价;(4)四个二氧化碳分子。
4)现有H 、O 、N 、C 、Na 五种元素,请选用其中的元素写出符合下列要求的物质各一个(用化学式表示):
(1)空气中含量最多的气体;(2)人体中含量最多的物质;
5.化学用语是学习化学的重要工具,请用数字和符号表示下列粒子:
①3个氢分子,②5个硫酸根离子。
6.按要求填空:⑴用化学符号表示:2个硝酸根离子氢氧化铁中铁元素的化合价。
⑶地壳中含量最多的元素与最多的金属元素形成的化合物的化学式。
7.用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是。
(2)水通电分解过程中,不变的微粒是。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是
8.用化学符号或者化学式填写
(1)2个氢原子2)五氧化二氮分子4)地壳中含量最高的金属元素。
9.正确读写化学符号是学好化学的基础,下列读法或写法正确的是()
A .3H —3个氢分子B.2Mg 2+—2个镁离子C .硫酸钾—KSO 4 D.氧化铁—FeO
10.下列化学用语表示正确的是()
A .两个氯原2Cl 2
B .镁离子
C .二氧化硫分子SO 2
D .碳酸钠NaCO 3
11.下列化学用语书写正确的是()
A .1个氖原子Na
B .+2价的铁元素Fe +2
C .4个氢分子4H
D .3个硝酸根离子3NO 3—
12..物质的化学式和相应的名称均正确的是()
A.O 3氧气
B.MgCl 2氯化镁
C. O 4Fe 3氧化铁
D.Fe(OH)2氢氧化铁
13.“2H”表示的意义是()
A.2个氢元素
B.2个氢原子
C.氢分子
D.氢离子
14.下列化学用语与含义不相符的是()
A.AlCl 3—氯化铝
B.钙离子—Ca 2+
C.2个氧元素—2O
D.2个水分子—2H 2O43.下列物质的化学符号书
写正确的是()
A.氧化镁MgO 2
B.氧化铝AL 2O 3
C.水银Ag
D.二氧化硫SO 2
15.在化学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。
下列化学符号中数字“2”表示的意义正确的是()
A .Mg 2+:一个镁离子带2个单位正电荷
B 、CO 2:二氧化碳分子中含有氧原子
C .2H :2个氢元素
D 、CaO +2:氧化钙的化合价为+2价。
