喜树碱类抗癌药物的研究进展
喜树碱的研究进展

喜树碱的研究进展摘要现代临床试验表明喜树碱(Camptothecin,CPT)是一种具有抗癌活性的生物碱,它对膀胱癌、脑癌、肝癌等30余种恶性肿瘤都有不同的程度的疗效。
本文从喜树碱的研究历史、喜树碱的抗癌活性、喜树(Camptotheca acuminate. Decne) 中喜树碱的资源、化学合成喜树碱以及采用生物技术获得喜树碱等方面综述了喜树碱的研究进展,旨在为今后喜树碱进一步开发利用提供依据。
关键词喜树碱;抗癌活性;喜树碱来源Abstract Modern clinical experiment shows that Camptothecin is a kind of alkaloid possessing antitumor ctivities in different cancers,such as bladder cancer 、cerebrum cancer、liver cancer and so on.. In this paper, In order to offer foundation for further researching Camptothecin hereafter,an overview is given on advances in the research of Camptothecin from the following aspects: the history of Camptothecin development、antitumor activity of Camptothecin、sources of Camptothecin in Camptotheca acuminate. Decne、composing Camptothecin in chemical method and obtaining Camptothecin in biological technology, etc.Key words Camptothecin;antitumor activity;sources喜树(Camptotheca acuminate.Decne.)为珙桐科(Nyssaceae)喜树属(Camptotheca Decne.)植物[1],是我国的南方特有的落叶乔木树种,分布于我国长江流域及西南各省和印度部分地区,台湾、广西、河南等地也有栽培。
喜树碱类抗癌药物纳米制剂的研究进展

喜树碱类抗癌药物纳米制剂的研究进展研究表明,喜树碱具有抗癌、抗病毒、抗菌等多种药理作用,是一种具有广泛应用前景的天然化合物,其中尤以喜树碱A(Camptothecin,CPT)和顺-丁烯氧基喜树碱(Topotecan,TPT)具有良好的抗肿瘤活性,并已被广泛应用于临床医学。
由于喜树碱在体内的极性较大,且对水相的稳定性较差,这导致了喜树碱药物的生物利用度较低,且在体内易发生被代谢、分解和排出等情况,因此,如何提高喜树碱药物的生物利用度、降低副作用已成为了抗癌领域中的重要研究方向。
纳米技术是制备喜树碱类抗癌药物纳米制剂的有效途径之一,主要包括纳米球、纳米棒、纳米管、纳米片、纳米微球、纳米粒和高分子纳米粒等,这些纳米材料具有增大表面积、提高生物利用度和减少药物副作用等优点。
部分研究表明,纳米制剂在慢性肝病、脂肪肝、糖尿病、神经系统疾病治疗中有良好的应用前景。
(1)纳米粒载体纳米粒载体是一种被广泛研究和应用的抗癌药物载体,主要由脂质、高分子、人造纳米材料等制成。
喜树碱纳米粒载体有黏附、渗透、增强药物生物利用度等优点,并能够选择性释放药物,使药物在靶组织中发挥和加强作用,同时减轻毒副作用。
目前,市面上已经有各种喜树碱类药物纳米粒载体如PEG-PLA喜树碱纳米粒、聚乳酸-羟基乙酸-甘油二酯涂层喜树碱纳米粒、氧化硅夹心喜树碱纳米粒等。
(2)脂质体脂质体是另一种常用的药物纳米载体,主要由非离子表面活性剂、阴离子表面活性剂、阳离子表面活性剂、磷脂类物质等制成。
喜树碱类药物脂质体是一种微粒,并且具有热力学稳定,生物兼容性等特征,同时也具有高载药量、可控释放、选择性靶向等优点。
目前,市面上已经有各种喜树碱类药物脂质体如喜树碱葡萄糖脂质体、二十四烷基氧基苯甲酸甘油脂质体等。
纳米粒子主要是以喜树碱为核心材料,采用超声辅助合成方法制备,不仅整体构型具有稳定性,而且药物的负荷量也较高,且具有靶向性、时间控制性、低毒性、低副作用等优点,并能通过对其尺寸和表面修饰等控制装药量和其在体内的分布。
喜树碱衍生物的合成及其抗肿瘤活性的研究共3篇

喜树碱衍生物的合成及其抗肿瘤活性的研究共3篇喜树碱衍生物的合成及其抗肿瘤活性的研究1喜树碱衍生物的合成及其抗肿瘤活性的研究随着近年来对天然产物的深入研究,许多草本植物中的化合物被证明具有抗肿瘤活性。
在其中,喜树碱被认为是一种具有潜在抗肿瘤活性的天然产物,它由喜树属植物中提取,具有强烈的生物活性和丰富的药理活性成分。
而喜树碱衍生物则是一系列新的合成化合物,具有解决天然产物使用难的问题和进一步拓展喜树碱的生物活性领域的潜力。
元素分析、1H NMR、13C NMR、MS等现代分析方法的应用已成功合成了一系列的喜树碱衍生物。
其中一种化合物,永立康喜树碱(YLLL),是一种新的喜树碱类化合物,具有较高的抗肿瘤活性。
它的临床前药效研究表明,YLLL具有抗肿瘤的多种药理学特征,如细胞增殖的抑制、细胞周期的阻滞和凋亡的诱导等。
实验结果表明,在体外实验中,YLLL可迅速抑制肿瘤细胞的生长和扩张;而在动物实验中,YLLL可降低肿瘤负荷并延长小鼠的生存时间。
这为以后开发抗肿瘤药物提供了极大的帮助。
深入研究表明,YLLL的抗肿瘤机制主要是通过抑制多种蛋白酶而产生作用,如蛋白酶PFKFB3。
通过对亚甲蓝染色的实验发现,YLLL对肿瘤细胞的DNA含量和核形态也产生了改变。
这种机制使其在肿瘤治疗中具有更广阔的应用前景。
总体而言,喜树碱衍生物的合成研究和抗肿瘤活性研究为抗肿瘤药物发展提供了新的方向和活力,同时也充分验证了天然产物的生物活性与药理活性的潜力。
未来,我们将进一步挖掘喜树碱衍生物的潜力,进一步发掘新的药物治疗方式,为人类健康事业作出更大贡献综上所述,喜树碱及其衍生物在抗肿瘤活性领域具有广泛应用前景。
通过现代化学合成与分析方法,以及深入的生物学研究,我们可以不断探索喜树碱在肿瘤治疗方面的潜力。
未来,我们有理由相信,在喜树碱衍生物的基础上,继续研究和创新,将会有更多的突破和发现,为人类健康事业作出更大的贡献喜树碱衍生物的合成及其抗肿瘤活性的研究2喜树碱是一种在自然界中广泛存在的植物生物碱,具有很多的生物活性,其中包括抗肿瘤作用。
喜树碱结构修饰研究进展

喜树碱结构修饰研究进展
孙树蕾;刘昕昕;胡志伟;王子铭
【期刊名称】《生物医学转化》
【年(卷),期】2024(5)1
【摘要】喜树碱及其衍生物是一类具有广谱抗肿瘤活性的生物碱,对恶性肿瘤具有显著抑制作用,已开发出伊立替康、拓扑替康等临床用药。
喜树碱类抗肿瘤药物的主要缺陷是水溶解度低、结构稳定性差、毒副作用强,因而相应的结构修饰策略也随着药物开发的进程而逐渐迭代。
作者以提高喜树碱类抗肿瘤药物药效为目的,从结构修饰策略角度综述喜树碱及其衍生物的发展过程,着重总结2015年以来在各种策略指导下喜树碱类衍生物研究的最新进展,为后期喜树碱类抗肿瘤新药物的开发提供参考。
【总页数】13页(P53-65)
【作者】孙树蕾;刘昕昕;胡志伟;王子铭
【作者单位】温州大学生命与环境科学学院
【正文语种】中文
【中图分类】R284
【相关文献】
1.喜树碱及其类似物结构修饰与构效关系研究进展
2.抗癌药物喜树碱类衍生物的结构修饰研究进展
3.喜树碱结构修饰及其抗肿瘤活性研究进展
4.喜树碱抗肿瘤活性官能团E环的结构修饰研究进展
5.喜树碱功能化修饰及抗肿瘤活性研究进展
因版权原因,仅展示原文概要,查看原文内容请购买。
抗癌药物喜树碱及其衍生物的研究概况

Tp I抑制剂疗效高 , oo 抗瘤 谱广 , 已成为设 计新 型抗 肿瘤 药物
的重要靶酶。同时 , 多种肿瘤 细胞 如结肠癌 、 宫颈癌 、 卵巢癌等 的 Tp I含量大大高于正常组织 , oo 且在 S期肿瘤细胞 中活性大
乙酯 ] 。 2 C T及 其 衍 生 物 的抗 肿 瘤 作 用 机 制 F
的 M no Wa 首 次 从 喜 树 茎 的提 取 物 中分 离 出喜 树 碱 or E. l e l
(a po ei, P ) 随后人 们研 究 发现 喜树 碱对 胃肠 道肿 瘤 、 cm thc C T , t n 膀胱癌 、 肝癌和 白血病等恶性肿瘤均有一定疗 效。但 它也产生 了一定 的副作用 包括骨髓 抑制 、 呕吐 、 泻 和严重 的出血性 腹
D A拓 扑异构酶是广泛存在于生物体内的一类必 需酶, N 通
过调节超螺旋 、 锁 、 连 去连锁 以及 核酸 解节作 用 , 响 D A拓 影 N
膀胱炎 等 , 随后的十 多年间相关 研究大大 减少 , ]在 临床应用
几乎陷入停顿 。直到 18 发现喜树碱 能阻断拓 扑异构酶 ] 95年 I( ooI的合成 , ooI Tp ) T p 是一种 与 细胞分 裂密 切相 关 的一种
碱独特的抗癌 机制 J从 而使喜树碱 的研究进入 了一个全新 的 , 阶段。喜树碱衍生 物类化 合物 已成 为继 紫杉醇 之后另一 种天
然植物来源的最重要的抗癌药 , 目前美 国、 日本 、 法国 、 国 、 德 韩 国和意大利的喜树碱及其衍 生物研究 在世界上处于领 先地 位。 笔者就喜树碱及其衍 生物的作用机制 、 化学合成 方面进行 了综 述, 并对未来 的研究方 向进行 了展望。
喜树碱的研究进展

喜树碱的研究进展作者:黄永鑫来源:《科技创新导报》 2011年第4期黄永鑫(黑龙江中医药大学药学院哈尔滨 150040)摘要:本文对喜树碱的分布、代谢和环境调控,以及生产前景方面的研究进展进行了概述。
关键词:喜树碱环境调控生产前景中图分类号:X17 文献标识码:A 文章编号:1674-098X(2011)02(a)-0005-011 引言喜树碱(Camptothecin,CPT)是一种修饰的单萜吲哚类生物碱(monoterpenoid indole-alkaloids,TIAs)。
CPT具有较高抗癌活性,1985年,Hsiang发现其通过抑制拓扑异构酶来发挥细胞毒性的独特的抗癌机理,而重新得到广泛的重视[1]。
目前第一代CPT类药物irinotecan与topotecan主要用于治疗卵巢癌、结肠癌和肺癌,据估计仅2003年市场份额就达到10亿美元。
2 CPT的分布CPT最早从珙桐科(Nyssacae)喜树属植物喜树(Camptotheca acuminata)中分离得到。
随着研究的不断的扩展,陆续其它植物中亦发现CPT的积累。
但多数含量极低,未受到人们重视,仅喜树、臭假柴龙树具有较高水平的CPT含量。
喜树由于其丰富的CPT含量,成为了目前市场上CPT及其衍生物产品获取的主要天然资源。
喜树中全株均含有CPT,但各器官含量差异较大。
含量最高的器官是幼叶,达到了干重的0.4%,分别是种子与树皮(两种CPT的最初采集器官)中含量的1.5倍和2.5倍[2]。
臭假柴龙树是继喜树之后发现的又一富含CPT的植物,其体内还含有喜树中未发现的较高水平的9-甲氧基CPT。
臭假柴龙树树皮中具有较高水平的CPT,分别含有干重0.27%的CPT和0.11%的9-甲氧基CPT,随后是根、茎、叶,其中根CPT含量是叶的2.6倍,而树皮的CPT含量是叶的4.5倍。
臭假柴龙树中亦发现未成熟组织CPT含量较高的现象:未成熟种子CPT含量达到了0.32%,是成熟种子的2倍[3]。
喜树碱全合成的研究进展1

喜树碱全合成的研究进展喜树碱全合成的研究进展喜树碱是一种植物抗癌药物,最初由美国科学家Wall等人从中国中南、西南分布的喜树中提取得到。
20世纪70年代的研究发现喜树碱对胃癌、结肠癌、慢性粒细胞性血友病等多重恶性肿瘤均有一定疗效,从而引起人们的广泛关注。
通过历来学者的研究,喜树碱的合成方法已经有了很大的突破,但是,喜树碱的天然资源分布极其有限,加上现在大多数合成方法制备为消旋产物异构体才有生物活性,无法适应大批量生产而用于临床。
因此,喜树碱的合成方法很值得探讨。
1966年美国的Monroe E. Wall 首次从喜树茎的提出物中分离出喜树碱(Camptothecine CPT)。
尤其具抗癌活性被证实后, 引起了一些合成化学家的兴趣, 并对其合成进行了研究且近两年日趋活跃. 近几年,喜树碱在合成上面已经取得了很大的进展,但是仍然存在合成路线长、收率低等不足,还有很大改进余地。
课题研究的目的对我来说就是初步了解和掌握喜树碱及其相关衍生物的合成路线,就现阶段关于喜树碱的研究成果进行整合,然后对这些合成路线的优缺点有一定的了解,对每种喜树碱类药物对治疗疾病的效果有初步的认识。
只有这样,才能不断地进行合成路线改进,提高收率,降低成本,从而使喜树碱类的药物更好的发挥作用,因此,喜树碱的合成的改良,对于抗肿瘤药物的研发起到重要作用。
最早报道 CP T 手性合成的是 Corey 等 [ 8 ] 。
尽管该方法产率很低 ,但极有创意 ,通过手性的假酸氯代物 ( 环 E) 与三环二胺 ( 环 A ,B ,C) 反应 ,经中间体 r2醛2t2胺环化形成环 D 。
环 E 中 3 ,42二取代呋喃α2羟酸 ( 6) 的拆分经非对映异构体喹啉盐和内酯中季羟基的保护形成有光学活性的 7 ,光照氧化 ,DM F 中经 SOCl2 处理得 8 ,再经三环胺 ( 9) 缩合即可到到 ( S) 2CP T 。
Ejima 等[ 10 ] 则通过一个新的非对映异构体乙基化反应过程合成( S) 2CP T 。
喜树碱的全合成研究进展

最早报道 CP T 手性合成的是 Corey 等[ 8] 。尽管该方法产率很低 , 但极有创意 , 通过手性的假酸 氯代物 ( 环 E) 与三环二胺 ( 环 A, B, C) 反应 , 经中间体 r 醛 t 胺环化形成环 D。环 E 中 3, 4 二取代呋 喃 羟酸 ( 6) 的拆分经非对映异构体喹啉盐和内酯中季羟基的保护形成有光学活性的 7 , 光照氧化, DMF 中经 SOCl2 处理得 8 , 再经三环胺( 9) 缩合即可到到 ( S) CPT 。
[ 1] [ 2] [ 3] [ 4] [ 5] [ 6] [ 7] [ 8] [ 9] [ 10] [ 11] [ 12] [ 13] [ 14] [ 15] [ 16] Wall, M . E. ; Wani, M . C. ; Cook, C. E. , et al. : J. Am. Chem. Soc. , 1966, 88, 3888. Schultz, A. G. : Chem, Rev. , 1973, 73, 385. 上海药物研究所 : 中华医学杂志 , 1975, 55, 274. Hsiang , Y . H. ; Hertzber g, R . ; Hecht, S. , et al. : J. Biol. Chem. , 1985, 260, 14873. K ingsbur y, W . D. ; Bochm, J. C. ; Jakas, D. R . , et al. : J. M ed. Chem. , 1991, 34, 98. Saw ada, S. : Chem. Pham. Bull. , 1991, 39, 1446. Wall, M . E. : J. M ed. Chem. , 1987, 30( 12) , 2317. Cor ey , E. J. ; Crouse, D. N. ; Anderson, J. E. , et al. : J. Or g. Chem. , 1975, 40, 2140. T agawa, H. : JP. App. No. JP 85 296 127. Ejima, A . ; T er asaw a, H. ; Gima, A. , et al. : T etrahedro n L ett. , 1989, 30( 20) , 2639. Comins, D. L. ; Baevsky, M . F . ; Hong, H. , et al. : T etrahedron Lett. , 1993, 34, 801. F ortunak, J. M . D. ; K itter ing ham, J. ; M astrocola, A. R. , et al. : T etrahedron Lett. , 1996, 37( 32) , 5683. F ang, F. G. ; Xie, S. P . ; Lowery , M . W. : J. Org. Cehm. , 1994, 59, 6142. Shar pless, K. B. : Cataly tic Asynmetr ic Sythesis; VCH P ublishers, N Y, 1993. Ciufolini, M . A . : T etrahedron, 1997, 53( 32) , 11049. M urata, N . : Syn. L ett. , 1997, ( 3) , 298.
喜树碱及其衍生物提取工艺进展研究

喜树碱及其衍生物提取工艺进展研究朱宏宇(西南林业大学,云南昆明)摘要:喜树碱(CPT)是一种细胞毒性喹啉生物碱,可以抑制DNA酶拓扑异构酶I.1966年,M.E. Wall和M.C. Wani 等从喜树植物中分离出喜树碱并认为其是一种天然的抗癌药物。
实验室提取喜树碱及其衍生物的方法多为乙醇为溶剂,使用微波法、浸提法、超声波法或匀浆提取法从树木的叶子中提取喜树碱及其衍生物。
有研究通过正交试验对提取温度、提取时间以及匀浆时间对提取效率的影响进行了分析。
笔者将从简单综述以上多种喜树碱及其提取工艺,并简述各种工艺操作的优缺点。
关键字:喜树碱;提取工艺;研究进展Research of Extraction Methods for Camptothecin and its derivatives from Camptotheca acuminataAbstract: Camptothecin (CPT) is a cytotoxic quinoline alkaloid which inhibits the DNA enzyme topoisomerase I (topo I). It was discovered in 1966 by M. E. Wall and M. C. Wani in systematic screening of natural products for anticancer drugs. Using ethanol as solvem, 4 metllods including stirring extraction,homogenate extraction,ultrasonic extraction or microwave—assisted extraction were adopted to extract camptothecinand its derivatives from Camptotheca acuminata.Studies through the orthogonal experiment of extracting temperature, extracting time and the influence of homogenate of time on the extraction efficiency were analyzed.The author will from simple overview over a variety of camptothecin and its extraction technology, and describes the advantages and disadvantages of various process operations.Key words:camptothecin; Extraction process; Research progress喜树碱(Camptothecin,CPT)喜树(Camptotheca acuminata Decaisne)为山茱萸目(Cornlales)珙桐科(Nyssaceae)旱莲属植物。
浅谈抗肿瘤药物喜树碱的研究进展

浅谈抗肿瘤药物喜树碱的研究进展喜树碱是从我国特有的珙桐科植物喜树中分离得到的具有很强抗癌活性的天然化合物。
其有效的抗癌能力及独特的抗癌作用机理引起科学界的极大兴趣。
但是因为其水溶性差、副作用大等因素,使其临床应用受到限制。
所以针对喜树碱的分子修饰及剂型的改造是研究的热点。
本文针对喜树碱的作用机理、分子修饰及剂型研究等做了概述。
1作用机理目前相对来说,无论是临床还是处在研究阶段的抗癌药物,作为哺乳动物异构酶Ⅱ型毒素的药物较多,只有极少数的药物作为拓扑异构酶Ⅰ型毒素。
其中喜树碱及其类似物是研究最为广泛的拓扑异构酶Ⅰ型毒素。
DNA拓扑异构酶有两类,拓扑异构酶Ⅰ是与双链DNA解旋有关的酶,它的作用是暂时切断一条DNA 链,形成拓扑异构酶Ⅰ-DNA共价中间物而松弛化超螺旋DNA,然后再将切断的单链DNA连接起来,不需要任何辅助因子。
研究表明喜树碱类药物能阻断拓扑异构酶Ⅰ的修复作用,从而起到抗癌效果。
2分子修饰喜树碱为五环结构,由共轭吡啶环、吡咯喹啉环和六元羟基内酯环组成,其中20S-2-羟基、E环的-2-羟基内酯和D环的氢化吡啶酮是保持活性的必要结构。
喜树碱的分子改造是在保持这些必需活性基团存在的前提下进行结构修饰而得,且大多是在C7、C9、C10位进行基团修饰,以增加喜树碱的稳定性及改善药物的溶解性。
研究人员对不同位点结构修饰的喜树碱新衍生物内酯环稳定性进行研究后发现:在10位与20位引入含氮杂环修饰喜树碱均能显著提高其内酯环的稳定性,在所连接的取代基团中,以吡唑和羟基修饰后的喜树碱内酯环最为稳定,且不受取代位置影响,这与药效学考察结果一致,药效学研究显示这两个取代基所得到的化合物抗肿瘤效果良好,所测定其他取代基修饰的喜树碱衍生物内酯环也较稳定,但在水解过程中可能会受到取代位置的影响,从而得到不同的水解产物。
总之,无论在10位还是20位修饰的喜树碱衍生物均能有效提高内酯环的稳定性。
3喜树碱类药物的剂型31纳米乳纳米乳是一种新型药物传递系统,它能够提高药物的水溶性,使药物在体内更加稳定,同时降低药物毒副作用,并且在缓、控释和基因传输等方面有着广泛的应用。
喜树碱类抗癌药物纳米制剂的研究进展

喜树碱类抗癌药物纳米制剂的研究进展1. 引言1.1 喜树碱类抗癌药物的背景喜树碱类抗癌药物是一类来源于马兜铃科植物的生物碱化合物,具有抗肿瘤作用。
自从20世纪中期发现喜树碱的抗癌活性以来,科学家们就对其进行了深入研究,希望能够利用这一类化合物来治疗癌症。
喜树碱类抗癌药物的作用机制主要包括干扰肿瘤细胞的有丝分裂、抑制DNA合成、促进细胞凋亡等,从而达到抑制肿瘤细胞增殖和扩散的效果。
喜树碱类抗癌药物在临床应用中也存在一些问题,比如副作用较大、药效不稳定等。
为了解决这些问题,科研人员开始探索利用纳米技术来制备喜树碱类抗癌药物的纳米制剂。
纳米制剂可以改善药物的药效和减少副作用,从而提高药物在治疗癌症中的效果。
研究喜树碱类抗癌药物纳米制剂成为当前癌症治疗领域的热点之一。
【字数:227】。
1.2 纳米制剂在癌症治疗中的应用在癌症治疗中,纳米制剂可以有效地减少药物的副作用,提高药物的靶向性,减少给患者带来的伤害。
由于纳米制剂的微观尺度,可以更好地穿透肿瘤组织,将药物释放到靶向部位,减少对正常组织的损伤。
纳米制剂还可以提高抗药性癌症细胞对药物的敏感性,从而提高药物的抗肿瘤效果。
通过纳米技术,可以将药物包裹在纳米粒子中,增加药物在细胞内的停留时间,提高药物的疗效。
纳米制剂在癌症治疗中的应用为喜树碱类抗癌药物的研究带来了新的希望和可能性。
通过纳米技术的引入,可以更好地克服传统药物的局限性,提高治疗效果,为癌症患者带来更好的治疗体验。
2. 正文2.1 纳米载体技术在喜树碱类抗癌药物纳米制剂中的应用纳米载体技术在喜树碱类抗癌药物纳米制剂中的应用是近年来癌症治疗领域的重要研究方向之一。
纳米载体技术可以将喜树碱类抗癌药物封装在纳米粒子中,有效地提高药物的溶解度和稳定性,延长药物在体内的循环时间,并增加药物在靶细胞内的富集度。
通过纳米载体技术,喜树碱类药物可以更准确地传递到癌细胞表面,减少对健康组织的损害。
纳米载体还可以调控药物的释放速度和途径,实现对药物释放的精准控制,从而增强药物疗效并降低副作用。
喜树碱是一种植物抗癌药物

3 分析讨论近几年中药逐渐被国外所认同。
青蒿素作为治疗疟疾的良药,以被国际认同,并远销非洲。
中药有效成分的提取发展变的迅速起来,除了传统的提取方法,各种新的方法也逐渐发展起来。
天诚公司主要经营各种中草药原料的提取,然后将其产品出售给成品药生产公司。
天诚公司应用的还是传统的中药提取方法,所用设备比较落后。
当然,公司以利润效益为主。
中药有效成分的提取是一个复杂的过程,当中药样品加入溶剂后,溶剂通过浸泡扩散作用,将中药所含的化学成分逐渐溶解,使其扩散到溶剂中,直到细胞内外溶液中被溶解的化学成分的浓度达到平衡。
因此,在提取过程中,中药的粉碎度、提取温度、时间、溶剂等,都是影响提取的因素,必须选用合理的条件,提高有效成分的提取率。
(1)温度对提取质量的影响渗透、溶解、扩散能力随温度升高而增大,溶液的黏度随温度升高而降低,因此,提取中加热可加强分子运动,又可软化组织,提高溶解度,加速扩散,从而提高提取率。
但对含有多量淀粉、黏液质等多糖类的中草药,由于加热可增加它们在水中的溶解度或有效成分遇热易分解,因而影响过滤速度或成品疗效,故应避免加热提取。
对新鲜中草药,加热能将阻滞扩散与渗透的原生质凝固,因而有利于成分的提取。
用有机溶剂提取中草药时,加热虽可提高提取率,但需注意防止溶剂挥发损失,且应注意操作安全。
(2)提取时间对提取质量的影响中草药成分的提取率随提取时间的延长而增加,直至达到平衡为止。
当然过长是没有必要的,不仅浪费时间,且往往使无效成分随时间延长而大量提出,影响质量。
如在对大黄主要成分结合型大黄酸的提取时,用很短的热浸法煮沸3min,其含量可达最高值,几乎接近原料生药中的含量。
与此相反,提取黄连中的小檗碱和黄连碱时,要加入大量的水,进行较长时间的提取,才能使有效成分溶出。
所以应当选择合适的提取时间。
目前水煎中药一般以煮沸后再煎0.5h即可,用乙醇加热提取则多为煮沸后再延长0.5~1h。
(3)粉碎度对提取质量的影响中草药粉末的表面积越大即药粉越细,提取率越高。
喜树碱类抗癌药物纳米制剂的研究进展

喜树碱类抗癌药物纳米制剂的研究进展喜树碱是一种来源于喜树科植物的天然化合物,具有抗肿瘤活性。
喜树碱类药物在临床上应用受到了一些限制,如药物的疗效和毒副作用之间的平衡以及药物的生物利用度等。
近年来,通过纳米技术对喜树碱类药物进行制剂改进已成为研究的热点之一。
本文将综述喜树碱类抗癌药物纳米制剂的研究进展。
目前,对于喜树碱类药物纳米制剂的研究主要集中在三个方面:载体材料的选择、制剂方法的优化和药物释放机制的研究。
在载体材料的选择中,常用的纳米载体材料包括脂质体、聚合物纳米粒子、金属纳米粒子等。
脂质体是最常用的载体材料之一,其优点是结构简单、生物相容性好。
聚合物纳米粒子具有良好的稳定性和可调控性。
金属纳米粒子具有较高的比表面积和特殊的物理化学性质。
通过选择不同的纳米载体材料,可以实现喜树碱类药物的靶向输送、缓释释放等功能。
在制剂方法的优化中,常用的方法有乳化法、溶剂挥发法、共沉淀法等。
乳化法是最常用的制备脂质体和聚合物纳米粒子的方法之一,其原理是通过机械剪切等作用使药物包裹在纳米粒子中。
溶剂挥发法是制备聚合物纳米粒子的一种常用方法,其优点是操作简单、成本低。
共沉淀法是制备金属纳米粒子的常用方法,其优点是可以在溶剂中一步生成纳米粒子。
通过优化制剂方法,可以提高制剂的稳定性和药物的包封率。
在药物释放机制的研究中,常用的方法有扫描电镜、透射电镜、动态光散射等。
扫描电镜可以观察制剂的粒径和形态。
透射电镜可以观察制剂的内部结构。
动态光散射可以分析制剂的粒径分布和稳定性。
通过研究药物的释放机制,可以了解纳米制剂在体内的释放行为,进而优化制剂的释放性能。
喜树碱类抗癌药物纳米制剂的研究是当前药物纳米技术研究的热点之一。
通过选择合适的载体材料、优化制剂方法和研究药物的释放机制,可以提高药物的生物利用度和抗肿瘤活性,为抗癌药物的临床应用提供新的思路和方法。
抗癌药物——喜树碱类衍生物研究进展

1] 1
『1 2
l u D “ r bD a
J
肿 2 1 9 1 6:0 5 .9 6,5 2 9
.9 1 99. 8 8 9 82 2 4: 1 — 2
13 0
Ta g HL e n taL &
Mo B a.N t m帆 .0 12:2 — 1 8 1 a 2 0 , 13 2
Ca E h in K
2 7 53
『 3’ Kao t l m ah 12 0 . 5 1 6 — 1 7 1 tu F e o A J P t o . 0 1 1 8:2 3 2 0
至8 O年代 , 发现 了喜 树碱 作为细胞核 中拓扑 异构酶 I 制剂 的新 作用 机制 , 抑 又引起 国 内 外 医药 界极 大 的 重 视 , 而 以 拓 扑 异 构 酶 I 从 为分子模 型 , 计 并合成 了一 系 列新 型抗 癌 设
药物 。
拓 扑 异 构 酶 I的催 化 活 性 分 4步 完 成 : ( )T p I与 D A结 合 使 双链 解 旋 ; 2) 1 oo N ( 使
村 碱 类 衍 生 物
1 拓 扑 异 构 酶 I 制剂 的 作 用 机 制 . 抑 喜 树 碱 ( a ttei C T) 印 年 代 empohen, P 是 从 我 国植 物 喜 树 中提 取 分 离 的 一 种 化 合 物 , 通过体外研 究发 现 了喜树 碱 的抗肿 瘤 活性 。 最 早 的 临床 研究 也 证 实 了这 些 临床 前 研究 的 结 果 , 而 , 于 不可 预 知 的 副 反 应 如 出 血性 然 由 膀胱炎 , 以及 药 物 的 溶 解 性 问 题 ,O年 代 停 7 止 了将 喜 树 碱 作 为 细 胞 毒 性 药 物 的研 究 。 直
喜树碱结构改造的研究进展

喜树碱结构改造的研究进展(杨治刚,12331161,安徽中医药大学)摘要喜树碱是从我国特有植物喜树中分离得到的。
它是一种广谱杭癌药物,对多种肿瘤有疗效,但同时也有副作用。
为了寻找一种既具杭癌活性,毒性又小的喜树碱类似物,国外学者对喜树碱的五个环分别进行了修饰,并对修饰产物进行了药理研究,找到了杭癌活性与结构之间的关系。
本文着重介绍他们的研究结果并简要总结一下喜树碱的结构、性质。
AbstractCamptothecin was isolated from the tree Camptotheca acuminate, Nyssaceae, a native of China. It is abroad spectrum antitumor drug, efficient to a series of tumors, but by-effective. In order to find camptothecin analogues with high-antitumor activities but low-toxicities, for-eign scholars have modified the five rings of camptothecin and studied the pharmacology of modified products, they found out the correlations between the structure and the activities. This paper focuses on introducing these results and Summarizing the structure, characters of camPtothecin. 关键字喜树碱,结构改造,生物碱,广谱抗癌,抗肿瘤喜树碱是一种植物抗癌药物,从中国中南、西南分布的喜树中提取得到。
喜树碱类抗癌药物的研究进展

南京师范大学研究生课程学习考试成绩单(试卷封面)任课教师签名:批改日期:注:1、以撰写论文为考核形式的,填写此表,综合考试可不填;2、本成绩单由任课教师填写,填好后与作业(试卷)一并送院(系)研究生秘书处;3、学位课总评成绩须以百分制记分。
喜树碱类抗癌药物的研究进展王坤(111102026 分析化学化学与材料科学学院)摘要:喜树碱类药物是用于临床的拓扑异构酶Ⅰ抑制剂,是继紫杉醇后又一个很有发展前途的抗癌药,已成为目前抗癌药物中研究的热点。
20-(S)-喜树碱(CPT) 是一种具有广谱抗癌活性的生物碱,其抗癌活性主要体现在CPT的内酯环能够与DNA拓扑异构酶І结合并异化DNA拓扑结构,进而诱导肿瘤细胞的凋亡。
然而,喜树碱内酯环在生理环境下极易水解开环形成羧酸盐,导致药物失活;同时喜树碱本身所存在的水溶性差、对正常机体组织毒副作用大等缺点也极大限制了CPT的临床应用。
因此,针对提高CPT稳定性、水溶性及靶向性的改性研究对推广CPT的临床应用具有重要意义。
本文主要介绍了最近几年关于喜树碱改性方面的一些工作,包括针对CPT的A、B和内酯E环上活泼氢改性得到的小分子衍生物及前体药物,以及利用共价或非共价键合作用设计合成的聚合物或天然大分子以及胶束等可担载喜树碱的给药系统等关键词:抗肿瘤药物;喜树碱;作用机理;改性喜树为山茱萸目珙桐科乔木植物,是我国特有的一种高大落叶乔木,广泛分布于长江流域及西南各省区。
1966年美国的Monroe E. Wall首次从喜树茎的提取物中分离出喜树碱(camptothecin,CPT),随后人们研究发现喜树碱对胃肠道肿瘤、膀胱癌、肝癌和白血病等恶性肿瘤[9]均有一定疗效。
但它也产生了一定的副作用包括骨髓抑制、呕吐、腹泻和严重的出血性膀胱炎等,在随后的十多年间相关研究大大减少,临床应用几乎陷入停顿。
直到1985年发现喜树碱能阻断拓扑异构酶Ⅰ(TopoⅠ)的合成,TopoⅠ是一种与细胞分裂密切相关的一种酶,阻断这种酶的产生即可阻止癌细胞的生长,说明喜树碱的作用靶标是TopoⅠ而不是拓扑异构酶Ⅱ( TopoⅡ),这正是喜树碱独特的抗癌机制,从而使喜树碱的研究进入了一个全新的阶段。
喜树碱的药物设计-靶向癌细胞死亡和基因

• 20-(S)-Camptothecin (CPT)最早是在1966年,由 美国旳Wall等从中国特有旳珙桐科植物喜树中提 取到旳,由美国国立肿瘤研究所(NCI)动物模型 上证明其抗肿瘤作用,并将其水溶性钠盐用于临床 试验。在过去旳四十年,从大量旳植物科中发觉了 这种单萜吲哚类生物碱,涉及茜草科、夹竹桃科、 钩吻科、茶茱萸科等。
• CPT类化合物旳作用机制是参加TopoⅠ作用过程 中与DNA形成旳“可切割复合物”,阻碍DNA 链旳闭合,造成细胞DNA单链断裂(SSB), 这种单链断裂对细胞来说并不是致死性旳,当可 切割复合物与正在进行复制旳DNA复制又相遇 时,会继发性旳造成不可逆旳DNA双链断裂 (DSB),最终引起细胞死亡。
• 氟尿嘧啶是目前临床上应用最广旳抗嘧啶类药 物,对多种肿瘤如消化道肿瘤、乳腺癌、卵巢 癌、子宫颈癌、肝癌、膀胱癌等都有一定疗效。
• 不良反应:1.胃肠道:迟发性腹泻(给药24h 后发生旳腹泻)、恶心与呕吐、厌食、腹痛及 黏膜炎。2.血液学:中性粒细胞降低。3.急性 胆碱能综合症:主要症状为:早发性腹泻及其
他症状,如用药后第一种二十四小时内发生:
腹痛、结膜炎、鼻炎、低血压、血管舒张、出
汗、寒战、全身不适、头晕、视力障碍、瞳孔
2.喜树碱:拓扑异构酶ⅠDNA复合体旳分子钳
• DNA拓扑异构酶Ⅰ是生物体内及其主要旳细胞 核内酶,参加DNA复制、转录、重组和修复等 全部关键旳核内过程。拓扑异构酶Ⅰ为单体性 100kDa旳多肽,由染色体20q12~13.2位基因编 码,可松解过分卷曲旳DNA双链,以利于复制 及转录旳进行。酶先与DNA结合,成为可断裂 复合物,在DNA磷酸二酯键上形成一种单链缺 口,让未受损旳单链从缺口中回转,使DNA松 弛,以利于复制或转录,随即将缺口连接。
抗癌药物喜树碱的功能化改

• Huang等比较了这3类脂质体作为喜树碱载体的 优缺点,发现由甘油棕榈酸硬脂酸酯 (PrecirolATO5)与水溶性乳化剂Myverol制备得 到的固体脂质纳米粒因具有良好的持续释药、高 效的细胞杀伤性能、较低的溶血性和高载药量而 可作为CPT的脂质体类载药体系。最近,Shen等 提出了一种多功能、类脂质体胶囊载药体系。该 体系以CPT作为疏水链,以寡聚PEG为亲水头, 以减少载药体系中不必要的惰性成分,该体系不 仅可以作为CPT的前药发挥抗癌活性,同时作为 纳米胶囊,对喜树碱的载药率高达58%,并能用 于如盐酸阿霉素(DOX· HCl)等亲水药物的包裹。
存在问题
• CPT的水溶性差、毒副作用大以及在生理 条件下80%的CPT会因发生开环而失去抗 癌活性等,极大地限制了它的临床应用。 喜树碱在体内会发生内酯环形式与羧酸盐 形式的转变(图式1),因此提高喜树碱内酯E 环的稳定性,降低对正常组织的细胞毒性, 同时保持高效的抗癌活性,是推广喜树碱 在抗癌领域应用的前提条件
抗癌作用机理
DNA拓扑异构酶 DNA拓扑异构酶存在于细胞核中,可与 DNA主链上的磷酸二酯基团共价结合形 成可瞬间断裂的二元复合物,连接键的断 裂将超螺旋DNA结构中的扭力释放出来, 进而形成具有正常拓扑结构的DNA链,从 而完成细胞DNA的复制和RNA的转录。根 据拓扑异构酶是与单链还是双链DNA作用 将其分为topⅠ型和topⅡ型。
生物中的成功代表。
拓扑替康相关信息
拓扑替康
英文名称中文名称 Topotecan 拓普替康 123948-87-8 C23H23N3O5 421.4458 中文别名 CAS RN
•Thank
EINECS号 分子式 分子量 危险品标志 风险术语
安全术语 物化性质 用 途源自you用作抗肿瘤药伊立替康
喜树碱全合成方法的研究进展
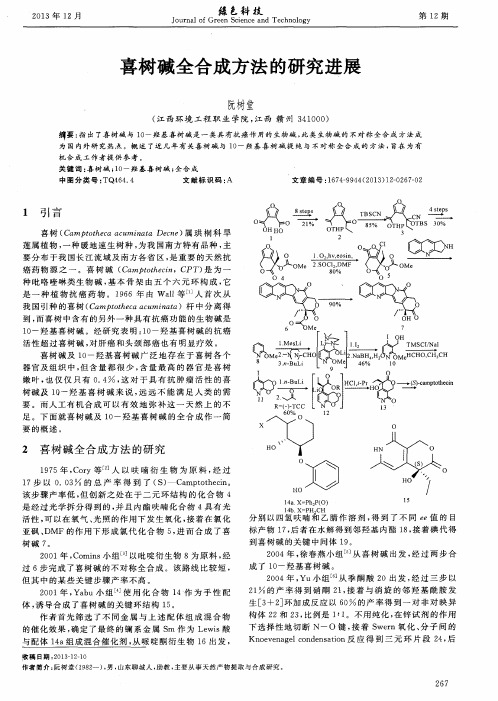
过 6步 完 成 了喜 树 碱 的 不 对 称 全 合 成 。该 路 线 比较 短 ,
但 其 中 的某 些 关 键 步 骤 产 率 不 高 。 2 0 0 1年 , Ya b u小 组 I 4 使用 化 合物 1 4作 为 手 性 配
2 1 的产率得 到硝 酮 2 1 , 接 着 与 消 旋 的 邻 羟 基 酰 胺 发
2 0 0 4年 , Yu小 组 _ 6 从 季酮酸 2 O出 发 , 经 过 三 步 以
亚砜 、 D MF的作 用 下形 成 氯 代 化 合 物 5 , 进 而 合 成 了 喜 树碱 7 。
2 0 0 1年 , C o mi n s小 组 以 吡 啶衍 生 物 8为 原 料 , 经
捕要 : 指 出 了喜 树 碱 与 1 O 一羟 基 喜 树 碱 是 一 类 具 有 抗 癌 作 用 的 生 物碱 , 此 类 生物 碱 的 不 对 称 全 合 成 方 法 成 为 国 内 外研 究 热 点 。概 述 了近 几 年 有 关 喜 树 碱 与 1 O 一羟基喜树碱 提 纯与不对 称全合成 的方 法, 旨在 为 有
2 0 1 3 年1 2 月
J o u r n a 1 Байду номын сангаас o f Gr e e n S c i e n c e a n d T e c h n o l o g y
缘 色科 技
第 1 2期
喜树碱全合成方法 的研究进展
阮 树堂
( 江西 环境 工程 职业 学院 , 江西 赣州 3 4 1 0 0 0 )
Kn o e v e n a g e l c o n d e n s a t i o n反 应 得 到 三 元 环 片 段 2 4 , 后
体, 诱 导 合 成 了喜 树 碱 的关 键 环 结 构 1 5 。 作 者 首 先 筛 选 了不 同 金 属 与 上 述 配 体 组 成 混 合 物 的催 化 效 果 , 确 定 了最 终 的镧 系 金 属 S m 作为 L e w i s 酸 与配体 1 4 a 组成混合催化剂 , 从 哌 啶酮 衍 生 物 1 6出发 ,
植物喜树碱生物合成代谢途径研究

植物喜树碱生物合成代谢途径研究植物喜树碱是一类广泛存在于植物中的次生代谢产物,其结构多样,具有重要的生理活性和药用价值。
近年来,随着对植物喜树碱生物合成代谢途径的研究不断深入,人们对于它的生理作用和开发利用的认识也日益加深。
一、喜树碱的概述喜树碱是一类氮杂环化合物,结构复杂,存在于广泛的植物中,如番茄、菠菜、柑橘等。
喜树碱具有广泛的生理活性和药用价值,如兴奋中枢神经、抗氧化、抗肿瘤、抗菌、抗病毒等作用。
对于喜树碱的生物合成代谢途径的深入研究,不仅可以揭示植物次生代谢调控原理,还可能为开发新型抗癌药物、农药、食品保鲜剂等提供理论依据和技术支持。
二、喜树碱的生物合成代谢途径喜树碱的生物合成代谢途径至今仍存在争议,但大致可以分为两种:甲基丙酮酸通路和型上式色氨酸途径。
其中,型上式色氨酸途径被认为是主要的喜树碱生物合成途径。
型上式色氨酸途径中,色氨酸在脱氨酶的催化下转化为吲哚丙酮酸,随后与丙酮酸经过包括四氢喜树碱•甲醇、美洲链霉菌素E、菌酸、理光碱、帕卢碱、紫锥菊碱等关键酶催化的一系列反应,合成最终产品。
其中,四氢喜树碱•甲醇催化吲哚丙酮酸与丙酮酸的首要缩合反应,其次是美洲链霉菌素E催化的两个羟基化步骤,以及最后的环醇化反应。
不同种类的植物中,喜树碱的结构和含量都存在差别,这与不同植物细胞内喜树碱代谢酶的多样性和特异性有关。
三、喜树碱生物合成途径的研究进展近年来,关于喜树碱生物合成途径的研究不断深入,涉及的领域越来越广泛,如遗传、生化、分子进化、生理学等。
其中,最新的研究成果得出,植物中可能存在多条喜树碱生物合成途径,具体途径的选择受到不同的生态环境、生长发育状态、个体差异等因素的影响。
同时,研究人员正在努力探索喜树碱生物合成调控机制、分子交互作用、多样性演化等问题。
四、喜树碱的开发利用喜树碱具有多种生理活性和药用价值,因此,开发利用其代谢途径也广泛的应用于农业和医学领域。
如在农业领域,喜树碱可以作为天然的重要农药成分,防治植物病虫害。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
南京师范大学研究生课程学习考试成绩单(试卷封面)任课教师签名:批改日期:注:1、以撰写论文为考核形式的,填写此表,综合考试可不填;2、本成绩单由任课教师填写,填好后与作业(试卷)一并送院(系)研究生秘书处;3、学位课总评成绩须以百分制记分。
喜树碱类抗癌药物的研究进展王坤(111102026 分析化学化学与材料科学学院)摘要:喜树碱类药物是用于临床的拓扑异构酶Ⅰ抑制剂,是继紫杉醇后又一个很有发展前途的抗癌药,已成为目前抗癌药物中研究的热点。
20-(S)-喜树碱(CPT) 是一种具有广谱抗癌活性的生物碱,其抗癌活性主要体现在CPT的内酯环能够与DNA拓扑异构酶І结合并异化DNA拓扑结构,进而诱导肿瘤细胞的凋亡。
然而,喜树碱内酯环在生理环境下极易水解开环形成羧酸盐,导致药物失活;同时喜树碱本身所存在的水溶性差、对正常机体组织毒副作用大等缺点也极大限制了CPT的临床应用。
因此,针对提高CPT稳定性、水溶性及靶向性的改性研究对推广CPT的临床应用具有重要意义。
本文主要介绍了最近几年关于喜树碱改性方面的一些工作,包括针对CPT的A、B和内酯E环上活泼氢改性得到的小分子衍生物及前体药物,以及利用共价或非共价键合作用设计合成的聚合物或天然大分子以及胶束等可担载喜树碱的给药系统等关键词:抗肿瘤药物;喜树碱;作用机理;改性喜树为山茱萸目珙桐科乔木植物,是我国特有的一种高大落叶乔木,广泛分布于长江流域及西南各省区。
1966年美国的Monroe E. Wall首次从喜树茎的提取物中分离出喜树碱(camptothecin,CPT),随后人们研究发现喜树碱对胃肠道肿瘤、膀胱癌、肝癌和白血病等恶性肿瘤[9]均有一定疗效。
但它也产生了一定的副作用包括骨髓抑制、呕吐、腹泻和严重的出血性膀胱炎等,在随后的十多年间相关研究大大减少,临床应用几乎陷入停顿。
直到1985年发现喜树碱能阻断拓扑异构酶Ⅰ(TopoⅠ)的合成,TopoⅠ是一种与细胞分裂密切相关的一种酶,阻断这种酶的产生即可阻止癌细胞的生长,说明喜树碱的作用靶标是TopoⅠ而不是拓扑异构酶Ⅱ( TopoⅡ),这正是喜树碱独特的抗癌机制,从而使喜树碱的研究进入了一个全新的阶段。
喜树碱衍生物类化合物已成为继紫杉醇[16]之后另一种天然植物来源的最重要的抗癌药,目前美国、日本、法国、德国、韩国和意大利的喜树碱及其衍生物研究在世界上处于领先地位。
本文主要从喜树碱小分子改性衍生物以及大分子共价或非共价键修饰的载药体系两个方面出发,综述了喜树碱功能化改性的研究进展及发展趋势望。
1 喜树碱的理化性质1.1喜树碱的分子结构喜树碱的分子式为C2OH16N2O4,分子量348.34,由4个六元环和1个五元环构成,且在E环有1个不对称中心(20S构型) (图1)。
化学名为(S)-4, 9-二羟基-4-乙基1H-吡喃-(3',4',6,7)氮茚(1,2b)-喹啉-3,14-(4H,12H)-二酮,属于喹啉类生物碱[5]。
图1 喜树碱的环结构和碳序号1.2 CPT的理化性质喜树碱为淡黄色针状晶体,熔点高达264~267℃;喜树碱类生物碱不溶于水,难溶于一般溶剂,可溶于氯仿、乙醇、乙酸、乙酸乙酯。
喜树碱的化学性质也不同于普通的生物碱,其没有明显的碱性,属于中性的喜树碱[1]。
与一般生物碱试剂无反应,如常用的检测试剂:得拉盖道夫(Dragendorft用碘化铋钾试验生物碱形成特性及加成化合物的结晶)和苯酚(FeCl3)试剂,呈阴性;吲哚分析,负反应;与各种酸不形成结晶盐;也不能用重氮甲烷或二甲基硫酸酯进行甲基化;其内酯环可被氢氧化钠在室温下打开生成盐,酸化后又重新生成喜树碱,溶于硫酸显黄绿色,紫外线下显黄绿色荧光。
喜树碱易转化成乙酯或氯代乙酯,氯代乙酯与碘化钠-丙酮反应形成碘代乙酯[7]。
2 喜树碱抗癌作用机理虽然喜树碱存在着诸多不利于临床推广使用的缺点,然而20世纪80年代,喜树碱独特的抗癌机理:与DNA 的拓扑异构酶Ⅰ作用,影响DNA的复制和RNA 的转录过程的发现使其再度被认为是一类具有良好应用前景的抗癌药物而得到广泛研究。
DNA拓扑异构酶存在于细胞核中,可与DNA主链上的磷酸二酯基团共价结合形成可瞬间断裂的二元复合物,连接键的断裂将超螺旋DNA结构中的扭力释放出来,进而形成具有正常拓扑结构的DNA链。
根据拓扑异构酶是与单链还是双链DNA作用将其分为topⅠ型和topⅡ型。
目前发现的抗癌药物主要都是与Ⅱ型DNA拓扑异构酶作用,而喜树碱则是唯一一种得到广泛研究的Ⅰ型DNA 拓扑异构酶抑制剂[2-4]。
在DNA的复制和RNA的转录过程中,型拓扑异构酶的酪氨酸羟基与单链DNA上的3'-磷酸盐反应,进而形成可分裂的二元复合物。
正常情况下,该连接键会瞬间断裂,从而完成DNA的复制或RNA的转录。
但是,当喜树碱等top Ⅰ抑制剂存在时,会与DNA-topⅠ二元复合物非共价结合,形成CPT-topⅠ-DNA三元复合物,长时间作用会使细胞复制过程出现致命的此类三元复合物,结果导致细胞凋亡。
由于CPT抗癌机理的独特性以及作用过程中不需要能量辅助因子ATP或NAD等,其应用前景被广泛看好。
然而,早期的CPT衍生物,如10-羟基-喜树碱,在体外实验中表现出良好的活性,临床效果却较差。
后期改性的衍生物如托普替康等对结肠癌等表现出较好的体内抑制活性但对脑癌等效果也较差CPT与拓扑异构酶Ⅰ的作用过程如图2所示[13,14]。
图2 喜树碱抗癌作用机理示意图3 喜树碱改性喜树碱改性过程中,必须保持内酯E环的完整性和CPT的(S)-型手性构型。
其中,喜树碱小分子衍生物和大分子给药体系是两种既能保持CPT抗癌活性又能增加水溶性、稳定性,降低毒副作用的改性方法。
3.1 喜树碱小分子衍生物3.1.1喜树碱A、B、E环的改性20世纪80年代,随着喜树碱的独特抗癌机理被发现,研究主要集中在对喜树碱活性位点的化学改性上。
研究发现,喜树碱A环上的9~12号位氢以及B 环上的7号位氢相对较为活泼,在有效催化剂作用下,通过硝化、氧化、取代、酯化反应等可合成较为活泼的喜树碱衍生物。
特殊基团的引入不仅可有效改变CPT 的溶解性,增加稳定性,还可以在此基础上进行更多的改性除此之外,桥接键、扩环反应等也常用于喜树碱改性中[6]。
与A 、B环相比,喜树碱的CD环较稳定,因而相关改性研究尚未见报道E环的完整性和稳定性是喜树碱发挥抗癌活性的关键因素,但对E环氢的改性较难协调好内酯环稳定性和抗癌活性之间的关系。
随后发现20位羟基的酯化反应不仅能提高喜树碱的溶解性和抗癌活性,同时内酯环稳定性也得到极大改善9号位被三级胺取代的托普替康(topotecan)以及7号位和10号位分别被乙基及二哌啶氨基甲酸酯取代的依立替康( irinotecan)是喜树碱小分子衍生物中的成功代表。
表1总结了喜树碱A、B、E 环小分子衍生物的结构特点及优缺点和应用[8]。
近几年关于喜树碱小分子改性方面的研究热情与20多年前相比已有所减少,目前更多的研究集中在对已有的小分子衍生物的临床疗效的测评和治疗方式的优化上。
表1 喜树碱A/B/E环活泼氢改性衍生物的优缺点及其应用3.1.2 喜树碱的前体药物小分子前药(prodrug)是一类不同于大分子载药体系的药物改性方式,它一般需要利用人体自身对该前药的某些特殊官能团的刺激响应机制,使小分子前药体系在达到靶向部位之后才将药物释放而小分子则被机体吸收降解。
与未改性药物相比,小分子前药不仅降低了药物对正常细胞的毒副作用。
增加药物的稳定性和水溶性,同时机体自身代谢使药物释放行为更理想。
前药体系的刺激响应机制多种多样,如酶催化型、氧化还原敏感型、pH敏感型等。
已经获得临床应用的依立替康即是一种喜树碱小分子衍生前药体系的成功例子,它利用肿瘤细胞的羧酸酯酶2(hCE-2)含量高于正常细胞这一特点,使前药在hCE-2和肝微粒体(human hepatic microsomes)作用下代谢为7-乙基-10-羟基-喜树碱而发挥药效。
肽酶对肽键的敏感释放也是一种常见的前药设计机制。
如Henne等设计的叶酸介导的靶向及S~S还原敏感型可控释放的喜树碱前药体系,也是利用肿瘤细胞内叶酸和谷胱甘肽的过度表达,达到靶向和可控释放的双重功效。
然而由于病人之间的个体差异,使人体内的酶含量也不尽相同,导致病人对酶敏感型前药的反应也参差不齐,对此Ohwada等研究了一种水溶性的pH敏感型前药体系,可获得较为单一的生物学数据,目前正在进行I期临床试验Endo 等也设计了一种pH敏感的的前药体系,有望实现临床应用[10]。
3.2 喜树碱的控制释放体系随着纳米科技的蓬勃发展,纳米材料的小尺寸效应使其穿越人体天然屏障而进入细胞成为可能通过共价或非共价键作用将CPT与这些纳米尺寸的功能性大分子相连,形成纳米载药体系是喜树碱改性的另一重要途径。
纳米载药体系一方面可以提高药物稳定性和溶解性及生物利用率,另一方面还可以利用肿瘤细胞对大分子良好的通透效应和对某些修饰基团的靶向选择性,使复合体系进入细胞膜杀死癌细胞。
常用到的大分子载药体系主要包括聚合物纳米颗粒、聚合物胶束、水凝胶、微乳液等。
3.2.1喜树碱的纳米微球制剂用于运载喜树碱的大分子纳米颗粒主要是聚合物,因为聚合物纳米颗粒尺寸可控,结构可自行设计,同时链段上活性位点较多,可进行多样化改性,被广泛用于制备CPT载药系统,比如,线性聚乙二醇(PEG)、聚羟丙甲基丙烯酰胺(PHPMA)、聚丙交酯-聚乙交酯(PLGA)、聚酰胺-胺(PAMAM)、聚乙二醇-聚赖氨酸(PEG/PLL)等[15]。
制备喜树碱-聚合物纳米微球制剂的一般步骤为:先对聚合物和喜树碱分别进行活化,然后各自的活性基团反应形成含可降解的酯键或肽键的纳米微球制剂载药体系进入人体后发生多肽酶解或水解,而聚合物链段要么被机体降解,要么被肾脏排出体外。
选择不同的键合可调控药物的释放速率。
IT-101是第一个进入临床治疗的喜树碱的聚合物类药物载体,它是一种以PEG和环糊精(CD)为骨架的聚合物载体,以寡聚肽链与CPT键合,形成10nm 左右的聚合物-喜树碱纳米链,纳米链自组装成直径为50nm左右的纳米微球。
载药微球进入细胞后,酯键被降解而将药物缓慢释放,聚合物则分散为单条链段,通过肾脏排出体外。
除此之外,具有高稳定性、水溶性、靶向性以及缓控释性的多功能聚合物纳米微球制剂也被设计出来。
比如,Minko等对PEG进行纤维素酰化(PEG-biotin) 改性,使肿瘤细胞对生物素酰化的PEG-CPT载药体系的通透性增大,因而对癌细胞杀伤力也更大。
为了进一步提高载药量,树枝状聚合物因具有可精确控制其尺寸、形状、密度、极性、溶解性而且功能性基团多、载药量高等特点,也被广泛用于CPT载药体系的制备。
