化工原理(下)复习各章知识点及复习题
化工原理知识点总结复习重点(完美版)图文

第一章、流体流动一、 流体静力学 二、 流体动力学 三、 流体流动现象四、流动阻力、复杂管路、流量计一、流体静力学:● 压力的表征:静止流体中,在某一点单位面积上所受的压力,称为静压力,简称压力,俗称压强。
表压强(力)=绝对压强(力)-大气压强(力) 真空度=大气压强-绝对压大气压力、绝对压力、表压力(或真空度)之间的关系 ● 流体静力学方程式及应用:压力形式 )(2112z z g p p -+=ρ 备注:1)在静止的、连续的同一液体内,处于同一 能量形式g z p g z p 2211+=+ρρ水平面上各点压力都相等。
此方程式只适用于静止的连通着的同一种连续的流体。
应用:U 型压差计 gR p p )(021ρρ-=- 倾斜液柱压差计 微差压差计二、流体动力学● 流量质量流量 m S kg/sm S =V S ρ体积流量 V S m 3/s质量流速 G kg/m 2s(平均)流速 u m/s G=u ρ ● 连续性方程及重要引论:22112)(d d u u = ● 一实际流体的柏努利方程及应用(例题作业题) 以单位质量流体为基准:f e W pu g z W p u g z ∑+++=+++ρρ222212112121 J/kg 以单位重量流体为基准:f e h gp u g z H g p u g z ∑+++=+++ρρ222212112121 J/N=m 输送机械的有效功率: e s e W m N = 输送机械的轴功率: ηeN N =(运算效率进行简单数学变换)应用解题要点:1、 作图与确定衡算范围:指明流体流动方向,定出上、下游界面;2、 截面的选取:两截面均应与流动方向垂直;3、 基准水平面的选取:任意选取,必须与地面平行,用于确定流体位能的大小;4、 两截面上的压力:单位一致、表示方法一致;5、 单位必须一致:有关物理量的单位必须一致相匹配。
三、流体流动现象:流体流动类型及雷诺准数:(1)层流区 Re<2000 (2)过渡区 2000< Re<4000 (3)湍流区 Re>4000本质区别:(质点运动及能量损失区别)层流与端流的区分不仅在于各有不同的Re 值,更重要的是两种流型的质点运动方式有本质区别。
化工原理试题库及答案下册

化工原理试题库及答案下册一、选择题1. 在化工生产中,下列哪项不是传热的主要方式?A. 热传导B. 热对流C. 热辐射D. 热交换答案:D2. 根据牛顿冷却定律,冷却速率与温差的什么成正比?A. 一次方B. 二次方C. 三次方D. 四次方答案:A3. 在非理想溶液中,下列哪项不是影响相平衡的因素?A. 温度B. 压力C. 溶质浓度D. 溶剂质量答案:D二、填空题4. 根据菲克扩散定律,扩散通量与_______的梯度成正比。
答案:浓度5. 在填料塔中,气液两相接触面积的增大是通过使用_______来实现的。
答案:填料6. 化工生产中,塔设备的作用不包括_______。
答案:加热反应物三、简答题7. 简述板式塔与填料塔在工业应用中各自的优缺点。
答案:板式塔的优点包括结构紧凑、处理量大、操作弹性大等,缺点是造价高、安装复杂。
填料塔的优点是造价低、安装方便、适用于处理腐蚀性介质,缺点是压降大、操作弹性相对较小。
8. 描述精馏塔中回流比的重要性及其对塔性能的影响。
答案:回流比是精馏塔操作中的一个重要参数,它影响着塔内传质效率和塔的能耗。
适宜的回流比可以提高分离效率,减少能耗,但过高或过低的回流比都会导致塔性能下降。
四、计算题9. 某连续精馏塔处理100 kmol/h的原料,原料中A组分的摩尔分数为0.05。
塔顶产品中A组分的摩尔分数为0.95,塔底产品中A组分的摩尔分数为0.01。
若回流比为3,求塔顶产品和塔底产品的流量。
答案:根据物料平衡和简化的塔板理论,可以计算出塔顶产品流量为35 kmol/h,塔底产品流量为65 kmol/h。
10. 一个理想气体在绝热条件下膨胀,初始压强为p1 = 2 MPa,初始体积为V1 = 0.1 m³,最终体积为V2 = 0.3 m³。
假设气体的初始温度为T1 = 500 K,求最终的温度T2。
答案:根据理想气体状态方程和绝热过程方程,可以计算出最终的温度T2为333.33 K。
化工原理知识点总结复习重点(完美版)

无论是层流或揣流,在管道任意截面上,流体 质点的速度均沿管径而变化,管壁处速度为零,离 开管壁以后速度渐增,到管中心处速度最大。
层流:1、呈抛物线分布;2、管中心最大速度 为平均速度的2倍。
湍流:1、层流内层;2、过渡区或缓冲区;3、 湍流主体
湍流时管壁处的速度也等于零,靠近管壁的流 体仍作层流流动,这-作层流流动的流体薄层称为 层流内层或层流底层。自层流内层往管中心推移, 速度逐渐增大,出现了既非层流流动亦非完全端流 流动的区域,这区域称为缓冲层或过渡层,再往中
出上、下游界面;
2、 截面的选取:两截面均应与流动方向垂直;
3、 基准水平面的选取:任意选取,必须与地面平
行,用于确定流体位能的大小;
4、 两截面上的压力:单位一致、表示方法一致;
5、 单位必须一致:有关物理量的单位必须一致相
匹配。
三、流体流动现象:
流体流动类型及雷诺准数:
(1)层流区
Re<2000
离心泵:电动机 流体(动能)转化 静压能
一、离心泵的结构和工作原理:
离心泵的主要部件:
离
心泵的的启动流程:
叶
轮
吸液(管泵,无自吸能力)
泵壳
液体的汇集与能量的转换
转能
泵
轴
排放
密封 填料密封 机械密封(高级)
叶轮 其作用为将原动机的能量直接传给液体,
以提高液体的静压能与动能(主要为静压能)。
泵壳 具有汇集液体和能量转化双重功能。
(2)过渡区
2000< Re<4000
(3)湍流区
Re>4000
本质区别:(质点运动及能量损失区别)层流与端
流的区分不仅在于各有不同的Re 值,更重要的是
化工原理各章知识点汇总
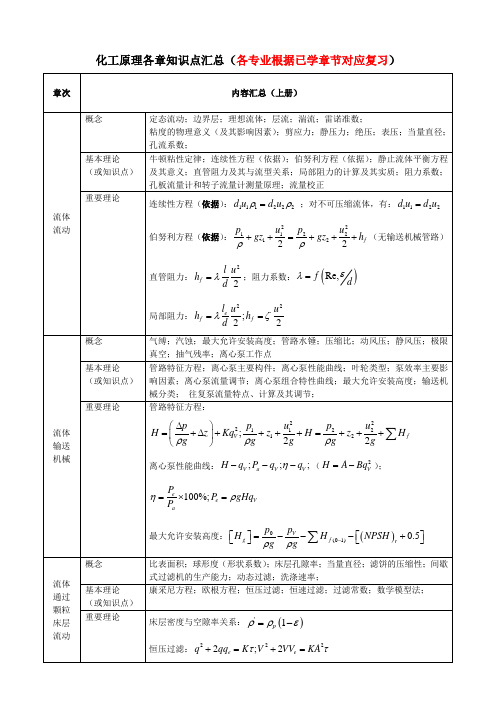
斯托克斯区:
牛顿区:
降尘室生产能力;传热Fra bibliotek概念载热体;传热速率;热流量;温度梯度;强制对流;自然对流;定性温度;汽化核心;膜状冷凝;滴状冷凝;黑体;灰体;镜体;黑度;总传热系数;壳程;管程;逆流传热;并流传热;
基本理论
(或知识点)
传热分类;傅里叶导热定律;导热系数;对流给热系数及其方程;总传热速率方程;热阻分析;黑体辐射热流量;
重要理论
负荷性能图(组成、操作弹性、调节);气液两相非理想流动;
液液
萃取
概念
萃取相;萃余相;选择性;和点;差点;萃取液;萃余液;选择性系数;
基本理论
(或知识点)
萃取剂的特点:萃取操作的适应性;液液相平衡;溶解度曲线;共轭相;杠杆定律;互溶度对萃取影响;
重要理论
单级萃取计算;
固体
干燥
概念
露点;湿度;相对湿度;湿球温度;干球温度;绝热饱和温度;湿空气的焓;湿空气的比体积;绝热增湿过程;结合水;非结合水;自由水分;干燥速率;恒速干燥;减速干燥;临界含水量;平衡含水量;干燥过程的热效率;
重要理论
相平衡方程:
连续精馏过程计算(物料衡算、热量衡算、操作线方程、q线方程、最小回流比):
逐板计算法;
气液
传质
设备
概念
液沫夹带;气泡夹带;漏液;夹带液泛;溢流液泛;板效率;返混;湿板效率;正系统;负系统;填料的特性(比表面积、空隙率、几何形状)
基本理论
(或知识点)
传质设备分类;板式塔构件;填料塔构件;筛板塔气液接触状态分类;筛板塔阻力(组成、各自特点);气液两相非理想流动;负荷性能图(组成、操作弹性、调节);液体成膜的条件;填料塔的持液量;填料塔液泛;填料塔实际气速与液泛气速的关系;填料塔的附属机构;
(完整版)化工原理下册习题及章节总结(陈敏恒版)

第八章课堂练习:1、吸收操作的基本依据是什么?答:混合气体各组分溶解度不同2、吸收溶剂的选择性指的是什么:对被分离组分溶解度高,对其它组分溶解度低3、若某气体在水中的亨利系数E值很大,说明该气体为难溶气体。
4、易溶气体溶液上方的分压低,难溶气体溶液上方的分压高。
5、解吸时溶质由液相向气相传递;压力低,温度高,将有利于解吸的进行。
6、接近常压的低浓度气液平衡系统,当总压增加时,亨利常数E不变,H 不变,相平衡常数m 减小1、①实验室用水吸收空气中的O2,过程属于(B )A、气膜控制B、液膜控制C、两相扩散控制②其气膜阻力(C)液膜阻力A、大于B、等于C、小于2、溶解度很大的气体,属于气膜控制3、当平衡线在所涉及的范围内是斜率为m的直线时,则1/Ky=1/ky+ m /kx4、若某气体在水中的亨利常数E值很大,则说明该气体为难溶气体5、总传质系数与分传质系数之间的关系为l/KL=l/kL+1/HkG,当(气膜阻力1/HkG) 项可忽略时,表示该吸收过程为液膜控制。
1、低含量气体吸收的特点是L 、G 、Ky 、Kx 、T 可按常量处理2、传质单元高度HOG分离任表征设备效能高低特性,传质单元数NOG表征了(分离任务的难易)特性。
3、吸收因子A的定义式为L/(Gm),它的几何意义表示操作线斜率与平衡线斜率之比4、当A<1时,塔高H=∞,则气液两相将于塔底达到平衡5、增加吸收剂用量,操作线的斜率增大,吸收推动力增大,则操作线向(远离)平衡线的方向偏移。
6、液气比低于(L/G)min时,吸收操作能否进行?能此时将会出现吸收效果达不到要求现象。
7、在逆流操作的吸收塔中,若其他操作条件不变而系统温度增加,则塔的气相总传质单元高度HOG将↑,总传质单元数NOG 将↓,操作线斜率(L/G)将不变。
8、若吸收剂入塔浓度x2降低,其它操作条件不变,吸收结果将使吸收率↑,出口气体浓度↓。
9、在逆流吸收塔中,吸收过程为气膜控制,若进塔液体组成x2增大,其它条件不变,则气相总传质单元高度将( A )。
化工原理复习知识点

化工原理复习知识点一、填空题:1、物料衡算的理论依据是质量守恒定律,热量衡算的理论基础是能量守恒定律。
2、雷诺数的表达式是Re=duρ/μ。
当密度ρ=1000㎏·m-3,粘度μ=1厘泊,半径d=10mm,以流速为0.15m·s-1在管中流动时,其雷诺准数等于1500,流动类型为层流。
3、流体在圆形直管中作层流流动,若流量不变,管径不变,管长增加一倍,则摩擦阻力损失为原来的2倍。
4、根据按单元操作所遵循的基本原理不同,可将单元操作分为动量传递、热量传递、质量传递。
5、离心泵主要部件有如下三部分:泵壳、叶轮、泵轴。
6、当安装高度超过允许安装高度时,离心泵会发生气蚀现象。
7、平壁稳定传热过程,通过三层厚度相同的不同材料,每层间温度变化如图所示,试判断λ1、λ2、λ3的大小顺序λ3〉λ1〉λ2,以及每层热阻的大小顺序δ3/λ3〈δ1/λ1〈δ2/λ2。
8、1140W。
(属于第二章内容)9、热量传递的基本方式有传导传热、对流传热和辐射传热。
10、精馏过程,就是利用混合液的各组分具有不同的沸点(或挥发度),利用多次部分汽化_.多次部分冷凝的方法,将各组分得以分离的过程。
11、某连续精馏塔, 已知其精馏段操作线方程为y=0.78x+0.204,则该塔的回流比R=3.54,馏出液组成xd=0.926。
12、由于吸收过程气相中的溶质分压总大于液相中溶质的平衡分压,所以吸收操作线总是在平衡线的上方。
增加吸收剂用量,操作线的斜率增大,则操作线向远离平衡线的方向偏移,吸收过程推动力(y-ye)增大。
13、用相平衡常数m表达的亨利定律表达式为y=mx。
在常压下,20℃时, 氨在空气中的分压为166mmHg, 与之平衡的氨水浓度为20(kgNH3/100kgH2O)。
此时亨利系数m=1.250。
14、当空气的湿含量一定时,其温度越高,则相对温度越低,表明空气的吸湿能力越强,所以湿空气在进入干燥器之前都要经预热器预热。
化工原理知识点总结复习重点

化工原理知识点总结复习重点化工原理是化学工程与工艺专业的一门基础课程,主要介绍化学工程与工艺中的物质平衡、能量平衡和动量平衡等基本原理及其应用。
下面是化工原理的知识点总结和复习重点的详细版:1.化学反应平衡-反应物与生成物的化学计量关系-反应的平衡常数与平衡常数表达式- Le Chatelier原理和平衡移动方向-改变反应条件对平衡的影响2.物质平衡-物质守恒定律-化学工程中常见的物质平衡问题-不可压缩流体的物质平衡-反应器中的物质平衡-非理想流动下的物质平衡3.能量平衡-能量的守恒定律-热力学一、二、三定律-热力学方程与热力学性质-各种热力学过程的分析-标准生成焓与反应焓-反应器中的能量平衡4.动量平衡-动量的守恒定律-流体的运动学性质-流体的连续性方程、动量方程和能量方程-流体的黏度、雷诺数与运动阻力-流体的流动模式与阻力系数5.质量传递-质量传递的基本概念和规律-质量传递过程中的浓度梯度-净质量流率和摩尔质量流率-质量传递的速率方程和传质系数-各种传质装置的设计和分析6.物料的流动-流体的本构关系和流变特性-流体的流变模型和流变学方程-各种物料的流动模式和流动参数-孔板、喷嘴、管道等流体动力装置的设计和分析7.反应工程学-反应器的分类与特性-反应速率方程和反应级数-决定反应速率的因素-等温、非等温反应的热力学分析-反应器的设计和分析8.分离工程学-分离过程的基本原理-平衡闪蒸和分馏过程-萃取、吸附和吸附过程-结晶和干燥过程-分离设备的设计和分析9.管道和设备-化工工艺流程图的绘制-管道的基本特性和设计原则-常见流体设备的结构和工作原理-设备的选择、设计和运行控制以上是化工原理的知识点总结和复习重点的详细版。
在复习时,需要重点掌握每个知识点的基本概念、原理和公式,并通过习题和实例进行巩固和应用。
同时,建议结合实际工程问题,加深对知识点的理解和运用能力。
《化工原理》(下)第二章 吸收第六次课

y2
−1
x2 L
此题中: x 2 = 0 , y 1 = 0.05 , V = 1500 22.4 = 67 kmol ⋅ h − 1
φ = 0 .95 , a = 93 m 2 ⋅ m -3 , H = 1 / 5 . 78 m ⋅ kN ⋅ kmol
思路就是由所求目标推至已知条件。 ( 1) 求 x 1
6
三、增大单位吸收传质面积
面积主要由设备来决定,对于填料塔,应该注意: 面积主要由设备来决定,对于填料塔,应该注意: 填料的选型,应尽量选比表面积大的填料。 填料的选型,应尽量选比表面积大的填料。 增大气液分散度,液体喷淋均匀,填料充分润湿, 增大气液分散度,液体喷淋均匀,填料充分润湿, 保证上升气泡和液层充分接触,达到传质目的。 保证上升气泡和液层充分接触,达到传质目的。 采用湍流塔,促使气液充分湍动, 采用湍流塔,促使气液充分湍动,两相接触面不 断更新,扩大了接触面积。 断更新,扩大了接触面积。
用量为最少用量的1.5 倍。该塔在30℃和101.3kN ⋅ m−2 压力下操作,在操作条件下的平衡 关系为 pe = 5.78C kN ⋅ m−2 ,试求: (已知吸收为逆流吸收过程。) (1)出塔溶液浓度 x1 ; (2)用平均推动力法求填料层高度 Z ; (3)用吸收因数法求 Z 。
12
首先列出已知条件,并用公式符号和标准单位表达出来。
4
对于易溶气体, 约等于k 是气膜控制过程; 对于易溶气体,KG约等于kG ,是气膜控制过程; 关键是降低气 膜层的厚度。增加气体总压,增加气流速度, 膜层的厚度。增加气体总压,增加气流速度,增大气相的湍动 程度,则膜分系数增大,KY=P·kG 。但是,气流速度应根据设备 但是, 程度,则膜分系数增大, =P· 大小来考虑,不能超过液流速度。 大小来考虑,不能超过液流速度。 对于难溶气体,K 约等于k 是液膜控制过程: 对于难溶气体,KL约等于kL ,是液膜控制过程: 关键是降低液膜 厚度。提高吸收剂的流速,增大液相的湍流程度, 厚度。提高吸收剂的流速,增大液相的湍流程度,使液膜分系 数增大,KX约等于C·kL 。 数增大, 约等于C 溶解度适中的气体,其吸收速度由两个膜控制,同时增大气相 溶解度适中的气体,其吸收速度由两个膜控制, 和液相流速,增大两相的湍动程度,从而减小两膜的厚度。 和液相流速,增大两相的湍动程度,从而减小两膜的厚度。
化工原理各章节知识点总结

第一章流体流动质点含有大量分子的流体微团,其尺寸远小于设备尺寸,但比起分子自由程却要大得多.连续性假定假定流体是由大量质点组成的、彼此间没有间隙、完全充满所占空间的连续介质.拉格朗日法选定一个流体质点,对其跟踪观察,描述其运动参数如位移、速度等与时间的关系.欧拉法在固定空间位置上观察流体质点的运动情况,如空间各点的速度、压强、密度等,即直接描述各有关运动参数在空间各点的分布情况和随时间的变化.定态流动流场中各点流体的速度u、压强p不随时间而变化.轨线与流线轨线是同一流体质点在不同时间的位置连线,是拉格朗日法考察的结果.流线是同一瞬间不同质点在速度方向上的连线,是欧拉法考察的结果.系统与控制体系统是采用拉格朗日法考察流体的.控制体是采用欧拉法考察流体的.理想流体与实际流体的区别理想流体粘度为零,而实际流体粘度不为零. 粘性的物理本质分子间的引力和分子的热运动.通常液体的粘度随温度增加而减小,因为液体分子间距离较小,以分子间的引力为主.气体的粘度随温度上升而增大,因为气体分子间距离较大,以分子的热运动为主.总势能流体的压强能与位能之和.可压缩流体与不可压缩流体的区别流体的密度是否与压强有关.有关的称为可压缩流体,无关的称为不可压缩流体.伯努利方程的物理意义流体流动中的位能、压强能、动能之和保持不变. 平均流速流体的平均流速是以体积流量相同为原则的.动能校正因子实际动能之平均值与平均速度之动能的比值.均匀分布同一横截面上流体速度相同.均匀流段各流线都是平行的直线并与截面垂直,在定态流动条件下该截面上的流体没有加速度,故沿该截面势能分布应服从静力学原理.层流与湍流的本质区别是否存在流体速度u、压强p的脉动性,即是否存在流体质点的脉动性.稳定性与定态性稳定性是指系统对外界扰动的反应.定态性是指有关运动参数随时间的变化情况.边界层流动流体受固体壁面阻滞而造成速度梯度的区域.边界层分离现象在逆压强梯度下,因外层流体的动量来不及传给边界层,而形成边界层脱体的现象.雷诺数的物理意义雷诺数是惯性力与粘性力之比.量纲分析实验研究方法的主要步骤:①经初步实验列出影响过程的主要因素;②无量纲化减少变量数并规划实验;③通过实验数据回归确定参数及变量适用范围,确定函数形式.摩擦系数层流区,λ与Re成反比,λ与相对粗糙度无关;一般湍流区,λ随Re增加而递减,同时λ随相对粗糙度增大而增大;充分湍流区,λ与Re无关,λ随相对粗糙度增大而增大.完全湍流粗糙管当壁面凸出物低于层流内层厚度,体现不出粗糙度过对阻力损失的影响时,称为水力光滑管.Re很大,λ与Re无关的区域,称为完全湍流粗糙管.同一根实际管子在不同的Re下,既可以是水力光滑管,又可以是完全湍流粗糙管.局部阻力当量长度把局部阻力损失看作相当于某个长度的直管,该长度即为局部阻力当量长度.毕托管特点毕托管测量的是流速,通过换算才能获得流量.驻点压强在驻点处,动能转化成压强称为动压强,所以驻点压强是静压强与动压强之和.孔板流量计的特点恒截面,变压差.结构简单,使用方便,阻力损失较大.转子流量计的特点恒流速,恒压差,变截面.非牛顿流体的特性塑性:只有当施加的剪应力大于屈服应力之后流体才开始流动.假塑性与涨塑性:随剪切率增高,表观粘度下降的为假塑性.随剪切率增高,表观粘度上升的为涨塑性.触变性与震凝性:随剪应力t作用时间的延续,流体表观粘度变小,当一定的剪应力t所作用的时间足够长后,粘度达到定态的平衡值,这一行为称为触变性.反之,粘度随剪切力作用时间延长而增大的行为则称为震凝性.粘弹性:不但有粘性,而且表现出明显的弹性.具体表现如:爬杆效应、挤出胀大、无管虹吸.第二章流体输送机械管路特性方程管路对能量的需求,管路所需压头随流量的增加而增加.输送机械的压头或扬程流体输送机械向单位重量流体所提供的能量J/N. 离心泵主要构件叶轮和蜗壳.离心泵理论压头的影响因素离心泵的压头与流量,转速,叶片形状及直径大小有关.叶片后弯原因使泵的效率高.气缚现象因泵内流体密度小而产生的压差小,无法吸上液体的现象.离心泵特性曲线离心泵的特性曲线指He~qV,η~qV, Pa~qV.离心泵工作点管路特性方程和泵的特性方程的交点.离心泵的调节手段调节出口阀,改变泵的转速.汽蚀现象液体在泵的最低压强处叶轮入口汽化形成气泡,又在叶轮中因压强升高而溃灭,造成液体对泵设备的冲击,引起振动和侵蚀的现象.必需汽蚀余量NPSHr泵入口处液体具有的动能和压强能之和必须超过饱和蒸汽压强能多少离心泵的选型类型、型号①根据泵的工作条件,确定泵的类型;②根据管路所需的流量、压头,确定泵的型号.正位移特性流量由泵决定,与管路特性无关.往复泵的调节手段旁路阀、改变泵的转速、冲程.离心泵与往复泵的比较流量、压头前者流量均匀,随管路特性而变,后者流量不均匀,不随管路特性而变.前者不易达到高压头,后者可达高压头.前者流量调节用泵出口阀,无自吸作用,启动时关出口阀;后者流量调节用旁路阀,有自吸作用,启动时开足管路阀门.通风机的全压、动风压通风机给每立方米气体加入的能量为全压Pa=J/m3,其中动能部分为动风压.真空泵的主要性能参数①极限真空;②抽气速率.第三章液体的搅拌搅拌目的均相液体的混合,多相物体液液,气液,液固的分散和接触,强化传热.搅拌器按工作原理分类搅拌器按工作原理可分为旋桨式,涡轮式两大类.旋桨式大流量,低压头;涡轮式小流量,高压头.混合效果搅拌器的混合效果可以用调匀度、分隔尺度来度量.宏观混合总体流动是大尺度的宏观混合;强烈的湍动或强剪切力场是小尺度的宏观混合.微观混合只有分子扩散才能达到微观混合.总体流动和强剪切力场虽然本身不是微观混合,但是可以促进微观混合,缩短分子扩散的时间.搅拌器的两个功能产生总体流动;同时形成湍动或强剪切力场.改善搅拌效果的工程措施改善搅拌效果可采取增加搅拌转速、加挡板、偏心安装搅拌器、装导流筒等措施.第四章流体通过颗粒层的流动非球形颗粒的当量直径球形颗粒与实际非球形颗粒在某一方面相等,该球形的直径为非球形颗粒的当量直径,如体积当量直径、面积当量直径、比表面积当量直径等.形状系数等体积球形的表面积与非球形颗粒的表面积之比.分布函数小于某一直径的颗粒占总量的分率.频率函数某一粒径范围内的颗粒占总量的分率与粒径范围之比.颗粒群平均直径的基准颗粒群的平均直径以比表面积相等为基准.因为颗粒层内流体为爬流流动,流动阻力主要与颗粒表面积的大小有关.床层比表面单位床层体积内的颗粒表面积.床层空隙率单位床层体积内的空隙体积.数学模型法的主要步骤数学模型法的主要步骤有①简化物理模型②建立数学模型③模型检验,实验确定模型参数.架桥现象尽管颗粒比网孔小,因相互拥挤而通不过网孔的现象.过滤常数及影响因素过滤常数是指 K、qe.K与压差、悬浮液浓度、滤饼比阻、滤液粘度有关;qe与过滤介质阻力有关.它们在恒压下才为常数.过滤机的生产能力滤液量与总时间过滤时间和辅助时间之比.最优过滤时间使生产能力达到最大的过滤时间.加快过滤速率的途径①改变滤饼结构;②改变颗粒聚集状态;③动态过滤.第五章颗粒的沉降和流态化曳力表面曳力、形体曳力曳力是流体对固体的作用力,而阻力是固体壁对流体的力,两者为作用力与反作用力的关系.表面曳力由作用在颗粒表面上的剪切力引起,形体曳力由作用在颗粒表面上的压强力扣除浮力的部分引起.自由沉降速度颗粒自由沉降过程中,曳力、重力、浮力三者达到平衡时的相对运动速度.离心分离因数离心力与重力之比.旋风分离器主要评价指标分离效率、压降.总效率进入分离器后,除去的颗粒所占比例.粒级效率某一直径的颗粒的去除效率.分割直径粒级效率为50%的颗粒直径.流化床的特点混合均匀、传热传质快;压降恒定、与气速无关.两种流化现象散式流化和聚式流化.聚式流化的两种极端情况腾涌和沟流.起始流化速度随着操作气速逐渐增大,颗粒床层从固定床向流化床转变的空床速度.带出速度随着操作气速逐渐增大,流化床内颗粒全被带出的空床速度.气力输送利用气体在管内的流动来输送粉粒状固体的方法.第六章传热传热过程的三种基本方式直接接触式、间壁式、蓄热式.载热体为将冷工艺物料加热或热工艺物料冷却,必须用另一种流体供给或取走热量,此流体称为载热体.用于加热的称为加热剂;用于冷却的称为冷却剂.三种传热机理的物理本质传导的物理本质是分子热运动、分子碰撞及自由电子迁移;对流的物理本质是流动流体载热;热辐射的物理本质是电磁波. 间壁换热传热过程的三个步骤热量从热流体对流至壁面,经壁内热传导至另一侧,由壁面对流至冷流体.导热系数物质的导热系数与物质的种类、物态、温度、压力有关.热阻将传热速率表达成温差推动力除以阻力的形式,该阻力即为热阻.推动力高温物体向低温传热,两者的温度差就是推动力.流动对传热的贡献流动流体载热.强制对流传热在人为造成强制流动条件下的对流传热.自然对流传热因温差引起密度差,造成宏观流动条件下的对流传热.自然对流传热时,加热、冷却面的位置应该是加热面在下,制冷面在上,这样有利于形成充分的对流流动.努塞尔数、普朗特数的物理意义努塞尔数的物理意义是对流传热速率与导热传热速率之比.普朗特数的物理意义是动量扩散系数与热量扩散系数之比,在α关联式中表示了物性对传热的贡献.α关联式的定性尺寸、定性温度用于确定关联式中的雷诺数等准数的长度变量、物性数据的温度.比如,圆管内的强制对流传热,定性尺寸为管径d、定性温度为进出口平均温度.大容积自然对流的自动模化区自然对流α与高度h无关的区域.液体沸腾的两个必要条件过热度tw-ts、汽化核心.核状沸腾汽泡依次产生和脱离加热面,对液体剧烈搅动,使α随Δt急剧上升.第七章蒸发蒸发操作及其目的蒸发过程的特点二次蒸汽溶液沸点升高疏水器气液两相流的环状流动区域加热蒸汽的经济性蒸发器的生产强度提高生产强度的途径提高液体循环速度的意义节能措施杜林法则多效蒸发的效数在技术经济上的限制第八章气体吸收吸收的目的和基本依据吸收的目的是分离气体混合物,吸收的基本依据是混合物中各组份在溶剂中的溶解度不同.主要操作费溶剂再生费用,溶剂损失费用.解吸方法升温、减压、吹气.选择吸收溶剂的主要依据溶解度大,选择性高,再生方便,蒸汽压低损失小.相平衡常数及影响因素m、E、H均随温度上升而增大,E、H与总压无关,m 反比于总压.漂流因子P/PBm表示了主体流动对传质的贡献.气、液扩散系数的影响因素气体扩散系数与温度、压力有关;液体扩散系数与温度、粘度有关.传质机理分子扩散、对流传质.气液相际物质传递步骤气相对流,相界面溶解,液相对流.有效膜理论与溶质渗透理论的结果差别有效膜理论获得的结为k∝D,溶质渗透理论考虑到微元传质的非定态性,获得的结果为k∝.传质速率方程式传质速率为浓度差推动力与传质系数的乘积.因工程上浓度有多种表达,推动力也就有多种形式,传质系数也有多种形式,使用时注意一一对应.传质阻力控制传质总阻力可分为两部分,气相阻力和液相阻力.当mky<<kx 时,为气相阻力控制;当mky>>kx时,为液相阻力控制.低浓度气体吸收特点①G、L为常量,②等温过程,③传质系数沿塔高不变. 建立操作线方程的依据塔段的物料衡算.返混少量流体自身由下游返回至上游的现象.最小液气比完成指定分离任务所需塔高为无穷大时的液气比.NOG的计算方法对数平均推动力法,吸收因数法,数值积分法.HOG的含义塔段为一个传质单元高,气体流经一个传质单元的浓度变化等于该单元内的平均推动力.常用设备的HOG值~m.吸收剂三要素及对吸收结果的影响吸收剂三要素是指t、x2、L.t↓,x2↓,L↑均有利于吸收.化学吸收与物理吸收的区别溶质是否与液相组分发生化学反应.增强因子化学吸收速率与物理吸收速率之比.容积过程慢反应使吸收成容积过程.表面过程快反应使吸收成表面过程.第九章液体精馏蒸馏的目的及基本依据蒸馏的目的是分离液体混合物,它的基本依据原理是液体中各组分挥发度的不同.主要操作费用塔釜的加热和塔顶的冷却.双组份汽液平衡自由度自由度为2P一定,t~x或y;t一定,P~x或y;P 一定后,自由度为1.泡点泡点指液相混合物加热至出现第一个汽泡时的温度.露点露点指气相混合物冷却至出现第一个液滴时的温度.非理想物系汽液相平衡关系偏离拉乌尔定律的成为非理想物系.总压对相对挥发度的影响压力降低,相对挥发度增加.平衡蒸馏连续过程且一级平衡.简单蒸馏间歇过程且瞬时一级平衡.连续精馏连续过程且多级平衡.间歇精馏时变过程且多级平衡.特殊精馏恒沸精馏、萃取精馏等加第三组分改变α.实现精馏的必要条件回流液的逐板下降和蒸汽逐板上升,实现汽液传质、高度分离.理论板离开该板的汽液两相达到相平衡的理想化塔板.板效率经过一块塔板之后的实际增浓与理想增浓之比.恒摩尔流假设及主要条件在没有加料、出料的情况下,塔段内的汽相或液相摩尔流率各自不变.组分摩尔汽化热相近,热损失不计,显热差不计.加料热状态参数q值的含义及取值范围一摩尔加料加热至饱和汽体所需热量与摩尔汽化潜热之比,表明加料热状态.取值范围:q<0过热蒸汽,q=0饱和蒸汽,0<q<1汽液混和物,q=1饱和液体,q>1冷液.建立操作线的依据塔段物料衡算.操作线为直线的条件液汽比为常数恒摩尔流.最优加料位置在该位置加料,使每一块理论板的提浓度达到最大.挟点恒浓区的特征汽液两相浓度在恒浓区几乎不变.芬斯克方程求取全回流条件下,塔顶塔低浓度达到要求时的最少理论板数.最小回流比达到指定分离要求所需理论板数为无穷多时的回流比,是设计型计算特有的问题.最适宜回流比使设备费、操作费之和最小的回流比.灵敏板塔板温度对外界干扰反映最灵敏的塔板,用于预示塔顶产品浓度变化.间歇精馏的特点操作灵活、适用于小批量物料分离.恒沸精馏与萃取精馏的主要异同点相同点:都加入第三组份改变相对挥发度;区别:①前者生成新的最低恒沸物,加入组分从塔顶出;后者不形成新恒沸物,加入组分从塔底出.②操作方式前者可间歇,较方便.③前者消耗热量在汽化潜热,后者在显热.多组分精馏流程方案选择选择多组分精馏的流程方案需考虑①经济上优化;②物性;③产品纯度.关键组分对分离起控制作用的两个组分为关键组分,挥发度大的为轻关键组分;挥发度小的为重关键组分.清晰分割法清晰分割法假定轻组分在塔底的浓度为零,重组分在塔顶的浓度为零.全回流近似法全回流近似法假定塔顶、塔底的浓度分布与全回流时相近第十章气液传质设备板式塔的设计意图①气液两相在塔板上充分接触,②总体上气液逆流,提供最大推动力.对传质过程最有利的理想流动条件总体两相逆流,每块板上均匀错流.三种气液接触状态鼓泡状态:气量低,气泡数量少,液层清晰.泡沫状态:气量较大,液体大部分以液膜形式存在于气泡之间,但仍为连续相.喷射状态:气量很大,液体以液滴形式存在,气相为连续相.转相点由泡沫状态转为喷射状态的临界点.板式塔内主要的非理想流动液沫夹带、气泡夹带、气体的不均匀流动、液体的不均匀流动.板式塔的不正常操作现象夹带液泛、溢流液泛、漏液.筛板塔负荷性能图将筛板塔的可操作范围在汽、液流量图上表示出来. 湿板效率考虑了液沫夹带影响的塔板效率.全塔效率全塔的理论板数与实际板数之比.操作弹性上、下操作极限的气体流量之比.常用塔板类型筛孔塔板、泡罩塔板、浮阀塔板、舌形塔板、网孔塔板等. 填料的主要特性参数①比表面积a,②空隙率ε,③填料的几何形状.常用填料类型拉西环,鲍尔环,弧鞍形填料,矩鞍形填料,阶梯形填料,网体填料等.载点填料塔内随着气速逐渐由小到大,气液两相流动的交互影响开始变得比较显着时的操作状态为载点.泛点气速增大至出现每米填料压降陡增的转折点即为泛点.最小喷淋密度保证填料表面润湿、保持一定的传质效果所需的液体速度. 等板高度HETP分离效果相当于一块理论板的填料层高度.填料塔与板式塔的比较填料塔操作范围小,宜处理不易聚合的清洁物料,不易中间换热,处理量较小,造价便宜,较宜处理易起泡、腐蚀性、热敏性物料,能适应真空操作.板式塔适合于要求操作范围大,易聚合或含固体悬浮物,处理量较大,设计要求比较准确的场合.第十一章液液萃取萃取的目的及原理目的是分离液液混合物.原理是混合物各组分溶解度的不同.溶剂的必要条件①与物料中的B组份不完全互溶,②对A组份具有选择性的溶解度.临界混溶点相平衡的两相无限趋近变成一相时的组成所对应的点.和点两股流量的平均浓度在相图所对应的点.差点和点的流量减去一股流量后剩余的浓度在相图所对应的点.分配曲线相平衡的yA ~ xA曲线.最小溶剂比当萃取相达到指定浓度所需理论级为无穷多时,相应的S/F为最小溶剂比.选择性系数β=yA/yB/xA/xB.操作温度对萃取的影响温度低,B、S互溶度小,相平衡有利些,但粘度大等对操作不利,所以要适当选择.第十二章其他传质分离方法溶液结晶操作的基本原理溶液的过饱和.造成过饱和度方法冷却,蒸发浓缩.晶习各晶面速率生长不同,形成不同晶体外形的习性.溶解度曲线结晶体与溶液达到相平衡时,溶液浓度随温度的变化曲线. 超溶解度曲线溶液开始析出结晶的浓度大于溶解度,溶液浓度随温度的变化曲线为超溶解度曲线,超溶解度曲线在溶解度曲线之上.溶液结晶的两个阶段晶核生成,晶体成长.晶核的生成方式初级均相成核,初级非均相成核,二次成核.再结晶现象小晶体溶解与大晶体成长同时发生的现象.过饱和度对结晶速率的影响过饱和度ΔC大,有利于成核;过饱和度ΔC 小,有利于晶体成长.吸附现象流体中的吸附质借助于范德华力而富集于吸附剂固体表面的现象.物理吸附与化学吸附的区别物理吸附靠吸附剂与吸附质之间的范德华力,吸附热较小;化学吸附靠吸附剂与吸附质之间的化学键合,吸附热较大. 吸附分离的基本原理吸附剂对流体中各组分选择性的吸附.常用的吸附解吸循环变温吸附,变压吸附,变浓度吸附,置换吸附.常用吸附剂活性炭,硅胶,活性氧化铝,活性土,沸石分子筛,吸附树脂等. 吸附等温线在一定的温度下,吸附相平衡浓度随流体相浓度变化的曲线. 传质内扩散的四种类型分子扩散,努森扩散,表面扩散,固体晶体扩散. 负荷曲线固定床吸附器中,固体相浓度随距离的变化曲线称为负荷曲线. 浓度波固定床吸附器中,流体相浓度随距离的变化曲线称为浓度波.透过曲线吸附器出口流体相浓度随时间的变化称为透过曲线.透过点透过曲线中,出口浓度达到5%进口浓度时,对应的点称为透过点.饱和点透过曲线中,出口浓度达到95%进口浓度时,对应的点称为饱和点. 膜分离基本原理利用固体膜对流体混合物各组分的选择性渗透,实现分离.分离过程对膜的基本要求截留率,透过速率,截留分子量.膜分离推动力压力差,电位差.浓差极化溶质在膜表面被截留,形成高浓度区的现象.阴膜阴膜电离后固定基团带正电,只让阴离子通过.阳膜阳膜电离后固定基团带负电,只让阳离子通过.气体混合物膜分离机理努森流的分离作用;均质膜的溶解、扩散、解吸.第十四章固体干燥物料去湿的常用方法机械去湿、吸附或抽真空去湿、供热干燥等.对流干燥过程的特点热质同时传递.主要操作费用空气预热、中间加热. tas与tW在物理含义上的差别 tas由热量衡算导出,属于静力学问题;tW 是传热传质速率均衡的结果,属于动力学问题.改变湿空气温度、湿度的工程措施加热、冷却可以改变湿空气温度;喷水可以增加湿空气的湿度,也可以降低湿空气的湿度,比如喷的是冷水,使湿空气中的水分析出.平衡蒸汽压曲线物料平衡含水量与空气相对湿度的关系曲线.结合水与非结合水平衡水蒸汽压开始小于饱和蒸汽压的含水量为结合水,超出部分为非结合水.。
化工原理各章节知识点总结

化工原理各章节知识点总结化工原理是化学工程与技术的基础课程之一,主要涉及物质的物理性质、能量转化、传质现象、化学反应等方面的知识。
下面是化工原理各章节知识点的总结。
第一章:化工基本概念与物质的物理性质1.1化学工程与化学技术的发展历史与现状1.2化工过程及其特点1.3物质的物理性质-物质的密度、比重、相对密度-物质的表观密度、气体密度-物质的粘度、表面张力、折射率-物质的热容、导热系数、热膨胀系数-物质的流变性质第二章:能量转化与传递2.1能量的基本概念2.2热力学第一定律2.3热力学第二定律2.4热力学第三定律2.5热力学循环第三章:物质的传递过程3.1传质的基本概念与分类3.2质量传递平衡方程3.3传质速率和传质通量3.4界面传质-液-气界面传质-液-液界面传质-固-液界面传质-固-气界面传质3.5传质过程中的最速传质与弛豫时间第四章:化工流体的流动4.1流体的基本性质4.2流体的流动类别4.3流体的流动方程-流体的质量守恒方程-流体的动量守恒方程-流体的能量守恒方程4.4流体内运动的基本规律-斯托克斯定律-流体的相对运动-流体的运动粘度4.5流体的管道流动-管道内的雷诺数-管道的流动阻力第五章:多元物系中物质的平衡与分离5.1多元物系基本概念5.2雾滴定律5.3吸附平衡5.4蒸汽液平衡5.5溶液中的平衡情况5.6气相-液相-固相三相平衡第六章:化学反应与反应工程6.1化学反应动力学6.2化学平衡6.3化学反应速率6.4反应器的基本类型-批次反应器-连续流动反应器-均质反应器-非均质反应器6.5反应器的设计与操作以上是化工原理各章节的知识点总结,涵盖了物理性质、能量转化、传质现象、化学反应等方面的内容。
这些知识点是化学工程与技术的基础,对于理解和应用化工原理具有重要意义。
化工原理知识点总结复习重点完美版

化工原理知识点总结复习重点完美版为了更好地进行化工原理的复习和理解,以下是一份完整的知识点总结,帮助你复习和复盘学到的重要内容。
一、化学平衡1.化学反应方程式的写法2.反应物和生成物的摩尔比例3.平衡常数的定义和计算4.浓度和活度的关系5.反应速率和速率常数的定义及计算6.动态平衡和平衡移动原理7.影响平衡的因素:温度、压力、浓度二、质量平衡1.质量守恒定律2.原料消耗和产物生成的计算3.原料和产物的流量计算4.反应含量和反应度的计算5.塔的进料和出料物质的计算三、能量平衡1.能量守恒定律2.热平衡方程及其计算3.基础能量平衡方程的应用4.燃料燃烧的能量平衡计算5.固体、液体和气体的热容和焓变计算6.直接、间接测定燃烧热的方法及其原理7.燃料的完全燃烧和不完全燃烧四、流体流动1.流体的基本性质:密度、粘度、黏度、温度、压力2.流体的流动模式:层流和湍流3.流量和速度的计算4.伯努利方程及其应用5.流体在管道中的阻力和压降6.伽利略与雷诺数的关系7.流体静力学公式的应用五、气体平衡1.理想气体状态方程的计算2.弗拉索的原理及其应用3.气体的混合物和饱和汽4.气体的传递和扩散5.气体流动和气体固体反应的应用6.气体和液体的溶解度计算六、固体粒度和颗粒分离1.颗粒的基本性质:颗粒大小、形状和密度2.颗粒分布函数和粒度分析3.颗粒分离的基本过程和方法4.难磨性颗粒的碾磨过程5.颗粒的流动性和堆积性6.各种固体分离设备的工作原理和应用领域七、非均相反应工程1.反应器的分类和基本概念2.反应速率方程的推导和计算3.反应的平均摩尔体积变化和速率方程的确定方法4.反应动力学和机理的研究方法5.混合反应和连续反应的计算6.活性物质的拟合反应速率方程7.补偿反应的控制和模拟以上是化工原理的主要知识点总结,希望能够帮助你更好地进行复习和理解。
祝你取得好成绩!。
化工原理各章知识点

化工原理各章知识点化工原理是化工专业的基础课程之一,它主要涉及到化工过程中的一些原理、原理和理论。
下面是化工原理各章节的一些重点知识点的介绍。
第一章:化学工程概述化学工程概述主要介绍了化学工程的定义、发展历程、相关行业和化学工程的各种应用。
通过这一章节的学习,可以了解化学工程的基本概念、发展历史和现状,为后续章节的学习奠定基础。
第二章:物料平衡与能量平衡物料平衡和能量平衡是化工过程设计的基本工具。
学习这一章节,主要掌握物料平衡和能量平衡的基本原理和计算方法,能够进行物料和能量平衡的计算和分析。
第三章:化工流程与流体力学化工流程与流体力学主要介绍了流体在化工过程中的流动原理和流动性能的参数。
掌握这一章节的知识,可以了解流体在管道、泵以及其他设备中的流动特性,同时了解液体和气体的物理性质和计算方法。
第四章:传递过程与传递操作基础传递过程与传递操作基础主要涉及质量传递和能量传递的基本原理和方法。
通过学习这一章节,可以了解质量传递和能量传递的基本概念、原理和计算方法,为后续章节的学习打下基础。
第五章:多相反应与反应器多相反应与反应器是化学工程中的核心内容之一、这一章节主要介绍液相反应和气相反应的基本原理、机理和反应器的种类、结构和设计方法。
掌握这一章节的知识,可以理解多相反应的基本原理和反应器的工作原理,能够进行反应器的设计和优化。
第六章:分离工程基础分离工程基础主要介绍化工过程中的物质分离原理和技术。
学习这一章节,可以了解物质分离的基本原理和方法,能够进行分离工艺的设计和操作。
第七章:化工热力学化工热力学主要涉及化学反应的热力学原理和计算方法。
通过学习这一章节,可以了解化学反应的热力学基本原理和计算方法,能够进行热力学计算和分析。
第八章:化工流程动力学化工流程动力学主要涉及化学反应过程的动力学原理和方法。
学习这一章节,可以了解化学反应动力学的基本原理和计算方法,能够进行反应过程的动力学分析和优化。
第九章:计算机在化学工程中的应用计算机在化学工程中的应用主要介绍了计算机在化学工程中的应用方法和工具。
《化工原理》期末复习用 各章习题+参考答案

水 W(60-70)×1=-10W 热量衡算:98.85-40 W=-10W 所以水流量 W=98.85/30≈3.3kg 水/kg 苯
2
第一章 流体流动
1.试计算空气在-40℃和 310mmHg 真空度下的密度和重度(用 SI 制和工程单位制表 示。)
1
5. 1atm 下苯的饱和蒸汽(80.1℃)在换热器中冷凝并冷却到 70℃。冷却水于 30℃下送 入,于 60℃下送出。求每千克(重量)苯蒸汽需要多少冷却水。1atm 下苯的汽化潜热为 94.2kcal/kg,在 0~70℃内的平均比热为 0.42kcal/(kg⋅℃)。
解:以 1kg 苯蒸汽为基准作热量衡算,基准温度 70℃,设水流量为 W 以整个体系为研究对象: 热量输入:苯 94.2+0.46(80.1-70)=98.85
解:如图取 a-a 为等压面,则静力学方程式可得: R=0.32m,Δh=0.004m p1+ρcgR=p2+ρcgΔh+ρAgR 实际压差 p1-p2=(ρA-ρc)gR+ρcgΔh
=(1000-910)×9.81×0.32+910×9.81×0.004
=282.5+35.7=318.2Pa 若不计两液面高差则
第 5 题图
6.用一复式 U 管压差计测定水流管道 A、B 两点 的压差,压差计的指示液为汞,两段汞柱之间放的是 水,今若测得 h1=1.2m,h2=1.3m,R1=0.9m,R2=0.95m, 问管道中 A、B 两点间的差压ΔpAB 为多少?(先推导 关系式,再进行数字运算)。
解:如图取等压面,推导 p1 与 p6 的关系 已知 p1 =p2,p3=p4,p5= p6 p1= p4+ρHggR1 p6= p4+ρg(R1+h2-h1) p1-ρHggR1= p6-ρg R1-ρg h2+ρg h1 p1= pA+ρg h1 p6= pB+ρHggR2+ρg(h2-R2) 则 pA- pB=ρHggR1-ρg h1+ρHggR2+ρg h2-ρgR2-ρg R1-ρg h2+ρg h1
化工原理知识点复习

第一章 流体流动 流体静力学密度 不可压缩(恒密度)流体和可压缩性(变密度)流体压力 压强常用单位P8-9 真空度= - 表压 静力学基本方程U 型压差计测得的是修正压强或阻力损失和动能水平之和,水平管测得的是压强差 流体动力学连续性方程柏努利方程 基准、各项单位物理意义g∆Z+∆u 2/2+∆p/ρ=We -∑h f能量转换g∆Z+∆u 2/2+∆p/ρ=0有效功率 N e =W e W=W e V ρ 轴功率 N=N e /η 流动阻力直管阻力+局部阻力 直管阻力粘性:年顿粘性定律(层流时的牛顿型流体) 液体:T 增大,μ减小 μ液体> μ气体气体:T 增大,μ增大动力粘度μ SI 制:Pa·s运动粘度μ :粘度μ与密度之比 SI 制:m 2/s流动型态 层流Re≤2000 u=u max /2 λ=64/ReRe>4000湍流区:λ=φ(Re 光滑管:Re=3×103~1×105 λ=0.3164/Re 0.25 完全湍流区:λ=λ(ε/d) 局部阻力 ζ进口 = 0.5 ζ出口 = 1总阻力等径管)(2112z z g p p -+=ρ变径管:∑h f =∑h f1+∑h f2+∑h f3+…. 流速与流量的测量 测速管(皮托管):测量点速度 孔板流量计:恒截面、变压差文丘里流量计:恒截面、变压差;能量损失小,造价高 转子流量计:恒压差、恒流速、变截面第二章 流体输送机械 离心泵结构 叶轮作用 静压能增大和动能增大分类 ① 闭式② 半闭式③敞式泵壳作用 :汇集由叶轮抛出的液体;动能→静压能)。
气缚现象性能参数:流量/扬程/有效功率/轴功率 Ne=WeW=WeVρg/g=ρgVH 轴功率N=Ne/η=ρgVH/η泵的进口处安_真空表_,泵出口处安_压力表_和_出口阀门_,而在出口处,_出口阀门_必须安在_压力表_之前,在出口管路上还应安装测量_流量_的仪表 2. 离心泵的特性曲线p67转速n 一定时,由实验测得H ~V ,Na ~V ,η~V ,这三条曲线称为特性曲线,由泵制造厂提供。
化工原理下册总结知识点

化工原理下册总结知识点第一章:化工原理的基本概念本章主要介绍了化工原理的定义、研究对象、基本问题和基本概念。
化工原理是揭示化学工艺生产过程中涉及的物质和能量转化规律的科学原理。
化工原理的研究对象是化学工艺生产过程。
化工原理的基本问题包括反应动力学、传质和传热、流体力学等。
化工原理的基本概念包括物质平衡、能量平衡、反应速率、传质速率、传热速率、动量传递等。
第二章:物质的热力学性质本章主要介绍了物质的热力学性质,包括物质的状态函数、状态方程、状态图,热力学基本定律,热力学函数等。
物质的状态函数包括内能、焓、熵等。
物质的状态方程包括理想气体状态方程、克拉珀龙方程等。
物质的状态图包括P-V图、P-T图、T-S图等。
热力学基本定律包括热力学第一定律、热力学第二定律等。
热力学函数包括焓、自由能、吉布斯函数等。
第三章:理想气体混合物的平衡本章主要介绍了理想气体混合物的平衡,包括平衡态条件、混合物的平衡常数、Gibbs函数和反应平衡常数等。
平衡态条件包括稳定平衡态和不稳定平衡态。
混合物的平衡常数包括形成常数、平衡常数、活度等。
Gibbs函数和反应平衡常数包括Gibbs自由能、反应平衡常数等。
第四章:液体混合物的平衡本章主要介绍了液体混合物的平衡,包括液体混合物的正则方程、活度系数、汽液平衡和液-液平衡等。
液体混合物的正则方程包括盖丁方程、运动方程等。
活度系数包括活度系数的概念、求取方法等。
汽液平衡包括汽液平衡的条件、汽液平衡的计算等。
液-液平衡包括液-液平衡的条件、液-液平衡的计算等。
第五章:化工动力学本章主要介绍了化工动力学,包括化工反应动力学基本概念、速率方程和反应机理等。
化工反应动力学基本概念包括化学反应动力学的研究对象、动力学方程等。
速率方程包括速率常数、速率表达式等。
反应机理包括反应机理的确定方法、反应过程中的化学反应类型等。
第六章:传质基本概念和传质作用本章主要介绍了传质基本概念和传质作用,包括传质的基本概念、Fick定律、传质系数、传质规律等。
化工原理第四版下册答案

化工原理第四版下册答案化工原理第四版下册答案。
第一章,化工原理概述。
1.1 选择题。
1.(A)化工原理是研究化工产品生产的基本原理和方法的一门学科。
2.(C)化工原理的研究对象包括化工产品的生产工艺、原理和技术。
3.(B)化工原理的研究内容主要包括物质平衡、能量平衡和动量平衡等方面。
4.(D)化工原理的研究方法包括实验研究、理论分析和数值计算等。
5.(A)化工原理的研究目的是为了提高化工产品的生产效率和质量。
1.2 填空题。
1. 化工原理是研究化工产品生产的基本原理和方法的一门学科。
2. 化工原理的研究对象包括化工产品的生产工艺、原理和技术。
3. 化工原理的研究内容主要包括物质平衡、能量平衡和动量平衡等方面。
4. 化工原理的研究方法包括实验研究、理论分析和数值计算等。
5. 化工原理的研究目的是为了提高化工产品的生产效率和质量。
第二章,化工原理基本理论。
2.1 简答题。
1. 请简要介绍化工原理的基本概念和研究内容。
化工原理是研究化工产品生产的基本原理和方法的一门学科,其研究内容包括物质平衡、能量平衡和动量平衡等方面。
2. 请简要说明化工原理的研究方法和研究目的。
化工原理的研究方法包括实验研究、理论分析和数值计算等,其研究目的是为了提高化工产品的生产效率和质量。
2.2 计算题。
1. 请计算某化工生产过程中的物质平衡,并给出计算步骤和结果。
步骤,根据输入和输出的物质量,利用物质平衡的公式进行计算。
结果,经计算得出,物质平衡为XXkg。
2. 请计算某化工生产过程中的能量平衡,并给出计算步骤和结果。
步骤,根据输入和输出的能量量,利用能量平衡的公式进行计算。
结果,经计算得出,能量平衡为XXkJ。
第三章,化工原理在实际生产中的应用。
3.1 分析题。
1. 请分析化工原理在实际生产中的应用,以某化工产品生产过程为例进行说明。
化工原理在实际生产中可以用于优化生产工艺、提高产品质量和降低生产成本。
例如,在某化工产品生产过程中,通过物质平衡和能量平衡的分析,可以找出生产过程中的瓶颈和不足之处,从而进行改进和优化。
理工类专业课复习资料-《化工原理》基本知识点

第一章流体流动一、压强1、单位之间的换算关系:221101.3310330/10.33760atm kPa kgf m mH O mmHg====2、压力的表示(1)绝压:以绝对真空为基准的压力实际数值称为绝对压强(简称绝压),是流体的真实压强。
(2)表压:从压力表上测得的压力,反映表内压力比表外大气压高出的值。
表压=绝压-大气压(3)真空度:从真空表上测得的压力,反映表内压力比表外大气压低多少真空度=大气压-绝压3、流体静力学方程式0p p ghρ=+二、牛顿粘性定律F du A dyτμ==τ为剪应力;du dy 为速度梯度;μ为流体的粘度;粘度是流体的运动属性,单位为Pa·s;物理单位制单位为g/(cm·s),称为P (泊),其百分之一为厘泊cp111Pa s P cP== 液体的粘度随温度升高而减小,气体粘度随温度升高而增大。
三、连续性方程若无质量积累,通过截面1的质量流量与通过截面2的质量流量相等。
111222u A u A ρρ=对不可压缩流体1122u A u A =即体积流量为常数。
四、柏努利方程式单位质量流体的柏努利方程式:22u p g z We hf ρ∆∆∆++=-∑22u p gz E ρ++=称为流体的机械能单位重量流体的能量衡算方程:Hf He gp g u z -=∆+∆+∆ρ22z :位压头(位头);22u g :动压头(速度头);p gρ:静压头(压力头)有效功率:Ne WeWs=轴功率:Ne N η=五、流动类型雷诺数:Re du ρμ=Re 是一无因次的纯数,反映了流体流动中惯性力与粘性力的对比关系。
(1)层流:Re 2000≤:层流(滞流),流体质点间不发生互混,流体成层的向前流动。
圆管内层流时的速度分布方程:2max 2(1)r r u u R =-层流时速度分布侧型为抛物线型(2)湍流Re 4000≥:湍流(紊流),流体质点间发生互混,特点为存在横向脉动。
化工原理(下)复习各章知识点及复习题

第1章蒸馏 内容小结复习题1 蒸馏概述蒸馏操作是借混合液中各组分挥发性的差异而到达别离目的。
轻组分:混合物中的易挥发组分;重组分:混合物中的难挥发组分例:蒸馏是别离的一种方法,其别离依据是混合物中各组分的,别离的条件是。
答:均相液体混合物,挥发性差异,造成气液两相系统精馏操作压力的选择减压蒸馏:降低了液体的沸点。
应用场合:别离沸点较高的热敏性混合液,混合物沸点过高的物系〔防止采用高温载热体〕。
加压蒸馏:提高冷凝温度防止使用冷冻剂。
应用场合:别离常压下呈气态的物系,馏出物的冷凝温度过低的物系。
举例:脱丙烷塔操作压力提高到1 765kPa时,冷凝温度约为50℃,便可使用江河水或循环水进行冷却,石油气常压呈气态,必须采用加压蒸馏。
2 双组分溶液的气液相平衡例:当混合物在t-x-y图中的气液共存区内时,气液两相温度,但气相组成液相组成,而两相的量可根据来确定。
答: 相等,大于,杠杆规那么例:当气液两相组成相同时,那么气相露点温度液相泡点温度。
答:大于例:双组分溶液的相对挥发度α是溶液中的挥发度对的挥发度之比,假设α=1表示。
物系的α值愈大,在x-y图中的平衡曲线愈对角线。
答:易挥发组分,难挥发组分,不能用普通蒸馏方法别离,远离理想溶液的含义例:理想溶液满足拉乌尔定律,也满足亨利定律;非理想稀溶液满足亨利定律,但不满足拉乌尔定律;服从亨利定律并不说明溶液的理想性,服从拉乌尔定律才说明溶液的理想性例:精馏塔别离某二元物系,当操作压强降低时,系统的相对挥发度 ( ),溶液的泡点( ),塔顶蒸汽冷凝温度( )。
答:增大,减小,减小3 平衡蒸馏与简单蒸馏4 精馏例:精馏塔的作用是。
答:提供气液接触进行传热和传质的场所。
例:在连续精馏塔内,加料板以上的塔段称为,其作用是;加料板以下的塔段〔包括加料板〕称为_____,其作用是。
答:精馏段提浓上升蒸汽中易挥发组分提馏段提浓下降液体中难挥发组分例:离开理论板时,气液两相到达状态,即两相相等,____互成平衡。
化工原理(下)参考卷及答案

一、选择题(每题2分,共20分)1. 下列哪种传热方式在化工生产中应用最广泛?A. 对流传热B. 辐射传热C. 导热D. 蒸发传热2. 下列哪个设备不属于流体输送设备?A. 风机B. 泵C. 压缩机D. 蒸汽锅炉3. 在精馏操作中,下列哪种因素对分离效果影响最大?A. 塔板数B. 回流比C. 进料量D. 塔内压力4. 下列哪种干燥方式属于内部干燥?A. 真空干燥B. 热风干燥C. 辐射干燥D. 冷冻干燥5. 下列哪个过程不属于膜分离过程?A. 微滤B. 超滤C. 纳滤D. 反渗透6. 下列哪种萃取剂适用于萃取苯甲酸?A. 乙醇B. 乙酸乙酯C. 水D. 氯仿7. 下列哪个设备用于气体的吸收?A. 填料塔B. 泡罩塔C. 喷射泵D. 转子流量计8. 下列哪种因素对搅拌效果影响最大?A. 搅拌器类型B. 搅拌器直径C. 搅拌速度D. 容器形状9. 下列哪种设备用于固液分离?A. 滤布B. 沉淀池C. 离心机D. 膜分离设备10. 下列哪个过程属于热力学第一定律的应用?A. 热量传递B. 功的传递C. 能量守恒D. 熵增原理二、填空题(每题2分,共20分)1. 化工生产过程中的三大基本操作是______、______、______。
2. 传热的基本方式有______、______、______。
3. 流体在管道中的流动状态分为______和______。
4. 精馏过程中,回流比的大小对______和______有直接影响。
5. 干燥过程中,湿空气的相对湿度越低,其______能力越强。
6. 膜分离过程中,膜的截留分子量越大,表示膜的______越强。
7. 萃取过程中,萃取剂的选择应考虑______、______和______等因素。
8. 气体吸收过程中,填料塔的流体力学性能主要取决于______和______。
9. 搅拌过程中,搅拌器的______和______对搅拌效果有显著影响。
10. 固液分离过程中,离心分离的推动力是______。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第1章蒸馏 内容小结复习题1 蒸馏概述蒸馏操作是借混合液中各组分挥发性的差异而达到分离目的。
轻组分:混合物中的易挥发组分;重组分:混合物中的难挥发组分例:蒸馏是分离的一种方法,其分离依据是混合物中各组分的,分离的条件是。
答:均相液体混合物,挥发性差异,造成气液两相系统精馏操作压力的选择减压蒸馏:降低了液体的沸点。
应用场合:分离沸点较高的热敏性混合液,混合物沸点过高的物系(避免采用高温载热体)。
加压蒸馏:提高冷凝温度避免使用冷冻剂。
应用场合:分离常压下呈气态的物系,馏出物的冷凝温度过低的物系。
举例:脱丙烷塔操作压力提高到1 765kPa时,冷凝温度约为50℃,便可使用江河水或循环水进行冷却,石油气常压呈气态,必须采用加压蒸馏。
2 双组分溶液的气液相平衡例:当混合物在t-x-y图中的气液共存区内时,气液两相温度,但气相组成液相组成,而两相的量可根据来确定。
答: 相等,大于,杠杆规则例:当气液两相组成相同时,则气相露点温度液相泡点温度。
答:大于例:双组分溶液的相对挥发度α是溶液中的挥发度对的挥发度之比,若α=1表示。
物系的α值愈大,在x-y图中的平衡曲线愈对角线。
答:易挥发组分,难挥发组分,不能用普通蒸馏方法分离,远离理想溶液的含义例:理想溶液满足拉乌尔定律,也满足亨利定律;非理想稀溶液满足亨利定律,但不满足拉乌尔定律;服从亨利定律并不说明溶液的理想性,服从拉乌尔定律才表明溶液的理想性例:精馏塔分离某二元物系,当操作压强降低时,系统的相对挥发度 ( ),溶液的泡点( ),塔顶蒸汽冷凝温度( )。
答:增大,减小,减小3 平衡蒸馏与简单蒸馏4 精馏例:精馏塔的作用是。
答:提供气液接触进行传热和传质的场所。
例:在连续精馏塔内,加料板以上的塔段称为,其作用是;加料板以下的塔段(包括加料板)称为_____,其作用是。
答:精馏段提浓上升蒸汽中易挥发组分提馏段提浓下降液体中难挥发组分例:离开理论板时,气液两相达到 状态,即两相 相等,____互成平衡。
答: 平衡 温度 组成例:精馏塔的塔顶温度总是低于塔底温度,其原因有(1) 和(2) 。
答: 塔顶易挥发组分含量高 塔底压力高于塔顶加料热状态参数q 的计算例:已知汽液混合物进料中,汽相与液相的摩尔数之比为3:2,易挥发组分的摩尔分数为0.3,则q =______。
答:0.4(q=2/(3+2)=0.4)例:精馏塔有 进料热状况,其中以 进料q 值最大,进料温度____泡点温度。
答:五种 冷液体 小于对于不同的进料热状况,x q 、y q 与x F 的L 与L , V 与V 的关系为(1)冷液进料:x q >x F ,y q >x F ,q>1,L >L+F, V <V ;(2)饱和液体进料:x q =x F ,y q >x F ; q =1, L =L+F, V=V ;(3)气液混合物进料:x q <x F ,y q >x F 0<q<1, L >L, V >V ;(4)饱和蒸汽进料:x q <x F ,y q =x F ; q=0, L =L, V=V +F ;(5)过热蒸汽进料:x q <x F ,y q <x F ; q<0, L <L, V >V +F ;操作线方程例:某连续精馏塔, 已知其精馏段操作线方程为y=0.80x+0.172,且塔顶产品量为100kmol/h ,则馏出液组成=D x _________, 塔顶上升蒸汽量=V _________。
答:0.86, 500 kmol/h例:某连续精馏塔中,若精馏段操作线方程的截距等于零,则回流比等于____,馏出液流量等于 ,操作线方程为 。
答: ∞ 零 y n+1=x n例:在操作的精馏塔中,第一板及第二板气液两相组成分别为y 1,x 1及y 2,x 2(自塔顶开始计数), 则它们的大小顺序为 。
答: y 1 >y 2>x 1>x 2例:精馏的两操作线都是直线,主要是基于 恒摩尔流假设5 双组分精馏的设计型计算例:精馏过程回流比R 的定义式为 ;对于一定的分离任务来说,当R= 时,所需理论板数为最少,此种操作称为 ;而R= 时,所需理论板数为∞。
答案: DL ∞ 全回流 R min例:完成某分离任务需理论板数为N T =7(包括再沸器),若E T =50%,则塔内需实际板数(不包括再沸器)为( )答: 12层 (7-1)/0.5=12例:在精馏操作中,若进料位置过高,会造成釜残液中易挥发组分含量增高。
例:精馏塔采用全回流时,其两操作线 与对角线重合最优加料位置精馏计算中,以下说法正确的是____________。
A.再沸器算一块理论板B.分凝器算一块理论板C.加料板算一块理论板答:A 、B6 双组分精馏的操作型计算操作条件变化对产品质量的影响例:操作间接蒸汽加热的连续精馏塔时,由于某种原因,再沸器中加热蒸汽压力下降而使提馏段上升蒸汽流量V 下降,而进料热状况q 、浓度x F 及进料量F 不变,同时回流量L 恒定,则馏出液浓度x D 及流量D 、残液浓度x W 的变化趋势为:x D _______、D _______、x W _______。
(变大,变小,不变,不确定) 答:x D 增大、D 减小、x W 增大 解: D=F-W F V L L qF L W D V L W ⎫=+⇒⎪⇒↑⇒↓⎬=-↓⎪⎭不变不变 /L V L V ⇒↑不变 减小 //()1/(1/)L D L V L L D D L ⇒=+=+↑不变 减小假设x D 减小,则x W 减小,此时塔板数将小于实际板数,假设不成立;同理,x D 不变也不成立,所以x D 增大,x W 也增大。
精馏操作时,增大回流比R ,其他操作条件不变,则精馏段液气比L/V ( ),馏出液组成x D ( ),釜残液组成x W ( )。
.答: 增加 增加 减小精馏塔的设计中,若进料热状况由原来的饱和蒸气进料改为饱和液体进料,其他条件维持不变,则所需的理论塔板数N T ( ),提馏段下降液体流量( )。
答:减小 增加7 间歇精馏、恒沸精馏与萃取精馏间歇精馏间歇精馏往往采用填料塔间歇精馏为一非定态过程间歇精馏时全塔均为精馏段为保持间歇精馏时馏出液组成恒定,其回流比应不断增大为保持间歇精馏时回流比成恒定,其馏出液组将不断减小计算题1.某连续精馏塔进料液中含易挥发组分55%(摩尔百分数,下同)(与此相平衡的汽相组成为75% ),要求塔顶产品含易挥发组分95%,饱和液体进料。
试求:(1)求最小回流比。
(2)若加料板上液体组成与进料组成相同,回流比为最小回流比的1.5倍时,求进料板上一板流下的液体组成。
***答案*** Rmin=(x D-y e)/(y e-x e)=(0.95-0.75)/(0.75-0.55)=1,x F=x F,y F=[R/(R+1)]x F-1+x D/(R+1) , 0.75=[1.5/(1.5+1)] x F-1+0.95/(1.5+1), x F-1=0.62 2. 用连续精馏塔每小时处理100 kmol含苯40%和甲苯60%的混合物,要求馏出液中含苯90%,残液中含苯 1%(组成均以kmol%计)。
试求:(1)馏出液和残液各多少kmol.h -1。
(2)饱和液体进料时,已估算出塔釜每小时汽化量为132kmol,问回流比为多少?***答案*** ①F=D+W Fx F=Dx D+Wx W W=56.2kmol.h -1 D=43.8kmol.h -1②∵q=1 V'=V ∴L=V-D=132-43.8=88.2 R=L/D=88.2/43.6=2.023. 用常压精馏塔分离双组分理想混合物,泡点进料,进料量100kmol.h-1,加料组成为50%,塔顶产品组成x D=95%,产量 D=50kmol.h-1,回流比R=2Rmin,设全塔均为理论板,以上组成均为摩尔分率。
相对挥发度α=3。
求:(1).Rmin(最小回流比) (2).精馏段和提馏段上升蒸汽量。
(3).列出该情况下的精馏段操作线方程。
4.在连续精馏塔中分离两组分理想溶液。
已知原料液组成为0.6(摩尔分数,下同),馏出液组成为0.9,釜残液组成为0.02,泡点进料,物系的平均相对挥发度为3。
试求:(1) 每获得1 kmol/h馏出液时的原料液用量F;(W=0.52 kmol/h,F=1.52 kmol/h。
)(2) 若回流比为1.5,它相当于最小回流比的多少倍?(3.99)(3) 假设原料液加到加料板上后,该板的液相组成仍为0.6,求上升到加料板上的气相组成。
(0.721)5. 在一双组分连续精馏塔中,已知精馏段操作线方程为271.0715.0+=x y ;q 线方程为91.081.2-=x y ,求:(1) 回流比及进料热状况参数;(q =1.55) (2) 馏出液及原料液组成; (0.951D x =,0.501F x =)(3) 若回流比为3,测得从精馏段第二层塔板下降液体的组成为0.82(摩尔分数,下同),从第三层塔板上升的蒸汽组成为0.86,则此时的馏出液组成又为多少?(98.0'=D x )化工原理吸收复习基本原理与概念在总压P 、温度T 一定时的气液平衡关系: 全塔物料衡算;V B (Y 1-Y 2)=Ls(X 1-X 2)P A *=f (C A ) (由实验确定) 塔顶与塔任一截面间的物料衡算:P A *=Ex A 适合低浓度气体 V(y 1-y 2)=L(x 1-x 2)P A *=C A /H稀溶液*1 y A *=mX A 吸收操作线方程:(亨利定律) Y A *=mX X m mX =-+)1(1 y )22(x V L y x V L -+=N A =k G (P-P i )=k L (C i -C) K y a(y-y*)Sdh=GSdx=LSdx 推出填料高度的公式N A =K G (P-P*)=K L (C*-C) 吸 η=112211y V y V y V -=进塔气体中的溶质量被吸收的溶质量 N A =k y (y-y*)=K x (x*-x) 收 低浓度气体η=121y y y -N A =K y (y-y*)=K x (x*-x) 率η定义:气体吸收操作中液体流率与气体流率之比。
L/V 即操作线斜率,它可影响吸收质量和本。
一个技术指标,亦是一个经济指标。
液气比L/V min ))(2.1~1.1()_______(2*121min )(V L V L x x y y V L =--=操dZA dC AB D A J -=)(Ai P A P Bm P P G RTZ D C A C N A J A N -=+= )()(A C Ai C L k A C Ai C m C C L Z L D A N -=-=提高吸收率的两种途径:增加液气比用新型填料如环鞍型,Mellapak 填料改变操作条件如改变V 、L 流率或温度、压力对数平均推动力:)21ln(21Y Y Y Y m Y ∇-∇∇-∇=∇ 当ΔY 1/ΔY 2小于2时,可用算术平均推动力:221Y Y m Y ∇+∇=∇计算填料层高度Z 的两种方法:N OG -气相总传质单元数;H OG -气相总传质单元高度1、 平均推动法(适合平衡线、操作线为直线)Z= H OG *N OG =m X X X a X K L m Y Y Y a Y K V ∇-⋅⋅=∇-⋅⋅21212、吸收因数法(适合平衡线为过原点的直线,操作线为直线):N OG 查图 ;H OG =V/K Y a3、图解积分法:N OG =⎰*-12Y Y Y Y dY (图解积分),H OG =a Y K V⋅, Z=N OG ×H OG4、近似图解法:根据传质单元数的定义,由图解法求N OG理论板数×H 等板高度,Z=N 理/η板×板间距习题讲解【例7-1】 操作中的吸收塔,当生产任务一定,若吸收剂用量小于最小用量,则吸收效果____ __ __。
