钢铁及合金中的锰的测定方法
低合金钢—碳、硅、锰等26元素含量的测定—火花源原子发射光谱法
通过制作预燃曲线选择分析元素的适当预燃时间。积分时间是以分析精度为基础进行实验确定的。 5.4 分析条件和分析步骤
5.4.1 分析条件 本标准推荐的分析条件见表 2、分析线与内标线列入表 3 中。
表 2 分析条件
网
项
目
内
容
分析间隙
GB/T 14203-1993 钢铁及合金光电发射光谱分析法通则 GB/T 6379-1986 测试方法的精密度 通过实验室间试验确定标准测试方法的重复性和再现性
4 仪器 火花源原子发射光谱仪主要由以下单元组成。
4.1 激发光源
中 激发光源应是一个电容放电稳定的光源。
4.2 火花室 火花室应使用氩气保护,火花室直接装在分光计上,有一个氩气冲洗火花架。火花室的氩气路应能
FCLHSDHJGCSi26 001 低合金钢—碳、硅、锰等 26 元素含量的测定—火花源原子发射光 谱法
F_CL_HS_DHJG_CSi26_ 001
低合金钢—碳、硅、锰等 26 元素含量的测定—火花源原子发射光谱法
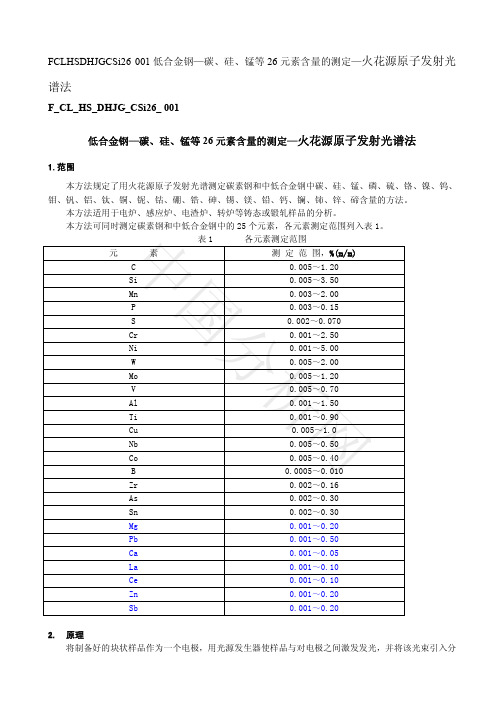
1.范围
本方法规定了用火花源原子发射光谱测定碳素钢和中低合金钢中碳、硅、锰、磷、硫、铬、镍、钨、
Mn
293.30
Cr Si
218.49
Ni
231.60
Cr
206.54
267.71
Cr
286.25
Si
中 Mo
298.91 202.03 277.53 281.61
Mn Ni Mn
国386.41 214.09 290.88
V
分311.07
311.67 310.22
Al
钢铁中锰含量的测定 (2)

实验报告钢铁中锰含量的测定——银盐氧化光度法班级:应111-1姓名:王海花学号:201169503147指导老师:王老师一.实验目的:1.通过实验,了解钢铁中锰的存在形式,测定意义。
2.了解测定钢铁中锰含量的测定方法。
3.掌握钢铁中锰含量的测定原理。
4.熟练掌握分光光度计的使用,进一步训练移液管、容量瓶的正确使用。
5.掌握用比色法测定钢材中锰含量的方法二.实验原理:1.锰在钢铁中主要以MnC、MnS、FeMnSi或固溶体状态存在。
生铁中一般含锰0.5%~6%,普通碳素钢中锰含量较低,含锰0.8%~14%的为高锰钢,含锰12%~20%的铁合金称为镜铁,含锰60%~80%的铁合金称为锰铁。
2.锰溶于稀酸中,生成锰(Ⅱ)。
锰化物也很活泼,容易溶解和氧化。
在化学反应中,由于条件的不同,金属锰可部分或全部失去外层价电子,而表现出不同的价态,分析上主要有锰(Ⅱ)、锰(Ⅲ)、锰(Ⅳ)、锰(Ⅶ),少数情况下亦有锰(Ⅵ),这就为测定锰提供了有利条件。
3.常用测定方法:一般碳素钢,低合金钢,生铁试样常以HNO3(1+3)或硫磷混酸溶解。
难溶的高合金钢以王水溶解,加HClO4或H2SO4冒烟溶解。
溶解试样的酸主要依靠H2SO4,HCl,HNO3,因H2SO4-HCl可使MnS分解。
HNO3分解碳化物(Mn3C)生成CO2逸出,加磷酸可使Fe3+配合成无色而消除Fe3+的干扰。
同时因为磷酸的存在,防止了MnO2沉淀的生成和HMnO4的分解。
4.主要反应方程式:3MnS+12HNO3=3Mn(NO3)2+6HNO3+3SO2+6H2O3Mn3C+28HNO3=29Mn(NO3)2+3CO2+10NO+14H2OMnS+H2SO4=MnSO4+H2S2AgNO3+(NH4)2S2O8=Ag2S2O8+2NH4NO3Ag2S2O8+2H2O=Ag2O2+2H2SO45Ag2O2+2 Mn(NO3)2+6HNO3=2HMnO4+10AgNO3+2H2O三.实验仪器及试剂:1.实验仪器:721型分光光度计,分析天平,容量瓶(50mL),移液管(1ml,2ml,3ml),滴管,洗耳球,电炉2.实验试剂:硝酸溶液(1:3),王水(1浓硝酸+3浓盐酸)硫磷混酸(700ml水中加入150ml磷酸及硫酸150ml,摇匀),0.5%硝酸银溶液,20%过硫酸铵溶液,5%EDTA,锰标准溶液(0.1mg/ml)四.实验步骤:1.溶样:钢样0.2630g于50ml烧杯,加5mlH2O,15ml王水溶解,(可稍热)2mlHClO4加热至冒白烟2min冷却,加硫磷混酸10ml加热至冒白烟,除尽Cl-冷却,定量转移至50ml容量瓶定容,摇匀,备用。
分光光度法联合测定钢铁及合金中硅、磷、锰含量

摘 要: 本文介绍了分光光度法联合测定钢铁及其合金中硅、 锰含量的改进方法, 磷、 与国标方法进行 比较 , 本方法具有灵敏度高、 选择性好、 操作简便、 试剂及样品用量少、 分析快速、 结果稳定、 准确度高等优
点。
关键词 : ; ; ; ; 钢铁 硅 磷 锰 分光光度法
中图分 类号 : 文献标识 码 : A
尤其是 P 还需高温将 c 氧化为六价后 , r 多次加酸使 其形成氧酰挥发除去 , 操作处理流程繁琐 , 各种酸 试剂消耗量大 , 同合金钢材操作条件要 求各异 , 不
往往会造成处理不当, 引进 C 干扰, r 使测定结果与
先经 15o 0 C烘干至恒重 , 用适量蒸馏水溶解 , 定量 转移至 l0 m O0 L容量瓶 中, 5 L 1+ ) 2O , 加 m ( 1 H S 4用
的标准溶液 。
10 1 m M 00 g・ L n标 准溶 液 ( x 国家钢 铁研 究
1 实验部分
11 仪器和试 剂 .
T 新世纪型分光光度计。 6
6 o L H S 4 液 ;0 g・ ~N 2O 溶 o t L・ 2O 溶 10 L aS 3 液 ;s A 隐蔽剂 : 0 L 1 m 水中含有 0 5 aS0 ; 0 .gN 22 钼酸 铵溶液 : 分别将 1g03 g 3 、.5 钼酸铵及酒石酸锑钾溶
此次公布的工业生物技术新产品及新工艺课题将针对生物能源生物基化学品等重要工业生物技术领域开发以工业或生活废水为原料生产生物柴油的高效清洁技术用于获得可发酵糖类丁酸等生物基化学品生产的新型纤维素处理技术基于非粮生物质为原料的生物基化学品或单体生产技术以及工业残渣的高值化利用技术等具有自主知识产权成本低可工业化生产的新产品或新工艺并开展中试规模工艺技术研究或生产性试验
4298 锰矿和锰精矿锰含量的测定电位法

4298 锰矿和锰精矿锰含量的测定电位法4298 锰矿和锰精矿锰含量的测定电位法1. 引言锰矿和锰精矿是重要的矿产资源,其锰含量的测定对于矿产开发和利用具有重要意义。
本文将着重介绍4298 锰矿和锰精矿锰含量的测定电位法,并探讨其在工业生产中的应用。
2. 4298 锰矿和锰精矿的重要性锰矿和锰精矿是重要的冶金原料,主要用于生产钢铁、不锈钢以及合金钢等。
其锰含量的高低直接影响到产品的质量和性能。
准确测定锰矿和锰精矿中的锰含量是十分重要的。
3. 锰含量的测定方法目前,测定锰含量的方法有很多种,其中电位法是一种常用的测定方法。
该方法以电位变化规律作为测定锰含量的依据,具有操作简单、准确度高的特点。
4. 4298 锰矿和锰精矿锰含量的测定电位法的原理该电位法测定锰含量的原理是基于在特定条件下,锰存在于溶液中以二价态和四价态的平衡,随着溶液pH值的变化,锰的氧化还原电位也会相应发生变化。
通过测定这种电位的变化,可以间接得出锰含量的浓度。
5. 实验步骤(1)样品制备:取适量的锰矿或锰精矿样品,经过干燥和研磨处理,使其成为均匀、细小的粉末状。
(2)溶液制备:将样品溶解于适量的硫酸或盐酸中,得到含有锰离子的溶液。
(3)电位测定:将测得含有锰离子的溶液倒入电位计中,通过控制溶液pH值的变化,测定锰的氧化还原电位。
(4)计算分析:根据测得的电位值,利用相关的计算公式,计算出锰含量的浓度。
6. 应用与展望4298 锰矿和锰精矿锰含量的测定电位法在工业生产中具有广泛的应用前景。
随着工业技术的不断进步,该方法还有进一步优化和改进的空间,以提高测定的准确度和稳定性。
7. 结语通过本文的介绍,我们了解了4298 锰矿和锰精矿锰含量的测定电位法的原理和实验步骤。
这一方法的准确度和操作简便性使得其在工业生产中具有重要的应用价值。
希望通过持续的科研工作,能够进一步完善该方法,为锰矿和锰精矿的开发利用提供更多的技术支持。
8. 个人观点作为一种重要的测定方法,4298 锰矿和锰精矿锰含量的测定电位法在工业生产中有着广泛的应用前景。
钢铁中锰含量的测定实验报告

钢铁中锰含量的测定实验报告实验目的:通过重量分析法测量给定钢锭中锰的含量。
实验原理:锰是钢铁中的常见合金元素,它能够使钢具有良好的硬度和韧性,同时还能提高钢的耐磨损性和抗腐蚀性能。
因此,锰合金钢在工业生产中使用较为普遍。
本实验采用浓硝酸将样品中的锰完全溶解,然后再通过比色法来测量其浓度,从而计算出样品中锰的含量。
实验仪器和药品:1.恒重天平2.分析天平3.酸洗玻璃器皿4.密码锁保险柜5.2N硝酸6.去离子水7.KMnO₄(二氧化锰)8.FeSO₄(硫酸亚铁)9.H₂SO₄(硫酸)实验步骤:1.在恒重天平上称取约1克左右的样品(钢锭)。
2.将样品加入酸洗玻璃器皿中,加入足量的2N硝酸,并将其密封。
3.将加有样品的酸洗玻璃器皿放入加热器中进行加热,直至样品完全溶解。
4.在加热的过程中,用分析天平称取一定比例的KMnO₄和FeSO₄,分别放置于两个玻璃烧杯内备用。
5.将一定量的去离子水加入玻璃烧杯中,然后分别加入已称好的KMnO₄和FeSO₄,搅拌均匀,使其完全退色。
6.将上述溶液依次加入原样中,使其达到定容(一般为100ml)。
7.将上述溶液振荡均匀,并取一定体积的样品(一般为25ml)加入2N硝酸校正瓶中,制成样品稀释液。
8.取校正瓶中的样品稀释液,用比色管进行比色,测定其AB值。
9.参照比色管上的色板,找到对应的AB值,根据铁漏斗的倒数和样品稀释液的配比,计算出样品中锰的含量。
实验结果:在本次实验中,我们分别进行了3次测量,得出的结果如下所示:第一次测量:锰含量为0.033%第二次测量:锰含量为0.031%第三次测量:锰含量为0.032%实验结论:经过三次测量,我们得出了钢锭中锰的含量分别为0.033%、0.031%、0.032%。
取其平均值,可以得出样品中锰的平均含量为0.032%左右。
因此,我们可以得出结论:本次实验通过重量分析法,准确地测量出了给定钢锭中锰的含量。
极度详细的钢五大元素分析方法

普通钢五元素分析一碳硫分析用定碳定硫仪测定二硅磷锰的分析1所需试剂硝酸(1+3) (1份硝酸+3份水)2过硫酸铵(固体)①测锰混酸:硝酸银1g溶于500ml水中,加硫酸25ml磷酸30ml,硝酸30ml,用水稀至于1升。
②钼酸铵溶液:5%③草酸溶液:5%④硫酸亚铁铵溶液:6%(每100ml溶液中滴1+1硫酸6滴)⑤钒酸铵溶液:0.25%(取钒酸铵2.5g加入500ml水加热溶解冷却,加入浓硝酸30ml用水稀至1升)操作方法称取试样和相同牌号的标样各1g,分别臵于100ml两用瓶中。
加1:3的硝酸50ml加热溶解,加固体过硫酸铵1g左右,煮沸1分钟冷却,稀至100ml两用瓶中硅的测定吸取试液和标液各2ml,分别臵于100ml两用瓶中,加(1+3)硝酸1ml,水3ml,加钼酸铵溶液(5%)5ml,在沸水溶液中加热30秒钟,流水冷却,立即加5%草酸溶液10ml,6%硫酸亚铁铵溶液10ml,在波长650mm 处用1cm比色皿进行测定,记下试样和标样的消光值E1、E21) -锰的测定分别吸取试液和标液各5ml,分别臵于50ml的两用瓶中,加测锰混酸20ml,加过硫酸铵固体1g,加热煮沸1分钟左右,冷却稀至50ml两用瓶中,在波长530nm处用1cm比色皿进行测定,记下试样和标样的消光值E2、E1E1=2) 磷的测定吸取试样和标样各20ml分别臵于两只150ml烧杯中,其中一只空白加入8ml水,另一只加入0.25%钒酸铵溶液3ml,5%钼酸铵溶液5ml,在波长470nm处用2cm比色皿进行测定。
记下试样和标样的消光值E2、E1不锈钢中九元素分析A 碳硫测定 (仪器分析)B 硅、镍、钛、磷、锰、铬。
钼测定试样溶液的制备1试剂:稀王水盐酸+硝酸 +水=1+1+12操作:称取试样和相同牌号的标样各0.1g,分别臵于100ml的两用瓶中,加入1+1+1稀王水10ml,温热溶解,注意尽量减少蒸发,冷却后稀至刻度。
(一) 钛的测定一试剂1 盐酸:1+12 抗坏血酸:4% 当天配制3 二安替比林甲烷溶液:2.5% (称取2.5克DAM溶于1+10盐酸100ml中)二操作方法吸取试液10ml两份臵于50ml两用瓶中显色液:加4%抗坏血酸5ml,放臵使Fe的黄色退尽,加1+1盐酸5ml,加DAM溶液10ml,以水稀至刻度,放臵半小时后用2cm比色皿在420nm处测定消光值,标样同时操作。
锰铁中锰的化学分析方法的选择

锰铁中锰的化学分析方法的选择作者:国伟来源:《中国化工贸易·中旬刊》2018年第02期摘要:锰铁是锰和铁组成的铁合金。
锰铁中锰的测定一般参照采用国际标准ISO4173-1980《锰铁—锰量的测定—滴定法》。
根据这一标准,可选择的化学分析方法主要有两种,一种是高氯酸法,另一种过硫酸铵银盐法。
本文通过用这两种方法对比分析,从中选择更适用的操作方法。
关键词:锰铁;高氯酸法;过硫酸铵银盐法锰铁是锰和铁组成的铁合金。
由于锰与氧、硫亲和力比较大。
故锰铁是炼钢生产中钢液的脱氧剂和脱硫剂。
锰铁的主要分类:高碳锰铁(含碳为7%)、中碳锰铁(含碳1.0~1.5%)、低碳锰铁(含碳0.5%)、金属锰、镜铁、硅锰合金。
在炼钢中,用作脱氧剂和合金添加剂,是用量最多的铁合金。
锰铁中锰含量的测定,可选择的化学分析方法主要有两种,一种是高氯酸法,另一种过硫酸铵银盐法。
本文通过用这两种方法对比分析,从中选择更适用的操作方法。
工作中我们把这两种分析方法都进行了实验操作,并且对比分析了操作过程及结果,操作方法如下:1 高氯酸法方法要点:试样以磷酸溶解,用高氯酸将锰氧化为三价,以N-苯基代邻(位)氨基苯甲酸为指示剂,用硫酸亚铁铵标准溶液滴定。
1.1 试剂①磷酸:比重1.70;②高氯酸:70%;③N-苯基代邻(位)氨基苯甲酸指示剂:0.2%称取此试剂0.2克溶于100毫升0.2%的碳酸钠溶液中;④硫酸亚铁铵标准溶液:0.05N。
1.2 分析方法称取试样0.1克于250三角瓶中,加磷酸20毫升,中温加热溶解,加高氯酸2毫升,继续加热蒸发冒烟至小气泡消失,立即取下稍冷,加水30毫升,摇匀。
冷却至室温,加指示剂3-5滴,以硫酸亚铁铵标准溶液滴定至溶液呈亮绿色为终点。
计算:Mn=(V*N*0.05494)/G*100式中:V——滴定所耗硫酸亚铁铵标淮溶液之毫升数;N——硫酸亚铁铵标准溶液的当量浓度;G——试样重(克);0.05494——1毫升硫酸亚铁铵标液相当于锰的克数。
4298 锰矿和锰精矿锰含量的测定电位法

4298 锰矿和锰精矿锰含量的测定电位法在矿产资源的开发过程中,锰矿和锰精矿的生产与加工起到非常重要的作用。
而了解锰矿和锰精矿中锰含量的测定则对于生产加工具有关键的意义。
本文将针对4298 锰矿和锰精矿锰含量的测定电位法进行深入探讨。
1. 什么是锰矿和锰精矿?锰矿是指从锰矿石中提取的原始矿石,含有较高的锰元素。
而锰精矿则是在锰矿经过加工、提炼等一系列工艺后获得的产品,其锰含量更加纯净。
2. 锰含量的重要性锰是重要的合金元素,广泛用于钢铁生产中。
了解锰矿和锰精矿中锰含量的测定可以帮助生产者更好地掌握原料的质量和特性,从而指导生产过程,提高产品质量和市场竞争力。
3. 4298 锰矿和锰精矿锰含量的测定电位法介绍4298 锰矿和锰精矿锰含量的测定电位法是一种常用的测定方法,其基本原理是利用电位法对锰矿和锰精矿中的锰离子进行测定。
该方法具有测定迅速、准确度高、操作简便等优点,被广泛应用于生产实践中。
4. 实际操作步骤a. 样品准备:将待测样品粉碎、研磨成均质状态,以便后续的操作。
b. 化学药剂配置:准备好所需的标准溶液和试剂,确保测定过程中稳定的试剂条件。
c. 仪器准备:根据仪器要求进行电位计等仪器的准备工作。
d. 操作步骤:按照标准的操作步骤进行样品处理、电位测定等操作。
e. 结果处理:根据仪器读数和标准曲线等数据计算出样品中的锰含量。
5. 个人观点和总结通过4298 锰矿和锰精矿锰含量的测定电位法,我们可以快速、准确地了解样品中的锰含量,为生产提供宝贵的数据支持。
在实际操作过程中,我们需要严格遵守操作规程,确保测定结果的准确性和可靠性。
锰矿和锰精矿的锰含量测定是矿产资源开发中的重要一环,只有加强对其测定方法的研究和应用,才能更好地实现资源的有效利用和产品质量的提升。
总结而言,4298 锰矿和锰精矿锰含量的测定电位法在矿业生产中具有重要地位和意义。
通过深入学习和掌握这一测定方法,可以更好地满足生产过程中对于锰含量测定的需求,为产业发展和产品质量提升提供有力支持。
化学分析操作规程(C、Si、Mn、P、S、Cr、Ni、Ti、Mo、V)

1.钢铁中碳的测定碳是钢铁中最为重要的元素之一,它是钢铁编号的重要依据,也是衡量钢铁机械性能优劣的重要依据,所以说测准钢铁中碳的含量十分重要。
碳在钢铁中的存在形式一般有两种,一种是以游离状态的石墨形式,另一种是碳与其它金属元素如铁、铬、锰、钨等化合形成的化合碳化物(Fe3C2,Cr3C2, WC……)碳在钢铁中或以游离碳,或以化合碳、或以两种形式共存的形式出现。
由于化合碳易被酸溶解从而使分析成为可能,然而,游离碳即石墨具有很大的化学惰性,给溶解试样带来很大的困难,所以,在测定钢铁中含碳量(指游离碳与化合碳之和)时,不是用一般的酸进行溶解处理的方法,而是用高温燃烧法测定。
燃烧法测定钢铁中碳是首先制取合格的被测试样,将试样称量后放入船形瓷舟中,然后放入高温管式电炉内,经一段时间的予热后通氧气燃烧。
使碳生成二氧化碳再测定之。
根据测定形式的不同分为容量法和非水滴定法两种常见方法。
燃烧——气体容量法:原理:试样在高温下(1300)通氧燃烧,碳被氧化生成二氧化碳,二氧化碳气体通过氢氧化钾或氢氧化钠溶液将二氧化碳气体吸收,根据吸收前后的体积差,换算出碳的百分含量。
主要反应:⒈C+O2=CO24Fe3C+13O2=4CO2+6Fe2O3⒉CO2+2KOH=K2CO3 +H2O在高温氧化过程中,钢铁中的硫同时也被氧化生成二氧化硫,当燃烧气体通过氢氧化钾吸收液时二氧化硫也被吸收,这样就会影响碳的测定。
消除硫的影响是采用装有固体二氧化锰的特殊装置来吸收二氧化硫。
反应式:⒈4FeS+7O2=2Fe2O3 +4SO2⒉SO2+KOH=KHSO3Ⅰ仪器及试剂:氧气净化和燃烧装置及定碳仪(见图7—1)。
水银气压计。
氢氧化钾溶液:(40%)。
酸性水:于水中加数滴硫酸及钾基橙指示剂熔剂:纯锡、纯铋等。
Ⅱ操作步骤:称取试样0.2500~2.0000g,置于瓷舟内,加适当助溶剂约0.2克,立即将瓷舟用紫铜或低碳不锈钢长钩送于炉管高温处(1150~1250℃),立即用橡皮塞将燃烧管塞住,保温0.5—1分钟,通氧燃烧(氧气流量1.5~2升/分),生成的二氧化碳和混合气体,经过除硫器及冷凝管进入量气管内,待量气管内酸性水液面在稳定一段时间以后开始下降时,将水准瓶移至量气管的零点处,当液面降到接近零点时,将量气管通大气,切断氧气流。
钢中锰含量的测定实验报告

钢中锰含量的测定实验报告
实验目的
本实验旨在测定一种钢材中锰的含量。
实验原理
锰是钢材中常见的合金元素之一,对钢材的强度和硬度有一定
的影响。
本实验采用焰光法测定钢中锰的含量。
在酸性条件下,
钢样品与硫酸溶液反应,使得样品中的锰原子被氧化成Mn2+。
加入硫酸钠的石墨喷灯中,Mn2+会在火焰中激发出明亮的紫红色光
谱线,通过光谱仪进行测定,从而得到样品中锰的含量。
实验步骤
1. 取一定量的钢样品,将其加入锥形瓶中,加入稀硫酸溶液,
加热至样品完全溶解。
2. 移至通风橱中,将样品冷却至室温,然后加入氢氧化钠溶液,调节pH值至约7。
3. 加入硫酸过量,使得样品中的锰原子被完全氧化成Mn2+。
4. 在石墨喷灯中加入硫酸钠,点燃,进行吸光度测定。
5. 重复实验至稳定结果。
实验结果
在本实验中,我们取一定量的制品样品,经过测量,确定其中的锰含量为0.83%。
实验结论
本实验采用焰光法测定了一种钢材中锰的含量,结果表明,该样品中锰的含量为0.83%。
该结果与制品的批次指标值相符,具有可靠性。
光度法联合测定钛铁中的钛、硅、锰、磷、铜、镍

五倍爹, 且操 作方便 , 分析 结 果令人 满 意。
关 键词 : 钛铁
, 、 曾 古
碱 性混合 熔 剂 熔融 酸化 定容
光度 法联 合测 定
u 刚口
稀释 至刻 度 , 匀 。 摇
移取 5mL母液 ( . ) 10 m 2 1 于 0 L容量 瓶 中 ,加
1 0mL钳 酸 铵 溶 液 ,摇 匀 ,置 于 沸 水 浴 中 加 热 3 0
8 ,取 出,以流水冷却至室温 ,加 2 L草硫混酸 , 5m 立 即加入 5mL硫 酸亚铁 铵溶 液 ,用水 稀释 至刻度 ,
. . . 2 分析步骤
2 1 试 样溶 液0g g碱性 混 合 熔
剂的铂金坩埚 中, 混匀 , 再覆盖上面 1 碱性混合熔 g
剂 , 上坩埚 盖 , 盖 置于坩 埚架 上 , 90~1 0 在 5 0℃高 0
温炉内熔融 5mn 取出稍冷却 , i, 待熔融物凝 固, 将铂
钾 ( 高碘 酸钠 ) 液 :% ; 硝 酸钠 溶 液 :. % ; 或 溶 5 亚 O5
对分析结果 准确度 的要求也较高 。为保证钛铁质
量, 需要 对进 厂钛 铁 进 行 化学 成 分 的分 析 。 由于分 光光 度 法是 当今 国 内外化 学分 析铁 合金 中各元 素 常
高氯酸 : p=16 / L 硝 酸铋溶 液:% , .7gm ; 1 称取 1g
红指示 剂 1滴 , 氨 水 ( 用 1+1 调 节 至 溶 液 由 红 变 )
移取 1 L母液 (. ) 份 , 0m 2 1两 分别 于 10m 0 L钢 铁 两 用瓶 中 , 1 加 6mL硫 酸 ( 1+1 , ) 加热 蒸 发 至 冒 硫 酸 烟 , 下 冷却 , 瓶壁 加 水 3 L 冷 却 至室 温 取 沿 0m , 后 , 如下 处理 : 作 参 比液 : 水稀 释至刻 度 , 匀 。 用 摇 显色 溶液 : 8mL过 氧化 氢 ( 4 , 加 1+ ) 以水稀 释 至刻 度 , 摇匀 , 置 8~1 n 。将 显 色 溶 液 移 入 1 放 5ri n c 比色 皿 中 , m 在分 光光度 计 上于波 长 40n 2 m处 , 以 参 比液为参 比测 定 吸 光 度 , 去 空 白试 验 溶 液 吸光 减 度 , 工作 曲线 上计 算钛 的百分 含量 。 从
锰的原子质量

锰的原子质量介绍锰是一种化学元素,其原子符号为Mn,原子序数为25。
锰具有银白色的金属光泽,常见于自然界中的矿石或合金中。
在化学中,锰在许多重要的化合物和反应中起着重要的作用。
了解锰的原子质量对于研究和应用锰相关的科学和工程问题具有重要意义。
原子质量的定义原子质量是指一个元素的一个原子质量相对于碳-12同位素的质量的比值。
碳-12被定义为12个单位的原子质量,其质量约等于质子和中子的质量之和。
原子质量相关于一个元素的质量和原子数目,通常以原子量单位(amu)表示。
原子质量可以用来计算化学反应和物质的摩尔质量。
锰的原子质量为了确定锰的原子质量,我们可以查阅化学元素周期表。
根据最新的国际纯净化学和应用化学联合会(IUPAC)发布的数据,锰的原子质量约为54.938045 amu。
这个数值是通过多种实验方法和数据进行测量和推导得出的,可以被认为是相对准确的锰原子质量值。
原子质量的测量方法科学家们使用多种方法来测量元素的原子质量,包括质谱法、质心-碎片速度法和同位素质量分析法。
这些方法可以提供高精度的原子质量测量结果。
下面是几种常用的原子质量测量方法:1.质谱法:利用质谱仪测量元素的原子质量。
质谱仪通过将元素的原子或分子离子化,并根据它们的质量-电荷比进行分离和检测,从而确定其质量。
2.质心-碎片速度法:利用质心-碎片速度关系来测量元素的原子质量。
这种方法基于一个质心方程,其中原子或分子的质量与其与碎片的速度之积成反比。
3.同位素质量分析法:利用同位素的相对丰度和质量差异来测量元素的原子质量。
同位素质量分析法通常使用质谱仪来分离和检测不同同位素的离子。
锰的同位素和原子质量测量结果锰有多个稳定同位素,包括锰-55、锰-56、锰-57、锰-58和锰-59。
这些同位素的相对丰度和质量差异被用来确定锰的平均原子质量。
根据相关实验测量结果,锰的平均原子质量约为54.938045 amu。
以下是锰同位素和它们的相对丰度:•锰-55:相对丰度为100%。
高碘酸钠分光光度法测定钢铁锰含量的不确定度评定报告

1.5014%,算术平均值为 1.4992%,所以,由测量重复性引入的标准不确定度分量为:
uA
s(
xi 2
)
0.00657 2
%
0.0047 %
4.2 试液吸光度相对应的锰含量引入的标准不确定度分量 4.2.1 工作曲线引入的不确定度
用可见分光光度计测量锰含量时,根据的是郎伯-比尔定律: A KCL,其中 A 为物质的吸光度,K 为物质的吸光系数,C 为物质的浓度,L 为液层的厚度(即比色皿的厚度)。对同一物质,不同浓度的溶 液采用同样厚度的比色器,则 K、L 为常数,A 与 C 之间有正比关系,由此建立一个线性方程,可设 y A , x C ,即有: y a bx ,其中 a、b 均为常数。
平均值
x (%)
x 1 12
12 i1
xi
1.4979
单次测量 实验标准
偏差 s( x )
0.00657%
单次测量标准偏差 s(xi ) 为:
s(xi )
∑12
(xi - x)2
i 1
n -1
∑12
(xi - x)2
i 1
11
0.00657%…………………………………………(2)
实际测量时在重复性试验条件下独立测量 2 次的平均值作为检测结果,平行测定结果为 1.4970%、
第1页 共 10 页
1.2.1 GB 223.63-88《钢铁及合金化学分析方法 高碘酸钠(钾)光度法测定锰量》
1.3 主要测量仪器设备和试剂
1.3.1 可见分光光度计,上海元析仪器有限公司,型号 V-5800,分辨力 0.0001A,检定合格。 1.3.2 电子天平,Sartorius,型号 BSA124S,分辨力 0.1mg,检定合格,最大允许误差±1.0mg。 1.3.3 锰标准溶液,标准值 1000μg/mL,扩展不确定度 U=4μg/mL,k=2。 1.3.4 容量瓶 100mL,天玻,检定合格,最大允许误差±0.10mL。 1.3.5 容量瓶 25mL,天玻,检定合格,最大允许误差±0.030mL。 1.3.6 分度吸量管 10mL,天玻,检定合格,最大允许误差±0.050mL。 1.3.7 分度吸量管 5mL,天玻,检定合格,最大允许误差±0.025mL。
GB1467一78冶金产品化学分析方法标准的总则及一般规

GB / T 223. 40—1985钢铁及合金化学分析方法—离子交换别离—氯磺酚5光度法测定铌量
37
GB / T 223. 41—1985钢铁及合金化学分析方法—离子交换别离—连苯三酚光度法测定钽量
38
GB / T 223. 42—1985钢铁及合金化学分析方法—离子交换别离—溴邻苯三酚红光度法测定钽量
5
GB / T 223. 7—2002铁粉铁含量的测定—重铬酸钾滴定法
6
GB/T 223. 8—2000钢铁及合金化学分析方法—氟化钠别离—EDTA容量法测定铝量
7
GB / T 223. 9—2000钢铁及合金化学分析方法—铬天青S光度法测定铝量
8
GB/T 223. 10—2000钢铁及合金化学分析方法—铜铁试剂别离—铬天青S光度法测定铝量
28
GB/T 223.3l—1994钢铁及合金化学分析方法—蒸馏别离-钼蓝分光光度法测定砷量
29
GB/T 223. 32—1994钢铁及合金化学分析方法—次磷酸钠复原—碘量法测定砷量
30
GB/T 223. 33—1994钢铁及合金化学分析方法—萃取别离—偶氮氯膦mA光度法测定铈量
31
GB / T 223. 34—2000钢铁及合金化学分析方法—铁粉中盐酸不溶物的测定
9
—1991钢铁及合金化学分析方法—过硫酸铵氧化容量法测定铬量
10
GB/T 223. 12—1991钢铁及合金化学分析方法—碳酸钠别离—二苯碳酰二肼光度法测定铬量
11
GB / T 223. 13—2000钢铁及合金化学分析方法—硫酸亚铁铵容量法测定钒量
12
GB / T 223. 14—2000钢铁及合金化学分析方法—钽试剂萃取光度法测定钒量
钢铁中锰含量的测定

实验报告钢铁中锰含量的测定——银盐氧化光度法班级:应111-1姓名:魏颖颖同组:杨玉萍王海花学号:201169503145指导老师:王老师一.实验目的:1.通过实验,了解钢铁中锰的存在形式,测定意义。
2.了解测定钢铁中锰含量的测定方法。
3.掌握钢铁中锰含量的测定原理。
4.熟练掌握分光光度计的使用,进一步训练移液管、容量瓶的正确使用。
5.掌握用比色法测定钢材中锰含量的方法二.实验原理:1.锰在钢铁中主要以MnC、MnS、FeMnSi或固溶体状态存在。
生铁中一般含锰0.5%~6%,普通碳素钢中锰含量较低,含锰0.8%~14%的为高锰钢,含锰12%~20%的铁合金称为镜铁,含锰60%~80%的铁合金称为锰铁。
2.锰溶于稀酸中,生成锰(Ⅱ)。
锰化物也很活泼,容易溶解和氧化。
在化学反应中,由于条件的不同,金属锰可部分或全部失去外层价电子,而表现出不同的价态,分析上主要有锰(Ⅱ)、锰(Ⅲ)、锰(Ⅳ)、锰(Ⅶ),少数情况下亦有锰(Ⅵ),这就为测定锰提供了有利条件。
3.常用测定方法:一般碳素钢,低合金钢,生铁试样常以HNO3(1+3)或硫磷混酸溶解。
难溶的高合金钢以王水溶解,加HClO4或H2SO4冒烟溶解。
溶解试样的酸主要依靠H2SO4,HCl,HNO3,因H2SO4-HCl可使MnS分解。
HNO3分解碳化物(Mn3C)生成CO2逸出,加磷酸可使Fe3+配合成无色而消除Fe3+的干扰。
同时因为磷酸的存在,防止了MnO2沉淀的生成和HMnO4的分解。
4.主要反应方程式:3MnS+12HNO3=3Mn(NO3)2+6HNO3+3SO2+6H2O3Mn3C+28HNO3=29Mn(NO3)2+3CO2+10NO+14H2OMnS+H2SO4=MnSO4+H2S2AgNO3+(NH4)2S2O8=Ag2S2O8+2NH4NO3Ag2S2O8+2H2O=Ag2O2+2H2SO45Ag2O2+2 Mn(NO3)2+6HNO3=2HMnO4+10AgNO3+2H2O三.实验仪器及试剂:1.实验仪器:721型分光光度计,分析天平,容量瓶(50mL),移液管(1ml,2ml,3ml),吸量管(5mL),滴管,洗耳球,电炉2.实验试剂:硝酸溶液(1:3),王水(1浓硝酸+3浓盐酸)硫磷混酸(700ml水中加入150ml磷酸及硫酸150ml,摇匀),0.5%硝酸银溶液,20%过硫酸铵溶液,5%EDTA,锰标准溶液(0.1mg/ml)四.实验步骤:1.溶样:钢样0.25-0.3g于50ml烧杯加5mlH2O,10-15ml王水加热溶解,2mlHClO4加热至冒白烟约2min,冷却,加硫磷混酸10ml加热至冒白烟,除Cl-,冷却定量转移至50ml容量瓶定容,摇匀,备用。
锰矿石化验

锰矿石化验锰矿石是一种重要的金属矿石,可用于生产钢铁、不锈钢、合金、电池等众多工业领域。
而对于锰矿石的品质检测,也是十分关键的一步。
本文将介绍锰矿石化验的相关知识,包括化验方法、化验指标、化验仪器以及化验技术等方面,希望能帮助读者更好地认识这一领域。
一、化验方法目前,对于锰矿石的化验方法主要包括化学分析法和仪器分析法两种方式。
化学分析法又可分为湿法和干法两种。
其中,最为广泛使用的化学分析方法是湿法化学分析法。
常用的化学分析方法包括氧化铅滴定法、还原滴定法、草酸滴定法、重铁盐滴定法、紫外分光光度法等。
而仪器分析法则频繁使用的有原子吸收光谱法、电感耦合等离子体质谱法、荧光光谱法等。
二、化验指标锰矿石化验的关键指标主要包括锰含量、磷含量、硅含量、铁含量、钙镁含量等。
其中,锰含量是对锰矿石品质的最基本要求,通常要求锰含量在40%以上。
磷含量也是一项重要指标,因为磷会影响锰铁合金的质量。
一般要求磷含量在0.1%以下。
硅含量对于锰铁合金的成本、生产效率和质量都有着重要影响,因此要求硅含量在20%以下。
铁含量是指锰矿石中含有多少铁元素,它会影响锰矿石的化学成分和物理性能。
钙镁含量则包括了锰矿石中的钙元素和镁元素的含量,这两种元素也会对锰铁合金的质量产生一定的影响。
三、化验仪器在现代化验中,使用的化验仪器种类繁多。
常用的化验仪器主要包括火焰光度法,原子吸收光谱法和电感耦合等离子体质谱法等。
火焰光度法是一种用于分析金属离子的分析技术,具有分析速度快、操作方便等特点,但只能分析单一元素。
原子吸收光谱法则可以用于同时分析多种元素,但需要专业的操作技术和设备。
电感耦合等离子体质谱法(ICP-MS)则是一种超高灵敏度、高分辨率的元素分析技术,广泛应用于锰矿石化验领域,具有快速效率、精度高等优点。
四、化验技术在锰矿石的化验过程中,需要注意如下几点:1.样品的采集和制备:样品的采集和制备过程应注意防止污染和混杂,同时要遵循规范的操作流程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.分析步骤
(1)普通钢及低合金钢中锰的测定 称取0.5000g试样于250mL锥形瓶中,加入30mL混酸甲,加热溶解,煮沸2~3min,以驱尽氮的氧化物。于溶液中加入80mL水,5mL硝酸银溶液,10mL过硫酸铵溶液,加热.煮沸30~40s,取下.静置1-2min。流水冷却至室温。
(1)标准样品的曲线称取相同或相近牌号,不同锰量的标准样品,同试样操作,绘制吸光度和锰量的标准曲线。
(2)标液的曲线 吸取1,3,5,7,9mL高锰酸钾标准溶液于一组50mL容量瓶中,用水稀释至刻度,摇匀,同试样操作,绘制吸光度和锰量的标准曲线。
5.附注
(1)本法最适于高铬钢、镍铬不锈钢中锰的测定。
一、过硫酸铵与银盐氧化一亚砷酸钠与亚硝酸钠滴定法
1.方法要点
试样以硫、磷、硝混酸溶解,并以硝酸银为催化剂,用过硫酸铵将锰氧化为高锰酸。然后用亚砷酸钠-亚硝酸钠还原。
2.主要反应
2Mn(NO3)2+5Ag2O2+6HNO3=2HMnO4+10AgNO3+2H2O
5Na3AsO3+2HMnO4+4HNO3=2Mn(NO3)2+5Na3AsO4+3H2O
吸取5mL试液于150mL锥形瓶中,加入20mL混合酸,加热近沸.加入5mL过硫酸铵溶液,煮沸1min。冷却后,移人50mL容量瓶中.用水稀释至刻度,摇匀。
空白液:取少量试液加入2滴EDTA溶液,至颜色褪尽。
在渡长530nm处,用2cm比色皿,用空白液调零,测定吸光度。
4.标准曲线的绘制
锰的化合物易溶于硫酸、稀硝酸,形成二价离子。在锰的化台物中,二价锰离子最稳定。这种离子在酸性条件下可能被氧化成七价锰,即高锰酸。用还原剂标准溶液滴定或根据高锰酸根颜色的深度与含量成正比来用分光光度法都可测定锰含量。
国家标准分析方法有:GB/T223.4—1988《钢铁及合金化学分析方法 硝酸铵氧化容量法测定锰量》、GB/T223.58一1987《钢铁及合金化学分析方法 亚砷酸钠一亚硝酸钠滴定法测定锰量》、GB/T223.63—1988《钢铁及合金化学分析方法 高碘酸钢(钾)光度法测定锰量》.GB/T223.64-1988《钢铁及合金化学分析方法 火焰原于吸收光谱法测定锰量》。
5.计算
w(Mn)=V×f/m×100%"
式中 w(Mn)——试样中锰的质量分数,%;
V——消耗亚砷酸钠一亚硝酸钠的体积,mL;
f——亚砷酸钠一亚硝酸钠标准溶液对锰的滴定度,g/mL;
m——称取的试样量,g。
6.跗注
(1)分析生铁或钢中含有石墨碳时,加入25mL水将溶液稀释,并将石墨碳及硅酸沉淀滤去,用硝酸溶液(2%)洗涤数次。
三、锰的炉前快速分光光度法
1.方法要点
试样以酸溶解.在一定的酸度条件下.硝酸银作催化剂,过硫酸铵将锰氧化成高锰酸,测定其吸光度。
2.试剂
(1)混酸 4g硝酸银溶于750mL水中,加250mL浓硝酸,加20mL浓磷酸,混匀。
(2)7%)。
(6)过硫酸铵溶液(25%)。
(7)氯化钠溶液(1%)。
(8)亚砷酸钠一亚硝酸钠标准溶液{c[1/2(Na3AsO3-NaNO3)]=0.05mol/L}称取1.25g三氧化二砷固体于250mL烧杯中,加入50mL NaOH溶液(1mol/L),微热使其溶解,然后
(4)过硫酸铵溶液(15%)。
(5)EDTA溶液(5%)。
(6)高锰酸钾标准溶液[c(1/5KMnO4)=0.01mol/L]。
3.分析步骤
称取0.5000g试样于150mL锥形瓶中,加入15~20mL王水,加热溶解后加人5mL高氯酸,继续加热至冒白烟1min。冷却,加入少量水溶解盐类,并移人50mL容量瓶中,用水稀释至刻度,摇匀。
(2)碳钢或低合金钢可用以下方法:称取0.1000~0.5000g试样加20mL混酸溶解.加过硫酸铵5mL,并加热煮沸1min,冷却后以水稀释至50mL。以水作空白测其吸光度。
(3)生铁试样溶解后,需将石墨碳滤去,以后按(2)碳钢或低合金钢步骤进行。
6.测定范围
锰含量0.070%~1.00%。
(2)溶液煮沸时间不能太长,否则分析结果偏低。
(3)标准样品和试样溶液滴定速度要求一致。
(4)高铬钢等难溶试样,可先加浓盐酸初步溶解后,补加适量硝酸处理。
(5)赶Cl-时,要求冒高氯酸白烟时间达1min以上,以后继续操作至加硝酸银溶液时应无白色沉淀产生为宜;可适当补加硝酸及高氯酸冒烟除尽Cl-。
7.测定范围
锰含量≤10%。
二、分光光度法
1.方法要点
以酸溶解试样.用硝酸银作催化剂.过硫酸铵氧化锰成高锰酸,测定吸光度。
2.试剂
(1)王水(盐酸十硝酸=2+1)。
(2)高氯酸(浓)。
(3)混合酸 1g硝酸银溶于500mL水中,加入25mL浓硫酸,30mL浓磷酸.30mL浓硝酸,用水稀释至1L。
5.测定范围
锰含量0.50%~0.80%。
5NaNO2+2HMnO4+4HNO3=2Mn(NO3)2+5NaNO3+3H2O
3.试剂
(1)混酸甲(硫酸+磷酸+硝酸+水=100+125+250十525)。
(2)混酸乙(硝酸+磷酸+水=50+700+250)。
(3)王水(盐酸+硝酸=3+1)。
(4)高氯酸(浓)。
工厂实用分析方法有:过硫酸铵法、分光光度法。
过硫酸铵法的优点是简便、快速、准确;主要缺点是亚砷酸钠与高锰酸反应在终点时并不能完全将七价锰还原成二价,同时还存在三价和四价锰。因此,此法不能用理论值计算结果,而必须用标样计算滴定度。另外,铬量高时,终点不易观察.必须分离铬。
分光光度法为钢铁中锰的快速分析方法。
加入5mL氯化钠溶液,摇匀.立即用亚砷酸钠一亚硝酸钠滴至红色消失。
(3)高铬钢中锰的测定 称取0.5000g试样于250mL锥形瓶中.加入10mL王水,加热溶解.再加入10mL高氯酸,加热至冒高氯酸白烟,用浓盐酸使铬挥发尽,并驱尽Cl-至近干,取下,稍冷。
以下操作同(1)普通钢及低合金钢中锰的测定.,
溶液中加入5mL氯化钠溶液,立即用亚砷酸钠-亚硝酸钠滴定至红色消失。
(2)高锰钢中锰的测定 称取0.1000g试样于250mL锥形瓶中,加入10mL混酸乙,低温溶解,并驱尽氮氧化物。加入80mL水,10mL硝酸银溶液,40mL过硫酸铵溶液,加热,煮沸30-40s。取下,静置1min,流水冷却至室温;
锰是金属材料中的重要台金元索之一。它在钢中通常以固溶体及化合态形式存在。锰是良好的脱氧剂和脱硫剂,能降低由于钢中的硫所引起的热脆性,从而改善钢的热加工性能.提高钢的可锻性。增加锰的含量,可提高钢的强度和硬度。
普通钢中含锰量为0.25%~8%,低合金锰钢中锰的含量为0.8%~1.5%,耐磨的高锰钢的锰量达14%。
称取0.0500g试样于100mL三角瓶中,加入15mL混酸,加热溶解,加入5mL过硫酸铵(10%),煮沸10s,立即加入50mL水。于波长530nm处,用1cm比色皿,以水作空白,测定吸光度。
4.标准曲线的绘制
称取相同或相近牌号,不同锰量的标准样品,同试样操作,绘制吸光度和锰量的标准曲线或采用标样测定系数计算分析结果。
