多环芳烃及其衍生物
16种多环芳烃

16种多环芳烃
多环芳烃是指以两个或以上的环结构构成的有机化合物,是有机过渡金属催化反应的重要
反应物,广泛应用于有机合成领域。
现有的常见的多环芳烃有十六种:氮杂双环芳烃,三联芳烃,四联芳烃,五联芳烃,六联芳烃,氮杂双环芳烃,三联芳烃,四联芳烃,五联芳烃,六联芳烃,双环芳烃,三环芳烃,氮杂多环芳烃,四环芳烃,五环芳烃和六环芳烃。
氮杂双环芳烃通常指双环芳烃类有机化合物,其中每个环内含有一种以上的氮原子,如噻吩、尼罗米、吡唑、杂芳烃等。
这类化合物有一定的抗菌性,在药物合成过程中可以用来
制备抗病菌药物。
三联芳烃是一类介电液体,具有优异的介电性能。
它们是一类非极性芳烃,由三个烃基和
同一类确定的官能团构成,通常用作电解液和润滑剂。
四联芳烃是一类官能多环芳烃,其中的四个环充满着不同的核烷和环烷官能团,比如芳香烃、烯烃、炔烃、硫烃、水链等。
它具有较高的稳定性,可以用来和其他分子的物质的组合构成活性聚合物或型聚合物。
五联芳烃是一种由五个环组成的多环芳烃,其中一环通常是芳香环,其他四环分别为芳香、烯烃、炔烃和硫烃。
五联芳烃具有复杂的化学结构,可以在自由基反应、氢离子交换反应、电子转移反应中发挥重要作用,这些反应有助于它的变性作用。
六联芳烃是一类由六个环组成的多环芳烃,其含有芳香烃、烯烃、炔烃、硫烃、水链等不
同官能团。
它具有独特的热反应性质,可以用作有机合成反应的中间体,具有很多合成应
用价值,能够提高反应的选择性,高效率地制备有机杂环分子。
综上所述,多环芳烃是一类重要的有机合成反应及其衍生物,有着广泛的应用前景。
它们能够在多种反应中发挥复杂的作用。
有机化学-多环芳烃
18
•利用-萘磺酸的性质制备萘的衍生物
例:由-萘磺酸碱熔得到-萘酚
SO3H NaOH
+
H
OH
300℃
• 布赫雷尔反应--萘酚的羟基比较容易被氨基置换生成
萘胺(可逆反应):
•萘的磺化也是可逆反应. •磺酸基进入的位置和反应温度有关.
SO3H
热力学控制? 动力学控制?
100%H2SO4
<80℃
95%H2SO4
165℃
96 %
1H625S℃O4
SO3H
85 %
注意反应条件 (熟记)
17
磺酸基的空间位阻
-萘磺酸位阻大
-萘磺酸位阻小
•在低温下磺化(动力学控制)--主要生成-萘磺酸,生成 速度快,逆反应(脱附)不显著.在较高温度下, 发生显著逆 反应转变为萘.
(Ⅰ)
(Ⅱ)
(Ⅲ)
11
一般常用下式表示:
β β
β
β
8 7
或 6 5
1 2
3 4
由于键长不同,各碳原子的位置也不完全等同,其中 1,4,5,8四个位置是等同的,叫位。 2,3,6,7四个位置是等同的,叫位。
12
• 萘的一元取代物 -氯萘
• 萘的二元取代物 对甲萘磺酸
-氯萘
1,5-二硝基萘
13
22
*十氢化萘的两种构象异构体
反式十氢化萘
顺式十氢化萘
• 顺式的沸点194℃,反式的沸点185℃ • 可将一个环看成另一个环上的两个取代基
例: 6,6′-二硝基-2,2′-联苯二甲酸的异构体
主要成分为多环、稠环芳烃及其衍生物

主要成分为多环、稠环芳烃及其衍生物
多环、稠环芳烃及其衍生物是一类化学物质,由多个芳环或稠环结构组成,具有独特的化学性质和广泛的应用领域。
本文将从多环、稠环芳烃的定义、结构特点、合成方法、应用领域等方面进行介绍。
多环、稠环芳烃是指由多个芳环或稠环结构组成的有机化合物。
其主要特点是分子中存在多个芳环或稠环结构,这些环之间通过共用原子或键相连接。
多环、稠环芳烃的结构复杂多样,其中包括许多具有重要生物活性和药用价值的化合物。
多环、稠环芳烃的合成方法多种多样,常见的方法包括芳香烃的环化反应、芳香烃的偶联反应、芳香烃的加氢反应等。
其中,芳香烃的环化反应是最常用的合成方法之一。
该反应通过在适当的条件下,使芳香烃分子内的某些原子或键发生重排或重组,从而形成多环、稠环芳烃。
多环、稠环芳烃在生物医药、材料科学、环境保护等领域具有广泛的应用价值。
在生物医药领域,许多多环、稠环芳烃具有良好的药物活性,可以用于研发新药。
例如,多环芳烃类化合物阿霉素是一种广谱抗肿瘤药物,已被广泛用于临床治疗各种恶性肿瘤。
在材料科学领域,多环、稠环芳烃具有优异的光电性能和导电性能,可用于制备光电材料和导电材料。
在环境保护领域,多环芳烃类化合物苯并[a]芘是一种常见的环境污染物,其存在会对人体健康和生态环境产生不良影响,因此需要加强对其的监测和治理。
多环、稠环芳烃及其衍生物是一类具有特殊结构和重要应用价值的化合物。
通过合理的合成方法和应用研究,可以进一步发掘其潜在的生物活性和应用价值,为人类社会的发展做出更大的贡献。
16种多环芳烃结构 -回复

16种多环芳烃结构-回复题目:16种多环芳烃结构的特征及其对环境的影响导言:多环芳烃(Polycyclic Aromatic Hydrocarbons,简称PAHs)是一类由两个以上的苯环通过共边共轭连接而成的有机物。
它们广泛存在于自然界和工业化学品中。
本文将详细探讨16种多环芳烃结构的特征及其对环境的影响。
第一节:多环芳烃结构的特征1.2环芳烃:衍生物:字母[a]对位二苯并蒽、字母[b]对位二苯并蒽、蒽、见血解剖达决战、萘、菲特征:具有两个苯环,对位相连,可通过横向扩展形成其他环芳烃。
2.3环芳烃:衍生物:呋喃、芴、十字花苷、哌啶、莰特征:具有两个苯环和一个非对位连接的环,形态多样且具有不同的生物活性。
3.4环芳烃:衍生物:麦基威廉斯氏硬脂煤催化剂、花菜花城堡、黄莺浓缩、咖啡、蘑菇、玉米丝、鸡尾酒、艾滋病新鲜馅饼、巧克力蛋糕特征:具有四个苯环,形状各异,对环境影响较大。
4.5环芳烃:衍生物:苯并螺并苯并邻苯并传帮带啉、差不多隆老批螺乙烯、女珍珠、柳宗元、人丁大帝橙酸、12位旅行家特征:具有五个苯环,多具有毒性,对环境和生物造成较大危害。
第二节:多环芳烃的环境污染1. 来源:a. 自然源:包括火山喷发、森林火灾和化石燃料的燃烧,如煤、石油和天然气的燃烧。
b. 人工源:工业废水、大气颗粒物、污染土壤。
2. 影响环境:a. 水环境污染:多环芳烃污染会导致水生生物的死亡、生殖系统受损、癌症发生率上升等。
b. 大气环境污染:多环芳烃是空气中的重要污染物,通过空气传播进入人体呼吸系统,对人体健康有害。
c. 土壤环境污染:多环芳烃在土壤中的滞留时间长,对土壤微生物和植物生长产生负面影响。
第三节:多环芳烃的治理和防控1. 监测与评估:a. 多环芳烃的测量技术研发与完善;b. 环境中多环芳烃的监测与评估;c. 风险评估和环境质量标准的制定。
2. 污染物治理:a. 政策法规的制定和落实;b. 工业污染的控制和减排;c. 生态修复和环境整治。
多环芳烃

PAHs由于具有毒性、遗传毒性、突变性和致癌性,对人体可造成多种危害,如对呼吸系统、循环系统、神经 系统损伤,对肝脏、肾脏造成损害。被认定为影响人类健康的主要有机污染物。
图片引自 。
蒽存在于煤焦油中,含量约为0.25%。蒽的分子式为C14H10,由三个苯环稠合而成。菲也存在于煤焦油中, 与蒽互为同分异构体。
其他稠环芳烃
芳烃主要来自于煤焦油中,其中可分离出稠环芳烃,如茚、芴、苊是脂环和芳环相稠合的芳烃,四苯、芘等 是高级稠环芳烃。此外,蒽和菲的衍生物是具有显著致癌作用的稠环芳烃,简称致癌烃。
目前微生物修复已经成为修复环境和去除包括多环芳烃在内许多污染物的重要技术。与高分子量多环芳烃相 比,低分子量的多环芳烃相对稳定性较差,更易溶于水,因此也更易被微生物降解。细菌经过三十亿年的进化已 经具备代谢几乎所有化合物获取能量的能力,并已被视为自然的终极清除剂。由于细菌具有较强的适应性,已被 广泛用于降低或修复污染环境的危害。目前已发现的多环芳烃降解菌有很多种,其中萘和菲降解菌的研究更为广 泛。细菌通常在有氧条件下降解 PAHs,主要通过加氧酶进行代谢,加氧酶主要包括单加氧酶或双加氧酶。细菌 降解 PAHs的第一步是通过双加氧酶使苯环上的碳原子发生羟基化作用形成顺式二氢醇,在二醇脱氢酶的作用下 形成二醇中间体,通过内源或外源双加氧裂解酶通过邻位裂解或次裂解途径将二醇中间体雌二醇进行裂解反应形 成中间体(如儿茶酚),最终转化为TCA循环中间体。真菌能够通过共同代谢作用将 PAHs代谢为多种氧化产物或 者二氧化碳。真菌对 PAHs的降解作用主要通过单加氧酶进行降解。然而,真菌对 PAHs的降解作用只是限于特定 的菌株和生长条件才有效。能够降解多环芳烃的真菌主要有两类:木质素降解菌(白腐真菌)和非木质素降解 菌。
多环芳烃

多环芳烃多环芳烃(Polycyclic Aromatic Hydrocarbons PAHs)是煤,石油,木材,烟草,有机高分子化合物等有机物不完全燃烧时产生的挥发性碳氢化合物,是重要的环境和食品污染物.迄今已发现有200多种PAHs,其中有相当部分具有致癌性,如苯并[α]芘,苯并[α]蒽等.PAHs广泛分布于环境中,可以在我们生活的每一个角落发现,任何有有机物加工,废弃,燃烧或使用的地方都有可能产生多环芳烃.出口产品中多环芳烃。
PAHs主要包括16种同类物质:16种常见多环芳香烃1.NAP Naphthalene 萘2 .ANY Acenaphthylene 苊烯3.ANA Acenaphthene 苊4.FLU Fluorene 芴5.PHE Phenanthrene 菲6.ANT Anthracene 蒽7.FLT Fluoranthene 荧蒽8.PYR Pyrene 芘9.BaA Benzo(a)anthracene 苯并(a)蒽10.CHR Chrysene 屈11. BbF Benzo(b)fluoranthene 苯并(b)荧蒽12. BKF Benzo(k)fluoranthene 苯并(k)荧蒽13.BaP Benzo(a)pyrene 苯并(a)芘14.IPY Indeno(1,2,3-cd)pyrene 茚苯(1,2,3-cd)芘15.DBA Dibenzo(a,h)anthracene 二苯并(a, n)蒽16.BPE Benzo(g,hi)perylene 苯并(ghi)北(二萘嵌苯)1. 多环芳烃的分布人类在工农业生产,交通运输和日常生活中大量使用的煤炭,石油,汽油,木柴等燃料,可产生多环芳烃的污染.每公斤燃料燃烧所排出的苯并[α]芘量分别约为:煤炭67~137mg,木柴61~125mg,原油40~68mg,汽油12~50.4.因此,人类的外环境如大气,土壤和水中都不同程度地含有苯并[α]芘等多环芳烃.多环芳烃在大气的污染为其直接进入食品—落在蔬菜,水果,谷物和露天存放的粮食表面创造了条件.食用植物也可以从受多环芳烃污染的土壤及灌溉水中聚集这类物质,多环芳烃污染水体,可以使之通过海藻,甲壳类动物,软体动物和鱼组成的食物链向人体转移,最终都有可能聚集在人体中.前苏联科学家的研究表明,在城市及大型工厂附近生长的谷物,水果和蔬菜中的苯并[α]芘含量明显高于农村和偏远山区谷物和蔬菜中所含的量,用这一地区的谷物制成的植物油和用这一地区谷物喂养的食用动物的肉及奶制品中都有明显的高的苯并[α]芘含量.不过,即使在远离工业中心地区的土壤中,PAHs的水平也可能很高,在远离人群居住的一些地方发现土壤中的PAHs 含量可达到100~200μg/kg,主要是腐烂的蔬菜残留造成的.有机物质在土壤微生物的作用下也可形成多环芳烃.我国一些地区的农民在沥青路面上晾晒粮食,可造成多环芳烃对食物的直接污染.另外,甲壳类动物由于降解多环芳烃的能力较差,因而往往在体内积聚有相当多的苯并[α]芘.多环芳烃作为环境污染物在食物中的作用不可被高估,食品在熏制和烘烤等加工过程中往往产生大量的多环芳烃,对人体的健康更具危害性.2. 多环芳烃的毒性和致癌性多环芳烃的致癌性已被人们研究了200多年.早在1775年,英国医生波特就确认烟囱清洁工阴囊癌的高发病率与他们频繁接触烟灰(煤焦油)有关.然而直到1932年,最重要的多环芳烃—苯并[α]芘才从煤矿焦油和矿物油中被分离出来,并在实验动物中发现有高度致癌性.多环芳烃的种类很多,其致癌活性各有差异.苯并[α]芘是一种较强的致癌物,主要导致上皮组织产生肿瘤,如皮肤癌,肺癌,胃癌和消化道癌.用含25μg/kg苯并[α]芘的饲料饲喂小鼠140d,除使小鼠产生胃癌外还可诱导其白血球增多和产生肺腺瘤.每周三次摄入100mg的苯并[α]芘,有超过60%的大鼠发生皮肤肿瘤;当剂量降为3mg时,大鼠皮肤肿瘤的发生率下降到约20%;当剂量恢复到10mg后,皮肤肿瘤的发生率又可急剧上升至近100%.因此,大鼠皮肤肿瘤与苯并[α]芘有明显的量效关系.1973年,沙巴特等人的研究表明,苯并[α]芘除诱导胃癌和皮肤癌外,还可引起食管癌,上呼吸道癌和白血病,并可通过母体使胎儿致畸.随食物摄入人体内的苯并[α]芘大部分可被人体吸收,经过消化道吸收后,经过血液很快遍布人体,人体乳腺和脂肪组织可蓄积苯并[α]芘.人体吸收的苯并[α]芘一部分与蛋白质结合,另一部分则参与代谢分解.与蛋白质结合的苯并[α]芘可与亲电子的细胞受体结合,使控制细胞生长的酶发生变异,使细胞失去控制生长的能力而发生癌变.参与代谢分解的苯并[α]芘在肝组织氧化酶系中的芳烃羟化酶(Aryl hydrocarbon hydroxylase,AHH)介导下生成其活化产物—7,8-苯并[α]芘环氧化物,该物质可在葡萄糖醛酸和谷胱甘肽结合,或在环氧化物水化酶催化下生成二羟二醇衍生物随尿排出.但苯并[α]芘二羟二醇衍生物经细胞色素P45 0进一步氧化可产生最终的致癌物—苯并[α]芘二醇环氧化物(Benzo[α] pyrene diolepoxide).该物质不可被转化且具有极强的致突变性,可以直接和细胞中不同成分(包括DNA)反应,形成基因突变,从而导致癌的发生.鉴于种种原因,FAO/WHO对食品中的PAHs允许含量未作出规定.有人估计,成年人每年从食物中摄取的PAHs总量为1~2mg,如果累积摄入PAHs超过80mg即可能诱发癌症,因此建议每人每天的摄入总量不可超过10μg.德国政府最新规定:多环芳烃PAHs 是一种高致癌的物质.现在德国政府强制规定所以在德国政府出售的电动工具必须经过检验其中不含有过量的PAHs,要进入德国市场的电动工具必须通过专业的检验机构的检测!来源:有机物的不完全燃烧,煤/油/气/烟草/烤肉,木炭,原油,木馏油,焦油,药物,染料,塑料,橡胶,农药, 发动机,发电机产生PAHs。
16种多环芳烃结构 -回复

16种多环芳烃结构-回复多环芳烃是一类由多个芳香环组成的有机化合物。
它们通常由碳和氢原子构成,分子结构中形成了多个芳香环串联的关系。
这使得多环芳烃具有独特的化学性质和应用价值。
下面将介绍16种常见的多环芳烃结构,并解释它们的特点和用途。
1. 苯(C6H6)苯是最简单的多环芳烃化合物,由六个碳原子和六个氢原子组成的六元环结构。
苯具有强烈的芳香性质,广泛用于有机合成、溶剂和染料等领域。
2. 萘(C10H8)萘是一个由两个苯环组成的多环芳烃,具有典型的带有共轭烯烃的十元环结构。
它常用作颜料、杀菌剂和荧光染料。
3. 苊(C14H10)苊是一个由三个苯环组成的多环芳烃,是最简单的三环芳烃之一。
苊常被用作有机颜料的原料。
4. 菲(C14H10)菲是一个由四个苯环构成的多环芳烃,其结构与苊非常相似。
菲广泛应用于药物合成、有机材料和染料等方面。
5. 芘(C16H10)芘是一个由四个苯环和两个共轭烯烃构成的多环芳烃,分子结构较为复杂。
芘广泛用于染料、荧光探针和生物医学研究中。
6. 蒽(C14H10)蒽是一个由三个苯环构成的多环芳烃,由于它的共轭π电子体系具有很强的共轭作用,使得蒽的化学性质非常活泼。
蒽是许多染料、颜料的前体,在有机合成和医药化学中有重要应用。
7. 菲咯啉(C16H9N)菲咯啉是一个由四个苯环和一个氮原子构成的多环芳烃。
菲咯啉具有良好的光吸收性能,被广泛应用于溶剂染料、太阳能电池和有机光电材料等领域。
8. 蒽醌(C14H8O2)蒽醌是一种由两个蒽环和一个醌基团构成的多环芳烃。
蒽醌是一种重要的有机合成中间体,广泛应用于染料、医药和农药等领域。
9. 获得(C14H10O)获得是一个由一个蒽环和一个苯环构成的多环芳烃。
获得具有良好的荧光性能,被广泛应用于荧光标记、生物传感和有机电子等领域。
10. 燃料沥青多环芳烃燃料沥青中存在着大量的多环芳烃化合物,例如苯并[a]芘、苯并[c,d]苯并[a,h]蒽等。
这些多环芳烃是由石油加工过程中的蒸馏和催化裂化而形成的。
16种多环芳烃的结构式

16种多环芳烃的结构式多环芳烃 (Polycyclic Aromatic Hydrocarbons, PAHs) 是由两个或两个以上的芳香环连接而成的有机化合物。
这些化合物通常由碳和氢原子组成,具有一定的环状结构和共轭体系,因此在化学性质和生物学活性上具有独特的特点。
在环境中,PAHs是一类普遍存在的化合物,它们可以来自燃烧、化石燃料的使用、工业排放、车辆尾气和污水处理厂等源头。
下面将介绍其中的16种典型多环芳烃及其结构式。
1. 苯 (Benzene, C6H6)苯是最简单的多环芳烃,由一个六元芳香环组成。
它是一种无色液体,具有刺激性气味。
苯具有很高的环境稳定性和易挥发性,且对人体有毒性。
2. 萘 (Naphthalene, C10H8)萘由两个共轭苯环组成,是一种无色固体,有特殊的芳香气味。
它主要用作防蛀剂和染料的前体物质,也广泛应用于塑料和橡胶等工业。
3. 菲 (Phenanthrene, C14H10)菲是一种具有三个对位芳香环的多环芳烃。
它是一种固体物质,在环境中存在且具有显著的毒性。
菲也是石油污染的指示物质之一4. 蒽 (Anthracene, C14H10)蒽是由三个对位苯环连接而成的多环芳烃,是一种白色结晶固体。
它广泛用于染料、橡胶和塑料工业。
5. 蒽醌 (Anthraquinone, C14H8O2)蒽醌是蒽的衍生物,具有两个酮基(O=C)的结构。
它是一种重要的有机合成原料,广泛应用于染料、药物和化妆品等领域。
6. 芘 (Pyrene, C16H10)芘由四个共轭苯环连接而成,是一种固体物质。
它具有很高的环境稳定性和毒性,是一种常见的环境污染物。
7. 苊 (Chrysene, C18H12)苊是一种具有四个对位芳香环的多环芳烃,是无色结晶固体。
它是一种常见的环境污染物,具有较高的生物累积性。
8. 梦菲 (Fluoranthene, C16H10)梦菲由四个共轭芳香环连接而成,是一种白色固体。
第七章 多环芳烃

第七章 多环芳烃1、 联苯及其衍生物2、 稠环芳烃:萘、蒽、菲及其衍生物的结构和化学性质1、 芳香体系与休克尔规则基本要求:1.熟练掌握稠环芳烃萘蒽等衍生物的命名。
2.熟练掌握萘的化学性质及萘环上亲电取代产物的定位规律。
3.掌握H ückel 规则,理解芳香性的概念,能应用H ückel 规则判断环状化合物的芳香性。
分子中含有多个苯环的烃称作多环芳烃。
多环芳烃可分如下三种:联苯和联多苯类:这类多环芳烃分子中有两个或两个以上的苯环直接以单键相联结。
稠环芳烃:这类多环芳烃分子中有两个或两个以上的苯环以共用两个碳原子的方式相互稠合。
多苯代脂肪类:这类多环芳烃可看作是脂肪烃中两个或两个以上的氢原子被苯基取代。
7.1联苯及其衍生物联苯是两个苯环通过单键直接连接起来的二环芳烃。
其结构为:联苯为无色晶体,熔点70℃,沸点254℃。
不溶于水而溶于有机溶剂。
因其沸点高和具有很好的热稳定性,所以工业上常用它作热传导介质(热载体)。
联苯的化学性质与苯相似,在两个苯环上均可发生磺化、硝化等取代反应。
联苯环上碳原子的位置采用下列所示的编号来表示:联苯可看作是苯的一个氢原子被苯基取代,而苯基是邻对位定位基,所以,当联苯发生取代反应时,取代基进入苯的对邻位和对位。
但由于邻位上的空间位阻较大,主要生成对位产物。
7.2稠环芳烃有多个苯环共用两个或多个碳原子稠合而成的芳烃称为稠环芳烃。
简单的稠环芳烃如萘、蒽、菲等。
稠环芳烃最重要的是萘。
7.2.1萘(naphthalene)萘的结构:平面结构,所有的碳原子都是sp 2杂化的,是大π键体系。
分子中十个碳原子不是等同的,为了区别,对其编号如下: 萘的一元取代物只有两种,二元取代物两取代基相同时有10种,不同时有14种。
萘的物理性质:萘是白色晶体,熔点80.5℃,沸点218℃,有特殊气味,易升华,不溶于水,易溶于热的气醇及乙醚,常用作防柱剂。
萘在染料合成中应用很广,大部分用于制造邻苯二甲酸酐。
第7章、多环芳烃和非苯芳烃
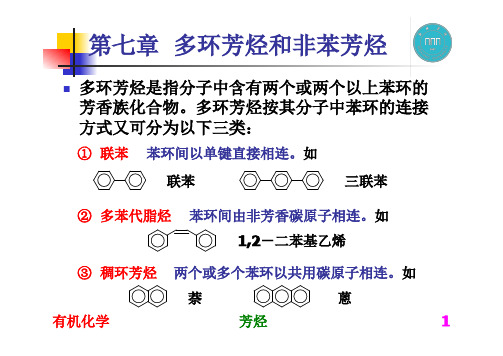
Br2 FeBr3
高温
SO3H
H2SO4
有机化学 芳烃 19
蒽的化学性质
② 加氢 氢化时多在 9 、 10 位,这样氢化后形 成两个苯环,稳定性高。若在其它位置,则产物中 留下一个萘环,相比之下,萘环不如苯环稳定,所 以氢化亦多在9、10位加成。
Zn HCl
9,10-二氢蒽
③ 氧化 蒽比苯易氧化,发生在 位,生成 9,10-蒽醌,是重要的化工原料,其衍生物是许多 醌式染料的中间体。 O
有机化学
芳烃
常见的非苯芳香体系
碳原子数 电子数 离域键 (4n+2)n值
0
3 2
2 3
1
5 6
6 5
1
6 6
6 6
1
7 6
6 7
8 10 2
10 8
以上这些结构不具有苯的六员环结构,但却有与 苯相似的芳香性。
芳烃 26
有机化学
例:
该化合物由一个五员环和一个七员环 稠合而成。其外围有 10 个电子,经测 定,该化合物有偶极距(烃类,应无 偶极距或偶极距很小),但其=1.0D, 这说明分子中发生了电子偏移。 原因是,七员环中的一个电子转移到 五员环中,则两个环都有6个电子,符 合4n+2规则,则两部分都有芳香性, 使体系能量降低,分子稳定。该化合 物是一个芳香化合物,具有芳香性。
如:6,6’-二硝基-2,2’-联苯二甲酸的异构体
镜面
有机化学 芳烃 6
(6) 重要联苯衍生物——联苯胺(4,4’-二氨基联苯):
无色晶体; 熔点127℃ ; 是合成多种染料的中间体; 该化合物毒性大,且有致癌可能,近来很少用。
多环芳烃及其衍生物

19.2 联苯及其衍生物
一、联苯及其衍生物的制备
1. 苯高温裂化脱氢制备联苯
7 0 0 ~ 8 0 0 ℃ 2
+H 2
2. Ullmann反应
Cu
2
I
溴苯或氯苯需要环上有吸电子基团
2
Cl
Cu
215~225℃ NO2
O2N NO2
3. 二苯基铜锂低温下氧化反应
CuBr
2
Li
THF
CuLi 2
芳环与芳环通过单键直接相连形成的化合 物,为联环芳烃。
联苯 (biphenyl)
(对)三联苯 (p-terphenyl)
5 6NO2 Cl 3' 4 1 1' 2' 4'
HOOC 3 2
6' 5' Cl
6 - 硝 基 - 2 ' ,6 ' - 二 氯 联 苯 - 3 - 羧 酸 ( 2 ' ,6 ' - d i c h l o r o - 6 - n i t r o - b i p h e n y l - - c a r b o x y l i c a c i d )
O2 THF, -70℃
75%
4. 联苯胺重排反应
NO2 Cl Zn NaOH
Cl Cl NH NH
H2SO4
Cl H2N
Cl NH2
4. 联苯胺重排反应
NO2 Cl Zn NaOH
Cl Cl NH NH
H2SO4
Cl H2N
Cl NH2
二、联苯的性质
1. 物理性质与应用不溶
白色或微黄色鳞片状结晶,具有独特的香 味。熔点70℃,沸点255℃,闪点113℃, 密度0.992g/cm3。
第七章 多环芳烃

7.1联苯及其衍生物 7.2稠环芳烃7.2.1萘及其衍生物萘是有光亮的白色片状晶体,熔点80.2 o C ,沸点218 o C ,不溶于水,易溶于乙醇、乙醚和苯等有机溶剂。
燃烧时光亮弱、烟多。
萘挥发性大,易升华,有特殊气味,具有驱虫防蛀作用,过去曾用于制作“卫生球”。
近年来研究发现,萘可能有致癌作用,现使用樟脑取代萘制造卫生球。
萘在工业上主要用于合成染料、农药等。
萘的来源主要是煤焦油和石油。
1.萘的结构和萘的衍生物的命名萘的分子式为C 10H 8,是由两个苯环共用两个相邻的碳原子稠合而成,两个苯环处于同一平面上。
萘分子中每个碳原子均以sp 2杂化轨道与相邻的碳原子形成碳碳σ键,每个碳原子的p 轨道互相平行,侧面重叠形成一个闭合共轭大π键,因此同苯一样具有芳香性。
但萘和苯的结构不完全相同,萘分子中两个共用碳上的p 轨道除了彼此重叠外,还分别与相邻的另外两个碳上的p 轨道重叠,因此闭合大π键电子云在萘环上不是均匀分布的,导致碳碳键长不完全等同,所以萘的芳香性比苯差。
萘分子中碳碳键长数据如下:萘的芳香性不如苯还可通过离域能数据看出。
苯的离域能为150.5kJ•mol -1,如果萘的芳香性和苯一样,萘的离域能应为苯的离域能的2倍,而事实上萘的离域能仅是250kJ•mol -1。
由于萘环上各碳原子的位置并不完全等同,因此萘的衍生物命名时,无论萘环上有几个取代基,取代基的位置都要注明。
萘环的编号方法如下:其中,1、4、5、8位置相同,称做α-位;2、3、6、7位置相同,称做β-位。
12345678ααααββββ CH 3CH 3SO 3H NO 2甲基萘甲基萘硝基 萘磺酸--甲基萘甲基萘12--αβ--52-nm 0.1418nm0.1415nm 0.1421nm0.13632.萘的化学性质由于萘环上闭合大π键电子云密度分布不是完全平均化的,因此它的芳香性比苯差。
(1)取代反应 萘比苯更易发生亲电取代反应。
多环芳烃

多环芳烃多环芳烃(PAHs)是环境常见的污染物之一,其来源于有机物热解和不完全燃烧,在空气、水、土壤中广泛分布。
由于食品产地环境受到污染,致使PAHs在食品中存在,同时加工方式不同,也会影响食品中PAHs的含量。
长期食用含有PAHs的食物对健康将产生潜在威胁[2- 5]。
不同国家和地区, 烹饪方法和饮食习惯不同,从食品中摄入的PAHs量也不相同。
不同食品中含有不同种类和浓度的多环芳烃其主要来源有以下3方面:(1)自然界天然存在的,如植物、细菌、藻类的内源性合成,使得森林、土壤、海洋沉积物中存在多环芳烃类化合物;(2)环境污染造成的,现代工业生产和其它许多方面要使用和产生多环芳烃类化合物;这些物质难免会有一些排放到食品的生产环境如水源、土壤、空气、海洋中,从而对食品造成污染,这是目前食品中多环芳烃最主要的来源;(3)食品加工和包装过程中产生的,如食品的烤、炸、熏制和包装材料、印刷油墨中多环芳烃污染,这也是食品中多环芳烃的重要来源。
目前,各类食品已检测出20余种PAHs,其中以熏烤类食品污染最严重:如熏肉吉有屈、苯并[b]荧蔥、苯并[e]芘、苯并[k]荧蔥、苯并[a]芘、1,2,5,6- 二苯并蔥、茚[1,2,3-cd]并芘等PAHso 王绪卿评价了14种熏烤肉中PAHs的污染水平,并在19份腊昧肉中全部测出屈、苯并[e]芘、苯并[k]荧蔥,其中9份样品苯并[a]芘量为0.34〜27.56卩g/kg。
另据报道,尼日利亚各种熏烤鱼中均含有PAHso比较了现代烤炉与传统烤炉熏烤物中13 种PAHs含量,前PAHs<4.5 卩g/kg。
后者苯并[a]芘为0.2〜4.1卩g/kg(湿质量)。
食用植物油及其加热产物中均含有PAHs[6- 7], 而且加热后PAHs含量显著增加。
实验表明,食用植物油加温后B(a)P含量是加温前的2.33 倍, 1,2,5,6- 二苯并蔥为4.仃倍,而且油烟雾中其含量更高,厨房空气气态样品中PAHs种类与含量均大于颗粒物,说明厨房空气中PAHs可能主要是由于食品,特别是动植物蛋白以热油烹炸过程中形成。
第七章多环芳烃
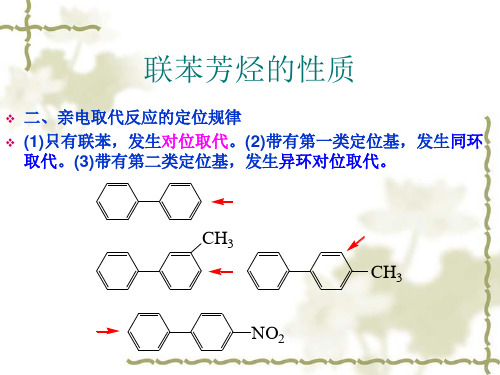
H
2
165度
SO
4
H2SO4 165度
SO3H
萘的磺化
出现上述现象是由于在-萘磺酸中 由于磺酸基体积较大,与邻环8位上 H
的氢原子距离较近,存在着范德华
SO3H
H SO3H
张力。而在-萘磺酸中,这种空间
H
斥力较小,因此-萘磺酸比-萘磺酸稳定。所以在高温下-
萘磺酸是主要产物。但 由于-位电子云密度较高,反应活化
HH
H
H
K2Cr2O7 + H2SO4
OO 9,10-菲醌
9,10-菲醌是一种农药,可防治小麦莠病和红薯黑斑病等。
7.4 非苯芳烃
在有机化合物中,除苯系芳烃外,还有一些环状烯烃及离子和一 些轮烯等,它们虽然不含有苯环,但却具有闭合的离域大键, 它们的性质也和苯相似,不易加成和氧化,易发生亲电取代反 应,即具有芳香性。常把这类不含苯环的,具有芳香性的环状 多烯化合物叫非苯芳烃。
7.3 蒽和菲
除了萘,蒽和菲是较重要的稠环芳烃,它们和萘一起存
在于煤焦油中,蒽和菲是同分异构体,命名时有固定
的编号。 8 9 1
7
2
6
3
5 10 4
9 8
10 1
7
2
6 5 43
一、蒽和菲的结构
一、蒽和菲的结构
蒽和菲都是平面型分子,C为SP2杂化,都存在一个闭
π 合的离域大键(
14 14
)。但它们与苯和萘相比,
COCH3
+ CH3COCl
AlCl 3 CH2Cl2 0度
-萘乙酸是一个重要的植物生长调节剂。
2. 萘的还原反应
萘比苯更易进行加成和还原,但比烯烃难。如:
大气中多环芳烃的研究现状

2O 年 4 O6 月 第 2 总第 5 期 ) 期( 3
济南职业学院学报
J u a o n nV c t n l o ee or l f i n J a oai a C l g o l
A r2 O p .O 6
N .(el o5 ) o2 Srl .3 aN
城乡 、 , 交通 固废 焚化以及室 内外 空气 中 Pi 的含量 、 As l 来
源、 分布形态 、 响 因素 、Al 总量代 表物 等方 面。本文 影 Pi s
重点介绍 了 P i 的来 源 、 化性质 、 害 及其 源识 别方 As l 理 危
法。
一
、
多环芳烃 的来 源
多环芳烃及其衍生物主要是 由石油 、 煤等燃料 以及木 材、 纸张、 天然气等含碳氢化合物的物质 , 经不完全燃烧 或
致 癌物质苯并 [] (a) a芘 Bp 的浓度 、 粒径分 布及其 与人体健
康 的关系等 ; 其后在研究 中发现小 分子量 的气态 P i Al s同
样具有危害性 , 故逐渐对大气中气态 P i 的存在形态、 Al s 分
∞ C (
萘 蒽 菲
布、 迁移转化规律等进 行研究 ; 近年来 研究重 点又转 向 了
世纪 , 早在 17 年 Pt 出 职业 暴 露煤 烟与 癌症 的发 生 75 o提 t
作者简介: 林勇 ( 8 一)男 , 1 O , 山东济南人 , 9 济南市环境保 护监测站助工 。
・
3 ・ 9
维普资讯
物质 。
1天 然 源 .
芳 烃的致癌物 。有人做过 实验 , 经过烟 熏达 数周 之久 的羊 肉, 苯并 [] ( a) a芘 B p含量 达 2 ~4 ̄ k。 3 6 g ( ) 他人为源 4其 在垃圾深填埋处理 过程 中 , 产 生大 量垃圾 渗透液 , 会 经水 浸泡后 , 产生含 有大 量多环芳 烃 的有 机废水 ; 焚烧 垃 圾也 会产生多环芳烃 , 每小时处 理 9 t 0 的垃圾 焚烧炉 每天 排放的致癌性多环芳烃 总量可达 2 千 克。 0
nphth化学基团

nphth化学基团Nphth化学基团是一种重要的化学分子,它们是多环芳烃衍生物,在含氧类有机物中具有重要的神经毒性。
它们可分为芳香环、卤素、芳香环和高等无芳香环等不同的类型。
现在已知的Nphth物质在自然界中主要有以下三种:1-戊二烯卤素、2-戊二烯卤素以及5-苯基并三唑。
1-戊二烯卤素是一种含羟基的卤素,它的分子式为C5H6O2。
它是由一个氧原子代替芳香碳族原子,而三唑环仍然保留了它的原形,结构上与苯基并三唑完全一样。
它具有良好的抑菌和抗真菌活性,广泛用于药物植物保护和农家药物。
2-戊二烯卤素是一种双卤素,它的分子式为C6H8O2,包含三个羟基和一个卤素羟基。
它比1-戊二烯卤素具有更好的抗菌和抗真菌活性,在药物中也有重要的应用。
5-苯基并三唑是一种三唑式的多环芳香族碳氢化合物,它的分子式为C8H12N2O2。
它的结构与苯并三唑类似,它们的主要区别是在碳原子上有一个氧原子,使它们具有极强的抑菌和抗真菌活性。
它们也被广泛用于药物植物保护和农家药物中。
Nphth物质在医药行业具有重要的应用,它们可用于治疗很多疾病,如抗癌、抗真菌、耐药性等。
它们还可用于除草剂、农家药物以及其他行业。
由于其良好的抑菌抗真菌活性,这些物质成为研究微生物的重要工具。
此外,由于Nphth物质的多种性质,它们可应用于多种工业,如染料、油墨、涂料以及其他产品中。
它们能够改善这些产品的性能,而且它们具有良好的稳定性,可以抗温度和氧化性变化,因此在高温高压环境中也具有良好的热稳定性。
总之,Nphth化学基团是一类重要的有机物质,它们具有良好的抗菌、抗真菌和稳定性等特性,从而在医药行业和工业行业中具有广泛的应用价值。
随着研究的深入,Nphth物质在不同领域的应用前景还将持续改善。
多环芳烃(PAHs)在淡水水体中的迁移转化规律

多环芳烃(PAHs)在淡水水体中的迁移转化规律1 概述多环芳烃( Polycyclic Aromatic Hydrocarbons ,简称PAHs)是指两个或两个以上苯环连在一起的一类化合物,具有高脂溶性和相对低的水溶性,具有“致癌、致畸和致基因突变”(目前已发现的致癌性多环芳烃及其衍生物超过400 种)作用的持久性有机污染物( Persistent Organic Pollutant s ,POPs) 。
这一类物质由于高毒性、低流动性和难降解性使其在环境保护领域备受关注。
美国EPA优先控制名单中确定了16种PAHs作为优先控制污染物,我国也将7 种多环芳烃列入“中国环境优先控制污染物”黑名单。
PAHs由于化石燃料燃烧、机动车、垃圾焚烧、精炼油、焦炭和沥青生产以及铝的生产等人类活动而广泛分布于环境中。
多环芳烃在环境中大多数是以吸附态和乳化态形式存在,一旦进入环境,便受到各种自然界固有过程的影响,发生变迁。
通过复杂的物理迁移、化学及生物转化反应,在大气、水体、土壤、生物体等系统中不断变化,改变分布状况。
处在不同状态、不同系统中的多环芳烃则表现出不同的变化行为。
多环芳烃进入大气后,可通过化学反应、降尘、降雨、降雪等过程进入土壤及水体中。
人们可以通过呼吸、饮食等多种途径摄入,对人类健康产生极大危害,因此研究多环芳烃在环境中的行为具有十分重要的意义。
多环芳烃在环境中,特别是水环境中的迁移转化和归宿也得到广泛关注。
本文着重探讨河流、湖泊等淡水水体中多环芳烃的迁移转化研究成果,并指出存在问题和今后努力的方向。
2 PAHs在淡水水体中的迁移转化规律2.1 PAHs 在大气-水体间迁移转化PAHs 在大气-水体间迁移转化方式有:气态湿沉降、携带PAHs 的颗粒物湿沉降与干沉降、水-气界面PAHs 交换。
李军等利用双膜理论计算多环芳烃在麓湖水面上的交换通量,除萘、苊、二氢苊的通量方向是从湖水到大气外,其它多环芳烃都是从大气进入水体。
环氧树脂漆热分解产物

环氧树脂漆热分解产物
环氧树脂漆热分解产物主要包括碳酸酯、酯化产物、芳烃及其衍生物、芳香族醇、氨基末端产物、多环芳烃、环烃及其衍生物、羰基化合物及其
衍生物、醛类产物、羧酸类产物、烃类产物等。
碳酸酯是环氧树脂漆热分解最主要的产物,它是树脂漆热分解产物中
最常见、最多的,其形式多样,包括醋酸、醛酸、酯酸、醇酸、酒精酸等,占据环氧树脂漆热分解产物的大部分。
酯化产物是环氧树脂漆热分解的重要产物,一般为脂肪酯和烃基酯,
它们一般具有较低的挥发性。
芳烃及其衍生物是环氧树脂漆热分解的另一主要产物,它们的形式复杂,包括了烷烃、芳烃、醇酸酯、醛酸酯、酯化物、芳醛类和羧酸酯等。
芳香族醇是环氧树脂漆热分解产物中最常见的化合物,包括酚类、醇
酸酯类、醛酸酯类、醇醛类、酯类等。
氨基末端产物主要是氨基和磺酸根构成的有机化合物,具有较高的挥
发性,它们主要是环氧树脂漆由于受热时从芳烃单体中分解出来的。
多环芳烃是指含有多个环结构的芳烃,它们是环氧树脂漆热分解中比
较稀少的化合物,而且它们的形式复杂,常见形式有苯、芘、芪、环苯并
三环芳烃等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
成的化合物成为多代脂烃。
命名时将苯环作为取代基,按链烃命名。
C H
三苯甲烷 (triphenylmethane) 二苯甲烷 (diphenylmethane) 1,2-二苯乙烷 (1,2-diphenylethane)
C H H
CH2 CH2
19.2 联苯及其衍生物
一、联苯及其衍生物的制备
1. 苯高温裂化脱氢制备联苯
第十九章
多环芳烃及其衍生物
19.1 多环芳烃的分类与命名
分子中有多个苯环的烃,称为多环芳烃。
主耍分稠环芳烃、联环芳烃和多苯代脂烃
三大类。
一、稠环芳烃
IUPAC保留了常见稠环芳烃的俗名; CCS一般采用这些化合物英文的音译并 给于特定汉字; 其它自学。
菲 蒽 萘 (naphthylene) (anthracene) (phenanthrene)
Ph3CH NaNH2 / NH3(液) -33℃ Ph3C-Na+
2. 三苯甲基正离子的形成
(1)三苯甲醇的制备
Ph3CH
CrO3
Ph3C
OH
2 PhMgBr PhCOOEt ; Et2O
MH4Cl/H2O
Ph3C
OH
思考:再举一个合成三苯甲醇的制备方法
(2)三苯甲醇正离子的形成
三苯甲醇溶于浓硫酸,生成金黄色的溶液
Na / C2H5OH
碱
H2 / Ni 140~160℃,3atm
H2 / Ni 200℃,10~30atm H2 / Pt
十氢化萘的两种构象
反式构象比顺式稳定
三、萘的合成
• 萘的合成仅具有理论意义。但是,萘的关
环方法可用以合成萘的衍生物。
1. Haworth合成法
O +
O
HO O
O O
AlCl3
O
Zn/Hg, 盐酸
HO
O
H2SO4 或PPA
Pd或Se 蒸馏脱氢
Zn/Hg, 盐酸
2. Diels-Alder合成法
O + O O O
OH
H+
OH
O Na2Cr2O7 H2SO4
O HNO3 O
O
19.4 三苯甲烷及衍生物
一、制备方法
1. 三苯甲烷由氯仿和苯
3
+ CHCl3
AlCl3
Ph3CH
1 2 3
7 6 5 4
α: 1、4、5、8 — 电子云密度最高
β: 2、3、6、7 — 电子云密度次之 9、10 — 电子云密度最低
Cl
NO2
Cl
NO2
-氯萘
CH3
-氯萘
1,5-二硝基苯
SO3H
Cl
CH3
6-甲基-1-氯萘
5-甲基-2-萘磺酸
二、萘的性质
萘为白色晶体,熔点80.5℃,沸点
溶于甲醇、乙醇、醚和苯等有机溶剂。 苯是重要的化工、医药、塑料和染料原料。
可制备出如乳化剂、荧光增白剂、织物染
料、合成树脂、农药和医药等。
2. 化学性质 联苯是苯环上的一个氢原子被另一个苯 环所取代,故,每一个苯环与单独苯环 的化学性质是类似的。 苯基取代基是邻对位定位基。
2. 化学性质 联苯是苯环上的一个氢原子被另一个苯 环所取代,故,每一个苯环与单独苯环 的化学性质是类似的。 苯基取代基是邻对位定位基。
三苯甲基溴(或氯)在无氧条件下,与活泼
金属锌粉反应,生成稳定的三苯甲基自由基,
显黄色。
Zn / 苯 Ph3C Br 隔绝空气 Ph3C
.
三苯甲基自由基与空气接触,生成无色过
氧化物。
2 Ph3C
.
O2
Ph3C
O
O
CPH3
三苯甲基在无氧条件下,高浓度的三苯甲 基自由基二聚成白色固体。
Ph C Ph
(对)三联苯 (p-terphenyl)
NO2 Cl 3' 5 6 1 1' 2' 4' 4 3 2 6' 5' HOOC Cl
6-硝基-2',6'-二氯联苯-3-羧酸 (2',6'-dichloro-6-nitro-biphenyl--carboxylic acid)
三、多苯代脂烃
多个苯环通过一个或多个碳原子连接形
.
H
.
Ph C Ph + Ph3C
.
Ph C Ph
Ph3C H
218℃,有特殊气味,易升华。
大部分用来制造邻苯二甲酸酐。
萘具有255kJ/mol的共振能(离域能),
苯具有152 kJ/mol。
1. 亲电取代反应
Br Br2 CCl4 72~75%
NO2 混酸 30~60℃ 72~75%
H
60℃
SO3H
动力学控制
165℃
H
165℃
SO3H
热力学控制
萘环上的取代规律
NO2 NO2
13%
取代规律受反应条件影响很大,无规律性。
COCH3 OCH3
OCH3 CH3COCl AlCl3
CS2
PhNO2
OCH3
CH3CO
40℃
SO3H OH
SO3H
OH 浓硫酸 95℃
OH
>100℃
OH HO3S
2. 氧化反应
V2O5 + 9 O2 385℃
O O O
3. 还原反应
700~800℃ 2
+
H2
2. Ullmann反应
2 Cu I
溴苯或氯苯需要环上有吸电子基团
O2N 2 Cl NO2 Cu 215~225℃ NO2
3. 二苯基铜锂低温下氧化反应
2
CuBr Li THF
CuLi 2
O2 THF, -70℃
75%
4. 联苯胺重排反应
NO2 Cl Zn NaOH
Br2 / 50% CH3COOH
Br
CH3
HNO3 / (CH3CO)2O
NO2 CH3
O2N + CH3
Br
Br2
Br
Br
3. 联苯化合物的立体异构
19.3 稠环芳烃
萘的分子式C10H8,是最简单的稠环芳烃。
萘是煤焦油中含量最多的化合物,约6%。
一、萘的结构
8
芘 (pyrene)
苝 (perylene)
并四苯(naphthacene)
k m
并五苯(pentacene)
n a l j b i h f e d g c
二苯并[a,b]蒽或 1,2,5,6-二苯并蒽
二、联环芳烃
芳环与芳环通过单键直接相连形成的化合 物,为联环芳烃。
联苯 (biphenyl)
范围:亲电取代反应。
萘环上原有第一类取代基——主要发
生“同环反应”。 萘环上原有第二类取代基——主要发 生“异环取代”。
OCH3 混酸
OCH3 85% NO2
NO2 CH3
CH3
HNO3 CH3COOH,80℃
80%
SO3H 发烟硫酸
பைடு நூலகம்
SO3H
SO3H 70%
NO2 混酸
NO2 + NO2 45%
用水或乙醇再将此溶液稀释,金黄色消失。
浓H2SO4
Ph3C
OH
Ph3C+HSO4-
H2O
Ph3COH + H2SO4
Ph3COC2H5 + H2SO4
Ph3C+HSO4-
C2H5OH
3. 三苯甲基自由基的形成 三苯甲烷与卤素光催化下发生自由基卤代 反应。
Ph3C
H
Br2 hv
Ph3C
Br + HBr
2. 苯甲醛和苯或取代苯缩合反应
CHO + 2 ZnCl2 H2O Ph3CH
CHO +
CH3 2
CH3 N ZnCl2 H2O
CH3 CH3 N C H N
CH3 CH3
二、三苯甲烷及其衍生物的性质 1. 酸性——三苯甲基负离子 的形成
三苯甲烷与强碱如氨基钠作用,生成三苯 甲基钠,呈深红色。
Cl Cl
NH NH
H2SO4
Cl H2N
Cl NH2
4. 联苯胺重排反应
NO2 Cl Zn NaOH
Cl Cl
NH NH
H2SO4
Cl H2N
Cl NH2
二、联苯的性质
1. 物理性质与应用不溶
白色或微黄色鳞片状结晶,具有独特的香 味。熔点70℃,沸点255℃,闪点113℃, 密度0.992g/cm3。 几乎不溶于水,不溶于酸及碱,
