不同温度下的饱和蒸汽压
饱和蒸汽压的测定的实验报告

饱和蒸汽压的测定的实验报告实验名称:饱和蒸汽压的测定实验目的:测量不同温度下的饱和蒸汽压,探究其变化规律,了解水的蒸发过程。
实验原理:饱和蒸汽压是指液体蒸发到一定程度时,与外界保持动态平衡时的蒸汽压强度。
在一定温度下,液体与蒸汽之间的这种平衡成为饱和状态,此时液体内部还有未蒸发的分子,但是已经达到了与空气中水分子蒸发相等的蒸汽压强度。
饱和温度的升高会使液体内部更多分子脱离表面蒸发,从而使蒸汽压增大。
实验器材:烧杯、温度计、热水浴、挂钩、弹簧秤、水。
实验步骤:1、将烧杯中加满水后用挂钩扣到弹簧秤上,测量其质量并记录下来。
2、在热水浴中加热烧杯,记下开始加热时的温度,并持续加热直到水沸腾,此时温度保持不变,可用温度计测量并记录下来。
3、记下水沸腾时的弹簧秤读数,用其减去起始重量,即得水的蒸发量。
4、重复实验步骤1-3并记录不同温度下水的蒸发量和弹簧秤读数。
5、利用实验得到的数据,根据公式P = PP/P计算出不同温度下的饱和蒸汽压。
实验数据记录:温度/℃质量/g 弹簧秤读数/N 蒸发量/g 饱和蒸汽压/Pa20 100.2 0.22 0 030 100.2 0.26 0.7 105440 100.2 0.30 1.3 194650 100.2 0.33 2.1 313860 100.2 0.38 3.1 4641实验结果分析:根据实验结果,可得到以下结论:1、随着温度的升高,饱和蒸汽压不断增大,增长速度逐渐加快。
2、在30-60℃范围内,每10℃饱和蒸汽压的增长约为1000 Pa。
3、实验数据与理论曲线存在小差距,可归因于实际操作中可能存在的误差差异。
实验结论:本实验通过测量不同温度下水的蒸发量和弹簧秤读数,计算出了不同温度下水的饱和蒸汽压。
实验结果表明,随着温度的升高,饱和蒸汽压呈现增长趋势,增长速度逐渐加快。
同时,实验数据还与理论曲线存在差距,可对实际误差进行进一步研究。
水在不同温度下的饱和蒸气压

水在不同温度下的饱和蒸气压Document number:WTWYT-WYWY-BTGTT-YTTYU-2018GT饱和蒸(saturatedvaporpressure)在密闭条件中,在一定下,与或处于相的蒸气所具有的称为饱和蒸气压。
同一在不同温度下有不同的蒸气压,并随着温度的升高而增大。
不同液体饱和蒸汽压不同,溶剂的饱和蒸汽压大于溶液的饱和蒸汽压;对于同一物质,固态的饱和蒸汽压小于液态的饱和蒸汽压。
例如,在30℃时,水的饱和蒸气压为,为。
而在100℃时,水的饱和蒸气压增大到,乙醇为。
饱和蒸气压是液体的一项重要,如液体的、液体的相对挥发度等都与之有关。
饱和蒸气压水在不同温度下的饱和蒸气压SaturatedWaterVaporPressuresatDifferentTemperatures饱和蒸汽压公式(1)Clausius-Claperon方程:dlnp/d(1/T)=-H(v)/(R*Z(v))式中p为蒸汽压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。
该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。
(2)Clapeyron方程:若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron方程:lnp=A-B/T式中B=H(v)/(R*Z(v))。
(3)Antoine方程:lnp=A-B/(T+C)式中,A,B,C为Antoine常数,可查数据表。
Antoine方程是对Clausius-Clapeyron方程最简单的改进,在~范围内误差小。
附录在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。
其公式如下lgP=A-B/(t+C)(1)式中:P—物质的蒸气压,毫米汞柱;t—温度,℃公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2)公式进行计算lgP=T+C(2)式中:P—物质的蒸气压,毫米汞柱;表1不同物质的蒸气压名称分子式范围(℃)ABC银Ag1650~1950公式(2)氯化银AgCl1255~1442公式(2)三氯化铝AlCl370~190公式(2)氧化铝Al2O31840~2200公式(2)砷As440~815公式(2)砷As800~860公式(2)三氧化二砷As2O3100~310公式(2)三氧化二砷As2O3315~490公式(2)氩~公式(2)金Au2315~2500公式(2)三氯化硼BCl3……6..钡Ba930~1130公式(2)铋Bi1210~1420公式(2)溴Br2……6..碳C3880~4430公式(2)二氧化碳CO2……二硫化碳CS2-10~+一氧化碳CO-210~-1606..四氯化碳CCl4……钙Ca500~700公式(2)钙960~1100公式(2)镉Cd150~公式(2)镉500~840公式(2)氯Cl2……6..107240二氧化氯ClO2-59~+11公式(2)钴Co2374公式(2)铯Cs200~230公式(2)铜Cu2100~2310公式(2)氯化亚铜Cu2Cl2878~1369公式(2)铁Fe2220~2450公式(2)氯化亚铁FeCl2700~930公式(2)氢~氟化氢HF-55~+氯化氢HCl-127~溴化氢HBr-120~-87①8..4270溴化氢-120~-606..68250碘化氢HI-97~-51公式(2)碘化氢-50~-34公式(2)氰化氢HCN-85~氰化氢-40~+过氧化氢H2O210~90公式(2)水②H2O0~水③60~硒化氢H2Se66~-26公式(2)硫化氢H2S-110~83公式(2)碲化氢H2Te-46~0公式(2)氦He……汞Hg100~汞200~3007..汞300~汞400~8007..氯化汞HgCl260~130公式(2)氯化汞130~270公式(2)氯化汞HgCl2275~309公式(2)氯化亚汞Hg2Cl2…碘I2…钾K260~760公式(2)氟化钾KF1278~1500公式(2)氯化钾KCl690~1105公式(2)氯化钾1116~1418公式(2)溴化钾KBr906~1063公式(2)溴化钾1095~1375公式(2)碘化钾KI843~1028公式(2)碘化钾1063~1333公式(2)氢氧化钾KOH1170~1327公式(2)氪~-169公式(2)氟化锂LiF1398~1666公式(2)镁Mg900~1070公式(2)锰Mn1510~1900公式(2)钼Mo1800~2240公式(2)氮N2-210~-1806..一氧化氮NO-200~161公式(2)一氧化氮~148公式(2)三氧化二氮N2O3-25~0公式(2)四氧化二氮N2O4-100~-40公式(2)四氧化二氮-40~-10公式(2)五氧化二氮N2O5-30~+30公式(2)氯化亚硝酰~公式(2)肼N2H4-10~+肼39~钠Na180~883公式(2)氯化钠NaF1562~1701公式(2)氯化钠NaCl976~1155公式(2)氯化钠1562~1430公式(2)溴化钠NaBr1138~1394公式(2)碘化钠NaI1063~1307公式(2)氰化钠NaCN800~1360公式(2)氢氧化钠NaOH1010~1402公式(2)氖Ne……7..镍Ni2360公式(2)四羰基镍Ni(CO)42~40公式(2)氧O2-210~-1606..臭氧O3……6..磷(白磷)P20~公式(2)磷(紫磷)P380~590公式(2)磷化氢PH3……6..铅Pb525~1325公式(2)氯化铅PbCl2500~950公式(2)铂Pt1425~1765公式(2)铷Rb250~370公式(2)氡Rn……硫S……二氧化硫SO2……三氧化硫SO324~48公式(2)锑Sb1070~1325公式(2)三氯化锑SbCl3170~253公式(2)硒Se……二氧化硒SeO2……硅Si1200~1320公式(2)四氯化硅SiCl4-70~+5公式(2)甲硅烷SiH4-160~112公式(2)二氧化硅SiO21860~2230公式(2)锡Sn1950~2270公式(2)四氯化锡SnCl4-52~-38公式(2)锶Sr940~1140公式(2)铊Tl950~1200公式(2)钨W2230~2770公式(2)氙Ke……锌Zn250~公式(2)甲烷XH4固体③7..甲烷液体6..氯甲烷CH3Cl-47~-10公式(2)三氯甲烷CHCl3-30~+二苯基甲烷C13H12217~283公式(2)氯溴甲烷CH2ClBr-10~+硝基甲烷CH3O2N47~100公式(2)乙烷C2HS……6..氯乙烷C2H5Cl65~+706..62230溴乙烷C2H5Br-50~+均二氯乙烷C2H4Cl2……均二溴乙烷C2H4Br2……环氧乙烷C2H4O-70~+偏二氯乙烷C2H2Cl20~30公式(2)1,1,2一三氯乙烷C2H3Cl3……丙烷C3H8……6..正氯丙烷C3H7Cl0~50公式(2)环氧丙烷(1,2)C3H6O-35~+正丁烷C4H10……6..异丁烷C4H10……6..正戊烷C5H12……异戊烷C5H12……环戊烷C5H10……正己烷C6H14……环已烷④C6H12-50~正庚烷C7H16……正辛烷C8H18-20~+正辛烷20~异辛烷(2-甲基庚烷)C8H18……正壬烷C9H20-10~+正壬烷60~正癸烷C10H2210~正癸烷70~正十一烷C11H2415~1007..正十一烷100~正十二烷C12H265~正十二烷115~正十三烷C13H2815~1327..正十三烷132~3306..正十四烷C14H3015~1457..正十四烷145~3406..正十五烷C15H3215~1607..正十五烷160~正十六烷C16H34……正十七烷C17H3620~1907..正十七烷190~正十八烷C18H3820~2007..正十八烷200~正十九烷C19H4020~408..正十九烷160~正二十烷C20H4225~2238..正二十烷223~乙烯C2H4……6..氯乙烯C2H3Cl-11~+506..1,1,2一三氯乙烯C2HCl3……苯乙烯C8H8……丙烯C3H6……6..丁稀-1C4H8……6..顺-2-丁烯C4H8……6..反-2-丁稀C4H8……6..2-甲基丙烯-1C4H8……6..1,2一丁二烯C4H6-60~+807..1,3一丁二烯C4H6-80~+656..2-甲基丁二稀-1,3C5H8-50~+乙炔C2H2-140~-82公式(2)甲醇CH4O-20~+苯甲醇C7H8O20~苯甲醇113~乙醇C2H6O……正丙醇C3H8O……异丙醇C3H8O0~1136..正丁醇C4H1075~公式(2)特丁醇C4H10……乙二醇C2H6O225~1128..乙二醇112~3407..乙醛C2H4O-75~-457..8250乙醛-45~+706..0230丙酮C3H6O……二乙基酮C5H10O……甲乙酮C4H3O……甲酸CH2O2……苯甲酸C7H6O260~110公式(2)乙酸C2H4O20~乙酸36~丙酸C3H6O20~丙酸60~正丁酸C4H8O20~正丁酸82~月硅酸C12H24O2164~205公式(2)十四烷酸C14H28O2190~224公式(2)乙酐C4H6O3100~140公式(2)顺丁烯二酸酐C4H2O360~160公式(2)邻苯二甲酸酐C3H4O3160~285公式(2)酷酸乙醋C4H8O2-20~+甲酸乙酯C3H6O2-30~+醋酸甲酯C3H6O2……苯甲酸甲酯C8H8O225~1007..苯甲酸甲酯100~甲酸甲酯C2H4O2……水杨酸甲酯C8H8O3175~215公式(2)氨基甲酸乙酯C3H7O2N……甲醚C2H6O……6..苯甲醚C7H8O……二苯醚C12H10O25~147⑤7..二苯醚147~甲乙醚C3H8O0~25公式(2)乙醚C4H10O……6..甲胺CH5N-93~-456..甲胺-45~+506..二甲胺C2H7N-80~二甲胺-30~+三甲胺C3H9N-90~三甲胺-60~+8506..乙胺C2H7N-70~乙胺-20~+二乙胺C4H11N-30~+三乙胺C6H15N0~1306..苯胺C6H7N……二甲替甲酰胺C3H7ON15~607..二甲替酰胺60~二苯胺C12H11N278~284公式(2)间硝基苯胺C6H6O2N2190~260公式(2)邻硝基苯胺C6H5O2N2150~260公式(2)对硝基苯胺C6H6O2N2190~260公式(2)苯酚C6H6O……邻甲酚C7H8O……间甲酚C7H8O……对甲酚C7H8O……α-萘酚C10H8O……β-萘酚C10H8O……苯⑥C6H6……氯苯C6H5Cl0~氯苯42~邻二氯苯C6H4Cl2……乙苯C8H10……氟苯C6H5F-40~+硝基苯C6H6O2N112~209公式(2)甲苯C7H8……邻硝基甲苯C7H7O2N50~225公式(2)间硝基甲苯C7H7O2N55~235公式(2)对硝基甲苯C7H7O2N80~240公式(2)三硝基甲苯C7H5O6N3……3..406160邻二甲苯C8H10……间二甲苯对二甲苯乙酰苯C8H8O30~100公式(2)乙腈C2H3N……丙烯腈C3H3N-20~+氰C2N2-72~-28公式(2)氰C2N2-36~-6公式(2)萘C10H8……α-甲基綦C11H10……β-甲基萘C11H10……蓖C14H10100~160公式(2)蓖223~342公式(2)蓖醌C14H3O2224~286公式(2)蓖醌285~370公式(2)樟脑C10H16O0~18公式(2)咔唑C12H9N244~352公式(2)芴C13H10161~300公式(2)呋喃C4H4O-35~+吗啉C4H9ON0~吗啉44~菲C14H10203~347公式(2)喹啉C9H7N180~240公式(2)噻吩C4H4S-10~草酸C2H2O455~105公式(2)光气COCl2-68~+686..25230氨⑥NH3-83~+氯化铵NH4Cl100~400公式(2)氰化铵NH4CN7~17公式(2)开放分类:。
水饱和蒸汽压曲线
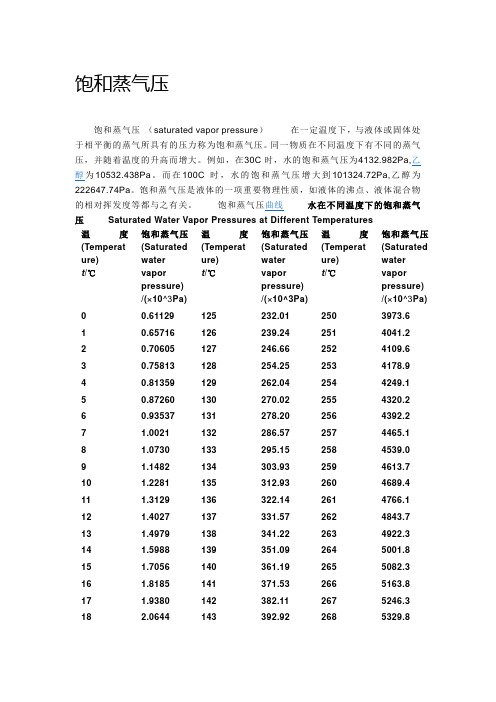
饱和蒸气压饱和蒸气压(saturated vapor pressure)在一定温度下,与液体或固体处于相平衡的蒸气所具有的压力称为饱和蒸气压。
同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。
例如,在30C时,水的饱和蒸气压为4132.982Pa,乙醇为10532.438Pa。
而在100C时,水的饱和蒸气压增大到101324.72Pa,乙醇为222647.74Pa。
饱和蒸气压是液体的一项重要物理性质,如液体的沸点、液体混合物的相对挥发度等都与之有关。
饱和蒸气压曲线水在不同温度下的饱和蒸气压Saturated Water Vapor Pressures at Different Temperatures温度(Temperat ure)t/℃饱和蒸气压(Saturatedwatervaporpressure)/(×10^3Pa)温度(Temperature)t/℃饱和蒸气压(Saturatedwatervaporpressure)/(×10^3Pa)温度(Temperature)t/℃饱和蒸气压(Saturatedwatervaporpressure)/(×10^3Pa)00.61129125232.012503973.6 10.65716126239.242514041.2 20.70605127246.662524109.6 30.75813128254.252534178.9 40.81359129262.042544249.1 50.87260130270.022554320.2 60.93537131278.202564392.27 1.0021132286.572574465.18 1.0730133295.152584539.09 1.1482134303.932594613.710 1.2281135312.932604689.411 1.3129136322.142614766.112 1.4027137331.572624843.713 1.4979138341.222634922.314 1.5988139351.092645001.815 1.7056140361.192655082.316 1.8185141371.532665163.817 1.9380142382.112675246.318 2.0644143392.922685329.819 2.1978144403.982695414.320 2.3388145415.292705499.921 2.4877146426.852715586.422 2.6447147438.672725674.023 2.8104148450.752735762.724 2.9850149463.102745852.425 3.1690150475.722755943.126 3.3629151488.612766035.027 3.5670152501.782776127.928 3.7818153515.232786221.929 4.0078154528.962796317.230 4.2455155542.992806413.231 4.4953156557.322816510.532 4.7578157571.942826608.933 5.0335158586.872836708.534 5.3229159602.112846809.235 5.6267160617.662856911.136 5.9453161633.532867014.137 6.2795162649.732877118.338 6.6298163666.252887223.739 6.9969164683.102897330.2 407.3814165700.292907438.0 417.7840166717.832917547.0 428.2054167735.702927657.2 438.6463168753.942937768.6 449.1075169772.522947881.3 459.5898170791.472957995.2 4610.094171810.782968110.3 4710.620172830.472978226.8 4811.171173850.532988344.5 4911.745174870.982998463.5 5012.344175891.803008583.8 5112.970176913.033018705.4 5213.623177934.643028828.35314.303178956.663038952.6 5415.012179979.093049078.2 5515.7521801001.93059205.1 5616.5221811025.23069333.4 5717.3241821048.93079463.1 5818.1591831073.03089594.2 5919.028*******.53099726.7 6019.9321851122.53109860.5 6120.8731861147.93119995.8 6221.8511871173.831210133 6322.8681881200.131310271 6423.9251891226.131410410 6525.022*******.231510551 6626.1631911281.931610694 6727.3471921310.131710838 6828.5761931338.831810984 6929.852*******.031911131 7031.1761951397.632011279 7132.5491961427.832111429 7233.9721971458.532211581 7335.4481981489.732311734 7436.9781991521.432411889 7538.5632001553.632512046 7640.2052011568.432612204 7741.9052021619.732712364 7843.6652031653.632812525 7945.4872041688.032912688 8047.3732051722.933012852 8149.3242061758.433113019 8251.3422071794.533213187 8353.4282081831.133313357 8455.5852091868.433413528 8557.8152101906.233513701 8660.1192111944.6336138768762.4992121983.633714053 8864.9582132023.233814232 8967.4962142063.433914412 9070.1172152104.234014594 9172.8232162145.734114778 9275.6142172187.834214964 9378.4942182230.534315152 9481.4652192273.834415342 9584.5292202317.834515533 9687.6882212362.534615727 9790.9452222407.834715922 9894.3012232453.834816120 9997.7592242500.534916320 100101.322252547.935016521 101104.992262595.935116825 102108.772272644.635216932 103112.662282694.135317138 104116.672292744.235417348 105120.792302795.135517561 106125.032312846.735617775 107129.392322899.035717992 108133.882332952.135818211 109138.502343005.935918432 110143.242353060.436018655 111148.122363115.736118881 112153.132373171.836219110 113158.292383288.636319340 114163.582393286.336419574 115169.022403344.736519809 116174.612413403.936620048 117180.342423463.936720289 118186.232433524.736820533 119192.282443586.336920780 120198.482453648.837021030121204.852463712.137121286 122211.382473776.237221539 123218.092483841.237321803 124224.962493907.0--。
不同温度下多聚甲醛的饱和蒸汽压

不同温度下多聚甲醛的饱和蒸汽压多聚甲醛是一种重要的化学物质,常被用作涂料、树脂等材料的原料。
在不同的温度下,多聚甲醛的饱和蒸汽压也会发生变化。
本文将详细介绍不同温度下多聚甲醛的饱和蒸汽压,并对其影响因素进行探讨。
多聚甲醛在不同温度下的饱和蒸汽压是指在一定温度下,多聚甲醛蒸气与其液态形成的动态平衡时,此时多聚甲醛的蒸汽压。
饱和蒸汽压是一个重要的物理化学性质,可以用来描述物质在不同温度下的挥发性。
多聚甲醛的饱和蒸汽压随温度的升高而增大,呈现出典型的温度-压强曲线。
多聚甲醛在常温下为固态,需要一定温度才能转化为液态、气态。
通过实验测得,20℃下多聚甲醛的饱和蒸汽压约为0.143kPa,温度升高到40℃时,饱和蒸汽压增加到0.569kPa。
随着温度的不断升高,多聚甲醛的饱和蒸汽压也随之增大。
这种温度-压强关系符合克劳修斯-克拉佩龙方程,即lnP=A-B/T,其中P为饱和蒸汽压,A和B为常数,T为温度。
这个方程表明,多聚甲醛的饱和蒸汽压与温度呈指数关系。
多聚甲醛的饱和蒸汽压受多种因素影响,其中温度是最主要的影响因素。
温度升高会增加多聚甲醛分子的平均动能,从而增大其蒸汽压。
此外,多聚甲醛的分子结构、纯度等因素也会对其饱和蒸汽压产生影响。
例如,分子结构的不同可能导致分子间相互作用的差异,进而影响其蒸汽压的大小。
另外,环境压力也会对多聚甲醛的饱和蒸汽压产生一定的影响。
在封闭的环境中,环境压力会影响多聚甲醛蒸气与液态的平衡,从而影响其饱和蒸汽压的测定。
一般来说,环境压力的增大会促进多聚甲醛的液态向蒸气的转化,从而增大其饱和蒸汽压。
而在开放的环境中,环境压力对多聚甲醛的饱和蒸汽压影响较小。
多聚甲醛的饱和蒸汽压的测定对于相关工程和生产过程具有重要意义。
在实际工程中,了解多聚甲醛在不同温度下的饱和蒸汽压能够帮助工程师合理选择材料、设计设备,并有效控制生产过程中的挥发性有机化合物的排放。
同时,多聚甲醛的饱和蒸汽压也是评估其毒性和危险性的重要参考指标。
饱和蒸汽压力与温度对照表

饱和蒸汽压力与温度对照表
按1MPa=1000kPa=10.2kgf/cm2(公斤/平方厘米),对照饱和蒸汽压力(MPa表示)与蒸汽温度的标准表,可以计算得到饱和蒸汽压力(kgf/cm2表示)与蒸汽温度之间的关系,如下所示:
饱和蒸汽的温度与压力之间一一对应,二者之间只有一个独立变量。
理想的饱和蒸汽状态,指的是温度、压力及蒸汽密度三者存在一一对应的关系,知道其中一个,其他二个值就是定数。
存在这种关系的蒸汽就是饱和蒸汽,并存在饱和蒸汽压力与温度对照表。
标准的饱和蒸汽压力与蒸汽温度对照表是根据国际单位制进行编制的,即压力单位为MPa,温度单位为℃。
扩展资料
饱和蒸汽压的测量方法可以分为两类:
1.动态法。
指在不同外界压力下,测定液体的沸点,又称沸点法。
这种方法只在测量常压附近的饱和蒸汽压时测量精度较好。
2.静态法。
指在不同温度下,直接测量液体饱和蒸汽压,即在恒温条件下测量饱和压力。
静态法测量相对简单,更具普遍性,通常的做法就是将待测物质充人密闭容器,并使其处于气液两相共存状态,然后放人恒温槽中,通过调节恒温槽温度来测量不同温度下的饱和蒸汽压数据。
水在不同温度下的饱和蒸汽压
305
9205.1
56
16.522
181
1025.2
306
9333.4
57
17.324
182
1048.9
307
9463.1
58
18.159
183
1073.0
308
9594.2
59
19.028
184
1097.5
309
9726.7
60
19.932
185
1122.5
310
9860.5
61
20.873
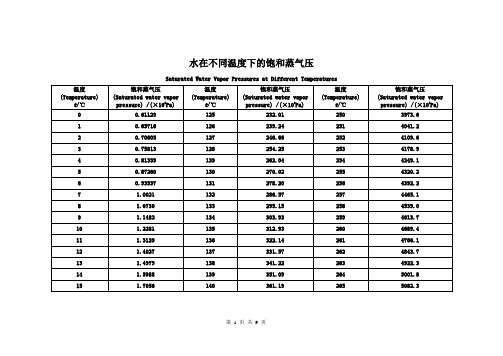
温度(Temperature)
t/℃
饱和蒸气压
(Saturated water vapor pressure) /(×103Pa)
温度(Temperature)
t/℃
饱和蒸气压
(Saturated water vapor pressure) /(×103Pa)
温度(Temperature)
t/℃
饱和蒸气压
18881
112
153.13
237
3171.8
362
19110
113
158.29
238
3288.6
363
19340
114
163.58
239
3286.3
364
19574
115
169.02
240
3344.7
365
19809
116
174.61
241
3403.9
366
20048
117
180.34
242
3463.9
239.24
水在不同温度下的饱和蒸气压
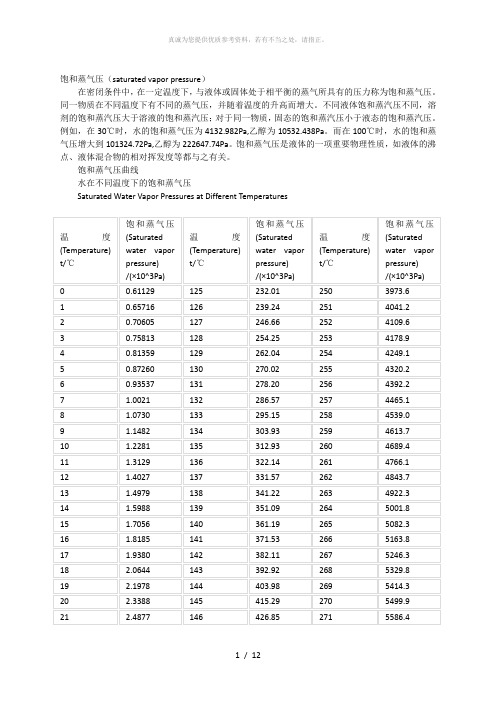
饱和蒸气压(saturated vapor pressure)在密闭条件中,在一定温度下,与液体或固体处于相平衡的蒸气所具有的压力称为饱和蒸气压。
同一物质在不同温度下有不同的蒸气压,并随着温度的升高而增大。
不同液体饱和蒸汽压不同,溶剂的饱和蒸汽压大于溶液的饱和蒸汽压;对于同一物质,固态的饱和蒸汽压小于液态的饱和蒸汽压。
例如,在30℃时,水的饱和蒸气压为4132.982Pa,乙醇为10532.438Pa。
而在100℃时,水的饱和蒸气压增大到101324.72Pa,乙醇为222647.74Pa。
饱和蒸气压是液体的一项重要物理性质,如液体的沸点、液体混合物的相对挥发度等都与之有关。
饱和蒸气压曲线水在不同温度下的饱和蒸气压Saturated Water Vapor Pressures at Different Temperatures编辑本段饱和蒸汽压公式(1)Clausius-Claperon方程:d lnp/d(1/T)=-H(v)/(R*Z(v))式中p为蒸汽压;H(v)为蒸发潜热;Z(v)为饱和蒸汽压缩因子与饱和液体压缩因子之差。
该方程是一个十分重要的方程,大部分蒸汽压方程是从此式积分得出的。
(2)Clapeyron 方程:若上式中H(v)/(R*Z(v))为与温度无关的常数,积分式,并令积分常数为A,则得Clapeyron方程:ln p=A-B/T式中B=H(v)/(R*Z(v))。
(3)Antoine方程:ln p=A-B/(T+C)式中,A,B,C为Antoine常数,可查数据表。
Antoine方程是对Clausius-Clapeyron方程最简单的改进,在1.333~199.98kPa范围内误差小。
编辑本段附录在表1中给出了采用Antoine公式计算不同物质在不同温度下蒸气压的常数A、B、C。
其公式如下lgP=A-B/(t+C)(1)式中:P—物质的蒸气压,毫米汞柱;t—温度,℃公式(1)适用于大多数化合物;而对于另外一些只需常数B与C值的物质,则可采用(2)公式进行计算lgP=-52.23B/T+C (2)式中:P—物质的蒸气压,毫米汞柱;表1 不同物质的蒸气压名称分子式范围(℃) A B C银Ag 1650~1950 公式(2)250 8.76氯化银AgCl 1255~1442 公式(2)185.5 8.179三氯化铝AlCl3 70~190 公式(2)115 16.24氧化铝Al2O3 1840~2200 公式(2)540 14.22砷As 440~815 公式(2)133 10.800砷As 800~860 公式(2)47.1 6.692三氧化二砷As2O3 100~310 公式(2)111.35 12.127三氧化二砷As2O3 315~490 公式(2)52.12 6.513氩Ar -207.62~-189.19 公式(2)7.8145 7.5741金Au 2315~2500 公式(2)385 9.853三氯化硼BCl3 …… 6.18811 756.89 214.0钡Ba 930~1130 公式(2)350 15.765铋Bi 1210~1420 公式(2)200 8.876溴Br2 …… 6.83298 113.0 228.0碳C 3880~4430 公式(2)540 9.596二氧化碳CO2 …… 9.64177 1284.07 268.432二硫化碳CS2 -10~+160 6.85145 1122.50 236.46一氧化碳CO -210~-160 6.24020 230.274 260.0四氯化碳CCl4 …… 6.93390 1242.43 230.0钙Ca 500~700 公式(2)195 9.697钙960~1100 公式(2)370 16.240镉Cd 150~320.9 公式(2)109 8.564镉500~840 公式(2)99.9 7.897氯Cl2 …… 6.86773 821.107 240二氧化氯ClO2 -59~+11 公式(2)27.26 7.893钴Co 2374 公式(2)309 7.571铯Cs 200~230 公式(2)73.4 6.949铜Cu 2100~2310 公式(2)468 12.344氯化亚铜Cu2Cl2 878~1369 公式(2)80.70 5.454 铁Fe 2220~2450 公式(2)309 7.482氯化亚铁FeCl2 700~930 公式(2)135.2 8.33氢H2 -259.2~-248 5.92088 71.615 276.337氟化氢HF -55~+105 8.38036 1952.55 335.52氯化氢HCl -127~-60 7.06145 710.584 255.0溴化氢HBr -120~-87① 8.4622 1112.4 270溴化氢-120~-60 6.88059 732.68 250碘化氢HI -97~-51 公式(2)24.16 8.259碘化氢-50~-34 公式(2)21.58 7.630氰化氢HCN -85~-40 7.80196 1425.0 265.0氰化氢-40~+70 7.29761 1206.79 247.532过氧化氢H2O2 10~90 公式(2)48.53 8.853水② H2O 0~60 8.10765 1750.286 235.0水③ 60~150 7.96681 1668.21 228.0硒化氢H2Se 66~-26 公式(2)20.21 7.431硫化氢H2S -110~83 公式(2)20.69 7.880碲化氢H2Te -46~0 公式(2)22.76 7.260氦He …… 16.1313 282.126 290汞Hg 100~200 7.46905 1771.898 244.831汞200~300 7.7324 3003.68 262.482汞300~400 7.69059 2958.841 258.460汞400~800 7.7531 3068.195 273.438氯化汞HgCl2 60~130 公式(2)85.03 10.888氯化汞130~270 公式(2)78.85 10.094氯化汞HgCl2 275~309 公式(2)61.02 8.409氯化亚汞Hg2Cl2 … 8.52151 3110.96 168.0碘I2 … 7.26304 1697.87 204.0钾K 260~760 公式(2)84.9 7.183氟化钾KF 1278~1500 公式(2)207.5 9.000氯化钾KCl 690~1105 公式(2)174.5 8.3526氯化钾1116~1418 公式(2)169.7 8.130溴化钾KBr 906~1063 公式(2)168.1 8.2470溴化钾1095~1375 公式(2)163.8 7.936碘化钾KI 843~1028 公式(2)157.6 8.0957碘化钾1063~1333 公式(2)155.7 7.949氢氧化钾KOH 1170~1327 公式(2)136 7.330氪Kr -188.7~-169 公式(2)10.065 7.1770氟化锂LiF 1398~1666 公式(2)218.4 8.753镁Mg 900~1070 公式(2)260 12.993锰Mn 1510~1900 公式(2)267 9.300钼Mo 1800~2240 公式(2)680 10.844氮N2 -210~-180 6.86606 308.365 273.2一氧化氮NO -200~161 公式(2)16.423 10.084 一氧化氮-163.7~148 公式(2)13.04 8.440三氧化二氮N2O3 -25~0 公式(2)39.4 10.30四氧化二氮N2O4 -100~-40 公式(2)55.16 13.40 四氧化二氮-40~-10 公式(2)45.44 11.214五氧化二氮N2O5 -30~+30 公式(2)57.18 12.647 氯化亚硝酰NOCl -61.5~-5.4 公式(2)25.5 7.870 肼N2H4 -10~+39 8.26230 1881.6 238.0肼39~250 7.77306 1620.0 218.0钠Na 180~883 公式(2)103.3 7.553氯化钠NaF 1562~1701 公式(2)218.2 8.640氯化钠NaCl 976~1155 公式(2)180.3 8.3297氯化钠1562~1430 公式(2)185.8 8.548溴化钠NaBr 1138~1394 公式(2)161.6 4.948碘化钠NaI 1063~1307 公式(2)165.1 8.371氰化钠NaCN 800~1360 公式(2)155.52 7.472氢氧化钠NaOH 1010~1402 公式(2)132 7.030 氖Ne …… 7.57352 183.34 285.0镍Ni 2360 公式(2)309 7.600四羰基镍Ni(CO) 4 2~40 公式(2)29.8 7.780氧O2 -210~-160 6.98983 370.757 273.2臭氧O3 …… 6.72602 566.95 260.0磷(白磷) P 20~44.1 公式(2)63.123 9.6511磷(紫磷) P 380~590 公式(2)108.51 11.0842磷化氢PH3 …… 6.70101 643.72 256.0铅Pb 525~1325 公式(2)188.5 7.827氯化铅PbCl2 500~950 公式(2)141.9 8.961铂Pt 1425~1765 公式(2)486 7.786铷Rb 250~370 公式(2)76 6.976氡Rn …… 6.6964 717.986 250硫S …… 6.69535 2285.37 155.0二氧化硫SO2 …… 7.32776 1022.80 240.0三氧化硫SO3 24~48 公式(2)43.45 10.022锑Sb 1070~1325 公式(2)189 9.051三氯化锑SbCl3 170~253 公式(2)49.44 8.090硒Se …… 6.96158 3256.55 110.0二氧化硒SeO2 …… 6.57781 1879.81 179.0硅Si 1200~1320 公式(2)170 5.950四氯化硅SiCl4 -70~+5 公式(2)30.1 7.644甲硅烷SiH4 -160~112 公式(2)12.69 6.996二氧化硅SiO2 1860~2230 公式(2)506 13.43锡Sn 1950~2270 公式(2)328 9.643四氯化锡SnCl4 -52~-38 公式(2)46.74 9.824锶Sr 940~1140 公式(2)360 16.056铊Tl 950~1200 公式(2)120 6.140钨W 2230~2770 公式(2)897 9.920氙Ke …… 6.6788 573.480 260锌Zn 250~419.4 公式(2)133 9.200甲烷XH4 固体③ 7.69540 532.20 275.00甲烷液体6.61184 339.93 266.00氯甲烷CH3Cl -47~-10 公式(2)21.988 7.481三氯甲烷CHCl3 -30~+150 6.90328 1163.03 227.4二苯基甲烷C13H12 217~283 公式(2)52.36 7.967氯溴甲烷CH2ClBr -10~+155 6.92776 1165.59 220.0硝基甲烷CH3O2N 47~100 公式(2)39.914 8.033乙烷C2HS …… 6.80266 656.40 256.00氯乙烷C2H5Cl 65~+70 6.80270 949.62 230溴乙烷C2H5Br -50~+130 6.89285 1083.8 231.7均二氯乙烷C2H4Cl2 …… 7.18431 1358.46 232.2均二溴乙烷C2H4Br2 …… 7.06245 1469.70 220.1环氧乙烷C2H4O -70~+100 7.40783 1181.31 250.60偏二氯乙烷C2H2Cl2 0~30 公式(2)31.706 7.9091,1,2一三氯乙烷C2H3Cl3 …… 6.85189 1262.57 205.17丙烷C3H8 …… 6.82973 813.20 248.00正氯丙烷C3H7Cl 0~50 公式(2)28.894 7.593环氧丙烷(1,2)C3H6O -35~+130 7.06492 1113.6 232正丁烷C4H10 …… 6.83029 945.90 240.00异丁烷C4H10 …… 6.74808 882.80 240.00正戊烷C5H12 …… 6.85221 1064.63 232.000异戊烷C5H12 …… 6.78967 1020.012 233.097环戊烷C5H10 …… 6.88676 1124.162 231.361正己烷C6H14 …… 6.87776 1171.530 224.366环已烷④ C6H12 -50~200 6.84498 1203.526 222.863正庚烷C7H16 …… 6.90240 1268.115 216.900正辛烷C8H18 -20~+40 7.37200 1587.81 230.07正辛烷20~200 6.92374 1355.126 209.517异辛烷(2-甲基庚烷)C8H18 …… 6.91735 1337.468 213.963正壬烷C9H20 -10~+60 7.26430 1607.12 217.54正壬烷60~230 6.93513 1428.811 201.619正癸烷C10H22 10~80 7.31509 1705.60 212.59正癸烷70~260 6.95367 1501.268 194.480正十一烷C11H24 15~100 7.3685 1803.90 208.32正十一烷100~310 6.97674 1566.65 187.48正十二烷C12H26 5~120 7.35518 1867.55 202.59正十二烷115~320 6.98059 1625.928 180.311正十三烷C13H28 15~132 7.5360 2016.19 203.02正十三烷132~330 6.9887 1677.43 172.90正十四烷C14H30 15~145 7.6133 2133.75 200.8正十四烷145~340 6.9957 1725.46 165.75正十五烷C15H32 15~160 7.6991 2242.42 198.72正十五烷160~350 7.0017 1768.42 158.49正十六烷C16H34 …… 7.03044 1831.317 154.528正十七烷C17H36 20~190 7.8369 2440.20 194.59正十七烷190~320 7.0115 1847.12 145.52正十八烷C18H38 20~200 7.9117 2542.00 193.4正十八烷200~350 7.0156 1883.73 139.46正十九烷C19H40 20~40 8.7262 3041.10 207.30正十九烷160~410 7.0192 1916.96 131.66正二十烷C20H42 25~223 8.7603 3113.0 204.07正二十烷223~420 7.0225 1948.7 127.8乙烯C2H4 …… 6.74756 585.00 255.00氯乙烯C2H3 Cl -11~+50 6.49712 783.4 230.01,1,2一三氯乙烯C2HCl3 …… 7.02808 1315.04 230.0苯乙烯C8H8 …… 6.92409 1420.0 206丙烯C3H6 …… 6.81960 785.0 247.00丁稀-1 C4H8 …… 6.84290 926.10 240.00顺-2-丁烯C4H8 …… 6.86926 960.100 237.00反-2-丁稀C4H8 …… 6.86952 960.80 240.002-甲基丙烯-1 C4H8 …… 6.84134 923.200 240.001,2一丁二烯C4H6 -60~+80 7.1619 1121.0 251.001,3一丁二烯C4H6 -80~+65 6.85941 935.531 239.5542-甲基丁二稀-1,3 C5H8 -50~+95 6.90334 1080.966 234.668 乙炔C2H2 -140~-82 公式(2)21.914 8.933甲醇CH4O -20~+140 7.87863 1473.11 230.0苯甲醇C7H8O 20~113 7.81844 1950.3 194.36苯甲醇113~300 6.95916 1461.64 153.0乙醇C2H6O …… 8.04494 1554.3 222.65正丙醇C3H8O …… 7.99733 1569.70 209.5异丙醇C3H8O 0~113 6.66040 813.055 132.93正丁醇C4H10 75~117.5 公式(2)46.774 9.1362特丁醇C4H10 …… 8.13596 1582.4 218.9乙二醇C2H6O2 25~112 8.2621 2197.0 212.0乙二醇112~340 7.8808 1957.0 193.8乙醛C2H4 O -75~-45 7.3839 1216.8 250乙醛-45~+70 6.81089 992.0 230丙酮C3H6O …… 7.02447 1161.0 224二乙基酮C5H10O …… 6.85791 1216.3 204甲乙酮C4H3O …… 6.97421 1209.6 216甲酸CH2O2 …… 6.94459 1295.26 218.0苯甲酸C7H6O2 60~110 公式(2)63.82 9.033乙酸C2H4O2 0~36 7.80307 1651.2 225乙酸36~170 7.18807 1416.7 211丙酸C3H6O2 0~60 7.71553 1690 210丙酸60~185 7.35027 1497.775 194.12正丁酸C4H8O2 0~82 7.85941 1800.7 200正丁酸82~210 7.38423 1542.6 179月硅酸C12H24O2 164~205 公式(2)74.386 9.768十四烷酸C14H28O2 190~224 公式(2)75.783 9.541 乙酐C4H6O3 100~140 公式(2)45.585 8.688顺丁烯二酸酐C4H2O3 60~160 公式(2)46.34 7.825 邻苯二甲酸酐C3H4O3 160~285 公式(2)54.92 8.022 酷酸乙醋C4H8 O2 -20~+150 7.09808 1238.71 217.0甲酸乙酯C3H6O2 -30~+235 7.11700 1176.6 223.4醋酸甲酯C3H6O2 …… 7.20211 1232.83 228.0苯甲酸甲酯C8H8O2 25~100 7.4312 1871.5 213.9苯甲酸甲酯100~260 7.07832 1656.25 95.23甲酸甲酯C2H4O2 …… 7.13623 1111.0 229.2水杨酸甲酯C8H8O3 175~215 公式(2)48.67 8.008 氨基甲酸乙酯C3H7O2N …… 7.42164 1758.21 205.0甲醚C2H6O …… 6.73669 791.184 230.0苯甲醚C7H8O …… 6.98926 1453.6 200二苯醚C12H10O 25~147⑤ 7.4531 2115.2 206.8二苯醚147~325 7.09894 1871.92 185.84甲乙醚C3H8O 0~25 公式(2)26.262 7.769乙醚C4H10O …… 6.78574 994.195 210.2甲胺CH5N -93~-45 6.91831 883.054 223.122甲胺-45~+50 6.91205 838.116 224.267二甲胺C2H7N -80~-30 7.42061 1085.7 233.0二甲胺-30~+65 7.18553 1008.4 227.353三甲胺C3H9N -90~-40 7.01174 1014.2 243.1三甲胺-60~+850 6.81628 937.49 235.35乙胺C2H7N -70~-20 7.09137 1019.7 225.0乙胺-20~+90 7.05413 987.31 220.0二乙胺C4H11N -30~+100 6.83188 1057.2 212.0三乙胺C6H15N 0~130 6.8264 1161.4 205.0苯胺C6H7N …… 7.24179 1675.3 200二甲替甲酰胺C3H7ON 15~60 7.3438 1624.7 216.2二甲替酰胺60~350 6.99608 1437.84 199.83二苯胺C12H11N 278~284 公式(2)57.35 8.008间硝基苯胺C6H6O2N2 190~260 公式(2)77.345 9.5595 邻硝基苯胺C6H5O2N2 150~260 公式(2)63.881 8.8684 对硝基苯胺C6H6O2N2 190~260 公式(2)77.345 9.5595 苯酚C6H6O …… 7.13617 1518.1 175.0邻甲酚C7H8O …… 6.97943 1479.4 170.0间甲酚C7H8O …… 7.62336 1907.24 201.0对甲酚C7H8O …… 7.00592 1493.0 160.0α-萘酚C10H8O …… 7.28421 2077.56 184.0β-萘酚C10H8O …… 7.34714 2135.00 183.0苯⑥ C6H6 …… 6.90565 1211.033 220.790氯苯C6H5Cl 0~42 7.10690 1500.0 224.0氯苯42~230 6.94594 1413.12 216.0邻二氯苯C6H4Cl2 …… 6.92400 1538.3 200乙苯C8H10 …… 6.95719 1424.255 213.206氟苯C6H5F -40~+180 6.93667 1736.35 220.0硝基苯C6H6O2N 112~209 公式(2)48.955 8.192甲苯C7H8 …… 6.95464 1341.800 219.482邻硝基甲苯C7H7O2N 50~225 公式(2)48.114 7.9728 间硝基甲苯C7H7O2N 55~235 公式(2)50.128 8.0655 对硝基甲苯C7H7O2N 80~240 公式(2)49.95 7.9815三硝基甲苯C7H5O6N3 …… 3.8673 1259.406 160邻二甲苯C8H10 …… 6.99891 1474.679 213.686间二甲苯C8H10 7.00908 1462.266 215.105对二甲苯C8H10 6.99052 1453.430 215.307乙酰苯C8H8O 30~100 公式(2)55.117 9.1352乙腈C2H3N …… 7.11988 1314.4 230丙烯腈C3H3N -20~+140 7.03855 1232.53 222.47氰C2N2 -72~-28 公式(2)32.437 9.6539氰C2N2 -36~-6 公式(2)23.75 7.808萘C10H8 …… 6.84577 1606.529 187.227α-甲基綦C11H10 …… 7.06899 1852.674 197.716β-甲基萘C11H10 …… 7.06850 1840.268 198.395蓖C14H10 100~160 公式(2)72 8.91蓖223~342 公式(2)59.219 7.910蓖醌C14H3O2 224~286 公式(2)110.05 12.305 蓖醌285~370 公式(2)63.985 8.002樟脑C10H16O 0~18 公式(2)53.559 8.799咔唑C12H9N 244~352 公式(2)64.715 8.280芴C13H10 161~300 公式(2)56.615 8.059呋喃C4H4O -35~+90 6.97533 1010.851 227.740吗啉C4H9ON 0~44 7.71813 1745.8 235.0吗啉44~170 7.16030 1447.70 210.0菲C14H10 203~347 公式(2)57.247 7.771喹啉C9H7N 180~240 公式(2)49.72 7.969噻吩C4H4S -10~180 6.95926 1246.038 221.354草酸C2H2O4 55~105 公式(2)90.5026 12.2229 光气COCl2 -68~+68 6.84297 941.25 230氨⑥ NH3 -83~+60 7.55466 1002.711 247.885氯化铵NH4Cl 100~400 公式(2)83.486 10.0164 氰化铵NH4CN 7~17 公式(2)41.481 9.978开放分类:。
水蒸气饱和蒸汽压与温度表

水蒸气饱和蒸汽压与温度表水蒸气饱和蒸汽压与温度表是查阅水蒸气饱和蒸汽所需的各种参数的便捷工具。
水蒸气饱和蒸汽的压力随着温度的升高而降低,正常来说,温度越低,水蒸气饱和蒸汽的压力就越大。
这就需要一个表格来描述两者之间的关系,因此就有了水蒸气饱和蒸汽压与温度表。
水蒸气饱和蒸汽压与温度表表明,水蒸气饱和蒸汽压力随着温度升高而减小。
表里所列出的海拔蒸汽压比中线仪器测量的温度和压力值有一些变化,因此,海拔和气压不同的地方也影响了测量结果。
水蒸气饱和蒸汽的温度可在几六摄氏度(20℃-173.9℃)的范围内进行调整。
此表中,温度和压力分别以摄氏度(℃)和克拉(kPa)为单位进行测量。
水蒸气饱和蒸汽压力和温度列表:(温度/℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 | 120 | 130 | 140 | 150 | 160 | 170 | 180 |(压力/kpa) | 0.6096 | 0.5246 | 0.4537 | 0.3956 | 0.3480 | 0.3093 | 0.2778 | 0.2509 | 0.2278 | 0.2073 | 0.1894 |0.1737 | 0.1599 | 0.1477 | 0.1370 | 0.1277 | 0.1197 | 0.1126 | 0.1011 |水蒸气饱和蒸汽压力和温度的表明,随着温度的增加,水蒸气饱和蒸汽的压力剧烈下降,在重要的工业运输,蒸汽测量等应用中,温度和压力的变化可能会产生很大差异。
因此,有必要根据此表检查温度和压力的有效范围,以便确保正确使用蒸汽。
对于从事工业气体量测仪器、液体测量、仪表调节、加热系统、工程物理、制冷或暖通系统等相关领域的任务者来说,水蒸气饱和蒸汽压与温度表是很重要的工具,可以更加精确有效地从事各种应用。
水在不同温度下的饱和蒸气压

286.57
257
4465.1
8
1.0730
133
295.15
258
4539.0
9
1.1482
134
303.93
259
4613.7
10
1.2281
135
312.93
260
4689.4
11
1.3129
136
322.14
261
4766.1
12
1.4027
137
331.57
262
4843.7
13
1.4979
164
683.10
289
7330.2
40
7.3814
165
700.29
290
7438.0
41
7.7840
166
717.83
291
7547.0
42
8.2054
167
735.70
292
7657.2
43
8.6463
168
753.94
293
7768.6
44
9.1075
169
772.52
294
7881.3
45
51
12.970
176
913.03
301
8705.4
52
13.623
177
934.64
302
8828.3
53
14.303
178
956.66
303
8952.6
温度(Temperature)
t/℃
饱和蒸气压
(Saturated water vapor pressure) /(×103Pa)
饱和蒸汽温度与压力对照表

饱和蒸汽温度与压力对照表
按1MPa=1000kPa=10.2kgf/cm2(公斤/平方厘米),对照饱和蒸汽压力(MPa表示)与蒸汽温度的标准表,可以计算得到饱和蒸汽压力(kgf/cm2表示)与蒸汽温度之间的关系,如下所示:
饱和蒸汽的温度与压力之间一一对应,二者之间只有一个独立变量。
理想的饱和蒸汽状态,指的是温度、压力及蒸汽密度三者存在一一对应的关系,知道其中一个,其他二个值就是定数。
存在这种关系的蒸汽就是饱和蒸汽,并存在饱和蒸汽压力与温度对照表。
标准的饱和蒸汽压力与蒸汽温度对照表是根据国际单位制进行编制的,即压力单位为MPa,温度单位为℃。
扩展资料
饱和蒸汽压的测量方法可以分为两类:
1.动态法。
指在不同外界压力下,测定液体的沸点,又称沸点法。
这种方法只在测量常压附近的饱和蒸汽压时测量精度较好。
2.静态法。
指在不同温度下,直接测量液体饱和蒸汽压,即在恒温条件下测量饱和压力。
静态法测量相对简单,更具普遍性,通常的做法就是将待测物质充人密闭容器,并使其处于气液两相共存状态,然后放人恒温槽中,通过调节恒温槽温度来测量不同温度下的饱和蒸汽压数据。
15摄氏度下的饱和蒸汽压

15摄氏度下的饱和蒸汽压15摄氏度下的饱和蒸汽压是指在温度为15摄氏度时,液体与气体之间达到平衡的状态下,液体中蒸发出的气体与液体中的气体重新凝结成液体的速度相等。
饱和蒸汽压是一个重要的物理参数,它与温度之间存在着密切的关系。
下面将详细介绍15摄氏度下的饱和蒸汽压的相关知识。
饱和蒸汽压是气体与液体之间的平衡状态。
在15摄氏度下,液体中的分子具有一定的能量,其中一部分分子具有足够的能量克服液体表面的吸引力,从而从液体中脱离出来,形成气体。
而另一部分分子则具有足够的能量被液体吸引回来,重新凝结成液体。
当这两个过程达到平衡时,液体中蒸发出的气体与液体中的气体重新凝结成液体的速度相等,此时的压强就是饱和蒸汽压。
15摄氏度下的饱和蒸汽压是一个固定的数值,可以通过实验或计算得到。
根据热力学的原理和实验数据,我们可以得到15摄氏度下的饱和蒸汽压为X单位。
这个数值代表了在15摄氏度下,液体与气体之间达到平衡的状态,液体中蒸发出的气体与液体中的气体重新凝结成液体的速度相等所需要的压强。
饱和蒸汽压的数值与温度之间存在着严格的关系。
一般来说,随着温度的升高,饱和蒸汽压也会随之增加。
这是因为温度的升高会使液体中的分子具有更大的能量,从而增加脱离液体的几率,进而增加蒸发速率。
当温度达到一定值时,液体的蒸发速率将与液体中的分子重新凝结成液体的速率相等,此时的压强就是饱和蒸汽压。
饱和蒸汽压的变化规律可以通过一些实验数据来验证。
实验表明,随着温度的升高,饱和蒸汽压呈指数增加。
这种指数增加的规律被称为饱和蒸汽压与温度的饱和蒸汽压的关系式,可以用来描述不同温度下的饱和蒸汽压的变化。
在工程和科学领域中,饱和蒸汽压是一个重要的参考参数。
它被广泛应用于各种热力学计算和工程设计中。
例如,在锅炉和汽轮机等热力设备中,饱和蒸汽压是计算设备效率和性能的关键参数之一。
在化学工程中,饱和蒸汽压常被用于计算液体与气体传质过程中的气液平衡。
15摄氏度下的饱和蒸汽压是指在温度为15摄氏度时,液体与气体之间达到平衡的状态下,液体中蒸发出的气体与液体中的气体重新凝结成液体的速度相等的压强。
