消毒产品委托加工调查表
消毒剂检验项目检查表

e食饮具、瓜果蔬菜、生活饮用水、食品加工工具和设备仅做铅、砷。
f标签说明书未标注不得用于金属物品消毒的消毒剂,应进行金属腐蚀性试验。
g同时进行金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌杀菌试验时,只选其中一个菌进行中和剂鉴定试验。h标签说明书标注用于医院感染常见细菌消毒的,应做铜绿假单胞菌定量杀菌试验。
±p
一项致突变试验q
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
注1:标签说明书标注用于其他消毒对象或者对其他微生物有杀灭效果的消毒剂,应根据标签说明书标注的消毒对象和杀灭微生物的类别确定检验项目;标注无毒性作用的,应做相应的毒理试验。
注2:“+”为必须做项目;“空格”为不做项目;“*”为任选其一项目;“±”为选做项目。
+
+
±
+
连续使用稳定性试验k
±
±
±
模拟现场试验
+
+
+
*
*l
+
+
*
*
*
*
*
+
+
*m
*
+
现场试验
+
+
总体性能试验
+n
急性经口毒性试验
+
+
+
消毒产品生产企业分类监督综合评价表

消毒产品生产企业分类监督综合评价表
单位名称: _________________________________________
生产地址:______________
生产类别:口消毒剂□消毒器械□卫生用品(抗抑菌制剂除外)口抗(抑)菌制剂产品风险类别:口第一类口第二类□第三类
许可证号:卫消证字()第号
生产状况:口营业□暂停口关闭
产品状况:口自有品牌□代加工
得分:
评价结果:优秀口合格口重点监督口
填表说明
1.评价时应同时对综合管理、生产过程管理、产品卫生质量3个大项检查评分后方可对该单位进行最终的综合评价。
2.应采用标化分作为分类监督综合评价的最终得分。
标化分二实际得分/应得分X100。
实际得分为现场评价后的总得分,应得分为评价表设定的总分数(100分)减去合理缺项后的分数。
3.评价结果:(1)优秀单位:标化分大于85分、关键项合格;(2)合格单位:标化分60-85分且关键项合格;(3 )重点监督单位:标化分小于60分或关键项不合格。
如
检查评价为优秀单位但受到行政处罚最终评价结果降为合格
单位。
4*为关键项,如发生即认定为重点监督单位。
5.*为重点项,此项不合格则该项目整体不得分。
6.*为合理缺项,未做监督抽检或评价的企业没有该项情。
国家消毒产品随机监督抽查计划表

1.2024年消毒产品国家随机监督抽查计划表
2.2024年消毒产品生产企业国家随机监督抽查检查表
3.2024年消毒产品国家随机监督抽查案件查处汇总表
4.2024年抗(抑)菌制剂生产企业国家随机监督抽查案件查处汇总表
5.2024年抗(抑)菌制剂膏、霜剂型国家随机监督抽查案件查处汇总表
6.2024年抗(抑)菌制剂膏、霜剂型违法添加禁用物质产品清单
— 1 —
表1
— 2 —
— 3 —
— 4 —
— 5 —
表2
2024年消毒产品生产企业国家随机监督抽查检查表
企业名称:卫生许可证号:地址:
法定代表人联系人联系电话
从业人员总数:生产车间面积:m2
— 6 —
— 7 —
检查人:检查时间:年月日— 8 —
表3
★2024年消毒产品国家随机监督抽查案件查处汇总表
市
填表单位(盖章):填表人:联系电话:填表日期:
— 9 —
表4
★2024年抗(抑)菌制剂生产企业国家随机监督抽查案件查处汇总表市
填表单位(盖章):填表人:联系电话:填表日期:
— 10 —
表5
★2024年抗(抑)菌制剂膏、霜剂型国家随机监督抽查案件查处汇总表市
填表单位(盖章):填表人:联系电话:填表日期:
— 11 —
表6
★2024年抗(抑)菌制剂膏、霜剂型违法添加禁用物质产品清单市
填表单位(盖章):填表人:联系电话:填表日期:
— 12 —。
2020年消毒产品生产企业国家随机监督抽查检查表

生产条件
全部类别
生产车间布局、流程、生产设施设备是否与申报时一致
是□ 否□
第一类产品
医疗器械高水平消毒剂、灭菌剂生产用水是否符合相应要求
是□ 否□
皮肤黏膜消毒剂的净化车间和生产用水是否符合相应要求
是□ 否□
生物指示物、灭菌效果化学指示物、医疗器械高水平消毒器械、灭菌器械的生产设施是否符合相应要求
是□ 否□
第二类产品
用于皮肤黏膜的抗(抑)菌的净化车间、生产用水、生产设施是否符合相应要求
是□ 否□
第三类产品
空气消毒设施是否符合相应要求
是□ 否□
生产过程
全部类别
是否有合格的出厂检验报告
是□ 否□
是否有合格的生产记录
是□ 否□
原材料卫生质量
全部类别
是否能满足产品质量要求,符合相关质量标准和卫生行政部门的有关要求,符合企业标准要求,并能提供相应的检验报告或相应的产品质量证明材料
附表4
2020年消毒产品生产企业国家随机监督抽查检查表
企业名称:卫生许可证号:地址:
法定代表人联系人联系电话
从业人员总数:生产车间面积:
项目
风险类别
重点检查内容
检查结果
备注
卫生许可
持证情况
全部类别
法定代表人、企业名称、企业生产地址是否与实际一致
是□ 否□
生产类别、项目是否与实际一致
是□ 否□
卫生许可证是否在有效期
个
是否有未按要求进行卫生安全评价的消毒产品
是□ 否□
个
卫生安全评价报告是否均合格
是□ 否□
各评价报告内容是否完整
是□ 否□
消毒产品标签(铭牌)、说明书
消毒产品生产企业日常监督检查表

单位名称
法定代表人
联系人
联系电话
注册地址
生产地址
卫生许可证
是否在有效期内
□是□否
是否每年按期复核
□是□否
标注地址与实际生产地址是否一致
□是□否
生产条件及产品是否与许可项目相符
□是□否
生产区
更衣室是否设于工作人员入口处□是□否源自是否配有流动水洗手、消毒设施
□是□否
是否有与生产批准产品无关的原辅料和生产设备
□是□否
是否做到人物流分开
□是□否
生产记录是够齐全
□是□否
仓储
原材料和成品是否分开存放
□是□否
是否有通风、防鼠防虫设施
□是□否
是否离墙离顶存放
□是□否
待检产品、合格产品、不合格产品是否分开存放
□是□否
出入库记录是否齐全
□是□否
人员
从业人员是否有健康培训证明
□是□否
卫生管理员是否有卫生管理员培训证书
□是□否
卫生质量控制
产品出厂检验采用何种方式
□委托□自检□不检
是否有相应的检测设备
□是□否
是否有原料、半成品、成品检验记录
□是□否
委托检验能否提供出相应批次的检验报告
□是□否
是否按产品批次留样
□是□否
消毒剂生产企业监督检查表

消毒剂生产企业监督检查表
生产企业名称联系电话
生产企业地址实际生产企业地址
卫生许可证号生产方式生产□分装□生产项目第一类消毒剂□第二类消毒剂□
生产类别
消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
陪同检查人:检查人:检查时间:年月日
附件2
医疗卫生机构消毒产品管理自查表
单位名称(盖章):
地址:
联系电话:联系人:
医疗机构(三级□二级□一级□未定级□):疾控机构□妇幼保健机构□购进消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
自查时间:年月日附件3
医疗卫生机构消毒产品管理检查表
单位名称:
地址:联系电话:
联系人:
医疗机构(三级□二级□一级□未定级□):疾控机构□妇幼保健机构□购进消毒剂目录
卫生安全评价报告不合格产品名录:
产品标签说明书违规产品名录:
陪同检查人:检查人:检查时间:年月日
附件4
消毒剂生产企业检查情况汇总表
辖区消毒产品生产企业数家检查消毒剂生产企业家
填表单位(盖章):填表人:联系电话:填表日期:
附件5
填表单位(盖章):填表人:联系电话:填表日期:附件6
消毒剂专项整治案件查处汇总表
填表单位(盖章):填表人:联系电话:填表日期:。
表2消毒产品生产企业监督检查表

表2 消毒产品生产企业监督检查表生产企业名称生产企业地址实际生产企业地址法定代表人联系电话职工总数从业人员数持健康合格证明人数卫生知识培训合格人数厂区面积生产车间面积生产车间环境无净化要求□ 10万级净化车间□ 30万级净化车间□卫生许可证号生产方式生产□ 分装□生产项目消毒剂□ 消毒器械□ 卫生用品□生产类别生产产品目录:注:1、检查项目有打√,无打X。
2、有①标记的,为开展委托检验的生产企业填;3、有②标记的,注明卫生许可批件号和有效期。
陪同检查人:检查人:检查日期:表2-3 消毒产品卫生质量抽检- 3 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.- 4 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表3 消毒产品生产企业监督检查情况汇总表- 5 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表4 消毒产品监督检查情况汇总表市单位(盖章):- 6 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表5 注销/吊销消毒产品生产企业名单汇总表市单位(盖章):- 7 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.填表人:联系电话:填表日期:审核人:单位负责人(签字)- 8 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表6 不合格消毒产品名单汇总表市单位(盖章):注:1. 卫生安全评价不合格包括第一类消毒产品卫生安全评价报告有效期满未重新进行卫生安全评价的;出具虚假卫生安全评价报告;有《消毒产品卫生安全评价规定》第十二条规定情形之一,未重新进行检验的;产品上市后如有改变(配方或结构、生产工艺)或未按《消毒产品卫生安全评价规定》第十二条规定情形之一,未对卫生安全评价报告内容进行更新的。
2.检验包括抽检和批检。
填表人:联系电话:填表日期:审核人:单位负责人(签字)- 9 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.附件2放射卫生技术服务机构专项整治检查表表1 放射卫生技术服务机构基本信息汇总表(本省卫生计生行政部门批准机构)市填表人:联系电话:填表日期:审核人:单位负责人(签字):- 10 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表2 放射卫生技术服务机构基本信息汇总表(非本省卫生计生行政部门批准机构)填表人:联系电话:填表日期:审核人:单位负责人(签字)- 11 -文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持.表3 放射卫生技术服务机构监督检查表一、机构基本情况机构名称:法定代表人:资质类别:取得资质时间:1.取得资质以来是否开展技术服务工作。
消毒供应中心上报调查表

消毒供应中心上报调查表附件1:山东省医疗机构消毒供应中心(室)基本情况调查表一、一般情况1、医疗机构名称赵官镇中心卫生院,地市:山东省德州市齐河县地址:赵官镇北一村。
等级:三甲()三乙()二甲()二乙()一级(√)类别:公立(√)民营()股份制()。
2、2011年医院在院职工(含聘任制)118 人数:2011年门诊量19440 人次,实际开发放床位数50 张。
3、2011年手术数量855 台,其中门诊手术(含内镜)110 台,住院手术656 台。
4、2011年妇科手术270 台,其中产科手术(刨宫产)181 台,流产手术89 台。
5、2011年出院量6870 人次,平均住院日5 天。
二、建筑及设备情况是否已进行CSSD的建设:是(√)否()。
1、有无消毒供应中心(室):有(√)无()。
2、消毒供应中心(室)面积50m2;分区情况分区;卫浴间:有(√)无()。
3、设备情况:高温灭菌器数量,品牌及容积上海三申、双哈、75L ,每天灭菌锅数 2 ;低温灭菌器数量,品牌及容积,每天灭菌锅数;高压水枪无(√),有()清洗消毒机的数量,品牌及容积;超声清洗设备:无(),有()数量,品牌及容积。
干燥设备无:(),有(√)数量,品牌及容积通江、烘干机。
水处理设备:无(),有()数量,品牌及容积、日处理水量。
酸化水发生器:无(),有()数量,品牌及容积。
生物培养阅读器的数量,品牌及型号;4、无消毒供应中心(室)的医疗机构现在清洗消毒灭菌的方法:外包机构名称,外包内容,其他方式。
三、消毒供应中心的管理情况1、人员:(1)消毒供应室人员总数 2 。
平均年龄46 最大年龄48 最小年龄44 ;有否慢性疾病:有人,无(√)学历情况:硕士人本科人专科人中专2 人(2)护士长:年龄、供应室任职年限、学历、职称。
(3)护士人数其中:主任护师人副主任护师人主管护师人护师人护士人(4)其他技术人员人数;(5)消毒员人数,其中具有灭菌器操作上岗证的人数。
消毒供应中心问卷调查内容

消毒供应中心问卷调查内容
1. 您的姓名:__________
2. 您的职务:__________
3. 所属科室:__________
4. 您对消毒供应中心的了解程度?(请在1-10之间选择一个数字,10表示非常了解,1表示完全不了解)
5. 您认为消毒供应中心对医院的重要性如何?(请在1-10之间选择一个数字,10表示非常重要,1表示不太重要)
6. 您对消毒供应中心的工作流程了解吗?(请在1-10之间选择一个数字,10表示非常了解,1表示完全不了解)
7. 您认为消毒供应中心的工作流程是否合理?(请在1-10之间选择一个数字,10表示非常合理,1表示不太合理)
8. 您对消毒供应中心的工作人员态度是否满意?(请在1-10之间选择一个数字,10表示非常满意,1表示不太满意)
9. 您认为消毒供应中心的设备是否足够?(请在1-10之间选择一个数字,10表示非常足够,1表示不太足够)
10. 您认为消毒供应中心存在的最大问题是什么?请尽可能详细地描述您的看法。
11. 您对消毒供应中心有哪些建议或意见?请尽可能详细地描述您的看法。
感谢您参与本次问卷调查!我们将会认真分析您的反馈,并采取相应措施以提高消毒供应中心的服务质量。
如有需要,您可以随时联系我们。
再次感谢您!。
委托加工情况调查明细表
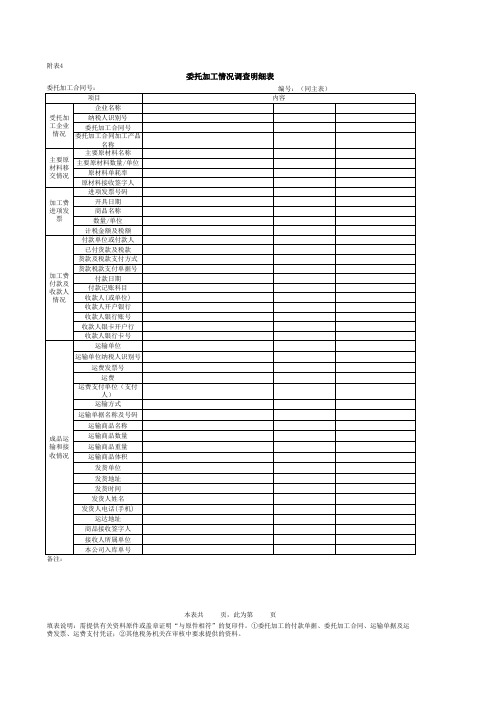
委托加工情况调查明细表
委托加工合同号: 项目 企业名称 受托加 纳税人识别号 工企业 委托加工合同号 情况 委托加工合同加工产品 名称 主要原材料名称 主要原 主要原材料数量/单位 材料移 原材料单耗率 交情况 原材料接收签字人 进项发票号码 开具日期 加工费 进项发 商品名称 票 数量/单位 计税金额及税额 付款单位或付款人 已付货款及税款 货款及税款支付方式 货款税款支付单据号 加工费 付款日期 付款及 付款记账科目 收款人 收款人(或单位) 情况 收款人开户银行 收款人银行账号 收款人银卡开户行 收款人银行卡号 运输单位 运输单位纳税人识别号 运费发票号 运费 运费支付单位(支付 人) 运输方式 运输单据名称及号码 运输商品名称 成品运 输和接 收情况 运输商品数量 运输商品重量 运输商品体积 发货单位 发货地址 发货时间 发货人姓名 发货人电话(手机) 运达地址 商品接收签字人 接收人所属单位 本公司入库单号 备注: 编号:(同主表) 内容
本表共
页,此为第
页
填表说明:需提供有关资料原件或盖章证明“与原件相符”的复印件。①委托加工的付款单据、委托加工合同、运输单据及运 费发票、运费支付凭证;②其他税务机关在审核中要求提供的资料。
卫生部办公厅关于开展整治消毒产品违法宣传疗效和添加药物专项行动的通知

卫生部办公厅关于开展整治消毒产品违法宣传疗效和添加药物专项行动的通知文章属性•【制定机关】卫生部(已撤销)•【公布日期】2009.03.27•【文号】卫办监督发[2009]42号•【施行日期】2009.03.27•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】卫生医药、计划生育综合规定正文卫生部办公厅关于开展整治消毒产品违法宣传疗效和添加药物专项行动的通知(卫办监督发[2009]42号)各省、自治区、直辖市卫生厅局,新疆生产建设兵团卫生局,中国疾病预防控制中心、卫生部卫生监督中心:最近一段时期,不断有消费者投诉举报,市场上有一些标有“卫消证字”或“卫消字”的产品,违法宣传治疗疾病、添加药物,欺骗和误导消费者,危害人民身体健康。
为严厉打击上述违法行为,保护人民群众健康,我部决定在全国范围内开展为期6个月的专项整治消毒产品违法宣传疗效和添加药物的行动。
现将具体工作要求通知如下:一、工作目标通过专项整治,进一步规范消毒产品生产经营行为,依法严肃查处消毒产品宣传疗效和添加药物等违法行为,切实加大对消毒产品生产经营的监管力度,增强消费者的使用安全感。
二、工作重点(一)对辖区内生产抗(抑)菌制剂的生产企业按照《消毒产品生产企业卫生规范》的要求逐一进行监督检查。
重点检查生产过程记录是否完整;原辅料的采购、使用管理是否符合要求;原材料是否与生产产品的配方成分、登记要求一致;原料库是否有卫生部禁止添加的物质和成分;产品标签说明书的合法性和规范性;必要时抽检部分产品的卫生质量;对委托生产的情况进行全面调查。
(二)对销售标注“卫消证字”或“卫消字”产品的药店等经营单位进行检查。
重点检查经营单位对销售的标有“卫消证字”或“卫消字”等产品,是否索取生产企业卫生许可证或产品卫生许可批件并存档备查;销售的消毒产品的标签说明书是否规范。
同时对宣传治疗疾病的抗(抑)菌产品进行抽检,抽检数量、项目见我部2009年国家公共卫生重点监督检查计划。
消毒产品卫生安全评价技术要求(卫生行业标准)

消毒产品卫生安全评价技术要求1 范围本标准规定了消毒产品卫生安全评价的基本要求及内容。
本标准适用于中华人民共和国境内生产、经营和使用的除新消毒产品以外的第一类、第二类消毒产品(消毒剂、消毒器械、指示物、抗(抑)菌制剂)的卫生安全评价。
本标准不适用于定制消毒器械的卫生安全评价。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
生活饮用水消毒剂和消毒设备卫生安全评价规范(试行)(2005年版)卫生部(卫监督发〔2005〕336号)3 术语和定义下列术语和定义适用于本文件。
3.1消毒产品卫生安全评价 hygiene and safety evaluation of disinfectant product对消毒产品有效性和卫生安全性进行的综合评价,评价内容包括产品标签(铭牌)、说明书、检验报告、企业标准或质量标准、生产企业卫生许可证(境外允许生产销售的证明文件及报关单)、消毒剂、指示物和抗(抑)菌制剂的产品配方、消毒器械的结构图等。
3.2产品责任单位responsible entity依法承担因产品缺陷而致他人人身伤害或财产损失的赔偿责任的个人、法人及其他组织。
委托生产加工时,特指委托方,进口产品的责任单位为在华责任单位。
3.3第一类消毒产品classⅠdisinfectant product用于医疗器械的高水平消毒剂和消毒器械、灭菌剂和灭菌器械,皮肤/黏膜消毒剂,生物指示物、灭菌效果化学指示物。
3.4第二类消毒产品class Ⅱ disinfectant product除第一类产品外的消毒剂、消毒器械、化学指示物,以及带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂。
3.5定制消毒器械customized disinfection instrument为单一项目设计制造,没有批量生产的非定型消毒器械。
卫生用品(消毒产品)生产企业现场监督审核表

附件5
卫生用品(消毒产品)生产企业
现场监督审核表
生产企业名称_____________________
生产企业地址_____________________
实际生产加工地址_____________________
现场监督审核日期年月日
卫生用品生产企业现场监督审核表
生产企业一般情况
法定代表人/负责人:卫生管理负责人:检验负责人:
通讯地址:联系电话:邮编:传真:职工总数:从业人员总数:生产区面积:
产品种类:
考评审核表:
备注:1. 本表用于卫生用品生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:
现场监督审核人(签名):被审核单位负责人(签名):
单位公章
审核日期:年月日年月日。
消毒产品委托书

消毒产品委托书
一、委托方信息
委托方:[委托方名称] 地址:[委托方地址] 联系人:[联系人姓名] 电话:[联系人电话]
二、受托方信息
受托方:[受托方名称] 地址:[受托方地址] 联系人:[联系人姓名] 电话:[联系人电话]
三、委托内容
1.委托方授权受托方进行消毒产品的检测和评估。
2.委托方将提供所需的消毒产品样品,并支付相关费用。
四、费用及支付方式
1.委托方应支付受托方定价的检测费用。
费用支付方式:[支付方式]。
2.如有额外费用(如运输费等),另行协商支付。
五、委托期限
1.本委托书自双方签字之日起生效,至[委托期限]为止。
2.受托方应在委托期限内完成检测并递交报告。
六、保密条款
双方在委托过程中应保守委托内容的秘密,不得向任何第三方透露。
七、其他事项
1.委托方应提供准确、完整的消毒产品样品,确保检测结果准确性。
2.受托方应按照国家相关标准和法规进行检测,保证检测结果的客观性
和可靠性。
八、解决争议
双方发生争议应先协商解决,如无法协商解决,应提交有关法律部门进行调解处理。
九、委托方签字
委托方签字:______________ 日期:______________
十、受托方签字
受托方签字:______________ 日期:______________
以上为【消毒产品委托书】内容,双方均已确认理解并同意。
消毒产品加工合同范本

消毒产品加工合同范本一、合同双方甲方(委托方): _________乙方(受托方): _________二、合同背景鉴于甲方在消毒产品领域拥有广泛的市场和客户基础,乙方拥有专业的生产设备和技术,甲乙双方本着平等、自愿、互利的原则,就甲方委托乙方进行消毒产品加工事宜,达成如下协议:三、加工产品及数量1. 产品名称:消毒液/消毒喷雾/消毒粉等2. 产品规格: _________3. 加工数量: _________4. 产品标准:符合_______(国家/行业标准)四、加工费用及支付方式1. 加工费用:每单位_______元(含税)2. 支付方式:预付款:合同签订后,甲方支付合同总金额的_______%作为预付款。
尾款:产品验收合格后,甲方支付剩余的_______%。
五、加工周期及交货1. 加工周期:自甲方提供原材料之日起_______个工作日内完成。
2. 交货地点: _________3. 交货方式: _________(乙方送货/甲方自提)六、原材料供应1. 原材料提供: _________(甲方提供/乙方自备)2. 原材料质量:应符合_______(国家/行业标准)七、质量保证1. 乙方保证:加工的产品符合合同约定的质量标准。
2. 验收标准: _________3. 不合格品的处理:乙方应及时更换或重新加工不合格产品。
八、知识产权1. 技术保密:乙方应对在加工过程中接触到的甲方商业秘密和技术资料保密。
2. 知识产权归属:加工过程中产生的知识产权归_______(甲方/乙方)所有。
九、违约责任1. 甲方违约:如甲方未按约定支付加工费用,应向乙方支付违约金,金额为未支付款项的_______%。
2. 乙方违约:如乙方未能按期交货或产品质量不符合标准,应向甲方支付违约金,金额为合同总金额的_______%。
十、争议解决本合同在履行过程中发生的任何争议,双方应通过友好协商解决;协商不成的,任何一方均可向合同签订地人民法院提起诉讼。
1、消毒产品证件审核登记表(有委托其他公司生产的企业)
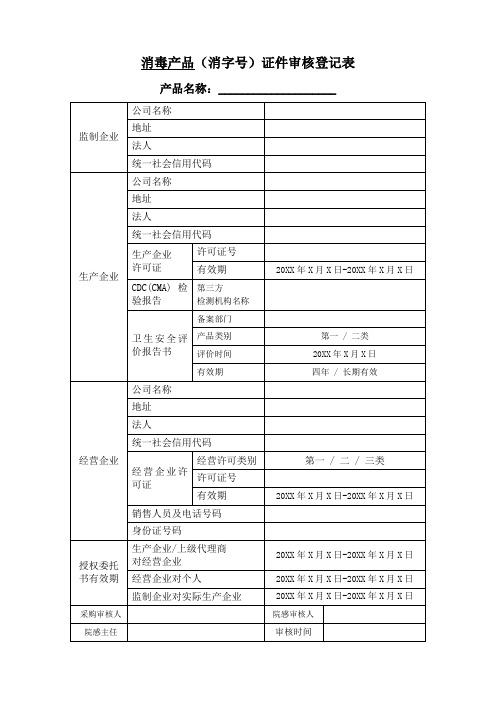
消毒产品(消字号)证件审核登记表产品名称:____________________
填写说明:
1、产品如无委托其他企业进行代为生产,则监制企业可不填;
2、CDC(CMA)检验报告送检部门:
广东省内均基本送至
广东省疾病预防控制中心或
广州出入境检测检疫综合检测中心;
外省按照实际送检部门填写。
3、卫生安全评价报告书有效期:
第一类消毒产品卫生安全评价报告有效期为4年;
(请扫描成一份PDF格式,并用产品名称命名,如“安多福0.1%PVP-I消毒液”)
1.监制企业
(如有委托其他企业进行代为生产,则需提供该项,如无则不需要);
2.生产企业营业执照;
3.生产企业许可证;
4.CDC(CMA)检验报告;
5.卫生安全评价报告书;
6.卫生安全评价报告书对应备案部门的网络备案截图!
7.经营企业营业执照;
8.经营企业许可证;
9.生产企业对经营企业授权书;
10.经营企业授权书对个人授权书;
11.监制企业对实际生产企业授权书;
(如有委托其他企业进行代为生产,则需提供该项,如无则不需要);
12.个人身份证;
13.
14.
15.
(专业素材和资料部分来自网络,供参考。
可复制、编制,期待您的好
评与关注)
16.
17.
18.。
消毒产品现场自查表
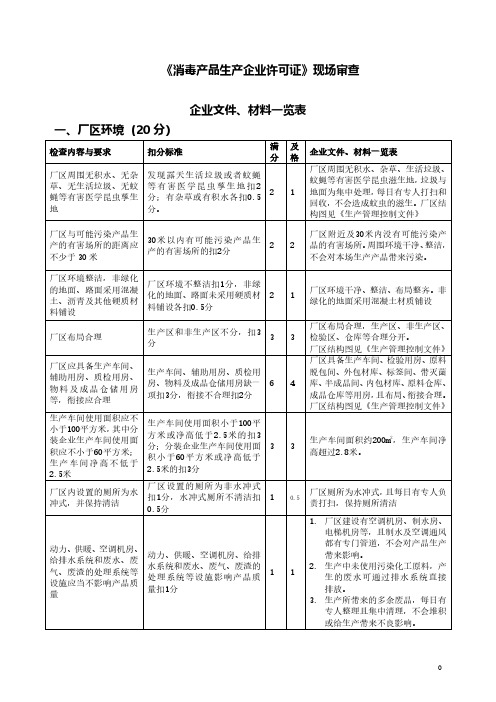
生产区根据洁净度级别 生产区未根据洁净度级别分
分为一般生产区、控制 区扣4分;同一生产区内(或
区和洁净室(区),同一 相邻生产区间)相互妨碍或交
生产区内或相邻生产区 叉污染各扣2分;不同洁净度
间的生产操作,不得相 级别的生产车间交叉污染扣2 4
生产车间设有换鞋间,男一、女一,
皮肤粘膜抗(抑)菌制 剂、隐形眼镜护理用品 生产企业生产车间包 括:配料间(区)、制作 功能间(区)缺一个扣1分 加工间(区)、分(灌) 装间(区)、包装间(区) 等功能间(区)
男二、女二,缓冲间,洁净走道、
洗衣间、整衣存放间、洁具清洗、
洁具存放间、器具清洗及器具存放
动力、供暖、空调机房、给排 水系统和废水、废气、废渣的 处理系统等设施影响产品质 量扣1分
1
1
厂区环境干净、整洁、布局整齐。非 绿化的地面采用混凝土材质铺设
厂区布局合理,生产区、非生产区、 3 检验区、仓库等合理分开。
厂区结构图见《生产管理控制文件》 厂区具备生产车间、检验用房、原料 脱包间、外包材库、标签间、带灭菌 4 库、半成品间、内包材库、原料仓库、 成品仓库等用房,且布局、衔接合理。 厂区结构图见《生产管理控制文件》
衔接合理。厂区结构及生产工
艺流程图间《生产管理控制文
件》
生产区各功能间(区) 应配置有效的防尘、防 虫、防鼠、通风等设施
无防尘、防虫、防鼠、通风设 施扣2分,未正常使用扣1分
2
1
生产区入口处都安有防虫防蚊灯, 各功能间及仓库全部安有防尘通 风设施。生产区安装有有效范围 100m2的电子驱鼠器、电子驱虫器。
无更衣室、专用工作服、流动 水洗手、手消毒、空气消毒等 设施各扣2分;无衣柜、鞋架 各扣1分。 洁净室(区)未设置二次更衣 室扣2分。 使用的消毒产品不符合国家 有关规定扣1分。
