九年级第一单元溶液 测试题
化学溶液测试题及答案

化学溶液测试题及答案一、选择题(每题2分,共20分)1. 下列物质中,属于强电解质的是()。
A. 醋酸B. 蔗糖C. 氯化钠D. 酒精2. 在溶液中,溶质的浓度越大,其沸点升高的原因是()。
A. 溶液的密度增加B. 溶质分子与溶剂分子间的作用力增强C. 溶液的表面张力增加D. 溶液的蒸气压降低3. 以下哪种物质不属于缓冲溶液?()A. 盐酸和碳酸钠的混合溶液B. 醋酸和醋酸钠的混合溶液C. 氨水和氯化铵的混合溶液D. 硫酸和硫酸钠的混合溶液4. 根据酸碱中和反应的原理,下列反应中属于中和反应的是()。
A. 硫酸铜与氢氧化钠反应B. 硫酸与碳酸钠反应C. 硫酸与氢氧化铜反应D. 硫酸与氢氧化钠反应5. 根据电离平衡的原理,下列物质中属于弱酸的是()。
A. 硫酸B. 盐酸C. 醋酸D. 硝酸二、填空题(每题3分,共30分)1. 溶液的pH值越小,表示溶液的酸性越_________。
2. 离子方程式中,表示水分子的符号是_________。
3. 根据电离平衡原理,弱酸的电离方程式通常用_________表示。
4. 缓冲溶液的pH值相对稳定,主要原因是它含有_________和_________。
5. 根据酸碱中和反应的原理,当酸和碱反应生成盐和水时,溶液的pH 值会_________。
三、简答题(每题10分,共20分)1. 请简述什么是溶液的饱和度,并举例说明如何测定溶液的饱和度。
2. 请解释什么是酸碱指示剂,并举例说明如何利用酸碱指示剂测定溶液的酸碱性。
四、计算题(每题15分,共30分)1. 已知某溶液的pH值为3,求该溶液的氢离子浓度。
2. 已知某溶液中溶质的摩尔浓度为0.1 mol/L,求该溶液的摩尔浓度对应的物质的量浓度。
答案:一、选择题1. C2. D3. D4. D5. C二、填空题1. 强2. H2O3. 可逆符号4. 弱酸、弱酸盐5. 升高三、简答题1. 溶液的饱和度是指在一定温度下,一定量的溶剂中能够溶解溶质的最大量。
九年级化学溶液单元测试题(可编辑修改word版)

九、1、溶液形成课堂练习一、判断题,判断下列说法是否正确1、溶液放置较长时间会出现分层和沉淀现象()2、溶液一定是液体。
()3、同一溶液的各部分性质相同。
()4、溶液的溶质一定只有一种。
()5、任何物质放入水中搅拌后都可得到溶液()6、均一,稳定的液体一定是溶液。
()7、溶液一定是无色透明的。
()8、蒸馏水是一种溶液。
()9、溶液一定是混合物。
()10、将KNO3溶液和NaCL 溶液混合后,所得液体仍是溶液。
()二、填空题1、将10 克食盐完全溶解在100 克水中,所得溶液总质量为克,溶剂质量为克,溶质质量和溶液质量比为,溶质质量和溶剂质量比为。
2、自习反馈1、将白糖、面粉、味精、食盐分别加入水中,充分搅拌后不能形成溶液的是()A、白糖B、面粉C、味精D、食盐2、下列说法中,不正确的是()A、溶液中的溶质可以是固体、液体或气体B、一定条件下,同种物质在不同物质里的溶解现象不一定相同C、溶液一定是由溶质和水组成D、一定条件下,不同物质在同一物质里的溶解现象不一定相同3、下列常见的医用溶液中,溶剂不是水的是()A、葡萄糖注射液B、生理盐水C、消毒酒精D、碘酒4、各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂不具有乳化功能是()A、用汽油除去衣服上的油污B、用餐具洗涤剂洗餐具上的油污C、用肥皂液洗衣D、用淋浴露洗澡5、海水淡化可采用膜分离技术。
如图所示,对淡化膜右侧的海水加压,水分子可能透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。
对加压后右侧海水成分变化进行分析,正确的是()A、溶质质量增加B、溶剂质量减少C、溶液质量不变D、溶质和溶剂的质量都减小6、澄清的石灰水中,溶质是,溶剂是。
通入一定量的CO2,发生反应的化学方程式为。
静置片刻,会有沉淀下来。
再滴加稀盐酸,待沉淀恰好完全溶解,此时发生反应的化学方程式为。
剩下的溶液中,溶质是,溶剂是。
7、小林就餐时不小心把油污弄到衣服上,发现用水怎么也洗不掉,他使用洗衣粉后,洗污被洗掉了,这是因为洗衣粉具有功能,小岩建议他可用汽油洗去,用汽油洗去油污的原因是。
(word版)九年级化学溶液单元测试题

火眼金睛1.以下物质分别放入水中,能形成溶液的是〔〕A.碳酸钙粉末B.面粉C.菜籽油D.白砂糖2.准确量取mL硫酸溶液,应选用的量筒是〔〕mL量筒 B.20mL量筒 C.50mL量筒 D.100 mL量筒℃有甲、乙、丙、丁四种物质,在以下四种情况下正好形成饱和溶液,其中最不易溶于水的是〔〕g甲溶于1g水B.1502g乙溶于100g水C.50g丙溶于300g水D.1g丁溶于20g水4.浓溶液在用水稀释的过程中保持不变的是〔〕A.溶液质量B.溶液体积C.溶质质量D.溶质的质量分数5.要使已被接近饱和的硝酸铵溶液变为饱和溶液,以下方法中不正确的选项是〔〕A.倒出少量溶剂B.投入硝酸铵C.蒸发局部水D.适当降温6.以下溶液一定是不饱和溶液的是〔〕A.浓溶液B.降温后会析出晶体的溶液C.蒸发水后会析出晶体的溶液D.投入固体溶质后溶质质量分数仍在改变的溶液7.有20℃时某物质的饱和溶液200g,从中取出100g,以下有关说法不正确的选项是〔〕A.此溶液中溶质质量分数不变B.此物质的溶解度〔20℃时〕不变C.溶液中溶质与溶剂的质量之比不变D.此物质的溶解度减小一半8.在t℃时,某固体物质的溶解度为ag,该温度下饱和溶液中溶质的质量分数为b%,那么a,b的关系为〔〕A.a〉bB.a<bC.a=bD.不能确定9.以下条件下的氯化氢气体的溶液即为盐酸,其溶质的质量分数最大的是〔〕A.20℃的饱和溶液B.20℃的不饱和溶液℃的饱和溶液 D.80℃的不饱和溶液10.现有以下仪器:①托盘天平②烧杯③集气瓶④药匙⑤玻璃棒⑥水槽⑦量筒,现配制含溶质x%的食盐水,应用到的仪器是〔〕A.①②③④B.①④⑥⑦C.①②④⑤⑦D.②③④⑤⑦11.现有三种物质组成的混合物,他们的性质如下表:物质状态溶于水的情况溶解度受温度影响I固体不溶于水──Ⅱ固体溶于水较小Ⅲ固体溶于水较小要将此固体混合物别离,不需要采用的方法是〔〕A.过滤B.蒸馏C.结晶D.冷却饱和溶液12.某氯化钠溶液中,氯化钠的质量分数为20%,那么配制时,在100g水中需溶解氯化钠〔〕g g g g13.把40g20%的氯化铵溶液与60g30%的氯化铵溶液混合,混合后的溶液中氯化铵的质量分数应〔〕A.大于30%B.小于20%C.等于25%D.在20%~30%之间画龙点睛1.右图中A、B、C分别表示三种物质的溶解度曲线。
初三溶液测试题及答案

初三溶液测试题及答案一、选择题1. 溶液的浓度是指溶质的质量与溶液的质量之比,这种说法正确吗?A. 正确B. 不正确正确答案:B2. 将一定量的盐溶解在一定量的水中,所得溶液的体积会等于溶质和溶剂的体积之和吗?A. 会B. 不会正确答案:B3. 溶液的均一性指的是什么?A. 溶液中各部分的组成完全相同B. 溶液的颜色分布均匀C. 溶液的密度分布均匀正确答案:A4. 当溶液中溶质的浓度达到饱和状态时,继续加入溶质会如何?A. 溶质会溶解B. 溶质会沉淀C. 溶质会悬浮正确答案:B5. 溶液的浓度可以用质量分数来表示,质量分数的计算公式是什么?A. 溶质质量/溶剂质量B. 溶质质量/溶液质量C. 溶剂质量/溶质质量正确答案:B二、填空题6. 溶液是由至少两种物质组成的均一、________的混合物。
答案:稳定的7. 饱和溶液是指在一定温度下,溶质在溶剂中达到最大溶解度的溶液,此时溶液为________。
答案:饱和状态8. 溶液的酸碱性可以用pH值来表示,pH值小于7表示溶液呈________性。
答案:酸性9. 溶液的稀释可以通过增加溶剂的量来实现,但溶质的质量________。
答案:不变10. 溶液的浓度越高,其渗透压________。
答案:越大三、简答题11. 为什么在配制溶液时,需要使用量筒来量取溶剂?答案:使用量筒可以准确量取一定体积的溶剂,保证溶液的浓度准确无误。
12. 什么是溶液的饱和度?请举例说明。
答案:溶液的饱和度是指在一定温度下,溶剂对溶质的最大溶解能力。
例如,20°C时,100克水中最多能溶解36克食盐,此时溶液达到饱和状态。
四、计算题13. 某溶液中溶质的质量分数为10%,若要配制100克的溶液,需要多少克的溶质?答案:首先,根据质量分数的定义,溶质的质量 = 溶液质量× 质量分数。
因此,需要的溶质质量 = 100克× 10% = 10克。
14. 如果在上述溶液中再加入10克的溶质,溶液的总质量变为多少?质量分数变为多少?答案:加入溶质后,溶液的总质量变为 100克 + 10克 = 110克。
鲁教版(五四制)九年级全一册第一单元溶液单元测试

第三单元溶液一、单选题(本大题共18小题,共36.0分)1.以下属于溶液,且溶质是单质的是()A.碘酒B.液态氧C.泥水D.稀盐酸2.水和溶液与我们的生活生产息息相关。
下列有关说法中,不正确的是()A.肥皂水可以区分硬水和软水B.洗涤剂除去油污的原理是将油污溶解C.溶液是均一、稳定的混合物D.饱和溶液不一定比不饱和溶液浓度大3.用溶质质量分数为49%的浓硫酸20mL (密度为1.84g•mL-1)配制溶质质量分数为10%的硫酸溶液,下列说法正确的是()A.应量取的水的体积为180mLB.量取浓硫酸时俯视读数,则所得溶液的质量分数小于10%C.实验中需要仪器有:烧杯、相应规格的量筒、玻璃棒D.装瓶时不小心洒漏一部分溶液,则瓶中硫酸溶液浓度小于10%4.实验室配制50g溶质质量分数为15%的氯化钠溶液。
下列说法不正确的是()A.计算:需氯化钠的质量为7.5g,需要水的体积为42.5mLB.称取氯化钠:托盘天平未经调零即用来称取氯化钠固体C.量取水:用规格为50mL的量筒量取所需体积的水D.把配制好的氯化钠溶液转移到指定的容器中,贴上标签备用5.下列有关溶液的说法中,正确的是()A.溶液都是无色透明的液体B.溶液是均一、稳定的混合物C.将NaCl放入植物油中搅拌,能形成溶液D.将40%的NaOH溶液均分成两份,每份溶液的溶质质量分数都为20%6.下列关于水的说法中不正确的是()A.水是一种常用的溶剂B.海水、湖水是混合物,蒸馏水是纯净物C.农业生产中不合理施用农药、化肥会对水体造成污染D.电解水生成了氢气和氧气,因此,水是由氢气和氧气组成的7.归纳推理是学习化学的重要方法之一。
下列有关事实和推理得到的结论合理的是()选项事实结论A二氧化锰对氯酸钾分解和过氧化氢分解均有催化作用不同的反应有时可以使用同一种物质作催化剂B溶液是均一、稳定的液体均一、稳定的液体都是溶液C C与O2反应能放出大量的热C与O2不需要任何条件就可以发生反应DAl在常温下就能与O2发生发应,Fe在常温下几乎不与O2反应Al的抗腐蚀性能比Fe弱A.AB.BC.CD.D8.为了探究物质在溶解时溶液温度的变化,小倩设计了如图所示的实验装置。
九年级化学---溶液单元测试题(含答案)

九年级化学---溶液单元测试题(含答案)九年级化学---溶液单元测试题(含答案)一、选择题:(本题有12小题,每小题2分,共24分。
每小题只有一个选项符合题意)1.下列对关于溶质类属和溶液的名称正确的是()A。
混合物、碘酒B。
单质、液态氢气C。
化合物、生理盐水D。
氧化物、白酒2.下列说法正确的是()A。
水和冰块的共存物是悬浊液B。
凡均一、稳定、透明、澄清液体一定是溶液C。
一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液D。
在泥水里,泥是溶质,水是溶剂3.要从高锰酸钾加热完全分解后的剩余物中回收二氧化锰固体,有下列操作可选择:①过滤;②烘干;③加水溶解;④水洗;⑤蒸发结晶。
其操作顺序正确的是()A。
①→②→③→④B。
③→②→①→⑤C。
③→①→④→②D。
③→①→⑤→④4.在一定温度下,向不饱和的NaNO3溶液中逐渐加入NaNO3晶体,在此变化过程中,溶液里溶质质量分数(ω)与时间(t)的关系正确的是()A。
ω随t的增加而增加B。
ω随t的增加而减小C。
ω先增加后减小D。
ω先减小后增加5.某医院需要配制生理盐水(质量分数为0.9%)1000g,下列配制过程正确的是()A。
只需要托盘天平和量筒两种仪器B。
用托盘天平称取9g氯化钠C。
配制生理盐水可以用粗盐D。
用量筒量取1000mL水6.要配制一定质量分数的NaOH溶液,正确的操作步骤是()A。
计算、量取、溶解B。
称量、溶解、搅拌C。
计算、称量、溶解D。
称量、加水、溶解7.向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低了些,左边液面上升了些,则加入的物质是()A。
硝酸铵B。
生石灰C。
活性炭D。
烧碱8.有W(g)浓度为15%的硝酸钾溶液,若将其浓度变为30%,可以采用的方法是()A。
蒸发掉溶剂的1/2B。
加入3/20W(g)的硝酸钾C。
蒸发掉W/2(g)溶剂D。
加入5/14W(g)硝酸钾9.下列有关溶液的说法中,正确的是()A。
初中化学鲁教版(五四制)九年级全册第一单元 溶液第一节 溶液的形成-章节测试习题(3)

章节测试题1.【答题】把少量下列物质分别放到水里,充分搅拌后,可以得到乳浊液的是()A.面粉B.植物油C.高锰酸钾D.蔗糖【答案】B【分析】本题考查乳浊液的概念。
【解答】乳浊液指的是小液滴分散到液体里形成的混合物。
面粉放到水里形成悬浊液;植物油放到水里形成乳浊液;高锰酸钾和蔗糖放到水里形成溶液。
故选B。
2.【答题】下列关于溶液的说法:①溶质只能是固体;②溶剂一定是水;③一种溶液中只含有一种溶质;④溶液是无色的纯净物。
其中错误的是()A.①②③④B.①②③C.②③④D.①③④【答案】A【分析】本题考查溶液的形成。
【解答】溶质可以是固体、气体或液体,如乙醇溶于水;酒精也可以做溶剂,如碘酒是碘溶于酒精形成的;一种溶液中可以有多种溶质;溶液并不一定是无色的,如硫酸铜溶液是蓝色的;溶液是一种物质分散到另一种物质里形成均一稳定的混合物。
故选A。
3.【答题】下列关于生理盐水的说法中,错误的是()A.生理盐水的溶剂是水B.各部分一样,体现了溶液成分的均一性C.饮用生理盐水放置一段时间不会分层D.水分子是保持NaCl性质的最小微粒【答案】D【分析】本题考查溶液的形成。
【解答】A、生理盐水是0.9%的氯化钠溶液,溶剂是水;B、溶液各部分的组成相同,说明溶液是均一的;C、溶液具有稳定性,所以生理盐水放置一段时间不会分层;D、由分子构成的物质,分子是保持物质化学性质的最小微粒。
水分子是保持水分子化学性质的最小微粒。
故选D。
4.【答题】锌与足量的盐酸反应后的液体和少量二氧化碳通入澄清石灰水后的液体分别是()A.乳浊液、溶液B.溶液、乳浊液C.悬浊液、乳浊液D.溶液、悬浊液【答案】D【分析】本题考查乳浊液、悬浊液的概念。
【解答】锌与足量的盐酸反应生成氯化锌,氯化锌溶于水形成的均一的、稳定的混合物,属于溶液;将少量二氧化碳气体通入足量的澄清石灰水后,二氧化碳和氢氧化钙反应能生成不溶于水的碳酸钙,碳酸钙悬浮在液体中形成悬浊液。
九年级化学专题测试---溶液(一)(含答案)

3.2 溶液3.2.1物质的溶解性一、选择题1、列物质属于溶液的是()A、液溴B、牛奶C、无水酒精D、含硝酸钾的食盐水2、下列各组物质,前一种物质分散到后一种物质中形成乳浊液的是()A.油脂汽油B.泥土水C.碘酒精D.精制油水3、对溶液的基本特征叙述错误的是()A、条件一定时,溶液长期放置,溶质不会从溶液里分离出来B、溶液各部分的浓度和密度完全相同C、凡是溶液都是澄清透明的无色液体D、溶液各部分的物理、化学性质相同4、老师要同学按要求进行以下四组实验,其中所得混合物一定为溶液的是()A、二氧化碳通入水中B、生石灰放入水中C、二氧化碳通入石灰水中D、菜油放入水中5 下列物质不属于结晶水合物的是()A、食盐B、石碱C、胆矾D、明矾6、下列液体不属于溶液的是()A、自来水B、冰水C、汽水D、白酒7、下列关于溶液的叙述错误的是()A、碘酒溶液中碘是溶质酒精是溶剂B、溶液中各部分的性质是相同的C、一种溶剂只能溶解一种溶质D、食盐溶液与蔗糖溶液混合后仍是溶液8、下列家庭常用物质中,属于纯净物的是()A、牛奶B、酱油C、蒸馏水D、葡萄酒9、下列常见的医用溶液中,溶剂不.是.水的是()A、葡萄糖注射液B、生理盐水C、消毒酒精D、碘酒二、填空题1、医用酒精中,酒精和水的质量比为3:1,该医用酒精的溶剂是。
2、一种或一种以上的物质分散在另一种物质中,形成的、的混合物叫溶液。
3、溶液是由组成的。
其中能溶解其它物质的物质叫,被溶解的物质叫。
溶质和溶剂是相对的,通常情况下不指明溶剂时,就是溶剂。
4、溶液的特征:,。
5、以下的分散系分别是(填入A、B、C)A.乳浊液 B. 悬浊液 C. 溶液牛奶()泥浆水()澄清石灰水()菜油放入水中()粉笔灰放入水中()面粉放入水中()6、.指出下列溶液中的溶质和溶剂(1)生理盐水(2)碘酒(3)75%的消毒酒精(4)硝酸银溶液(5)4 克汽油和2 克酒精混合形成的溶液7.填写下列溶液中各溶质的化学式(1)澄清石灰水(2)硝酸银溶液(3)硫酸钾溶液(4)氯化铝溶液(5)氯化钡溶液(6)氯化锌溶液(7)碘酒(8)生理盐水三、简答题学完溶液知识后,小松回家用蔗糖、碳酸钙、植物油、洗涤剂、水相互混合做了几个小实验。
2020届中考化学专题复习《溶液》测试试题(含答案)

B.将c的饱和溶液变为不饱和溶液,可采用降温的方法
C.t2℃时,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液
D.将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
12.如图为甲、乙两种固体物质的溶解度曲线,下列有关说法中错误的是
(2)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:①加入C物质;②恒温蒸发溶剂;③__________________;
(3)t3℃时,将等质量的A、B、C三种物质放入到一定量水中,均恰好配成饱和溶液,所得溶液的质量由大到小的顺序是_______________。
三、推断题
21.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
A.M的溶解度受温度影响较大
B.20℃时,M、N的溶解度相同
C.40℃时,将35gM加入50g水中所得溶液的质量为85g
D.40℃时,M、N饱和溶液溶质质量分数大小关系是M>N
7.一定温度下,向饱和的硫酸铜溶液中(底部还留有硫酸铜晶体)加入一定量的水,所得溶液与原溶液相比,一定正确的是()
A.溶质的质量增加B.所得溶液是不饱和溶液
温度(℃)
20
40
50
60
70
80
溶解度(g/100g水)
31.6
63.9
145
110
140
169
请根据表中的数据,在坐标图中描点、绘制符合硝酸钾溶解度变化规律的曲线。_____
可知:硝酸钾的溶解度随温度升高而_____(选填“增大”或“减小”);60℃时,将60g硝酸钾固体加入50g水中,所形成的溶液为_____溶液(填写“饱和”或“不饱和”),所得溶液的溶质质量分数为_____(精确到0.1%)。下图是有关硝酸钾溶液的实验操作及变化情况,已知溶液①到溶液②的过程中,溶液质量保持不变,
九年级化学册 第一单元 溶液同步测试 试题
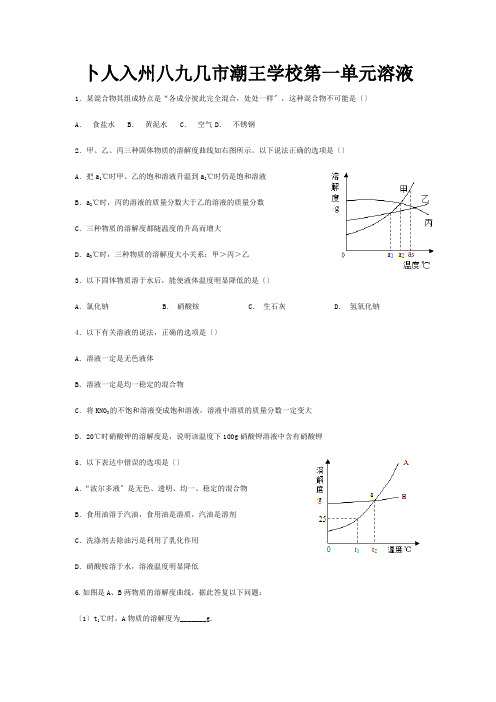
卜人入州八九几市潮王学校第一单元溶液1.某混合物其组成特点是“各成分彼此完全混合,处处一样〞,这种混合物不可能是〔〕A.食盐水B.黄泥水C.空气D.不锈钢2.甲、乙、丙三种固体物质的溶解度曲线如右图所示。
以下说法正确的选项是〔〕A.把a1℃时甲、乙的饱和溶液升温到a2℃时仍是饱和溶液B.a2℃时,丙的溶液的质量分数大于乙的溶液的质量分数C.三种物质的溶解度都随温度的升高而增大D.a3℃时,三种物质的溶解度大小关系:甲>丙>乙3.以下固体物质溶于水后,能使液体温度明显降低的是〔〕A.氯化钠B.硝酸铵C.生石灰D.氢氧化钠4.以下有关溶液的说法,正确的选项是〔〕A.溶液一定是无色液体B.溶液一定是均一稳定的混合物C.将KNO3的不饱和溶液变成饱和溶液,溶液中溶质的质量分数一定变大D.20℃时硝酸钾的溶解度是,说明该温度下100g硝酸钾溶液中含有硝酸钾5.以下表达中错误的选项是〔〕A.“波尔多液〞是无色、透明、均一、稳定的混合物B.食用油溶于汽油,食用油是溶质,汽油是溶剂C.洗涤剂去除油污是利用了乳化作用D.硝酸铵溶于水,溶液温度明显降低6.如图是A、B两物质的溶解度曲线,据此答复以下问题:〔1〕t1℃时,A物质的溶解度为_______g.〔2〕a点的含义是____________________。
〔3〕溶解度受温度影响较小的物质是___________。
〔4〕从A、B的混合物中别离A物质,一般采用_________的方法。
7.以下关于溶液的表达正确的选项是〔〕A.溶液一定是均一、稳定、无色、透明的液体B.溶液中各局部性质一样C.某物质的饱和溶液就是不能再溶解任何物质的溶液D.硝酸铵固体溶于水形成溶液时仅发生扩散吸热的过程8.右图是甲、乙、丙三种物质的溶解度曲线,以下表达不正确的选项是〔〕A.在t2℃时,把甲放入50g水中得到甲的饱和溶液,且溶液的溶质质量分数为50%B.t1℃时三种物质的溶解度大小关系是乙>甲=丙C.将t2℃时等质量的三种物质的饱和溶液分别降至0℃,析出甲最多D.将丙的饱和溶液变为不饱和溶液,可以采用降温的方法9.20℃时,取甲、乙、丙、丁四种物质各20g,分别参加到四个盛有50g水的烧杯中,充分溶解,情况如表〔温度保持20℃〕,以下说法正确的选项是〔〕物质甲乙丙丁未溶解固体的质量/g 2 0A.所得溶液一定都是饱和溶液B.溶质质量分数最大的是丙溶液C.所得四种溶液的质量关系为:甲=乙=丙=丁D.20℃时四种物质溶解度的关系为:丁>甲>乙>丙10.右图为硝酸钾和氯化钠两种物质的饱和溶液的质量分数随温度变化的曲线,M、N分别是50℃时硝酸钾和氯化钠质量分数随温度变化曲线上的点。
九年级化学册 第一单元 溶液测试卷 试题

第一单元溶液单元测试卷制卷人:歐陽文化、歐陽理複;制卷時間:二O二二年二月七日一、单项选择题1.将以下四种物质分别放入水中,能形成溶液的是〔〕A.泥土 B.氢气 C.蔗糖 D.汽油2.一种抗生素为粉末状固体,每瓶含,注射时应配成质量分数为20%的溶液,那么使用时每瓶至少需参加蒸馏水〔〕A. 1.5mL B.2mL C.3mL D.4mL100mL20%的NaCl溶液倒出10 mL后余下的溶液与最初的溶液相比〔〕A.溶质的质量分数变小了B.溶质和溶剂的比例变小了C.溶质的质量变少了D.B和C都正确4.以下关于溶液的说法正确的选项是〔〕A.溶液都是无色的中可能含有多物质C.稀溶液一定是不饱和溶液D.均一、稳定的液体一定是溶液5.有些游泳池中的水呈蓝色,是因为参加了一种能杀菌消毒的物质.这种物质可能是〔〕A.硫酸亚铁B.食盐C.硫酸铜D.硫酸铁6.在温度不变的条件下,以下欲使溶质的质量分数变为原来2倍的方法,最可行的是〔〕A.将20g硝酸钾饱和溶液蒸发掉10g水B.将20g硝酸钾不饱和溶液蒸发掉10g水C.在10g10%的硝酸钾溶液中,参加5g40%的硝酸钾溶液D.将10g硝酸钾不饱和溶液中参加10g硝酸钾固体7.在一定温度下,向盛有100克蔗糖溶液的烧杯中再参加5克蔗糖,充分搅拌后,一定保持不变的是〔〕A.溶质的质量 B.溶液的质量 C.溶质的质量分数 D.蔗糖的溶解度8.如下图,翻开止水夹,将液体A滴入试管②中与固体B接触.假设试管①中的导管口有较多气泡产生,那么液体A和固体B的组合不可能是〔〕A.双氧水和二氧化锰 B.水和生石灰 C.水和氢氧化钠 D.水和硝酸铵9.海水淡化可采用膜别离技术,如下图,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成分变化进展分析,正确的选项是〔〕A.溶质质量增加 B.溶液质量不变C.溶剂质量减少 D.溶质质量分数不变10.某溶液恒温蒸发掉局部溶剂后,无晶体析出,以下说法正确的选项是〔〕A.原溶液可能是饱和溶液B.剩余的溶液一定是不饱和溶液C.剩余的溶液可能是饱和溶液D.剩余的溶液与原溶液中的溶质的质量分数可能相等11.对于多数固体溶质的不饱和溶液,要使之成为饱和溶液的方法有〔〕①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂A.①③⑤B.②③④C.①②③D.②③⑤12.把某温度下m g的硝酸钾不饱和溶液恒温蒸发水分,直到有少量晶体析出。
九年级化学册 第一单元 溶液复习习题 试题

第一单元溶液制卷人:歐陽文化、歐陽理複;制卷時間:二O二二年二月七日1.以下物质溶于水形成溶液后,以离子形式存在于溶液中的是〔〕2.以下说法错误的选项是〔〕A. 用硬水洗衣服不如用软水洗得干净B. 洗涤剂能除去油污,是因为它具有乳化作用C. 用明矾净水是由于明矾溶于水后生成的胶状物有吸附作用D. 25 m3石油气压缩后可装入0.024 m3的钢瓶中,是因为分子大小发生了改变3.一定温度下,假设将一定质量的硝酸钾不饱和溶液变为饱和溶液,那么〔〕4.海水淡化可采用膜别离技术,如下图,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成分变化进展分析,正确的选项是〔〕A.溶质质量增加 B.溶液质量不变C.溶剂质量减少 D.溶质质量分数不变5.把少量以下物质分别放入水中,充分搅拌,可以得到溶液的是〔〕A.硝酸钾B.橄榄油C.面粉 D.泥土6.以下说法正确的选项是〔〕A.但凡均一的、稳定的液体一定是溶液B.洗涤剂可以洗涤油污是因为洗涤剂可以溶解油污C.饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液D.5g某物质完全溶于水配成100g溶液,所得溶液的溶质质量分数一定是5%7.以下溶液中,溶剂不是水的是〔〕A.蔗糖溶液 B.生理盐水 C.碘的酒精溶液 D.稀盐酸8.小刚同学做自制汽水的家庭小实验,可是家里没有冰箱,为了使自制的汽水变得冰凉可口,他想到可以从集上购置一种商品来产生制冷效果,他应该买的是〔〕9.一定温度下,向图I烧杯中参加一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,以下判断一定正确的选项是〔〕A.所得溶液是饱和溶液B.溶质的质量分数变大C.溶质的质量增加D.溶质的溶解度变大10.某温度下,在100g质量分数为20%的KNO3不饱和溶液甲中参加10gKNO3固体,恰好得到饱和溶液乙,以下说法正确的选项是〔〕A.该温度下,KNO3的溶解度为30gB.乙溶液的质量分数为30%C.降低温度,可以使甲溶液变成饱和溶液D.升高温度,甲、乙两溶液的质量分数都增大11.高氯酸钾〔KClO4〕可用作HY推进剂,其溶解度如表.以下说法正确的选项是〔〕温度/℃20 40 60 80溶解度/gA.高氯酸钾的溶解度随温度升高而减小B.20℃时,将2g高氯酸钾溶于98g水可配制2%的溶液C.60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%D.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象12.甲、乙两种物质的溶解度曲线如下图,以下说法正确的选项是〔〕A.甲的溶解度大于乙的溶解度B.两种物质的溶解度都随温度升高而增大C.t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等D.t2℃时,甲的饱和溶液溶质质量分数为50%13.甲物质的溶解度〔S〕随温度〔t〕变化曲线如下图,以下说法正确的选项是〔〕A.20℃时,甲易溶于水B.60℃C.将80℃时甲的溶液降温至40℃,一定析出甲晶体D.90℃时,在50g水中参加甲,充分搅拌后得到饱和溶液14.甲、乙两种物质的溶解度曲线如下图.以下说法中正确的选项是〔〕A.甲物质的溶解度大于乙物质的溶解度B.甲和乙的饱和溶液从t1℃升温到t2℃时都有晶体析出C.t1℃时,甲和乙各30g分别参加100g水中,充分溶解,均形成饱和溶液D.t2℃时,甲和乙的饱和溶液各100g其溶质的质量相等15.如图是不含结晶水的a、b、c 三种物质的溶解度曲线,以下说法正确的选项是〔〕A.t2℃时,将50g a物质参加到50g 水中充分搅拌,得到100g a的饱和溶液B.用等质量的a、b、c 三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液>b溶液>a溶液C.将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液M中溶质的质量分数的大小关系是:b>a=cD.将t2℃时a、b 两种物质的饱和溶液降温到t1℃时,析出晶体的质量:a>b16.如图是甲、乙、丙三种物质的溶解度曲线,以下说法中正确的选项是〕A.P点表示甲、丙两种物质的饱和溶液质量相等B.t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液C.t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4D.将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质17.甲、乙两种物质的溶解度曲线如下图,以下说法正确的选项是〔〕A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液B.乙的溶解度随温度的升高而增大C.一样温度时,甲的溶解度一定大于乙的溶解度D.分别将甲、乙的饱和溶液从a2℃降至a1℃时,所得溶液中溶质的质量分数相等18.如图是甲、乙、丙三种物质的溶解度曲线,以下表达正确的选项是〔〕A.t1℃时,等质量的甲、丙溶液中所含溶质的质量分数为丙>甲B.t2℃时,20g丙溶解于50g水中能形成70g溶液C.分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙D.假设要将组成在N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法19.列表和作图是常用的数据处理方法.结合所绘图表判断以下说法正确的选项是〔〕氢氧化钠、碳酸钠分别在水、酒精中的溶解度氢氧化钠碳酸钠20℃40℃20℃40℃水 109g 129g 49g酒精40g 不溶不溶A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观B.由表格数据可知,物质的溶解度只受温度影响C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成20.海水晒盐提取食盐晶体后留下的母液叫卤水,卤水中除含NaCl外,还含有MgCl2、MgSO4等物质.它们的溶解度曲线如右图所示.以下说法正确的选项是〔〕A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgSO4B.三种物质的溶解度都随温度升高而不断增大C.将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO4D.20℃时,向40gNaCl固体和40gMgCl2固体中分别参加100g水充分溶解后,两种溶液均能到达饱和状态21.如图是甲、乙、丙三种固体物质的溶解度曲线.以下表达正确的选项是〔〕A.t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲B.t2℃时,20g丙能溶解于50g水中形成70g溶液C.假设要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法D.t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙22.用硫酸铜进展如下图的实验,对所得溶液的分析正确的选项是〔〕A.三个溶液中溶质溶解度一样 B.②溶液是不饱和溶液C.③溶液颜色最深 D.温度不同,无法比拟①③溶液的溶质质量分数23.向100g质量分数为20%的NaCl溶液中参加3gNaCl固体和12g水,使其完全溶解,所得溶液中NaCl的质量分数是〔〕A.20% B.22.5% C.25% D.30%24.如下图,将少量液体X参加到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,符合题意的是〔〕①②③④X 双氧水水水水Y 二氧化锰氯化钠氢氧化钠硝酸铵A.①② B.①③ C.①③④D.②③④25.根据表中氯化钠和硝酸钠部分溶解度数据分析,答复以下问题.温度/℃0 10 20 30 40 50 60 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3溶解度/gKNO3110 〔1〕10℃时,氯化钠的溶解度是______g.〔2〕硝酸钾的溶解度随温度的升高而______,与硝酸钾相比拟,氯化钠的溶解度受温度变化影响______〔填“较大〞或者“较小〞〕.〔3〕20℃时,在100g水中参加40g硝酸钾,充分搅拌后,将溶液温度升高到30℃〔不考虑水分蒸发〕,所得溶液是______〔填〞饱和溶液“或者〞不饱和溶液“〕.〔4〕在20℃~30℃的某温度时,氯化钠和硝酸钾的溶解度〔x〕一样,x的取值范围是______.26.甲、乙、丙三种固体的溶解度曲线如下图,据图答复:①30℃时,丙的溶解度是______;②50℃时,在100g水中放入50g乙物质,充分搅拌后所得溶液的溶质质量分数为______.〔计算结果保存至0.1%〕.③假设将20℃时甲、乙、丙三种物质的饱和溶液升温至40℃〔不考虑水的蒸发〕,可析出晶体的是______.④将50℃时甲、乙、丙三种物质的饱和溶液均降温至10℃,所得溶液的溶质质量分数从大到小的顺序是______.〔2〕常温下欲配置100g溶质质量分数为10%的乙溶液,操作如下图.请答复以下问题:①图中操作有错误的选项是______〔填对应字母〕.②量取水时,假设采用仰视的方法读数,会导致所配溶液的溶质质量分数______〔填“偏大〞、“偏小〞或者“无影响〞〕27.如图是a、b、c三种固体物质〔均不含结晶水〕的溶解度曲线.〔1〕t1℃时,a、b、c三种固体物质的溶解度的大小关系是______.〔2〕t2℃,将30g物质a 参加到50g水中,形成溶液的质量为______g.〔3〕t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,仍为饱和溶液的是______.〔4〕在t2℃时,M点的a、b两种溶液的溶质质量分数大小关系为:a______b〔填“>〞或者“<〞或者“=〞〕28.根据如表答复以下问题.温度〔℃〕 20 40 50 60 80溶解度〔g/100g水〕 NaCl 37.3 38.4 NH4Cl 45.8 50.4 55.2 65.6 KNO363.9 85.5 110 169①20℃时,溶解度最大的物质是______②50℃时,100g水中最多溶解NaCl______g③量筒的部分示意见图,量取水时应沿______视线〔选填“a〞或者“b〞〕进展读数,______视线〔选填“a〞或者“b〞〕对应的读数较大.④A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体.Ⅰ.A溶液为______〔选填“饱和〞或者“不饱和〞〕溶液Ⅱ.对以上过程的分析,正确的选项是______〔选填编号〕a.A到B的过程中,溶质质量没有改变b.B中溶质与溶剂的质量比为169:100c.开场析出KNO3固体的温度在60℃至80℃之间d.A溶液的质量等于222g.29.如图是几种物质的溶解度曲线,根据图示答复:〔1〕在图1中,t2℃时甲物质的溶解度为______g.〔2〕甲、丙在______℃时溶解度一样.〔3〕图1中,假设将t3℃时等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得三种溶液的溶质质量分数由大到小的顺序是______〔析出晶体都不含结晶水〕.〔4〕气体的溶解度也有一定的变化规律,不同的温度下,氧气的溶解度随压强而变化的情况如图2所示,假设t1℃对应的温度为40℃,那么t2对应的温度______〔填字母序号〕.A.小于40℃B.等于40℃C.大于40℃D.无法确定.30.根据图中A、B、C三种固体的溶解度曲线答复:〔1〕在某一温度时,A、B两饱和溶液的溶质质量分数相等,此温度为______℃;〔2〕在t3℃时,将30gA物质充分溶解在50g水中,所得溶液的质量为______g;〔3〕要使C的饱和溶液变为不饱和溶液,可采用的一种方法是______;〔4〕将t3℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液的溶质质量分数由大到小的顺序是______.制卷人:歐陽文化、歐陽理複;制卷時間:二O二二年二月七日。
九年级化学溶液单元测试题

九年级化学溶液单元测试题Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】一、选择题1.一种“即食即热型快餐”适合外出旅行时使用。
其内层是用铝箔包裹并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是()A.硝酸铵与水B.生石灰与水C.熟石灰与水D.氯化钠与水2.下列有关溶液的叙述正确的是()A.一杯食盐水,下部分比上部分咸B.温度一定时,析出硝酸钾晶体的溶液未必是硝酸钾的饱和溶液C.物质溶于水时,常使溶液的温度发生改变D.75%的医用酒精消毒液,溶剂是酒精3.许多同学喜欢吃家庭腌制的小菜,腌制小菜的一般方法是:将食盐、香料等一起放入水中煮制得浓盐水,盐水冷却后放入洗净待腌制的鲜菜,腌制过程中还要不断打开缸盖晒缸并及时补充食盐,一段时间后,即得成品小菜。
若室温时食盐的溶解度为36g。
关于小菜腌制过程中的下列说法,错误的是()A.煮制浓盐水时,10kg水最多可得到浓盐水13.6kgB.腌菜的过程中,原来的浓盐水会逐渐变稀C.晒缸的目的一是防止腌菜腐败变质,二是促使水分蒸发以保持盐水的浓度D.补充食盐的目的是保持盐水的浓度,以利于食盐往蔬菜中渗透4.一定温度时,向密闭容器里的食盐饱和溶液中,加入5克食盐晶体。
经过一段时同后()A.饱和溶液的质量增大B.饱和溶液的浓度增大C.晶体的质量不变D.晶体的质量减小5.某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g 晶体,再恒温蒸发掉10g水,析出了3g晶体,则下列说法正确的是()A.原溶液在t℃时一定是不饱和溶液B.原溶液一定是稀溶液C.最后剩余的溶液一定比原溶液稀D.最后剩余溶液的溶质质量分数比原溶液的溶质质量分数小6.下列有关溶液的说法中,正确的是()A.固体物质的溶解度都随温度的升高而增大B.一定温度下,饱和溶液增加溶剂一定变为不饱和溶液C.将30 g硝酸钾投入到70 g水中,所得溶液质量一定是100 gD.5 g食盐完全溶于100 g水中,所得溶液中溶质的质量分数为5% 7.将20℃时的硝酸钾饱和溶液升温至50℃(不考虑水分蒸发),一定发生改变的是()A.溶剂的质量B.溶液的质量C.硝酸钾的溶解度D.溶质的质量饱和溶液中加入1gNaCl固体,下列叙述不正确的是() 8.在25℃时向100gKNO3A.NaCl固体不能溶解B.NaCl固体能溶解C.所得溶液的质量是101gD.溶液中溶剂的质量不变9.现有W克溶质的质量分数为15%的A溶液,欲使其溶质的质量分数增至30%,可采取的方法有()A.蒸发掉溶剂的二分之一B.蒸发掉0.5Wg溶剂C.加入0.15WgAD.加入3gA10.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。
九年级化学册 第1单元 溶液测试 试题

第一单元溶液测试题一.选择题,(每一小题只有一个答案3×12=36分)1.从溶液的定义看,以下可以看成溶液的是〔〕A.清新的空气B.尘土飞扬的空气C.黄河水D.大雾弥漫的空气2.以下物质分别加人水中充分搅拌,能得到蓝色溶液的是〔〕。
A.蔗糖B食盐C.硫酸铜D.面粉3.以下有关溶液的说法中正确的选项是()A.但凡均一丶稳定的液体就是溶液B、从溶液中取出局部溶液后,溶质的质量分数减小C.溶液的状态一定是液体D、溶液中的溶质可以是一种或者两种,溶剂只是一种4.现有20℅的硫酸50g,把它配成10℅的硫酸,应选用的一组仪器是()A.托盘天平、烧杯、玻璃棒B.量筒、托盘天平、烧杯C.量筒、烧杯、玻璃棒D.量筒、玻璃棒6.水溶液的特征是()①均一②稳定③混合物④无色⑤透明⑥化合物A.①②③④⑤⑥B.①②④⑤⑥C.④⑤⑥D.①②③“陈醋〞消费过程中有一步称为“冬捞夏晒〞.是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以进步醋的品质假设用醋酸的质量分数为3﹪的半成醋,消费500g﹪的优级醋,过程中醋酸没有损失,捞出的冰和蒸发的水的总质量为〔〕A、500gB、400gC、200gD、100g8.要配制50g溶质质量分数为10%的氢氧化钠溶液,以下操作不正确的选项是〔〕A.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签B.量取45mL水时,平视凹液面的最低处读数C.为加快固体溶解,用玻璃棒搅拌溶液D.将5g氢氧化钠固体直接放在天平的托盘上称量9.各种洗涤剂广泛进入人们的生活中,以下洗涤剂具有乳化功能的是〔〕A、用汽油去除衣服上的油污B、用洗洁精清洗餐具上的油污C、用水洗去盘子中的水果汁D、用醋洗去水壶的水垢10.用氯化钠固体配制100g质量分数为5%氯化钠溶液,以下仪器中需要〔〕。
A.②④⑥⑦B.①④⑤⑥C.①③⑤⑦D.①③④⑥11.用浓盐酸配制一定质量分数的稀盐酸,假设在用量筒量取盐酸时仰视刻度,而在量取水时俯视刻度.那么所得稀盐酸中溶质的质量分数比要求配制的稀盐酸的溶质质量分数()A.偏低B.偏高C.一样D.无法判断12.在25℃时,向100gKNO3饱和溶液中参加1gNaCl固体,以下表达正确的选项是①NaCl固体不溶解②KNO3在溶液中所占的质量分数不变③NaCl固体能溶解④KNO3的质量分数变小A.①②B.③④C.②③D.①④二.填空题(26分)13.(4分)分别指出以下各种溶液里的溶质和溶剂:稀硫酸、碘酒、澄清的石灰水、75%的酒精、14.(3分)在餐桌上,当我们发现某种汤太淡时,通常做法是向汤中参加。
