2.2共价键与分子的空间构型
化学键与分子的空间构型

化学键与分子的空间构型化学键是化学中的一个重要概念,它是描述原子之间结合的力。
在化学键的形成中,电子在原子之间转移、共享或重排,从而形成化学键。
通过化学键,原子可以组合成分子,并且这些分子的三维空间构型对它们在化学反应中的性质和活性起着至关重要的影响。
分子的空间构型是指分子中原子的空间排列方式。
原子之间的化学键的性质决定了分子的空间构型。
例如,共价键是由共享电子形成的一种连接形式。
共价键的键长和键角对分子的结构起着重要作用。
不同键长和键角会导致分子的不同构型。
例如,氨分子(NH3)和水分子(H2O)中的键角不同,从而使得氨分子呈现三角锥形构型,而水分子呈现微弯的构型。
除了共价键,离子键也是分子空间构型的一个重要因素。
离子键是由原子之间的电荷吸引力形成的。
正离子和负离子通过电荷吸引力相互结合形成离子键。
离子键的键能较高,使得离子在晶体中排列有序。
这种有序排列决定了离子晶体的空间构型。
例如,氯化钠晶体中,钠离子和氯离子以菱形密堆积的方式排列,形成立方晶系的构型。
另一种常见的化学键类型是金属键。
在金属中,金属原子之间通过顺滑的电子云相互结合形成金属键。
由于金属键的性质,金属具有良好的导电性和导热性。
金属键的强度和金属原子之间的排列方式决定了金属的物理性质和力学性质。
例如,钢中的铁原子通过金属键排列有序,形成具有高强度和韧性的晶格结构。
还有一种特殊的化学键类型是氢键。
氢键是由氢原子与较电负的原子(如氮、氧、氟)之间的电荷吸引力形成的键。
氢键通常较强,但比共价键和离子键弱。
氢键在生物体系中起着重要的作用。
例如,DNA分子的螺旋结构就是由氢键稳定的,这使得DNA能够保存遗传信息。
化学键的性质和分子的空间构型是相互关联的。
化学键的类型和强度决定了分子的整体结构。
分子的空间构型会影响分子的性质和反应性质。
例如,如果一个分子具有线性构型,那么它的极性可能较强,从而影响溶解度和反应性。
此外,分子的空间构型还与分子之间的相互作用有关,从而影响化学反应的速率和选择性。
人教版化学选修三2.2《分子的立体构型(第2课时)分子的空间结构和价层电子对互斥理论》教学设计

第二章第二节分子的立体构造第 2 课时分子的空间构造与价层电子对互斥理论【学习目标】 1、能应用价层电子对互斥理论判断分子的空间构型。
【学习要点】σ键电子对、孤电子对和价层电子对的计算,VSEPR 模型【学习难点】分子立体构型的推测课前预习案一、价层电子对互斥理论(阅读课本 P37-38 达成填空)1、价层电子对互斥理论以为,分子的“立体构型”是的结果。
2、价层电子对是指;价层电子对 =+;( 1)σ键电子对数:可由确立。
比如,H2O的中心原子是______,构造式是 __________,有个σ键,故σ键电子对数是______;(2)中心原子上的孤对电子对数:依据公式 _______________________确立,此中 a 为,关于主族元向来说,价电子数等于;x 为;b 为;氢为 _____,其余原子等于。
阳离子: a 为中心原子的价电子数减去 _______________;阴离子:a为中心原子的价电子数加上(绝对值)。
2-的孤对电子数 =1/2(6+2-2*3 )=13比如: SO【预习检测】1、运用你对分子的已有的认识,达成以下表格,写出C、 H、N、O 的电子式,依据共价键的饱和性议论C、H、N、 O、F 的成键状况。
原子H C N O F 电子式可形成的共用电子对数讲堂研究案研究一:价层电子对空间构型(即VSEPR 模型)价层电子对互斥理论的基本内容:对AB n型的分子或离子,中心原子A 价层电子对(包含成键σ键电子对和未成键的孤对电子对)之间因为存在排挤力,将使分子的几何构型老是采纳电子对互相排挤最小的那种构型,以使相互之间斥力最小,分子系统能量最低、最稳固。
问题 1:请你依据价层电子对互斥理论的基本内容,总结出价层电子对的空间构型(即 VSEPR 模型)(利用牙签与橡皮泥模拟)空间构型价电子对数量234VSEPR 模型形形形问题 2:依据价层电子对互斥理论,计算出以下分子的中心原子含有的σ键电子对数、孤对电子数及价层电子数。
选修3第2章第2节第1课时 一些典型分子的空间构型

碳原子的其他杂化类型sp2杂化
栏目导航
↓
栏目导航
栏目导航
Hale Waihona Puke 目导航杂化轨道只能形成σ键 或容纳未成键的孤电 子对,不能形成π键
栏目导航
苯分子的空间构型
栏目导航
栏目导航
苯分子的空间构型 根据杂化轨道理论,形成苯分子时每个碳原子的价电子原子轨道发生 _s_p_2杂化(如 s、px、py),由此形成的三个 sp2 杂化轨道在同一平面内。这样, 每个碳原子的两个 sp2 杂化轨道上的电子分别与邻近的两个碳原子的 sp2 杂化轨道上的电子配对形成 σ 键,于是六个碳原子组成一个正六边形 的 碳环;每个碳原子的另一个 sp2 杂化轨道上的电子分别与一个氢原子的 1s 电子配对形成 σ 键。与此同时,每个碳原子的一个与碳环平面垂直的未参
一不变:轨道数目不变 3、只有原子形成分子时才会发生轨道杂化,单个原子是不会杂化的 4、只有能量相近的轨道才会相互杂化
栏目导航
如何确定某原子成键时的杂化类型?
ABn型分子或离子
杂化轨道数=中心原子 的价层电子对数
杂化类型
sp 1
sp 2
sp 3
中心原子的价层电
?
?
?
子对中数心原子采取s_p__2_杂化,形成的__分__子一定是平面__三__角形吗?
杂化轨道的数目
__2__
杂化轨道间的夹角 __1_8__0__°__
_3___ __1_2__0_°___
4____ 10__9_._5__°___
空间构型
__直__线__型___ 平_面__三___角__形___ 正四__面__体__型_____
实例
C O 2、C 2H 2
共价键与分子的空间构型

2.ClO2-、ClO3-、ClO4-中Cl都是以sp3杂 化轨道与O原子成键的,试推测下列微粒 的立体结构。 ClO2- ClO3- ClO4- V形
三角锥 正四面体
分子空间 构型 直线型 BeCl2 直 线 CO2 形 平面三角型 BF3 平面 三角 BCl3 形 正四面体 CH4 正四面体 NH3 三角锥形 H2O V形
化 学 家 鲍 林
想出一个好点子Leabharlann 最好办法,就是想出很多个点子惟一一位先后两次单独获得诺贝尔奖的科学家 鲍林
鲍林是著名的量子化学家,曾两次荣获诺贝尔奖(1954年化 学奖, 1962年和平奖),有很高的国际声誉。他提出了价键理论、 电负性、共振论,并把化学研究推进到生物领域。鲍林坚决反对 把科技成果用于战争,特别反对核战争。他曾被英国《新科学家》 周刊评为人类有史以来20位最杰出的科学家之一,与牛顿、居里 夫人及爱因斯坦齐名。 为了解释甲烷的正四面体结构,说明碳原子四个键的等价性, 鲍林在1928一1931年,提出了杂化轨道的理论。该理论的根据是 电子运动不仅具有粒子性,同时还有波动性。而波又是可以叠加 的。所以鲍林认为,碳原子和周围4个氢原子成键时,所使用的 轨道不是原来的s轨道或p轨道,而是二者经混杂、叠加而成的 “杂化轨道”,这种杂化轨道在能量和方向上的分配是对称均衡 的。杂化轨道理论,很好地解释了甲烷的正四面体结构。
【巩固、提升】
1.关于原子轨道的说法正确的是( C ) A.凡是中心原子采取sp3杂化轨道成键的分子其几何 构型都是正四面体 B.CH4分子中的sp3杂化轨道是由4个H原子的1s 轨道和 C原子的2p轨道混合起来而形成的 C.sp3杂化轨道是由同一个原子中能量相近的s轨道和 p轨道混合起来形成的一组能量相同的新轨道 D.凡AB3型的共价化合物,其中心原子A均采用sp3杂 化轨道成键
高中化学 第二章 化学键与分子间作用力 2.2 共价键与分子的空间构型(第2课时)价电子对互斥理论

第2课时价电子对互斥理论等电子原理课标解读重点难点1.了解杂化轨道的三种类型(sp3、sp2、sp)。
2.初步认识分子的空间构型。
3.能运用杂化轨道理论和价层电子对互斥模型判断分子的空间构型。
4.结合实例说明“等电子原理”的应用。
1.判断分子中心原子的杂化轨道类型。
(重点)2.用价层电子对互斥理论及杂化轨道理论推断分子的空间构型。
(难点)课前自主导学一、杂化轨道理论与分子空间构型1.sp3杂化与CH4分子的空间构型(1)杂化轨道的形成碳原子2s轨道上的1个电子进入2p空轨道, 2s轨道和 2p轨道“混合”,形成的4个sp3杂化轨道。
图示为:(2)sp3杂化轨道的空间指向碳原子的4个sp3杂化轨道指向,每个轨道上都有一个未成对电子。
(3)共价键的形成碳原子的4个轨道分别与4个H原子的轨道重叠形成4个相同的σ键。
(4)CH4分子的空间构型CH4分子为空间结构,分子中C—H键之间的夹角都是。
2.sp2杂化与BF3分子的空间构型(1)sp2杂化轨道的形成硼原子2s轨道上的1个电子进入2p轨道。
1个2s轨道和 2p轨道发生杂化,形成能量相等、成分相同的 sp2杂化轨道。
图示为:(2)sp2杂化轨道的空间指向硼原子的3个sp2杂化轨道指向,3个sp2杂化轨道间的夹角为。
(3)共价键的形成硼原子的3个轨道分别与3个氟原子的1个2p轨道重叠,形成3个相同的σ键。
(4)BF3分子的空间构型BF3分子的空间构型为,键角为。
3.sp杂化与BeCl2分子的空间构型(1)杂化轨道的形成Be原子2s轨道上的1个电子进入2p轨道,1个2s轨道和1个2p轨道发生杂化,形成能量相等、成分相同的个sp杂化轨道。
图示为:(2)sp杂化轨道的空间指向两个sp杂化轨道呈,其夹角为。
(3)共价键的形成Be原子的2个sp杂化轨道分别与2个Cl原子的1个轨道重叠形成相同的σ键。
思考交流:1.任意不同的原子轨道都可以杂化吗?二、价层电子对互斥模型1.理论分子中的价电子对(包括电子对和孤电子对)由于相互排斥作用,而趋向于尽可能彼此远离以减小斥力,分子尽可能采取的空间构型。
高中有机化学选修物质结构与性质

第一课时 分子的空间构型与杂化轨道
• 结合价键理论,以表示原子的小球 和小棒(个别有弹簧)组装HCl、
CH4、H2O、CO2、C2H2、C2H4 等物 质的球棍模型
一、一些典型分子的空间构型
HCl
H2O
NH3
CO2
CH4 C2H4
C6H6 C2H2
思考5:描述甲烷中共价键的形成过程:
σ
4+
→
σ
σ
1s
σ
H
C
sp3
CH4
四个H原子分别以4个s轨道与C原子上的四个sp3杂化轨道相互重叠后,形成 了四个性质、能量和键角都完全相同的s-sp3的σ键。从而使CH4分子具有正 四面体构型
2、常见的SP型杂化
(1)sp3杂化 :由一个s轨道和三个p轨道杂化形成, 四个sp3杂化轨道。
• 由于共价键具有饱和性和方向性
• 所以原子以共价键所形成的分子具 有一定的空间构型
1、甲烷分子的空间构型
正四面体 键角:109.5°
阅读:P41中联想与质疑
• 客观存在与理论不相符,你能解释吗?
原子间要形成共价键,必须含有未成对的电子
2p
2p
2s
激发 2s
C的基态 CH2
激发态 CH4
甲烷分子的正四面体构型是怎样形成的呢?
• (2)原子轨道的杂化的原因——外部条件; • (3)杂化的结果—— 原子在形成分子时,
增强成键能力,使分子的稳定性增加;
• 杂化的目的——为了增强成键能力?
•
唯心
碳原子杂化过程
2s 2p 激发 2s
跃迁
2p 杂化
“共价键与分子的空间构型”难点突破的教学实践
鲁科版《物质结构与性质》第二章第2节共价键与分子的空间构型内容中涉及到的杂化理论,教师觉得难教,学生感到难学,如何突破难点,既能让教师讲得“清”,又能使学生学得“活”,无疑是我们教师应该认真研究的一个重要问题。
本文想就这方面谈一谈自己在教学中的想法和做法,供教师们在教学实践中参考。
一、本课时的教学要求:课程内容标准:认识共价分子结构的多样性和复杂性,能根据有关理论判断简单分子或离子的构型。
本课时教学目标:1.使学生知道一些常见简单分子的空间构型(如甲烷、氨分子、水分子、乙烯、乙炔、苯等)2.使学生了解一些杂化轨道理论的基本思想,并能用杂化轨道知识解释甲烷、乙烯、乙炔、苯、氨、水分子等分子中共价键的形成原因以及相应分子的空间构型。
本课时的重点和难点:杂化轨道理论的基本思想,甲烷、乙烯、乙炔、苯的共价键成因分析。
二、难点原因分析:教材对“杂化轨道理论”的编写按照由个别到一般、再从一般到个别的思路,即从简单分子甲烷(sp3杂化)入手,通过对甲烷分子成键情况和分子空间结构的学习,形成杂化轨道理论的基本思想,并认识sp 型的其它杂化形式,再运用杂化轨道理论剖析乙烯(sp2杂化)、乙炔分子(sp1杂化)等的成键情况和分子的空间构型;介绍了甲烷、乙烯、乙炔分子等的成键情况(均为等性杂化)和空间构型后,又以氨分子为例,引出“不等性杂化”的问题,使学生的认识扩展到杂化轨道理论的特殊情况。
应该说这样编排是符合学生的认知规律的,但不足的是学生自学时有一些问题无法解决,如:如何判断分子中中心原子的杂化方式?杂化轨道数如何计算?再者这部分知识原来是大学无机化学中的内容,杂化轨道理论中,关于几种杂化轨道形成过程需要高度的空间想象力和抽象思维,否则就很难理解,有些教师可能都得重新学习,才能跟学生说清楚,所以学生在学习“杂化轨道理论”时,往往感到抽象难懂就不难理解。
三、教学实践:要突破这一难点,我认为较好的办法是采用多媒体技术,变静态教材为动态教材,使用模型、多媒体等直观教具进行教学,让学生动手组建分子球棍模型,认识一些典型分子和离子(如H2O、CO2、NH3、CH4、C2H4、C2H2、C6H6、NH4+等)的空间构型,并学会根据共价键原理、杂化轨道理论、价电子对互斥理论以及配位键原理等基础知识,解释这些典型分子和离子的立体结构。
高三化学一轮复习——共价键与分子的空间构型

第33讲共价键与分子空间构型【考纲要求】1、了解共价键的主要类型σ键和π键,能用键能、键长、键角等说明简单分子的某些性质。
2、了解杂化轨道理论及常见的杂化轨道类型(sp、sp2、sp3),能用价层电子对互斥理论或着杂化轨道理论推测常见的简单分子或者离子的空间结构。
【课前预习区】一、共价键1、共价键⑴定义:⑵本质:⑶形成条件:⑷特征:2、类型⑴按成键原子间共用电子对的数目分为、、⑵按共用电子对是否偏移分为、⑶按原子轨道的重叠方式分为、3、键参数共价键的参数有__________、_________和。
其中决定分子稳定性的是和;决定分子的空间构型的是和。
二、分子的空间构型_______ _________理论和_________ _______理论可解释或预测分子的空间构型。
对比:下列有机物中碳原子的杂化方式是:CH4______ C2H4______ C2H2_______ 苯_____2、价层电子对互斥理论⑴基本思路:分子中的价电子对(包括成键电子对和孤电子对)由于相互排斥作用而趋向尽可⑵AB m 型分子(A 是中心原子、B 为配位原子),分子中价电子对数可能通过下式确定×2n +=中心原子的价电子数每个配位原子提供的价电子数m其中:①中心原子的价电子数等于中心原子的最外层电子数,配位原子中卤原子、氢原子提供1个价电子。
②氧原子和硫原子作为配位原子时按不提供价电子计算。
③离子的价电子对数计算 。
如:NH 4+ : 41415=-⨯+=n ; SO 42- :4206=++=n三、分子的性质1、阅读课本P44-46二、分子的空间构型与分子性质了解判断分子极性和手性分子的方法2、具有相同原子总数和相同价电子总数的分子或离子,具有相同的结构和物理性质,这一原理称为“等电子原理”。
应用:①应用等电子原理,可利用已知的分子的构型(几何构型、电子构型)和物理性质对相应等电子分子的构型和物理性质进行预测。
《分子的空间构型》PPT课件

2、下列各组分子中,都属于含有
极性键的非极性分子的是( C ) 3 A CH4和Br2 B NH3和H2O
4 C C2H4和CO2 D H2S和
C2H2
3 、下列分子中:SO2、SiF4、H2S、 H分2子O2的、NSiHF34、、BPFC3l3,、属BF于3,极属性于分非子极的性有
SO2、H2S、H2O2、NH3、PCl3
[探究一] 用毛皮摩擦的玻璃棒靠近 CCl4液流,观察现象
[探究二] 用上述橡胶棒靠近水流, 观察现象
编辑ppt
7
二、分子的极性
[问题组一]
1.水分子中氧原子和氢原子得电子能力 相比哪个强,为什么?
2.哪个原子带负电荷,哪个原子带正电 荷?
3.正电荷的重心和负电荷的重心分别在空间 的哪个位置,是否重叠?
分子极性
X2Y型 CO2
SO2
极性键
非极性分子
直线型
极性键 角形
极性分子
类型 实例
结构
XY3型 BF3
NH3
键的极性 分子极性
极性键
非极性分子
平面三角形
极性键
极性分子
三角锥形
判断非极性分子和极性分子子 HCl,CO,NO 非极性键→非极性分子 H2,O2,N2
多原子分子
4.四氯化碳和水的空间结构有什么区别?
5.为什么水分子有正负极而四氯化碳不存 在?
水和四氯化碳
编辑ppt
10
二、非极性分子和极性分子
(一) 非极性分子:整个分子的电荷分 布均匀的、正负电荷重心重合的分 子是非极性分子。如: H2、Cl2、N2、 O2等。
二、非极性分子和极性分子
(二) 极性分子:整个分子中电荷分 布不均匀、正负电荷重心不重合的分 子叫做极性分子。 如:HCl、H2O、NH3等。
高中化学 2.2.1 一些典型分子的空间构型规范训练 鲁科

第二节共价键与分子的空间构型第1课时一些典型分子的空间构型(时间:30分钟)考查点一一些典型分子的空间构型1.下列分子中键角最小的是 ( )。
A.H2O B.CO2 C.BF3 D.CH4解析四个选项中键角最大的为直线形的CO2分子,键角为180°,其次为平面三角形分子BF3,键角为120°,再次为正四面体形分子CH4,键角为、109.5°,最小的是V形分子H2O,由于其分子中存在着未成键的2对孤对电子,它对成键电子对的排斥作用较强,使键角从109.5°被压缩到104.5°。
答案 A2.下列各组分子中都属于含极性键的非极性分子的是( )。
A.CO2、H2S B.C2H4、CH4C.Cl2、C2H2D.NH3、HCl解析此题考查键的极性和分子的极性。
A中CO2结构为O===C===O,H2S为,所以都含极性键,但H2S是极性分子;B中C2H4为,CH4为,都含极性键,都属于非极性分子;C中Cl2不含极性键;D中NH3、HCl为极性分子,都不符合题意。
答案 B考查点二杂化轨道理论3.sp3杂化形成的AB4型分子的空间构型是 ( )。
A.平面四边形B.四面体形C.四角锥形D.平面三角形解析sp3杂化形成的AB4型分子的空间构型应为四面体形,例如CH4、CF4等。
答案 B4.下列分子中的碳原子采取sp2杂化的是 ( )。
A.C2H2B.C2H4C.C3H8D.CO2解析A项C2H2中的碳原子采取sp1杂化,B项C2H4中的碳原子采取sp2杂化,C项C3H8中的碳原子采取sp3杂化,D项CO2中的碳原子采取sp1杂化。
答案 B5.(2011·宁夏石嘴山高二检测)如图在乙烯分子中有5个σ键、一个π键,它们分别是( )。
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键C.C—H之间是sp2形成的σ键,C—C之间是未参加杂化的2p轨道形成的π键D.C—C之间是sp2形成的σ键,C—H之间是未参加杂化的2p轨道形成的π键解析乙烯分子中每个碳原子均采取sp2杂化,其中杂化轨道形成5个σ键,未杂化的2p轨道形成π键。
第2节 杂化理论和分子空间构型
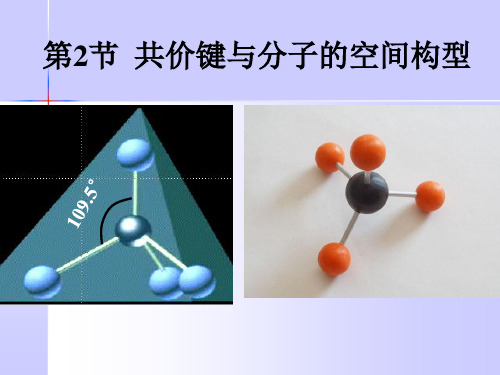
一、杂化轨道理论 1、SP3杂化
由1个s轨道和3个p轨道混杂并重新组合成4 个能量与形状完全相同的轨道。
14
6
为了四个杂化轨道在空间尽可能远 离,使轨道间的排斥最小,4个杂化 轨道的伸展方向分别指向正四面体的 四个顶点。
四个H原子分别以4个s轨道与C原子上的四 个sp3杂化轨道相互重叠后,就形成了四个性质、 能量和键角都完全相同的S-SP3σ键,形成一个 正四面体构型的分子。
•
1、有时候读书是一种巧妙地避开思考 的方法 。20.1 2.1320. 12.13Sunday, December 13, 2020
•
2、阅读一切好书如同和过去最杰出的 人谈话 。00:5 0:0500: 50:0500 :5012/ 13/2020 12:50:05 AM
•
3、越是没有本领的就越加自命不凡。 20.12.1 300:50: 0500:5 0Dec-20 13-Dec-20
n 中心原子的价电子数+每个配位原子提供的价电子数 m 2
ⅰ其中,中心原子的价电子数为中心原子的最外层电子数,例如:
B:3,C:4,N:5,O:6,X:7,稀有气体:8
ⅱ配位原子提供电子数的计算方法:
①H、卤素只提供1个共用电子;
② 在形成共价键时,作为配体的氧族可以认为不提供共用电子;
③当氧族原子作为中心原子时,则可以认为提供6电子
大π 键 (离域键) C6H6
思考:1、运用杂化轨道理论解释乙烯、乙炔、苯、 石墨和金刚石中C原子的杂化方式。
石墨的结构图
金刚石的结构图
小结二:含碳物质(有机物、石墨、金刚石等) 中碳原子的杂化方式
4、几种常见分子中心原子杂化类型(NH3、H2O)
N
高二化学集体备课共价键与分子的空间构型

如CH4、BF3、BeCl2、PCl5、SF6中心原子杂化轨道的空间构型
与分子的空间构型相同
(2)当杂化轨道中有孤电子对(m=1、2、3等)时:孤电子对与成键电子
对的排斥作用,会使分子或离子的构型与杂化轨道的形状有所不同。
如CH4、NH3、H2O分子中心原子都是sp3杂化,但由于C、N、O
知识回顾:
用杂化轨道理论解释CH4分子的空间构型-------正四面体构型.
思考:NH3分子中N原子的价电子排布式为2s22p3。H2O分子中O原子的价电子排布式为2s22p4。为什么?
(一):价电子对互斥理论
1.基本观点是:对ABn型分子或离子
(1)分子中的中心原子的杂化轨道数=分子中的中心原子的价电子对数
n+m=2时,为直线形,键角为1800 .CO2,BeCl2
总结:分子中组成原子有两个,有三个,四个,五个,六个空间构型。
典例1(P33典例1)下列有关氨分子杂化类型与空间构型
的叙述正确的是()
A.sp3三角锥109.50 B.sp2正三角型1200
C.sp3三角锥107.30D.sp2三角锥107.30
③直线形→中心原子为sp1杂化;
④判断杂化方式和分子构型还有其它方法
(二).根据共价键的类型判断
①中心原子形成1个叁键,则为sp1杂化,如CH≡CH,H—C≡N;分子为直线形分子。
②中心原子形成2个双键,则为sp1杂化,如O==C==O,S==C==S;分子为直线形分子。
③中心原子形成1个双键,则为sp2杂化,如HCHO、CH2=CH2;分子为平面形分子
孤电子对数分别是0、1、2,由于它们斥力的不同,分子构型不同,分别
2.2.2 分子的空间结构与分子性质 练习(解析版)—鲁科版选择性必修2

第二章微粒间相互作用与物质性质第2节共价键与分子的空间构型第2课时分子的空间结构与分子性质一.选择题:本题共10小题,每题2分,共20分。
每小题只有一个选项符合题意。
1.下列叙述中正确的是( )A.以非极性键结合起来的双原子分子一定是非极性分子B.以极性键结合起来的分子一定是极性分子C.非极性分子只能是双原子单质分子D.非极性分子中,一定含有非极性共价键【答案】A【解析】A项,如O2、H2、N2等是非极性分子,正确;B项,以极性键结合起来的分子不一定是极性分子,若分子的立体构型对称,就是非极性分子,如CH4、CO2、CCl4、CS2等,错误;C项,某些共价化合物如C2H4等也是非极性分子,错误;D项,非极性分子中不一定含有非极性键,如CH4、CO2,错误。
2.下列物质的分子中,都属于含极性键的非极性分子的是( )A.CO2、H2S B.C2H4、CH4C.Cl2、C2H2 D.NH3、HCl【答案】B【解析】C项,Cl2分子中无极性键,排除C;根据结构可以判断A项中H2S,D项中NH3、HCl分子属于极性分子,排除A、D,故正确答案为B。
3.已知CO2、BF3、CH4、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知AB n型分子是非极性分子的经验规律是( )A.分子中不能含有氢原子B.在AB n分子中A原子没有孤电子对(或A原子最外层电子均已成键)C.在AB n分子中每个共价键的键长和键能都相等D.分子中所有原子在同一平面内【答案】B【解析】CO2、BF3、CH4、SO3中所有电子都参与形成了共价键,都不含孤电子对,分子都是对称结构,为非极性分子。
H2S、SO2、H2O、NH3都含有孤电子对,分子都是不对称结构,为极性分子。
AB n分子的极性取决于分子的空间结构是否对称,而对称性与分子是否含有孤电子对有关,与其他因素无关。
4.下列有机物分子中属于手性分子的是( )①乳酸[CH3CH(OH)COOH] ②2丁醇[CH3CH(OH)CH2CH3]④丙三醇A.只有①B.①和②C.①②③D.①②③④【答案】C【解析】写出各分子的结构简式:,可知①②③中存在手性碳原子(用*标记的),而④中中间的碳原子连有2个相同的—CH2OH,不是手性碳原子。
高二化学共价键与分子的空间构型

①形成分子时,由于原子间的 相互作用,使同一原子内部能量 相近的不同类型原子轨道重新组 合形成的一组新的能量相同的杂 化轨道。有多少个原子轨道发生 杂化就形成多少个杂化轨道。
②杂化轨道的电子云一头大, 一头小,成键时利用大的一头, 可以使电子云重叠程度更大, 从而形成稳定的化学键。即杂 化轨道增强了成键能力。
由1个s轨道和3个p轨道混杂并重新组合成 4个能量与形状完全相同的轨道。 由于每个轨道中都含有1/4的s轨道成分和 3/4的p轨道成分,因此我们把这种轨道称之为 sp3杂化轨道。
四个H原子分别以4个s轨道与C原子上的 四个sp3杂化轨道相互重叠后,就形成了四个 性质、能量和键角都完全相同的S-SP3σ键, 形成一个正四面体构型的分子。
杂化轨道理论
杂化:原子内部能量相近的原子轨道,在外界条件 影响下重新组合的过程叫原子轨道的杂化. 杂化轨道:原子轨道组合杂化后形成的一组新轨道 杂化轨道类型:sp、sp2、sp3等杂化结果: 重新分配能量和空间方向,组成数目相等成键 能力更强的原子轨道 杂化轨道用于:容纳σ键电子和孤对电子
1.sp3 杂化
③杂化轨道之间在空间取最大 夹角分布,使相互间的排斥能最 小,故形成的键较稳定。不同类 型的杂化轨道之间夹角不同,成 键后所形成的分子就具有不同的 空间构型。
sp 杂化 同一原子中 ns-np 杂化成新轨道;一 个 s 轨道和一个 p 轨道杂化组合成两个新 的 sp 杂化轨道。
例:
2s 2p 激发 激发态
sp型的三种杂化
杂化类型 参与杂化 的原子轨 道 杂化轨道 数 杂化轨道 间夹角 空间构型 sp 1个s + 1个p 2个sp杂化轨 道 180o 直线 sp2 1个s + 2个p 3个sp2杂化 轨道 120o 正三角形 BF3, BCl3 sp3 1个s + 3个p 4个sp3杂化 轨道 109.5o 正四面体
第二章 共价键与分子结构

.
3 Π3
CH2-CH=CH2
+
2 Π3
4 CH2=CH-CH2: Π 3
上页 下页
22 首页
-
.. CH2=CH - Cl : ..
4 Π3
相关键长比较
CH3 — CH2
173pm
Cl
CH2
CH2
138pm
CH
169pm
Cl
134pm
CH2
上页
下页
23 首页
3. σ-π 超共轭
全重叠式 邻位交叉式 部分重叠式 对位交叉式
正丁烷各种构象的能差不大, 室温下可迅速转化, 正丁烷 实际上是各种构象异构体的混合物, 但对位交叉式为优势构象, 约占70%, 邻位交叉式约占30%, 其他构象所占比例极小。
30
3. 环己烷的构象异构
(1) 两种典型构象 —— 船式和椅式
偶极矩是向量,带有方向性,一般以“ 头表示从正电荷到负电荷的方向。 多原子分子的偶极矩是分子中各个键的 偶极矩的向量和。 H Br
μ = 2.60 × 10 -30 C.m
”来表示,箭
Cl C H μ = 5.34 × 10 Cl -30
6
H
C.m
分子的极性是分子中所有化学键极性的向量和。对于双 原子分子,键的极性就是分子的极性。多原子分子的极性不 仅取决于各个键的极性,也取决于分子的形状。分子的极性 越大,分子间相互作用力就越大。
17
诱导效应中电子偏移的方向以C—H键中H作为比较标准.
O C-C-O-H
H O H-C-C-OH H
X
Y
O C-C-O-H
-I
+I
物质结构与性质:2-2-2分子的空间构型

3.分子的极性
非极性分子:
电荷分布均匀对 称的分子
正电荷重心和负电荷重心相重合的分子
极性分子:
电荷分布不均匀 不对称的分子
正电荷重心和负电荷重心不相重合的分子
Cl
Cl
Cl
Cl
2个共C用l原电子子吸对引电子的能力相同,共用电 子对不偏向任何一个原子,整个分子的 电荷分布均匀,∴为非极性分子
只含有非极性键的分子因为共用电 子对无偏向,∴分子是非极性分子
第2节 共价键与分子的空间构型
第三课时
复习
杂化 参与杂 类型 化的原
子轨道
杂 sp
化
轨 道
sp2
理 论 sp3
1个s + 1 个p
杂化 轨道 数
3
4
杂化轨 道间夹 角 180°
120°
109028’
空间构型 实例
直线
BeCl2 ,
C2H2
平面三角形 BF3BCl3
四面体形
CH4CCl
4
杂化类型
sp型的三种杂化
H
H
H
H
109.5º C
正四面体型 ,对称结构,C-H键的极性 互相抵消( F合=0) ,是非极性分子。
ABm分子极性的判断方法
1. 化合价法
①若中心原子A的化合价的绝对值等于该元素所在 的主族序数,则为非极性分子,若不等则为极性分 子; ②若中心原子有孤对电子(未参与成键的电子对)则 为极性分子,若无孤对电子则为非极性分子。
条件:当四个不同的原子或基团连接在碳 原子上时,形成的化合物存在手性异构体。 其中,连接四个不同的原子或基团的碳原子 称为手性碳原子。
课堂练习
1.下列化合物中含有手性碳原子的是( B )
第二章 第二节 共价键与分子的空间构型

CO 和 N2 ; CO2 和 N2O 。
Li Be B C N O F Ne
第三课时
二、分子的空间构型与分子性质
1.手性分子
左手和右手不能重叠
左右手互为镜像
手性异构体和手性分子
概念:如果一对分子,它们的组成和原子 的排列方式完全相同,但如同左手和右手一 样互为镜像,在三维空间里不能重叠,这对 分子互称手性异构体。有手性异构体的分子 称为手性分子。
D.P4
课堂练习
• 3.若ABn型分子的中心原子A上没有未用于形 成共价键的孤对电子,运用价层电子对互斥模
型,下列说法正确的(C )
• A.若n=2,则分子的立体构型为V形 • B.若n=3,则分子的立体构型为三角锥形 • C.若n=4,则分子的立体构型为正四面体形 • D.以上说法都不正确
分子 或离子
总结:如何判断一个化合物的中心原子的 杂化类型?
一看 分子的空间构型,如果是直线型,则是sp杂 化;如果是平面三角形,则是sp2杂化;如果是正 四面体型,则是sp3杂化。
二看 中心碳原子有没有形成双键或叁键,如果有1 个叁键,则其中有2个是π键,用去了2个p轨道, 所以形成的是sp杂化;如果有1个双键则其中有1 个π键,用去了1个p轨道,所以形成的是sp2杂化; 如果全部是单键,则形成的是sp3杂化。
孤电子 杂化方式 对数
2
SP3
2
SP3
1
SP3
1
SP3
0
SP3
0
SP3
0
SP3
0
SP3
0
SP3
0
SP3
VSEPR 模型名称
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、下列分子中的中心原子杂化轨道的类 型相同的是 ( B ) A.CO2与SO2 B.CH4与NH3 C.BeCl2与BF3 D.C2H2与C2H4
2、对SO2与CO2说法正确的是( D ) A.都是直线形结构 B.中心原子都采取sp杂化轨道 C.S原子和C原子上都没有孤对电子 D.SO2为V形结构, CO2为直线形结构
3、指出中心原子可能采用的杂化轨道类型, 并预测分子的几何构型。 (1)PCl3 (2)BCl3 (3)CS2
4
1
2
四面体 四面体
三角锥 V形
NH3 H 2O
(3)判断共价分子结构的实例
例 1 利用价层电子对互斥理论判断下列分子和离子的几何 构型。要求写出价层电子总数、对数、电子对构型和分子构型 。
AlCl3 解:总数
对数 电子对构型 6 3
H2S
8 4
SO32 8 4
NH4 +
8 4
NO2
5 3
三角形
三角形 正四面体 正四面体 正四面体
第2节 共价健与分子的空间构型
C
2s
2px
2py
2pz
2s
2px
2py
2pz
C原子与H原子结合形成的分子为什么是 CH4,而不是CH2或CH3?CH4分子为什么具有 正四面体的空间构型(键长、键能相同, 键角相同为109°28′)?
1.杂化轨道理论简介
2s 2p
激发 2s
为了解决这一矛盾,鲍林提出了杂化轨道理论,
180。
(2)CO32–、NO3–、SO3等离子或分子具有相同的通 式—AX3,总价电子数24,有相同的结构—平面三角形分子,中 心原子上没有孤对电子而取sp2杂化轨道形成分子的s-骨架。 (3)SO2、O3、NO2–等离子或分子,AX2,18e,中心
原子取sp2杂化形式,VSEPR理想模型为平面三角形,中心
等电子体原理
具有相同的通式——ABm,而且价电子总数和原子数目
相等的分子或离子具有相同的结构特征,这个原理称为“等电 子体原理”。这里的“结构特征”的概念既包括分子的立体 结构,又包括化学键的类型,但键角并不一定相等,除非键 角为180或90等特定的角度。 (1)CO2、CNS–、NO2+、N3–具有相同的通式—AX2, 价电子总数16,具有相同的结构—直线型分子,中心原子上 没有孤对电子而取sp杂化轨道,形成直线形s-骨架,键角为
sp3 杂化 109.5º 正四面体
思考
BF3分子形成过程
2s
2p 激发 2s 2p 正三角形
B的基态
激发态
sp2 杂化态
F
B F F
120°
思考
BeCl2分子形成过程
2s 2p 激发 2s 2p 杂化 直线形
Be基态
激发态
sp杂化态 直线形
180
Cl
Be
Cl
键合 化合态
思考 请用杂化轨道理论分析乙烯和乙炔 分子的成键情况?
•确定中心原子的孤对电子对数,推断分子 的空间构型。 例如:
BeH2 n=
1 2 (2+2)=2 1 (3+3)=3 2 1 (4+4)=4 2
① 孤对电子=0:分子的空间构型=电子对的空间构型 直线形 平面三角形
BF3
n=
CH 4 n=
四面体
②孤对电子≠0 :分子的空间构型不同于电 子对的空间构型。 电子对的 分子的 例 孤对 空间构型 n 空间构型 电子 1 平面三角形 V形 3 SnCl2
2p 正四面体形
C的基态
激发态
sp3 杂化态
H
109°28’
C H H 在同一个原子中能量相近的不同类型的几个原子 轨道(S、P…)可以相互叠加而组成同等数目的 能量完全相等的杂化原子轨道—杂化轨道理论 H
杂化轨道类型
sp2 杂化 sp 杂化 杂化轨道夹角 杂化轨道 空间取向 180º 直线 120º 平面 三角形
原子上有1对孤对电子(处于分子平面上),分子立体结构为V 型(或角型、折线型) 。
(4)SO42–、PO43–等离子具有AX4的通式,总价电子数 32,中心原子有4个s-键,故取sp3杂化形式,呈正四面体立 体结构;
(5)PO33–、SO32–、ClO3–等离子具有AX3的通式,总 价电子数26,中心原子有4个s-轨道(3个s-键和1对占据s-轨 道的孤对电子),VSEPR理想模型为四面体,(不计孤对电 子的)分子立体结构为三角锥体,中心原子取sp3杂化形式, 没有p-pp键或p-p大键,它们的路易斯结构式里的重键是 d-p大键。
杂化轨道的类型与空间结构的关系
杂化类型 用于杂化的 原子轨道数 杂化轨道数 空间构型 实例 sp 2 2 直线型 BeCl2 CO2 sp2 3 3 平面三角形 BF3 BCl3 sp3 4 4 四面体 CH4 CCl4 sp3d2 6 6 八面体 SF6 SiF62-
价层电子对互拆理论
推断分子或离子的空间构型的具体步骤: •确定中心原子的价层电子对数, 以AXm为例 (A—中心原子,X—配位原子) :
(4) 各种杂化轨道的“形状”均为葫芦形,由分 布在原子核两侧的大小叶瓣组成,轨道的伸 展方向是指大叶瓣的伸展方向,为简明起见 往往不给出小叶瓣。 (5) 杂化轨道的数目等于参与杂化的轨道的总数 (6) 杂化轨道可分为等性杂化轨道与不等性杂化 轨道两种。 (7) 杂化轨道成键时,要满足化学键间最小排斥原 理,键角越大,排斥力越小。杂化轨道类型不 同,成键时键角不同,分子的空间结构也不同。
用杂化轨道理论解释苯分子的成键情况?
6. 杂化轨道要点
(1 ) 轨道杂化是指同一个原子中相关轨道的混合,由 此产生的杂化轨道也是原子轨道。 (2)参与杂化的轨道中电子所处的能级略有不同, 而杂化轨道中的电子则处于相同能级。杂化后 能 级 相 当 于 杂 化 前 有 关 电 子 能 级 的 中 间 值。 (3) 杂化只能发生在能级接近的轨道之间,如主量 子数相同的s、p、d轨道之间,或(n-1)d与ns、 np之间,能量也是相近的。亚层符号按能级升高 的顺序排列,例如d2sp3和sp3d2代表不同杂化轨 道。
Cl
分子构型
Cl
SLeabharlann ClSHH
Al
H
O
O O
H
N
N
H H
O
O
三角形
V字构型
三角锥
正四面体 V字形
小结:
代表 物 CO2 中心原子 CH2O 无孤对电子 CH4 中心原子 有孤对电子 H2O NH3 中心原子 结合的原子数 2 3 4 2 3 分子 类型 AB2 空间构型 直线形
AB3 平面三角形 AB4 AB2 AB3 正四面体 V形 三角锥形
n=1/2[A的价电子数+X提供的价电子数×m 负 ±离子电荷数( 正 )] 原则: ①A的价电子数 =主族序数; ②配体X:H和卤素每个原子各提供一个价电 子, 规定氧与硫不提供价电子;
③正离子应减去电荷数,负离子应加上电荷数。
•确定电子对的空间构型: n=2 直线形
n=3
n=4
平面三角形
正四面体
