官能团定位及保护
有机化学中的官能团保护与反应选择

有机化学中的官能团保护与反应选择在有机化学领域,官能团保护与反应选择是一项关键而重要的技术。
它们在有机合成中发挥着重要的作用,可以实现对特定官能团进行保护,以及控制反应的选择性。
本文将探讨有机化学中的官能团保护与反应选择的原理、方法和应用。
一、官能团保护的原理和方法官能团保护是在有机合成中使用特定的试剂或方法对特定官能团进行保护,以阻止其在反应中发生不需要的转化或损失。
这种保护可以临时地对官能团进行屏蔽,以防止不需要的反应发生。
一旦需要,这些保护官能团可以很容易地被去除,使得官能团再次可用。
常见的官能团保护方法包括酯化、缩醛、缩酮、硅烷保护、硼酸酯保护等。
例如,在酯化反应中,羧酸可以与醇发生酯化反应,形成酯。
这种反应可以通过加入催化剂、调节反应条件和使用适当的反应物比例来控制。
一旦酯形成,官能团保护就实现了。
二、反应选择性的控制在有机合成中,反应选择性是指在具有多个官能团的分子中,选择性地引发或控制特定官能团的反应。
反应选择性的控制对于合成复杂的有机化合物非常重要,可以避免副反应的发生,并帮助提高产率和纯度。
反应选择性的控制可以通过多种方法实现,如调节反应条件、选择适当的催化剂、改变反应物的比例、使用合适的试剂和溶剂等。
以亲核取代反应为例,当分子中存在多个能提供亲核位点的官能团时,可以通过调节反应条件和选择适当的反应物比例,去控制反应的进行。
三、官能团保护与反应选择的应用官能团保护和反应选择在有机合成中有广泛的应用。
其中最具代表性的应用之一是在多步合成中,其中的中间体需要在反应过程中保护起来,以防止意外的转化或副反应的发生。
通过对中间产物进行官能团保护,可以控制整个反应过程,确保预期产物的高产率和选择性。
另一个重要的应用是在天然产物合成中。
天然产物通常具有复杂的结构和多个官能团,官能团保护和反应选择技术可以被用来合成这些天然产物或其类似化合物。
通过选择性地引发或控制特定官能团的反应,可以构建复杂分子骨架,实现对天然产物的全合成。
官能团的保护

官能团的保护§官能团的保护1.易于被保护基团反应,且除被保护基团外不影响其他基团.2.保护基团必须经受得起在保护阶段的各种反应条件.3.保护基团易于除去.化学合成中常用的保护基碳氢键的保护羟基的保护氨基的保护羰基的保护羧基的保护1. 碳氢键的保护乙炔及末端炔烃中的炔氢较活泼,它可以与活泼金属`强碱`强氧化剂及有机金属化合物反应.常用的炔氢保护基为三甲硅基.将炔烃转变为格氏试剂后同三甲基氯硅烷作用.即可引入三甲硅基.该保护基对于金属有机试剂`氧化剂很稳定.可在使用这类试剂的场合保护炔基.2.羟基的保护醚类缩醛和缩酮类酯类羟基是一个活性基团,它能够分解格氏试剂和其他有机金属化合物,本身易被氧化,叔醇还容易脱水,并可以发生烃基化和酰基化反应.所以在进行某些反应时,若要保留烃基,就必须将它保护起来.醇羟基常用的保护方法有3类:2.1 转变成醚甲醚用生成甲醚的方法保护羟基是一个经典方法.通常使用硫酸二甲酯,在氢氧化钠或氢氧化钡存在下,在DMF或DMSO溶剂中反应得到.优点:该保护基很容易引入,且对酸,碱,氧化剂和还原剂都很稳定.缺点:难于脱保护,用氢卤酸回流脱保护基条件比较剧烈,常使分子遭到破坏,只有当分子中其他部位没有敏感基团时才适用.2.1 转变成醚叔丁醚将醇的二氯甲烷溶液或悬浮液在硫酸复合物存在下,在室温与过量的异丁烯作用,可得到叔丁醚.优点:对碱及催化氢化是稳定的.缺点:对酸敏感,其稳定性低于甲醚.由于脱保护基所用的酸性条件剧烈,当分子中存在对酸敏感的基团时不适用2.1 转变成醚三甲硅醚三甲硅醚广泛用于保护糖类,甾类及其他醇羟基.通常引入三甲基硅基保护基所用的试剂有三甲基氯化硅和碱;六甲基二硅氨烷.在含水醇溶液中加热回流即可除去保护基.优点:醇的三甲硅醚对催化氢化,氧化还原反应是稳定的,该保护基可在非常温和的条件下引入和去除.缺点:对酸和碱敏感,只能在中性条件下使用.2.2 转变成缩醛或缩酮2,3-二氢-4H-吡喃在酸的催化作用下,与醇类起加成反应,生成四氢吡喃醚衍生物.这是最常用的醇羟基的保护方法之一.此保护基广泛用于炔醇,甾类及核苷酸的合成中.2.3 转变成酯醇与酰卤,酸酐作用生成羧酸酯;与氯甲酸作用生成碳酸酯.所生成的酯在中性和酸性条件下比较稳定,因此可在硝化`氧化和形成酰氯时用成酯的方法保护羟基.保护基团可通过碱性水解除去,或在锌-铜的乙酸溶液中除去.3.氨基的保护伯胺和仲胺很容易被氧化,且易发生烃基化,酰基化以及与醛酮羰基的亲核加成反应.在合成中常采用:(1)氨基质子化(2)变为酰基衍生物(3)变为烃基衍生物等方法将氨基保护起来3.1 质子化此方法仅用于防止氨基的氧化,因为理论上说采用氨基质子化,即占据氮尚未共用电子对,以阻止取代反应的放生.这是对氨基保护最简单的法.3.2 转变为酰基衍生物将氨基酰化转变成酰胺是保护氨常用的方法.通常伯胺酰基化已足以保护基,防止其被氧化和烃化反应的发生.常用的酰基化试剂为酰卤和酸酐.保护基可在酸性和碱性条件下水解出去.3.2 转变为酰基衍生物邻苯二甲酸酐与伯胺所生成的邻苯二甲酰亚胺非常稳定,不受催化氢化碱性还原,醇解以及氯化氢,溴化氢,乙酸溶液的影响,也适用于保护伯胺.在酸性或碱性条件下水解或用肼解法脱去保护.3.3 转变为烃基衍生物用烃基保护氨基主要用三苯甲基或苯甲基.三苯甲基衍生物可用胺与溴或氯代三苯甲烷在碱存在下制备.三苯甲基由于空间位阻效应对氨基起到很好的保护作用,它对碱是稳定的.苯甲基衍生物用胺和氯化苯甲基在碱存下制得.4.羰基的保护羰基具有许多反应性能,是有机化学中最易发生反应的活性官能团之一.保护羰基常用的方法:生成缩醛和缩酮来降低羰基活性而保护羰基.4.羰基的保护保护醛酮羰基最常用的方法是通过乙二醇和2-疏基乙醇的反应,生成相应的叫做环缩醛或缩酮的产物.5.羧基的保护羰基通常用形成酯的方法保护.常见的有转变为甲酯,乙酯,叔丁酯,苯甲酯.甲酯和乙酯可以用羧酸直接与甲醇或乙醇发生酯化反应制得,又可以被碱水解.5.羧基的保护叔丁酯可由羧酸先变为酰氯,再与叔丁醇作用,或者通过羧酸与异丁烯直接作用而得.它不能氢解,在通常条件下也不被氨解及碱催化水解.5.羧基的保护苯甲酯可由羧酸与苯甲基卤在碱性条件下反应而得.它除了可在强酸性或碱性条件下水解,还可以被氢解.。
保护官能团的方法

保护官能团的方法嘿,朋友们!今天咱来聊聊保护官能团的那些事儿。
官能团就像是化学世界里的宝贝疙瘩,得好好保护着才行呢!你想想看啊,官能团就好比是一件珍贵的瓷器,稍有不慎就可能磕了碰了。
那怎么保护它们呢?这可得有点小技巧啦。
比如说,有些官能团特别怕水,那咱就得像给宝贝盖被子一样,把它们和水隔开呀。
不然一不小心让水给沾到了,那不就糟糕啦!还有些官能团怕酸怕碱,那咱就得像保护小公主一样,给它们创造一个酸碱适宜的环境,可不能让那些酸碱来捣乱呀。
就好像你有个特别喜欢的玩具,你肯定会小心翼翼地放在安全的地方,不会让别人随便碰到一样。
保护官能团也是这个道理呀。
有时候呢,我们还得给官能团穿上一层“保护衣”。
这层“保护衣”就像是冬天的棉袄,能帮它们抵御外界的各种干扰。
而且这“保护衣”还得选得合适,不能太大也不能太小,得刚刚好才行呢。
再打个比方,官能团就像是你养的小宠物,你得时刻关注着它,给它提供合适的食物、水和住所。
要是你不精心照料,它生病了或者出问题了,那你得多心疼呀!在实验操作中,我们可得加倍小心。
不能像个马大哈似的,随随便便就对待这些官能团。
每一个步骤都要考虑到它们的感受,就像哄小孩子一样,要温柔、细心。
还有啊,不同的官能团保护方法也不一样哦。
这就像是不同性格的人需要不同的对待方式一样。
有的需要特别的关照,有的则稍微注意一下就行。
总之呢,保护官能团可不是一件简单的事儿,但只要我们用心,就一定能把它们保护得好好的。
这样我们才能在化学的世界里畅游无阻,做出更多有趣的实验和发现呀!所以啊,大家可千万不能马虎对待哦,一定要把保护官能团这件大事放在心上!。
官能团定位及保护

-------------精选文档-----------------官能团的保护与定位有机合成中有时会遇到这样的情况,本意只想对某个官能团进行处理,结果却影响了其它官能团。
“投鼠忌器”,防止对其它官能的影响,常常采用先保护后恢复的方法。
有时官能取代的位置有多种可能性,但要求必须上到规定的位置上,那就要进行官能团的定位措施。
一、防官能团受还原影响的保护与恢复例1. 试以丙烯及其它必要的有机试剂为原料来合成CH 3COCH 20H ,无机试剂任选,写出有关反应的化学方程式。
已知:(1)RCR'ORCR'OCH 2CH 2O RCR'O HOCH 2CH 2OH H 2(2)R C OC 2HORCH 2OHC 2H 5OH[简析]解有机合成题可以根据所要合成的物质,采用顺推、逆推齐推的思维方法。
依题给的有关信息反应的规律并结合所学的知识,可由顺推法初步形成以下的合成路线; CH 3CH=CHCH 3CHBrCH 2CH 3CHOH-CH 23COCOOHBr 2若将-COOH 转化-CH 2OH 就“OK ”了。
再结合信息反应(2)可知,先将-COOH 转化为-COOC 2H 5,然后在LiALH 4作催化剂时与H 2成即可。
但要注意在这一转化过程中,CH 3-CO-中的O也可与H 2加成,故必须考虑将该官能团加以掩蔽和保护,最后重新将其 “复原”,这可以利用信息反应(2)的方法而达到目的。
从而易写出合成 CH 3-CO-CH 20H 的有关反应方程式如下CH 3CH=CH 2+Br 2CH 3CHBr-CH 2BrCH 3CHBr-CH 2Br CH 3CHOH-CH 2CH3CHOH-CH 23COCOOHCH 3COCOOHC2H 5OHCH 3COCOOC2H 5+H 2OCH 3COCOOC 2H 5+HOCH 2CH 2OHCH 3CCOOC 2H 5O O其他略。
官能团保护

官能团保护的意义
有机反应往往会伴有副反应,原因就是
有机反应的复杂性,反应条件、官能团 的相互影响等都会影响反应的进行.在 有些反应中,使某个官能团参加反应时, 可能会有其他的官能团受到影响,这样 就需要对官能团进行保护.
官能团的保护
一、保护基的基本条件 二、羟基保护 三、羰基保护
在一些例子中,最后一条可以放宽,允许保护基 被直接转变为另一种官能团。
二、羟基的保护基团
保护醇类 ROH 的方法一般是制成醚类 (ROR ′ ) 或酯 类(ROCOR′),缩醛或缩酮类。前者对氧化剂或还原剂都有 相当的稳定性。 1
. 醚类衍生物
①形成甲醚类 ROCH3 可以用碱脱去醇ROH质子,再与合成子 +CH3作用,如 使用试剂NaH/Me2SO4。也可先作成银盐 RO-Ag+ 并与碘甲 烷反应,如使用 Ag2O/MeI;但对三级醇不宜使用这一方法 。醇类也可与重氮甲烷CH2N2,在Lewis酸(如BF3·Et2O) 催化下形成甲醚.
以羧基为保护基:
OH CO2/NaHCO3 OH COOH OH Br Br2/AcOH OH COOH H3O OH
+
OH Br
OH
OH
以磺酸基为保护基:
CH3 浓H2SO4 CH3 Cl2,Fe CH3 Cl H3O
+
CH3 Cl
SO3H
SO3H
以硝基为保护基:
C(CH3)3
HNO3 H2SO4
Et2O AgNO3/H2O/EtOH
Ag
KCN/H2O -AgCN
H
格氏反应和有机锂合成中的保护
PhLi+RC CH
高中化学有机合成中的官能团保护

高中化学有机合成中的官能团保护在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下而产生副反应,这样就不能达到预计的合成目标,因此,必须采取措施保护某些官能团,待完成反应后再除去保护基,使其复原。
1、保护措施必须符合如下要求①只对要保护的基团发生反应,而对其它基团不反应;②反应较易进行,精制容易;③保护基易脱除,在除去保护基时,不影响其它基团。
2、常见的基团保护措施①羟基的保护在进行氧化或某些在碱性条件下进行的反应,往往要对羟基进行保护。
a.防止羟基受碱的影响,可用成醚反应。
b.防止羟基氧化可用酯化反应。
②对羧基的保护羧基在高温或碱性条件下,有时也需要保护。
对羧基的保护最常用的是酯化反应。
③对不饱和碳碳键的保护碳碳双键易被氧化,对它们的保护主要用加成反应使之达到饱和。
;④对羰基的保护(以信息题出现)羰基,特别是醛基,在进行氧化反应或遇碱时,往往要进行保护。
对羰基的保护一般采用生成缩醛或缩酮的反应。
(缩醛或缩酮)(缩酮)生成的缩醛或缩酮水解又变成原来的醛或酮。
3、题例解析例1、已知下列信息:①烯键在一定条件下氧化可生成二元醇:②醛能发生如下反应生成缩醛:缩醛比较稳定,与稀碱和氧化剂均难起反应,但在稀酸中温热,会水解为原来的醛。
现有如下合成路线:试回答下列问题:(1)写出A、B的结构简式:________、________。
(2)写出反应Ⅲ的化学方程式:________。
解析:由题给信息知,欲使CH2=CH—CHO变为CH2OH—CHOH—CHO,需将C=C双键氧化,而—CHO对氧化剂敏感,故应先进行保护,待C=C双键氧化完毕,再将醛基还原出来,故合成路线为:答案:(1)A:CH2=CH=CH(OC2H5)2 B:CH2OH—CHOH—CH(OC2H5)(2)CH2OH—CHOH—CH(OC2H5) CH2OH—CHOH—CHO+2C2H5OH例2、已知胺(R—NH2)具有下列性质:(Ⅰ)R—NH2+(CH3CO)2O R—NHCOCH3+CH3COOH(Ⅱ)R—NHCOCH3+H2O R—NH2+CH3COOH硝基苯胺是重要的化工原料,其合成路线如下:(1)a、c、e分别为________。
第三节官能团的保护

一个合适的保护基应具备下列要求: 1。引入时反应简单、产率高、无 毒(低毒) 2。能经受必要的和尽可能多的试 剂作用。 3。除去时反应简单、产率高,其 它官能团应不受影响。 4。对不同的官能团能选择性保护
R CH CH2OH NH2 KMNO4 H2SO4 R CH COOH NH2
螯合与质子化类似,过渡金属,例如 铜有d空轨道和氮孤对电子形成螯合物 最后用H2S处理除去。 3-2-2酰化 将氨基酰化成酰胺然后再水解。
NH2 O + CH3C Cl OH O NH C CH3
O RN C C O
OH
需要保护的官能团 有:
O C
OH
COOH
NH2
C H
C C
本节主要介绍羟基、羰基、氨基的保护
3-1 羟基的保护(醇、二醇、酚的羟基) 醇的活性较大,与金属反应放出氢气,容 易被氧化、取代、烷化、酰化,叔醇易脱 水,所以保护醇羟基很重要。保护醇羟基 时,可以制成醚、酯、缩醛、缩酮等。 醚在酸性中不稳定,在碱性中稳定;缩 醛、缩酮也是在酸性水溶液中不稳定, 而在碱性中稳定;而酯在碱中不稳定, 在酸中稳定。
H2O H
脱落
3-2 氨基的保护 氨基不稳定,较易氧化、酰化、烃化等 反应,因此在一些合成反应中,常常需 要将氨基加以保护。
3-2-1质子化及螯合 从理论上讲,氨基最简单的保护法是使氨 基完全质子化,即占据氮上的未共用电子 对以阻止亲核反应的发生。但是实际上能 在使氨基完全质子化所需的酸性条件下可 以进行的合成反应是很少的。因此,这种 方法仅用于防止氨基的氧化。
有机化学中的官能团保护与去保护

有机化学中的官能团保护与去保护官能团保护是有机化学中的一项重要技术。
官能团保护可以在合成反应中起到保护和控制官能团反应的作用,使其不受到其他反应条件的干扰。
而去保护则是将保护官能团去除,使官能团恢复原来的活性。
本文将重点讨论有机化学中的官能团保护与去保护的相关内容。
一、官能团保护1. 保护官能团的目的在有机合成中,有时候需要保护某些官能团,以免其受到其他反应条件的干扰。
官能团保护的目的有以下几个方面:(1) 避免副反应:有机合成中常常伴随着多步反应,有些副反应会发生在特定的官能团上,通过保护这些官能团可以有效地避免不必要的副反应。
(2) 控制反应速率:有机反应中,一些官能团可能会加速或减缓反应的进行,通过保护官能团,可以控制反应速率,以便更好地控制合成过程。
(3) 保护活性官能团:有机合成中的一些活性官能团,如羟基、胺基等,容易受到空气、湿气等环境因素的影响,通过保护这些官能团,可以保持其活性。
2. 常见的官能团保护方法官能团保护有多种方法,下面介绍几种常见的官能团保护方法:(1) 酯保护:通过酯化反应将酸敏感官能团(如羟基)保护成酯,常用的保护剂有甲基、乙基等醇酚和对甲苯磺酸等。
(2) 醚保护:通过醚化反应将醇敏感官能团(如胺基)保护成醚,常用的保护剂有甲基、乙基等醇酚和氯甲基、溴甲基等卤代烷。
(3) 硅保护:通过硅化反应将官能团保护成硅醚,常用的保护剂有三甲基氯硅烷、三甲基乙氧基硅烷等。
二、官能团去保护官能团去保护是官能团保护的反向操作,它将保护官能团还原为原来的活性官能团。
官能团去保护可通过以下几种方式实现:1. 氢化还原:对于酯保护,可以使用氢气和催化剂进行还原反应,还原成羟基。
对于醚保护,可以使用硼酸或三氟乙酸等酸性条件还原为胺基。
2. 碱性水解:对于酯保护,可以使用氢氧化钠或氢氧化钾等碱性条件进行水解反应,水解为羟基。
对于醚保护,可以使用氢氧化钠或氢氧化钾等碱性条件还原为胺基。
3. 酸性水解:对于碳酸酯或脲保护,可以使用酸性条件进行水解反应,恢复原来的官能团。
官能团之间的相互影响

官能团之间的相互影响在有机化学的学习中,掌握官能团的性质和它们之间的关系是学好有机化学的基本要求。
高中阶段必须掌握的官能团有:碳碳双键、碳碳叁键、卤素原子、羟基、醛基、羰基、羧基、氨基、硝基、磺酸基等。
有机物分子的官能团不同,则性质不同。
本文主要就官能团之间的影响,做一简要介绍:一、官能团的定位作用苯环上有连接有不同的基团或官能团,当进一步引入基团时,其引入的位置与原有官能团(基团)有关,而且不同的基团,还会使苯环的反应活性发生较大的变化。
1.邻对位定位基团,苯环的活性增强当苯环上连接烃基(甲基、乙基、苯基等)、氨基(-NH2、-NHR、-NR2,R 为烷基)、羟基(-OH)、烷氧基(-OCH3、-OC2H5)等基团,使苯的反应活性增强,新引入的基团进入原基团的邻对位位置。
教材上制备硝基苯需要在浓硫酸、浓硝酸混酸与苯在55℃条件下制得,而通常只能得到,很难得到二硝基化合物。
甲苯中新引入的-NO2均处于甲基(-CH3)的邻位或对位。
在过量硝酸存在下,很容易得到三硝基化合物(TNT),这也看出甲基提高了苯环的活性。
2.邻对位定位基团——苯的活性减弱当苯环上连接有卤素原子(-F、-Cl、-Br、-I)-CH2Cl、-CH=CH-等基团时,苯环的反应活性降低,这类反应比较特殊,往往需要在特殊溶剂、催化剂条件下才可能发生反应。
3.间位定位基当苯环上的取代基为-NO2、-SO3H、-SO2R、-COOH、-COOR、-CH O、-COR、-CN等时,使苯环钝化,但邻位和对位钝化程度较间位大,在取代反应中,新取代基大多进入间位,形成间位异构体。
这类取代基称为有钝化作用的间位取代基。
如硝基苯在发烟硝酸、发烟硫酸存在下,长时间加热,可以制得少量的间硝基苯(),同时比较硝基苯的制法可以看出,硝基的引入使苯的活性降低,反应的条件明显提高。
二、官能团(基团)之间相互影响1.官能团(基团)之间的相互活化(1)苯环与烷烃基的相互活化当苯环上连接饱和链烃基时,苯环的活动性增强,使苯的取代变的比较容易,如苯硝化一般得到一硝基化合物,而甲苯硝化则可以得到三硝基化合物。
官能团保护流程

官能团保护流程《官能团保护流程:化学世界里的“小心呵护”在化学这个奇妙又有点让人头疼的世界里,官能团保护流程就像是一场精心策划的保卫战。
你可以把官能团想象成一群性格各异的小怪兽,每个都有自己独特的本领和脾气。
有时候,化学家们就像超级英雄,但无奈这些小怪兽一不小心就会捣乱,所以得小心翼翼地给它们套上“保护罩”。
先说说为什么要搞这个官能团保护吧。
就好比你家里养了一群宠物,你想给其中一只洗澡,但又怕其他的在这个过程中搞破坏。
当我们在有机合成中,想要对一个分子里的某个官能团做点什么的时候,其他的官能团可能会跑来“搅局”。
比如说,你想把某个地方氧化一下,可旁边的羟基就像个调皮的小鬼,可能会抢先一步发生反应。
这时候,就得把羟基这个小调皮保护起来。
那保护的流程呢?首先是选择保护基,这就像是挑护盾一样。
这护盾可得合适才行,要容易加上去,等我们完成了主要的任务后,还能轻轻松松地取下来。
这就好比你给宠物套个项圈,不能太难戴,玩完了也得容易拆。
比如说,用酰氯来保护羟基,就像给羟基穿上了一件特制的衣服。
反应的时候呢,就像它们举办一场神秘的派对。
羟基被保护起来了,就在旁边安静地围观,其他该发生的反应顺利进行。
然而,这个流程也不是一帆风顺的。
就像你好不容易给宠物打扮好了,结果发现这打扮影响它吃饭睡觉了。
在化学里,可能保护基加错了或者反应条件不合适,那就会出现各种乱象。
有时候,这边保护起来了,那边又出新问题了,感觉像是在玩一个永远在补漏洞的游戏。
不过呢,当最后成功地完成了一系列操作,再把保护基去掉的时候,就像是一场精心策划的魔术表演顺利结束。
官能团毫发无损,而我们想要的产物也完美诞生。
这时候就特有成就感,就像你成功照顾好了一群调皮捣蛋却又无比重要的小怪物一样。
官能团保护流程虽然复杂又麻烦,但这也是化学合成中充满智慧和技巧的艺术展现啊。
它就像一场在微观世界里的巧妙博弈,让你在和那些看不见摸不着的小粒子互动的时候充满惊喜和挑战。
高中化学有机合成中的官能团保护

在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下而产生副反应,这样就不能达到预计的合成目标,因此,必须采取措施保护某些官能团,待完成反应后再除去保护基,使其复原。
1、保护措施必须符合如下要求①只对要保护的基团发生反应,而对其它基团不反应;②反应较易进行,精制容易;③保护基易脱除,在除去保护基时,不影响其它基团。
2、常见的基团保护措施①羟基的保护在进行氧化或某些在碱性条件下进行的反应,往往要对羟基进行保护。
a.防止羟基受碱的影响,可用成醚反应。
b.防止羟基氧化可用酯化反应。
②对羧基的保护羧基在高温或碱性条件下,有时也需要保护。
对羧基的保护最常用的是酯化反应。
③对不饱和碳碳键的保护碳碳双键易被氧化,对它们的保护主要用加成反应使之达到饱和。
;④对羰基的保护(以信息题出现)羰基,特别是醛基,在进行氧化反应或遇碱时,往往要进行保护。
对羰基的保护一般采用生成缩醛或缩酮的反应。
(缩醛或缩酮)(缩酮)生成的缩醛或缩酮水解又变成原来的醛或酮。
3、题例解析例1、已知下列信息:①烯键在一定条件下氧化可生成二元醇:②醛能发生如下反应生成缩醛:缩醛比较稳定,与稀碱和氧化剂均难起反应,但在稀酸中温热,会水解为原来的醛。
现有如下合成路线:试回答下列问题:(1)写出A、B的结构简式:________、________。
(2)写出反应Ⅲ的化学方程式:________。
解析:由题给信息知,欲使CH2=CH—CHO变为CH2OH—CHOH—CHO,需将C=C双键氧化,而—CHO 对氧化剂敏感,故应先进行保护,待C=C双键氧化完毕,再将醛基还原出来,故合成路线为:答案:(1)A:CH2=CH=CH(OC2H5)2 B:CH2OH—CHOH—CH(OC2H5)(2)CH2OH—CHOH—CH(OC2H5) CH2OH—CHOH—CHO+2C2H5OH例2、已知胺(R—NH2)具有下列性质:(Ⅰ)R—NH2+(CH3CO)2O R—NHCOCH3+CH3COOH(Ⅱ)R—NHCOCH3+H2O R—NH2+CH3COOH硝基苯胺是重要的化工原料,其合成路线如下:(1)a、c、e分别为________。
chapt3-官能团的保护
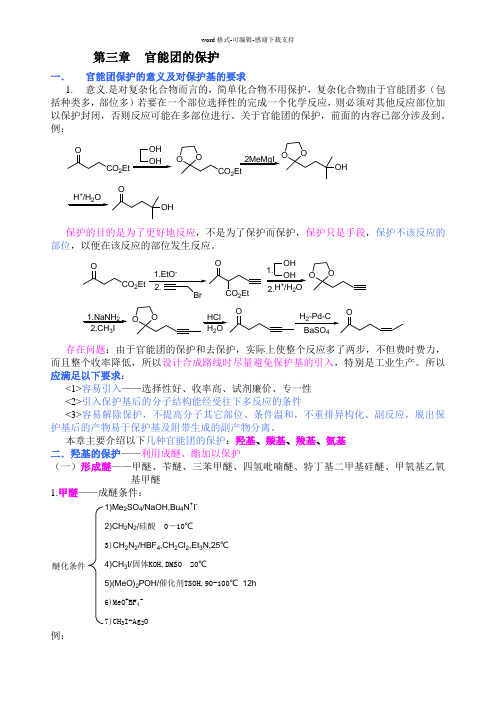
第三章 官能团的保护一. 官能团保护的意义及对保护基的要求1. 意义.是对复杂化合物而言的,简单化合物不用保护,复杂化合物由于官能团多(包括种类多,部位多)若要在一个部位选择性的完成一个化学反应,则必须对其他反应部位加以保护封闭,否则反应可能在多部位进行。
关于官能团的保护,前面的内容已部分涉及到。
例:CO 2EtOOH OHOOCO 2Et2MeMgI OOOH+2OOH保护的目的是为了更好地反应,不是为了保护而保护,保护只是手段,保护不该反应的部位,以便在该反应的部位发生反应。
CO 2EtOOH OH O O+2O-CO 2Et 1.2.1.NaNH 23OOHCl H 2O存在问题:由于官能团的保护和去保护,实际上使整个反应多了两步,不但费时费力,而且整个收率降低,所以设计合成路线时尽量避免保护基的引入,特别是工业生产。
所以应满足以下要求:<1>容易引入——选择性好、收率高、试剂廉价、专一性 <2>引入保护基后的分子结构能经受往下多反应的条件<3>容易解除保护,不提高分子其它部位、条件温和,不重排异构化、副反应,脱出保护基后的产物易于保护基及附带生成的副产物分离。
本章主要介绍以下几种官能团的保护:羟基、羰基、羧基、氨基 二.羟基的保护——利用成醚、酯加以保护(一)形成醚——甲醚、苄醚、三苯甲醚、四氢吡喃醚、特丁基二甲基硅醚、甲氧基乙氧基甲醚1.甲醚——成醚条件:1)Me 2SO 4/NaOH,Bu 4N +I -2)CH 2N 2/硅酸 0-10℃3)CH 2N 2/HBF 4,CH 2Cl 2,Et 3N,25℃4)CH 3I/固体KOH,DMSO 20℃5)(MeO)2POH/催化剂TSOH,90-100℃ 12h 6)MeO +BF 4-7)CH 3I-Ag 2O醚化条件例:OH+Me 2SO 4NaOHMeOSO 3Na+OCH3CH 2N 2+RCH 2OH RO -RCH 2OCH 3R 2CN 2ArOHR 2CHOAr CH2N 2ROHHBF 4ROCH 3+++N 2特别是酚羟基一般用MeO -醚保护,反应容易,解脱也容易,醇羟基形成甲醚较稳定,不易脱掉,故少用,在糖类化合物中羟基的保护勿用形成醚。
有关官能团的保护

有机合成中旳基团保护、导向基(高考必备) (一)基团保护在有机合成中,些不但愿起反映旳官能团,在反映试剂或反映条件旳影响下而产生副反映,这样就不能达到估计旳合成目旳,因此,必须采用对这些基团进行保护,完毕合成后再除去保护基,使其复原。
对保护措施一定要符合下列规定:①只对要保护旳基团发生反映,而对其他基团不反映;②反映较容易进行,精制容易;③保护基易脱除,在除去保护基时,不影响其他基团。
下面只简略简介要保护旳基团旳措施。
1、羟基旳保护在进行氧化反映或某些在碱性条件进行旳反映,往往要对羟基进行保护。
如避免羟基受碱旳影响,可用成醚反映。
避免羟基氧化可用酯化反映。
2、对氨基旳保护氨基是个很活泼旳基团,在进行氧化、烷基化、磺化、硝化、卤化等反映时往往要对氨基进行保护。
(1)乙酰化(2)对NR 2可以加H+ 质子化形成季铵盐,– NH 2也可加H+– OH–CH C 或酸–NH 2-C O-O -C O–成 – NH3而保护。
3、对羰基旳保护羰基,特别是醛基,在进行氧化反映或遇碱时,往往要进行保护。
对羰基旳保护一般采用缩醛或缩酮反映。
4、对羧基旳保护羧基在高温或遇碱性试剂时,有时也需要保护,对羧基旳保护最常用旳是酯化反映。
5、对不饱和碳碳键旳保护碳碳重键易被氧化,对它们旳保护重要要加成使之达到饱和。
(二)导向基在有机合成中,往往要“借”某个基团旳作用使其达到预定旳目旳,预定目旳达到后,再把借来旳基团去掉,恢复本来面貌,这个“借”用基团 我们叫“导向基”。
固然这样旳基团,要符合易“借”和易去掉旳原则,如由苯合成1,3,5 – 三溴苯,在苯旳亲电取代反映中,溴是邻、对位取代基,而1,3,5 – 三溴苯互居间位,显然不是由溴旳–COOH + R –OH H –CHO +2ROH H定位效应能引起旳。
但如苯上有一种强旳邻、对位定位基存在,它旳定位效应比溴旳定位效应强,使溴进入它旳邻、对位,这样溴就会呈间位,而苯环上本来并无此类基团,显然要在合成时一方面引入,完毕任务后,再把它去掉,正好氨基能完毕这样旳任务,由于它是一种强旳邻、对位定位基,它可如下引入:– H → – NO 2 → – NH 2 ,同步氨基也容易去掉:– NH2→ – N 2 → – H 因此,它旳合成路线是:根据导向基团旳目旳不同,可分为下列几种状况:1、致活导向 如果要合成 可以用 但这种措施产率低,由于丙酮两个甲基活性同样,会有副反映发生:但在丙酮旳一种甲基上导入一种致活基团,使两个甲基上旳氢旳活性有明显差别,这可用一种乙酯基(–C OO C2H 5)导入丙酮旳一种甲基上,则这个甲基旳氢有较大旳活性,使这个碳成为苄基溴攻打旳部位,因此,运用乙酰乙酸乙酯而不用丙酮,完毕任务后,把乙酯基OC 6O + C 6BrO C 6C 6Br O COOC C 2H 5O O COOC C6O COOC 1)2)△ C 6O OC6C 6Br碱C 6Br 碱OC 6C 6O水解成羧基,运用β– 酮酸易于脱羧旳特性将导向基去掉,于是得出合成路线为:2、致钝导向活化可以导向,有时致钝也能导向,如合成 氨基是很强旳邻、对位定位基,进行取代反映时容易生成多元取代物:如只在苯胺环上旳氨基旳对位引入一种溴,必须将氨基旳活性减少,这可通过乙酰化反映来达到,同步乙酰氨基是一种邻、对位定位基,而此状况下对位产物是重要产物:3、运用封闭特定位置来导向例如合成 ,用苯胺为起始原料,用混酸硝化,一方面苯胺易被硝酸氧化,另一方面,苯胺与硫酸还会生成硫酸盐,而 是一种H 2Br NH 2+ Br 2NH 2BrBr BrNH 2 BrNHCO BrBr 2H 2ONHCONH 2 NH 2NO–⊕间位定位基,硝化时得到,因此苯胺硝化时,要把苯胺乙酰化后,再硝化。
官能团之间的相互影响

官能团之间的相互影响在有机化学的学习中,掌握官能团的性质和它们之间的关系是学好有机化学的基本要求。
高中阶段必须掌握的官能团有:碳碳双键、碳碳叁键、卤素原子、羟基、醛基、羰基、羧基、氨基、硝基、磺酸基等。
有机物分子的官能团不同,则性质不同。
本文主要就官能团之间的影响,做一简要介绍:一、官能团的定位作用苯环上有连接有不同的基团或官能团,当进一步引入基团时,其引入的位置与原有官能团(基团)有关,而且不同的基团,还会使苯环的反应活性发生较大的变化。
1.邻对位定位基团,苯环的活性增强当苯环上连接烃基(甲基、乙基、苯基等)、氨基(-NH2、-NHR、-NR2,R为烷基)、羟基(—0H)、烷氧基(―0CH3、—OC2H5)等基团,使苯的反应活性增强,新引入的基团进入原基团的邻对位位置。
教材上制备硝基苯需要在浓硫酸、浓硝酸混酸与苯在55C条件下制得,而通常只能得到,很难得到二硝基化合物。
甲苯中新引入的一N02均处于甲基(一CH3)的邻位或对位。
在过量硝酸存在下,很容易得到三硝基化合物(TNT),这也看出甲基提高了苯环的活性。
2.邻对位定位基团——苯的活性减弱当苯环上连接有卤素原子(一F、一Cl、一Br、一I)—CH2CI、一CH= CH —等基团时,苯环的反应活性降低,这类反应比较特殊,往往需要在特殊溶剂、催化剂条件下才可能发生反应。
3.间位定位基当苯环上的取代基为-NO2、-SO3H、-SO2R、-COOH、-COOR、-CHO、-COR、-CN 等时,使苯环钝化,但邻位和对位钝化程度较间位大,在取代反应中,新取代基大多进入间位,形成间位异构体。
这类取代基称为有钝化作用的间位取代基。
如硝基苯在发烟硝酸、发烟硫酸存在下,长时间加热,可以制得少量的间硝基苯(),同时比较硝基苯的制法可以看出,硝基的引入使苯的活性降低,反应的条件明显提高。
二、官能团(基团)之间相互影响1.官能团(基团)之间的相互活化(1)苯环与烷烃基的相互活化当苯环上连接饱和链烃基时,苯环的活动性增强,使苯的取代变的比较容易,如苯硝化一般得到一硝基化合物,而甲苯硝化则可以得到三硝基化合物。
第7章基团的保护

精品资料
2、缩醛和缩酮衍生物
(1)四氢吡喃醚
O , TsOH
H2O ,H+
OH Et2O
第七章 官能团保护 (bǎohù)
精品资料
第一节 概 述
有 机 合 成 中, 如 果 分 子 中 有 几 个 部 位 或 官 能 团 可 能 发 生 反 应, 而 我 们 又 只 希 望 在 某 一 部 位 或 官 能 团 上 发 生 反 应, 比 较 直 接 的 办 法 是 采 用 选 择 性 的 反 应 条 件 和 试 剂。 但 是 在 复 杂 分 子 的 合 成 中, 许 多 情 况 下 会 找 不 到 这 样 的 直 接 条 件, 或 选 择 性 不 好, 于 是 必 须 采 用 另 外 的 办 法, 将 不 希 望 发 生 反 应 的 部 位 保 护 起 来 成 为 衍 生 物 形 式, 待 达 到 目 的 之 后 再 恢 复 原 来 的 官 能 团, 这 样 的 办 法 称 为 “保 护 基 团” (Protecting Groups) 法。
OO 混合型缩醛结构
OH
H+
ROH
-H+
O
O
RO O
H
一元醇在TsOH存在下与二氢吡喃作用生成四氢吡喃醚。
RO O
对碱、格氏试剂、烷基锂、氢化铝锂、烃化剂和酰化剂均稳定。
缺点是:不能用于在酸性介质中进行(jìnxíng)反应。此外,若用于旋光性醇,由 于引入了一个新的手性中心,将导致生成非对映异构体的混合物,分离困难,造 成产率降低。然而它在室温条件下,即能进行(jìnxíng)催化水解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
官能团的保护与定位
有机合成中有时会遇到这样的情况,本意只想对某个官能团进行处理,结果却影响了其它官能团。
“投鼠忌器”,防止对其它官能的影响,常常采用先保护后恢复的方法。
有时官能取代的位置有多种可能性,但要求必须上到规定的位置上,那就要进行官能团的定位措施。
一、防官能团受还原影响的保护与恢复
例1. 试以丙烯及其它必要的有机试剂为原料来合成CH 3COCH 20H ,无机试剂任选,写出有关反应的化学方程式。
已知:(1)R
C
R'
O
R
C
R'
O
C
H 2CH 2O R
C
R'
O HOCH 2CH 2OH H 2
(2)
R C OC 2H
O
RCH 2OH
C 2H 5OH
[简析]解有机合成题可以根据所要合成的物质,采用顺推、逆推齐推的思维方法。
依题给的有关信息反应的规律并结合所学的知识,可由顺推法初步形成以下的合成路线; CH 3CH=CH
CH 3CHBrCH 2Br
CH 3CHOH-CH 23COCOOH
Br 2
若将-COOH 转化-CH 2OH 就“OK ”了。
再结合信息反应(2)可知,先将-COOH 转化为-COOC 2H 5,然后在LiALH 4作催化剂时与H 2成即可。
但要注意在这一转化过程中,CH 3-CO-中的
O
也可
与H 2加成,故必须考虑将该官能团加以掩蔽和保护,最后重新将其 “复原”,这可以利用信息反应(2)的方法而达到目的。
从而易写出合成 CH 3-CO-CH 20H 的有关反应方程式如下 CH 3CH=CH 2+Br 2CH 3CHBr-CH 2Br
CH 3CHBr-CH 2Br CH 3CHOH-CH 2
CH
3CHOH-CH 2
3
COCOOH
CH 3COCOOH
C 2H 5
OH
CH 3COCOOC
2H 5+H 2O
CH 3COCOOC 2H 5+HOCH 2CH 2OH
CH 3CCOOC 2H 5
O O
其他略
二、防官能团受氧化的保护
例2.工业上用甲苯生产对羟基苯甲酸乙酯COOC 2H 5
O
H ,其生产过各如下图根据上
图
OH
CH
3
CH
3
I
CH 3
O CH 3
O CH 3
COOH
COOC 2H 5
OH
C 2H 5OH
IH
回答:
(1)有机物A 的结构简式为____________。
(2)反应⑤的化学方程式(有机物写结构简式,要注明反应条件):
(3)反应②的反应类型是__________(填编号,下同),反应④的反应类型属_________。
A.
取代反应 B.加成反应 C.氧化反应 D.酯化反应
(4)反应③的化学方程式(不用写反应条件,但要配平):____________。
(5)在合成线路中,设计第③和⑥这两步反应的目的是:____________________________。
答案:
(1)Cl
CH 3
(2)
O CH 3
HOOC
C 2H 5OH O CH 3
H
5C 2OOC (3)(4) (5)略
归纳小结:
1.酚羟基的保护
酚甲醚对碱稳定,对酸不稳定。
2.醛、铜羰基的保护
缩醛(酮)或环状缩醛(酮)对碱Grignard试剂,金属氢化物等稳定,但对酸不稳定。
3.羧基的保护
4.氨基的保护
三、官能团的定位
例3.维生素C(分子式为C6H8O6)可预防感染、坏血病等。
其工业合成路线如下图所示:
I.(1)上述①~③反应中,属于加成反应的有▲ (填数字序号)。
(2)A~G七种物质中与C互为同分异构体的有▲ (填字母序号)。
(3)比较D和G的结构可知,G可看成由D通过氧化得到。
工业生产中在第⑤步氧化的前后设计④和⑥两步的目的是▲ 。
(4)H的结构简式是▲ 。
Ⅱ.已知,
利用本题中的信息,设计合理方案由(用反应流程图表示,并注明反应条件)。
▲
例:由乙醇合成聚乙烯的反应流程图可表示为
解析:I题中④目的是保护羟基,只让另一个羟基氧化⑥为解保护II题中,就是要对酰卤的醇在定位在头一任一个羟基,那就要通过酮来,将其它两个羟基先“屏蔽”掉。
答案:、I (1)1 3 (2)A、D (3)保护D分子中其他羟基不被氧化
(4)
II。
