2 3金属与合金的晶体结构与结晶
第3讲:金属与合金的晶体结构

纯金属结晶的条件 就是应当有一定的 过冷度(克服界面能)
T
过冷度
T= T0 - Tn
T0
理论结晶温度
}T
ቤተ መጻሕፍቲ ባይዱTn
开始结晶温度
t
冷却曲线
3、 过冷现象
金属的实际结晶温度Tn低于理论结晶温 度T0的现象。 过冷度△T= T0-Tn,过冷是结晶的必要 条件。
同一金属,结晶时冷却速度越大,过冷 度越大,金属的实际结晶温度越低。
多晶体:这种实际上由许多晶粒组成的晶体称为多晶体。 其中每个小晶体的外形
多为不规则的颗粒,通 常称为晶粒。 晶粒与晶粒之间的界面
称为晶界。
晶粒(单晶体)
二、晶体的缺陷
晶体中原子完全为规则排列时,称为理想晶体。
实际上,金属由于多种原因的影响,内部总是存在着大 量缺陷。
根据晶体缺陷的几何特点,常分为:
一个空间格架,这种抽象的,用于描述原子在晶体中排列 形式的几何空间格架就叫晶格。
晶格中的每个点称为结点。晶格中各种不同方位的原子面 称为晶面。
2、晶胞 组成晶格的最基本几何单元称为晶胞。实际上整个晶格就是 由许多大小、形状和位向相同的晶胞在空间重复堆积而成 的。
3、晶格常数 晶胞的各棱边长为a、b、c和棱边夹角α、β、γ。其中,
2、 长大
晶体的长大过程是液体中原子迁移到固体表面, 使液—固界面向液体中推移的过程。
两种长大方式 —— 平面生长 与 树枝状生长。
平面长大
树枝状长大
三、晶粒大小对金属力学性能的影响
1、概念
1) 晶粒度——衡量晶粒大小的尺度,常以单位截面上晶粒数目或 晶粒的平均直径来表示。
2) 形核率——指单位时间、单位体积中所形成的晶核数目。 3) 长大速度——指单位时间内晶核向周围长大的平均线速度。
金相基础-金属结构与结晶

原子半径 0.05 nm
由正离子和共有电子以静电引力键合的形式即为金属键
3. 纯金属的晶体结构
体心立方晶格(如铁素体, Cr , Mo 等) 面心立方晶格(如奥氏体,Ni , Al 等) 密排六方晶格(如 Zn , Mg ,Cd 等)
金属化合物 ,其晶格类型和性能均不同于 任一组元。如渗碳体Fe3C。
Fe---C
Cu---Ni
间隙化合物--- Fe3C
一个碳原子在由6个铁原子构成的正八面体的体心位置 --- Fe3C晶胞结构
三种典型金属结构的晶体学特点
第二节 纯金属及合金的结晶
1. 纯金属 结晶 结晶金属由液态转变为固态的过程,称为凝固,亦称结晶。 过冷度实际结晶温度与理论结晶温度的差値,称为过冷度。 结晶过程分两步: 形 核-晶核的形成以非自发形核为主,如液体变固体:制造半导体
第一章 金相检验基础
第一节 金属与合金的晶体结构 1. “金属”定义和特点
金属是由众多原子(确切地说离子)组成的 集聚状态, 原子的排列有特定的规则。
金属的特征(不透明、高的导电导热性、有 金属光泽、高的强韧性和正的电阻温度系数等) 取决于金属原子的规则排列。 2. “晶体”定义和特点
原子呈规则排列的物质都是晶体。固体金属 都是晶体(部分的非金属也为晶体)。晶体具有 均匀性,各向异性, 固定的熔点,结构对称等 特点。
发达的 柱状晶
第三节 金属性能的分类
金属 性能
物理性能
化学性能
力学性能
工艺性能 #
密度 性
熔点
能 热膨胀
参
导热 数
耐腐蚀 抗氧化
强度 塑性 韧性 疲劳 硬度
金属与合金的结晶

度,也叫平衡结晶温度,是指液体的结晶速度与晶
体的熔化速度相等时的温度。
工程材料
第3章 金属与合金的结晶
4
实际上的结晶温度总是低于这一平衡结晶温度, 原因在结晶的能量条件上。 在自然界中,任何物质都具有一定的能量,而 且一切物质都是自发地由能量高的状态向能量低的 状态转变,结晶过程也同样遵循这一规律。
通常把组成合金的最简单、最基本,能够独立 存在的物质称为组元。但在所研究的范围内既不分解 也不发生任何化学反应的稳定化合物也可称为组元, 如Fe3C看作一组元。
2. 合金系
由两个或两个以上组元按不同比例配制成的一 系列不同成分的合金,称为合金系。
工程材料
第3章 金属与合金的结晶
37
3.相图
匀晶合金的结晶过程
T,C 1500 1400 c 1300 1200d 1100 1000 1083
T,C L
L
1455 a
L+ b
L
匀晶转变 L
L
Ni Cu 匀晶合金与纯金属不同,它没有一个恒定的熔点, t 100 而是在液、固相线划定的温区内进行结晶。 20 40 60 80 冷却曲线 Ni%
工程材料
第3章 金属与合金的结晶
39
工程材料
第3章 金属与合金的结晶
40
四、二元状态图的基本类型分析
1.二元匀晶相图
2.二元共晶相图 3.二元包晶相图 4.形成稳定化合物的相图 5.具有共析转变的相图 6.合金的性能与相图的关系
工程材料
晶体的结构和结晶

2.晶胞:晶体中有代表性的最胞 的三个棱边的尺 寸 a、b、c。用 埃(Å)表示。
1Å=10-8cm 各棱间的夹角用
、、表示。
晶体的结构和结晶
四、三种典型的晶体结构: 体心立方、面心立方、密排六方。
晶体的结构和结晶
晶体的结构和结晶
晶体的结构和结晶
▪ 密排六方晶格
晶格常数:底面边长 a 和高 c,
c/a=1.633
原子半径:r = 1 a
2 原子个数:6 配位数: 12 致密度:0.74 常见金属: Mg、Zn、 Be、Cd等
晶体的结构和结晶
§ 1-2 实际金属的晶体结构
一、 多晶体结构和亚结构 单晶体:晶体材料内部原子规律排列,位向不发 生改变的晶体。 多晶体:由许多晶格位向不同的小晶体构成的晶 体结构,称为多晶体。
位错上半部分原子受压,下半部分原子受拉。离位 错线越近晶格畸变越大,应力越大。
晶体的结构和结晶
▪ 位错密度:单位体积位错线总长度。
▪ = L/V(cm/cm3或1/cm2)
▪ 金属的位错密度为104~1012/cm2 ▪ 位错对性能的影响:以位错线为中心的管道区周
围晶格都发生了畸变,从而阻碍位错的运动,使 材料的强度提高。由于线缺陷的影响面比点缺陷 大的多,因此对材料性能的影响也大的多。 ▪ 减少或增加位错密度都可以提高金属的强度。
A
C B
D
晶界
晶体的结构和结晶
亚晶界
三、合金的晶体结构
1.几个重要概念:
▪ 合金:由两种或两种以上的金属或金属与非金属 元素组成的具有金属特性的物质叫合金。
▪ 组元:组成合金的独立的最基本的单元(一般是 一种元素或一种稳定的化合物)。
机械工程材料 第二章 金属的晶体结构与结晶

均匀长大
树枝状长大
2-2
晶粒度
实际金属结晶后形成多晶体,晶粒的大小对力学性能影响很大。 晶粒细小金属强度、塑性、韧性好,且晶粒愈细小,性能愈好。
标准晶粒度共分八级, 一级最粗,八级最细。 通过100倍显微镜下的 晶粒大小与标准图对 照来评级。
2-2
• 影响晶粒度的因素
• (1)结晶过程中的形核速度N(形核率) • (2)长大速度G(长大率)
面心立方晶 格
912 °C α - Fe
体心立方晶 格
1600
温 度
1500 1400
1300
1200
1100
1000
900
800
700 600 500
1534℃ 1394℃
体心立方晶格
δ - Fe
γ - Fe
γ - Fe
912℃
纯铁的冷却曲线
α – Fe
体心立方晶 格
时间
由于纯铁具有同素异构转变的特性,因此,生产中才有可能通过 不同的热处理工艺来改变钢铁的组织和性能。
2-3
• 铁碳合金—碳钢+铸铁,是工业应用最广的合金。 含碳量为0.0218% ~2.11%的称钢 含碳量为 2.11%~ 6.69%的称铸铁。 Fe、C为组元,称为黑色金属。 Fe-C合金除Fe和C外,还含有少量Mn 、Si 、P 、 S 、 N 、O等元素,这些元素称为杂质。
2-3
• 铁和碳可形成一系列稳定化合物: Fe3C、 Fe2C、 FeC。 • 含碳量大于Fe3C成分(6.69%)时,合金太脆,已无实用价值。 • 实际所讨论的铁碳合金相图是Fe- Fe3C相图。
2-2
物质从液态到固态的转变过程称为凝固。 材料的凝固分为两种类型:
金属的结晶构造和结晶过程

Logo
金属晶体模型
二、晶格、晶胞、晶格常数
Logo
晶体 原子呈有序排列
名 非晶体 原子呈无序排列
词 术 语
晶格 描述原子排列规律的空间格子 晶胞 组成晶格的最基本单元
晶格常数 晶胞的棱边长度
将晶体中原子排列,假想成空间的几何格架
Logo
二、晶格、晶胞、晶格常数
Logo
二、晶格、晶胞、晶格常数
Logo
一、晶体与非晶体
1、晶体:原子在三维空间内的周期性规则排列。
长程有序,各向异性。有固定熔点。
2、非晶体:原子在三维空间内不规则排列。
长程无序,各向同性。无固定熔点。
3、在自然界中除少数物质(如普通玻璃、松香、石蜡等) 是非晶体外,绝大多数都是晶体,如金属、合金、硅 酸盐,大多数无机化合物和有机化合物,甚至植物纤 维都是晶体。
1 538℃
1 394℃
912℃
L
δ-Fe
γ -Fe
α-Fe
(体心)
(面心)
(体心)
转变发生于固态 特点:在一定温度下进行
晶格类型发生变化
形核 + 长大
局部
整体
三、金属的同素异晶转变
纯铁的同素异构转变曲线
Logo
Logo
三、金属的同素异晶转变
❖ 金属的同素异晶有一定的转变温度并放出结晶潜 热。
❖ 金属的同素异晶转变具有较大的过冷倾向。
密排六方晶格
Logo
❖十二个金属原子分布在六方体的十二个角上, 在上 下底面的中心各分布一个原子, 上下底面之间均匀 分布三个原子。
❖ 密排六方晶胞的特征:
晶格常数:用底面正六边形的边长a和两底面之间 的距离c来表达, 两相邻侧面之间的夹角为120°, 侧面与底面之间的夹角为90°。
第三章金属的晶体结构与结晶

钢和铁是制造机器设备的主要材料,它们都是以铁和碳为 主而组成的合金,要了解钢和铸铁的本质,首先要了解纯铁的 晶体结构。固态物质按原子的聚集状态分为晶体和非晶体。
§3-1 金属的晶体结构 一、晶体的概念
金属在固态下一般都是晶体。 晶体:原子在空间呈规律性排列的固体物质; 注意:在固态时呈规律性排列,而在液态时金属原子的排列 并不规律。如图3-1(a) 金属的结晶就是由液态金属转变为固态金属的过程。
图3-5 实际金属晶体
在晶界上原子的排列不像晶粒内部那样有规则,这种原子 排列不规则的部位称为晶体缺陷。根据晶体缺陷的几何特点, 将晶体缺陷分为点缺陷、线缺陷和面缺陷三种。 1. 点缺陷:不规则区域在空间三个方向上的尺寸都很小, 例如空位、置换原子、间隙原子。如图3-6
空位
间隙原子
置换原子
间隙原子
图3-3 面心立方晶格Fra bibliotek 3.密排六方晶格:由两个简单六方晶胞穿插而成,晶胞为六 方柱体,柱体的12个顶角和上、下面中心上各排列一个原子, 在上、下面之间还有三个原子。如图3-4
图3-4 密排六方晶格
(一般规律)面心立方的金属塑性最好,体心立方次之,密排六方的 金属较差。
§3-2 实际金属的结构 一、多晶体结构
1.铸态晶:液态金属结晶后形成的晶体。将铸锭剖开可以 看到三个不同的晶区: 表面细小等轴晶粒层:组织致密,性能比较均匀一致,无 脆弱晶界面,有良好的热加工性能和力学性能,但易形成缩松。 柱状晶粒区:性能具有方向性;热加工性能较低;组织致 密,空隙和气孔较少,所以沿柱状晶粒的轴向强度高,韧性也 较好。 中心粗大等轴晶粒层:组织不均匀,还存在缩孔,缩松, 夹杂及偏析等缺陷。
图3-9 纯金属冷却曲线
金属的晶体结构与结晶

面缺陷能提高金属材料的强度。
晶体缺陷对性能的影响
1、当晶体中不存在位错时,强度最高 2、处于退火状态时,强度最低,位错 密度的增加或降低,都能提高金属的 强度 3、冷变形加工的金属,由于位错的增 加,强度提高
①使实际金属的强度远远小于理想金属 ②晶界处位错密度高,使其局部σ H ③对实际金属来说,晶体缺陷越多(尤其 位错),σ H δ (ψ ) ak
结晶时细化晶粒的方法
1、增加过冷度(为什么) 2、变质处理
(1)加入一些难熔形核剂,增加形核 率,细化晶粒,如液体铝中加入少量硼 (2)加入某些可熔物资,吸附在晶核 表面,降低长大速度,如在钢中加入钛、 硼、铝等,铸铁中加入硅、钙
3、振动,机械震动、超声波振动、 电磁振动
课堂练习
► 一、填空
1、自然界的固态物质,根据原子在内部的排列特 征可分为_____和________两大类。 2、金属的晶格类型主要有___________、 ___________、____________三大类。 3、晶体的缺陷主要有_______、_______、 __________。 4、根据溶质原子在溶剂中所占位置不同,固溶体 可分为_________和_________两种。 5、金属的结晶包括______和_______两个过程。
晶 向
晶向
晶 胞
2.1.2三种典型的金属晶格
1、体心立方晶格 体心立方晶格中: ① 原子半径 r ( 3 / 4)a ;
② 原子数为
1 8 1 2 个; 8
4 2 r 3 ④ 致密度 K 33 0.68 。 a
体心立方晶格
属这类晶格的金属有α-Fe、δ-Fe、Cr、 Mo、W、V、Na等。他们大都具有较高 的强度和韧性。
金属的结晶构造和结晶过程

Logo
一、晶体与非晶体
1、晶体:原子在三维空间内的周期性规则排列。
长程有序,各向异性。有固定熔点。
2、非晶体:原子在三维空间内不规则排列。
长程无序,各向同性。无固定熔点。
3、在自然界中除少数物质(如普通玻璃、松香、石蜡等) 是非晶体外,绝大多数都是晶体,如金属、合金、硅 酸盐,大多数无机化合物和有机化合物,甚至植物纤 维都是晶体。
➢ 在体心立方晶胞中, 每个角上的原子在晶格中同时 属于8个相邻的晶胞,因而每个角上的原子属于一个 晶胞仅为1/8, 而中心的那个原子则完全属于这个晶 胞。所以一个体心立方晶胞所含的原子数为 2个。
体心立方晶格
Logo
原子半径
❖晶胞中相距最近的两个原子之间距离的一半。 体心立方晶胞中原子相距最近的方向是体对 角线, 所以原子半径与晶格常数a之间的关系 为:
1 538℃
1 394℃
912℃
Lቤተ መጻሕፍቲ ባይዱ
δ-Fe
γ -Fe
α-Fe
(体心)
(面心)
(体心)
转变发生于固态 特点:在一定温度下进行
晶格类型发生变化
形核 + 长大
局部
整体
三、金属的同素异晶转变
纯铁的同素异构转变曲线
Logo
Logo
三、金属的同素异晶转变
❖ 金属的同素异晶有一定的转变温度并放出结晶潜 热。
❖ 金属的同素异晶转变具有较大的过冷倾向。
长。
二、金属的结晶过程
晶粒大小及其控制
Logo
细晶强化的基本原理 ↑v形核, ↓v长大
细晶强化的方法 -- 增大过冷度∆T (中、小型零件) ↑形核率, ↓v长大 -- 变质处理 ↑形核率 -- 震动、搅拌结晶 ↓v长大, ↑形核率
第二章 金属与合金的晶体结构与结晶

第二章 金属与合金的晶体结构与结晶第一节 金属的晶体结构自然界的固态物质,根据原子在内部的排列特征可分为晶体与非晶体两大类。
晶体与非晶体的区别表现在许多方面。
晶体物质的基本质点(原子等)在空间排列是有一定规律的,故有规则的外形,有固定的熔点。
此外,晶体物质在不同方向上具有不同的性质,表现出各向异性的特征。
在一般情况下的固态金属就是晶体。
一、晶体结构的基础知识(1)晶格与晶胞为了形象描述晶体内部原子排列的规律,将原子抽象为几何点,并用一些假想连线将几何点连接起来,这样构成的空间格子称为晶格(图2-1)晶体中原子排列具有周期性变化的特点,通常从晶格中选取一个能够完整反映晶格特征的最小几何单元称为晶胞(图2-1),它具有很高对称性。
(2)晶胞表示方法不同元素结构不同,晶胞的大小和形状也有差异。
结晶学中规定,晶胞大小以其各棱边尺寸a 、b 、c 表示,称为晶格常数。
晶胞各棱边之间的夹角分别以α、β、γ表示。
当棱边a b c ==,棱边夹角90αβγ===︒时,这种晶胞称为简单立方晶胞。
(3)致密度金属晶胞中原子本身所占有的体积百分数,它用来表示原子在晶格中排列的紧密程度。
二、三种典型的金属晶格1、体心立方晶格晶胞示意图见图2-2a。
它的晶胞是一个立方体,立方体的8个顶角和晶胞各有一个原子,其单位晶胞原子数为2个,其致密度为0.68。
属于该晶格类型的常见金属有Cr、W、Mo、V、α-Fe等。
2、面心立方晶格晶胞示意图见图2-2b。
它的晶胞也是一个立方体,立方体的8个顶角和立方体的6个面中心各有一个原子,其单位晶胞原子数为4个,其致密度为0.74(原子排列较紧密)。
属于该晶格类型的常见金属有Al、Cu、Pb、Au、γ-Fe等。
3、密排六方晶格它的晶胞是一个正六方柱体,原子排列在柱体的每个顶角和上、下底面的中心,另外三个原子排列在柱体内,晶胞示意图见图2-2c。
其单位晶胞原子数为6个,致密度也是0.74。
属于该晶格类型常见金属有Mg、Zn、Be、Cd、α-Ti等。
2 金属和合金的晶体结构
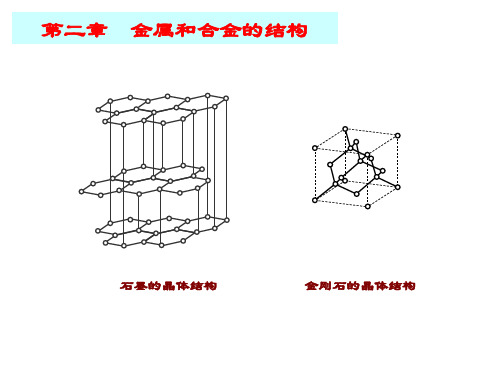
面心立方结构 fcc 密排六方结构 hcp
单斜
三斜
二、典型的金属晶体结构
§1纯金属的结构
1.体心立方晶格:bcc(body centred cubic)
具有bcc结构的金属: -Fe、Cr、W、Mo、V、 Nb等。
a
体心立方晶体模型
体心立方晶格
a
原子半径: 晶胞原子数: 配位数: 致密度:
r ( 3 / 4) a
空位
置换原子
晶体中的点缺陷
2)线缺陷—位错(dislocation)
§2实际金属的结构
E
EF—位错线
§2实际金属的结构
位错对晶格规律性的影响
在位错线附近,原子的错排使晶格发生畸变。
位错对晶体性能的影响
位错的存在可降低晶体
的强度。当位错大量产生后, 又可提高强度,同时使晶体 的塑性和韧性降低。
位错对晶体强度的影响
3)面缺陷:
§2实际金属的结构
晶体中存在一个方向上尺寸很小,另外两个方向上的尺寸相 对较大,呈面状分布的缺陷。有晶界、亚晶界和相界等。
>10 <10
晶界示意图
亚晶界示意图
晶界等面缺陷对晶体性能的影响
晶界等面缺陷能同时提高晶体的强度和塑性。 细化晶粒是改善金属力学性能的有效手段
总结:
实际的金属是一个多晶体,内部存在晶体缺陷。 空位
三、实际金属的结构
1.单晶体—晶格位向(或方 位)一致的晶体。 单晶体的特性:各向异性 现象。
§2实际金属的结构
原因:各晶面和各晶向上 原子排列的密度不一致。
z
0 x
y
2.多晶体
§2实际金属的结构
一块金属材料中包含着许多 小晶体,每个小晶体内的晶格 位向是一致的。
第三章 金属与合金的结晶

械 制
造
基
础
第三章 金属与合金的结晶
第三章 金属与合金的结晶
§3.1 纯金属的结晶
§3.2 合金的结晶
本章小结
习题
机 械
制
造
基
础
第三章 金属与合金的结晶
第三章 金属与合金的结晶
§3.1 纯金属的结晶
§3.2 合金的结晶
本章小结
习题
机 械
制
造
基
础
第三章 金属与合金的结晶
§3.1 纯金属的结晶
机
合金相图:表达温度、成分与相之间关系,又称为合金平衡图或 械
合金状态图。 合金相图是制订金属冶炼、铸造、锻压、焊接、热处理工艺的理
论基础。
制 造
基
础
第三章 金属与合金的结晶
习题
ቤተ መጻሕፍቲ ባይዱ
3-1 解释下列名词
结晶 过冷现象 过冷度 变质处理 晶核 同素异构转变 枝晶偏
析 共晶转变
3-2 晶粒大小对金属的力学性能有何影响? 生产中有哪些细化晶粒的
影响过冷度的因素:冷却速度
械 制
造
基
础
第三章 金属与合金的结晶
§3.1 纯金属的结晶
二、纯金属的结晶过程
形核
当液态金属冷却到接近理论结晶温度时,形成一
批类似于晶体中原子有规则排列的小集团。这些
小集团是不稳定的,时聚时散,此起彼伏。当温
度下降到低于理论结晶温度时,这些小集团中的
一部分就稳定下来,成为结晶核心。
理论结晶温度 实际结晶温度
开
结
始
晶
结
终
晶
了
实践证明,金属总是在一定的过冷度下结晶的,
金属材料的晶体结构与结晶

1.1.1 合金的晶体结构
合金是指由两种或两种以上的金属元素或由金属元素与非金属元素 组成的具有金属特性的物质。
组成合金的最基本的、独立的单元称为组元。由两个组元组成的合 金称为二元合金,由三个组元组成的合金称为三元合金,由三个以上组 元组成的合金称为多元合金。
合金中结构相同、成分相同和性能一致,并以界面相互隔开的组成 部分称为相。只有一种相组成的合金为单相合金,由两种或两种以上相 组成的合金为多相合金。用金相观察方法,在金属及合金内部看到的相 的形态、数量、大小和分布及相间结合状态称为显微组织。
非晶体
晶体
金属材料的晶体结构与结晶
1.晶体结构的基本知识
图2-1 晶体结构示意图
金属材料的晶体结构与结晶
1.常见的金属晶格类型 常见的金属晶格类型包括体心立方晶格、面心立方晶格和密排六方
晶格三大类。 1)体心立方晶格 body—centered cubic lattice 特点:b 较好。如:<912℃ Fe, Cr, Mo, V等。 含有2个原子体积组成。
图2-7 刃型位错示意图
金属材料的晶体结构与结晶
(3)面缺陷。面缺陷是指在晶体中呈面状分布(在两个方向上尺寸很大,在第 三个方向上尺寸很小)的缺陷。常见的面缺陷是晶界和亚晶界。
晶界是位向不同的晶粒间的过渡区,其宽度为5~10个原子间距。晶界区域的晶 粒的位向通过晶界的协调逐步过渡到相邻晶粒的位向,如图2-8(a)所示。亚晶界 是由位向相差很小的亚晶粒组成的,如图2-8(b)所示。晶界和亚晶界的原子排列 都不规则,会产生晶格畸变。因此,晶界和亚晶界均可提高金属的强度,改善塑性 和韧性。
图2-10 液态金属的结晶过程示意图
金属材料的晶体结构与结晶
第三章 金属与合金的结晶

第3章 金属与合金的结晶
凝固: 液体 ——> 固体(晶体 或 非晶体) 结晶: 液体 →晶体
液体 晶体
2015-1-4
材料科学与工程学院多媒体课件
3
第3章 金属与合金的结晶
§3.1 结晶的基本规律
一、冷却曲线:通过实验,测得液体金属在结晶时的 温度-时间曲线称为冷却曲线。
按处理均匀形核同样的方法可求出非均匀形核的临界半 径r’k和形核功ΔG’k:
2L 2LTm r' k GV LmT
(3-15)
3 1 2 3 cos cos (3-16) 2 G 4r kL 3 4
经比较知,均匀形核的临界半径与非均匀形核临界球冠半 径是相等的,而它们的临界形核功关系为:
2015-1-4 材料科学与工程学院多媒体课件 16
第3章 金属与合金的结晶
当 r<rk 时,晶胚的长大使系统自由能增加,晶胚不能长大。 当 r>rk 时,晶胚的长大使系统自由能降低,这样的晶胚称为
临界晶核,rk为临界晶核半径。 对 ΔG =-4/3πr3ΔGv+4πr2σ进行微分并令其等于零可得: 2Tm rk Lm T
σLα、σαβ、σLβ分别为各相应界面的表面能。 经整理化解可得:
2 3 cos cos3 4 3 2 r GV 4r L GV (3-14) 4 3
2015-1-4 材料科学与工程学院多媒体课件 23
第3章 金属与合金的结晶
结晶阻力:
液态金属结晶时,必须建立同液体相隔开的晶体界面而消 耗能量A(表面能)。这种产生新界面所需的能量A即为液态金属 结晶的阻力。
金属与合金的晶体结构

金属与合金的晶体结构一、引言金属与合金是一类重要的材料,它们具有优异的物理和化学性质,广泛应用于工业和科学领域。
金属与合金的晶体结构是影响其性能的重要因素之一。
本文将介绍金属与合金的晶体结构,包括晶体的组成、晶体的类型以及晶体的排列方式等。
二、金属晶体结构金属晶体结构由金属原子组成。
金属原子通常具有较大的离子半径和较小的电负性,因此它们倾向于形成金属键。
金属晶体结构可以分为以下几种类型:1. 面心立方结构(FCC)面心立方结构是最常见的金属晶体结构之一。
在面心立方结构中,金属原子分别位于晶格的每个面的中心以及每个顶点。
这种结构具有高度的对称性和密堆积性,因此具有较高的韧性和塑性。
2. 体心立方结构(BCC)体心立方结构是另一种常见的金属晶体结构。
在体心立方结构中,金属原子分别位于晶格的每个面的中心以及晶格的中心。
这种结构相对于面心立方结构来说,具有更高的密度和较低的韧性。
3. 密堆积六方结构(HCP)密堆积六方结构是一种较少见的金属晶体结构。
在密堆积六方结构中,金属原子分别位于晶格的每个面的中心以及每个顶点,形成六边形的密堆积结构。
这种结构具有较高的密度和较低的韧性。
三、合金晶体结构合金是由两种或更多种金属元素组成的混合物。
合金晶体结构可以由金属元素的晶体结构类型以及原子比例决定。
1. 固溶体固溶体是最常见的合金晶体结构之一。
在固溶体中,主要金属元素和溶质金属元素形成固溶体溶解体,原子之间的排列方式与纯金属相似。
固溶体可以分为完全固溶体和部分固溶体两种类型。
完全固溶体中,溶质原子完全溶解在主要金属晶体中;而在部分固溶体中,溶质原子只能部分溶解在主要金属晶体中。
2. 亚稳相亚稳相是指在合金中形成的相对于平衡相来说具有较低稳定性的晶体结构。
在亚稳相中,原子之间的排列方式发生改变,导致晶体结构和性能发生变化。
亚稳相的形成主要受到合金元素的浓度和固溶度限制的影响。
3. 间隙化合物间隙化合物是指合金中形成的一种特殊结构,其中金属原子和非金属原子之间的排列方式具有较高的有序性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
H F
A
E
B
① 位错也引起晶格畸变。金属强度与位错 密度的关系是:位错的存在可降低理想晶 体的强度,大量的位错又可使其强度提高。
② 生产中一般采用增加位错的办法提高 材料的强度。如加工硬化。
电子显微镜下的位错
透射电镜下钛合金中的位错线(黑线)
高分辨率电镜下的刃位错 (白点为原子)
BACK
3)面缺陷
晶界、亚晶界是晶体缺陷中的面缺陷,如图所示。 ① 晶界:指晶粒之间必然形成的交界面。 ② 亚晶界:指亚晶粒之间形成的交界面。亚晶粒是由被称为
镶嵌块的小晶粒组成的。
面缺陷能提高金属材料的强度和塑性。
总之,
2.1.4 合金的晶体结构
►一、合金的基本概念 ►1.合金是指由两种或两
种以上元素组成的具有 金属特性的物质。 ►组元的含义;多元合金 ►组成合金的元素相互作
用可形成不同的相。
黄铜 Al-Cu两相合金
► 2.相
单相
合金
► 所谓相是指金属或合金中凡成分
相同、结构相同,并与其它部分
有界面分开的均匀组成部分。
► 显微组织实质上是指在显微镜下 观察到的金属中各相或各晶粒的 形态、数量、大小和分布的组合。
► 固态合金中的相分为固溶体和金 属化合物两类。
► 二、合金的相结构
形 成的具有简单晶格结构 的间隙化合物。如
► M4X (Fe4N)、
► M2X (Fe2N、 W2C)、
► MX (TiC、VC、TiN)等。
► 间隙相具有金属特征和极高
VC的 结构
的硬度及熔点,非常稳定。
► 部分碳化物和所有氮化物属 于间隙相。
► b. 具有复杂结构的间隙化合 物
► 当r非/r金>0.59时形成复杂 结构间隙化合物。
2.1.3、实际金属的晶体结构
1.单晶体与多晶体 1)单晶体:把晶体看成是原子按一定几何规律作周期性排列 而成,即晶体内部的晶格位向是一致的。 2)多晶体 ① 位向不同的小晶体称为晶粒;
② 晶粒与晶粒之间的交界称为晶界。
晶粒
晶界
2.晶体缺陷
注:这些缺陷对金属的很多 性能有着极其重要的影响。
金属晶体中,原子排列或多或少地存在局部遭到破坏 呈现不完整或者偏离理想结构的区域,这一区域称为晶体缺 陷。
根据缺陷的几何形状,可分为: 1、点缺陷 2、线缺陷 3、面缺陷
1)点缺陷: 晶体中存在空位、间隙原子、置换原子都是晶格 的点缺陷,它们会导致“晶格畸变”的现象,如图所示。
间隙原子
晶格空位
点缺陷可提高材料的强度和硬度。
BACK
2)线缺陷
线缺陷就是晶格中的位错现象。常见的位错类型有刃型 位错、螺型位错等。如图所示。
► 晶体的这种“各向异性”的特点是它区别于非晶体的重要标 志之一。晶体的各向异性在其化学性能、物理性能和机械性 能等方面都同样会表现出来,即在弹性模量、破断抗力、屈 服强度、电阻率、磁导率、线膨胀系数以及在酸中的溶解速 度等许多方面都会表现出来,并在工业上得到了应用,如变 压器硅钢片利用了在不同晶向有不同磁化能力的特性。
► 单位长度晶向上的原子数称晶向原子密度。 ► 原子密度最大的晶面或晶向称密排面或密排方向。
密排面 数量 密排方向 数量
体心立方晶格 {110}
6
<111>
4
面心立方晶格 {111}
4
<110>
6
密排六方晶格 六方底面 1 底面对角线 3
► 2.1.3 晶体中的晶面与晶向
► 由于晶体中不同晶面和晶向上原子密度不同,因此在晶体中 不同晶面和晶向上原子结合力也就不同,从而在不同晶面和 晶向上显示出不同的性能,这就是晶体具有各向异性的原因。
► 如FeB、Fe3C、Cr23C6等。 Fe3C称渗碳体,是钢中重要 组成相,具有复杂斜方晶格。
Fe3C的晶格
► 化合物也可溶入其它元素原 子,形成以化合物为基的固 溶体。
高温合金中的Cr23C6
► 2.金属化合物的性能
(1)金属化合物的熔点一般较高,性能硬而脆。 (2)呈细小颗粒均匀分布在固溶体基体上时,将使 合金的强度、硬度和耐磨性明显提高,这一现象称为 弥散强化。 (3)是许多材料的重要组成相。 (4)工业用钢合金的组织一般是固溶体与少量的金 属化合物组成。
2
立方
面心 a
4
立方
密排 a、c 6 六方
0.68 8 0.74 12 a/2 0.74 12
a-Fe、 W、V
Al、 Cu
Zn、 Mg、 Be
► 4 晶体中的晶面与晶向
► 在金属晶体中,通过一系列原子所构成的平面,称为晶面, 表示晶面的符号称为晶面指数。通过两个以上原子的直线, 表示某一原子列在空间的位向,称为晶向,表示晶面的符号 称为晶面指数。单位面积晶面上的原子数称晶面原子密度。
③ 晶胞:晶格中能够完全反映晶格特征的最小几何单元。
晶胞各边的尺 寸a、b、c称晶格 常数,其大小以
0 表示;其棱边 夹角用α、β、γ表 示。
④晶格尺寸:用晶格常数表示。立方晶格中a=b=c,用一个 常数a表示即可。
⑤原子半径 :原子在某种晶格中的原子半径,等于晶胞中 原子密度最大的方向上相邻两原子的中心之间距离的一半 。⑥致密度:把原子看成刚性小球,原子所占体积与晶胞体积之 比K。用来表示原子在晶格中排列的紧密程度。
体心立方晶格
2.面心立方晶格
面心立方晶胞中: ① 原子半径为 r 2 a ;
4
② 原子数为 1 8 1 6 4 ;
82
③ 致密度为0.74 。 属这类晶格的金属有γ-Fe、
Ni、Al、Cu、Pb、Au等。
面心立方晶格
3.密排六方晶格
计算密排六方 晶体原子数
① 晶格常数用a、c表示,
晶体 : 固态下原子在物质内部作有规则排列即为晶体。 非晶体 : 固态下物质内部原子呈现无序堆积状况的,称为
非晶体。
2.1.1、晶体结构的基本知识
① 空间点阵:把构成固体的基本质点看成空间的几何点,这 些点的空间排列阵容即为空间点阵。
② 晶格:用一些假想线条将点阵中的质点连结起来所构成的 空间格架称为晶格。
► 组成元素原子半径、电化学特性 相近,晶格类型相同的置换固溶 体,才有可能形成无限固溶体。
► 间隙固溶体都是有限固溶体。
固 溶 体
化 合 物
Cu-Zn有限固溶体
► 3. 固溶体的性能 ► 随溶质含量增加, 固溶体
的强度、硬度增加, 塑性、 韧性下降—固溶强化。 ► 产生固溶强化的原因是 溶质原子使晶格发生畸 变及对位错的钉扎作用。 与纯金属相比,固溶体的强度、硬度高,塑性、韧 性低。但与化合物相比,其硬度要低得多,而塑性 和韧性则要高得多。
属元素,如C、N、B 等,而溶剂元素一般 是过渡族元素。 形成间隙固溶体的一
般规律为r质/r剂<0.59。
间隙固溶体都是无序 固溶体。
► 2. 固溶体的溶解度 ► 溶质原子在固溶体中的极限浓度。
溶解度有一定限度的固溶体称有 限固溶体。
► 组成元素无限互溶的固溶体称无 限固溶体。
Cu-Ni无限固溶体
第二章 金属与合金的晶体结构
► 2.1 金属的晶体结构 ► 2.1.1 晶体结构的基本知识 ► 2.1.2 三种典型的金属晶格 ► 2.2 实际金属的晶体结构 ► 2.3 合金的晶体结构
第三章 金属与合金的结晶
第一节 纯金属的结晶
第二节 合金的结晶
复习旧课:金属材料的力学性能
本节要求: 1、了解晶体与非晶体,晶格、晶胞、晶格
两相 合金
► (一)固溶体
► 合金中其结构与组成元素之一的晶体结构相构相同的元素称溶剂。
其它元素称溶质。 固溶体是合金的重要组成相,实际合
金多是单相固溶体合金或以固溶体为 基的合金。 按溶质原子所处位置分为置换固溶体 和间隙固溶体。 1.固溶体的分类
晶面
晶
晶
格
面
晶
晶 向 晶向
胞
2.1.2三种典型的金属晶格
1、体心立方晶格 体心立方晶格中:
① 原子半径 r ( 3 / 4)a ;
② 原子数为 1 8 1 2 个;
8
④ 致密度
。
2 4 r3
K
3 a3
0.68
属这类晶格的
金属有α-Fe、δ-Fe、
Cr、Mo、W、V、
Na等。
Cu-Ni置换固溶体 Fe-C间隙固溶体
► (1) 置换固溶体 ► 溶质原子占据溶剂晶格某些结点位置所形成的固溶体。 ► 溶质原子呈无序分布的称无序固溶体,呈有序分布的
称有序固溶体。
黄铜置换固溶体组织
► (2) 间隙固溶体 ► 溶质原子嵌入溶剂晶格间隙所形成的固溶体。 ► 形成间隙固溶体的溶质元素是原子半径较小的非金
常数的意义。 2、掌握三种常见的金属晶格类型,常见的
晶体缺陷,合金的相结构。 3、掌握纯金属和合金的结晶,二元合金匀
晶相图的建立,二元合金匀晶、共晶结晶过 程分析,合金性能与相图的关系。
第二章 金属与合金的晶体结构
思考:晶体与非 而同且状还态金具、属有不与较同非优成金良分属的也相工会比艺有,性很不能大仅。的具晶即差有体使异良的两金。好差属的者异材力性?料学能,性上不能同、金化属学、性不能, 2.1 金属的晶体结构
两者比值c/a≈1.633 ;
② 原子数为 1 12 1 2 3 6;
6
2
③ 原子半径 r 1 a ; 2
④ 致密度为0.74 。
属这类晶格的 金属有Mg、 Zn、Be、Cu等。
密排六方晶格
► 小小结:
晶体 类型
晶格 常数
晶胞 原子 数
原子 半径
致密 度
