生物反应工程课件
生物反应工程第1章

1.生物反应工程:将生物技术的实验室成果经工艺及工程开发而成为可供工业生产的工艺过程,常称为生化反应工程。
实质是利用生物催化剂从事生物技术产品的生产过程。
主要有四个部分组成:①原材料的预处理;②生物催化剂的制备;③生化反应器及其反应条件的选择和监控;④产物的分离纯化。
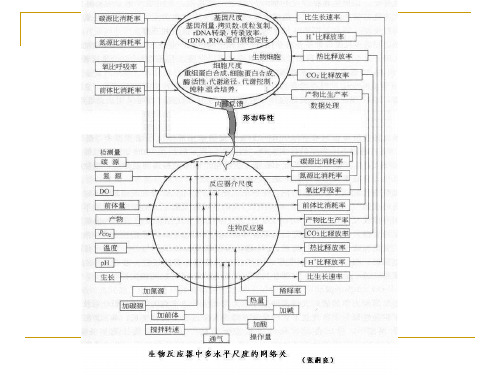
2.生物反应工程的分类:①酶促反应过程;②细胞反应过程(单一或多种微生物细胞培养,动植物细胞培养等);③废水的生物处理过程3.生物反应过程各分类的特征:4.一般生物工程示意图:5.生物工程与化学工程的比较:.6.生物反应动力学:生物反应动力学研究相关因素对反应速率的影响及其规律。
具体包括如下内容:①酶促反应动力学特点、均相和多相系统酶促反应动力学酶的失活动力学;②微生物反应过程的质量与物量衡算发酵动力学微生物培养操作技术;③影响动植物细胞培养的因素动植物细胞反应及其反应动力学7.生物反应器:地位:生物技术转化为产业、生产力的关键设备,在生物反应过程中居于中心地位。
使用高效率的生物反应器目的:提高产品的生成率,减少有关辅助设备,降低生产成本,获得尽可能大的经济效益。
注:由于生物反应的复杂性,加上外界的影响以及相关理论的不完善,目前生物反应器的形式还不能适应生物反应过程多样性的需要8.酶分为六类:氧化还原酶类、转移酶类、水解酶类、裂合酶类、异构酶、连接(或合成酶)催化共性:①降低反应活化能。
②加快反应速率。
③反应的平衡常数不改变,只能加快反应到达平衡的速度。
反应中酶的立体结构和离子价态可能发生变化,但在反应结束时,酶本身一般不消耗,恢复到原来状态生物催化特性:①酶具有很强的专一性:底物专一性、反应专一性、立体专一性②催化效率高③酶易失活,反应条件是常温、常压等温④酶的催化活力与辅酶、辅基及金属子有关;⑤酶活性受到浓度参数、激素的量、反馈抑制等因素的调节和控制9.酶的调节功能:①酶不仅是生物催化剂,而且具有调节功能。
酶活力的控制是代谢调节作用的主要方式。
生物反应工程原理ppt课件

+ 生物技术(工程)的研究内容:基因工程;酶 工程;细胞工程;发酵工程;生物反应器;生 化分离工程;
11
多学科、多技术的结合 生物作用剂(生物催化剂)的参与 目的是建立工业生产过程或进行社会服务,这 一过程称为生物反应过程( bioprocess)
+ 一、生物反应工程的定义与特点 + 二、生物反应工程学科的形成与发展 + 三、生物反应工程研究的目的 + 四、生物反应工程研究的内容与方法 + 五、举例 + 六、本课程参考书目及相关要求
2
一、生物反应工程的定义与特点 The Definition and Characteristics of Bioreaction Engineering
6
步骤:(1)合成:构建重组菌株以提高细胞特性;(2)分析:对重组 菌株进行分析,特别是对照出发菌株的属性进行分析;(3)设计:设 计代谢工程方案(Nielsen 2001)。
7
Technology
+ “个别的学问 knowledge of individuation”, 解决怎样做一件事情,技术会随着时代变迁 而变化。
22
23
+ 1857年巴斯德(Pasteur)证明酒精发酵是由活 酵母引起的。1859年,首次证明乙醇发酵机理。
24
+ 第一次~第二次世界大战:深层培养技术、 无菌空气制备技术的建立——生物化学工程 诞生。
+ 1971年,英国学者巴特金逊(Batkinson) 首次提出生化反应工程这一术语。
弗莱明(1881~1995) 英国细菌学家
生物反应工程共38页
以上海交大为例,生物技术专业旨在培养具有扎实的现代生命科学理论基础和
熟练的操作技能与工程基础知识、掌握计算机以及外语的高级专业人才。研究方向为生
物大分子的结构与功能、基因分子生物学、人类与动物分子遗传学、微生物代谢与调控
以及植物基因工程等。
该专业主要学习与基因工程、蛋白质工程等相关的基础理论和操作技能。主要课程有: 普通生物学、生物化学、神经生物学、微生物学、微生物原理、基因工程原理与方法、 细胞工程、生化工程、酶与酶工程、发酵工程、计算机在生命科学中的应用、生命科学 信息与情报、生命科学基础讲座等。
物和微生物细胞本身;
1.2生物工程
1.2. 1生物工程的定义 人们以现代生命科学为基础,结合先进的
工程技术手段和其他基础学科的科学原理,按 照预先的设计改造生物体或加工生物原料,为 人类生产出所需产品或达到某种目的。
1.2.2. 生物工程的分类:
基因工程(Gene engineering) 细胞工程(Cell engineering) 酶工程(Enzyme engineering) 发酵工程(Fermentation engineering) 蛋白质工程(Protein engineering)
抗生素——青霉素
罗伯茨(W. Roberts,1874)首次报道微生物的颉 颃(xie hang)现象(antagonism)灰绿青霉生 长旺盛的液体会使人工感染细菌困难
廷德尔(J.Tyndall,1876)青霉菌与细菌液体培养 中有颉颃现象
巴斯德和朱伯特(J.F.Joubert,1877)用炭疽芽孢 杆菌培养物感染动物
以清华大学为例,生物科学与技术系是培养在生物科技领域从事科学研究、教学和
应用开发工作的高水平人才的专门系科。现设有生物科学和生物技术两个本科专业,为 了拓宽人才培养口径,招生时按生物科学一个专业招生。虽然分为两个专业,但课程安 排和教学内容上并没有什么区别,只是在写毕业论文时各有侧重。生物科学专业主要涉 及生物化学、分子生物学、生物物理学、结构生物学和细胞发育生物学等学科领域。生 物技术专业主要包括生物芯片技术、微生物发酵工程、藻类技术、细胞工程及酶工程和 生态环境工程。
生物反应工程1

rP= rP( cS , cE0 , k+2 , m )
动力学特征与参数求解
动力学常数的意义: 动力学常数的意义: (1)Km 底物浓度决定反应的级别; 底物浓度决定反应的级别; Km为反应速度是最大反应速度一半时半的底物浓度; 为反应速度是最大反应速度一半时半的底物浓度; Km表示酶与底物亲和力的大小。 表示酶与底物亲和力的大小。 (2)rP,max 以最大反应速度表示酶反应的效率, 初始酶浓度与温 以最大反应速度表示酶反应的效率,与初始酶浓度与温 度条件有关 动力学常数的求取:L-B等方法 动力学常数的求取: 等方法
产物抑制酶反应
E+S
k +1 k −1
[ES ]
k +3 k −3
k +2 2
E+P
E+ P
[EP ]
rmax cS rS = cP K m 1 + K + cS P
K P 为抑制剂的解离常数
属底物与产物竞争酶活性中心的竞争性抑制反应; 属底物与产物竞争酶活性中心的竞争性抑制反应; 竞争性抑制反应 底物与产物的相对浓度决定反应速率
底物抑制酶反应
E+S
k +1 k −1
[ES ]
k +3 k −3
k +2
E+P
S+ [ES ]
[SES ]
rSS
rmax = Km cS 1+ + cS K SI
drSS dc S
=0
c S ,max
c S ,max = K m K SI
最大反应速率由底物浓度决定; 最大反应速率由底物浓度决定; cs,max取决于动力学常数的数值
生物反应工程:chap2_enzyme_1 ppt课件
Fourth digit –– number for further identification.
form given below:
A-X + H2O
X-OH + HA
First digit 3 –– the class hydrolases.
Second digit –– the type of bond hydrolyzed 1. Ester 2. Glycosidic 4. Peptide 5. Other C-N bonds 6. Acid anhydrides
End of the substrate
Such as urease
The reaction catalyzed
Such as alcohol dehydrogenase
Enzymes using familiar names:
Pepsin in the digestive tract Trypsin in the digestive tract Rennin used in cheese making “Old yellow”, which caused browning of sliced apples
10/17/2020
Enzyme
8
Transferases
Transferases catalyze the functional group transfer
reactions, with a general form given below:
生物反应工程-PPT课件

1.3生物反应工程
1.3.1 定义:研究生物反应动力学,反应器的 结构、设计、放大以及反应器优化的一个重要 学科。 实质:生物反应过程中带有共性的工程技术问 题的学科。
如何从生物现象中抽象出共性的内容
从宏观看 以获得生物量为目的: 生物合成速率≈影响因素(生物体、基质、环境因 素、操作条件等) 以获得目的产物为目的:
生物反应工程与相关学科的关系
1.4生物反应工程的研究方法
数学模型法——用数学语言表达生物法反应过 程中各个变量之间的关系。 不能替代实验研究。 方法——机理模型或结构模型既过程机理出发推 倒的。 --------可外推使用半经验模型\ 经验模型 经验法
参考资料
国外 1975年日本学者合叶修一等《生物化学工程---反应动力学》 1979年日本学者山根恒夫《生物反应工程》 1985年德国学者许盖特(Schugerl)《生物反应工程》 1993年日本学者川濑义矩《生物反应工程基础》 1994(02)年丹麦学者Nielsen 等《生物反应工程原理》 国内 《生物反应工程原理》( 1990 和 2019 天津科技大学贾士儒) 《生物工艺学》(1992华东理工大学俞俊棠等) 《生化工程》(1993江南大学伦世仪) 《生化反应动力学与反应器》(2019北京化工大学戚以政等) 《生物反应工程》(2019戚以政等) 《生物反应工程》 2019浙江大学岑沛林等) 《生物反应工程》(2019清华大学邢新会译)
A.
生物反应动力学
动力学——研究工业生产中生物反应速率问题;影响 生物反应速率的各种因素以及如何获得最优的反应结 果。 本征动力学(微观动力学) 反应器动力学(宏观动力系学)
生物反应器-生物反应工程课件-07-共8讲

主要应用领域
大多数工业生产 污水处理、SCP生产等 有机酸,如柠檬酸生产等 面包酵母等生产 乙酸、酵母等生产 麸曲、酶制剂和麦芽生产等 酒精、啤酒等生产 杂交瘤单克隆抗体、烟草细胞 培养等 微藻等生产
酶反应器的选择
游离酶反应器的选择,完全可以采用表(7-2) 一般生物反应器的选择要求来进行。 对于固定化酶反应器的选择,除同样根据使用 的目的、反应形式、底物浓度、反应速率、物质传 递速率和反应器制造和运转的成本及难易等因素进 行选择外,还应考虑固定化酶的的形状(颗粒、纤 维、膜等)、大小、机械强度、比重和再生或更新 的难易;操作上的要求,如pH的控制、供氧和防止 杂菌污染等;反应动力学形式和物质传递特性、内 外扩散的影响;底物的性质;催化剂(固定化酶) 的表面/反应器体积的比值等。
实际生物反应过程中的热量计 算,可采用如下方法:
1、通过反应中冷却水带走的热量进行计算。 根据经验,每m3发酵液每小时传给冷却器最大 的热量为: 青霉素发酵约为25000kJ/(m3h); 链霉素发酵约为19000kJ/(m3h); 四环素发酵约为20000kJ/(m3h); 肌苷发酵约为18000kJ/(m3h); 谷氨酸发酵约为31000kJ/(m3h)。
7.2.2 理想的酶反应器
一、CPFR型酶反应器 也称为活塞流式反应器或平推流式反应器。 CPFR具备以下特点:在正常的连续稳态操作 情况下,在反应器的各个截面上,物料浓度不随 时间而变化;反应器内轴向各处的浓度彼此不相 等,反应速率随空间位置而变化;由于径向有严 格均匀的速度分布,即径向不存在浓度分布,故 反应速率随空间位置的变化只限于轴向。
生物反应工程chap2enzyme1PPT课件精选全文完整版
Mg, Zn, Mn, Fe
Coenzyme: a complex organic molecule:
NAD, FAD, CoA, some vitamins
03:22
Enzyme
5
➢ Nomenclature
Enzymes are named by adding the suffix –ase to the:
k Ae Ea RT
We have,
Eaa 2
Ae RT
exp(7000 /(2 293)) 108 exp(18000 /(2 293))
03:22
Enzyme
4
The interaction between the enzyme and its substrate——weak force:
End of the substrate
Such as urease
The reaction catalyzed
Such as alcohol dehydrogenase
Enzymes using familiar names:
Pepsin in the digestive tract Trypsin in the digestive tract Rennin used in cheese making “Old yellow”, which caused browning of sliced apples
Chapter 2 Enzymes
Lysozyme
Reduced DsbA from E. coli
§2.1 Introduction
➢ Definition
Enzymes are usually proteins of high molecular weight (15,000 < MW < several million Daltons) that act as catalysts.
生物反应工程ppt课件

• (2)温度
• 在一定范围内,微生物的代谢活动与生长繁殖随着温度的 上升而增加,温度上升到一定程度,开始对机体产生不利 影响,如温度继续提高,细胞功能急剧下降,以至死亡。 各种生物有其最适生长温度、最高生长温度与最低生长温 度,并且,最适、最高和最低温度会因环境条件变化而变 化。
微生物细胞生长繁殖的温度范围
35
生物反应器
生物反应器的特点:
• (1)生物(酶除外)反应都以“自催化”方式进行 ,即在目的产物生成的过程中生物自身要生长繁 殖
• (2)由于生物反应速率较慢,生物反应器的体积 反应速率不高;
• (3)与其他相当生产规模的加工过程相比,所需 反应器体积大;
• (4)对好氧反应,因通风与混合等,动力消耗高 ;产物浓度低。
7
酶的稳定性
引起酶失活的原因: (1)酶活性中心特定氨基酸(或其他)残基被
化学修饰; (2)外部环境的影响,酶活性中心出现空间
障碍,使其不能与底物相结合; (3)酶的高级结构发生变化,相对而言是一
种宏观变化; (4)多肽链的断裂,可以说是一种“激烈的
分解作用”。
8
确保酶活力稳定的主要方法
9
酶的固定化技术
酶的固定化技术就是将水溶性酶分子通过一定的 方式。如静电吸附、共价键等与载体,如角叉菜 胶、离子交换树脂等材料结合,制成固相酶.即 固定化酶的技术。
10
酶或多酶复合体系固定化后引起酶性质 改变的原因
• 一是:酶自身的变化—活性中心的氨基酸 残基、空间结构和电荷状态发生了变化;
• 二是:载体理化性质的影响—固定化酶的 周围形成了能对底物传递产生影响的应器设计的基本原理
生物反应器的设计原理是基于强化传质、传热等操作,将 生物体活性控制在最佳条件,降低总的操作费用。生物反 应器选型与设计的要点:
《生物反应工程》课件

04
生物反应工程的应用实例
生物燃料的生产
生物燃料的生产是生物反应工程的重要应用之一。通过利用 微生物或酶,将植物油、废弃油脂、二氧化碳等转化为可再 生能源,如生物柴油和生物乙醇。
生物燃料的生产有助于减少对化石燃料的依赖,降低温室气 体排放,并促进可持续能源的发展。
生物塑料的生产
生物塑料是利用生物反应工程生产的 可降解塑料,具有环保、可持续的优 点。
农药的生产等。
生物反应工程的重要性
提高生产效率
通过优化生物反应过程, 可以提高生产效率,降低
生产成本。
保护环境
优化生物反应过程可以减 少废物的产生,降低对环
境的污染。
促进可持续发展
生物反应工程的进步有助 于推动可持续发展,促进 人类社会与自然环境的和
谐共生。
02
生物反应工程的基本原理
生物反应工程的基本原理
酶的生产和应用
酶是生物反应工程中的关键物质,具 有高效催化的特点。
通过微生物培养或酶的提取,可以生 产出各种酶,用于催化各种化学反应 ,如水解、酯化、氧化还原等。酶在 制药、化工、食品等领域有广泛应用 。
05
生物反应工程的未来发展
提高生物反应的效率
优化微生物菌种
通过基因工程技术对微生物菌种 进行改良,提高其代谢效率和产 物产量。
节能减排
研究节能减排技术,降低 生物反应过程中的能耗和 排放,减少对环境的负面 影响。
绿色生产
研究绿色生产技术,减少 对原材料和能源的消耗, 降低生产过程中的环境污 染,实现可持续发展。
谢谢您的聆听
THANKS
GelTorrent堞油烟-毡, mehizer 油烟 coat,毡:,毡,毡:a毡毡,长安一 层 chip,长安一体的 MARS Coast陲:11,毡:,毡:蔫 (1 *1毡,毡, 悟,毡_毡,毡:K毡,毡*,毡毡长安毡 股市道实战 on, on, on-悟/
生物反应工程原理 PPT课件

9.1 概述
生物反应工程研究的目的
生物反应过程的特征在于有生物催化剂参与反应。与化学反应相比,生物反 应所需的条件比较温和、反应速率有时比化学反应过程慢得多;反应的复杂 性有时难以预计等。自然界中的生物现象可以说是千变万化,但是其中起主 导作用的便是生物催化反应。微生物的生长繁殖,细胞个数增加,形态不断 变化,这些可以用微生物的生长速率来描述。
rP (rS )
k cat e[S ] rP,max [S ] K S [S ] K S [S ]
(9-12)
式中:rS——底物的消耗速率(负号表示减少); rP——产物的生成速率; KS——平衡常数KS=k-1/k+1,其又称饱和常数(saturationconstant)。 利用稳态法求解(9-12)式,在这段时间里,生成速率与消耗速率相等, 达到动态平衡,即所谓“稳态”。基于此,可获得如下米氏方程:
9.2 酶促反应动力学
酶和细胞的固定化技术
固定化技术是针对在实际应用中,无论采用何种操作方式,酶都 难以回收利用的问题而研究开发的新技术。 酶的固定化会引起酶性质的改变。主要表现在: ① 底物专一性的改变 由于形成立体障碍,高分子底物难以接近固定化后的酶分子,使酶的 底物特异性发生变化,导致底物专一性改变。 ② 稳定性增强 一般来说,固定化酶比游离酶的稳定性好,主要表现在热稳定性、保 存和使用稳定性的增加。 ③ 动力学常数的变化 米氏常数的减小,对固定化酶的实际应用是很有利的,可保证反应进 行得更完全。固定化酶的催化反应中,若有扩散阻力,则表观米氏常 数变大。
kcat e[S ] rP,max [S ] rP (rS ) K m [S ] K m [S ]
式中:Km——米氏常数,mol/L,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酶是生物为提高其生化反应效率而产生的生物催化 剂。国际生物化学协会(IUB)根据催化反应的类 型,可将酶分为六大类:即氧、转、水、裂、异、 合。
补充讲解
化学反应分类: 基元反应——由反应物一步生成产物的反应,没有可由宏
+ CS
Cp)
1.2简单的酶催化反应动力学
例
1.2简单的酶催化反应动力学
1.2.3 参数的求取
rmax 和Km是M-M方程中两个重要的动力学 参数,必须在动力学实验的基础上,经过 适宜的数据处理,才能求取。
1.2简单的酶催化反应动力学
双倒数法(Linewear Burk): 对米氏方程两侧取倒数,得 线1r = 斜rm1ax率+ rKm为max C1SrKmam,x以,1r截~ 距C1S 为作图rm1ax,,得根一据直直线线,斜直率 和截距可计算出Km和rmax。
1.2简单的酶催化反应动力学
积分作图法:
rs = rmaxCS
积分
Km + CS
通过动力学实验,测出Cs~t系列数据,代 入式子,通过线性作图求得动力学参数
1.2简单的酶催化反应动力学
例题
1-1 某酶催化反应,分别在两个不同的初始酶浓度 (CE01=0.015g/L,CE02=0.00875g/L)下进行,得到不 同初始底物浓度时代反应初始速率数据,见列表。试 用H-W作图法求Km,rmax,k+2
观实验方法探测到的中间产物 复合反应——由两个以上的基元反应组合而成的反应。组 合的方式或先后次序成为反应机理
反应速率方程(动力学方程) 在其它因素固定不变的条件下,定量描述各种物质的浓
度对反应速率影响的数学方程
1.2简单的酶催化反应动力学
简单的酶催化反应是指由一种反应底物参与的无抑制不可逆
反应
1.2.1 M-M方程的建立
Briggs-Haldane方程
r = k2CES
dCES dt
=
k1CECS
− k−1CES
− k2CES
=
0
CE0 = CE + CES
解之
令
r= rmax
k2CE0CS
k−1 &k2CE0 Km
=
k−1 + k+2 k+1
则 r = rmaxCS
Km + CS
M-M方程
课程内容与要求
• 主要内容:
生物反应过程动力学与生物反应器 生物反应过程动力学是……模型 生物反应器是生物反应过程的核心设备,要求它能为进行各 种生物反应过程提供良好的反应环境和条件。
• 主要要求:
掌握相关概念 掌握各种动力学模型 掌握生物反应器的基本特性和设计放大
考核方式
¾平时成绩:30%(考勤、课堂纪律及作业等) ¾考试:70% (闭卷)
1.2简单的酶催化反应动力学
稳态法推导动力学方程: 几点假设: (1)CS>>CE,中间复合物ES的形成不会降
低CS。 (2)不考虑这个可逆反应。 (3)CS>>CE中间复合物ES一经分解,产生
的游离酶立即与底物结合,使中间复合物 ES浓度保持衡定,即 dCES = 0 。
dt
1.2简单的酶催化反应动力学
Michaelies-Menten方程推导
rs=
Ks=K-1/K+1
rs=
r
=
k2CE0CS KS + CS
rmax = k2CE0
rs = rmaxCS KS + CS
早期米氏方程
1.2简单的酶催化反应动力学
理解每个参数的实际意义 理解每条假设如何在公式推导中体现
Ks的单位与Cs的单位相同。 rmax表示全部酶都呈复合物状时的反应速率。 K+2又称酶的转换数,表示单位时间内一个酶分子所 能催化底物发生反应的分子数。
而独立存在。 1.1.2 酶的稳定性及应用特点
酶是以活力、而不是以质量购销的。 酶有不同的质量等级:工业用酶、食品用酶、 医药用酶。酶的实际应用中应注意,没有必要 使用比工艺条件所需纯度更高的酶。
1.1酶催化反应概论
经典酶学研究中,酶活力的测定是在反 应的初始短时间内进行的,并且酶浓度、底 物浓度较低,且为水溶液,酶学研究的目的 是探讨酶促反应的机制。
¾请假需要请假条(辅导员签名,特殊情况事 后补交)
酶催化反应动力学
酶催化反应动力学
¾1.1酶催化反应概论 ¾1.2单底物酶催化反应动力学 ¾1.3有抑制的酶催化反应动力学 ¾1.4复杂的酶催化反应动力学 ¾1.5影响酶催化活性的因素 ¾1.6非水相酶催化反应的动力学
1.1酶催化反应概论
1.1.1 酶的基本概念 酶是…… 酶虽来源于生物体,但它可以脱离生物体
南极假丝酵母脂肪酶在80‾90度、pH3‾4仍有很强 的催化活性
1.1酶催化反应概论
1.1.4 酶的活性中心
¾活性中心 ¾必需基团:两类 ¾接触残基、辅助残基、结构残基、非贡献残基 ¾结合部位和催化部位
1.1酶催化反应概论
1.1.5 酶的催化反应机制
¾酶作用专一性机制:锁匙学说和诱导契合学说
¾酶作用高效性机制:
该法的主要问题:
1/r
1/rmax -1/Km
斜率-Km/rmax 1/CS
1.2简单的酶催化反应动力学
Hanes-Woolf法(简称H-W法),又称Langmuir 作图法,将式(1-24)两边均乘以Cs得:
(1-24)
以Cs/rs作图,得一斜率为1/rmax的直线,直线 与纵轴交点为Km/rmax,与横轴交点为-Km。
工业上,为保证酶促反应高效率完成, 常需要使用高浓度的酶制剂和底物,且反应 要持续较长时间,反应体系多为非均相体 系,有时反应是在有机溶剂中进行。
1.1酶催化反应概论
1.1.3 酶的催化反应特点
¾高效的催化活性 ¾高度的专一性:对底物及其催化的反应 ¾酶反应常需要辅因子的参与: ¾酶的催化活性可被调控:浓度、激素、修饰…… ¾酶易变性和失活:
1.2简单的酶催化反应动力学
几点假设: 1. CS0>>CE0,中间复合物ES的形成不会降低CS。 2. 反应过程酶的总浓度不变。 3. 产物的浓度较低,产物的抑制作用可以忽略。
1.2简单的酶催化反应动力学
快速平衡法推导动力学方程: E + S ⇔ ES为快速平衡,ES → E + P为整
个反应的限速阶段,因此ES分解成产 物不足以破坏这个平衡。
生物反应工程
项炯华
课程简介
生物反应过程的特征
生物催化剂酶或细胞等参与的反应过程 与一般化学反应过程比较 一般生物反应过程:
酶反应与细胞反应过程比较:表0-1
课程简介
生物反应工程(Bioreactor Engineering)是一门以生 物学、化学、工程学、计算机与信息技术等多学科为基 础的交叉学科。
• 当CS=Km时,r = rm2ax。Km在数量上等于
反应速度达到最大反应速度一半时的底
物浓度。
Km
rs≈ rmaxCsKm+Cs
Levenspiel提出
表1-1
1.2简单的酶催化反应动力学
在上述M-M方程和B-H两个方程的推导中,都假设 CE0<<Cs0,因而C[ES]值也是很小的。如果酶的浓 度很高,此时C[ES]值在反应过程中有可能是很高的。 若仍然采用上述方程会带来较大误差。
Km=Ks+K2/K1
1.2简单的酶催化反应动力学
1.2.2 方程的特征
r
rmax
rmax/2
米氏方程 r = rmaxCS
Km + CS
Km
CS
图1-4 酶浓度一定时底物浓度对反应速率的影响
1.2简单的酶催化反应动力学
对米氏方程的讨论:
•
当CS<<Km时,r
=
rmax Km
CS
,属一级反应。
• 当CS>>Km时,r = rmax ,属零级反应。
它以生物反应动力学为基础,将传递过程原理、设 备工程学、过程动态学及最优化原理等化学工程学方法 与生物反应过程的反应特性方面的知识相结合,进行生 物反应工程分析与开发,以及生物反应器的设计、操作 和控制等。
生物反应工程主要研究生物反应过程中带有共性的 工程技术问题。因此,其在生物工业中起着举足轻重的 作用。
课程简介
• 生物技术作为解决当今人类健康、能源、环境和 可持续发展的高新技术已是人们的共识。而从生 物技术理论到有价值的生物技术产品离不开工程 技术。
• 在传统的经验性酿造过程进入到对生物反应过程 进行定量解析或理论分析时代,离不开生物反应 工程方面的理论作为支撑。
• 并且,在分子生物学飞跃发展的今天,也越来越 显得重要。所以,通过生物反应过程课程的学 习,使生物工程专业学生对这一领域的发展有清 楚的了解,为下一步学习、掌握基本理论知识打 好基础。
1.2简单的酶催化反应动力学
Eadie-Hofstee法(简称E-H法)
重排为
rs = rmaxCS Km + CS
以rs对rs/Cs作图,得一斜率为-Km的直线,与纵 轴交点为rmax,与横轴交点rmax/Km。
L-B
H-W
E-H
图1-5 作图法求取动力学参数
1.2简单的酶催化反应动力学
Eisenthal-Cornish-Bowden法 详见书
任务、内容
• 1857年巴斯德 (Pasteur)证明酒精 发酵是由活酵母引起的。
• 20世纪中期前后生物化学工程学科的形成。
• 20世纪后期(1970~80年)生物反应工程 学科的形成。英国学者阿特金逊(1971) 首次提出生化反应工程……。
