大鼠肿瘤坏死因子α(TNF-α)说明书
小鼠肿瘤坏死因子α(TNF-α)说明书
200 ng/L
3 号标准品
150µl 的 4 号标准品加入 150µl 标准品稀释液
100 ng/L
2 号标准品
150µl 的 3 号标准品加入 150µl 标准品稀释液
50 ng/L
1 号标准品
150µl 的 2 号标准品加入 150µl 标准品稀释液
2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、
计算 以标准物的浓度为横坐标,OD 值为纵坐标,在坐标纸上绘出标准曲线,根据样品的
OD 值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与 OD 值计算出标
准曲线的直线回归方程式,将样品的 OD 值代入方程式,计算出样品浓度,再乘以稀释倍数, 即为样品的实际浓度。 注意事项 1.试剂盒从冷藏环境中取出应在室温平衡 15-30 分钟后方可使用,酶标包被板开封后如未
用完,板条应装入密封袋中保存。 2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。 3.各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。一次加样时间最好
控制在 5 分钟内,如标本数量多,推荐使用排枪加样。 4. 请每次测定的同时做标准曲线,最好做复孔。如标本中待测物质含量过高(样本 OD 值
大于标准品孔第一孔的 OD 值),请先用样品稀释液稀释一定倍数(n 倍)后再测定,计 算时请最后乘以总稀释倍数(×n×5)。 5. 封板膜只限一次性使用,以避免交叉污染。 6.底物请避光保存。 7.严格按照说明书的操作进行,试验结果判定必须以酶标仪读数为准. 8.所有样品,洗涤液和各种废弃物都应按传染物处理。 9.本试剂不同批号组分不得混用。 10. 如与英文说明书有异,以英文说明书为准。 保存条件及有效期 1.试剂盒保存:;2-8℃。 2.有效期:6 个月
肿瘤坏死因子(TNF)

肿瘤坏死因子( tumor necrosis factor,TNF )是由巨噬细胞分泌的一种小分子蛋白,正常人血清为4.3±2.8 mg/L。
TNF-α主要由单核—巨噬细胞分泌;TNF-β主要由活化的T 淋巴细胞分泌。
TNF在体内外均能刺激IL-1的产生,不耐热,70℃30min失活。
1975年Carswell等发现接种BCC的小鼠注射LPS后,血清中含有一种能杀伤某些肿瘤细胞或使体内肿瘤组织发生血坏死的因子,称为肿瘤坏死因子。
1985年Shalaby把巨噬细胞产生的TNF命名为TNF-α,把T淋巴细胞产生的淋巴毒素(lymphotoxin,LT)命名为TNF-β。
TNF-α又称恶质素。
TNF的蛋白特性1、人TNF-α前体由233个氨基酸组成(26 kDa),其中包含由76个氨基酸残基组成的信号肽,在TNF转化酶TACE的作用下,切除信号肽,形成成熟的157个氨基酸残基的TNF-α(17 kDa)。
由于没有蛋氨酸残基,故不存在糖基化位点,其中第69位和101位两个半胱氨酸形成分子内二硫键。
人类TNF-α与小鼠TNF-α有79%氨基酸组成同源性,TNF-α的生物学作用似无明显的种属特异性。
最近有人报道通过基因工程技术表达了N端少2个氨基酸(Val、Arg)的155氨基酸人TNF-α,具有更好的生物学活性和抗肿瘤效应。
此外,还有用基因工程方法,将TNF-α分子氨基端7个氨基酸残基缺失,再将8Pro、9Ser和10Asp 改为8Arg、9Lys和10Arg,或者再同时将157Leu改为157Phe,改构后的TNF-α比天然TNF体外杀伤L929细胞的活性增加1000倍左右,在体内肿瘤出血坏死效应也明显增加。
TNF-α和β发挥生物学效应的天然形式是同源的三聚体。
2、人类TNF-β分子由205个氨基酸残基组成,含34氨基酸残基的信号肽,成熟型TNF-β分子为171个氨基酸残基,分子量25kDa。
大鼠肿瘤坏死因子α(TNF-α)说明书
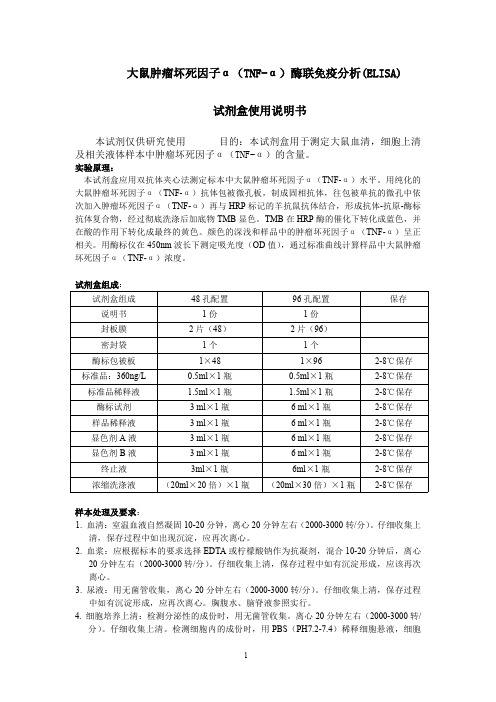
大鼠肿瘤坏死因子α(TNF-α)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定大鼠血清,细胞上清及相关液体样本中肿瘤坏死因子α(TNF-α)的含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中大鼠肿瘤坏死因子α(TNF-α)水平。
用纯化的大鼠肿瘤坏死因子α(TNF-α)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入肿瘤坏死因子α(TNF-α)再与HRP标记的羊抗鼠抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的肿瘤坏死因子α(TNF-α)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中大鼠肿瘤坏死因子α(TNF-α)浓度。
试剂盒组成:试剂盒组成48孔配置96孔配置保存说明书1份1份封板膜2片(48)2片(96)密封袋1个1个酶标包被板1×481×962-8℃保存标准品:360ng/L0.5ml×1瓶0.5ml×1瓶2-8℃保存标准品稀释液 1.5ml×1瓶 1.5ml×1瓶2-8℃保存酶标试剂3ml×1瓶6ml×1瓶2-8℃保存样品稀释液3ml×1瓶6ml×1瓶2-8℃保存显色剂A液3ml×1瓶6ml×1瓶2-8℃保存显色剂B液3ml×1瓶6ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存样本处理及要求:1.血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
肿瘤坏死因子TNFα

人肿瘤坏死因子α(TNF-α)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定人血清,细胞上清及相关液体样本中肿瘤坏死因子α(TNF-α)的含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中人肿瘤坏死因子α(TNF-α)水平。
用纯化的人肿瘤坏死因子α(TNF-α)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入肿瘤坏死因子α,再与HRP标记的肿瘤坏死因子α(TNF-α)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的人肿瘤坏死因子α呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人肿瘤坏死因子α(TNF-α)浓度。
试剂盒组成:试剂盒组成48孔配置96孔配置保存说明书1份1份封板膜2片(48)2片(96)密封袋1个1个酶标包被板1×481×962-8℃保存标准品:450pg/ml0.5ml×1瓶0.5ml×1瓶2-8℃保存标准品稀释液 1.5ml×1瓶 1.5ml×1瓶2-8℃保存酶标试剂3ml×1瓶6ml×1瓶2-8℃保存样品稀释液3ml×1瓶6ml×1瓶2-8℃保存显色剂A液3ml×1瓶6ml×1瓶2-8℃保存显色剂B液3ml×1瓶6ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存样本处理及要求:1.血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
肿瘤坏死因子-α、白细胞介素-6在高血压心肌肥厚大鼠实验中的意义

【 图分 类 号】 5 22 中 R 4 .
【 献标 识 码】 文 A
【 文章 编号】1 7 — 2 0( 0 2)2( 一 0 3 0 6 3 7 1 2 1 0 c)0 2 — 3
The sg fc c ft o c o i a t r i ni an e o um r ne r ssf c o -a nd i e luk n-6 n e pe i e i a nt re i i x rm nt o y c r u pe t o hy fm o a di m】 jcieT v s gt eepes no h n ea ds nf a c b u mo ers co-  ̄(N - 0 i— Ab ta t Obet oi et aet x rsi f a g n i icn ea o tu r coi f trc T F c ,n v n i h o c gi t n sa tr u i- ( - )nsrm a dmycril f oada h p r o h as Me o s2 s rrt w r a dml dvd el kn 6 I 6 i eu n oada o cril y e rp yrt. t d 0Wi a s eern o y i - e L my t h t a i e t t ogo p : o ada y et p ygo p( G a d cnrl ru C ) E c ru o tie 0 rt T ep ra d i o w ru s myc ri h p r oh ru O ) n o t o p(G . ahgop cna d 1 as h at n l r og n . i l
RD 豚鼠肿瘤坏死因子α 中文说明书 600pg

SYSTEMS®中文说明书UNIONHONEST酶联免疫吸附测试Enzyme linked lmmunosorbent Assay_____________________________________________________________________________________ 豚鼠(Guinea Pig)肿瘤坏死因子α(TNF-α) ELISA检测试剂盒本试剂仅供研究使用试验原理:TNF-Α试剂盒是固相夹心法酶联免疫吸附实验(ELISA).已知TNF-Α浓度的标准品、未知浓度的样品加入微孔酶标板内进行检测。
先将TNF-Α和生物素标记的抗体同时温育。
洗涤后,加入亲和素标记过的HRP。
再经过温育和洗涤,去除未结合的酶结合物,然后加入底物A、B,和酶结合物同时作用。
产生颜色。
颜色的深浅和样品中TNF-Α的浓度呈比例关系。
试剂盒内容及其配制:试剂盒成份96孔配置48孔配置96/48人份酶标板1块板(96T)半块板(48T)塑料膜板盖1块半块标准品:600pg/ml 1瓶(1.0ml)1瓶(0.5ml)空白对照1瓶(1.0ml)1瓶(0.5ml)标准品稀释缓冲液1瓶(8.0ml)1瓶(4.0ml)生物素标记的抗TNF-Α抗体1瓶(8.0ml)1瓶(4.0ml)亲和链酶素-HRP 1瓶(12ml)1瓶(5ml)洗涤缓冲液1瓶(20ml)1瓶(10ml)底物A 1瓶(6.0ml)1瓶(3.0ml)底物B 1瓶(6.0ml)1瓶(3.0ml)终止液1瓶(6.0ml)1瓶(3.0ml)自备材料:1. 蒸馏水。
2. 加样器:5ul、10ul、50ul、100ul、200ul、500ul、1000ul。
3. 振荡器及磁力搅拌器等。
4.样品收集、处理及保存方法:1、血清……操作过程中避免任何细胞刺激。
使用不含热原和内毒素的试管。
收集血液后,1000×g离心10分钟将血红细胞迅速小心地分离。
大鼠(Rat)肿瘤坏死因子α(TNF-α)ELISA检测试剂盒说明书

大鼠(Rat)肿瘤坏死因子α(TNF—α)ELISA检测试剂盒说明书大鼠(Rat)肿瘤坏死因子α(TNFα)ELISA检测试剂盒使用说明书检测原理试剂盒采纳双抗体一步夹心法酶联免疫吸附试验(ELISA)。
往预先包被肿瘤坏死因子α(TNFα)抗体的包被微孔中,依次加入标本、标准品、HRP标记的检测抗体,经过温育并彻di洗涤。
用底物TMB显色,TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最后的黄色。
颜色的深浅和样品中的肿瘤坏死因子α(TNFα)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),计算样品浓度。
样品收集、处理及保存方法1.血清:使用不含热原和内毒素的试管,操作过程中避开任何细胞刺激,收集血液后,3000转离心10分钟将血清和红细胞快速当心地分别。
2.血浆:EDTA、柠檬酸盐或肝素抗凝。
3000转离心30分钟取上清。
3.细胞上清液:3000转离心10分钟去除颗粒和聚合物。
4.组织匀浆:将组织加入适量生理盐水捣碎。
3000转离心10分钟取上清。
5.保存:假如样本收集后不适时检测,请按一次用量分装,冻存于20℃,避开反复冻融,在室温下解冻并确保样品均匀地充分解冻。
自备物品1.酶标仪(450nm)2.高精度加样器及枪头:0.510uL、220uL、20200uL、2001000uL3.37℃恒温箱操作注意事项试剂盒保存在28℃,使用前室温平衡20分钟。
从冰箱取出的浓缩洗涤液会有结晶,这属于正常现象,水浴加热使结晶wan全溶解后再使用。
试验中不用的板条应立刻放回自封袋中,密封(低温干燥)保存。
浓度为0的S0号标准品即可视为阴性对比或者空白;依照说明书操作时样本已经稀释5倍,最结束果乘以5才是样本实际浓度。
严格依照说明书中标明的时间、加液量及次序进行温育操作。
全部液体组分使用前充分摇匀。
试剂的准备20×洗涤缓冲液的稀释:蒸馏水按1:20稀释,即1份的20×洗涤缓冲液加19份的蒸馏水。
肿瘤坏死因子α抑制剂对糖尿病大鼠肾脏的保护作用

肿瘤坏死因子α抑制剂对糖尿病大鼠肾脏的保护作用侯嘉声;程东生;吴睿;汪年松;王锋;赵婷;周炉;刘宣辰;林莹莹;张光远;赵清;尹建永;梁如练【摘要】目的探讨肿瘤坏死因子α(TNF-α)抑制剂对糖尿病肾小管间质病变的作用及其相关机制.方法采用链脲霉素(STZ)诱导建立1型糖尿病大鼠模型,并将大鼠分为模型组(不给予药物治疗)、IgG治疗组(给予IgG 1 mg/kg治疗,每周一次,腹腔注射,治疗12周)和TNF-α抑制剂治疗组(给予阿达木单抗1 mg/kg治疗,每周一次,腹腔注射,治疗12周),另外设立正常对照组.测定各组大鼠肾功能指标、氧化应激指标、炎性因子及炎症小体Nod样受体蛋白3(nod like receptor protein3,NLRP3)水平.结果与IgG治疗组相比,TNF-α抑制剂能够显著减少糖尿病大鼠的白蛋白尿、抑制氧化应激、保护肾小球和肾小管损伤,并减少肾小球和肾小管的NL-RP3炎症小体表达(P<0.05).结论 TNF-α抑制剂可减轻糖尿病肾小管间质病变,其机制可能是通过抑制NLRP3炎性小体的表达来发挥作用.【期刊名称】《临床肾脏病杂志》【年(卷),期】2019(019)004【总页数】5页(P282-286)【关键词】肿瘤坏死因子α;糖尿病肾病;肾小管间质病变;NLRP3炎症小体【作者】侯嘉声;程东生;吴睿;汪年松;王锋;赵婷;周炉;刘宣辰;林莹莹;张光远;赵清;尹建永;梁如练【作者单位】200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233上海,上海市第八人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233 上海,上海交通大学附属第六人民医院肾内科;210009 南京,东南大学附属中大医院泌尿科;200233 上海,上海交通大学附属第六人民医院心内科;200233 上海,上海交通大学附属第六人民医院肾内科;200233上海,上海市第八人民医院肾内科【正文语种】中文糖尿病肾病(DN)是引起中国人群发生终末期肾病的第2位病因,更是欧美人群发生终末期肾病的最主要病因[1]。
TNF-a说明书

人(human)肿瘤坏死因子a(TNF-a)说明书本试剂盒仅供研究使用标本:血清或者血浆一、试剂组成精密度微孔板96孔 (Microtitration Strips) 1块 2~8℃干燥保存酶标偶合液 (Conjugate ) 1瓶 12.0毫升 2~8℃冷藏保存标准品 (Standard) 5瓶各1.0毫升 2~8℃冷藏保存呈色剂A (Substrate A) 1瓶 6.0毫升 2~8℃避光冷藏保存呈色剂B (Substrate B) 1瓶 6.0毫升 2~8℃避光冷藏保存终止液 (Stopping Solution) 1瓶 6.0毫升室温保存20倍浓缩洗涤液 (Rinsing Buffer x 20) 1瓶 60.0毫升 2~8℃冷藏保存5倍浓缩样品稀释液 (Diluent x 5) 1瓶 15.0ml 2~8℃冷藏保存英文说明书,中文说明书各一份室温保存二、注意事项1. 此试剂为体外检测试剂,效期内使用,试剂应视为传染物,不同总批号的试剂不能混用。
2.使用前应将盒内各试剂取出。
室温放置至少30分钟,3.浓缩洗涤液出现结晶后,请于37℃孵育15分钟。
4.浓缩样品稀释液出现结晶后,请于37℃孵育15分钟5.若24小时内进行实验,标本可存放于2~8℃。
不需及时实验,标本-20℃保存,避免反复冻融。
6.在反复清洗微孔板,并扣干微孔中的残余液体,否则将降低精确度,造成吸光度偏离的假像。
7.加样完毕后,应注意轻微摇动微孔反应条,以便使孔中的液体充分混匀。
8.试剂盒保存于2~8℃,请勿冷冻,有效期请见盒内标示。
三、实验前准备1.使用前应将盒内各试剂取出,室温放置至少30分钟。
2.准备各种实验仪器及材料,如微量移液器,吸头,医用蒸馏水等3.浓缩洗液与医用蒸馏水1︰19倍稀释后成为应用洗涤液4.浓缩样品稀释液与医用蒸馏水1︰4倍稀释成应用样品稀释液5.用应用样品稀释液来稀释样品,按照1:100的体积比来稀释样品如10μl的样品加入到1ml的应用样品稀释液中,充分混匀待用。
肿瘤坏死因子—α在急性胰腺炎中的作用

肿瘤坏死因子—α在急性胰腺炎中的作用细胞因子在急性胰腺炎发病机制的作用日益被重视,其中肿瘤坏死因子-α(TNF-α)作为急性胰腺炎发病过程中极其重要的因子及其在疾病中的作用也同样被重视。
TNF-α不仅通过对胰腺、肠道、肝脏等多器官的损伤,导致机体出现严重的炎症反应,还介导其他炎症因子的释放,加重对机体的损伤。
标签:急性胰腺炎;TNF-α急性胰腺炎(acute pancreatitis)是临床上的急腹症,其发病机制目前尚不明确。
自从1988年Rinderknecht提出了白细胞过度激活学说[1]后,细胞因子在急性胰腺炎发病机制中的作用逐渐被重视,肿瘤坏死因子-α(TNF-α)作为急性胰腺炎始动因子的作用已经得到证实[2]。
现就促炎性细胞因子TNF-α在急性胰腺炎中的作用综述如下。
1 肿瘤坏死因子1.1 TNF-α的产生1975 年Carswell等发现了能使荷瘤鼠肿瘤发生出血、坏死而对正常组织细胞无明显作用的肿瘤细胞毒因子,Old将其命名为肿瘤坏死因子(tumor necrosis factor TNF)。
TNF主要分为由活化T细胞产生的TNF-β和活化的单核细胞产生的TNF-α。
在人体内,产生TNF-α的主要细胞是单核巨噬细胞。
Ramudo等的研究表明,胰腺相关性腹水时胰腺腺泡细胞中的TNF-α量增加,而非单核细胞或淋巴细胞,可见腺泡细胞是真正产生TNF-a的炎症细胞[3]。
1.2 TNF-α的调节正常人循环中的TNF-α水平为(10~80)pg/mL。
在人和动物,能诱导产生TNF-α物质为LPS,静脉输入LPS后2h,血清TNF-α达到高峰,4h内恢复到基线水平。
部分细胞因子也能诱导TNF-α,例如:IFN、IL-1、IL-2等。
糖皮质激素、IL-4、IL-6、IL-10、PAF受体拮抗剂和抗MHC-Ⅱ类分子抗体等均能在转录水平或转录后水平抑制TNF-α产生。
能抑制NF-κB活性的物质(N-乙酰半胱氨酸、谷胱甘肽等)和能抑制氧化酶的物质均能抑制TNF-α产生。
肿瘤坏死因子α正常值

肿瘤坏死因子α正常值
肿瘤坏死因子α(TNF-α)是一种由免疫细胞产生的蛋白质,其作用是促进炎症反应和细胞凋亡。
在某些疾病中,TNF-α的水平可能升高,如类风湿关节炎、克隆氏病和结肠炎等。
因此,了解TNF-α的正常值对于这些疾病的诊断和治疗非常重要。
TNF-α的正常值因人而异,一般来说成年人的正常值范围为
0-8.1pg/ml。
然而,这个范围可能因性别、年龄、生理状态等因素而有所变化。
通常情况下,TNF-α的水平会在炎症反应和感染时升高。
因此,如果患者在检测时处于这种状态,可能会出现异常高的TNF-α水平。
另外,一些药物如抗炎药和抗肿瘤药等也可能影响TNF-α水平的测量结果。
总之,了解TNF-α的正常值对于疾病的诊断和治疗非常重要。
然而,需要注意的是,TNF-α的水平可能受到多种因素的影响,因此在进行检测时需要考虑到这些因素的影响。
- 1 -。
tnf-α的蛋白结构

tnf-α的蛋白结构TNF-α(肿瘤坏死因子-α)是一种重要的促炎细胞因子,它在免疫应答中扮演着重要的角色。
该蛋白的结构包含多个功能区域,这些区域在维持其生物活性和相互作用中起着关键的作用。
TNF-α蛋白的结构主要由两个相互作用的链组成,每个链都包含约157个氨基酸残基。
这两个链分别被称为可见域链和胞浆域链。
可见域链负责与受体结合,而胞浆域链则通过细胞内信号转导途径来传递其生物学功能。
TNF-α的可见域链由一个稳定的β-片层结构组成,其中包含两个重要的结构域:结构域1和结构域2。
结构域1是与TNF-α受体TNF-R1结合的关键区域,而结构域2则负责与另一个受体TNF-R2结合。
这两个结构域的结构都非常精确,能够提供与受体结合所需的特异性和亲和力。
TNF-α的胞浆域链则通过一个短的跨膜区连接到细胞膜上。
这个跨膜区由23个氨基酸残基组成,并具有高度保守性。
胞浆域链包含一个“死亡域”(death domain),这个结构域在信号转导中起到重要的作用。
当TNF-α与其受体结合时,胞浆域链的死亡域会与受体的相应结构域相互作用,从而激活下游信号传递通路。
除了可见域链和胞浆域链外,TNF-α还包含一个信号肽序列,这个序列位于蛋白的N-端。
信号肽序列在蛋白的分泌过程中起着重要的作用,它指示了TNF-α蛋白在内质网中的正确折叠和转运。
TNF-α的蛋白结构对其生物学功能具有重要的影响。
研究表明,TNF-α与其受体的结合能够触发多种信号通路,包括NF-κB、MAPK 和JNK等信号通路。
这些信号通路参与了细胞增殖、细胞凋亡、炎症反应等多种生物学过程。
此外,TNF-α还可以通过诱导其他促炎细胞因子的产生来进一步放大炎症反应。
由于TNF-α在多种疾病的发生和发展中扮演着重要的角色,研究人员一直致力于寻找针对TNF-α的治疗方法。
目前,已经开发出多种针对TNF-α的生物制剂,如抗TNF-α抗体和TNF-α受体拮抗剂。
这些药物通过阻断TNF-α与其受体的结合来抑制其生物学功能,从而起到抗炎作用。
肿瘤坏死因子-α、白细胞介素-6在高血压心肌肥厚大鼠实验中的意义

肿瘤坏死因子-α、白细胞介素-6在高血压心肌肥厚大鼠实验中的意义目的探讨肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)在心肌肥厚大鼠血清和心肌中的表达变化及意义。
方法Wistar大鼠20只,随机分成两组,心肌肥厚组(OG)和假手术组(CG),每组10只。
腹主动脉部分缩窄法制作压力负荷性心肌肥厚大鼠模型,手术后按要求饲养8周后处死,采血并取心肌标本。
采用放射性免疫法检测大鼠血清TNF-α、IL-6含量,应用RT-PCR法检测心肌组织中TNF-α、IL-6 mRNA表达的变化。
结果与假手术组比较,心肌肥厚组血清中TNF-α、IL-6含量增加(P <0.05);心肌中TNF-α、IL-6 mRNA表达增多(P <0.05)。
结论TNF-α、IL-6参与心肌肥厚的发生和发展过程。
[Abstract] Objective To investigate the expression of change and significance about tumor necrosis factor-α(TNF-α), interleukin-6 (IL-6) in serum and myocardial of myocardial hypertrophy rats. Methods 20 Wistar rats were randomly divided into two groups: myocardial hypertrophy group (OG) and control group (CG). Each group contained 10 rats. The partial abdominal aorta ligature was used to induce hypertrophy in rats. After surgery, rats were feeded according to the requirements for eight weeks, then put to death. Blood and myocardial specimens were obtained. TNF-α and IL-6 content in serum were detected with radioactive immune method. The expression changes of TNF-α mRNA and IL-6 mRNA in myocardial tissue were detected with RT-PCR method. Results Compared with control group, it was found that in myocardial hypertrophic group the content of TNF-α and IL-6 in serum increased greatly (P < 0.05); the express of myocardial of TNF-α mRNA and IL-6 mRNA increased (P < 0.05). Conclusion TNF-α and IL-6 play a role in myocardial hypertrophy pathogenesis.[Key words] Tumor necrosis factor-α; Interleukin-6; Myocardial hypertrophy心肌肥厚主要是由于心脏在长期压力负荷过重的情况下,肥大的心肌需氧量增加,而冠状动脉的供血量往往不能予以满足,造成心肌缺血从而引起心肌重构,其发生的结构基础主要是心肌细胞增大和纤维化。
TNF-α_重组人TNF-α_肿瘤坏死因子使用说明书

GMP级重组人肿瘤坏死因子α(冻干粉)Recombinant Human TNF-α(rhTNF-α)作用机理:TNF-α是一个同源三聚体,每个亚基的分子量为 17kDa,它在生长调节、分化、炎性反应、病毒复制、肿瘤发生、自身免疫性疾病以及病毒、细菌、真菌和寄生虫感染中都起到重要的作用。
除了诱导肿瘤的出血性坏死外,TNFα还和肿瘤发生、肿瘤转移、病毒复制、败血性休克、发热、发炎和罗恩氏病、风湿性关节炎、器官移植排斥等自身免疫性疾病发生有关。
TNF-α是一种在多种肿瘤细胞和其他特定靶细胞中具有细胞毒素效应的强效淋巴因子。
规格参数:货号:TL-303 规格:100ug产品信息:表达宿主:HEK293细胞效价:≥1×107 IU/mg纯度:>95%内毒素:<0.01EU/ug纯化方式:层析纯化性状:白色疏松体保存温度:2-8℃有效期:24 个月生产厂家:同立海源生物使用说明:推荐使用浓度为 1000IU/ml。
如需分装,可用注射用水、生理盐水、培养基或 PBS 稀释,稀释后浓度保持在 100ug/mL 以上。
稀释后置于-20℃保存期 6 个月,-80℃保存期 12 个月。
适用范围:用于 DC 细胞体外培养,适用于直肠癌、乳腺癌、肺癌、肾癌、淋巴瘤、白血病、多发性骨髓瘤、恶性黑色素瘤、卵巢癌等多种肿瘤的细胞免疫治疗临床研究。
相关产品推荐:Human IL-2、Human IL-15、Human IL-12、Human IL-6、Human IL-18、Human IL-21、Human IFN-γNK细胞培养试剂盒、Human GM-CSF、Human EGF等。
Human TNF-α 预包被 ELISA kit说明书

产品信息和操作指南Human TNF-α预包被 ELISA kit Cat# : DKW12-1720-048 / DKW12-1720-096本试剂盒专用于科研,而非用于诊断Human TNF-αDKW12-1720目录产品简介 (1)知识背景 (1)试剂盒提供的试剂 (2)需要实验者自行准备的试剂与仪器 (2)注意事项 (3)试剂的配制 (5)操作过程 (7)结果分析 (9)试剂盒的保存 (9)操作步骤一览表 (10)参考文献 (11)ELISA测定中可能会出现的问题及解决方法 (12)预包被ELISA 试剂盒系列产品 (15)1、产品简介:达优®人TNF-α ELISA试剂盒是通过酶联免疫吸附技术,体外定量检测人血清、血浆、缓冲液或细胞培养液中的TNF-α,可同时检测天然的和重组的TNF-α。
本试剂盒为预包被板,“夹心一步”完成,整个过程孵育时间不超过4小时,洗涤6次,操作时间大大减少。
本试剂盒专用于科研,而非用于诊断。
使用前请仔细阅读说明书并检查试剂盒组分,若有任何疑问请与达科为生物工程有限公司联系,E-mail:*************.检测范围:800-25 pg/mL灵敏度:8 pg/mL重复性:板内、板间变异系数均<10%。
2、知识背景:肿瘤坏死因子-α(Tumor necrosis factorα,TNF-α)亦称为恶质素,由活化的巨噬细胞和其它类型的细胞分泌,包括T细胞、B 细胞、NK细胞、LAK细胞、星形胶质细胞、内皮细胞、平滑肌细胞和一些肿瘤细胞(1-4),在正常宿主对抗感染和恶性肿瘤的生长过程中起重要的作用。
其过量表达跟一系列的病理状态有关,包括恶病质、败血性休克和自身免疫失调。
3、试剂盒提供的试剂:试剂规格配制Cytokine standard 2/1瓶* 干粉状,按瓶上说明操作Biotinylated antibody 2/1瓶* 1:50用Dilution buffer R(1×)稀释Streptavidin-HRP 2/1瓶* 1:100用Dilution buffer R(1×)稀释Dilution buffer R(1×) 3/2瓶* 即用型Washing buffer(50×)1瓶 150∶用蒸馏水稀释TMB 1瓶即用型Stop solution 1瓶即用型Precoated ELISA plate 8×12或8×6*即用型封板膜 2/1张* 即用型说明书1份*:96/48 Tests4、需要实验者自行准备的试剂与仪器:1.酶标仪(建议参考仪器使用说明提前预热)2.微量加液器及吸头:P10,P50,P100,P200,P1000 3.蒸馏水或去离子水4.全新滤纸5.旋涡振荡器和磁力搅拌器5、注意事项:1.试剂应按瓶上标签说明储存,使用前室温平衡20-30分钟。
TNF肿瘤坏死因子的介绍

肿瘤坏死因子(TNF)1975年carswell等发现接种bcg的小鼠注射lps后,血清中含有一种能杀伤某些肿瘤细胞或使体内肿瘤组织发生血坏死的因子,称为肿瘤坏死因子(tumor necrosis factor,tnf)。
1985年shalaby把巨噬细胞产生的tnf命名为tnf-α ,把t淋巴细胞产生的淋巴毒素(lymphotoxin,lt)命名为tnf-β。
tnf-α又称恶质素。
1.tnf的产生(1)tnf-α是一种单核因子,主要由单核细胞和巨噬细胞产生,lps是较强的刺激剂。
ifn-γ、m-csf、gm-csf对单核细胞/巨噬细胞产生tnf-α有刺激作用,而pge则有抑制作用。
前单核细胞系u937、前髓细胞系hl-60在pma刺激下可产生较高水平的tnf-α。
t淋巴细胞、t细胞杂交瘤、t淋巴样细胞系以nk细胞等在pma刺激下也可分泌tnf-α。
sac、pma、抗igm可刺激正常b细胞产生tnf-α。
此外,中性粒细胞、lak、星状细胞、内皮细胞、平滑肌细胞亦可产生tnf-α。
(2)tnf-β是一种淋巴因子,抗原和丝裂原均可刺激t淋巴细胞分泌tnf-β。
pma刺激rpmi1788b 淋巴母细胞可分泌高水平tnf-β。
2.tnf的分子结构和基因(1)人的tnf-α基因长约2.76kb,小鼠为2.78kb,结构非常相似,均由4个外显子和3个内含子组成,与mhc基因群密切连锁,分别定位于第6对和第17对染色体上。
1984年从hl-60、u937等细胞中克隆成功rhu tnf-α cdna,并在大肠杆菌中获得高表达。
人tnf-α前体由233个氨基酸残基组成,含76个氨基酸残基的信号肽,切除信号肽后成熟型tnf-α为157氨基酸残基,非糖基化,第69位和101位两个半胱氨酸形成分子内二硫键。
rhu tnf-α分子量为17kda。
小鼠tnf-α前体为235氨基酸残基,信号肽79氨基酸残基,成熟的小鼠tnf-α(rmutnf-α)分子量为17kda,由156个氨基酸残基组成,第69位和100位两个半胱氨酸形成分子内二硫键,有一个糖基化点,但糖基化不影响其生物学功能。
肿瘤坏死因子(TNF-α):自身免疫系统疾病关键靶点

肿瘤坏死因⼦(TNF-α):⾃⾝免疫系统疾病关键靶点导语:⽬前,⽆论是传统的化药龙头,⾎制品公司还是很多初创的创新性药企,越来越多的公司致⼒于抗体类药物的研发。
⼀夜之间,似乎变成了不研究⼏个单抗产品,出去都不好意思打招呼的局⾯:)但是⽬前全球抗体类药物的市场还是集中在⼏家巨头⼿中,我国的抗体类药物更是⾯临着起步晚,⼤规模制备技术较落后,医保不能覆盖等很多问题,但随着研发技术的提⾼,制备⼯艺的优化,以及医保⽬录的调整等,相信我国的抗体类药物会迎来发展的春天。
民⽣证券医药⾏业研究团队负责⼈吴汉靓将通过⼀系列的报告来研究说明整个抗体药物领域,⽬前的主题包括:靶点的选择,⼯艺的优化,双抗产品的研发等。
下⾯是第⼀篇:肿瘤坏死因⼦(TNF-α):⾃⾝免疫系统疾病关键靶点。
主要涉及阿达⽊单抗,英夫利昔单抗,依那西普以及我国⾃主研发的益赛普,安佰诺等TNF抑制剂的现状和未来前景。
⼀、单克隆抗体:⽣物药领域最⼤的⼦⾏业,2016年全球市场900亿美⾦1)单克隆抗体:⽣物药领域最⼤的⼦⾏业,占据⽣物药市场的43%根据Transparency Market Research预测,全球⽣物药市场将从2016年的2098亿美⾦增长到2024年的4798亿美⾦,复合增长率11%。
图1:全球⽣物药市场⽣物药可以细分为单克隆抗体、⽣长激素、融合蛋⽩、疫苗等⼦⾏业,其中单克隆抗体是⽣物药领域最⼤的⼦⾏业,2016年占据⽣物药市场的43%,预计从2016年的900亿美⾦增长到2024年的2217亿美⾦,复合增长率11.9%。
单克隆抗体(Monoclonal Antibody, mAb),简称单抗,是由⼀种类型的B细胞分泌产⽣的,具有和特定抗原发⽣特异性结合的免疫球蛋⽩。
单抗药物针对的靶点包括细胞表⾯分化抗原、细胞⽣长因⼦、⾎管内⽪⽣长因⼦等。
其中临床获批和临床研究最多的四个靶点是CD20、TNF-α、EGFR和HER2。
图2:临床研发和上市的⽣物药靶点2)肿瘤坏死因⼦-α(TNF-α):细胞信号通路中重要⼀环,药物研发的热门靶点肿瘤坏死因⼦-α(Tumor Necrosis Factor-α, TNF-α)是⼀种涉及到系统性炎症的细胞因⼦,主要由巨噬细胞分泌。
tnf-a名词解释

tnf-a名词解释
TNF-α(肿瘤坏死因子-α)是一种由多种细胞产生的细胞因子,它在机体的免疫反应和炎症过程中起着重要作用。
它主要由活化的巨噬细胞、单核细胞、淋巴细胞和自然杀伤细胞等细胞产生。
TNF-α可以通过与细胞表面TNF受体结合而发挥其生物学效应。
它可以激活巨噬细胞和中性粒细胞,促进炎症反应和免疫反应的发生。
TNF-α还能增强血管通透性,促进内皮细胞黏附分子的表达,并促使白细胞向炎症部位迁移。
此外,TNF-α还能刺激胃酸分泌和肠蠕动增强,对机体的代谢和造血功能也有一定影响。
在炎症疾病中,过度产生的TNF-α可导致炎症反应过激,引
发组织损伤和疾病的恶化,如类风湿关节炎、炎症性肠病等。
因此,抑制TNF-α的生理功能已成为多种治疗炎症性疾病的
方法,如使用抗TNF-α药物来控制炎症反应,减轻相关疾病
的症状和病程。
小鼠肿瘤坏死因子α(TNF-α)ELISA 实验说明书

小鼠肿瘤坏死因子α (TNF-α)酶联免疫试剂盒使用说明书【预期应用】ELISA法定量测定小鼠血清、血浆、细胞培养物上清、组织裂解液中TNF-α含量。
【产品性能指标】1、检测范围:15.6 pg/ml-1000 pg/ml2、灵敏度:3.9 pg/ml3、精密度:批内差CV%<8%,批间差CV%<10%4、特异性:本试剂盒特异性检测小鼠TNF-α,且与其他相关蛋白无交叉反应。
【实验原理】用纯化的抗体包被微孔板,制成固相载体,往包被抗TNF-α抗体的微孔中依次加入标本或标准品、生物素化的抗TNF-α抗体、HRP标记的亲和素,经过彻底洗涤后用底物TMB显色。
TMB 在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样本中的TNF-α呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),计算样本浓度。
【试剂盒组成成分】组份96T酶标板(Assay plate) 12条×8孔标准品(Standard) 2瓶(冻干品)生物素标记抗体(Biotin-antibody) 1 x 120 μl/瓶(100×)辣根过氧化物酶标记亲和素(HRP-avidin) 1 x 120 μl/瓶(100×)生物素标记抗体稀释液(Biotin-antibody Diluent) 1 x 15 ml/瓶辣根过氧化物酶标记亲和素稀释液(HRP-avidin Diluent) 1 x 15 ml/瓶样本稀释液(Sample Diluent) 1 x 50 ml/瓶浓洗涤液(Wash Buffer) 1 x 20 ml/瓶(25×)底物溶液(TMB Substrate) 1 x 10 ml/瓶终止液(Stop Solution) 1 x 10 ml/瓶板贴 4【存储条件及有效期】未开封试剂盒试剂盒避光保存于2-8℃。
有效期为六个月。
请在试剂盒标注的有效日期内使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
品稀释液 50μl,混匀后从第九第十孔中各取 50μl 弃掉。(稀释后各孔加样量都为 50μl,
浓度分别为 240ng/L,160ng/L ,80ng/L,40ng/L, 20ng/L)。
2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、待测样
品孔。在酶标包被板上待测样品孔中先加样品稀释液 40μl,然后再加待测样品 10μl(样
15 分钟. 10. 终止:每孔加终止液 50μl,终止反应(此时蓝色立转黄色)。 11. 测定:以空白空调零,450nm 波长依序测量各孔的吸光度(OD 值)。 测定应在加终止
液后 15 分钟以内进行。
计算 以标准物的浓度为横坐标,OD 值为纵坐标,在坐标纸上绘出标准曲线,根据样品的
OD 值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与 OD 值计算出标 准曲线的直线回归方程式,将样品的 OD 值代入方程式,计算出样品浓度,再乘以稀释倍数, 即为样品的实际浓度。 注意事项 1.试剂盒从冷藏环境中取出应在室温平衡 15-30 分钟后方可使用,酶标包被板开封后如未
2.不能检测含 NaN3 的样品,因 NaN3 抑制辣根过氧化物酶的(HRP)活性。
操作步骤
1. 标准品的稀释与加样:在酶标包被板上设标准品孔 10 孔,在第一、第二孔中分别加标
准品 100μl,然后在第一、第二孔中加标准品稀释液 50μl,混匀;然后从第一孔、第二
孔中各取 100μl 分别加到第三孔和第四孔,再在第三、第四孔分别加标准品稀释液 50μl,
正相关。用酶标仪在 450nm 波长下测定吸光度(OD 值),通过标准曲线计算样品中大鼠肿
瘤坏死因子α(TNF-α)浓度。
试剂盒组成
1 20 倍浓缩洗涤液
30ml×1 瓶
7 终止液
36ml×1 瓶
2 酶标试剂
3ml×1 瓶
8 标准品(360ng/L) 0.5ml×1 瓶
3 酶标包被板
12 孔×4 条
品最终稀释度为 5 倍)。加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混
匀。 3. 温育:用封板膜封板后置 37℃温育 30 分钟。 4. 配液:将 20 倍浓缩洗涤液用蒸馏水 20 倍稀释后备用 5. 洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置 30 秒后弃去,如此
重复 5 次,拍干。 6. 加酶:每孔加入酶标试剂 50μl,空白孔除外。 7. 温育:操作同 3。 8. 洗涤:操作同 5。 9. 显色:每孔先加入显色剂 A50μl,再加入显色剂 B50μl,轻轻震荡混匀,37℃避光显色
混匀;然后在第三孔和第四孔中先各取 50μl 弃掉,再各取 50μl 分别加到第五、第六孔
中,再在第五、第六孔中分别加标准品稀释液 50ul,混匀;混匀后从第五、第六孔中各
取 50μl 分别加到第七、第八孔中,再在第七、第八孔中分别加标准品稀释液 50μl,混
匀后从第七、第八孔中分别取 50μl 加到第九、第十孔中,再在第九第十孔分别加标准
的大鼠肿瘤坏死因子α(TNF-α)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中
依次加入肿瘤坏死因子α(TNF-α)再与 HRP 标记的羊抗鼠抗体结合,形成抗体-抗原-酶
标抗体复合物,经过彻底洗涤后加底物 TMB 显色。TMB 在 HRP 酶的催化下转化成蓝色,
并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的肿瘤坏死因子α(TNF-α)呈
大于标准品孔第一孔的 OD 值),请先用样品稀释液稀释一定倍数(n 倍)后再测定,计 算时请最后乘以总稀释倍数(×n×5)。 5. 封板膜只限一次性使用,以避免交叉污染。 6.底物请避光保存。 7.严格按照说明书的操作进行,试验结果判定必须以酶标仪读数为准. 8.所有样品,洗涤液和各种废弃物都应按传染物处理。 9.本试剂不同批号组分不得混用。 10. 如与英文说明书有异,以英文说明书为准。 检测范围: 15ng/L -300ng/L 规格: 48 人份/盒 保存条件及有效期 1.试剂盒保存:;2-8℃。 2.有效期:6 个月
用完,板条应装入密封袋中保存。 2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。 3.各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。一次加样时间最好
控制在 5 分钟内,如标本数量多,推荐使用排枪加样。 4. 请每次测定的同时做标准曲线,最好做复孔。如标本中待测物质含量过高(样本 OD 值
9 标准品稀释液
1.5ml×1 瓶
4 样品稀释液
3ml×1 瓶
10 说明书
1份
5 显色剂 A 液
3ml×1 瓶
11 封板膜
2张
6 显色剂 B 液
3ml×1/瓶
12 密封袋
1个
标本要求Βιβλιοθήκη 1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。若不能
马上进行试验,可将标本放于-20℃保存,但应避免反复冻融
大鼠肿瘤坏死因子α(TNF-α)酶联免疫分析(ELISA)
试剂盒使用说明书
本试剂盒仅供研究使用。
药品名称:
通用名:大鼠肿瘤坏死因子α(TNF-α)酶联免疫分析试剂盒
使用目的:
本试剂盒用于测定大鼠血清,血浆及相关液体样本中肿瘤坏死因子α(TNF-α)含量。
实验原理
本试剂盒应用双抗体夹心法测定标本中大鼠肿瘤坏死因子α(TNF-α)水平。用纯化
