浙江省大学物理试题库204-热力学第一定律、典型的热力学过程
第一章 热力学第一、二定律试题及答案

第一章 热力学第一定律一、选择题1.下述说法中,哪一种正确( )(A )热容C 不是状态函数; (B )热容C 与途径无关;(C )恒压热容C p 不是状态函数;(D )恒容热容C V 不是状态函数。
2.对于内能是体系状态的单值函数概念,错误理解是( )(A) 体系处于一定的状态,具有一定的内能;(B ) 对应于某一状态,内能只能有一数值不能有两个以上的数值;(C ) 状态发生变化,内能也一定跟着变化;(D) 对应于一个内能值,可以有多个状态.3.某高压容器中盛有可能的气体是O 2 ,Ar , CO 2, NH 3中的一种,在298K 时由5dm3绝热可逆膨胀到6dm3,温度降低21K ,则容器中的气体( )(A ) O 2 (B) Ar (C ) CO 2 (D ) NH 34.戊烷的标准摩尔燃烧焓为—3520kJ·mol -1,CO 2(g)和H 2O(l )标准摩尔生成焓分别为—395 kJ·mol —1和-286 kJ·mol —1,则戊烷的标准摩尔生成焓为( )(A ) 2839 kJ·mol —1 (B ) -2839 kJ·mol —1 (C) 171 kJ·mol -1 (D ) —171 kJ·mol —15.已知反应)()(21)(222g O H g O g H =+的标准摩尔反应焓为)(T H m r θ∆,下列说法中不正确的是( ).(A )。
)(T H m r θ∆是H 2O (g )的标准摩尔生成焓 (B)。
)(T H m r θ∆是H 2O (g)的标准摩尔燃烧焓 (C)。
)(T H m r θ∆是负值 (D ). )(T H m r θ∆与反应的θm r U ∆数值相等 6.在指定的条件下与物质数量无关的一组物理量是( )(A ) T , P , n (B ) U m , C p, C V(C) ΔH, ΔU , Δξ (D) V m , ΔH f,m (B ), ΔH c,m (B )7.实际气体的节流膨胀过程中,下列那一组的描述是正确的( )(A ) Q=0 ΔH=0 ΔP< 0 ΔT≠0 (B ) Q=0 ΔH<0 ΔP 〉 0 ΔT>0(C) Q 〉0 ΔH=0 ΔP 〈 0 ΔT 〈0 (D ) Q<0 ΔH=0 ΔP 〈 0 ΔT≠08.已知反应 H 2(g) + 1/2O 2(g ) →H 2O (l)的热效应为ΔH ,下面说法中不正确的是( )(A ) ΔH 是H 2O (l)的生成热 (B ) ΔH 是H 2(g)的燃烧热(C) ΔH 与反应 的ΔU 的数量不等 (D ) ΔH 与ΔH θ数值相等9.为判断某气体能否液化,需考察在该条件下的( )(A) μJ —T > 0 (B ) μJ-T < 0 (C ) μJ-T = 0 (D) 不必考虑μJ —T 的数值10.某气体的状态方程为PV=RT+bP (b>0),1mol 该气体经等温等压压缩后其内能变化为( )(A) ΔU>0 (B) ΔU <0 (C)ΔU =0 (D)该过程本身不能实现11.均相纯物质在相同温度下C V 〉C P的情况是()(A) (∂P/∂T)V<0 (B) (∂V/∂T)P〈0(C)(∂P/∂V)T〈0 (D)不可能出现C V〉C P12.理想气体从相同始态分别经绝热可逆膨胀和绝热不可逆膨胀到达相同的压力,则其终态的温度,体积和体系的焓变必定是()(A)T可逆> T不可逆,V可逆〉V不可逆,ΔH可逆〉ΔH不可逆(B)T可逆< T不可逆, V可逆< V不可逆,ΔH可逆〈ΔH不可逆(C) T可逆〈T不可逆, V可逆> V不可逆, ΔH可逆<ΔH不可逆(D) T可逆〈T不可逆,V可逆< V不可逆, ΔH可逆〉ΔH不可逆13.1mol、373K、1atm下的水经下列两个不同过程达到373K、1atm下的水汽:(1)等温可逆蒸发,(2)真空蒸发。
大学物化习题及答案

19. 理 想 气 体 经 历 绝 热 不 可 逆 过 程 从 状 态 1 (P1,V1,T1) 变 化 到 状 态 2
(P2,V2,T2),所做的功为
()
(A) P2V2-P1V1
(B) P2(V2-V1)
(C) [P2V2γ/(1-γ)](1/V2γ-1)- (1/ V1γ-1) (D) (P2V2-P1V1)/(1-γ)
(B) Q = 0 W < 0 △U > 0
(C) Q > 0 W < 0 △U > 0
(D) △U = 0 , Q = W ≠ 0
3. 有一容器四壁导热,上部有一可移动的活塞,在该容器中同时放入锌块和
盐酸,发生化学反应后活塞将上移一定距离,若以锌和盐酸为体系则( )
(A ) Q < 0 , W = 0 , △rU < 0 (B) Q = 0 , W > 0 , △rU < 0
基本单元,则反应进度ξ应是: H2(g) + Cl2(g) → 2HCl(g)
(A) 1 mol
(B) 2 mol
(C) 4 mol
(D) 5 mol
二 . 填空题:
1. 对于任何宏观物质,其焓 H 一定 _______ 内能 U,(填上 >、<、=) 因
为_________;对于等温理想气体反应,分子数增多的△H 一定 _________ △
13. 理想气体从同一始态 (P1,V1) 出发,经等温可逆压缩或绝热可逆压缩,使
其终态均达到体积为 V2,此二过程做的功的绝对值应是: (
)
(A ) 恒温功大于绝热功
(B) 恒温功等于绝热功
(C) 恒温功小于绝热功
(D) 无法确定关系
大学物理 热力学第一定律 习题(附答案)

A13 = Q13 = 1.25 × 10 4 ( J)
(5)由(1)有系统终态的体积为
hi
5 R , R = 8.31 J / mol ⋅ K 。 2
na
T V3 = V2 ( 2 ) γ−1 = 40 × 21. 5 = 113 ( l) T1 nRT3 2 × 8.31 × 300 p3 = = ÷ 1.013 × 10 5 = 0.44 ( atm) −3 V3 113 × 10
0 . 44
O
om
p (atm ) 1 2
3
三、计算题: 1.2 mol 初始温度为 27 � C ,初始体积为 20 L 的氦气,先等压过程膨胀到体积加倍, 然 后绝热过程膨胀回到初始温度。 (1)在 p-V 平面上画出过程图。 (2)在这一过程中系统总吸热是多少? (3)系统内能总的改变是多少? (4)氦气对外界做的总功是多少?其中绝热膨胀过程对外界做功是多少? (5)系统终态的体积是多少?
5 = 1 × R × 60 = 1.25 × 10 3 ( J) 2
γ
(B) p 0 γ (D) p 0 / 2
(γ = C
p
/ Cv )
p0
解:绝热自由膨胀过程中 Q = 0,A = 0,由热力学第一定律,有 ∆ E = 0 ,膨胀前后系统
[
]
(A) (B) (C) (D)
这是一个放热降压过程 这是一个吸热升压过程 这是一个吸热降压过程 这是一个绝热降压过程
将状态 a、b 分别与 o 点相连有
om
A
O
V1
V2
V
T B
C
Q
V
等压过程中吸收了相同的热量,则它们对外做功之比为 A 1: A 2 = (各量下角标 1 表示氢气,2 表示氦气)
204-热力学第一定律、典型的热力学过程

204热力学第一定律、典型的热力学过程1.选择题1,如图所示,一定量理想气体从体积V 1,膨胀到体积V 2分别经历的过程是:A →B 等压过程,A →C 等温过程;A →D 绝热过程,其中吸热量最多的过程(A) 是A →B.(B) 是A →C.(C) 是A →D.(D) 既是A →B 也是A →C , 两过程吸热一样多。
[ ]2,质量一定的理想气体,从相同状态出发,分别经历等温过程、等压过程和绝热过程,使其体积增加一倍.那么气体温度的改变(绝对值)在(A) 绝热过程中最大,等压过程中最小.(B) 绝热过程中最大,等温过程中最小.(C) 等压过程中最大,绝热过程中最小.(D) 等压过程中最大,等温过程中最小.[ ]3,一定量的理想气体,从a 态出发经过①或②过程到达b 态,acb为等温线(如图),则①、②两过程中外界对系统传递的热量Q 1、Q 2是(A) Q 1>0,Q 2>0. (B) Q 1<0,Q 2<0. (C) Q 1>0,Q 2<0. (D) Q 1<0,Q 2>0.[ ]4,一定量的理想气体分别由初态a 经①过程ab 和由初态a ′经②过程a ′cb 到达相同的终态b ,如p -T 图所示,则两个过程中气体从外界吸收的热量 Q 1,Q 2的关系为:(A) Q 1<0,Q 1> Q 2. (B) Q 1>0,Q 1> Q 2. (C) Q 1<0,Q 1< Q 2. (D) Q 1>0,Q 1< Q 2. [ ]5,理想气体向真空作绝热膨胀.(A) 膨胀后,温度不变,压强减小.(B) 膨胀后,温度降低,压强减小.(C) 膨胀后,温度升高,压强减小.(D) 膨胀后,温度不变,压强不变.Vp[ ]6,一定量的理想气体,从p -V 图上初态a 经历(1)或(2)过程到达末态b ,已知a 、b 两态处于同一条绝热线上(图中虚线是绝热线),则气体在(A) (1)过程中吸热,(2) 过程中放热. (B) (1)过程中放热,(2) 过程中吸热. (C) 两种过程中都吸热.(D) 两种过程中都放热.[ ]7,1 mol 理想气体从p -V 图上初态a 分别经历如图所示的(1) 或(2)过程到达末态b .已知T a <T b ,则这两过程中气体吸收的热量Q 1和Q 2的关系是(A) Q 1> Q 2>0. (B) Q 2> Q 1>0. (C) Q 2< Q 1<0. (D) Q 1< Q 2<0. (E) Q 1= Q 2>0.[ ]8,如图,bca 为理想气体绝热过程,b 1a 和b 2a 是任意过程,则上述两过程中气体作功与吸收热量的情况是:(A) b 1a 过程放热,作负功;b 2a 过程放热,作负功. (B) b 1a 过程吸热,作负功;b 2a 过程放热,作负功.(C) b 1a 过程吸热,作正功;b 2a 过程吸热,作负功. (D) b 1a 过程放热,作正功;b 2a 过程吸热,作正功.[ ]9,对于理想气体系统来说,在下列过程中,哪个过程系统所吸收的热量、内能的增量和对外作的功三者均为负值?(A) 等体降压过程. (B) 等温膨胀过程.(C) 绝热膨胀过程. (D) 等压压缩过程.[ ]10,理想气体经历如图所示的abc 平衡过程,则该系统对外作功W ,从外界吸收的热量Q 和内能的增量E 的正负情况如下:(A) ΔE >0,Q >0,W <0.(B) ΔE >0,Q >0,W >0. (C) ΔE >0,Q <0,W <0. (D) ΔE <0,Q<0,W <0. [ ]p V V p O a b(1)(2) p O V b 1 2 a c p O V a b c11,一物质系统从外界吸收一定的热量,则(A) 系统的内能一定增加.(B) 系统的内能一定减少.(C) 系统的内能一定保持不变.(D) 系统的内能可能增加,也可能减少或保持不变.[ ]12,一物质系统从外界吸收一定的热量,则(A) 系统的温度一定升高.(B) 系统的温度一定降低.(C) 系统的温度一定保持不变.(D) 系统的温度可能升高,也可能降低或保持不变.[ ]13,两个完全相同的气缸内盛有同种气体,设其初始状态相同,今使它们分别作绝热压缩至相同的体积,其中气缸1内的压缩过程是非准静态过程,而气缸2内的压缩过程则是准静态过程.比较这两种情况的温度变化:(A) 气缸1和2内气体的温度变化相同.(B) 气缸1内的气体较气缸2内的气体的温度变化大.(C) 气缸1内的气体较气缸2内的气体的温度变化小.(D) 气缸1和2内的气体的温度无变化.[ ]14,热力学第一定律表明:(A) 系统对外作的功不可能大于系统从外界吸收的热量.(B) 系统内能的增量等于系统从外界吸收的热量.(C) 不可能存在这样的循环过程,在此循环过程中,外界对系统作的功不等于系统传给外界的热量.(D) 热机的效率不可能等于1.[ ] 15,一定量的某种理想气体起始温度为T ,体积为V ,该气体在下面循环过程中经过三个平衡过程:(1) 绝热膨胀到体积为2V ,(2)等体变化使温度恢复为T ,(3) 等温压缩到原来体积V ,则此整个循环过程中(A) 气体向外界放热 (B) 气体对外界作正功(C) 气体内能增加 (D) 气体内能减少[ ]16,理想气体卡诺循环过程的两条绝热线下的面积大小(图中阴影部分)分别为1S 和2S ,则两者的大小关系为:(A )1S >2S ; (B )1S <2S ;(C )1S =2S ; (D )无法确定。
物理化学-第一章-热力学第一定律-习题精选全文

273.15K
Q p1T1 p2T2
T2
p1T1 p2
2101.325 273.15 4 101.325
136.6K
V2
nRT2 p2
2.80dm3
2. U nCVmT 1.70kJ
H nCpmT 2.84kJ
3. QT C
p
Q pV RT CR p
p2 CR V
p CR V
(2)
9.反响CO〔g〕+1/2O2〔g〕→CO2〔g〕的 △rHmθ,以下说法何者是不正确的?
〔1〕△rHmθ是CO2〔g〕的标准摩尔生成焓 〔2〕△rHmθ是CO〔g〕的标准摩尔燃烧焓 〔3〕△rHmθ是负值 〔4〕△rHmθ与△rUmθ值不等
(1)
三.填空
1.在一绝热箱中置一绝热隔板,将箱分成两 局部。分别装有温度压力都不同的两种气 体。将隔板抽走使气体混合,假设以气体 为系统,那么Q0=〔 〕;W0=〔 〕; △U=〔 0 〕。
四 计算
1.1mol单原子理想气体,始态 2×101.325kPa,11.2dm3,经pT=常数的 可逆过程,压缩到终态为4×101.325kPa, Cvm=3/2R,求:
〔1〕终态的体积和温度; 〔2〕△U和△H; 〔3〕所作的功。
1.
T1
p1V1 nR
2 101.325 11.2 1 8.314
〔1〕B→C过程的△U2; 〔2〕B→C过程的Q2。
U U1 U2 U3 0 U1 0
U2 U3 W3
(2) B→C过程的Q2
∵△U=0, Q=-W(ABC围起的面积) ∵Q=Q1+Q2+Q3, Q3=0 ∴Q2=Q-Q1 Q1 (AB线下面的面积)
浙江省大学物理试题库

浙江省高等学校大学物理课程试题库组题要求及其分工根据2007年9月22日在杭州玉泉山庄召开的浙江省高等学校大学物理试题库建设小组工作会议讨论的集体意见,本次组织的浙江省高等学校大学物理试题库建设的组题要求如下。
请各位专家组题时严格按照下列要求执行。
1、试题库建设按128学时的基本要求进行,大致适用于非物理类理工学科100学时到128学时的大学物理课程。
2、试题库组题的基本范围:教育部高等学校非物理类专业物理基础课程教学指导分委员会所制定的“非物理类理工学科大学物理课程教学基本要求”中所规定的A类(A为核心内容)教学内容(除几何光学4条暂不纳入建设范围外),并再加质点力学综合,共71条。
其中(1)力学7条+1条(质点力学综合)(2)振动和波9条(3)热学10条(4)电磁学20条(5)光学10条(几何光学4条除外)(6)狭义相对论力学基础4条(7)量子物理基础10条3、试题库的题型、分值、答案与评分标准:分选择题、判断题、填空题、计算题四类。
其中,选择题占30%的分值,判断题占10%分值,填空题占20%分值,计算题占40%分值。
(1)选择题为单选题,4个选择中选一个答案,每题3分;(2)判断题每题只能是一个判断(以概念、原理等判断为主),只是判断对与错,每题2分;(3)填空题每题只能是一个填空(并预留足够学生书写格子),每题2分;(4)计算题可以只有一个小题,也允许由2-3个小题组成,一个计算题每题10分。
选择题、判断题、填空题、计算题都得给出答案与评分标准,式样见附件1。
选择题、判断题、填空题比较简单,只要给出答案即可。
计算题的答案要比较详细,并按题目要求给每个解题步骤赋予一定分值(评分标准);每个解题步骤分值原则上为1-3分,不宜设置过细或过粗(如把一个题目解题分为10个步骤,每个步骤1分,这样显然太细了;再如把一个题目解题分为2个步骤,每个步骤5分,这样显然太粗了;这些题目均不合适),每个解题步骤不设置0.5分、1.5分、2.5分之类的半分分值,4、难度系数及确定方式:每题均得赋予一定的难度系数,难度系数分1-5级,其中1级:表示容易――预计几乎所有学生均能答对;2级:表示中等偏容易――预计80%左右的学生能做对;3级:表示中等难度――预计60%左右的学生能做对;4级:表示中等偏难――预计40%左右的学生能做对;5级:表示难――预计20%左右的学生能做对。
第二章-热力学第一定律--题加答案
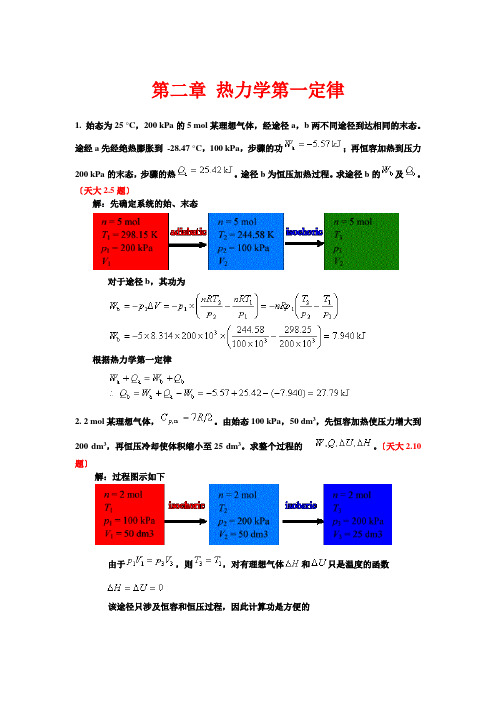
第二章热力学第一定律1. 始态为25 °C,200 kPa的5 mol某理想气体,经途径a,b两不同途径到达相同的末态。
途经a先经绝热膨胀到-28.47 °C,100 kPa,步骤的功;再恒容加热到压力200 kPa的末态,步骤的热。
途径b为恒压加热过程。
求途径b的及。
〔天大2.5题〕解:先确定系统的始、末态对于途径b,其功为根据热力学第一定律2. 2 mol某理想气体,。
由始态100 kPa,50 dm3,先恒容加热使压力增大到200 dm3,再恒压冷却使体积缩小至25 dm3。
求整个过程的。
〔天大2.10题〕解:过程图示如下由于,则,对有理想气体和只是温度的函数该途径只涉及恒容和恒压过程,因此计算功是方便的根据热力学第一定律3. 单原子理想气体A与双原子理想气体B的混合物共5 mol,摩尔分数,始态温度,压力。
今该混合气体绝热反抗恒外压膨胀到平衡态。
求末态温度及过程的。
〔天大2.18题〕解:过程图示如下分析:因为是绝热过程,过程热力学能的变化等于系统与环境间以功的形势所交换的能量。
因此,单原子分子,双原子分子由于对理想气体U和H均只是温度的函数,所以4. mol〔单原子分子〕理想气体,由、300K按以下两种不同的途径压缩到、300K,试计算并比较两途径的Q、W、ΔU及ΔH。
(1〕等压冷却,然后经过等容加热;(2)等容加热,然后经过等压冷却。
解:C p,m=2.5R, C V,m〔1〕、、、300K30.09858 dm30.09858 dm3Q=Q1+Q2××××(300-119.8)=-3745+2247=-1499(J)W=W1+W2×103×(0.09858-0.2470)+0=1499(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0〔2〕、、、300K330.09858 dm3Q=Q1+Q2××××(300-751.6)=5632-9387=-3755(J)W=W1+W2×103×(0.09858-0.2470) =3755(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0计算结果说明,Q、W与途径有关,而ΔU、ΔH与途径无关。
高三物理热力学第一定律试题答案及解析

高三物理热力学第一定律试题答案及解析1.(5分)关于一定量的理想气体,下列说法正确的是 (填正确答案标号。
选对1个得2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分为0分).A.气体分子的体积是指每个气体分子平均所占有的空间体积B.只要能增加气体分子热运动的剧烈程度,气体的温度就可以升高C.在完全失重的情况下,气体对容器壁的压强为零D.气体从外界吸收热量,其内能不一定增加E. 气体在等压膨胀过程中温度一定升高。
【答案】BDE【解析】每个气体分子平均所占有的空间体积比气体分子的体积要大得多,选项A 错误;温度是分子平均动能的标志,则只要能增加气体分子热运动的剧烈程度,气体的温度就可以升高,选项B正确;气体的压强不是由气体的重力产生的,所以在完全失重的情况下,气体对容器壁的压强也不为零,选项C错误;根据热力学第一定律,气体从外界吸收热量,若同时对外做功,则其内能不一定增加,选项D 正确;根据可知气体在等压膨胀过程中温度一定升高,选项E 正确。
【考点】温度;气体的压强;热力学第一定律;气态方程。
2.如图所示,用销钉固定的导热活塞把水平放置的导热汽缸分隔成容积相同的两部分,分别封闭着A、B两部分理想气体:A部分气体压强为pAO =2.5×105 Pa,B部分气体压强为pBO=1.5×105Pa.现拔去销钉,待活塞重新稳定后.(外界温度保持不变,活塞与汽缸间摩擦可忽略不计,整个过程无漏气发生)①求此时A部分气体体积与原来体积之比;②判断此过程中A部分气体是吸热还是放热,并简述理由.【答案】①5∶4. ②吸热 A部分气体由于温度不变,所以内能不变;体积膨胀,对外做功,由热力学第一定律可知,一定从外界吸收热量.【解析】①设A部分气体原来体积为V,由玻意耳定律得p A0V=pA(V+ΔV)p B0V=pB(V-ΔV)又pA =pB由以上各式可解得ΔV=V,因此,A部分气体此时体积与原来体积之比为5∶4.②吸热.A部分气体由于温度不变,所以内能不变;体积膨胀,对外做功,由热力学第一定律可知,一定从外界吸收热量.【考点】本题考查1气体状态方程和热力学第一定律。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
浙江工业大学学校 204 条目的4类题型式样及交稿式样热力学第一定律、典型的热力学过程一. 选择题题号:20412001分值:3分难度系数等级:21 如图所示,一定量理想气体从体积V1,膨胀到体积V2分别经历的过程是:A→B等压过程,A→C等温过程;A→D绝热过程,其中吸热量最多的过程(A) 是A→B.(B) 是A→C.(C) 是A→D.(D) 既是A→B也是A→C, 两过程吸热一样多。
[ ]答案:A题号:20412002分值:3分难度系数等级:22 质量一定的理想气体,从相同状态出发,分别经历等温过程、等压过程和绝热过程,使其体积增加一倍.那么气体温度的改变(绝对值)在(A) 绝热过程中最大,等压过程中最小.(B) 绝热过程中最大,等温过程中最小.(C) 等压过程中最大,绝热过程中最小.(D) 等压过程中最大,等温过程中最小.[]答案:D题号:20412003分值:3分难度系数等级:2V3 一定量的理想气体,从a 态出发经过①或②过程到达b 态,acb 为等温线(如图),则①、②两过程中外界对系统传递的热量Q 1、Q 2是 (A) Q 1>0,Q 2>0. (B) Q 1<0,Q 2<0.(C) Q 1>0,Q 2<0. (D) Q 1<0,Q 2>0. [ ] 答案:A题号:20413004 分值:3分 难度系数等级:34 一定量的理想气体分别由初态a 经①过程ab 和由初态a ′经②过程a ′cb 到达相同的终态b ,如p -T 图所示,则两个过程中气体从外界吸收的热量 Q 1,Q 2的关系为:(A) Q 1<0,Q 1> Q 2. (B) Q 1>0,Q 1> Q 2. (C) Q 1<0,Q 1< Q 2. (D) Q 1>0,Q 1<Q 2.[ ] 答案:B题号:20412005 分值:3分 难度系数等级:25. 理想气体向真空作绝热膨胀. (A) 膨胀后,温度不变,压强减小. (B) 膨胀后,温度降低,压强减小. (C) 膨胀后,温度升高,压强减小. (D) 膨胀后,温度不变,压强不变. [ ] 答案:A题号:20412006 分值:3分 难度系数等级:26. 一定量的理想气体,从p -V 图上初态a 经历(1)或(2)过程到达末态b ,已知a 、b 两态处于同一条绝热线上(图中虚线是绝热线),则气体在(A) (1)过程中吸热,(2) 过程中放热. (B) (1)过程中放热,(2) 过程中吸热. (C) 两种过程中都吸热. (D) 两种过程中都放热. [ ]答案:B 题号:20412007 分值:3分pppV难度系数等级:2 7. 1 mol 理想气体从p -V 图上初态a 分别经历如图所示的(1) 或(2)过程到达末态b .已知T a <T b ,则这两过程中气体吸收的热量Q 1和Q 2的关系是 (A) Q 1> Q 2>0. (B) Q 2> Q 1>0. (C) Q 2< Q 1<0. (D) Q 1< Q 2<0. (E) Q 1= Q 2>0. [ ] 答案:A题号:20413008 分值:3分难度系数等级:38 如图,bca 为理想气体绝热过程,b 1a 和b 2a 是任意过程,则上述两过程中气体作功与吸收热量的情况是: (A) b 1a 过程放热,作负功;b 2a 过程放热,作负功. (B) b 1a 过程吸热,作负功;b 2a 过程放热,作负功. (C) b 1a 过程吸热,作正功;b 2a 过程吸热,作负功.(D) b 1a 过程放热,作正功;b 2a 过程吸热,作正功.[ ] 答案:B题号:20412009 分值:3分难度系数等级:29. 对于理想气体系统来说,在下列过程中,哪个过程系统所吸收的热量、内能的增量和对外作的功三者均为负值?(A) 等体降压过程. (B) 等温膨胀过程.(C) 绝热膨胀过程. (D) 等压压缩过程. [ ] 答案:D题号:20413010 分值:3分难度系数等级:310. 理想气体经历如图所示的abc 平衡过程,则该系统对外作功W ,从外界吸收的热量Q 和内能的增量E 的正负情况如下: (A) ΔE >0,Q >0,W <0. (B) ΔE >0,Q >0,W >0. (C) ΔE >0,Q <0,W <0.(D) ΔE <0,Q<0,W <0. [ ]VpO ab(1)(2)pOV b12 acpO Va bc答案:B题号:20412011分值:3分难度系数等级:211. 一物质系统从外界吸收一定的热量,则(A) 系统的内能一定增加.(B) 系统的内能一定减少.(C) 系统的内能一定保持不变.(D) 系统的内能可能增加,也可能减少或保持不变.[]答案:D题号:20413012分值:3分难度系数等级:312 一物质系统从外界吸收一定的热量,则(A) 系统的温度一定升高.(B) 系统的温度一定降低.(C) 系统的温度一定保持不变.(D) 系统的温度可能升高,也可能降低或保持不变.[]答案:D题号:20413013分值:3分难度系数等级:313 两个完全相同的气缸内盛有同种气体,设其初始状态相同,今使它们而气缸2内的压缩过程则是准静态过程.比较这两种情况的温度变化:(A) 气缸1和2内气体的温度变化相同.(B) 气缸1内的气体较气缸2内的气体的温度变化大.(C) 气缸1内的气体较气缸2内的气体的温度变化小.(D) 气缸1和2内的气体的温度无变化.[]答案:B题号:20414014分值:3分难度系数等级:414. 氦气、氮气、水蒸汽(均视为刚性分子理想气体),它们的摩尔数相同,初始状态相同,若使它们在体积不变情况下吸收相等的热量,则(A) 它们的温度升高相同,压强增加相同.(B) 它们的温度升高相同,压强增加不相同.(C) 它们的温度升高不相同,压强增加不相同.(D) 它们的温度升高不相同,压强增加相同.[]答案:C题号:20413015分值:3分难度系数等级:315. 热力学第一定律表明:(A) 系统对外作的功不可能大于系统从外界吸收的热量.(B) 系统内能的增量等于系统从外界吸收的热量.(C) 不可能存在这样的循环过程,在此循环过程中,外界对系统作的功不等于系统传给外界的热量.(D) 热机的效率不可能等于1.[]答案:C题号:20414016分值:3分难度系数等级:416. 一定量的理想气体,经历某过程后,温度升高了.则根据热力学定律可以断定:(1) 该理想气体系统在此过程中吸了热.(2) 在此过程中外界对该理想气体系统作了正功.(3) 该理想气体系统的内能增加了.(4) 在此过程中理想气体系统既从外界吸了热,又对外作了正功.以上正确的断言是:(A) (1)、(3). (B) (2)、(3).(C) (3). (D) (3)、(4).(E) (4).[]答案:C题号:20414017分值:3分难度系数等级:417. 一个绝热容器,用质量可忽略的绝热板分成体积相等的两部分.两边分别装入质量相等、温度相同的H 2气和O 2气.开始时绝热板P 固定.然后释放之,板P 将发生移动(绝热板与容器壁之间不漏气且摩擦可以忽略不计),在达到新的平衡位置后,若比较两边温度的高低,则结果是:(A) H 2气比O 2气温度高.(B) O 2气比H 2气温度高. (C) 两边温度相等且等于原来的温度. (D) 两边温度相等但比原来的温度降低了. [ ] 答案:B题号:2045018 分值:3分难度系数等级:518. 理想气体经历如图中实线所示的循环过程,两条等体线分别和该循环过程曲线相切于a 、c 点,两条等温线分别和该循环过程曲线相切于b 、d 点a 、b 、c 、d 将该循环过程分成了ab 、bc、cd 、da 四个阶段,则该四个阶段中从图上可肯定为放热的阶段为(A) ab . (B) bc . (C) cd . (D) da . [ ] 答案:C题号:20413019 分值:3分 难度系数等级:319.一定量的某种理想气体起始温度为T ,体积为V ,该气体在下面循环过程中经过三个平衡过程:(1) 绝热膨胀到体积为2V ,(2)等体变化使温度恢复为T ,(3) 等温压缩到原来体积V ,则此整个循环过程中(A) 气体向外界放热 (B) 气体对外界作正功(C) 气体内能增加 (D) 气体内能减少 [ ] 答案:A 题号:20413020 分值:3分 难度系数等级:320. 理想气体卡诺循环过程的两条绝热线下的面积大小(图中阴影部分)分别为1S 和2S ,则两者的大小关系为:O(A )1S >2S ; (B )1S <2S ;(C )1S =2S ; (D )无法确定。
[ ] 答案:C二、判断题题号:20422001 分值:2分难度系数等级:21.1mol 单原子分子理想气体在定压下温度增加T ∆时,内能的增量 .25T R T C E p ∆=∆⋅=∆.答案:错 ,应改为T R T C E V Δ23==∆∆,题号:20421002 分值:2分难度系数等级:12.在如图所示的pV 图中,曲线abcda 所包围的面积表示系统内能的增量. 答案:“表示系统内能增量”是错误的,应改正为:“表示整个过程中系统对外所做的净功.”题号:20423003 分值:2分难度系数等级:33. 摩尔数相同的三种气体:He 、N 2、CO 2 (均视为刚性分子的理想气体),它们从相同的初态出发,都经历等体吸热过程,若吸取相同的热量,则三者的温度升高相同. 答案:错,它们的温度升高依次是:22CO N He )()()(T T T ∆>∆>∆题号:20423004分值:2分难度系数等级:34. 摩尔数相同的三种气体:He 、N 2、CO 2 (均视为刚性分子的理想气体),它们从相同的初态出发,都经历等体吸热过程,若吸取相同的热量,则三者压强的增加相同. 答案:错。
(它们的压强增加依次是: 22CO N He )()()(p p p ∆>∆>∆或22CO N He )(2)(35)(p p p ∆=∆=∆])pOVabc d题号:20422005 分值:2分 难度系数等级:25.质量为M 的氦气(视为理想气体),由初态经历等体过程,温度升高了T ∆.气体内能的改变为E ∆V = (M /M mol )C V T ∆。
答案:对题号:20422006 分值:2分 难度系数等级:26.质量为M 的氦气(视为理想气体),由初态经历等压过程, 温度升高了T ∆.气体内能的改变为E ∆P = (M /M mol )C P T ∆。
