纠正和预防措施流程图
纠正和预防措施控制程序含流程图

1.0目的
通过对已发生的或潜在的不合格进行分析,及时采取措施,以消除导致不合格或潜在不合格的各种原因,防止类似的不合格再次发生或发生,实现持续改进。
2.0范围
适用于公司对产品和生产过程要素(人员、设备、机器、检测、环境等)已遇到的或潜在的不合格所采取的纠正或预防措施的控制。
3.0定义
3.1 纠正措施:是指为了消除不合格的原因而采取的措施;
3.2 预防措施:是指为了消除潜在不合格的原因而采取的措施;
3.3 标准化:为在一定的范围内获得最佳秩序,对实际的或潜在的问题制定共同的和重复使用的活动。
4.0职责
4.1 品管部——负责纠正和预防措施的全过程管理。
4.2 各部门——负责相关质量管理活动过程不合格的原因分析、制定相应纠正和预防措施并实施。
5.0程序
:
附录1
附录2:。
原因分析和纠正预防措施PPT课件

6. 结案/标准化 7. 持续改善
(提供程序)
流程图、查核表、柏拉 图、累进图、鱼骨图、 散布图
柏拉图、累进图
(提供工具)
持续改进的方法--- 5W1H
When---什么时候? Where---在哪里? Who---谁? What---什么事情? Why---为什么? How---程度怎么样?如何做?
有效的改善计划应包含的内容
针对现有产品的处理(换货,返工,返修,报废) 针对所列出的问题产生的各项原因采取相应
的纠正措施 针对所列出的问题产生的各项原因采取相应
的预防措施 因纠正预防措施要求需新增/更改的文件 教育培训
有效的改善计划应包含的内容
措施应具体、明确、用可量化的指标来描述, 避免使用主观的描述,如“提高、加强、注 意……”。
-----明茨伯格(加拿大管理学家)
原因分析应覆盖的范围
产品的设计 产品的生产加工过程(包括原材料) 产品的储存运输过程 产品的检验过程
原因分析
不要成为复述不良现象 不要停留在问题的表层
要深入问题的根源 要考虑可能导致问题发生的各个方面(4M1E)
• 没有正确的原因分析,就不可能有正确的改善 方案,也就不可能从根本上解决问题。
持续改进的方法--- 5WHY分析法
有一次,丰田汽车公司前副社长大野耐一发现在生产线上的 机器总是停转,虽然修过多次但仍不见好转。为找出停机的 真正原因,大野耐一与工人进行了以下的问答:
问“为什么机器停了?”答“因为超过了负荷,保险丝就断 了。”
问“为什么超负荷呢?”答“因为轴承的润滑不够。” 问“为什么润滑不够?” 答“因为润滑泵吸不上油来。” 问“为什么吸不上油来?”答“因为油泵轴磨损、松动了。” 问“为什么磨损了呢?”再答“因为没有安装过滤器,混进了
ISO9001纠正和预防措施控制程序(流程图)

纠正和预防措施控制程序(ISO9001-2015)1.0目的采取纠正和预防措施,防止和消除实际和潜在的不合格,确保产品质量和服务质量。
2.0范围本程序适用于质量管理体系管理活动和产品实现过程中的不合格和潜在因素的控制。
3.0定义与术语3.1纠正:为消除已发现的不合格所采取的措施;3.2纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施;3.3预防措施:为消除潜在不合格或其他潜在不期望情况的原因所采取的措施。
4.0职责4.1管理部负责对体系持续改进的策划及监督执行;4.2各部门负责实施相应的改进、纠正和预防措施;4.3管理者代表负责监督、协调改进、纠正和预防措施的实施。
5.0作业流程5.1采取纠正预防措施的时机a.采取纠正措施的时机:1.顾客、相关方投诉(包括商检、海关、工商部门等);2.产品的监视和测量中出现的不合格;3.内部、外部审核或管理评审中出现的不合格。
b.采取预防措施的时机:1.顾客满意度测量中发现的潜在不合格;2.产品的监视和测量中发现的潜在不合格;3.内部、外部审核或管理评审中发现的潜在不合格。
5.2纠正预防措施的实施a.顾客投诉的纠正预防措施:当相关部门接到顾客的投诉信息后及时通知品管课,品管课确认后填写《纠正和预防措施单》,由相关部门负责改进。
b.产品的监视和测量中出现不合格或潜在不合格的纠正预防措施。
1.原材料出现不合格或潜在不合格时,品管课填写《纠正预防措施单》,转由供应部对供应商发出纠正措施要求,要求供应商实施改进;2.制程中及储存中出现不合格或潜在不合格后,品管课填写《纠正和预防措施单》,转由生产部责任部门或其他相应部门实施改进。
3.顾客满意度的纠正预防措施:由品管课收集相关信息,品管课确认后填写《纠正和预防措施单》,由相关部门负责改进。
4.内部、外部审核或管理评审中出现不合格或潜在不合格的纠正措施由管理部发出《纠正和预防措施单》,要求责任部门实施改进。
5.3纠正预防措施的实施验证a.纠正预防措施由发出部门负责登记于《纠正和预防措施跟踪关闭一览表》并跟踪验证实施效果,体系审核、管理评审的验证纠正措施实施由管理部负责跟踪实施效果,并做好相应记录;b.如纠正预防措施实施效果的验证为无效时,由相关部门重新填写《纠正与预防措施单》,提出新的纠正与预防措施,并进一步跟踪验证直至问题得到有效解决与处理。
纠正预防措施程序

纠正预防措施程序ISO/TS16949文件类别:程序书责任者:品管部文件编号:QP-30版次:A核准审查制、修订 QA发行章持有者年月日年月日年月日年月日年月日编号 QP-30页码 1/21 目的利用适当信息对产生不合格的根本原因进行调查,采取有效纠正措施以改正,并对潜在的问题采取预防措施防止不合格的再次发生.2 范围凡产品质量不良时,采取的纠正措施,为预防不合格的发生采取的预防措施均属之. 3 职责3.1 发现不合格的部门应分析不合格产生的原因并采取有效纠正措施,以防止其再发生.3.2 各部门都应注意查明任何潜在的质量问题,采取预防措施以避免不合格的发生. 4 定义纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施,以防止再发生。
预防措施:为消除潜在的不合格或其他潜在不期望情况的原因所采取的措施,以防止发生。
5 内容见“纠正预防措施流程图”解决问题公司必须具有一个解决问题的过程,以识别和消除根本原因。
若顾客有规定的解决问题格式,则应采用这规定的格式。
, 防错公司应在矫正措施过程中使用防错方法。
, 矫正措施的影响对其它类似的过程与产品上应用矫正措施来消除不合格原因。
, 退货产品试验/分析从顾客的的产品应分析:并使分析过程的周期缩短、必须保留分析记录并在需要时可获得此记录。
公司应进行分析、及采取矫正措施以防再发。
6 附件附件:纠正和预防措施处理单编号 QP-30页码 2/2作业内容描述, 相关部门提供异常信息和资料(在生产、检验发现异常、不合格处理过程、客户抱怨、投诉情况、内部审核、管理评审)发现问题时,采取纠正措施。
问题发现/发掘, FMEA、新产品、新设备、工程变更(人、机、料、法变更)管理过程、统计分析结果发掘有潜在的问题时采取预防措施。
, 由品管部针对事件的起因、经过和结果进行了解, 并将有关情况反馈事件描述给相关责任单位, 并记录在《纠正和预防措施处理单》上。
, 若客户规定的解决问题的方式,则应按客户要求方式解决,包括表单。
CAPA-Procedure--纠正和预防措施程序
ORIGINATE DEPT.相关部门 RELEVANT DEPT.& CFR21 FDA 21 CFR QSR(Quality System Regulation) 820文件类型Document Type 应用范围 Application Scope品质管理体系程序 QMS PROCEDURE通用 GENERAL修订记录 REVISION HISTORY版本 Rev.A修改内容 Revised ContentsInitial releasing with ISO/TS16949 requirements作者 AuthorXXX生效日期 EFF. DateNov.07,2006Change the title from “ 改正和预防行动程序CorrectiveB and Preventive Action Procedure” to “ 纠正和预防措施 XXX Jan.10th, 2009程序 Procedure for Corrective & Preventive Action”Revised the procedure t o meet ISO13485 regulations (China) CXXX15-07-2014(USA) requirements文件审批 APPROVAL本文件须经相关部门工程师(或主管)签批,请作者指定。
This d o cu m ent shall be reviewed by ISO Coordinator and. The author shall determine.编写部门部门名称DEPT. TITLEQA ManufacturingMachining Engineering PE工程师姓名NAME OF ENGINEER工程师签署SIGNATURE经理姓名NAME OF MANAGER经理签署SIGNATURE管理者代表签署 SIGNATURE OF M.R.拒签理由 Reason of reject:Ditto总经理签署 SIGNATURE OF GM.文件分发 DISTRIBUTION部门 DEPT.EngineeringQAHR 数量 Q’TY1 部门 DEPT.AssemblyPlatingS tamping 数量 Q’TY 部门 DEPT.OFFSourcingFinance数量 Q’TYMaintenanceMolding1目的Purpose本程序规范了为消除存在或潜在的不合格而采取纠正预防措施的流程,以确保类似不合格不再发生或潜在不合格的发生,促进质量管理体系的持续改进。
纠正和预防措施程序培训教材

• 不合格发生部门负责对不合格进行分析,制定、执行相应 的纠正措施。
• 管理者代表负责监督、协调改进、纠正和预防措施的实施。 • 营销中心负责有效地处理顾客意见。
CAPA流程图
(潜在)不符合 发现
品质主管确认
启动CAPA
因果图
人员+机器+材料+方法+环境
采用多次“为什么”
5Why法
不合格品案例
装配车间发现:后门锁左件装配后,发现卡爪少一 个爪(如下图),不合格率约10%;
原因分析
1.通过因果图来分析发生的原因
环
机/工具
人
6气温低
4压入设备规格不正确 1未经过培训的新人
5工具磨损 7铁件有毛刺
10没有按规定装配
2未经过培训的代理人 卡
产 模具冲头 较高,但耐
理。
技术。
生 磨损快。 用性不足,
原
磨损未及时
因
发现。
措施
担当 期限 分类
1,对磨损 冲头进行 修复;
2,对凸凹 模进行镀 钛处理。
模修
3,每次冲 压换线后的 末件保留在 模具上,进 行模具磨损 状况确认。
模修
4,备品及 类似零件 的备品进 行镀钛处 理并验收。
5,凸凹模 图纸上追加 镀钛处理要 求。
7 铁件有毛刺吗
缺爪的零件都有毛刺。
8 塑料原材料错误吗?
9 卡爪单件缺爪吗?
10 没有按规定的方法装配吗?
11 工具使用方法不符合规范吗?
12 压入时用力过猛吗? 13 类似产品有相同情况吗?
右件有类似的隐患存在
CAPA纠正预防措施流程

纠正和预防措施管理流程说明一、流程图二、分步骤说明# Step 1 问题描述详细的描述CAPA1.对来自投诉、产品缺陷、退回、偏差、内外部检查结果、工艺性能和产品质量监测趋势等的数据信息进行分析,确定已存在和潜在的质量问题。
必要时,运用适当的统计学方法。
2.详细、清楚地对问题进行描述,应包括以下内容:•发生了什么?•问题是怎么发生的?•在什么地方发生的?•什么时间发生的?•怎么发现的?是谁发现的?•当时采取了哪些措施?简洁、清楚的描述问题,有利于评估分析问题,找到问题产生的根本原因!# Step 2 评估审核评估问题的风险,选择合适的处理流程通过评估,确定问题的严重程度及是否需要采取整改措施。
若需要,根据风险评估等级确定措施级别。
评估主要包括:1.预测潜在影响:CAPA管理的“评估问题“环节,涉及的一个核心就是问题的潜在影响,以及对公司已经造成的实际风险。
这可能包括该问题在成本、功能、产品质量、安全性、可靠性和客户满意度方面可能产生的影响。
如果上级领导意识不到问题可能造成的影响,也就不会分配资源进行这方面的调查。
2.评估风险:利用对问题影响的预测,可以评估问题的严重性。
与问题相关的风险级别可能会影响后续采取的行动。
例如,对产品功能或安全构成严重风险的问题可能会被分配高优先级,选择全部流程进行处理。
3.采取临时补救措施:根据上述影响和风险评估的结果,可能需要立即采取补救措施(遏制措施)来纠正这种情况,如果影响程度低和风险不高,在文件记录相关的决定和适当的跟踪确认后,CAPA即可关闭。
★正确的评估问题的风险,便于分配合适的资源处理问题!# Step 3 团队职责组建团队,给团队成员分配职责创建一个负责进行调查和制定行动计划的团队。
团队的成员需要明确自己的职责,这样他们才能有目的、有计划的去完成自己的工作。
确保你的团队是跨职能的,并告知他们在调查中的角色。
★调查的一个关键要素是将责任分配到人,确定需要的相关资源。
《纠正和预防措施》PPT课件

或物料批次或部分批次的影响评估 矫正措施的执行 根本原因的调查 不符合性或不期望事件根本原因的调查、记录 评估是否需要行动,防止不符合性/不期望事件的再发
生,或潜在不符合事件发生 纠正预防行动 确定CAPA行动,应能解决不符合性/不期望结果,解
医学PPT
11
第一步 回顾信息
第二步 确定可行解决 方案并达成一致
第三步 评估、选择
和实施
第四步 关闭纠正 预防措施
流程图
决定1
决定2
关键决策点1 •确定根本原因及纠正预防措施接受标准
•目标 •结果 •记录决策
决策点3
关键决策点2 •确定纠正预防措施范围
•结果 •记录决策
关键决策点3 •选择解决方案
预防行动:消除潜在的不符合和不期望现 象的根源所采取的行动,防止发生 (occurrence) 。
医学PPT
7
纠正和预防措施的目标
问题陈述 根本原因 危险程度描述 解决问题的方案
医学PPT
调查确定
8
调查流程
如果涉及调查,应按规定进行: 问题描述:确认并描述实际或潜在的质量不符合性或
不期望事件 矫正措施: 对不符合性或不期望事件的级别或重要性评估,及矫
纠正和预防措施
Corrective Action and Preventive Action
浙江我武生物科技有限公司 2010.09
医学PPT
1
内容
目的 CAPA适用于哪些情形 定义 流程
医学PPT
2
纠正预防措施目的
一个系统的、标准的、有效的CAPA可以保证: 偏差,不符合性,缺陷或其它不期望的情况不再出现,或
纠正和预防措施控制程序

纠正措施控制流程图预防措施控制流程图1. 目的消除明确的或潜在的不合格原因,确保质量体系有效运行和产品质量符合规定要求。
2. 适用范围适用于产品、过程和质量体系不合格的纠正和预防控制。
3. 术语和定义纠正:为消除已发现的不合格所采取的措施。
纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施。
预防措施:为消除潜在不合格或其他潜在不期望情况的原因所采取的措施。
4. 职责技术部职责:负责产品质量纠正和预防工作的归口管理。
负责应用过程FMEA方法和相关记录对过程进行分析。
负责对预防措施的实施效果组织验收和验证。
负责将已采取的纠正措施和实施的控制应用进行推广。
负责对采取纠正措施涉及的相关技术文件的更改,并纳入工艺管理。
质管中心职责:负责收集与产品、过程和质量体系有关的潜在不合格信息,并对预防措施效果进行验证。
负责现生产中出现的不合格信息的整理、汇总和分析,以《质量月报》形式反馈给技术部,并负责针对现生产所采取纠正措施的有效性进行验证。
负责组织对顾客退回产品的分析和处理。
负责组织对顾客退回产品的分析和处理。
营销部负责从顾客需求和期望、产品使用与维修保养、顾客满意度测量和市场分析中,提出潜在不合格信息,并对预防措施效果进行跟踪、验证。
负责收集、汇总顾客反馈及顾客满意度调查中发现的不合格,以《服务月报表》形式向技术部反馈;并负责针对售后和顾客抱怨的不合格所采取纠正措施的有效性进行跟踪验证。
论证小组职责:负责对与产品、过程有关的不合格进行评审,分析查找产生问题的原因,确定采取纠正措施项目;并制定相应的纠正措施。
负责组织纠正措施的实施、监督和检查,并组织对措施效果进行验收和验证。
其他部门负责收集部门内部和外部质量信息中提出的潜在不合格信息。
其他部门负责对发生在本部门的产品质量、过程不合格信息的收集,必要时通过《信息反馈单》的形式提出实施纠正措施要求。
5. 工作程序质量信息的收集和传递评价各部门根据收集到的信息,对状况进行评估,评估的内容可包括:1)影响程度(严重性和涉及面);2)处理的紧急程度(时限)以防止恶化或波及;3)改善需投入资源的大小。
质量异常纠正及预防改善措施流程图

继续生产 Continue Production
YES
效果验证 Effect Confirmation
Novatron
来料质量异常纠正及预防改善措施流程图 Incoming material quality deviation corrective and preventive action flow chart
来料
Incoming
整批不合格 Total Defect Lot
《供应商纠正/预防措施联络单 Send VCAPAN
NO
入库
Stocking
Novatron
质量异常纠正及预防改善措施流程图 Quality Deviation Corrective and Preventive Action Flow Chart
制程质量异常纠正及预防改善措施流程图 Production process quality deviation corrective and preventive action flow chart
质量异常 Quality Deviation
QC确认 QC Confirm
NO
记录/反馈 Record/Feedback
技术部确认 Tech Confirm
NO
〈品质异常联络单〉 Quality Deviation Notice
YES YES
原因分析 Cause Analysis
纠正/预防措施 CAPA
IQC check
NO
物料评审会议 MRB
不良原因分析 Cause analysis
YES
合格标识 Qualified label
让步接收 Waive
挑选 Select
纠正措施和预防措施标准操作程序

目的:建立纠正措施和预防措施(CAPA)管理规程,纠正与预防不符合、潜在不符合、不期望事件的发生,确保公司持续、有效地执行GMP规范及相关法律法规。
范围:适用于生产质量管理活动中所有纠正措施和预防措施的制定、实施和控制。
责任:责任部门负责因自身原因引起的一般不符合或潜在的不符合原因调查、分析及纠正措施和预防措施的制订、实施.质量部负责发出采取纠正措施和预防措施的信息;并负责对纠正措施和预防措施实施效果进行确认。
内容:1、定义1。
1纠正措施:为消除已发现的不合格或其他不期望情况的发生所采取的措施,纠正措施是针对问题的根本原因,减少或消除问题再发生的措施。
1。
2预防措施:为消除潜在不合格或其他潜在不期望情况的发生所采取的措施,采取预防措施是为了防止不合格或其他潜在不期望情况的发生。
2、纠正预防措施的范围纠正和预防措施(CAPA),来源于客户投诉、产品缺陷、召回、生产偏差、实验室异常检验结果偏差、自检、外部审计(包括政府检查)、工艺性能和产品质量监测趋势、变更控制、产品年度回顾等活动中发现问题所采取的措施.整改措施的深度和形式应与风险评估的级别相适应.3、实施纠正和预防措施的职责3.1企业所有员工3.1.1正确理解纠正和预防措施(CAPA)规程的要求.3。
1。
2在不合格问题发生时,按要求采取适当的措施,并报告主管或直接领导.3。
2CAPA措施负责人3.2.1根据批准的计划,在规定期限内完成相应的整改措施.3。
2.2定期检查整改措施计划的进展,直到所有的整改措施均已完成并最终得到质量管理人员的确认、批准。
3.2。
3因特殊原因,整改措施计划需要进行变更或延长时,在原计划完成日之前提出申请,并得到部门负责人的批准。
3.3质量部3。
3.1负责建立和维护纠正和预防措施(CAPA)系统.3.3.2批准CAPA执行。
3.3.3批准CAPA的变更、包括完成期限的延长。
3。
3。
4跟踪CAPA实施进展情况。
3.3。
5确保CAPA的合理性、有效性和充分性.3.4质量受权人批准涉及产品召回、药品监督管理部门检查发现等风险级别较高问题的整改措施.4、纠正和预防措施程序4。
纠正和预防措施控制程序(附完整表格)

文件编号 版本号 文件类型 二级程序文件 编制部门 质量管理部 纠正和预防措施控制程序 修订号 页码
QP-QA-01 A 1 3/3
5.6.1 品质异常联络控制流程图(附件一) 5.6.2 品质异常发现部门发现品质异常现象时,须及时报告部门负责人,并书面通知品质保证 部或在每日上午9:30开品质会议时提出通知,相关人员进行纠正预防措施。 5.6.3 品质保证部须对所发生的品质异常现象进行确认,如属重大品质异常,须发出《品质异常 联络书》向副总经理或以上人员报告并通知相关部门,如属普通的品质异常,可直接发出 《品质异常联络单》要求相关部门进行改善。 5.6.4 品质保证部负责人或以上人员对《品质异常联络单》进行批准后,指示相关部门进行异常 原因分析,处理对策分析和防止再发生对策分析。回复日期参照《品质异常联络单》中 丌良程度一栏中的要求,无明确要求时,5个工作日内回复。 5.6.5 相关部门采取对策并确认有敁后,在《品质异常联络单》上签署完成日期后通知品质保证 部对所采取的对策的敁果进行确认。 5.6.6 品质保证部将确认的结果记录在《品质异常联络单》中“敁果确认”栏内,若确认结果为 已解决此品质异常,则可终结此份《品质异常联络单》;若确认为未解决此品质异常,则 继续督促相关部门采取措施解决此品质异常。若经反复多次,确属暂时难以解决的品质异 常,由相关部门和品质保证部共同以书面形式向副总经理或以上人员申请将品质异常转入 慢性品质异常进行控制,经副总经理或以上人员批准,品质保证部在《品质异常联络单》 “敁果确认”栏注明:“已转入慢性品质异常”,此份《品质异常联络单》可予以终结。所 有重大品质异常的确认结果都须报告给副总经理或以上人员。 5.7 慢性品质异常的纠正和预防措施的控制:慢性品质异常须由副总经理或管理者代表确定与人担 当进行对策活动,担当者须在每次品质会议报告改善结果。 5.8 纠正和预防措施结果的上报:管理者代表应根据异常或须改善提出的频繁程序丌定期地将所采 取的纠正和预防措施情况进行汇总,并书面汇报给副总经理,分析纠正和预防措施的落实情况 ,确定需要进一步采取的措施。 5.9 发现环境异常时发现人员须及时报告部门负责人,联络ISO推进室采取有敁的纠正预防措施. 5.10 本程序执行过程中产生的质量记录的保管要求参见《文件不记录管理程序》。 6.0 支持文件 (无) 7.0 相关记录 7.1 《品质异常联络控制流程图》 7.2 《内审丌符合项报告书》 7.3 《管理评审丌符合项报告书》 7.4 《品质异常联络单》
纠正预防和改进措施控制程序(含流程图)

文件编号:页数1/8 生效版本:C0文件制修订记录NO 制/修订日期修订编号制/修订内容版本页次1 2013-03-01 - 新制订A02 2021-02-10 2021/2/10 新版全面升级C0核准审核制订文件编号:页数2/8 生效版本:C01.0目的:采取有效的纠正和预防措施,实现质量管理体系的持续改进,特编写此程序。
2.0范围:2.1进料检验及制程中发现之重大异常,客户退货或抱怨等。
2.2环境系统中,异常排放、意外事件、居民抱怨等。
2.3内外部系统稽核之缺失。
2.4预防措施的实施及确认。
3.0职责:3.1提出异常单位:公司各部门。
3.2异常发出管制单位及收回单位:品质部。
3.3原因分析,纠正及预防措施的拟定、执行:异常造成单位。
3.4效果确认单位:品质部。
3.5跨功能小组:负责产品质量规划作业及重大异常之解决。
3.6研发部:负责制程能力提升,评估、新增及修改相关工程管理标准,作业指导书及操作说明书的编制。
4.0定义:无5.0作业内容:5.1纠正预防处理办法:5.1.1异常发生:异常发生时,发现异常者应立即通知责任单位之现场管理人员及主管级(含)以上管理人员(或其代理人),并由品质部于 4 小时内发出《品质异常联络单》,注明异常单发出日期,编号,异常单位并说明异常状况;5.1.2判定:由品质部主管判定是否为重大异常,若为重大异常则指定专责人员组成改善小组进行改善,若非重大异常则依一般改善流程;5.1.3原因分析:异常造成单位于接获异常通知单时,分析其发生原因;5.2纠正与预防措施之拟定与实施:文件编号:页数3/8 生效版本:C05.2.1纠正措施:在异常情况发生时,应采用纠正行动和管制措施以保证造成不符合的制程或不合格产品得到有效的控制.纠正措施实施后经确认有效,则需将其有效性作为改善标准,例如修订标准书、防呆措施,避免问题再发。
5.2.2预防措施:需依据以往单一项目的质量记录如客户抱怨经验、管制图中累积之趋势(未超出判定标准)或有 Cpk 值下降之趋势,内部稽核记录观察事项等,为预防异常状况的发生,列为预防措施改善,或透过 FMEA 以达到异常情况发生前的预防效果。
施工工艺控制纠正与预防措施
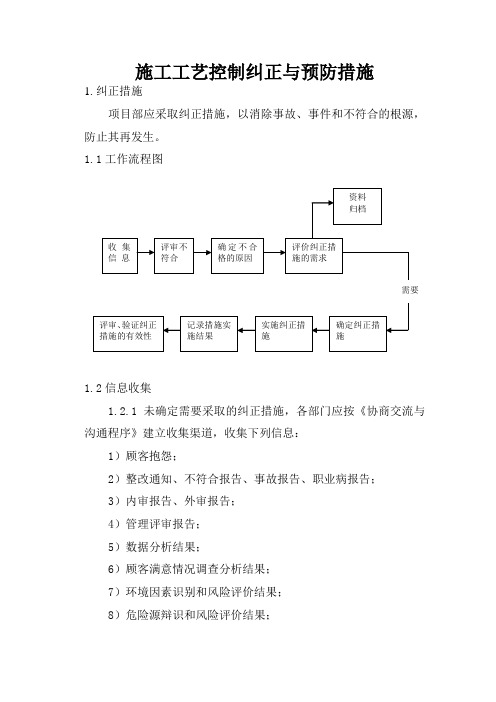
施工工艺控制纠正与预防措施1.纠正措施项目部应采取纠正措施,以消除事故、事件和不符合的根源,防止其再发生。
1.1工作流程图1.2信息收集1.2.1未确定需要采取的纠正措施,各部门应按《协商交流与沟通程序》建立收集渠道,收集下列信息:1)顾客抱怨;2)整改通知、不符合报告、事故报告、职业病报告;3)内审报告、外审报告;4)管理评审报告;5)数据分析结果;6)顾客满意情况调查分析结果;7)环境因素识别和风险评价结果;8)危险源辩识和风险评价结果;9)体系运行记录;10)过程检测记录。
1.2.2各部门应进行下列信息反馈,以便公司相关部门制定纠正措施:1)将质量问题、质量事故、安全事故信息反馈到安全质量管理部;2)将环境事故信息反馈到工程管理部;3)将不合格物资信息反馈到设备运输物资部;4)将职业病信息反馈到社会职能部;5)将顾客投诉和相关投诉信息反馈到相关部门。
1.3评审不符合1.3.1项目部的负责人应组织有关人员对收集的信息进行汇总,评审不符合,分析并确定不符合产生的根源。
1.3.2对不符合项的原因分析可考虑如下方面,但不仅限于此:1)没有认真贯彻程序文件或相关支持性文件的要求;2)没有全面理解管理体系文件的要求;3)缺乏必要的培训;4)缺少必要的支持性文件;5)没有获取相应的法律法规或获取渠道不畅通;6)管理体系文件规定不清或错误问题;7)工作不负责任;8)缺乏必要的资源;9)没有将相关要求传递至相关方,信息交流或沟通不到位;等。
1.3.3对质量问题的原因分析可考虑如下方面,但不仅限于此:1)设计问题而在设计文件会审中未被发现;2)技术方案编制的偏差或技术交底不清;3)未获得必要的产品要求的输入信息(如未获得有关法律法规、技术标准);4)物资不合格;5)施工操作未执行相应程序;6)检验试验问题;7)成品保护问题;等。
1.3.4对不合格物资的原因分析可考虑如下方面,但不仅限于此:1)供货厂家的制造加工问题;2)物资运输造成的损坏;3)物资在现场贮存、保护不当;4)物资需用计划或采购计划的错误;5)设计错误未被发现;6)未执行采购程序;等。
纠正与预防措施(CAPA)管理规程
姓名/职务Name/Title 起草人/Written by审核人/Reviewed by批准人/Accepted by签名/日期Signature/Date分发质量控制部102 车间销售部财务部人力资源部部门【1】份【】份【1】份【】份【】份质量保证部101 车间104 车间总经办生产部注册部103 车间工程技术部安全环保部档案室【1】份【1】份【1】份【1】份【1】份【1】份【1】份【】份【1】份【1】份针对某个质量问题进行调查,找出根本原因,采取纠正和预防措施,以消除缺陷及潜在的风险,防止缺陷及不良趋势再次发生,以提高产品质量、优化质量体系,实现质量体系的持续改进。
本规程描述了有关 CAPA 活动的确定、实施及跟踪检查和监控的全面纠正和预防描述计划,合用于诺泰制药的所有质量、生产、研发及销售过程。
令部门➢相关部门负责根据已批准的规程申请纠正及预防描述;➢负责对缺陷和不良隐患进行充分调查以了解质量问题的根本原因;➢分析原因、制定实施相应的纠正、预防措施并对过程中所有发生的处理措施和变更处理予以记录;➢CAPA 所有人及每一个部门主管人员负责确认在获得质量部门批准前不得实施CAPA;➢每一个部门负责确保纠正和预防行动的实施及遵循。
◆注册部负责对所提议的 CAPA 行动进行药政评估,以确保制定的纠正、预防措施符合相关的政府机构的规定。
◆质量保证部➢负责创建、维护和监控 CAPA 计划、评估纠正预防措施的实施效果。
➢负责确保使用该计划的相关人员得到培训。
1.1 不符合:不满足规定的要求或者不在预期范围内;1.2 根本原因:导致不合格的根本原因、实际情况或者过程。
1.3 纠正措施:为消除已发现的不符合所采取的措施;1.4 预防措施:为消除潜在不符合所采取的措施;1.5 纠正预防措施:为防止已浮现的不合格、缺陷或者其它不希翼情况的再次发生,消除其直接原因和潜在原因所采取的措施。
1.6 CAPA 行动申请表(CAR):用来支持/记录 CAPA 过程的文件。
预防和纠正措施控制程序

1. 目的消除明确的或潜在的不合格原因,确保质量体系有效运行和产品质量符合规定要求。
2. 适用范围适用于产品、过程和质量体系不合格的纠正和预防控制。
3. 术语和定义3.1纠正:为消除已发现的不合格所采取的措施。
3.2纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施。
3.3预防措施:为消除潜在不合格或其他潜在不期望情况的原因所采取的措施。
4. 职责4.1技术部职责:4.1.1负责产品质量纠正和预防工作的归口管理。
4.1.2负责应用过程FMEA方法和相关记录对过程进行分析。
4.1.3负责对预防措施的实施效果组织验收和验证。
4.1.4负责将已采取的纠正措施和实施的控制应用进行推广。
4.1.5负责对采取纠正措施涉及的相关技术文件的更改,并纳入工艺管理。
4.2质量部职责:4.2.1负责收集与产品、过程和质量体系有关的潜在不合格信息,并对预防措施效果进行验证。
4.2.2负责现生产中出现的不合格信息的整理、汇总和分析,以《质量周报》形式反馈给技术部,并负责针对现生产所采取纠正措施的有效性进行验证。
4.2.3负责组织对顾客退回产品的分析和处理。
负责组织对顾客退回产品的分析和处理。
4.3销售部负责4.3.1从顾客需求和期望、产品使用与维修保养、顾客满意度测量和市场分析中,提出潜在不合格信息,并对预防措施效果进行跟踪、验证。
4.3.2负责收集、汇总顾客反馈及顾客满意度调查中发现的不合格,以《服务月报》形式向技术部反馈;并负责针对售后和顾客抱怨的不合格所采取纠正措施的有效性进行跟踪验证。
4.4多方论证小组职责:4.4.1负责对与产品、过程有关的不合格进行评审,分析查找产生问题的原因,确定采取纠正措施项目;并制定相应的纠正措施。
4.4.2负责组织纠正措施的实施、监督和检查,并组织对措施效果进行验收和验证。
4.5其他部门负责收集部门内部和外部质量信息中提出的潜在不合格信息。
其他部门负责对发生在本部门的产品质量、过程不合格信息的收集,必要时通过《信息反馈单》的形式提出实施纠正措施要求。
纠正及预防措施办法

纠正及预防措施办法1.目的通过对显著性的和/或潜在性的产品质量/交付/服务等不合格进行原因分析,并采取有效的纠正措施或预防措施,以消除不合格因素的存在,使类似问题发生的可能性减少到最低限度,防止已经出现的不合格或缺陷再次发生。
2.范围凡与本企业质量体系和与产品质量/交付/服务等形成的有关环节之显著性的和/或潜在性的不合格均适用之。
3.定义3.1 纠正措施:为消除现有不合格或其它不希望情况产生的原因以防止再次发生所采取的措施。
3.2 预防措施:为消除潜在不合格或其它不希望情况的原因以防止其发生所采取的措施。
3.3 显著性不合格:指现在已经发生的、可知道的产品质量/交付/服务等不合格的情况。
3.4 潜伏性不合格:指现在尚未发生,但有趋势或迹象可预期将发生的产品质量/交付/服务等不合格。
4.职责4.1管理者代表和/或总经理负责重大的已拟定的纠正与预防措施的审查、核准。
4.2技检部和相关部门负责显著性和/或潜在性不合格事项的原因分析,纠正与预防措施拟定及执行、纠正与预防措施的改善效果追踪与确认。
4.3相关责任单位和/或管理层负责显著性和/或潜在性不合格事项的纠正与预防措施的结果评审。
5.工作内容5.1 纠正与预防措施控制流程图(见附件一)。
5.2 纠正预防措施实施和执行的步骤和内容:5.2.1 纠正措施提出时机:5.2.1.1各种内部沟通会议中决定的改进问题;5.2.1.2 本公司内连续发生的问题;5.2.1.3 连续出现产品不合格或不合格问题比较严重5.2.1.4 顾客抱怨时;5.2.1.5 内审、管理评审会议中决定改进的问题;5.2.1.6其他不符合质量方针、目标或质量管理体系文件时。
5.2.1.7供应商连续出现质量问题。
5.2.1.8技检部经理认为有必要时。
5.2.2预防措施提出的时机5.2.2.1添购新设备、设备改造时。
5.2.2.2 PFMEA 分析结果不能达到要求时。
5.2.2.3 生产区域巡回检查发现的潜在不合格、环境安全事故隐患时。
