《有机化学反应方程式》书写练习
有机化学反应方程式的书写

2012届高二化学有机复习高二有机化学基本反应方程式书写训练
班级姓名学号成绩1.实验室中以乙醇为原料来制取乙烯:
2.用乙醇为原料来制备乙醛:
3.实验室用CaC2和水制乙炔:
4.用1,2-二氯乙烷为原料来制取乙炔:
5.乙醇和CH3CO18OH在浓硫酸作用下加热制乙酸乙酯:
6.乙醇为原料制备乙醚:
7.CH3CHO发生的银镜反应:
8.2-丙醇的催化氧化反应:
9.甲烷在光照时与氯气发生反应,生成气态有机产物:
10.丙烯使溴的四氯化碳溶液褪色:
11.苯的硝化反应:
12.苯的溴代反应:
13.苯酚的溴代反应:
14.制备酚醛树脂:
15.溴乙烷的水解反应:
16.甘油与硝酸的酯化反应:
17.甲醛与足量的新制的氢氧化铜浊液在加热反应:
18.烃(CxHy)在氧气中完全燃烧:
19.烃的含氧衍生物(CxHyOz)在氧气中完全燃烧:
20.乙醇的分子间脱水反应:
21.环己醇的催化氧化反应:
22.甲酸乙酯的水解反应:
23.向苯酚钠溶液中通入CO2气体:
24.用甲苯制备TNT的反应:
25.乙烯水化法制乙醇:
26.苯酚与金属钠:
27.加热条件下,用乙醇和浓氢溴酸来制备溴乙烷:
28.2-丁烯的加聚反应:
29.乙二酸和乙二醇反应生成环酯:
30.乙二酸和乙二醇反应生成聚酯:。
课外化学方程式的书写

课外化学方程式的书写1、铜器在潮湿的空气中,在氧气、二氧化碳和水份的作用下、表面会慢慢地生成一层绿色的铜锈,主要成分的化学式为Cu2(OH)2CO3。
该反应的化学方程式为:___________________________ 。
2、人类很早就发现,孔雀石[主要成分的化学式Cu2(OH)2CO3]在熊熊燃烧的树木中灼烧后,发生分解反应,生成三种氧化物,剩余固体再与碳反应,余烬里有一种红色光亮的金属显露出来。
试用化学方程式表示孔雀石变化的两个主要反应:(1)____________________ _。
(2)______________________。
3、将铜粉放入稀硫酸中并通入氧气,溶液的颜色变成蓝色。
这一反应的化学方程式是________ 。
4、黑火药是我国古代四大发明之一,它是由木炭、硫黄、火硝(硝酸钾)按一定比例混合而成的,爆炸时生成硫化钾、氮气和二氧化碳。
黑火药爆炸的化学方程式是_______________________ 。
5、家庭使用的液化气是碳氢化合物,化学式可写为CxHy在空气中完全燃烧生成 ________,化学方程式为_______________________________________________________。
6、取8克某有机化合物(相对分子质量为32),在氧气中完全燃烧生成11克二氧化碳和9克水,则该有机物中一定含有________________元素,误服该有机物会使人中毒失明甚至死亡,写出此有机物在空气中燃烧的化学方程式____________________________________。
7、海洛因、鸦片、大麻都是严重危害人类健康的毒品,其中大麻主要成分的化学式为C21H30O2,在空气中焚烧大麻主要成分的化学方程式是_______________________________。
8、河水里的微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需的O2量叫生化需氧量(BOD),BOD是衡量水体质量的一个指标。
2014福建化学会考有机反应方程式书写题

(福建会考·2013)(2)乙烯能使溴水褪色,生成1,2—二溴乙烷(CH2Br—CH2Br)。
写出该反应的化学方程式:。
(福建会考·2012)(2)2011年12月16日,印度发生假酒中毒事件,导致200多人伤亡。
假酒中的有毒物质是甲醇(CH3OH),它是一种理想燃料。
写出在CH3OH空气中燃烧的化学方程式:。
(福建会考·2011)(1)“可燃冰”是天然气的水合物,外形似冰,它的主要可燃成分是甲烷,写出甲烷燃烧的化学方程式:。
(福建会考·2010)(2)CH4与Cl2在光照条件下能生成CH3Cl,写出该反应的化学方程式:。
(福建会考·2009)(2)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,请用化学方程式表示该反应的原理:。
(福建会考·2008)(2)聚氯乙烯( )有毒,不能用于制作食品保鲜袋。
由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为:。
高中经典有机化学反应方程式

章末回顾排查专练(十二)排查一、重要有机反应方程式再书写1.2.2C 2H 5OH +2Na →2C 2H 5ONa +H 2↑; 3.CH 3CH 2OH ―――――――――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O ; 4.C 2H 5OH +HBr ――→△ C 2H 5Br +H 2O ;5.2C 2H 5OH +O 2―――――――――→Cu 或Ag △2CH 3CHO +2H 2O ;9.2CH 3CHO +O 2―――――――――→催化剂△2CH 3COOH ; 10.CH 3CHO +H 2――――――――――→催化剂△CH 3CH 2OH ; 11.CH 3CHO +2Ag(NH 3)2OH ――→△ CH 3COONH 4+2Ag ↓+3NH 3+H 2O ;12.CH 3CHO +2Cu(OH)2――→△ CH 3COOH +Cu 2O ↓+2H 2O ;13.CH 3COOH +C 2H 5OH 浓H 2SO 4△CH 3COOC 2H 5+H 2O ;14.CH 3COOC 2H 5+H 2O 稀H 2SO 4△CH 3COOH +C 2H 5OH ;15.乙二醇和乙二酸生成聚酯16.排查二、常考易错再排查 1.按碳原子组成的分子骨架分,有机物可分为链状化合物和环状化合物,环状化合物又包括脂环化合物和芳香族化合物。
按官能团分,有机物可分为烃(烷烃、烯烃、炔烃、芳香烃)和烃的衍生物(卤代烃、醇、酚、醛、酸、酯等)。
( )2.具有相同分子式,不同结构的化合物互为同分异构体。
包括碳链异构(如CH 3CH 2CH 2CH 3与)、位置异构(如CH 3CH===CHCH 3与CH 3CH 2CH===CH 2)、官能团异构(如CH 3CH 2OH 与CH 3OCH 3)、顺反异构(顺2-丁烯与反2-丁烯)、手性异构等。
( )3.发生加成反应或加聚反应的有机物分子必须含有不饱和键。
高考化学陌生方程式的书写练习题(含答案)

高考化学陌生方程式的书写练习题(含答案)1.利用石灰乳和硝酸尾气中的NO、NO2反应可以净化尾气同时获得Ca(NO2)2,但在生产中溶液需要保持弱碱性,因为在酸性溶液中Ca(NO2)2会分解,其中产生的一个产物是NO。
该反应的离子方程式为:Ca(OH)2 + 2NO → Ca(NO2)2 + H2O2.生产硫化钠通常采用无水芒硝(Na2SO4)-碳粉还原法,煅烧所得气体中 CO 和 CO2 的量相等。
该反应的化学方程式为:Na2SO4 + 2C → Na2S + 2CO2 + SO23.向含碘废液中加入稍过量的Na2SO3溶液可以将废液中的I2还原为I-。
该反应的离子方程式为:2Na2SO3 + I2 → 2NaI + Na2S2O64.向含Cr2O7的酸性废水中加入FeSO4溶液可以使Cr2O7全部转化为Cr3+。
该反应的离子方程式为:FeSO4 + Cr2O7^2- + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 +H2O5.当温度高于200℃时,硝酸铝会完全分解成氧化铝和两种气体,其体积比为4:1.该反应的化学方程式为:4Al(NO3)3 → 4A l2O3 + 12NO2 + O26.(1) AgNO3在光照下会分解生成Ag和红棕色气体,其光照分解反应的化学方程式为:2AgNO3 + hv → 2Ag + 2NO2 + O22) 以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。
该反应的化学方程式为:2H2O → 2H2 + O23) 当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为8)中的SO3将NO2转化为NO。
该反应的离子方程式为:2NO2 + CaSO3 + H2O → 2NO + CaSO4·2H2O4) CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜。
该反应的化学方程式为:2CuSO4 + P4 → 2Cu + P4O10 + 2SO25) 工业制法中,将白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。
2022年高考化学有机转化关系及反应方程式书写
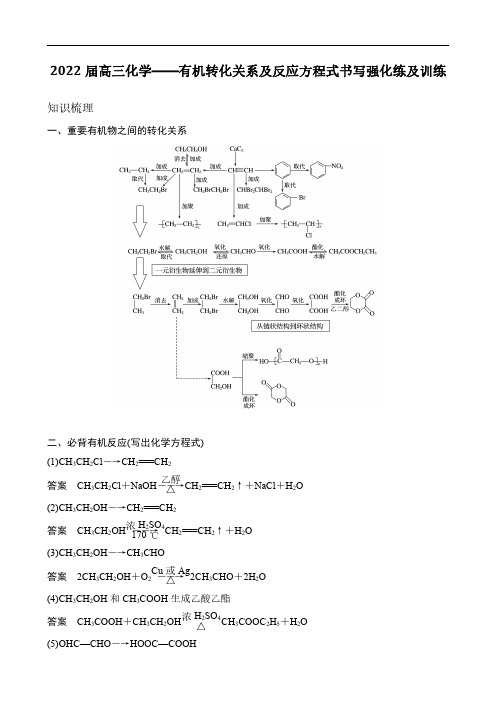
2022届高三化学——有机转化关系及反应方程式书写强化练及训练知识梳理一、重要有机物之间的转化关系二、必背有机反应(写出化学方程式)(1)CH 3CH 2Cl ―→CH 2===CH 2答案CH 3CH 2Cl +NaOH ――→乙醇△CH 2===CH 2↑+NaCl +H 2O(2)CH 3CH 2OH ―→CH 2===CH 2答案CH 3CH 2OH ――→浓H 2SO 4170℃CH 2===CH 2↑+H 2O (3)CH 3CH 2OH ―→CH 3CHO 答案2CH 3CH 2OH +O 2――→Cu 或Ag △2CH 3CHO +2H 2O(4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O (5)OHC—CHO ―→HOOC—COOH答案OHC—CHO +O 2――→催化剂△HOOC—COOH(6)乙二醇和乙二酸生成聚酯答案n HOCH 2—CH 2OH +n HOOC—COOH――→一定条件+(2n -1)H 2O (7)乙醛和银氨溶液的反应答案CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O(9)答案(10)答案(11)和饱和溴水的反应答案(12)和溴蒸气(光照)的反应答案(13)和HCHO 的反应答案+(n -1)H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)和NaOH 的反应三、常考有机物的检验1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
人教版(2019)高中化学选择性必修3:有机化学基础方程式练习题(含答案)

人教版(2019)高中化学选择性必修3:有机化学基础方程式练习题一、烷烃通式:C n H2n+21.氧化反应(1)甲烷的燃烧:2. 取代反应(1)甲烷和氯气在光照条件下发生取代反应(一氯取代)二、烯烃通式:C n H2n官能团名称:碳碳双键1. 加成反应(1)乙烯与溴水(Br2的CCl4溶液)加成:(2)乙烯与氢气加成:(3)乙烯与水加成:(4)丙烯与HBr加成:(5)1,3-丁二烯与Br2发生1,2-加成,1,4-加成:(6)1,3-丁二烯与乙烯发生环加成反应:2. 加聚反应(1)乙烯发生加聚反应生成聚乙烯:(2)丙烯发生加聚反应生成聚丙烯:3. 乙烯的制取(1)溴乙烷发生消去反应:(2)乙醇发生消去反应:三、炔烃通式:C n H2n-2 官能团名称:碳碳三键1. 乙炔的制取:2. 加成反应(1)乙炔与溴水(Br2的CCl4溶液)完全加成:(2)乙炔与HCl加成得到氯乙烯:四、苯和甲苯通式:C n H2n-61. 取代反应(1)苯和液溴发生取代反应:(2)苯和浓硝酸发生取代反应:(3)甲苯和浓硝酸发生取代反应:(4)甲苯和甲苯与氯气在光照条件下发生取代反应(一氯取代):(5)甲苯与氯气在FeCl3催化下发生对位取代反应:注意:甲苯在光照条件下发生侧链的取代,在催化剂条件下发生苯环上的取代。
2. 加成反应(1)苯和氢气发生加成反应:五、卤代烃(溴乙烷)官能团名称:卤素原子1. 水解反应(取代反应)(1)溴乙烷与氢氧化钠水溶液反应:2. 消去反应(2)溴乙烷与氢氧化钠醇溶液反应:1. 置换反应(1)乙醇与钠反应:2. 氧化反应(1)乙醇燃烧:(2)催化氧化①乙醇在铜或银催化下与氧气反应:②1-丙醇在铜或银催化下与氧气反应:③2-丙醇在铜或银催化下与氧气反应:3. 消去反应(1)乙醇发生消去反应:4. 取代反应(1)乙醇生成乙醚:(2)乙醇与浓氢溴酸反应生成溴乙烷:(3)乙醇与乙酸发生酯化反应生成乙酸乙酯:七、苯酚官能团名称:羟基1. 弱酸性(1)苯酚与氢氧化钠溶液反应:(2)往苯酚钠溶液中通入CO2气体:(3)苯酚与碳酸钠溶液反应:2. 取代反应(1)苯酚与浓溴水反应:3. 显色反应(1)苯酚能和FeCl3溶液反应,使溶液呈紫色。
有机化学方程式练习

有机化学方程式练习班级姓名座号1. 2-氯丙烷与氢氧化钠的醇溶液共热2-氯丙烷与氢氧化钠的水溶液共热2. 1-丁醇发生下列反应(1)与Na反应(2)与Mg反应(3)与CuO反应(4)在银催化下被氧气氧化(5)与浓硫酸混合共热至170℃3. 2 -丁醇发生下列反应(1)与Mg反应(2)与CuO反应(3)在银催化下被氧气氧化(4)与浓硫酸混合共热至140℃4.苯酚发生下列反应(1)与钠反应(2)与氢氧化钠反应(3)与浓溴水反应5.苯酚钠发生下列反应(1)水解(2)CO2(3)醋酸6.乙醛发生下列反应(1)H2(2)O2(3)氢氧化铜悬浊液(4)银氨溶液7.乙酸发生下列反应(1)NaHCO3(2)Cu(OH)2(3)CaO(4)甲醇(5)2-丙醇(6)乙二醇(7)3-甲基-2-戊醇8.下列酯与稀硫酸共热(1)乙酸乙酯(2)甲酸丁酯(3)苯甲酸甲酯9.下列酯与氢氧化钠溶液共热(1)乙酸丙酯(2)甲酸苯甲酯(3)丙烯酸异丙酯10.完全下列转化过程的化学方程式(1)乙烯→乙酸乙酯(2)溴乙烷→乙二醇(3)乙醇→(4)乙醛→乙烷11.写出下面物质分别与足量的钠、氢氧化钠、碳酸氢钠反应的化学方程式。
12.写出下列两物质分别与足量氢氧化钠反应的化学方程式。
(1)(2)12.写出制备下列物质的化学反应方程式:(1)溴苯(2)硝基苯(3)苯磺酸(4)TNT(5)用电石、食盐水等物质置备聚氯乙烯13.葡萄糖跟下列物质反应(1)氢气(2)银氨溶液(3)新制氢氧化铜14.丙氨酸与下列物质反应(1)NaOH(2)HCl(3)跟甘氨酸形成二肽。
有机方程式书写(有答案)

高三化学二轮复习——有机方程式书写【训练一】写出下列反应的化学方程式(要标注反应条件和配平!):1、由甲苯制2-溴甲苯:2、由甲苯制一溴苯基甲烷():3、由甲苯制TNT(2,4,6-三硝基甲苯):4、由苯甲醛制苯甲醇:5、与Br2按1:1发生加成::6、氯乙烷与NaOH水溶液反应:7、一氯乙酸与足量NaOH水溶液混合加热反应:8、与NaOH醇溶液反应:9、的催化氧化反应:10、发生消去反应:11、乙二醇与乙二酸酯化成环反应:12、乙二醇与乙二酸酯化成高分子化合物:13、苯酚溶液滴入浓溴水:14、与溴水反应:15、乙醛发生银镜反应:16、与新制氢氧化铜反应:17、二乙酸乙二酯发生完全水解:18、一氯乙酸乙酯与足量的NaOH溶液加热反应:19、2-甲基-1,3-丁二烯发生加聚反应:20、丙烯酸甲酯发生加聚反应:【训练二】读懂信息,正确迁移:根据题给信息进行信息迁移是有机综合题的热点。
题给信息理解错了,就无法正确运用信息进行迁移。
平时多做信息题可以提高信息的理解和迁移能力!1、已知:则苯甲醛与丙醛发生上述反应的方程式为:__________________________________________________.2、已知:则两分子乙醛在上述条件下反应的化学方程式:_ 。
3、已知:请写出实现由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH的方程式:_________________________________________________________________________________________________________________________________________________ 4、已知:已知环氧氯丙烷可与乙二醇发生如下聚合反应:则:环氧氯丙烷与发生类似反应生成高聚物,该高聚物的结构式是:5、已知:则:+6、已知:则:+7、已知:则8、已知:①②则:⑴⑵+→9、已知:碱存在下,卤代烃与醇反应生成醚(R—O—R‘):R—X + R‘OH R—O—R ’ +HX 则:B的结构简式为:10、已知:通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:下面是9个化合物的转变关系:(1)化合物①的名称是它跟氯气发生反应的条件A是(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:______________ ,名称是(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。
有机化学方程式 练习题
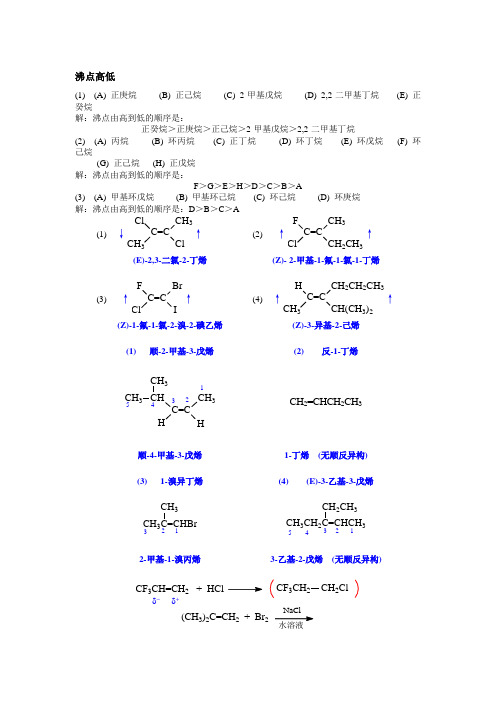
沸点高低(1) (A) 正庚烷 (B) 正己烷 (C) 2-甲基戊烷 (D) 2,2-二甲基丁烷 (E) 正癸烷解:沸点由高到低的顺序是:正癸烷>正庚烷>正己烷>2-甲基戊烷>2,2-二甲基丁烷(2) (A) 丙烷 (B) 环丙烷 (C) 正丁烷 (D) 环丁烷 (E) 环戊烷 (F) 环己烷(G) 正己烷 (H) 正戊烷 解:沸点由高到低的顺序是:F >G >E >H >D >C >B >A(3) (A) 甲基环戊烷 (B) 甲基环己烷 (C) 环己烷 (D) 环庚烷 解:沸点由高到低的顺序是:D >B >C >A(1) ↓C=CCH 3CH 3ClCl↑(2) ↑C=CCH 3ClCH 2CH 3F↑(E)-2,3-二氯-2-丁烯 (Z)- 2-甲基-1-氟-1-氯-1-丁烯(3) ↑C=CBr ClIF↑ (4) ↑C=CCH 2CH 2CH 3CH 3CH(CH 3)2H↑(Z)-1-氟-1-氯-2-溴-2-碘乙烯 (Z)-3-异基-2-己烯 (1) 顺-2-甲基-3-戊烯(2) 反-1-丁烯C=C CH 3HCH 3HCH 312345CH 2=CHCH 2CH 3顺-4-甲基-3-戊烯 1-丁烯 (无顺反异构) (3) 1-溴异丁烯(4) (E)-3-乙基-3-戊烯CH 3C=CHBr CH 3123CH 3CH 23CH 2CH 3123452-甲基-1-溴丙烯 3-乙基-2-戊烯(无顺反异构)CF 3CH=CH 2 + HClCF 3CH 2CH 2Clδ+δ-(CH 3)2C=CH 2 + Br 2(CH 3)2C CH 2Br Br(CH 3)2C CH 2Cl Br (CH 3)2C CH 2OHBr ++CH 3CH 2C CH CH 3CH 2CH 2CHO CH 3CH 2C CH OH H 3222-(硼氢化反应的特点:顺加、反马、不重排)CH 3+ Cl2+ H 2OCH 3OHCl CH 3ClOH +33CH 3CH 3(1) 1/2(BH )22CH 3CH2Cl 500 Co(A)(B)CH 3CH 2ClHBr ROORCH 3CH 2Br ClCH3CH 2C CH + H 2O4H SO CH3CH 2C CH 3O(1) O (2) H 2O , ZnOOBr+ NaCCHC=C C 6H 5C 6H 5HH 33CCO H6H 5HC 6化学方法鉴别化合物:(1) (A)(B)(C)解:(A)(B)(C)4褪色褪色xx褪色(2) (A)(B)(C)CH 3(C 2H 5)2C=CHCH 3CH 3(CH 2)4C CH解:(A)(B)(C)褪色褪色xx银镜(A)CH3,(B) CH3解:(A)中甲基与碳-碳双键有较好的σ-π超共轭,故(A)比较稳定。
高考有机化学方程式训练过关
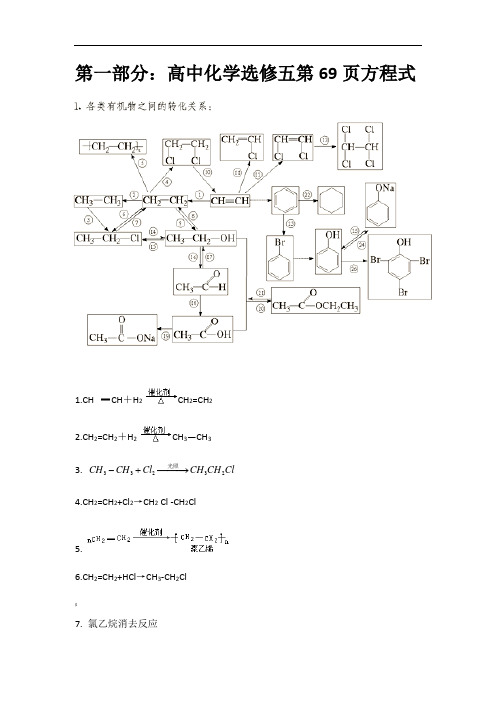
第一部分:高中化学选修五第69页方程式1.CH CH +H 2 CH 2=CH 22.CH 2=CH 2+H 2 CH 3—CH 33. 33232CH CH Cl CH CH Cl -+−−−→光照 4.CH 2=CH 2+Cl 2→CH 2 Cl -CH 2Cl5.6.CH 2=CH 2+HCl →CH 3-CH 2Cl$7. 氯乙烷消去反应CH3CH2 Cl +NaOH CH2=CH2↑+ Na Cl + H2O 8.9.CH2CH2+H—OH CH3CH2OH11. HC CH十HCl CH2=CHCl12.2CH CH Cl CHCl CHCl≡+→=[13.222CHCl CHCl Cl CHCl CHCl=+→-14.氯乙烷水解CH3CH2Cl+ NaOH CH3CH2OH + NaBr15.16. 乙醇催化氧化2CH3CH2OH + O2Cu∆−−→2CH3CHO + 2H2O》17.18.. 乙醛制乙酸2CH3CHO + O2催化剂△2CH3COOH19. CH3COOH+ NaOH→CH3COONa+ H2O20. 乙酸乙酯制取(用饱和碳酸钠溶液收集)CH3COOH + CH3CH2OH CH3COOC2H5+ H2O21.水解反应浓硫酸$H2O△醇△CH3COOC2H5+H2O CH3COOH+C2H5OH22.加成反应(环己烷)23. 取代反应+ Br2−−→−3FeBr+ HBr24. 苯酚与氢氧化钠溶液反应+ NaOH + H2O25. 苯酚钠溶液中通入二氧化碳!+ CO2+ H2O + NaHCO326.苯酚的取代反应(鉴别苯酚)1、将对应反应类型写到方程式后。
取代反应、加成反应、消去反应、聚合反应~氧化反应、还原反应、水解反应、酸碱反应2、观察以上26个转化及方程式,可知有如下常见的反应条件,试举例能发生什么反应。
(1)浓硫酸,加热。
—OH —ONa—ONa—OH(2)稀硫酸,加热(3)NaOH水溶液,加热(4)NaOH醇溶液,加热(5)Cu或Ag催化剂,加热(6)光照(7),(8)Fe或FeX3催化(9)溴水(10)浓溴水(11)银氨溶液Ag(NH3)2OH或 新制氢氧化铜悬浊液(12)酸性高锰酸钾溶液KMnO4(H+)(13)不需要条件即可转化3、官能团的引入或转化总结(1)产物中引入羟基-OH—(2)引入卤素原子-X[(3)引入碳碳双键?第二部分:高中有机化学方程式基础篇一、烃/1.乙烯乙烯的制取:(1)氧化反应高温乙烯的燃烧:H2C=CH2+3O22CO2+2H2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
有机化学方程式
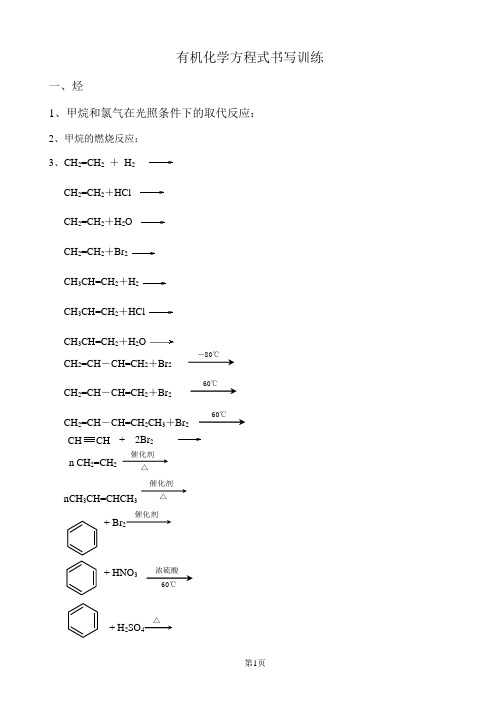
有机化学方程式书写训练一、烃1、甲烷和氯气在光照条件下的取代反应:2、甲烷的燃烧反应:3、CH 2=CH 2 + H 2CH 2=CH 2+HCl CH 2=CH 2+H 2OCH 2=CH 2+Br 2 CH 3CH=CH 2+H 2 CH 3CH=CH 2+HCl CH 3CH=CH 2+H 2OCH 2=CH -CH=CH 2+Br 2CH 2=CH -CH=CH 2+Br 2CH 2=CH -CH=CH 2CH 3+Br 2 + 2Br 2n CH 2=CH 2催化剂 △nCH 3CH=CHCH 3催化剂△+ Br 2催化剂+ HNO 3+ H 2SO 4△CH CH ―80℃60℃ 60℃浓硫酸 60℃+ CH 2=CH 2催化剂+ CH 3CH=CH 2催化剂+ 3HNO 3(写出主要有机产物)(写出主要有机产物)nCH 2=CHCl催化剂 △二、卤代烃1、溴乙烷与氢氧化钠水溶液共热: CH 3CH 2Br +2、溴丙烷与氢氧化钠水溶液共热:CH 3CH 2CH 2Br +NaOH3、2—溴丙烷与氢氧化钠水溶液共热: (CH 3)2CHBr +NaOH4、1,2—二溴乙烷与氢氧化钠水溶液共热: BrCH 2CH 2Br +2NaOH5、溴乙烷与氢氧化钠的乙醇溶液共热: CH 3CH 2Br +NaOH6、1—溴丙烷与氢氧化钠的乙醇溶液共热:CH 3CH 2CH 2Br +NaOH7、2—溴丁烷与氢氧化钠的乙醇溶液共热:加热乙醇 加热乙醇加热加热加热 浓硫酸100℃CH CH 3 CH3 KMNO4 H +2 CH 3KMNO4 H +CH 3CHBrCH 2CH 3+NaOH8、2,3—二溴丁烷与氢氧化钠的乙醇溶液共热: CH 3CHBrCHBrCH 3+2NaOH 二、乙醇与醇类1、乙醇与钠的反应:2CH 3CH 2OH +2Na2、乙二醇与钠的反应:HOCH 2CH 2OH +2Na3、乙醇与钙的反应:2CH 3CH 2OH +Ca4、乙醇与氢溴酸共热:CH 3CH 2OH +HBr5、2—丙醇与氢溴酸共热:(CH 3)2CHOH +HBr6、乙醇分子间脱水:2CH 3CH 2OH7、甲醇分子间脱水:2CH 3OH8、甲醇与乙醇分子间脱水:CH 3CH 2OH +CH 3OH9、乙醇使酸性高锰酸钾溶液褪色: 5CH 3CH 2OH +4KMnO 4+6H 2SO 45CH 3COOH +2K 2SO 4+4MnSO 4+11H 2O10、 乙醇的催化氧化:2CH 3CH 2OH +O 211、甲醇的催化氧化:2CH 3OH +O 212、乙二醇的催化氧化:HOCH 2CH 2OH +O 2 13、乙醇与浓硫酸共热170℃:CH 3CH 2OH14、丙醇与浓硫酸共热:CH 3CH 2CH 2OH15、 乙醇与乙酸和浓硫酸共热:CH 3COOH +CH 3CH 2OH16、甲醇与乙酸和浓硫酸共热:CH 3COOH +CH 3OH加热浓硫酸 加热浓硫酸170℃浓硫酸 170℃浓硫酸 加热 催化剂加热催化剂 加热催化剂140℃浓硫酸140℃浓硫酸 140℃浓硫酸加热加热加热乙醇加热乙醇17、甲酸、乙醇与浓硫酸共热:HCOOH +CH 3CH 2OH18、乙酸、2—丙醇与浓硫酸共热: CH 3COOH +(CH 3)2CHOH19 2021、乙二酸与乙二醇和浓硫酸共热: 22、3—羟基丙酸与浓硫酸共热:HOCH 2CH 2COOH+H 2O23324、1,4—丁二酸与乙二醇和浓硫酸共热:三、苯酚与酚类1、苯酚燃烧:C 6H 6O +7O 26CO 2+3H 2O2、苯酚与氢氧化钠溶液反应:C 6H 5OH +NaOH3、苯酚钠溶液中通入二氧化碳气体: C 6H 5O -+CO 2+H 2O ===C 6H 5OH +HCO 3-4、苯酚钠溶液与氯化铝溶液混合:3C 6H 5O -+Al 3++3H 2O ===3C 6H 5OH +Al(OH)3↓5、苯酚溶液中加入浓溴水: OH +3Br 2 7、苯酚在一定条件下与氢气反应:点燃 浓硫酸 加热浓硫酸 加热浓硫酸COOH COOH +2CH 3CH 2OH浓H 2SO 4加热 +2H 2O CH 2OH CH 2OH +2CH 3COOH 浓H 2SO 4加热+2H 2O CH 2OH CH 2OH COOH COOH 浓H 2SO 4加热+2H 2O nHOCH 2CH 2COOH H [ OCH 2CH 2CO ]n OH +(n -1)H 2O浓H 2SO 4加热 nHOOCCH 2CH 2COOH +nHOCH 2CH 2OH HO [OCCH 2CH 2COOH +nHOCH 2CH 2O] n H +(2n -1)H 2O 浓H 2SO 4加热—OH +3H 2 —OH8、酚醛树脂的制备:9、苯酚与乙醛的缩聚:四、乙醛与醛类1、乙醛的燃烧:2C 2H 4O +5O 24CO 2+4H 2O3、乙醛与溴水反应:CH 3CHO +Br 2+H 2O CH 3COOH +2HBr4、乙醛与银氨溶液反应: CH 3CHO +2[Ag(NH 3)2]OH5、甲醛与少量的银氨溶液反应: HCHO +2[Ag(NH 3)2]OH6、甲醛与过量的银氨溶液反应: HCHO +4[Ag(NH 3)2]OH7、乙二醛与银氨溶液反应: OHCCHO +2[Ag(NH 3)2]OHH 4NOOC —COONH 4+2H 2O +4Ag +6NH 3↑8、乙醛与新制的氢氧化铜反应:CH 3CHO +2Cu(OH)2 CH 3COOH +Cu 2O↓+2H 2O9、甲醛与少量的新制的氢氧化铜反应:HCHO +2Cu(OH)2HCOOH +Cu 2O↓+2H 2O10、甲醛与过量的新制的氢氧化铜反应:HCHO +4Cu(OH)2 CO 2↑+2Cu 2O↓+5H 2O11、乙醛与新制的氢氧化铜反应:CH 3CH 2CHO +2Cu(OH)2CH 3CH 2COOH +Cu 2O↓+2H 2O12、乙醛的催化氧化: 2CH 3CHO +O 2催化剂加热加热加热加热 加热加热 加热加热点燃 加热催化剂 OH+nHCHO 催化剂nOHCH 2+nH 2OCH 3OH+nCH 3CHO 催化剂n OHCH+nH 2O13、乙二醛的催化氧化:OHCCHO +O 214、乙醛与氢气反应:CH 3CHO +H 215、乙二醛与氢气反应:OHC —CHO +2H 2HOCH 2CH 2OH五、丙酮与酮类1、丙酮燃烧:C 3H 6O +4O 23CO 2+3H 2O2、丙酮与氢气反应:CH 3COCH 3+H 2六、乙酸与羧酸类1、乙酸与钠反应:2CH 3COOH +2Na3、乙酸与氢氧化钠反应:CH 3COOH +NaOH4、乙酸与碳酸钙反应:CH 3COOH +CaCO 35、乙酸与碳酸氢钠反应:CH 3COOH +NaHCO 36、乙酸与乙醇和浓硫酸共热: CH 3COOH +CH 3CH 2OH7、乙酸和甲醇与浓硫酸共热: CH 3COOH +CH 3OH8、乙酸与2—丙醇和浓硫酸共热: CH 3COOH +(CH 3)2CHOH9、对苯二甲酸与乙二醇的缩聚:10、1,6—己二酸与1,6—己二胺的缩聚:七、乙酸乙酯与酯类 加热浓硫酸加热浓硫酸 加热浓硫酸点燃加热催化剂 加热催化剂加热催化剂催化剂 催化剂 nHOOC — —COOH + nHOCH 2CH 2OH +(2n -1)H 2O HO —OC — —CO O CH 2CH 2O — [ ]n H nHOOC(CH 2)6COOH +nH 2N(CH 2)6NH 2 催化剂—OC(CH 2)6CONH(CH 2)6NH — +(2n -1)H 2O HO [ ]n H1、乙酸乙酯的燃烧:C 4H 8O 2+5O 24CO 2+4H 2O4、乙酸乙酯在酸性条件下的水解反应: CH 3COOCH 2CH 3+H 2O5、甲酸甲酯在酸性条件下的水解反应: HCOOCH 2CH 3+H 2O6、乙酸甲酯在酸性条件下的水解反应: CH 3COOCH 3+H 2O7、丙酸乙酯在酸性条件下的水解反应: CH 3CH 2COOCH 2CH 3+H 2O8、乙酸乙酯与氢氧化钠溶液共热: CH 3COOCH 2CH 3+NaOH9、甲酸乙酯与氢氧化钠溶液共热: HCOOCH 2CH 3+NaOH10、乙酸甲酯与氢氧化钠溶液共热:CH 3COOCH 3+NaOH11、丙酸乙酯与氢氧化钠溶液共热:CH 3CH 2COOCH 2CH 3+NaOH12、浓硫酸 △13、+ 3NaOH加热加热加热加热 加热稀硫酸加热稀硫酸 加热稀硫酸 加热稀硫酸点燃 2 CH 2 COOH CH 2CH 2OH 2 Br 水 △。
高二有机化学方程式练习题

高二有机化学方程式练习题有机化学是化学学科中的一个重要分支,研究有机化合物的结构、性质和变化规律等。
其中,方程式是有机化学中非常重要的一部分,通过方程式可以描述化学反应的发生过程。
下面将提供一些高二有机化学方程式练习题,帮助同学们加深对有机化学方程式的理解和掌握。
1. 丙醇脱水生成丙烯的方程式是什么?答案:丙醇(C3H8O)在适当的条件下脱水反应生成丙烯(C3H6)的方程式如下:C3H8O → C3H6 + H2O2. 乙醚和二氯甲烷反应生成什么产物?写出反应方程式。
答案:乙醚(C4H10O)和二氯甲烷(CH2Cl2)反应生成甲醇(CH3OH)和氯乙烷(C2H5Cl)的方程式如下:C4H10O + CH2Cl2 → CH3OH + C2H5Cl3. 甲醛和甲胺反应生成什么产物?写出反应方程式。
答案:甲醛(CH2O)和甲胺(CH3NH2)反应生成甲肼(CH6N2)和甲酸(HCOOH)的方程式如下:2CH2O + 2CH3NH2 → CH6N2 + HCOOH4. 己二酸和乙醇反应生成什么产物?写出反应方程式。
答案:己二酸(C6H10O4)和乙醇(C2H5OH)反应生成乙酸己酯(C10H18O4)和水(H2O)的方程式如下:C6H10O4 + 2C2H5OH → C10H18O4 + 2H2O5. 碳酸氢钠和盐酸反应生成什么产物?写出反应方程式。
答案:碳酸氢钠(NaHCO3)和盐酸(HCl)反应生成二氧化碳(CO2)、水(H2O)和氯化钠(NaCl)的方程式如下:NaHCO3 + HCl → CO2 + H2O + NaCl6. 甲醇和乙酸反应生成什么产物?写出反应方程式。
答案:甲醇(CH3OH)和乙酸(CH3COOH)反应生成甲酸(HCOOH)和乙酸甲酯(CH3COOCH3)的方程式如下:CH3OH + CH3COOH → HCOOH + CH3COOCH3以上是一些高二有机化学方程式练习题,通过解答这些题目,可以加深对有机化学方程式的理解和记忆。
高考-有机陌生方程式书写

高二化学方程式训练七班级:姓名:1.+ →,反应类型是:。
2.化合物与足量H 2在一定条件下反应方程式上一反应的产物与NaOH溶液反应的方程式:。
3. 化合物CH2ClCH2COOH与NaOH醇溶液反应的化学方程式为。
5.龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是:。
(不用写反应条件)6.和过量NaOH溶液共热时反应的化学方程式为。
7.CHCH2CH2CH2OH(足量)+3反应类型是:。
8.BrCH 2CH 2Br +2NaOH反应类型是: 。
9. +2NaOH反应类型是: 。
10. 与Cl 2在光照下发生反应,其有机产物的分子式为C 7H 6OCl 2,化学方程式为_______________________________________,反应类型为___________。
11.化合物 在银氨溶液中发生反应化学方程式: ;反应类型是: 。
13.(1)卤代烃CH 3CHBrCH 3发生消去反应可以生成化合物Ⅲ(分子式为C 3H 6),相应的化学方程 为 (注明条件)。
(2)已知反应①:醇溶液、△一定条件下,与也可以发生类似反应①的反应,则其方程式为:。
反应类型是:。
14.向溶液中加入少量浓溴水,发生反应的化学方程式。
反应类型是:。
与足量NaOH溶液共热时,发生反应的化学方程式。
15.苯为原料生成有机物的化学方程式(注明反应条件)是。
由有机物III制备的反应方程式是。
反应类型是:。
有机陌生方程式书写练习1.+→加成反应2.+H2(3分)3.5.分)6.7. 2CH 3CH 2CH 2CH 2OH+COOH COOH--22232223C O CH CH CH CH C O CH CH CH CH ------+2H 2O 酯化反应(取代反应)8.BrCH 2CH 2Br +2NaOH HOCH 2CH 2OH + 2NaBr 水解反应(或取代反应)HO COCOO CH 2CH 2OH n COOH HOOC++HOCH 2CH 2H 2On n 2n-1()缩聚反应9.+2NaOH +2NaBr+2H2O 消去反应 10.11.ONa CH CHCHOONaCH CHCOONH 4Ag(NH 3)2OH2++H 2O +2Ag 3NH 3+银镜反应(或氧化反应)ONaCH CHCOONa OHCH 2CHCOOH +3NaCl H2O 3++或(3 分)13.CH 3CHBrCH 3+2NaOH CH 2=CHCH 3↑++NaBr+H 2O2+ HCl 取代反应醇溶液、△醇溶液、△14(因题目条件为“加入少量浓溴水”,该反应写任一种苯环上羟基邻、对位的一取代产物也都得分,产物写“↓”不扣分,没配平扣1分)15.(3分;条件不写扣1分)+ H 2O 消去反应。
高中化学-有机反应方程式的书写要求

有机反应方程式的书写要求1.反应箭头和配平:书写有机反应方程式时应注意,反应物和产物之间用“―→”连接,有机物用结构简式表示,并遵循元素守恒进行配平。
2.反应条件:有机物反应条件不同,所得产物不同。
题组三有机转化关系中反应方程式的书写5.一种常见聚酯类高分子材料的合成流程如下:请写出各步反应的化学方程式①________________________________________________________________________;②________________________________________________________________________;③________________________________________________________________________;④________________________________________________________________________;⑤________________________________________________________________________;⑥________________________________________________________________________;⑦________________________________________________________________________。
答案①CH2==CH2+Br2―→②光③――→④⑤⑥+O2――→催化剂⑦+n HO—CH2—CH2—OH浓H2SO4△+(2n-1)H2O1.同分异构体的种类(1)碳链异构(2)官能团位置异构(3)类别异构(官能团异构)有机物分子通式与其可能的类别如下表所示:组成通式可能的类别典型实例C n H2n烯烃、环烷烃CH2==CHCH3与C n H2n-2炔烃、二烯烃CH≡C—CH2CH3与CH2==CHCH==CH2C n H2n+2O饱和一元醇、醚C2H5OH与CH3OCH3C n H2n O醛、酮、烯醇、环醚、环醇CH3CH2CHO、CH3COCH3、CH2==CHCH2OH、与C n H2n O2羧酸、酯、羟基醛、羟基酮CH3CH2COOH、HCOOCH2CH3、HO—CH2—CH2—CHO与C n H2n-6O酚、芳香醇、芳香醚、与C n H2n+1NO2硝基烷、氨基酸CH3CH2—NO2与H2NCH2—COOHC n(H2O)m单糖或二糖葡萄糖与果糖(C6H12O6)、蔗糖与麦芽糖(C12H22O11)2.同分异构体的书写规律书写时,要尽量把主链写直,不要写得歪扭七八的,以免干扰自己的视觉;思维一定要有序,可按下列顺序考虑:(1)主链由长到短,支链由整到散,位置由心到边,排列邻、间、对。
有机方程式练习

有机化学方程式练习一、脂肪烃1、烷烃燃烧通式2、烯烃燃烧通式3、炔烃燃烧通式4、烃燃烧通式5、有机物CxHyOz燃烧通式6、甲烷和氯气取代(4个)7、乙烯和氢气加成8、乙烯和溴的四氯化碳溶液加成10、丙烯和氯化氢加成11、乙烯和水加成11、异戊二烯(2-甲基-1,3-丁二烯)和溴的1,4-加成12、1,3-丁二烯和溴的1,2-加成13、异戊二烯和足量溴的加成14、1-丁炔和等物质的量氢气加成15、2-丁炔和足量的氢气加成16、乙炔和等物质的量的氯化氢加成17、乙烯加聚18、丙烯加聚19、苯乙烯加聚20、异戊二烯加聚21、氯乙烯加聚22、等物质的量的乙烯和氯乙烯加聚23、等物质的量的苯乙烯和1,3-丁二烯加聚24、实验室制乙烯25、实验室制乙炔二、芳香烃1、苯的溴代2、苯的硝化(50-60℃)3、苯与氢气加成4、甲苯制TNT 三、卤代烃1、1-溴丙烷的水解反应2、1-溴丙烷的消去反应3、2-溴丁烷的消去反应(2个方程式)4、由乙醇制氯乙烷四、醇1、乙二醇与钠反应2、乙醇分子间脱水3、甲醇与HBr反应4、苯甲醇与乙二酸酯化生成二酯5、2-丙醇和苯甲酸酯化6、乙醇在浓硫酸作用下分子内脱水7、乙二醇催化氧化8、丙三醇与浓硝酸酯化9、2-丙醇催化氧化10、发生消去反应五、酚1、苯酚的电离2、苯酚与钠3、苯酚与氢氧化钠溶液4、苯酚钠溶液与二氧化碳5、苯酚钠溶液与盐酸6、苯酚与碳酸钠溶液7、苯酚与浓溴水8、苯酚与甲醛反应制酚醛树脂9、苯酚与氢气六、醛和酮1、乙醛的催化氧化2、丙醛与新制的氢氧化铜悬浊液3、丙醛的银镜反应4、甲醛与氢气5、甲醛与新制的氢氧化铜悬浊液6、甲醛的银镜反应7、苯甲醛与足量氢气—CH2CH2OH8、苯甲醛的催化氧化9、苯甲醛与新制氢氧化铜悬浊液10、苯甲醛与银氨溶液11、丙酮与氢气七、羧酸1.乙酸溶液与氢氧化钠溶液混合2.甲酸溶液与碳酸钠溶液混合3.乙酸溶液与碳酸氢钠溶液混合4.甲酸与乙醇的酯化反应5.乙酸与新制氢氧化铜悬浊液常温下反应6.甲酸与新制氢氧化铜悬浊液常温下反应7、甲酸与新制的氢氧化铜悬浊液加热反应8.乙二酸溶液与足量碳酸钠溶液反应9.乙二酸与乙醇酯化生成一元酯9、乙二酸与乙醇酯化生成二酯10、乳酸生成六元环状交酯11、乙二酸与乙二醇生成一元酯12、乙二酸与乙二醇生成环酯13、乳酸缩聚15、乙二酸与乙二醇生成聚酯八、酯1.乙酸乙酯的酸性水解2.苯甲酸甲酯的碱性水解3.硬脂酸甘油酯的酸性水解4.软脂酸甘油酯的碱性水解5、油酸甘油酯的氢化九、糖类1、葡萄糖的还原反应2、葡萄糖的银镜反应3、葡萄糖与新制氢氧化铜悬浊液共热4、葡萄糖的在酒化酶作用下分解5、蔗糖的水解6、麦芽糖的水解7、淀粉的水解9、纤维素的水解十、氨基酸与蛋白质1、甘氨酸生成二肽2、等物质的量的甘氨酸与丙氨酸生成多肽3、聚丙氨酸水解。
高二有机化学方程式书写

高二年化学有机化学方程式练习完成下列反应的化学方程式(有机物写结构简式)1、甲烷的氯代反应(只写二氯代反应) 取代反应CH 4Cl 2CH 2Cl 22+光照+2HCl2、乙烯在硫酸作用下与水反应 加成反应 CH 2=CH 2H-OHCH 3CH 2OH+硫酸3、乙烯与溴水的反应 加成反应CH=CH 2Br 2CH 2=CHBr+4、乙烯在一定条件下与溴化氢的反应 加成反应CH=CH 2CH 3CH 2Br+HBr6、乙炔在催化剂存在下与氯化氢反应生成氯乙烯 加成反应CH 2=CHClCH+CHHCl7、由丙烯制聚丙烯(7、8、9不要求写反应条件) 加聚反应nCH 2=CHCH3CH-----CH 2CH 3n 催化剂8、由氯乙烯制聚氯乙烯 加聚反应nCH 2=CHCH3CH---CH 2Cln 催化剂9、由苯乙烯制聚苯乙烯 加聚反应nCH 2=CHCH3CH--CH 2n 催化剂10、苯的溴代取代反应(溴代)Br 2FeBr++HBr11、苯的氯代反应 取代反应(氯代)Cl 2FeCl++HCl12、苯的硝化 取代反应(硝化)HNO 3NO 2+(浓)浓硫酸水浴加热+H2O13、甲苯与较稀硝酸、较低温度下的硝化反应 取代反应(硝化)HNO 3NO 2CH 3CH 3+(浓)浓硫酸加热+H2OHNO 3CH 3CH 3NO 2+(浓)浓硫酸加热+H2O14、甲苯在较高温度、浓硝酸下的硝化反应 取代反应(硝化)HNO 3NO 2O 2N NO 2CH 3CH 3+(浓)浓硫酸加热+H2O3315、2-溴丙烷在氢氧化钠水溶液中的反应 取代反应(水解) CH 3CHBrCH 3NaOHCH 3CHOHCH 3NaBr+水/加热+16、2-溴丙烷在氢氧化钠醇溶液中的反应 消去反应 CH 3CHBrCH 3NaOHCH 2=CHCH 3NaBr醇/加热++H2O+17、1-丙醇的催化氧化 氧化反应CH 3CH 2CH 2OHO 2CH 3CHO2+Cu/加热2+2H2O18、2-丙醇的催化氧化 氧化反应 O 2CH 3COCH 3CH 3CHOHCH 32+Cu/加热2+2H2O19、1-丙醇氢溴酸的溴代反应 取代反应(溴代)CH 3CH 2CH 2OH CH 3CH 2CH 2Br+HBr加热+H2O20、1-丙醇的消去反应 消去反应CH 2=CHCH 3CH 3CH 2CH 2OH浓硫酸170度+H2O21、乙二醇与足量的金属钠的反应 置换反应HOCH 2CH 2OHNaOCH 2CH 2ONaH2+2Na+22、乙二醇的催化氧化 氧化反应HOCH 2CH 2OHO 2CHO CHO+铜 /加热+2H2O23、苯酚与氢氧化钠溶液的反应 中和反应OHNaOHONa++H2O24、苯酚与碳酸钠溶液的反应 复分解反应OHNa 2CO 3ONaNaHCO 3++25、在苯酚钠溶液中通入二氧化碳气体 复分解反应OHONaNaHCO 3CO 2++H2O+26、苯酚的溴代 取代反应(溴代)OHBr 2BrOHBrBr+33HBr+26、由苯酚和甲醛制酚醛树脂 缩聚反应OHHCHOCH 2--nOH+nn +nH2O27、乙醛的氢化 加成反应(还原反应)CH 3CHOH2CH 3CH 2OH+Ni/加热P ,T28、乙醛的催化氧化 氧化反应CH 3CHOO 2CH 3COOH2+催化剂229、乙醛的银镜反应 氧化反应CH 3CHOCH 3COONH 4NH 3+2水浴加热+2Ag+3+H2OAg (NH3)2OH30、乙醛与新制的氢氧化铜悬浊液的反应 氧化反应CH 3CHOCH 3COONaNaOHCu 2O+2加热Cu (OH )2+++3H2OCH 3CHOCH 3COONaCu 2O+2加热Cu (OH )2++2H2O31、乙酸与碳酸钠溶液的反应 复分解反应CH 3COOHNa 2CO 3CH 3COONa+22+H2O32、乙酸与乙醇的酯化反应 取代反应(酯化)CH 3COOHCH 3CH 2OHCH 3COOC 2H 5浓硫酸/加热++H2O33、乙二醇与乙二酸形成六元环状酯 取代反应(酯化)HOCH2CH 2OHHOOCCOOHOCH 2CCCH 2OO=O=+2H2O +催化剂34、乙二醇与乙二酸形成高聚酯 取代反应(缩聚)HOCH 2CH 2OHHOOCCOOH---OCCOOCH 2CH 2O---nOH2n +n 催化剂+2n35、2-羟基丙酸形成内酯(三元环状酯) 取代反应(缩聚)CH 3CHCOOHOH CH 3CHC=OO催化剂+H2O36、2-羟基丙酸形成六元环状酯 取代反应(酯化)CH 3CHCOOHOHO=O OO CH 3CH 32催化剂+2 H2O37、2-羟基丙酸形成高聚酯 取代反应(缩聚)CH 3CHCOOHOH---OCHC---nO催化剂+H2On n38、乙二酸二乙酯的碱性水解 取代反应(水解)COOC 2H 5COOC 2H 5NaOHCOONaCOONaCH 3CH 2OH+2水加热+239、醋酸苯酯的碱性水解、酸性水解(与38比较) 取代反应(水解)OOCCH 3NaOHONaCH 3COONa +2H2O加热++H2O40、淀粉(或纤维素)的水解 取代反应(水解)C 6H 10O 5nH 2SO 4C 6H 12O 6+n H2O加热n41、蔗糖的水解 取代反应(水解)C 12H 22O 11C 6H 12O 6C 6H 12O 6+H2O酸加热+蔗糖葡萄糖果糖42、葡萄糖的氢化 加成反应(还原)CH 3OH(CHOH)4CHO H2NiCH 3OH(CH 2OH)4CH 3OH+P,T43、葡萄糖的银镜反应 氧化反应CH 3OH(CHOH)4CHO Ag(NH 3)2OHCH 3OH(CH 2OH)4COONH 4+2水浴、加热Ag+2+H2O44、葡萄糖的无氧酵解CH 3OH(CHOH)4CHOCH 3CH 2OHCO 2酵母菌2+245、硝化纤维素的制备 取代反应(酯化)C 6H 7O 2OHOH nOHHNO 3C 6H 7O 2ONO 2ONO 2nONO 2+3n (浓)浓硫酸、加热+3nH2O46、硬脂酸甘油酯的皂化反应 取代反应(水解)CH 2OOCC 17H 35CHOOCC 17H 35CH 2COOCC 17H 35NaOHC 17H 35COONa CH 2OHCHOHCH 2OH+3水、加热3+47、硬脂酸甘油酯的酸性水解 取代反应(水解)CH 2OOCC 17H 35CHOOCC 17H 35CH 2COOCC 17H 35CH 2OHCHOH CH 2OHC 17H 35COOH+33+H20稀 硫酸、加热48、H 2N- -COOH 制聚酰胺 缩聚反应OH 2NCOOH n HNnCn +nH2O49、丙氨酸与盐酸反应CH 3CHCOOHNH 2CH 3CHCOOHNH 3Cl+HCl50、丙氨酸与氢氧化钠反应CH 3CHCOOHNH 2CH 3CHCOOHNaOHNH 2++H2O51、由CH 2=C (CH 3)-CH=CH 2 制聚异戊二烯 加聚反应---CH 2-CH=C-CH 2--CH 2=CH-C=CH 2CH 3nCH 3n。
《有机化学反应方程式》书写练习

寒假作业《有机化学反应方程式》书写练习一、取代反应1 .卤代反应(1CH4与Cl2在光照下反应:(2苯、液溴在铁屑催化下反应:(3苯酚溶液中加入过量浓溴水:2 .硝化反应(1由苯制硝基苯:(2由甲苯制TNT:3 .磺化反应由苯和浓硫酸共热制苯磺酸:4 .醇与氢卤酸共热下反应例如:乙醇与氢溴酸反应:5 .醇分子间脱水成醚例如:由乙醇制乙醚:6 .卤代烃的水解例如:溴乙烷与NaOH溶液共热:7 .酯的水解(1乙酸乙酯与稀H2SO4共热:(2乙酸乙酯与NaOH溶液共热:。
8 .酯化反应(1乙酸与乙醇在浓硫酸下共热制乙酸乙酯:。
(2苯甲酸、甲醇、浓硫酸三者混合后共热:。
二、加成反应1.烯烃的加成(1C2H4加成H2:。
(2C2H4加H2O:。
(3C2H4通入溴水中:现象为:。
2.炔烃的加成(1C2H2与足量H2加成:。
(2C2H2通入溴水中:。
(3C2H2水化法制乙醛:。
(4C2H2与HCl制氯乙烯:H23.例如:苯加成H2:。
4 .乙醛加成氢气:。
5 .丙酮(CH3COCH3加成氢气:。
6 .油脂的硬化(或氢化:。
三、消去反应1 .部分卤代烃的消去反应结构要求为:;条件为:。
例如:溴乙烷、乙醇、NaOH三者混合共热:。
2 .部分醇的消去反应结构要求为:;条件为:。
例如:(1由乙醇制乙烯:。
(2符合分子组成为C7H15OH、不能发生消去反应的物质有种,其结构简式为:。
四、氧化反应1 .有机物的燃烧反应(1烃(C x H y完全燃烧的通式为:。
①天然气的完全燃烧:②乙烯完全燃烧:;_现_象_为_:③乙炔完全燃烧:;__现_象_为:_④苯完全燃烧:;现象为:。
(2含氧衍生物(c x H y o k完全燃烧的通式为:。
例如:酒精作燃料完全燃烧:。
葡萄糖的生理氧化:2.得氧或失氢方式的氧化反应(1乙烯氧化法制乙醛:。
(2由乙醇制乙醛:。
(3乙醛发生银镜反应:。
(4乙醛与新制氢氧化铜悬浊液共热:。
(5乙醛与氧气的催化氧化:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《有机化学基础知识》练习
反应方程式的书写
一、取代反应
1.卤代反应
(1) 苯、液溴在铁屑催化下反应:_____________________________________________。
(2) 苯酚溶液中加入过量浓溴水:_____________________________________________。
2.硝化反应
(1)由苯制硝基苯:______________________________________________________。
(2)由甲苯制TNT:______________________________________________________。
3.醇与氢卤酸共热下反应
例如:乙醇与氢溴酸反应:_________________________________________________。
4.醇分子间脱水成醚
例如:由乙醇制乙醚:_____________________________________________________。
5.卤代烃的水解
例如:溴乙烷的水解:___________________________________________。
6.酯的水解
(1)乙酸乙酯与稀H2SO4共热:______________________________________________。
(2)乙酸乙酯与NaOH溶液共热:_____________________________________________。
二、加成反应
1.烯烃的加成
(1) C2H4加H2O:_______________________________________________________。
2.炔烃的加成
(1)C2H2与足量H2加成:____________________________________________________。
(2)C2H2与H21:1加成:_______________________________________________________。
3.芳香烃的加H2
例如:苯加成H2:_________________________________________________。
4.乙醛加成氢气:_________________________________________________。
三、消去反应
1.部分卤代烃的消去反应
结构要求为:__________________________;条件为:_____________________。
例如:溴乙烷的消去反应:____________________________________。
2.部分醇的消去反应
结构要求为:___________________________;条件为:__________________________。
例如:(1) 的消去反应:_____________________________________________。
(2)符合分子组成为C7H15OH、不能发生消去反应的物质有________种,其中主链为4个”C”的结构简式为:_____________________________________。
四、氧化反应
1.有机物的燃烧反应
2.得氧或失氢方式的氧化反应
(1)的催化氧化:_______________________________________________。
(2) )乙醛发生银镜反应:_________________________________________________。
(3) 乙醛与新制氢氧化铜悬浊液共热:________________________________________。
(4) 乙醛与氧气的催化氧化:________________________________________________。
(5) 葡萄糖发生银镜反应:_________________________________________________。
(8)由乙二醇制乙二醛:__________________________________________________。
(9)由乙二醛制乙二酸:_________________________________________________。
五、还原反应
1.加成H2
注意:能加氢的几类结构。
六、水解反应
1.卤代烃的水解
例如:1,2 ―二溴乙烷的水解反应:_____________________________________。
2.酯的水解反应
(1)阿斯匹林与NaOH溶液共热:_____________________________。
(2)化合物与NaOH溶液共热:
___________________________________________________________________________。
七、酯化反应
1.由乙酸与乙二醇制二乙酸乙二酯:_____________________________________________。
2.由甘油与硝酸制三硝酸甘油酯:_______________________________________________。
3.乙二醇与乙二酸发生完全酯化反应制乙二酸乙二酯:_____________________________。
4.由乳酸(CH3CHOHCOOH)制C6H10O5的酯化反应:________________________________。
5.由乳酸(CH3CHOHCOOH)制环酯(C6H8O4)的酯化反应:_____________________________。
八、加聚反应
1.由乙烯制聚乙烯:__________________________________________________________。
2.由乙炔制聚氯乙烯:______________________________________________________。
________________________________________________________________。
3.甲基丙烯酸甲酯的加聚反应:________________________________________________。
九、其它有机反应
1.由电石与饱和食盐水作用制乙炔:_____________________________________________。
2.钠与乙醇的置换反应:______________________________________________________。
3.苯酚与NaOH溶液反应的化学方程式为:_____________________________________;离子方程式为:______________________________________________________。
4.苯酚钠溶液中通入少量CO2的化学方程式为:___________________________________;
离子方程式为:___________________________________________________。
5.银氨溶液的配制:____________________________________________________。
___________________________________________________。
6.乙酸与碳酸氢钠溶液反应的离子方程式为:____________________________________;少量乙酸滴入碳酸钠溶液中的离子方程式为:_______________________________________。
7. 苯酚与碳酸氢钠溶液反应的化学方程式为____________________________________
化学用语部分
(1).名称电子式结构式结构简式空间构型甲烷,;,
乙烯,;,
乙炔,;,;(2).名称电子式结构简式名称电子式结构简式
羟基,;甲基,;(3).写出下列基团的中文名称:
H2N—___________O2N—_____________OHC—_____________HOOC—_____
有机分离与除杂
有机合成1.由溴乙烷制乙酸乙酯
2.由溴乙烷制乙二酸乙二酯。
