燃烧图(2X400)
燃烧基础知识-ppt课件

综化上的所物述质,不一物定质都燃是烧能是够氧燃化烧反的应物,质而氧化反应不一定是燃烧,能被氧8
可燃物质的多数氧化反应不是直接进行的,而是经过一系列复杂的中 间反应阶段;不是氧化整个分子,而是氧化连锁反应中间产物——游 离基或原子。
可见,燃烧是一种极其复杂的化学反应,游离基的连锁反应是燃烧反 应的实质,光和热使燃烧过程中发生的物理现象。
如:汽油、柴油、煤油、酒精 。
气体可燃物
14
河南消防职业培训学校(漯河站) 2019/9/16
凡是在空气中能发生燃烧的气体,都称为可燃气 体。可燃气体在空气中需要与空气的混合比在一 定浓度范围内(即燃烧最低浓度),并还要一定 的温度(即着火温度)才能发生燃烧。
如:H2 CL2 CH4、 氢气 氯气 甲烷此外, 有些物质在通常情况下不燃烧。但在一定条件下 又可以燃烧。如:赤热的铁在纯氧中能发生剧烈 燃烧;赤热的铜能在纯氯气中发生剧烈燃烧;铁、 铝本身不燃,但把铁、铝粉碎成粉末,不但能燃 烧,而且在一定条件下还能发生爆炸。
3、一定的点火能量
20
河南消防职业培训学校(漯河站) 2019/9/16
可燃物发生燃烧,都有本身固有的最小点火能要求,达到一定的 强度才能引起可燃物着火。否则燃烧就不会发生。所需火源的强度, 取决于可燃物质的最小点火能(引燃温度),不同可燃物质燃烧所需 的引燃温度各不相同。汽油0.2mJ,乙醚0.19mJ。
河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站河南消防职业培训学校漯河站第二章燃烧基础知识主要内容
工程燃烧学_4

第四章预混合气体火焰第四章预混合气体火焰从可燃混合气的制备及燃烧的方式将燃烧现象分成预混合燃烧及扩散燃烧。
预混合燃烧是燃料与氧化剂事先混合成可燃混合气以后才进行燃烧的。
扩散燃烧就是燃料与氧化剂边混合边燃烧。
图2-1 燃烧现象(a)喷灯1观察Bensun火焰的圈顶效应、壁面淬熄效应及火焰外凸效应;燃料浓度对火焰颜色的影响;气流速度对火焰形状的影响等各种火焰现象。
预混合火焰浓度测量2了解本生灯火焰内外锥分离的原理和方法。
测定预混合火焰的稳定浓度界限(回火曲线的绘制) Smithell法火焰分离第四章预混合气体火焰4熟悉和掌握火焰传播速度u 0、火焰行进速度u p 和来流(供气)速度u s 相互之间的关系。
气体燃料的射流燃烧层流火焰传播速度的测量•巩固火焰传播速度的概念,掌握本生灯法测量火焰传播速度的原理和方法。
测定液化石油气的层流火焰传播速度。
•掌握不同的气/燃比对火焰传播速度的影响,测定出不同燃料百分数下火焰传播速度的变化曲线。
第四章预混合气体火焰4.1 概说在低温时由于化学反应速度慢,与扩散及传热相比,它在燃烧过程中所需的时间长,因此,化学反应动力学(即反应速度)对火焰的传播起控制作用(即对燃烧过程其主要作用)。
在高温时则化学反应速度极快而扩散速度与传热却相对是速度慢的环节。
因而,扩散与传热对火焰的传播起着控制作用。
在预混合火焰的传播过程中化学反应速度、扩散、流动、传热等都起着各自的重要的作用。
第四章预混合气体火焰预混合气体的火焰锋面将燃料混合气体与燃料产物分开。
由于燃烧过程是复杂的化学反应过程,通常它是由许多个中间反应过程所组成,因而,在火焰锋面处有许多复杂的、不稳定的、极为活泼的中间产物。
火焰锋面及其前后成分、温度、密度、速度、压力等变量随火焰锋面厚度方向的变化情况,称为火焰的结构。
4.1 概说第四章预混合气体火焰4.2 爆燃与缓燃在燃烧现象火焰的传播速度与其载气流的流速有关。
当预混合气的流速大到有激波出现并同时伴随着燃烧时,在火焰锋面两侧有很大的压力突变,称之为爆燃(爆震波)。
火灾动力学——4c_理论可燃性图

图
0.2
CH4+He CH4+N2 CH4+CO2 Cst theory (He, LFL)
theory (He, UFL)
theory (N2, UFL) theory (N2, LFL) theory (CO2, LFL) theory (CO2, UFL)
00
2
4
6
8 10 12 14
Inertant/fuel Ratio
Non-ignitablLeFMCFliC lniene
2021/4/18
例题:室内惰化
在一间200 m3 的室内发 生泄漏,甲烷的体积浓
度达到30% ,需要多少
氮气来吹扫这间屋子, 让室内的氛围完全不可 点?
VN2
V0
ln
xF xF ,0
200
ln
0.13 0.3
167m3
临界氧量
控制成功
A B
C D E
20 10
2021/4/18
可燃性图中的临界点
重要参考 原有名
点
称
MFC
MIC MOC
MIC/MAI LOC
MMR
ICR
MMF
MIR
IAR
LFC OSFC/MXC
LDC
定义
惰化点的最小燃料浓度 惰化点的最小惰气浓度 惰化点的最小氧量浓度 惰化点的最小惰气/燃料体积比
惰化点的最大惰气/燃料份量
21.180 17.370 17.550 19.001
0.430 0.500 0.430 0.469
40.447 22.930 23.719 29.419
理论
0.505
0.537 0.477 0.443 0.515
聚合物燃烧特点图表
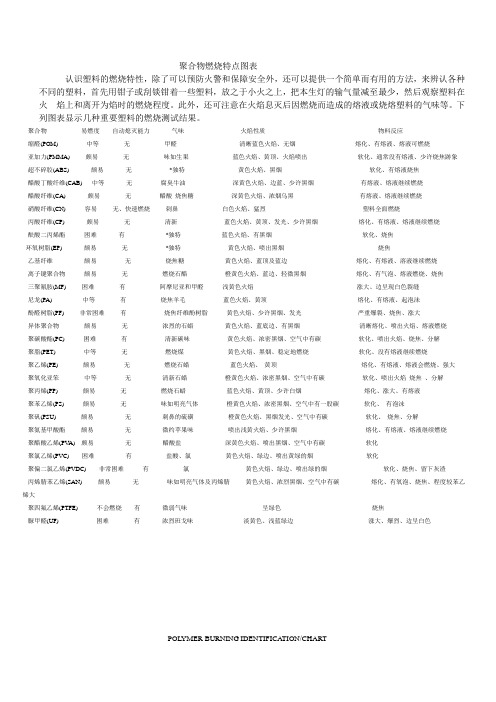
聚合物燃烧特点图表认识塑料的燃烧特性,除了可以预防火警和保障安全外,还可以提供一个简单而有用的方法,来辨认各种不同的塑料,首先用钳子或刮锬钳着一些塑料,放之于小火之上,把本生灯的输气量减至最少,然后观察塑料在火焰上和离开为焰时的燃烧程度。
此外,还可注意在火焰息灭后因燃烧而造成的熔液或烧熔塑料的气味等。
下列图表显示几种重要塑料的燃烧测试结果。
聚合物易燃度自动熄灭能力气味火焰性质物料反应缩醛(POM) 中等无甲醛清晰蓝色火焰、无烟熔化、有熔液、熔液可燃烧亚加力(PMMA) 颇易无味如生果蓝色火焰、黄顶、火焰喷出软化、通常没有熔液、少许烧焦跡象超不碎胶(ABS) 颇易无*独特黄色火焰、黑烟软化、有熔液烧焦醋酸丁酸纤维(CAB) 中等无腐臭牛油深黄色火焰、边蓝、少许黑烟有熔液、熔液继续燃烧醋酸纤维(CA) 颇易无醋酸烧焦糖深黄色火焰、浓烟乌黑有熔液、熔液继续燃烧硝酸纤维(CN) 容易无、快速燃烧刺鼻白色火焰、猛烈塑料全面燃烧丙酸纤维(CP) 颇易无清新蓝色火焰、黄顶、发光、少许黑烟熔化、有熔液、熔液继续燃烧酜酸二丙烯酯困难有*独特蓝色火焰、有黑烟软化、烧焦环氧树脂(EP) 颇易无*独特黄色火焰、喷出黑烟烧焦乙基纤维颇易无烧焦糖黄色火焰、蓝顶及蓝边熔化、有熔液、溶液继续燃烧离子键聚合物颇易无燃烧石醋橙黄色火焰、蓝边、轻微黑烟熔化、有气泡、熔液燃烧、烧焦三聚氰胺(MF) 困难有阿摩尼亚和甲醛浅黄色火焰涨大、边呈现白色裂缝尼龙(PA) 中等有烧焦羊毛蓝色火焰、黄顶熔化、有熔液、起泡沬酚醛树脂(PF) 非常困难有烧焦纤维酚树脂黄色火焰、少许黑烟、发光严重爆裂、烧焦、涨大异体聚合物颇易无浓烈的石蜡黄色火焰、蓝底边、有黑烟清晰熔化、喷出火焰、熔液燃烧聚碳酸酯(PC) 困难有清新碳味黄色火焰、浓密黑烟、空气中有碳软化、喷出火焰、烧焦、分解聚脂(PET) 中等无燃烧煤黄色火焰、黑烟、稳定地燃烧软化、没有熔液继续燃烧聚乙烯(PE) 颇易无燃烧石蜡蓝色火焰、黄顶熔化、有熔液、熔液会燃烧、强大聚氧化亚笨中等无清新石蜡橙黄色火焰、浓密黑烟、空气中有碳软化、喷出火焰烧焦、分解聚丙烯(PP) 颇易无燃烧石蜡蓝色火焰、黄顶、少许白烟熔化、涨大、有熔液聚苯乙烯(PS) 颇易无味如明亮气体橙黄色火焰、浓密黑烟、空气中有一股碳软化、有泡沬聚矾(PSU) 颇易无刺鼻的硫磺橙黄色火焰、黑烟发光、空气中有碳软化、烧焦、分解聚氨基甲酸酯颇易无微约苹果味喷出浅黄火焰、少许黑烟熔化、有熔液、熔液继续燃烧聚醋酸乙烯(PV A) 颇易无醋酸盐深黄色火焰、喷出黑烟、空气中有碳软化聚氯乙烯(PVC) 困难有盐酸、氯黄色火焰、绿边、喷出黄绿的烟软化聚偏二氯乙烯(PVDC) 非常困难有氯黄色火焰、绿边、喷出绿的烟软化、烧焦、留下灰渣丙烯腈苯乙烯(SAN) 颇易无味如明亮气体及丙烯腈黄色火焰、浓烈黑烟、空气中有碳熔化、有氧泡、烧焦、程度较苯乙烯大聚四氟乙烯(PTFE) 不会燃烧有微弱气味呈绿色烧焦脲甲醛(UF) 困难有浓烈班戈味淡黄色、浅蓝绿边涨大、爆烈、边呈白色POLYMER BURNING IDENTIFICA TION/CHARTKnowing the burning characteristics of plastics is useful not only for fire and safety but it provides a Simpleand useful method for their identification . Star by holding the piece of plastics with a pair of tweezers of a spatula in a low flame. Reduce the gas supply to the Bunsen burner to its minimum. Observe the flammability of the plastic in and out of the flame. Also note the formation of drops of burning or melting plastic as well as the flame is extinguished. The following chart shows the behavior of the most important plastics in the flame test.POL YMER EASE OF SELF ODOR NA TURE OF FLAME BEHA VIOR OFLIGHTING EXTINGUISHING MA TERIAL Acctal Moderate No Formaldehyde Clean blue flame no smoke Melts,drips drippingsmay burn Acrylic(PMMA) readily No Fruit-like Blue flame;yellow top, Soften,usually no drip,littlespurts char leftAcrylonitrile Butadiene readily No *Characteristic Yellow flame; black smoke Softens drips,chars Styrene (ABS)Cellulose Acetic(CA) readily No Acetic acid, Dark yellow flame; some Melts,drips,drippingsburned sugar sooty black smoke continue to burn Cellulose Acetic moderate No Rancid butter Dark yellow flame with blue Melts, drips, drippings Butyrate(CAB) edges. Some black smoke Continue to burn Cellulose Nitrate(CN) very readily No. burns fast Sharp White flame; very rapid Material burns completely Cellulose Propionate(CP) readily No Fragrant Blue flame; yellow top, Melts, drips, drippingsSparks, some black smoke continue to burnDiallyl Phthalate Difficult Yes *Characteristic Yellow: black smoke softens, charsEpoxy(EP) Readily No *Characteristic Yellow; spurts black smoke charsEthyl Cellulose Readily No Burned sugar Yellow flame; blue top and edges Melts,drips, drippings continueto burnLonomer Readily No Burning paraffin yellow-orange flame; blue edges; Melts, bubbles, drips andslight black smoke burns charsMelamine Formaldehyde Difficult Yes Ammonla and Light yellow swells, cracks turns(MF) formaldehyde white at edgesNylon(PA) Moderate Yes Burned wool Blue flame; yellow top Melts, drips, froths Phenolic, molded(PF) Very difficult Yes Burned fabric Yellow; a little black Cracks badly, chars, swellsPhenoilc smoke, sparksPolyallomer Beadily No Stringent paraffin Yellow flame; blue bottom Melts clear, spurfs,edge; black smoke dripping burn Polycarbonate(PC) Difficult Yes Sweet carbon odor Yellow flame; dense black softens, spurts ,charssmoke, carbon in the air decomposesPolyester(PET) Moderate No Burning coal Yellow; black smoke, softens, no drip continuesburn steadily to burnPolyethylene(PE) Readily No Burning paraffin Blue flame ;Yellow top Melts, drips dippings mayburn,swell Polyphyenylene Oxid Moderate No Sweet paraffin Yellow-orange flame; dense black softens, spurt, chars,smoke; carbon in the air decomposes Polypropylene(PP) Readily No Burning paraffin Blue flame; yellow top, some Melts, swells, dripsWhite smoksPolystyrene(PS) Readily No Illuminating gas Orange-yellow flames; dense smoke, Softens, bubbleclumps of carbon in airPolysulfone(PSU) Readily No Pungent sulfur odor Yellow-orange flame; black smoke Softens, chars, decomposessparkles, carbon in airPolyurethane(PU) Readily No Faint apple odor Light yellow spuring flame; slingt Melts, drips, drippings burnblack smokePolyvinyl Acctate(PV A) Readily No Acctic acid Dark yellow flame; spurts black Softenssmoke ,carbon in the airPolyvinyl Chloride(PVC) Difficult Yes Hydrochloric Yellow flame; green on edge, spurts Softensacid, chlorine green and yellow ,white smokePolyvinylidene very difficult Yes Chlorine Yellow flame; green on edges ,spurts Soften, chars, leaves ash Chloride(PVDC) green smokeStyrene Acrylonitrile Readily No Illuminating gas Yellow flame; heavy black smoke Melts, bubbles (SAN) and acrylonitrile some carbon in air chars more than styrene Tetrafluoroethylene will no ignite Yes Very little odor Yellow; green near base Melts, bubbles, slight (PTFE) charringUrea Formaldehyde(UF) Difficult Yes Strong pancake odor Pale yellow flame; light Swells, cracks, turns whitegreenish-blue edge at edges*Odors are difficult to describe, but recognizable-use controls(known sample)。
薄膜火焰燃烧实验报告

一、实验目的1. 探究薄膜火焰燃烧的特性。
2. 分析薄膜火焰燃烧的原理。
3. 了解薄膜火焰燃烧的应用。
二、实验原理薄膜火焰燃烧是一种利用薄膜将燃料与空气隔离,使燃料在薄膜内部燃烧的燃烧方式。
薄膜火焰燃烧具有燃烧温度高、燃烧速度快、燃烧效率高、污染小等优点。
实验原理如下:1. 燃料在薄膜内部燃烧,与空气接触较少,燃烧充分。
2. 薄膜起到隔离作用,使燃料与空气充分混合,燃烧速度快。
3. 燃烧过程中,薄膜内部温度高,燃烧效率高。
三、实验器材1. 薄膜:选用聚四氟乙烯(PTFE)薄膜,厚度为0.1mm。
2. 燃料:选用乙醇,浓度为95%。
3. 火焰源:酒精灯。
4. 温度计:量程为0-1000℃,精度为0.1℃。
5. 气体流量计:量程为0-10L/min,精度为0.1L/min。
6. 热电偶:量程为0-1000℃,精度为0.1℃。
7. 数据采集系统:用于实时采集温度、流量等数据。
四、实验步骤1. 将薄膜剪成适当大小的圆片,厚度保持一致。
2. 在薄膜中央滴加一定量的乙醇,使乙醇均匀分布。
3. 用酒精灯点燃乙醇,观察火焰燃烧情况。
4. 使用温度计、气体流量计等设备,实时采集火焰温度、流量等数据。
5. 改变薄膜厚度、乙醇滴加量等参数,重复实验,分析薄膜火焰燃烧特性。
五、实验现象1. 薄膜火焰燃烧时,火焰呈蓝色,燃烧稳定。
2. 随着薄膜厚度的增加,火焰温度逐渐降低,燃烧速度减慢。
3. 随着乙醇滴加量的增加,火焰温度逐渐升高,燃烧速度加快。
六、实验结果与分析1. 薄膜火焰燃烧温度较高,可达500℃以上,燃烧速度快,燃烧效率高。
2. 薄膜厚度对火焰燃烧有较大影响,厚度越大,火焰温度越低,燃烧速度越慢。
3. 乙醇滴加量对火焰燃烧也有较大影响,滴加量越大,火焰温度越高,燃烧速度越快。
七、结论1. 薄膜火焰燃烧具有燃烧温度高、燃烧速度快、燃烧效率高、污染小等优点。
2. 薄膜厚度和乙醇滴加量对薄膜火焰燃烧特性有较大影响。
3. 薄膜火焰燃烧在工业、民用等领域具有广泛的应用前景。
掌握这8张图,搞定高中化学实验装置图和化学实验现象

掌握这8张图,搞定高中化学实验装置图和化学实验现象化学实验装置图化学实验现象1.镁条在空气中燃烧:发出耀眼强光,放出大量的热,生成白烟同时生成一种白色物质。
2.木炭在氧气中燃烧:发出白光,放出热量。
3.硫在氧气中燃烧:发出明亮的蓝紫色火焰,放出热量,生成一种有刺激性气味的气体。
4.铁丝在氧气中燃烧:剧烈燃烧,火星四射,放出热量,生成黑色固体物质。
5.加热试管中碳酸氢铵:有刺激性气味气体生成,试管上有液滴生成。
6.氢气在空气中燃烧:火焰呈现淡蓝色。
7.氢气在氯气中燃烧:发出苍白色火焰,产生大量的热。
H2 + Cl2=(点燃) 2HCl8.在试管中用氢气还原氧化铜:黑色氧化铜变为红色物质,试管口有液滴生成。
9.用木炭粉还原氧化铜粉末,使生成气体通入澄清石灰水,黑色氧化铜变为有光泽的金属颗粒,石灰水变浑浊。
10.一氧化碳在空气中燃烧:发出蓝色的火焰,放出热量。
11. 向盛有少量碳酸钾固体的试管中滴加盐酸:有气体生成。
K2CO3+ 2HCl = 2KCl + H2O + CO2↑12.加热试管中的硫酸铜晶体:蓝色晶体逐渐变为白色粉末,且试管口有液滴生成。
13.钠在氯气中燃烧:剧烈燃烧,生成白色固体。
2Na+Cl2 =(点燃)2NaCl14.点燃纯净的氢气,用干冷烧杯罩在火焰上:发出淡蓝色火焰,烧杯内壁有液滴生成。
15.向含有C1-的溶液中滴加用硝酸酸化的硝酸银溶液,有白色沉淀生成。
Ag++Cl-=AgCl↓16.向含有SO42-的溶液中滴加用硝酸酸化的氯化钡溶液,有白色沉淀生成。
SO42-+Ba2+= BaSO4↓17.一带锈铁钉投入盛稀硫酸的试管中并加热:铁锈逐渐溶解,溶液呈浅黄色,并有气体生成。
Fe2O3+6H+=2Fe3++3H2OFe+2H+=Fe3++3H2↑18.在硫酸铜溶液中滴加氢氧化钠溶液:有蓝色絮状沉淀生成。
19.将Cl2通入无色KI溶液中,溶液中有褐色的物质产生。
Cl2+ 2I- = I2 + 2Cl-20.在三氯化铁溶液中滴加氢氧化钠溶液:有红褐色沉淀生成。
人教版高中化学选修四课件01-2燃烧热(ppt).pptx

思考:应根据什么标准来选择燃料?
二、能源
能源:能源就是能提供能量的自然资源,包括 化石燃料(煤、石油、天然气)阳光、风力、流水、 潮汐以及柴草等
能源是人类社会发展进步的基础,在当代,能源 同信息、材料一起构成现代文明的三大支柱
分类: 常规能源:技术比较成熟、使用比较普遍的能源。如: 煤炭、石油等。 新能源:近几十年才开始利用或正在研究开发的能源: 如:太阳能、核能、地热能等。
目前用的主要能源是化石燃料,储藏量有限 而且不可再生,最终会枯竭,解决办法是什么?
3.已知:
△H=-285.83 KJ/mol
△H=-282.9 KJ/mol
若氢气与一氧化碳的混合气体完全燃可生成5.4gH2O , 并放出114.03 KJ热量,则混合气体中CO的物质的量为
A.0.22 mol B.0.15 mol
C.0.1 mol
D.0.05 mol
C
空白演示
在此输入您的封面副标题
燃烧热 能源
一、燃烧热
25oC,101KP时,1mol纯物质完全燃 烧生成稳定化合物时所放出的热量,叫做 该物质的燃烧热。 例如:
CH4(g)+2O2(g)==CO2(g)+H2O(l) H=-890.31KJ/mol
即甲烷的燃烧热为890.31KJ/mol
重点探究(燃烧热)
③能源可分为一级能源和二级能源。自然界以现
存形式提供的能源称为一级能源;需要依靠其他
能源的能量间接制取的能源称为二级能源。有人 认为,气体C是一种优质能源,你认为气体C作 为能源的最突出的优点是
《工程燃烧学》PPT课件

t热
(t''t') i''i'
12
方程求解燃料理论发热温度
t热
Q低 V0 c产
方程求解法
c=A1+A2t+A3t2 如认为只有三种成分CO2、H2O、N2,则 V0 c产 =VCO2 (A1CO2 +A2CO2t+ A3CO2t2) + VH2O (A1H2O
+A2H2Ot+ A3H2Ot2) +VN2 (A1N2 +A2N2t+ A3N2t2) V0 c产 =a+bt+ct2
根据具体的燃料成分计算V0 =(VCO2+VH2O+VN2 +…) ,并根据表3-3确定c产
适用性:燃烧产物的平均比热受温度的影响不 显著,特别是空气作助燃剂
9
比热近似法求解过程
假定发热温度在某 个范围内
t热
Q低 V0 c产
提高假定温度 是
查找对应温度下的烟 气比热c热,计算V0,
计算烟气温度t
因此 ct3+bt2+at-Q低=0 解方程即得t热
13
理论燃烧温度计算
t理Q低QV空 ncQ 产燃Q分
理论燃烧温度表达式如下
Q低、Q空、Q燃都容易计算
需要计算Vn.c产
更关键的是计算Q分
14
高温热分解
温 工度业Q 越炉分 高中,, 分只1 2 解考6 越 虑0 0 强 温V ; 度C O 压 , 力 且1 越 只0 高 有8 0 ,大0 分于V 1解H 82 较00弱
V0、L0根据燃料的成分计算
注意:右边c产是理论燃烧产物的比热 17
影响理论燃烧温度的因素
燃料种类和发热量
主要取决于单位体积燃烧产物的热含量
燃烧学第五章 ppt课件

五、着火延滞期
• 实际的燃烧设备,不仅要求燃料能稳定地燃烧,而且 要求预混气体能及时地着火,因此了解பைடு நூலகம்燃混合物的 着火延滞期具有实际意义
•
着温v火度12T延ck所滞0 e经期xp历就的R是ET时c可C间燃0n 混合物从结气初论压始:力愠着和度火自T0延燃上迟温升期度到随的着混升火合高
i C0Ccv
32
几种可燃气体的着火范围
名称
着火温度℃
可燃物着火
着火范围相应
的浓度范围
的过量空气系数
低限 % 高限 % 高限 % 低限 %
氢 (H2)
571
一氧化碳 (CO)
609
4.0
74.2
12.4
73.8
2.94
0.184
甲烷 (CH4)
632
乙烷 (C2H6)
472
4.6
14.6
2.17
0.61
2.9
14
2
一、着火的概念
1、着火的方式与机理
–自然界中燃料的着火方式
自燃着火
(自燃)
把一定体积的混合气预热到某一温度,在该 温度下,混合气的反应速率即自动加速, 急剧增大直到着火。—— 整体加热。
强迫着火
(点燃或点火)
可燃混合气内的某一处用点火热源点着相 邻一层混合气,尔后燃烧波自动的传播到 混合气的其余部分。 ——局部加热。
Q
1
dC d
C p
dT d
Q
1
dC d
C p
dT d
Q 1 dC C p dT
dT Q 1 dC C p
2020/9/6
哈尔滨工业大学(威海)汽车工程学院
10
火灾过程的基本参数及燃烧速度理论(精)
Q Q LV F L (kJ/g) (kW/m2) (kW/m2)
GS (g/m2s) 11 16 14 25 14 13 35 17 13 24 33
3.34 24.3 2.32 2.07 2.3 1.2 1.76 1.75 1.64 1.62 1.52
25.1 38.5 32.6 51.9 28.0 23.0 61.5 29.3 21.8 38.5 50.2
高聚物
聚乙烯 聚丙烯 聚氯乙烯 聚醋酸乙烯 脂 聚苯乙烯
分解温度
335~450 328~410 200~300 213~325 300~400
高聚物
聚氟乙烯 聚三氟氯乙 烯 聚四氟乙烯 天然橡胶 丁二烯橡胶
高聚物
372~480 347~418 508~538 400~900 400~1000
分解温度
第二节 火灾过程的基本参数及燃烧速度理论
一、物质燃烧过程及其温度分布* 二、火灾过程的基本参数 三、燃烧速度理论 环境散失的热量。此时若撤掉热源,可燃物将降低温度,燃烧不能发生;若 继续在热的环境中加热,则因氧化反应速度逐步加快,使温度上升较快。 C点的温度为TC,当可燃物温度升高至TC时,可燃物氧化产生的热量和 体系向环境散失的热量相等,也就是说,在TC温度时体系产生的热量和向环 境散失的热量达到干衡。若热源的温度稍有扰动,使体系的温度略高于TC, 热平衡被打破,此时可燃物氧化产生的热量大于体系向环境散失的热量,体 系产生热量积累,温度继续上升。因此TC为体系从不燃烧到燃烧的转折点, 即为可燃物的燃点。 D点的温度为TD,当可燃物温度上升到TD时,可燃物已发生燃烧,同时出 现火焰,且温度继续上升。 E点的温度为TE,此时是可燃物经燃烧后,其产物达到的最高温度。 可燃物在TA和TB温度之间,是它的受热区域,在TB和TC温度之间是可燃物在 凝聚相中的反应区域;在TC和TD温度之间是可燃物在气相中的反应区域;TD 温度以后,可燃物产生火焰,反应物变成了生成物,温度达到燃烧最高温度 TE。
焚烧炉CAD图纸

焚烧炉CAD图纸本文介绍焚烧炉CAD图纸的重要性和目的。
焚烧炉CAD图纸是指使用计算机辅助设计(CAD)软件制作的焚烧炉的技术图纸。
这些图纸是焚烧炉的设计和制造过程中必不可少的工具,它们有助于确保焚烧炉的精确制造和操作。
焚烧炉CAD图纸的重要性在于它们提供了焚烧炉的详细设计信息,包括尺寸、结构、材料和组件等。
这些信息对焚烧炉的制造商和操作者非常关键,能够确保焚烧炉的性能和安全性。
焚烧炉CAD图纸的目的是为了协助设计师和工程师进行焚烧炉的设计和制造。
通过使用CAD软件,设计师可以将焚烧炉的各个组件进行精确建模,并在图纸中标注详细的尺寸和特征。
这样一来,制造商可以根据焚烧炉CAD图纸进行制造,确保每个焚烧炉的一致性和质量。
总之,焚烧炉CAD图纸是焚烧炉设计和制造过程中不可或缺的工具。
它们的重要性在于提供了焚烧炉的详细设计信息,而目的则是为了协助设计师和工程师进行焚烧炉的设计和制造。
本图纸主要描述了焚烧炉CAD图纸的尺寸、构造和细节。
下面是图纸的主要要素:尺寸:长度:X mm宽度:Y mm高度:Z mm构造:焚烧炉主体:包括焚烧室、燃烧器、加热元件等部件的布局和连接方式。
进料口:用于向焚烧室投料的口部。
出料口:焚烧完成后,将残渣排出的口部。
排气管道:导出燃烧产生的气体的管道。
细节:焚烧室内的温度计:用于监测焚烧室内部温度的仪器。
控制面板:用于控制焚烧炉的开关、温度和燃料供给等参数的面板。
支撑结构:用于支持焚烧炉主体的结构。
该图纸为焚烧炉CAD模型的可视化表达,可以作为制造、安装和维修焚烧炉的参考依据。
焚烧炉CAD图纸主要用于呈现和解释焚烧炉的设计和布局。
它具有以下主要功能和用途:设计参考:焚烧炉CAD图纸提供了设计人员参考,帮助他们了解焚烧炉的整体结构和组成部分。
通过CAD图纸,设计人员可以详细了解焚烧炉的尺寸、形状和位置安排,以便进行合理的设计和布局。
设计参考:焚烧炉CAD图纸提供了设计人员参考,帮助他们了解焚烧炉的整体结构和组成部分。
