磺胺氯吡嗪钠可溶性粉检验SOP
磺胺氯吡嗪钠可溶性粉生产工艺规程

磺胺氯吡嗪钠可溶性粉生产工艺规程目录1 产品概述2 处方和依据3 工艺流程图4 制剂工艺过程及工艺条件5 原辅材料的预处理6 原辅材料质量标准和检查方法7 中间产品质量标准和检查方法8 成品质量标准和检查方法9 包装规格、包装材料质量标准10 说明书、产品文字说明和标志11 工艺要求12 设备一览表和主要设备生产能力13 技术安全与劳动保护14 劳动组织15 原辅料消耗定额16 包装材料消耗定额17 动力消耗定额18 综合利用与环境保护目的:制定本标准的目的是规范磺胺氯吡嗪钠可溶性粉生产过程,对一定数量的成品所需的起始原辅料和包装材料,以及工艺、加工说明、技术参数、注意事项等进一步标准化。
适用范围:适用于磺胺氯吡嗪钠可溶性粉生产全过程。
责任人:质量部部长、生产部部长、车间主任。
内容:1 产品概述:本品为磺胺氯吡嗪钠可溶性粉。
1.1 产品特点:1.1.1性状:本品为淡黄色粉末。
1.1.2规格:100g:磺胺氯吡嗪钠30g1.1.3贮藏:遮光,密闭保存。
1.1.7有效期:二年1.1.8批准文号:2.处方和依据2.1处方:100g磺胺氯吡嗪钠: 30g无水葡萄糖:加至100g2.2处方依据:3生产工艺流程图及环境区域划分示意图4 制剂工艺过程及工艺条件4.1总述:按生产指令领取磺胺氯吡嗪钠原料药和预处理过的无水葡萄糖,将磺胺氯吡嗪钠与无水葡萄糖用等量递增法混合均匀,定量分装即可。
4.2分述:4.2.1投料量:为处方量的整数倍。
5 原辅材料的预处理5.1 按生产指令单领取无水葡萄糖粉的预处理按粉碎机操作规程操作,粉碎,使完全通过80目筛。
过筛结束后,检查合格将粉碎好的药粉装入洁净容器,称量、记录,挂上标签,注明品名、批号、数量、日期等,填写中间产品交接单,转入下工序。
进行物料平衡计算,收率99.0%~99.5%。
5.2 称量配料:按生产指令单称取磺胺氯吡嗪钠和无水葡萄糖5.3混合:将上述称量好的药粉置V型混合机中,用等量递增法每次预混10分钟,再总混合30分钟,检验含量合格后,装入洁净不锈钢桶密封并标明名称、规格、批量(或数量)等,填写中间产品交接单,转入中间站。
磺胺氯吡嗪钠可溶性粉内控质量标准

GMP管理文件一.目的:制定磺胺氯吡嗪钠可溶性粉内控质量标准(成品),规范公司磺胺氯吡嗪钠可溶性粉的生产。
二.适用范围:适用于磺胺氯吡嗪钠可溶性粉生产和质检。
三.责任者:生产部经理、质管部经理、检验员四.正文:磺胺氯吡嗪钠可溶性粉本品为磺胺氯吡嗪钠与乳糖配置而成,含磺胺氯吡嗪钠(C10H8ClN4NaO2·H2O)应为标示量的92.0~109.0%。
【性状】本品为淡黄色粉末。
【鉴别】(1)取本品,加甲醇制成每1ml中含磺胺氯吡嗪钠1mg的溶液,作为供试品溶液,另取磺胺氯吡嗪钠对照品,加甲醇制成每1ml含磺胺氯吡嗪钠1mg的溶液,作为对照品溶液。
吸取上述两种溶液各2ul,照有关物质项下的方法试验,供试品溶液所显主斑点的颜色与位置应与对照品溶液的主斑点相同。
(2)取本品适量(约相当于磺胺氯吡嗪钠50mg),加稀盐酸2ml使溶解,显芳香第一胺类的鉴别反应。
【检查】溶解性取本品15g,加水100ml,搅拌后应全部溶解。
粒度取本品,用500um孔径筛检查,500um孔径筛通过率不少于95%。
有关物质取本品适量,加甲醇制每1ml中含磺胺氯吡嗪钠10mg的溶液,超声助溶,取上清液,作为供试品溶液;另取磺胺氯吡嗪钠对照品,加甲醇制成每1ml中含0.3mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各2μl分别点于同一硅胶G薄层板上,用甲苯-醋酸乙酯-甲醇(3:1:1)为展开剂,展开后,晾干,将薄层板置于充满压硫酸气体(用压硫酸钠2g,加盐酸5ml产生,)的密闭容器中,5分钟后取出,室温下放置3~5分钟,喷以0.1%盐酸萘乙二胺溶液,供试品溶液如显杂质斑点,其颜色与对照品溶液的主斑点比较,不得更深。
水分取本品,照水分测定法测定,含水分不得过2.0%。
【含量测定】取本品(约相当于磺胺氯吡嗪钠0.5g),精密称定,加水25ml溶解,加二甲基甲酰胺15ml,缓慢加入氢溴酸溶液40ml,照永停滴定法,用亚硝酸钠液(0.1mol/L)滴定。
磺胺氯吡嗪钠钠可溶性粉

相对偏差=
计算:含量
X1=
X2=
相对偏差=
取样量w:(1)g (2)g
编号1(V1)2(V2)
滴定仪初读数
滴定仪终读数
滴定仪消耗体积
计算公式:含量(%)=
公式中Cr为亚硝酸钠滴定液(0、1mol/L)的实际浓度;
CR为亚硝酸钠滴定液(0.1mol/L)的标准浓度;
V为滴定样品所消耗的亚硝酸钠滴定液(0.1mol/L)的体积(ml);
T为每1ml亚硝酸钠液(0.1mol/L)相当于C14H11N4NaO2S的毫克数;
济南百鸣生物制药有限公司
留样检验记录
第1页共2页
检品名称
磺胺氯吡嗪钠钠可溶性粉
生产车间
取样地点
普通留样室
生产批号
规格
100g:30g
批数量
包装规格
100g×30瓶/箱
检验日期
报告日期
检验项目
性状、酸度、干燥失重、含量测定
检验单号
检验依据
BM—ZG—01—020—00
检验日期年月日—年月日
检验人
年月日
复核人
年月日
负责人
年月日
【性状】本品为粉末。
【检查】(1)水分仪器AB135-S型电子分析天平(编号:P-05)室温()℃湿度()% SH10A型水分快速测定仪(编号:P-07)室温()℃湿度()%
取本品()g,精密称定,加无水甲醇()ml,密塞,振摇()分钟,依法测定。
计算公式:F=水分(%)=
F:每1ml费休氏试液相当于水的重量(mg); F:每1ml费休氏试液相当于水的重量(mg);
W:称取重蒸馏水的重量(mg);W:供试品的重量(g);
磺胺氯吡嗪钠可溶性粉成产工艺规程

制药有限公司磺胺氯吡嗪钠可溶性粉工艺规程颁发单位:GMP办公室工艺规程批准程序目录1、产品概述 (3)2、生产的工艺流程图 (5)3、操作过程及工艺条件 (6)4、工艺过程中所需SOP名称及要求 (9)5、工艺卫生及环境卫生 (9)6、工艺验证及具体要求 (10)7、设备一览表及主要设备生产能力 (10)8、物料平衡及经济技术指标计算 (10)9、技术安全及劳动保护 (11)10、岗位定员 (12)1.产品概述1.1 产品名称:通用名:磺胺氯吡嗪钠可溶性粉商品名:1.2 性状:本品为淡黄色的粉末1.3 规格:30%磺胺氯吡嗪钠30g 口服葡萄糖70g。
1.5 依据:2005版《中国兽药典》一部。
1.6 适应症:磺胺类药。
主用于球虫病。
1.7 有效期:二年1.8 成品贮存方法及注意事项:遮光、密封,在干燥处保存。
1.9 原辅材料、半成品和成品质量标准:磺胺氯吡嗪钠质量标准见磺胺氯吡嗪钠内控质量标准。
口服葡萄糖质量标准见口服葡萄糖内控质量标准。
半成品质量标准见磺胺氯吡嗪钠可溶性粉可溶性粉半成品内控质量标准。
成品内控质量标准见磺胺氯吡嗪钠可溶性粉内控质量标准。
1.10 原辅材料贮存注意事项:磺胺氯吡嗪钠:遮光、密封,在干燥处保存。
口服葡萄糖:密封保存。
1.11 半成品检查方法及岗位控制:a质量控制要点:b 半成品检查方法见磺胺氯吡嗪钠可溶性粉半成品检验操作规程。
1.12包装要求:应符合铝箔袋质量内控标准要求。
1.13用法用量:肉鸡、火鸡混饮每1L水 1g 混饲每1000kg饲料2000g 连用3天兔混饲每1000kg饲料 2000g 连用5-10天羊内服配成 10%水溶液每1kg体重 1.2ml 连用3-5天1.15 批准文号:2.生产的工艺流程图注:加粗部分为主要控制点3.操作过程及工艺条件3.1 生产前准备:3.1.1 上一批次是否进行清场。
清场者、检查者是否签字,将“清场合格证”副件归入本批生产记录。
磺胺氯吡嗪残留检测方法标准(试行)

磺胺氯吡嗪残留检测方法标准(试行)鸡可食性组织中磺胺氯吡嗪残留量的测定高效液相色谱法(试行)1.范围本方法规定了鸡可食组织中磺胺氯吡嗪残留量检测的制样和高效液相色谱测定方法。
本方法适用于鸡的肌肉、肝脏、肾脏和脂肪中磺胺氯吡嗪残留量的检测。
2.规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 6682 分析实验室用水规格和试验方法。
3.方法原理试样中磺胺氯吡嗪残留物用乙腈提取酸化后,经混合型阳离子交换反相吸附固相萃取小柱净化,氮气吹干,流动相溶解,用高效液相色谱法测定,外标法定量。
4.试剂和材料以下所用的试剂,除特别注明者外均为分析纯试剂;水为符合GB/T 6682规定的一级水。
4.1 磺胺氯吡嗪钠对照品:纯度≥99.0%。
4.2 甲醇:色谱纯。
4.3 乙腈:色谱纯。
4.4 氨水。
4.5 盐酸。
4.6 磷酸二氢钾。
4.7 5 %氨化乙腈:准确吸取氨水5 mL,置于100 mL容量瓶中,用乙腈稀释至刻度,摇匀即得。
4.8 0.1 mol/L盐酸水溶液:准确吸取37 %浓盐酸829 μL,置于100 mL容量瓶中,用水稀释并定容至刻度,摇匀即得。
4.9 0.02 mol/L磷酸二氢钾水溶液:准确称取磷酸二氢钾2.7218 g,置于1000 mL容量瓶中,用水稀释并定容至刻度,摇匀即得。
4.10 复溶液:将乙腈和0.1 mol/L盐酸水溶液按50∶50(V/V)比例混匀,现配现用。
4.11 流动相:将乙腈和0.02 mol/L磷酸二氢钾水溶液按35∶65(V/V)比例混匀,经0.22 μm有机滤膜过滤,超声脱气20 min。
现配现用。
4.12 磺胺氯吡嗪标准储备液(1 mg/mL):准确称取磺胺氯吡嗪钠对照品25 mg,置于25 mL容量瓶中,用甲醇溶解并定溶至刻度,摇匀即得。
药品检验操作规程

一.目的:建立磺胺喹噁啉钠可溶性粉检验的标准操作程序,使操作过程规化。
二. 围:适用于磺胺喹噁啉钠可溶性粉的检验操作。
三.责任者:QC主管、检验人员四.正文1.性状取本品观察,本品为白色或微黄色粉末。
具有以上任何一种性状均符合规定。
2.鉴别2.1芳香第一胺类的鉴别反应2.1.1仪器及试剂天平、刻度吸管、漏斗、恒温干燥箱、可控温电炉、烧杯、滴管、漏斗架;醋酸、稀盐酸、亚硝酸钠溶液(0.1mol/L)、碱性β-萘酚试液。
2.1.2操作方法及结果判断取本品约1g,加水25ml溶解后,加醋酸2ml,即析出黄色沉淀;滤过,沉淀用水洗涤,在105℃干燥1小时,取干燥后沉淀50mg,加稀盐酸1ml,必要时缓缓煮沸使溶解,放冷,加0.1mol/L亚硝酸钠溶液3滴,滴加碱性β-萘酚试液3滴,生成由橙黄到猩红色沉淀,则判符合规定,反之,则判不符合规定。
2.2最大吸收2.2.1仪器及试剂紫外分光光度计、容量瓶、电子天平、烧杯、0.01mol/L氢氧化钠溶液。
2.2.2操作方法及结果判定取2.1.2项下105℃干燥1小时的沉淀,加0.01mol/L氢氧化钠溶液制成每1ml中含5µg 的溶液,照紫外分光光度法操作规程(SOP-JT00200)测定,在230~350nm的波长围测定,在252nm的波长处有最大吸收,吸收度约0.55。
则判符合规定,反之,则判不符合规定。
2.3钠盐鉴别反应2.3.1仪器及试剂铂丝、酒精灯、镊子、试管、滴管、试管架;盐酸、醋酸氧铀锌试液。
2.3.2操作方法及结果判断合规定,反之,则判不符合规定。
2.3.2.2取本品水溶液,加醋酸氧铀锌试液,生成黄色沉淀,则判符合规定,反之,则判不符合规定。
3.检查3.1干燥失重3.1.1仪器与用具扁形称量瓶(干燥至恒重)、电子天平、干燥箱、干燥器。
照干燥失重测定法操作规程(SOP-JT00500)依法检查,取本品1g ,置与供试品同样条件下干燥至恒重的扁形称量瓶中,精密称定,放入105℃的恒温干燥箱中进行干燥4小时,干燥后取出置干燥器中放冷至室温一般约30分钟,精密称定,记录数据。
饲料中磺胺氯吡嗪钠含量的高效液相色谱检测方法的建立

饲料中磺胺氯吡嗪钠含量的高效液相色谱检测方法的建立唐姝;陈娟;高建龙;鲍恩东【期刊名称】《南京农业大学学报》【年(卷),期】2012(35)2【摘要】为建立饲料中磺胺氯吡嗪钠的高效液相色谱检测方法,饲料经乙腈提取,旋转蒸发浓缩,2 mL甲醇+8 mL 0.05mol.L-1KH2PO4溶解,固相萃取净化,0.2μm有机相滤器过滤后,回收液经Agilent 1100液相色谱仪进行检测。
检测条件:在C18色谱柱上,流速为1.000 mL.min-1,柱温25℃,紫外检测波长为272 nm,流动相为乙腈和0.2%磷酸混合液(体积比为35∶65)。
试验结果显示:磺胺氯吡嗪钠的色谱峰保留时间为7.5 min;在添加0.5、1和2μg.mL-1条件下,回收率为90.6%~97.1%;检测限为0.5 mg.kg-1,定量限为1.0 mg.kg-1,线性范围为0.50~10.00μg.mL-1,回归方程为Y=57.332X+2.972 9(R2=0.999 3);4种饲料样本的相对标准偏差(RSD)为1.0%~2.9%。
结论:本试验所建立的高效液相色谱检测方法灵敏度高、准确性和重现性好,可以对饲料中的磺胺氯吡嗪钠进行定量检测。
【总页数】5页(P105-109)【关键词】磺胺氯吡嗪钠;高效液相色谱;饲料;检测【作者】唐姝;陈娟;高建龙;鲍恩东【作者单位】南京农业大学动物医学院;宁夏回族自治区兽药饲料监察所【正文语种】中文【中图分类】S816.17;S859.84【相关文献】1.高效液相色谱法检测鸡可食性组织中的磺胺氯吡嗪残留 [J], 邢玉娟;吕凤霞;陈玲;牛华星;刘运镇;邱树磊;冯文丽;刘联盟;李灵娟2.鸡血浆中磺胺氯吡嗪钠和甲氧苄啶含量HPLC检测方法的建立 [J], 卓国荣; 聂巧; 王东亮; 陈鸿雨; 秦琪; 卜仕金; 张明珠; 杨海峰; 孙晨明3.高效液相色谱-蒸发光散射检测法测量饮料中三氯蔗糖含量的不确定度评估 [J], 贾寒冰; 李荣; 郭端; 王涛; 孙晓4.高效液相色谱法测定磺胺氯达嗪钠含量 [J], 邵耀东;尹登刚;周卫斌;由力;徐峰;张风5.高效液相色谱法测定磺胺氯吡嗪钠含量 [J], 李秋菊因版权原因,仅展示原文概要,查看原文内容请购买。
磺胺类药物检测(高效液相色谱法)

测定步骤
4.定量测定
取标准工作液和样品试液分别注入液相色谱仪,记录谱图, 按外标法以峰面积进行计算。
测定步骤
5.结果计算
按照下式计算试样中各种药物残留的含量:
试剂
15.标准贮备液(1mg/mL):准备称取SD、SM2、SMM、SMZ、SQ对照品各 100mg,用乙腈溶解并稀释至100mL容量瓶中,必要时超声。贮存于0℃8℃冰箱中,有效期90d。 16.标准工作液:取上述标准贮备液,用流动相稀释,得到磺胺类药物 0.02μg/mL、0.1μg/mL、0.2μg/mL、0.5μg/mL、1.0μg/mL的标准混 合溶液。贮存于0℃-8℃冰箱中,有效期7d。
式中:X——试样中各种药物的含量,单位为微克每千克(ug/kg) A——试样溶液对应的色谱峰面积响应值; AS——标准溶液对应的色谱峰面积响应值 V1——加入提取液的体积,单位为毫升(mL) V2——取出提取液的体积,单位为毫升(mL)
试剂
本实验用水均为去离子水,试剂为分析纯度或优级纯。 7.氯仿。 8.硫酸钠。 9.磷酸。 10.C18粉。 11.中性氧化铝粉,用前于600℃马弗炉烘烤5h。 12.氯仿乙腈溶液:取乙腈10mL加氯仿90mL。 13.磷酸三乙胺溶液:取3.4mL磷酸加水至1000mL,用三乙胺调节pH 为3.0。 14.流动相:磷酸三乙胺溶液-乙腈(25:75)。
测定步骤
2.试样提取净化
称取(6±0.05g)均质动物组织样品于50mL离心管中,依次加入14mL氯仿乙 腈溶液、1.0ml 10%硫酸钠溶液,振荡提取15min,以5000r/min离心5min。准确吸 取10mL提取液,氮吹或浓缩至近干,用4mL氯仿乙腈溶液溶解后,分别加入C18粉、 中性氧化铝粉各100mg,涡旋混2min,8000r/min离心3min。准确移取1.0mL上清液 于另一10mL离心管中,氮气吹干,加入1.0mL流动相,涡混溶解残渣,过0.45μm 滤膜。待HPLC测定。
成品检验操作规程

河南惠通天下生物工程有限公司GMP管理文件一、目的:规范氧氟沙星可溶性粉的检验操作规程。
二、适用范围:适用于氧氟沙星可溶性粉的质量检验。
三、责任者:QC负责执行,质量管理部主管负责监督。
四、正文:本品为氧氟沙星与葡萄糖或乳糖配制而成。
含氧氟沙星(C18H20FN3O4)应为标示量的92.0~108.0%。
1.性状本品为白色或微黄色粉末。
2.鉴别2.1吸收度2.1.1仪器及试剂分光光度计、电子天平、容量瓶(100ml)、盐酸溶液(0.1mol/L)。
2.1.2操作方法及结果判断取含量测定项下的照分光光度法(附录17页)侧定,在293nm的波长处有最大吸收。
则符合规定,反之,则不符合规定。
2.2薄层法2.2.1仪器及试剂电子天平、紫外灯、展开缸、氯仿、甲醇、氨溶液、硅胶GF254薄层板。
2.2.2操作方法及结果判断取本品适量(约相当于氧氟沙星40mg),加氯仿10ml,振摇使氧氟沙星全部溶解,滤过,取滤液作为供试品溶液;另取氧氟沙星对照品适量,加氯仿制成每1ml中含4mg 的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各5ul,分别点于同一硅胶GF254薄层板上,以氯仿-甲醇-氨溶液(4→100)(10:5:1)为展开剂,展开后,晾干,置紫外光灯(254nm)下检视,供试品溶液所显主斑点的颜色与位置应与对照品溶液的主斑点相同,则符合规定,反之,则不符合规定。
3.检查3.1溶解性3.1.1仪器及试剂天平、烧杯,玻璃棒。
3.1.2操作方法及判定结果取本品1.0g,加水50ml,搅拌,应全部溶解。
全部溶解则符合规定,反之,则不符合规定。
3.2干燥失重3.2.1仪器及试剂恒温干燥箱、电子天平、干燥器、扁形称量瓶。
3.2.2操作方法照干燥失重检查法操作规程,依法检查,取本品1g,置与供试品同样条件下干燥至恒重的扁形称量瓶中,精密称定,放入105℃的恒温干燥箱中进行干燥,干燥后取出置干燥器中放冷至室温一般约30分钟,精密称定,接着继续按上法干燥,直至恒重。
6.磺胺脒检验标准操作规程 编号:SOP-ZH-10-00
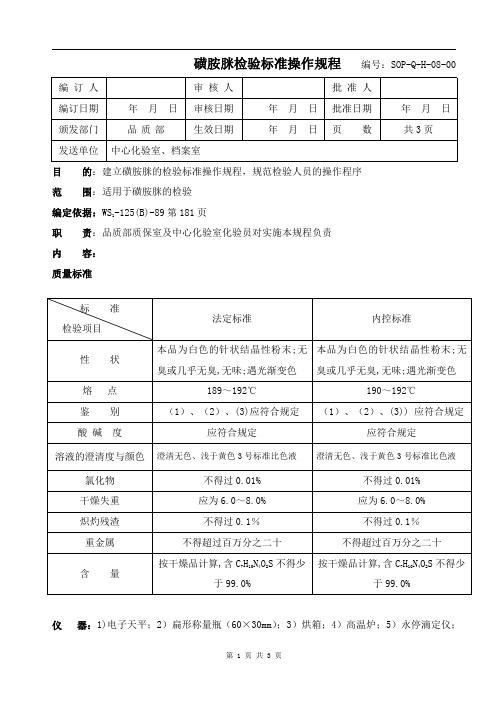
磺胺脒检验标准操作规程编号:SOP-Q-H-08-00编订人审核人批准人编订日期年月日审核日期年月日批准日期年月日颁发部门品质部生效日期年月日页数共3页发送单位中心化验室、档案室目的:建立磺胺脒的检验标准操作规程,规范检验人员的操作程序范围:适用于磺胺脒的检验编定依据:WS 1-125(B)-89第181页职责:品质部质保室及中心化验室化验员对实施本规程负责内容:质量标准仪器:1)电子天平;2)扁形称量瓶(60×30mm);3)烘箱;4)高温炉;5)永停滴定仪;标准检验项目法定标准内控标准性状本品为白色的针状结晶性粉末;无臭或几乎无臭,无味;遇光渐变色本品为白色的针状结晶性粉末;无臭或几乎无臭,无味;遇光渐变色熔点189~192℃190~192℃鉴别(1)、(2)、(3)应符合规定(1)、(2)、(3))应符合规定酸碱度应符合规定应符合规定溶液的澄清度与颜色澄清无色、浅于黄色3号标准比色液澄清无色、浅于黄色3号标准比色液氯化物不得过0.01%不得过0.01%干燥失重应为6.0~8.0%应为6.0~8.0%炽灼残渣不得过0.1%不得过0.1%重金属不得超过百万分之二十不得超过百万分之二十含量按干燥品计算,含C 7H 10N 4O 2S 不得少于99.0%按干燥品计算,含C 7H 10N 4O 2S 不得少于99.0%6)熔点仪。
试药1)氢氧化钠溶液(1→5);2)酚酞指示液;3)氢氧化钠液(0.1mol/L);4)盐酸((1→2);5)亚硝酸钠滴定液(0.1mol/L)本品为对氨基苯磺酰胺基脒.按干燥品计算,含C7H10N4O2S不得少于99.0%。
[性状]本品为白色的针状结晶性粉末;无臭或几乎无臭,无味;遇光渐变色。
本品在沸水中溶解,在水、乙醇或丙酮中微溶;在稀盐酸中易溶,在氢氧化碱溶液中几乎不溶。
熔点本品的熔点(见熔点检查法SOP)为189~192℃。
[鉴别](1)本品显芳香第一胺类的鉴别反应。
复方磺胺氯哒嗪钠粉2010年版兽药典质量标准

复方磺胺氯哒嗪钠粉Fufang Huang’an Lvdaqinna FenCompound Sulfachlorpyridazine Sodium Powder 本品为磺胺氯哒嗪钠、甲氧苄啶和蔗糖配制而成。
含磺胺氯哒嗪钠(C10H8ClN4NaO2S)应为标示量的90.0%~105.0%,含甲氧苄啶(C14H18N4O3)应为标示量的90.0%~110.0%.【处方】处方1 处方2磺胺氯哒嗪钠 100g 625g甲氧苄啶 25g 125g辅料适量适量100g 1000g【性状】本品为淡黄色粉末。
【鉴别】(1)取本品适量(约相当于甲氧苄啶1mg),置分液漏斗中,加0.4%氢氧化钠溶液5ml与三氯甲烷5ml,轻轻振摇,静置,分取三氯甲烷层,加稀硫酸5ml,振摇,加碘试液数滴,水层即生成黄褐色沉淀。
(2)在含量测定项下记录的色谱图中,供试品溶液两主峰的保留时间应与对照品溶液相应两主峰的保留时间一致。
(3)本品显方向第一胺类的鉴别反应(附录22页)。
【检查】粒度本品应全部通过二号筛,三号筛通过率不得少于70%。
水分取本品,照水分测定法(附录79页第一法A)测定,含水分不得过3.0%。
其他应符合粉剂项下有关的各项规定(附录13页)。
【含量测定】照高效液相色谱法(附录36页)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;以0.1%磷酸溶液-乙腈(90:18)为流动相,检测波长为230nm。
理论板数按甲氧苄啶峰计算不低于1600,甲氧苄啶峰与磺胺氯哒嗪钠峰的分离度应符合要求。
测定法取本品适量(约相当于磺胺氯哒嗪钠0.2g和甲氧苄啶40mg),精密称定,置100ml量瓶中,加水50ml,振摇使溶解,加甲醇稀释至刻度,摇匀;精密量取5ml,置50ml量瓶中,用流动相稀释至刻度,摇匀;精密量取20μl,注入液相色谱仪,记录色谱图;另取磺胺氯哒嗪钠对照品与甲氧苄啶对照品,同法测定。
按外标法以峰面积计算,即得。
sop氯化钠检验操作规程

1目的确定氯化钠检验的操作程序和方法,确保合格的氯化钠投入生产。
2适用范围适用于本厂质监科化验室对本厂生产所需的氯化钠的检验。
3责任化验员有责任按照本操作规程对生产所需的氯化钠进行检验、判定,并对检验结果负责。
4内容4.1性状本品为无色、透明的立方形结晶或白色结晶性粉末;无臭,味咸。
本品在水中易溶,在乙醇中几乎不溶。
4.2鉴别4.2.1钠盐4.2.1.1仪器铂丝、分析天平、试管、量筒、玻璃漏斗等。
4.2.1.2试液及配制醋酸氧铀锌试液:取醋酸氧铀10g,加冰醋酸5ml与水50ml,微热使溶解,另取醋酸锌30g,加冰醋酸3ml与水30ml,微热使溶解,将两液混合后,放冷,滤过,即得。
4.2.1.3操作a.取铂丝,用盐酸湿润后,蘸取供试品在无色火焰中燃烧,火焰即显鲜黄色。
b.取氯化钠1g,加水10ml溶解,再滴加醋酸氧铀锌试液,即产生黄色沉淀。
4.2.2氯化物第2页/共8页4.2.2.1仪器分析天平、量筒、试管、电炉等。
4.2.2.2试液及配制a.硝酸银试液取硝酸银1.75g,加水至100ml,使溶解,摇匀,即得。
b.氨试液取浓氨40ml,加水使成100ml,摇匀,即得。
c.碘化钾淀粉试纸取滤纸条浸入含有碘化钾0.5g的新制的淀粉指示液100ml中,湿透后,取出干燥,即得。
4.2.2.3操作A、取本品水溶液加硝酸使成酸性后,加硝酸银试液,即生成白色凝乳状沉淀;分离,沉淀加氨试液即溶解,再加硝酸,沉淀复生成。
B、取本品少量,置试管中,加等量的二氧化锰,混匀,加硫酸湿润,缓缓加热,即发生氯气,能使湿润的碘化钾淀粉试纸显蓝色。
4.3检查4.3.1酸碱度4.3.1.1仪器量筒、分析天平、容量瓶、刻度吸管等。
4.3.1.2试液及配制氐澳麝香草酚蓝指示液取澳麝香草酚蓝0.1g,加氢氧化钠液(0.05mol/L)3.2ml使溶解,再加水稀释至200ml,即得。
b.0.02mol/L氢氧化钠滴定液取0.1mol/L的氢氧化钠滴定液10ml,加水至50ml,摇匀,即得。
磺胺氯吡嗪钠可溶性粉

磺胺氯吡嗪钠可溶性粉本品为磺胺氯吡嗪钠与乳糖配制而成。
含磺胺氯吡嗪钠(C10H8C1N4NaO2S·H2O)应为标示量的90.0%~110.0%。
[处方][制法][性状]本品为淡黄色粉末。
[鉴别][检查]粒度500μm筛通过率应不少于90%。
溶解性取本品15g,加水100ml,搅拌,应全部溶解。
水分取本品约1.0g,精密称定,加无水甲醇20ml,密塞,振摇10分钟,照水分测定法(第一法)测定,含水分不得过2.1%。
有关物质取本品,加甲醇制成每1ml中含磺胺氯吡嗪钠10mg的溶液,置超声浴中超声助溶,静置,取上清液,作为供试品溶液,另取磺胺氯吡嗪钠对照品,加甲醇制成每1ml中含0.3mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各2μl,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲醇(3:1:1)为展开剂,展开后,晾干,将薄层板置于充满亚硝酸气体(用亚硝酸钠2g 加浓盐酸5ml产生)的密封容器中,5分钟后取出,室温下放置3~5分钟,喷以0.1%的盐酸萘乙二胺溶液,供试品溶液如显杂质斑点,其颜色与对照品溶液主斑点比较,不得更深。
装量按最低装量检查法检查,应符合规定。
[含量测定]取本品(约相当于磺胺氯吡嗪钠0.5g),精密称定,加水25ml 使溶解,加二甲替甲酰胺15ml,缓慢加入24%氢溴酸40ml,照电位滴定法,用亚硝酸钠滴定液(0.1mol/L)滴定,即得。
每1ml亚硝酸钠滴定液(0.1mol/L)相当于32.47mg的C10H8ClN4NaO2S·H2O。
[功能与主治]/[作用与用途]抗菌药。
用于治疗羊、鸡、兔球虫病(盲肠球虫),鸡霍乱及伤寒病。
[用法与用量]/[用法与判定]混饮每1L水肉鸡、火鸡300mg 混饲每1000kg饲料肉鸡、火鸡600mg 连用3天兔600mg, 连用5~10天内服每1kg 体重羊120mg 连用3~5天[注意事项]不得作饲料添加长期使用,产蛋期禁用。
磺胺氯吡嗪钠兽药原粉使用方法

【性 状】本品为类白色或淡黄色粉末,无臭。本品在水中易溶,在乙醇中 微溶。 【药理作用】本品主要与对氨基苯甲酸竞争二氢叶酸合成酶,防碍二氢叶酸 的合成最终影响核蛋白的合成,抑制球虫的生长与繁殖。作用峰期在感染后 的第4天。具有抗球虫、抗菌、控制肠道感染的双重功效。 【适 应 症】本品属磺胺类药物,具有性质稳定,抗菌谱较广,水溶性好等 优点。口服有效,并能很快分布至其它器官。主要用于抗球虫病。 【用法用量】混饲:每1000kg饲料,兔:加本品600g,连用5-10天,鸡: 加本品为600g,连用3天。 混饮:鸡每1L水加本品0.3g(即100kg水加本品30g), 连用3天。 【注意事项】1、不宜作饲料添加剂长期使用。 2、家禽用药不宜超过5天,以3天为宜。 3、作饮水给药时,不得与酸性药物同时使用,以免发生沉淀。 【规 格】按干燥品计算,含磺胺氯吡嗪钠不低于98% 【包 装】100g/袋X10袋/桶;10kg/桶
磺胺喹恶啉钠可溶性粉(成品)检验操作规程
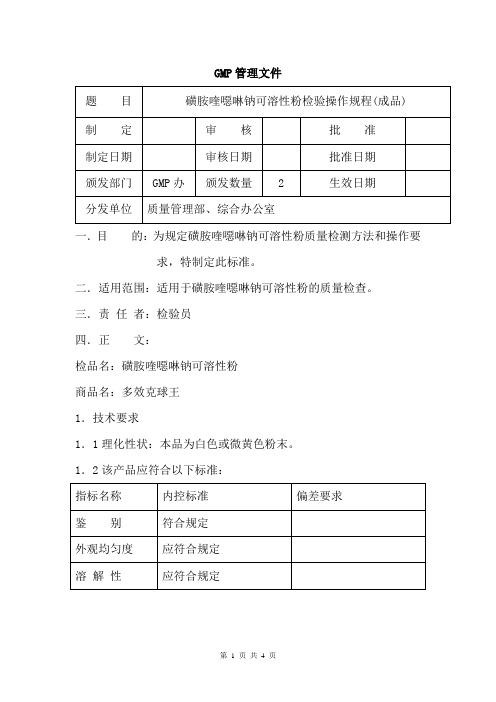
GMP管理文件一.目的:为规定磺胺喹噁啉钠可溶性粉质量检测方法和操作要求,特制定此标准。
二.适用范围:适用于磺胺喹噁啉钠可溶性粉的质量检查。
三.责任者:检验员四.正文:检品名:磺胺喹噁啉钠可溶性粉商品名:多效克球王1.技术要求1.1理化性状:本品为白色或微黄色粉末。
1.2该产品应符合以下标准:2.实验方法2.1鉴别:2.1.1试剂与溶液氢氧化钠溶液(0.01mol/L)2.1.2仪器与设备分光光度计2.1.3鉴别方法2.1.3.1取本品约1g,加水25ml溶解后,加醋酸2ml,即产生黄色沉淀;过滤,沉淀用水洗涤,在105℃干燥,照磺胺喹噁啉项下鉴别1、2项,试验,显相同的结果。
2.1.3.2本品的水溶液,显钠盐的鉴别反应。
2.2检查:2.2.1外观均匀度:取本品适量,平铺于光滑纸上,成5cm2,将表面压平,在亮的背景下观察,呈均匀色泽,无花纹与色斑。
2.2.2溶解性:取本品0.1g,,置纳氏比色管中,加水50ml,上下翻转10次,应全部溶解。
静置30分钟,无浑浊与沉淀产生。
2.2.3干燥失重:2.2.3.1仪器与用具:恒温干燥箱:温度在 105±2℃干燥扁形称量瓶:玻璃,带盖2.2.3.2测定方法:用干燥至恒重的称量瓶称取试样1g,准确至0.0002g,放入105±2℃的干燥箱中,打开称量瓶盖,干燥4小时。
盖好盖,放入干燥器中,冷却至室温,称量。
2.2.3.3结果的计算干燥失重百分含量=(m1-m2)/(m1-m)×100%式中:m1—样品与称量瓶干燥前重量m2—样品与称量瓶干燥后重量m—称量瓶干燥后重量2.2.4装量:2.2.4.1仪器与用具:干燥器:用氯化钙或硅胶作为干燥剂2.2.4.2测定方法取样品3个,清洗干净并在干燥器中干燥,称重,准确至0.1g。
除去内容物,将外包装清洗干净,干燥,称重,求出每个的装量及平均装量。
2.3含量测定;2.3.1仪器与设备:永停滴定仪、天平2. 3. 2试剂与溶液:亚硝酸钠滴定液见亚硝酸钠滴定液的配制与操作规程(0.1mol/L) 2.3.3测定方法取本品适量(约相当于磺胺喹噁啉钠0.5g),精密称定,加水20ml,溴化钾5g,溶解后,加甘油15ml,硫酸(1→2)20ml,照永停滴定法,用亚硝酸钠滴定液(0.1 mol/L)滴定,即得。
磺胺氯吡嗪102-65-8

据我们所知,此化学,物理和毒性性质尚未经完整的研究。
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
5 消防措施
5.1 灭火介质
火灾特征 无数据资料 灭火方法及灭火剂 用水雾,耐醇泡沫,干粉或二氧化碳灭火。
5.2 源于此物质或混合物的特别的危害
碳氧化物,氮氧化物,硫氧化物,氯化氢气体,钠的氧化物
无数据资料
10 稳定性和反应活性
10.1 反应性
无数据资料
10.2 化学稳定性
无数据资料
10.3 敏感性(危险反应的可能性)
无数据资料
10.4 避免接触的条件
无数据资料
10.5 不兼容的材料
强氧化剂
10.6 危险的分解产物
无数据资料
11 毒理学资料
11.1 毒理学影响的信息
急性毒性 无数据资料 亚 急性毒性 无数据资料 刺激性(总述) 无数据资料 皮肤腐蚀/刺激 无数据资料 严重眼损伤 / 眼刺激 无数据资料 呼吸道或皮肤过敏 无数据资料 生殖细胞诱变 无数据资料 致癌性 此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。 生殖毒性 无数据资料 特异性靶器官系统毒性(一次接触) 无数据资料 特异性靶器官系统毒性(反复接触) 无数据资料 潜在的健康影响
14.4 包裹组
欧洲陆运危规 : 无数据资料 国际海运危规 : 无数据资料 国际空运危规 : 无数据资料
14.5 环境危害
欧洲陆运危规 :否
国际海运危规 海运污染物 :否 国际空运危规 : 否
14.6 对使用者的特别预防
无数据资料
15 法规信息
15.1 专门对此物质或混合物的安全,健康和环境的规章 / 法规
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
GMP管理文件
一、目的:建立磺胺氯吡嗪钠可溶性粉检验的标准操作规程,保证正确操作。
二、依据:《磺胺氯吡嗪钠可溶性粉内控质量标准》。
三、适用范围:适用于磺胺氯吡嗪钠可溶性粉的检验。
四、责任者:QC检验员
五、正文:
1.检验项目和指标
2.检验方法:
除特别注明外,试验中所用试剂为分析纯试剂,水为纯化水,仪器设备为一般实验室仪器设备。
2.1 性状
取供试品5袋,肉眼在自然光下观察颜色,为淡黄色粉末,则判定该项合格。
2.2 鉴别
2.2.1 溶液与试剂:
甲醇
稀盐酸:取盐酸23.4ml,加水稀释至100ml,即得。
0.1mol/L亚硝酸钠溶液:取0.1mol/L亚硝酸钠滴定液,即得。
碱性β-萘酚试液:取β-萘酚0.25g,加氢氧化钠溶液(1→10)10ml使溶解,即得。
本液应临用新制。
2.2.2 方法:
(1) 取本品,加甲醇制成每1ml中含磺胺氯吡嗪钠1mg的溶液,作为供试品溶液;另取磺胺氯吡嗪钠对照品,加甲醇制成每1ml中含磺胺氯吡嗪钠1mg的溶液,作为对照品溶液。
吸取上述两种溶液各2μl,照有关物质项下的方法试验,供试品溶液所显主斑点的颜色与位置应与对照品溶液的主斑点相同。
(2)取本品约0.5g,加稀盐酸2ml使溶解,必要使缓缓煮沸使溶解,放冷,加0.1mol/L亚硝酸钠溶液数滴,滴加碱性β-萘酚试液数滴,视供试品不同,生成由橙黄到猩红色沉淀。
2.2.3 结果判定:上述(1)应符合规定,(2)应呈正反应,则判定该项合格。
2.3 溶解性:取本品15g,加水100ml,搅拌后应全部溶解。
则判定该项合格。
2.4 粒度:取本品,用500µm孔径筛检查,500µm孔径筛通过率不得少于90.0%。
则判定该项合格。
2.5 有关物质:取本品适量,加甲醇溶解并稀释成每1ml中含磺胺氯吡嗪钠10mg 的溶液,超声,取上清液,作为供试品溶液;精密量取供试品溶液适量,加甲醇稀释成每1ml中含磺胺氯吡嗪钠0.3mg的溶液,最为对照溶液。
照薄层色谱法(详见薄层色谱法标准操作规程)试验,吸取上述两种溶液各2µl,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲醇(3:1:1)为展开剂,展开,晾干。
将薄层板置于充满亚硝酸气体(用亚硝酸钠2g,加盐酸5ml产生)的密闭容器中,5分钟后取出,室温下放置3~5分钟,喷以0.1%盐酸萘乙二胺溶液,供试品溶液如显杂质斑点,其颜色与对照溶液的主斑点比较,不得更深。
则判定该项合格。
2.6 水分:取本品,照水分测定法(详见水分测定法第一法A标准操作规程)测定,含水分不得过2.0%。
则判定该项合格。
2.7 外观均匀度取本品适量置光滑纸上,平铺约5cm2,将其表面压平,在亮处观察,应呈现均匀的色泽,无花纹、色斑,则判定该项合格。
2.8 装量:照最低装量法(详见最低装量法标准操作规程)检查, 应为应为每袋装量98.0g-105.0g ,平均装量不少于标示量100g 。
则判定该项合格。
2.9 含量测定: 2.9.1 试剂和溶液 二甲基甲酰胺
氢溴酸溶液(1→2):取氢溴酸50ml 加水使成100ml 。
0.1mol/L 亚硝酸钠滴定液(详见滴定液配制及标定标准操作规程)
2.9.2 操作步骤:取本品(约相当于磺胺氯吡嗪钠0.5g ),精密称定,加水25使溶解,加二甲基甲酰胺15ml ,缓缓加入氢溴酸溶液(1→2)40ml ,照永停滴定法(详见永停滴定法标准操作规程),用亚硝酸钠滴定液(0.1mol/L )滴定。
每1ml 亚硝酸钠滴定液(0.1mol/L)相当于32.47mg 的C 10H 8ClN 4NaO 2S ·H 2O 。
2.9.3 计算公式 2.9.4 计算公式如下:
V :亚硝酸钠滴定液消耗毫升数; F :亚硝酸钠滴定液实际浓度; T :滴定度32.47; M :取供试品的重量。
相对偏差=%+-100
B A B
A 2.9.5 结果判定:供试品含量为标示量的92.0~110.0%,相对偏差不得过0.3%,则判定该项合格。
3.验收规则
3.1 本品由质量检验部门检验,转入合格品贮藏区和出厂的本品均应符合内控质量标准,每批出厂的本品都应附有产品合格证。
3.2 如果在检验中有一项指标不符合内控质量标准时,质量检验部门应重新抽样,产品重新检验结果只要有一项不符合厂内定的质量标准时,则整批判为不合格。
×100%。
