2016中考化学知识精细梳理--解推断题必备“题眼”集锦
初三化学推断题知识点大全

州理科、县全能竞赛推断题知识点一、推断题所用到的化学方程式:1、3Fe+2O 2==Fe 3O 42、Fe 2O 3+3CO =====高温2Fe +3CO 2 3、Fe+CuSO 4═FeSO 4+Cu 4、2Fe 2O 3+3C 4Fe+3CO 2↑5、Fe 2O 3+3H 2 ==2Fe+3H 2 O6、Fe + H 2SO 4 = FeSO 4 + H 2↑7、Fe + 2HCl =FeCl 2 + H 2↑ 8、Fe 2O 3 + 6HCl =2FeCl 3 + 3H 2O9、Fe 2O 3 + 3H 2SO 4 = Fe 2(SO 4)3 + 3H 2O 1、C+O 2==CO 2 2、CO 2+C =====高温2CO 3、2C+O 2(不足)==2CO 4、2CO+O 22CO 2 5、CO 2+Ca (OH )2═CaCO 3↓+H 2O 6、CaCO 3=====高温 CaO+CO 2↑7、CaO+ H 2O ==Ca (OH )2 8、Na 2CO 3+ Ca (OH )2═CaCO 3↓+2Na OH 9、2NaOH + CO 2 = Na 2CO 3 + H 2O 10、Na 2CO 3 + 2HCl = 2NaCl + H 2O + CO 2↑11、 12、CO+CuO =====高温Cu+ CO 213、H 2 +CuO == Cu + H 2O 14、2H 2O2H 2↑+O 2↑ 15、CuSO 4+2NaOH ═Na 2SO 4+Cu (OH )2↓ 16、CuO + 2HCl =CuCl 2 + H 2O17、CuO + H 2SO4 =CuSO 4 + H 2O 18、2Mg+O 2=2MgO (白色) 19、2Cu+O 2== 2CuO (黑色)1、H 2SO 4 + BaCl 2 ===BaSO 4 ↓+ 2HCl2、H 2SO 4+2NaOH═Na 2SO 4+2H 2O3、BaCl 2+ Na 2SO 4==Ba SO 4↓+ 2NaCl4、NaOH +HCl==NaCl +H 2O5、Zn +H 2SO 4===ZnSO 4+H 2↑6、Na 2CO 3+2HCl===NaCl +H 2O +CO 2↑7、CaCl 2+ Na 2CO 3==Ca CO 3↓+ 2NaCl 8、CaCl 2+ Na 2SO 4==Ca SO 4↓+ 2NaCl9、BaCl 2+ Na 2CO 3==Ba CO 3↓+ 2NaCl 10、NH 4H CO 3NH 3↑+H 2O +CO 2↑ 11、2NaHCO 3Na 2CO 3+H 2O +CO 2↑ 12、Cu 2(OH)2CO 3 2CuO+ H 2O +CO 2↑ 13、2NaOH + CO 2 = Na 2CO 3 + H 2O最后两点知识:①根据金属活动性顺序判断是否符合客观事实;②根据复分解反应定义判断是否符合客观事实。
初三化学推断题知识点总结

初三化学推断题知识点总结在初三化学学习中,推断题是常见的考查形式之一。
它要求学生根据提供的实验现象、化学反应或观察结果,推断出相应的物质、条件或过程。
以下将总结初三化学推断题的一些常见知识点,帮助学生在解题过程中更加得心应手。
1. 酸碱中和反应推断酸碱中和反应是化学反应的一种常见类型。
在推断题中,根据实验现象,可以根据酸碱指示剂的变化来推断酸碱中和反应的发生。
常见的酸碱指示剂有酚酞、甲基橙、溴酸铵等。
例如,如果实验中某种指示剂从红色变成橙色,表明反应溶液中酸性物质被中和。
2. 钢铁和空气中氧气的反应推断钢铁与空气中的氧气发生反应产生铁锈是初中化学中的常见现象。
根据实验现象,可以推断出这一反应是一种氧化反应。
如果实验材料表面出现红色的铁锈,就可以判断钢铁与空气中的氧气反应生成了一种氧化物。
3. 金属和酸的反应推断金属与酸反应也是初中化学中常见的实验现象。
根据观察结果,可以推断出金属与酸反应生成了相应的盐和气体。
例如,实验中发现金属片溶解产生气泡,并有酸性气味时,可以判断金属与酸反应生成了相应的盐和气体。
4. 酸与金属碱反应推断酸与金属碱反应也是推断题中常见的内容。
通过观察反应现象,可以推断出酸与金属碱反应生成了相应的盐和水。
如果实验中观察到溶液变得中性,并有少量白色沉淀生成,就可以推断出酸与金属碱反应产生了相应的盐和水。
5. 燃烧反应推断燃烧反应是初中化学中的重要内容。
根据观察燃烧现象,可以推断出反应物是燃烧物质。
例如,实验中观察到可燃物质燃烧时产生火焰和烟雾,并释放了大量的热量,可以推断出反应物是一种燃烧物质。
6. 氧化还原反应推断氧化还原反应是化学反应中一种重要的类型。
在推断题中,可以根据观察到的颜色变化、气体的产生、电流的流动等现象来判断是否发生了氧化还原反应。
例如,实验中观察到某个物质从蓝色变成棕色,并伴随着气泡的产生,可以推断出反应中发生了氧化还原反应。
7. 离子交换反应推断离子交换反应是指两种离子在溶液中发生交换的反应。
初中化学推断题常用“题眼”归纳

初中化学推断题常用“题眼”归纳初中化学推断题常用的“题眼”可以归纳为以下几个方面:溶液颜色、火焰颜色、常见气体、常见固体、元素之最等。
比如,含Cu2+的溶液通常呈现蓝色,如CuSO4、Cu(NO3)2等;含Fe2+的溶液通常呈现浅绿色,如FeCl2、Fe(NO3)2、FeSO4等;含Fe3+的溶液通常呈现黄色,如FeCl3、Fe(NO3)3、Fe2(SO4)3等;KMnO4溶液呈现紫红色;H2S气体呈现淡蓝色,CO、CH4呈现蓝色,S在氧气中呈现蓝紫色;O2、N2、H2、CO、CO2、CH4等气体无色无味,而SO2、NH3、HCl等则有刺激性气味。
常见的固体有黄色硫磺(S)、暗紫色高锰酸钾(KMnO4)、碘(I2)、铜绿(Cu2(OH)2CO3)、Cu(OH)2沉淀、Fe(OH)3沉淀、Cu、赤铁矿、铁锈主要成分(Fe2O3)、红磷(P)、Fe3O4、FeO、CuO、MnO2、C粉等。
常见的白色沉淀有CaCO3、BaCO3、Mg(OH)2(可溶于酸)和BaSO4、AgCl(不溶于酸)等。
在元素之最方面,地壳(人体)中含量最多的非金属元素是氧(O),含量最多的金属元素是铝(Al),人体中含量最多的金属元素是钙(Ca),形成化合物最多的元素是碳(C)。
一些常用的化学物质包括:O2和CO2等气体,CaO和Ca(OH)2等石灰,生石灰和纯碱等。
值得注意的是,有些化学物质的使用需要特别小心,比如NaOH(烧碱、火碱、苛性钠)和Hg(水银)等。
气体的命名方式有很多种,如沼气、瓦斯、天然气等。
酒精等一些物质也有俗称。
气体成分的检验时,应先检验水蒸气,再检验其他气体。
其中,无水硫酸铜可检验H2O,铜可检验O2,石灰水可检验CO2.H2和CO可先转化后检验。
气体除杂时,应先除去其他气体,最后除去水蒸气。
无水硫酸铜、无水氯化钙和碱石灰可吸收水蒸气和CO2,氧化铜和碳粉可转化CO2,铜可吸收氧气,浓硫酸和氢氧化钠溶液可吸收水蒸气和CO2,碳酸钠或碳酸氢钠溶液可转化CO2中的HCl。
(完整版)初中化学推断题常用归纳

初中化学推断题常用“题眼”归纳突破口1.以物质特征颜色为突破口⑴固体颜色:Fe、C、CuO、MnO2、Fe3O4(黑色);Cu、Fe2O3(红色);Cu2(OH)2CO3(绿色);CuSO4·5H2O(蓝色)。
⑵溶液颜色:CuCl2、CuSO4(蓝色);FeCl2、FeSO4(浅绿色);FeCl3、Fe2(SO4)3(黄色)。
⑶火焰颜色:S在O2中燃烧(蓝紫色);S、H2在空气中燃烧(淡蓝色);CO、CH4在空气中燃烧(蓝色)。
⑷沉淀颜色:BaSO4、AgCl、CaCO3、BaCO3(白色);Cu(OH)2(蓝色);Fe(OH)3(红褐色)。
2.以物质特征状态为突破口常见固体单质有Fe、Cu、C、S;气体单质有H2、N2、O2;无色气体有H2、N2、O2、CO、CO2、CH4、SO2;常温下呈液态的物质有H2O。
3.以物质特征反应条件为突破口点燃(有O2参加的反应);通电(电解H2O);催化剂(KCIO3分解制O2);高温(CaCO3分解,C、CO还原CuO、Fe2O3);加热(KCIO3、KMnO4、Cu2(OH)2CO3等的分解,H2还原CuO、Fe2O3)。
4.以物质特征现象为突破口⑴能使澄清石灰水变浑浊的无色无味气体是CO2。
⑵能使黑色CuO变红(或红色Fe2O3变黑)的气体是H2或CO,固体是C。
⑶能使燃烧着的木条正常燃烧的气体是空气,燃烧得更旺的气体是O2,熄灭的气体是CO2或N2;能使带火星的木条复燃的气体是O2。
⑷能使白色无水CuSO4粉末变蓝的气体是水蒸气。
⑸在O2中燃烧火星四射的物质是Fe。
⑹在空气中燃烧生成CO2和H2O的物质是有机物,如CH4、C2H5OH等。
⑺能溶于盐酸或稀HNO3的白色沉淀有CaCO3、BaCO3;不溶于稀HNO3的白色沉淀有AgCl、BaSO4。
5.以元素或物质之最为突破口⑴地壳中含量最多的元素是O,含量最多的金属元素是AI。
⑵人体中含量最多的元素是O。
初中化学推断题常用“题眼”归纳——基础知识梳理.doc

初中化学推断题常用“题眼”归纳——基础知识梳理 固体颜色 里侄 八、、1 i 磁铁矿 Fe 304> Cu0、Mn02. C 粉、Fe 粉红色Cu 、赤铁矿、铁锈主要成分(FeA ) >红磷(P ) 绿色Cu 2(0II)2C03 (铜绿) 黄色硫磺(S ) 紫黑色高镒酸钾(KMnOJ 溶液颜色 蓝色CuSO,、Cu (NO) 2等含 Cu”的溶液 浅绿色FeCl 2> Fe(N03)2. FeSO 4 等含 Fe*'的溶液 黄色FeCL 、Fe(N03)3> Fe 2(S04) 3等含 Fe"溶液 紫红色KMnO 4溶液 火焰颜色 淡蓝色用、S (空气中) 蓝色co 、CH 4 蓝紫色s (氧气中) 沉淀颜色 蓝色沉淀Cu(0II)2 红褐色沉淀Fe(0II)3 白色沉淀(可溶于酸)C&CO3、Bag 、Mg (OH) 2白色沉淀(不溶于酸)BaS04> AgCl常见气体无色无味O2、应、&、CO 、CO2、CH 4 有刺激性气味 SO2、NH3、HC1 常见液体 H 2O , H 2O 2元素之最 1. 地壳(人体)中含量最多的非金属元素是氧(0)2. 地壳中含量最多的金属元素是铝(A1)3. 人体中含量最多的金属元素是钙(Ca )4. 形成化合物最多的元素是碳(C )质的相对分子质Ca (OH) 2-一些物质的俗称Hg-水银;1.使带火星木条复燃的气体是2.使澄清石灰水变浑浊的气体是CO”但通入CO2后变浑浊的溶液不一定是澄清石灰水,也可以是Ba (OH)2溶液。
3.最简单的有机物是甲烷CH」4.天然最硬的物质是金刚石(C)5.吸水后由白变蓝的是无水CuS046.最常见的液态物质是也0、相对分子质量最小的氧化物是凡07.常用的食品干燥剂是生石灰CaO8.常用的食品脱氧剂是Fe粉9.与峻反应有COa产生的物质是碳酸盐(或NaIIC03)10.与碱反应(研磨)有NH3产生的物质是铉盐(铉态氮肥)11.常温下唯一有氨味的铉态氮肥是NH4HCO3(碳铉)H20-18; CO厂44; CaC03-100; HC1-36. 5; H2S0-98; Na0H-40;NaOH-烧碱、火碱、苛性钠;Na2C0:-纯碱、苏打;NaHCO:-小苏打;CO?-干冰;CaO-生石灰;Ca(0H)2-熟石灰、消石灰;CaC03-石灰-些常用物石、大理石;CH厂沼气、瓦斯、天然气;C2H5OH-酒精。
(完整版)初中化学推断题常用“题眼”归纳

初中化学推断题常用“题眼”归纳1.以物质特征颜色为突破口⑴ 固体颜色:Fe、C、CuO、MnO2、Fe3O4(黑色);Cu、Fe2O3(红色);Cu2(OH)2CO3(绿色);CuSO4·5H2O(蓝色)。
⑵ 溶液颜色:CuCl2、CuSO4(蓝色);FeCl2、FeSO4(浅绿色);FeCl3、Fe2(SO4)3(黄色)。
⑶ 火焰颜色:S在O2中燃烧(蓝紫色);S、H2在空气中燃烧(淡蓝色);CO、CH4在空气中燃烧(蓝色)。
⑷ 沉淀颜色:BaSO4、AgCl、CaCO3、BaCO3(白色);Cu(OH)2(蓝色);Fe(OH)3(红褐色)。
2.以物质特征状态为突破口常见固体单质有Fe、Cu、C、S;气体单质有H2、N2、O2;无色气体有H2、N2、O2、CO、CO2、CH4、SO2;常温下呈液态的物质有H2O。
3.以物质特征反应条件为突破口点燃(有O2参加的反应);通电(电解H2O);催化剂(KCIO3分解制O2);高温(CaCO3分解,C、CO还原CuO、Fe2O3);加热(KCIO3、KMnO4、Cu2(OH)2CO3等的分解,H2还原CuO、Fe2O3)。
4.以物质特征现象为突破口⑴ 能使澄清石灰水变浑浊的无色无味气体是CO2。
⑵ 能使黑色CuO变红(或红色Fe2O3变黑)的气体是H2或CO,固体是C。
⑶ 能使燃烧着的木条正常燃烧的气体是空气,燃烧得更旺的气体是O2,熄灭的气体是CO2或N2;能使带火星的木条复燃的气体是O2。
⑷ 能使白色无水CuSO4粉末变蓝的气体是水蒸气。
⑸ 在O2中燃烧火星四射的物质是Fe。
⑹ 在空气中燃烧生成CO2和H2O的物质是有机物,如CH4、C2H5OH等。
⑺ 能溶于盐酸或稀HNO3的白色沉淀有CaCO3、BaCO3;不溶于稀HNO3的白色沉淀有AgCl、BaSO4。
5.以元素或物质之最为突破口⑴ 地壳中含量最多的元素是O,含量最多的金属元素是AI。
中考化学推断题题眼归纳

中考化学推断题题眼归纳推断题可以全面地考查同学们的逻辑思维能力和分析推理能力,是历年中考常考题型。
解答推断题的关键是要抓住“题眼”,即找到突破口,然后“顺藤摸瓜”,进行顺推、逆推等严密推理后,才能顺利解题。
现将初中化学中可作“题眼”的知识小结如下,供同学们复习时参考。
一、抓住物质的特征颜色1. 固态物质的颜色红色:32O Fe Cu 、 黄色:S 蓝色:O H 5CuSO 24⋅ 绿色:322CO )OH (Cu 黑色:43O Fe C 、、CuO 、、2MnO 铁粉 2. 溶液的颜色蓝色溶液:含+2Cu 的盐溶液。
如:2CuCl 溶液、4CuSO 溶液、23)NO (Cu 溶液。
浅绿色溶液:含+2Fe 的盐溶液。
如:2FeCl 溶液、4FeSO 溶液、23)NO (Fe 溶液。
黄色溶液:含+3Fe 的盐溶液。
如:3FeCl 溶液、342)SO (Fe 溶液、33)NO (Fe 溶液。
3. 沉淀的颜色(1)不溶于水也不溶于稀硝酸的白色沉淀:AgCl 、4BaSO 。
(2)不溶于水但能溶于酸,且有气泡产生的白色沉淀:3CaCO 、3BaCO 。
(3)不溶于水但能溶于酸,且无气泡产生的白色沉淀:2)OH (Mg 、3)OH (Al 。
(4)不溶于水的蓝色沉淀:2)OH (Cu 。
(5)不溶于水的红褐色沉淀:3)OH (Fe 。
4. 火焰的颜色蓝紫色:硫在氧气中燃烧。
淡蓝色:S OH H C CH CO H 5242、、、、在空气中燃烧。
二. 抓住物质的特性1. 常见气体的特性(1)能使带火星的木条复燃是氧气的特性。
(2)能使澄清石灰水变浑浊的无色无味气体是二氧化碳。
(3)溶于水呈碱性,且能使湿润的红色石蕊试纸变蓝是氨气的特性。
(4)在空气中燃烧产生淡蓝色火焰,且燃烧产物仅为水是氢气的特性。
(5)能使人煤气中毒的气体是一氧化碳。
(6)具有刺激性气味的大气污染物是二氧化硫。
2. 常见离子的特性(1)与硝酸银溶液反应产生既不溶于水也不溶于酸的白色沉淀是-Cl 的特性。
初三化学推断题专题复习以及必背知识
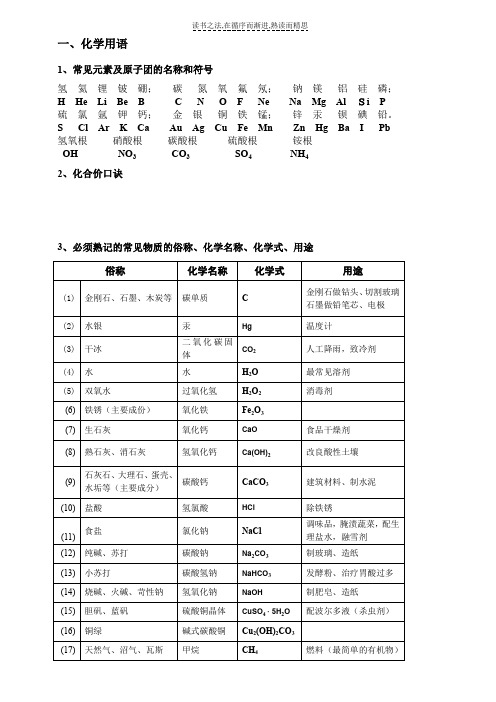
一、化学用语1、常见元素及原子团的名称和符号氢氦锂铍硼;碳氮氧氟氖;钠镁铝硅磷;H He Li Be B C N O F Ne Na Mg AlSi P 硫氯氩钾钙;金银铜铁锰;锌汞钡碘铅。
S Cl Ar K Ca Au Ag Cu Fe Mn Zn Hg Ba I Pb 氢氧根硝酸根碳酸根硫酸根铵根OH NO3CO3SO4 NH42、化合价口诀3、必须熟记的常见物质的俗称、化学名称、化学式、用途俗称化学名称化学式用途(1)金刚石、石墨、木炭等碳单质 C 金刚石做钻头、切割玻璃石墨做铅笔芯、电极(2)水银汞Hg温度计(3)干冰二氧化碳固体CO2人工降雨,致冷剂(4)水水H2O 最常见溶剂(5)双氧水过氧化氢H2O2消毒剂(6) 铁锈(主要成份)氧化铁Fe2O3(7) 生石灰氧化钙CaO食品干燥剂(8) 熟石灰、消石灰氢氧化钙Ca(OH)2改良酸性土壤(9) 石灰石、大理石、蛋壳、水垢等(主要成分)碳酸钙CaCO3建筑材料、制水泥(10) 盐酸氢氯酸HCl除铁锈(11) 食盐氯化钠NaCl调味品,腌渍蔬菜,配生理盐水,融雪剂(12) 纯碱、苏打碳酸钠Na2CO3制玻璃、造纸(13) 小苏打碳酸氢钠NaHCO3发酵粉、治疗胃酸过多(14) 烧碱、火碱、苛性钠氢氧化钠NaOH制肥皂、造纸(15) 胆矾、蓝矾硫酸铜晶体CuSO4 · 5H2O配波尔多液(杀虫剂)(16) 铜绿碱式碳酸铜Cu2(OH)2CO3(17) 天然气、沼气、瓦斯甲烷CH4燃料(最简单的有机物)(18) 酒精乙醇C2H5OH燃料、乙醇汽油(19) 醋酸乙酸CH3COOH调味品(20) 氨水氢氧化铵NH4OH或NH3·H2O氮肥4、必须熟记的化学方程式九年级化学方程式分类:1.碳充分燃烧: C+O2点燃CO22.碳不充分燃烧: 2C+O2点燃2CO3.一氧化碳燃烧: 2CO+O2点燃2CO24.产生一氧化碳: C+CO2高温2CO5.硫燃烧: S+O2点燃SO26.红磷燃烧: 4P+5O2点燃2P2O57.氢气燃烧: 2H2+O2点燃2H2O8.铁燃烧: 3Fe+2O2点燃Fe3O49.镁燃烧: 2Mg+O2点燃2MgO 10.铝燃烧: 4Al+3O2点燃2Al2O311.甲烷燃烧: CH4+2O2点燃CO2+2H2O12.酒精燃烧: C2H5OH+3O2点燃2CO2+3H2O13.呼吸原理: C6H12O6+6O2酶6CO2+6H2O14.高锰酸钾制氧气: 2KMnO4△K2MnO4+MnO2+O2↑15.氯酸钾制氧气: 2KClO3MnO22KCl+3O2↑16.过氧化氢制氧气: 2H2O2 MnO2 2H2O +O2↑17.水通电分解: 2H2O通电2H2↑+O2↑18.氧化汞分解: 2HgO△2Hg+O2↑19.实验室制氢气的原理:Zn+H2SO4=ZnSO4+H2↑20.镁或硫酸性质:Mg+H2SO4=MgSO4+H2↑21.铁或硫酸性质:Fe+H2SO4=FeSO4+H2↑22.铝或硫酸性质:2Al+3H2SO4=Al2(SO4)3+H2↑23.镁或盐酸性质:Mg+2HCl=MgCl2+H2↑24.锌或盐酸性质:Zn+2HCl=ZnCl2+H2↑25.铁或盐酸性质:Fe+2HCl=FeCl2+H2↑26.铝或盐酸性质:2Al+6HCl=2AlCl3+3H2↑△27.酸或碱的性质:NaOH+HCl=NaCl+H2O28.酸或碱的性质:Ca(OH)2+2HCl=CaCl2+H2O29.酸或碱的性质:2NaOH+H2SO4=Na2SO4+2H2O30.酸或碱的性质:Ca(OH)2+H2SO4=CaSO4+2H2O31.除铁锈的原理或金属氧化物与酸的性质:Fe2O3+6HCl=2FeCl3+3H2O Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、32.碳酸盐或酸的性质:Na2CO3+2HCl=2NaCl+CO2↑+H2O33.治疗胃酸过多症的原理:NaHCO3 +HCl=NaCl+CO2↑+H2O34.氯化钠与硝酸银反应产生白色沉淀:NaCl+AgNO3=NaNO3+AgCl↓35.制取氢氧化钠的原理:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH36.氢氧化钠与硫酸铜反应产生蓝色沉淀:2NaOH+CuSO4=Na2SO4+Cu(OH)237.制取水煤气的原理:C+H2O高温H2+CO38.氢气还原氧化铜:H2+CuO△Cu+H2O39.碳还原氧化铜:C+2CuO高温2Cu+CO2↑40.一氧化碳还原氧化铜:CO+CuO△Cu+CO241.氢气还原氧化铁:Fe2O3+3H2高温2Fe+3H2O42.碳还原氧化铁:2Fe2O3+3C高温4Fe+3CO2↑43.工业炼铁的原理:Fe2O3+3CO高温2Fe+3CO244.铁置换硫酸铜中的铜:Fe+CuSO4=Cu+FeSO445.铜置换硝酸银中的银:Cu+2AgNO3=2Ag+Cu(NO3)246.铝置换硫酸铜中的铜:2Al+3CuSO4=3Cu+Al2(SO4)347.生石灰制熟石灰:H2O+CaO=Ca(OH)248.碳酸不稳定:H2CO3=H2O+CO2↑49.工业制生石灰的原理:CaCO3高温CaO+CO2↑50.检验CO2或澄清石灰水变浑浊原理:CO2+Ca(OH)2=CaCO3↓+H2O51.烧碱变质的原理:CO2+2NaOH=Na2CO3+H2O52.碱与非金属氧化物的性质:SO2+2NaOH=Na2SO3+H2O SO3+2NaOH=Na2SO4+H2O53.非金属氧化物的性质:H2O+CO2 =H2CO3 H2O+SO2 =H2SO3 H2O+SO3 =H2SO454.制取CO2或CaCO3 作补钙药剂:CaCO3+2HCl=CaCl2+CO2↑+H2O二、常见酸、碱、盐的溶解性口诀最常见六种难溶于水的碱和盐:CaCO3、BaCO3、BaSO4、AgCl均为白色沉淀,Cu(OH)2蓝色沉淀,Fe(OH)3红褐色沉淀。
2016年中考化学推断题技巧整理和题型归纳大全

专题复习推断题一、解题的一般思路找到突破口进行联想,联系所学的相关知识,一半猜一半代,顺藤摸瓜,然后逐一突破。
推断题题干中的信息千丝万缕、错综复杂,真正是“剪不断,理还乱,太难求,别有一番滋味在心头”。
所以造成了高失分的现象,对好多学生来说是一道难以逾越的难关。
解推断题就好比是公安人员侦破案情,要紧抓蛛丝马迹,并以此为突破口,顺藤摸瓜,最终推出答案。
1.审题:认真审读原理,弄清文意和图意,理出题给条件,深挖细找,反复推敲。
2.分析:抓住关键,找准解题的突破口,突破口也称为“题眼”,指的是关键词、特殊现象、物质都特征等等,然后从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果。
3.解答:根据题目的要求,按照分析和推理的结果,认真而全面地解答。
4.检验:得出结论后切勿忘记验证。
其方法是将所得答案放回原题中检验,若完全符合,则说明答案正确。
二、解题方法1、顺推法2、逆推法3、分层法4、剥离法三、常见题型:1、文字叙述型;2、方程式叙述型;3、框图型;4、连线型;5、表格型。
四、常见突破口1.以物质特征颜色为突破口⑴固体颜色:(黑色)、、、、;(红色)红棕色、紫红色、红磷;⑵溶液颜色:(蓝色)(浅绿色)(黄色)⑶燃烧火焰颜色:(蓝紫色)(淡蓝色)(蓝色)(明亮的蓝色)⑷沉淀颜色:能溶于盐酸或稀HNO3的沉淀:(5个白色)、、、、(蓝色)(红褐色)不溶于稀HNO3的白色沉淀有、。
2.以物质特征反应条件为突破口(写学过涉及的化学方程式)点燃(有O2参加的反应)通电催化剂高温加热3.以物质特征现象为突破口⑴能使澄清石灰水变浑浊的无色无味气体是。
⑵还原性物质:能使黑色CuO变红的气体为或,固体为⑶能使燃烧着的木条正常燃烧的气体是空气,燃烧得更旺的气体是,熄灭的气体是CO2或N2;能使带火星的木条复燃的气体是。
(4)在O2中燃烧火星四射的物质是,在O2中燃烧耀眼白光的物质是。
初中化学推断题知识汇总,初中化学推断题答题技巧

推断题是中考化学试题中常见的一种题型,既考查知识,又考查能力,具有考查知识面广、综合性强、难度大等特点。
很多同学面对这种题的时候都会出现无从下手的感觉,其实就是因为“题眼”太难找到,只要学会找“题眼”,就能顺藤摸瓜找到答案。
题眼一般是物质颜色、状态、用途、反应现象、组成、分类、反应条件、俗名、相互转化等,所以,在复习中,要善于积累,善于归纳总结。
今天给大家整理推断题的相关内容:
一、颜色
(1)固体颜色
(2)溶液颜色
(3)沉淀颜色
二、气体的特征
三、物质俗称
四、物质用途
五、反应条件
反应条件是通电的——电解水
反应条件是高温的——CaCO3分解、CO和C炼铁,还原氧化铜等
反应条件是催化剂的——过氧化氢分解制氧气、氯酸钾加热制氧气六、物质的组成元素相同的
固体:四氧化三铁和三氧化二铁
液体:水和双氧水
气体:CO2和CO
河南天星教育一家致力于教育图书出版及提供教育信息服务的文化教育机构,1998年成立至今始终在“为优质教育资源的普及不懈努力”。
公司目前业务范围涵盖教辅书出版、课外书出版、数字出版等领域,产品覆盖小初高K12学段,图书品类包含讲解、练习、中考备考、高考备考、课外阅读等类别,《金考卷》《试题调研》《教材帮》《一遍过》《疯狂阅读》读者遍布全国,得到了市场和用户的广泛好评。
可在京东、天猫、当当搜索“天星教育旗舰店”查看、购买图书。
2016年中考化学推断题

初中化学推断题100题(后附答案及解析)(本题集中了近年来各地中考精粹,由名师作答并解析,是一份难得的专题训练!)1.下列物质均由C、Na、Cl、O、H、Ca六种元素中的两种或三种组成。
根据要求回答问题:(1)上述元素中属于金属元素的是。
(2)胃液中含有的酸(写化学式,下同);能做为燃料的无机化合物。
(3)A、B、C、D、E、F、G、H是初中化学常见的物质,其转化关系如图所示。
写出反应①、③的化学方程式、;属于复分解反应的有(填数字序号)。
2.从铜、氧化铜的混合粉末中回收铜的具体流程如下:回答下列问题:(1)操作1是。
(2)滤液Ⅰ中加入过量铁粉所发生的反应的化学方程式是。
(3)试剂A的作用是。
(4)此实验过程中,下列哪些做法会导致回收到的Cu不纯A.往混合粉末中加入的稀H2SO4不足B.往滤液Ⅰ中加入铁粉不足C.往滤渣Ⅱ中加入试剂A不足(5)请写出铜的一种用途:。
3.不同类别的物质间存在着一定的关系,如图1、图2所示。
(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质。
)(1)碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图1所示,回答下列问题: ①乙物质是 ,它的一种用途是 。
②写出“乙→丙”的化学方程式 。
(2)图2能体现某些物质间变化关系的是 。
(填标号)4.已知A 、B 、C 、D 、E 分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液 、氧化铁和一氧化碳中的一种,E 是实验室一种常见溶液,它们之间的关系如图所示,“——”两端的(1)C 的一种用途是 ;D 、E 反应的化学方程式为 。
(2)上述各物质间的反应均可用“甲+乙→丙+丁”表示,其中不属于四种基本反应类型,但能用上式表示的一个化学方程式是 。
(3)若B 、C 、D 、E 都不变,五种物质之间的关系也不变,A 还可能是 _。
5.(12分)利用海水(含氯化钠、氯化镁)处理含二氧化硫废气的方法如下:Ⅰ.海水处理流程:(1)写出生成Mg(OH)2沉淀的化学反应方程式 ;(2)经操作a 得到的Mg(OH)2沉淀需要洗净,为证明是否洗净,可取洗涤液少量,向其中加入下列试剂中的 ,即可达到实验目的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2016中考化学知识精细梳理--解推断题必备“题眼”集锦
类型一:以物质的特征颜色为突破口
1.固体颜色
(1)黑色固体(5种):Fe(粉)、C粉、__CuO__、MnO
2、__Fe
3
O
4
__。
(2)红色固体(2种):__Fe
2O
3
__、P(红磷)。
(3)紫红色固体:__Cu__。
2.三种溶液颜色
(1)蓝色溶液:CuCl
2、__CuSO
4
__、__Cu(NO
3
)
2
__。
(2)浅绿色溶液:__FeCl
2__、__Fe(NO
3
)
2
__、FeSO
4。
(3)黄色溶液:__FeCl
3__、Fe(NO
3
)
3
、Fe
2
(SO
4
)
3。
3.沉淀颜色
(1)有色沉淀:蓝色沉淀__Cu(OH)
2__、红褐色沉淀__Fe(OH)
3
__。
(2)白色沉淀(7个):BaSO
4、AgCl、CaCO
3
、BaCO
3
、Ag
2
CO
3
、Mg(OH)
2
、Al(OH)
3。
①其中不溶于稀硝酸的白色沉淀(2个):__BaSO
4
、AgCl__;
②溶于酸并有气体放出的白色沉淀(3个):__CaCO
3__、__Ag
2
CO
3
__、BaCO
3
;
③溶于酸但没有气体放出的白色沉淀(2个):__Mg(OH)
2__、Al(OH)
3。
类型二:以“反应的特征现象”为突破口
1.能使澄清石灰水变浑浊的无色无味气体是__CO
2
__。
2.能使黑色CuO变红(或红色Fe
2O
3
变黑)的气体是H
2
或CO,固体是__C__。
3.能使燃着的木条正常燃烧的气体是空气,燃烧更旺的气体是__O
2
__,使
火焰熄灭的气体是CO
2或__N
2
__;能使带火星的木条复燃的气体是__O
2
__。
4.在O
2
中燃烧火星四射的物质__Fe__。
5.在O
2
中燃烧发出耀眼的白光的物质是Al、__Mg__。
6.在空气中燃烧生成水和二氧化碳的物质是__有机物__,如CH
4、C
2
H
5
OH等。
7.溶于水呈碱性的是__NH
3
__。
类型三:以元素或物质之最为突破口
1.化学元素、微粒
(1)地壳中含量最多的元素__O__。
(2)形成化合物最多的元素__C__。
(3)地壳中含量最多的金属元素__Al__。
(4)人体中含量最多的元素是__O__。
空气中含量最多的元素是__N__。
2.常见化学物质
(1)最理想的清洁燃料__H
2
__。
(2)最简单的有机物__CH
4
__。
(3)最常用的溶剂__H
2
O__。
(4)人体中含量最多的物质__H
2
O__。
(5)空气中含量最多的气体__N
2
__。
(6)相对分子质量最小的有机物__CH
4
__。
(7)自然界中硬度最大的物质__金刚石__。
(8)相对分子质量最小、密度最小的气体__H
2
__。
(9)当今世界上最重要的三大矿物燃料__煤__、__石油__、__天然气__。
类型四:以物质的用途为突破口
1.用于医疗急救中供给呼吸且能支持燃烧的是__O
2
__。
2.可作为生产氮肥的原料、食品保护气的是__N
2
__。
3.用作电极、制铅笔芯的是__石墨__。
4.用作玻璃刀刀头、钻探机钻头的是__金刚石__。
5.用作灭火、制冷剂、人工降雨和气体肥料的是
__CO
2
__。
6.引起温室效应、光合作用的主要原料的是__CO
2
__。
7.用作吸附剂的是__活性炭__。
8.可用于制作高压线和防锈漆的是__Al__。
9.用作灯丝的是__钨丝__。
10.可以作高能燃料的是__CH
4
__。
11.是胃液的主要成分,能帮助人消化的是__盐酸__。
12.能除去水垢、除铁锈的是__盐酸__、____硫酸__、__醋酸__。
13.能治疗胃酸过多的是__Mg(OH)
2__、__Al(OH)
3
__、__NaHCO
3
__。
14.可作干燥剂的是______CaO__、__浓H
2SO
4
__、__碱石灰__。
15.能改良酸性土壤的是__熟石灰__。
16.家庭常用的调味品是__NaCl__。
17.含氢元素且是焙制糕点发酵粉的主要成分之一的是__NaHCO
3
__。
18.可用于生产玻璃、洗涤剂的是__Na
2CO
3
__。
19.配制波尔多液的两种原料__CuSO
4__、__Ca(OH)
2
__。
20.可作补钙剂的是__CaCO
3
__。
21.常用作复合肥的盐是__KNO
3
__。
22.家用调味品食醋的主要成分是__CH
3
COOH__。
23.用作医疗上的消毒剂的是__C
2H
5
OH__。
类型五:以组成元素相同的物质为突破口
1.组成元素相同且常温下为气态的物质是__CO__和__CO
2
__。
2.组成元素相同且常温下为液态的物质是__H
2O
2
__和__H
2
O__。
3.组成元素相同且常温下为固态的物质是__Fe
2O
3
__和_。
