第二章 烷烃 环烷烃Chapter-2-Alkane & Cycloalkane
第2章烷烃和环烷烃.ppt

第2章烷烃和环烷烃.ppt第2章烷烃和环烷烃2.1烷烃的结构饱和烃:烷烃链烃不饱和烃:烯烃、炔烃烃(碳氢化合物)(hydrocarbon)环烃脂环烃:环烷烃、环烯(炔)烃芳(香)烃烷烃的通式:CnH2n+2同系列:凡具有同一通式,具有相似的构造和性质,而在组成上相差一个或多个C H2原子团的一系列化合物.同系物:同系列中的各个化合物.例如:CH3OH、CH3CH2OH、CH3CH 2CH2OH甲烷的结构:分子中的碳原子以四个sp3杂化轨道分别与四个氢原子的1s轨道重叠,形成四个等同的C–Hσ键,键角为109.5°,呈正四面体的空间结构,体系最稳定.如图2–1所示.其它烷烃的结构与此类似(图2–2).σ键:两个原子轨道沿键轴方向以头碰头方式重叠所构成的共价键.σ键的形状呈圆柱形沿键轴对称分布,σ键可沿键轴自由旋转.伯、仲、叔、季碳原子和伯、仲、叔氢原子1°2°3°4°1°2°3°一级二级三级四级一级二级三级2.2烷烃的命名法2.2.1普通命名法常用于简单烷烃和烷基的命名命名原则:根据烷烃分子中的碳原子总数叫做某烷.甲、乙、丙、丁、戊、己、庚、辛、壬、癸、十一、十二……“正”某烷:直链烷烃,“正”字可省略.“异”某烷:具有(CH3)2CH(CH2)nCH3结构的烷烃.(CH3)3CCH3(CH3)3CCH2CH3新戊烷新己烷烷基的命名:烷基:从烷烃去掉一个H后剩下的基团,用R表示.要记忆碳原子总数4(包括4)以下的烷基.(见书P22~23)2.2.2系统命名法重点掌握.命名原则:(结合书中例子)1.直链烷烃的命名与普通命名法基本相同,但不加“正”字.2.支链烷烃的命名是以主链为母体,所连的支链做取代基.(1)主链的选择:选择最长的含取代基最多的碳链做主链,以此作为母体,按其碳原子数称某烷.(2)主链的编号:遵循最低系列原则,使取代基的位次之和最小.其次是使较不优先(注:按次序规则排列)的取代基的位次最小.(3)取代基的处理:把取代基的位次、个数和名称依次写在母体名称之前.如果主链上连有多个取代基,相同的取代基应合并,不同的取代基按次序规则(见P51)排列,较优先的取代基后列出.2.3烷烃的同分异构2.3.1烷烃的构造异构只有碳链异构.推出碳链异构体的方法:逐步缩短碳架,去掉重复的构造式.例:写出正己烷所有的构造异构体.2.3.2烷烃的构象异构1.乙烷的构象①构象的定义:由于碳碳单键的旋转,导致分子中原子或基团在空间的不同排列方式.②乙烷的两种典型构象:交叉式构象:能量最低,最稳定,是乙烷的优势构象.重叠式构象:能量最高,最不稳定.两种构象的能量相差不大(12.6kJ·mol-1),室温时分子所具有的动能即能克服这一能垒,足以使各构象间迅速转化,成为无数个构象异构体的动态平衡混合物.室温时乙烷分子大都以最稳定的交叉式构象状态存在.③构象的两种表示方法:锯架式:从侧面观察分子.Newman(纽曼)投影式:沿着C-Cσ键轴观察分子.HHHHHHHHHHHHHHHHHHHHHHHH2.丁烷的构象沿着C2-C3σ键旋转时形成四种典型构象:见P26图能量:对位交叉式邻位交叉式>部分重叠式>全重叠式丁烷在室温下主要以对位交叉式和邻位交叉式构象存在.2.4烷烃的物理性质有机物的物理性质通常是指:物态、沸点、熔点、密度、溶解度、折射率、比旋光度和光谱性质等.通过测定物理常数可以鉴定有机物和分析有机物的纯度.1.状态(常温常压下)(了解)正烷烃:C1~C4C5~C16C17以上气体液体固体2.沸点(b.p.)见表2–1沸点主要与下列因素有关:①分子间vanderWaals引力:包括色散力、诱导力和取向力.分子的极性越大,vanderWaals引力越大.②分子间是否形成氢键.氢键的影响明显.烷烃是非极性或极性很弱的分子,分子间仅存在很弱的色散力∴与分子量相同或相近的其它有机物相比,烷烃的沸点最低.直链烷烃随着碳数的增加,分子间色散力增大,因而沸点逐渐升高.同碳数的烷烃中,直链烃的沸点较高,支链越多,沸点越低.3.熔点(m.p.)(了解)烷烃的熔点也随着碳数的增加而升高,但不像沸点变化那样有规律.4.密度比水轻,<1g·cm﹣35.溶解性根据“极性相似者相溶”的规律,所有烷烃均不溶于水,易溶于非极性或弱极性溶剂如乙醚、苯、CCl4.2.5烷烃的化学性质烷烃由于分子中只含有比较牢固的C-Cσ键和C-Hσ键,所以它们的化学性质不活泼,对一般化学试剂表现出高度稳定性,在室温下与强酸、强剂及强还原剂都不发生反应.但在一定条件下,如高温、高压、光照、加入催化剂等,它们也能发生一些化学反应.2.5.1甲烷的卤代反应紫外光或高温CH4+Cl2CH3Cl+HClCl2Cl2Cl2CH2Cl2CHCl3CCl4反应产物为混合物,但控制适当的反应条件,可使反应主要生成一种卤代物.分子中氢原子被卤素取代的反应称为卤代反应.2.5.2烷烃的卤代反应机理–––自由基链反应(freeradicalchainreaction)反应机理(反应历程):化学反应所经历的途径或过程.只有了解反应机理,才能认清反应的本质,掌握反应的规律,从而达到控制和利用反应的目的.1.以甲烷的氯代反应为例,自由基链反应包括三个阶段:(1)链引发:Cl22Cl·吸热(2)链增长:Cl·+CH4CH3·+HClCH3·+Cl2CH3Cl+Cl·放热类似地Cl·+CH3Cl·CH2Cl+HCl·CH2Cl+Cl2CH2Cl2+Cl·同理生成CHCl3和CCl4(3)链终止:Cl·+Cl·Cl2CH3·+CH3·CH3CH3CH3·+Cl·CH3Cl[了解]自由基反应的引发剂:自由基本身或容易产生自由基的试剂,如过氧化物ROOR′.自由基反应的抑制剂:能抑制自由基生成或降低自由基活性的物质,如酚类.活性氧:人体内O2通过一系列单电子转移反应衍生出的化学性质活泼的含氧物质,如·O2–(超氧化物阴离子自由基)、·OH、H2O2和单线态氧1O2–.活性氧在人体内的作用和危害.2.甲烷氯代反应的能量变化(见图2–6)(1)反应热:生成物与反应物之间的能量差(焓差).负值:放热反应正值:吸热反应(2)活化能和过渡态过渡态:在反应中新的化学键开始形成,旧的化学键被拉长但尚未断裂,体系的能量达到最高点时的结构.活化能:过渡态与反应物之间的能量差,用Ea表示.过渡态越稳定,活化能就越低,反应速率就越快.在一个多步骤的反应中,最慢的一步(Ea值最大)是决定反应速率的步骤.2.5.3烷烃的卤代反应取向CH3CH2CH3+Cl2CH3CH2CH2Cl+CH3CH(Cl)CH3次产物主产物烷烃分子中氢原子的卤代反应活性次序:3°H>2°H>1°H2.5.4自由基的稳定性从反应机理来看,丙烷氯代可生成两种自由基:CH3CH2CH3+Cl·CH3CH2CH2·+CH3CHCH3+HCl更稳定烷基自由基的稳定性次序:R3C·>R2CH·>RCH2·>CH3·(从C–H键离解能或超共轭效应来判断)2.6环烷烃的结构与稳定性环烷烃可分为:小环(三、四碳环)、普通环(五~七碳环)中环、大环.自然界存在的环状化合物多为五元环和六元环,其中六元环最稳定.1.不同环烷烃的稳定性次序:环丙烷环己烷2.结构上的原因:环烷烃中成环碳原子均为sp3杂化对小环(环丙烷、环丁烷)而言,为了成环,环上C–C键间的夹角要偏离正常的109.5°,形成弯曲键(见图2–8),轨道重叠的程度较小而不稳定.此外,环丙烷相邻C–H键都是全重叠式构象,非键原子间的斥力较大.从环丁烷开始,成环碳原子不在同一平面上(见图),轨道重叠的程度有所增大,非键原子间的斥力有所降低,使分子内能降低,稳定性提高.环己烷存在最稳定的椅型构象,环上C–C键间的夹角保持109.5°,所有相邻C–H键都处于较稳定的交叉式构象,环内氢原子之间相距较远,几乎无张力.其它环烷烃:环上C–C键间的夹角虽然能够保持109.5°,但环内氢原子之间比较拥挤而存在扭转张力和空间张力,因此不如环己烷稳定.3.影响环烷烃稳定性的三种张力:角张力:由键角偏差引起的张力.扭转张力:由于环上单键旋转的受阻使构象不易达到内能最低的交叉式排列,非键原子或基团发生相互作用而产生的张力.跨环张力(或称空间张力):在跨环的原子或基团之间,相距小于vanderWaals半径而产生斥力.2.7单环烷烃的同分异构2.7.1单环烷烃的构造异构通式:CnH2n,与单烯烃互为官能团异构.还可因环的大小和环上取代基的不同而形成构造异构.2.7.2单环烷烃的顺反异构环烷烃碳环的C–C单键,因受环的限制而不能自由旋转,所以环上两个或两个以上碳原子各连有一个取代基的环烷烃,可产生顺反异构体.例如:(掌握其画法)H3CCH3HCH3顺–1,2–二甲基环戊烷反–1,2–二甲基环戊烷2.8环烷烃的构象2.8.1环戊烷的构象(了解)优势构象是信封型构象(见P38图)2.8.2环己烷的构象环己烷的典型构象是椅型构象和船型构象.常温下二者可以相互转变,椅型构象比船型构象能量低(23.5kJ·mol–1),是最稳定的优势构象,在平衡混合物中占绝大多数(99.9﹪).椅型构象的透视图:(掌握其画法)为什么椅型构象最稳定?①环上C–C键间的夹角均保持109.5°.②所有相邻C–H键都处于较稳定的交叉式构象.③环内氢原子之间相距较远,不产生斥力.翻环作用:两种椅型构象的互相转变.环己烷实际上是以两种椅型构象互相转化达到动态平衡的形式存在的.HCH3H(较稳定,约占95﹪)CH32.8.3取代环己烷的构象取代基处于横键较稳定.取代基若处于竖键,则存在1,3–双竖键效应(见P39图),分子内能增加而不稳定.当环上有多个取代基时,通常有较多取代基和较大的取代基处于横键是较稳定的优势构象.例如,反–1,4–二甲基环己烷有两种构象:CH3HHCH3HH3CCH3H优势构象顺–1,4–二甲基环己烷的优势构象?顺–1–甲基–2–叔丁基环己烷的优势构象?(见书)反–1–甲基–2–叔丁基环己烷的优势构象?(见书)2.8.4十氢化萘的构象(了解)2.9环烷烃的命名法按成环碳原子数称环“某”烷.若环上有支链,命名时一般以碳环为母体,支链视作取代基.环上碳原子的编号应遵循最低系列原则,其次是使较简单的取代基的位次最小.例:1,2–二甲基–3–乙基环戊烷注:当环上有较复杂的支链时,命名时可将环视作取代基,以支链为母体.2.9.1螺环烃的命名法(了解)2.9.2桥环烃的命名法(了解)2.10环烷烃的性质2.10.1环烷烃的物理性质(了解)与烷烃相似.但熔点、沸点和密度都比相应的烷烃高.2.10.2环烷烃的化学性质1.除小环外的其它环烷烃的化学性质与烷烃相似,可发生自由基卤代反应,很难发生开环加成反应.+Br2–Br+HBr2.小环(环丙烷、环丁烷)的开环加成反应(1)加氢+H2CH3CH2CH2CH3(2)加卤素、氢卤酸+Br2BrCH2CH2CH2BrH3CCH3+HBr(CH3)2C–CH(CH3)2H3CBr碳环开环多发生在连H最多的C和连H最少的C之间.HX中的H加到连H较多的C 上,X加到连H较少的C上.(Markovnikov规则)光或热过渡态反应物反应进程生成物能量紫外光·a键(竖键或直立键)e键(横键或平伏键)紫外光或高温Ni△。
2-alkanes(烷烃和环烷烃)

C H
>
C H
H
(−COOH > −CHO > −CH2CH3 > −CH3)
C C C C C C C O C O C O C C C C C C C C
命名:
a. 取代基以阿拉伯数字编号,写在最前面; b. 相同取代基要合并,以二、三、四······(di, tri, tetra ·····) 表示; c. 相同取代基的编号,数字之间以“,”隔开; d. 数字与汉字(英文)之间以“-”隔开; e. 简单取代基写在前 (英文命名以字母顺序排列) f. 最后加上主链名称 (直链烷烃名称,碳数目 + 烷)
1
2
2. 丁烷的构象
4 CH
3
3
4
H3C H CH3 H H3C H
CH2
CH2 CH3 CH3 H3C H H H H
H H
3
H
2 H
C2旋转 60
o
60 H
o
1 CH3
交叉式 (anti) (对位交叉式) 甲基间距离最远 最稳定
H3C CH3 60
o
部分重叠式 较不稳定
CH3 H H H CH3 H
描述立体结构的几种方式
1. 乙烷的构象
H H H
o H 60 H
<60o H
C1旋转
H H H
H H
C1旋转
H H
H H HH
H
交叉式构象 staggered conformation 原子间距离最远 内能较低 (最稳定)
扭曲式构象 (有无数个) skewed conformation
H C H H H
H H3C
HH
6 kJ/mol
第二章 烷烃和环烷烃

支链烷烃: (CH3)2CH
(CH3)3C
称异(iso )某烷 称新(neo )某烷
6
CH3CH2CH2CH2CH3 CH3(CH2)10CH3 CH3CHCH2CH2CH3 CH3 CH3 CH3CCH2CH3 CH3
正戊烷(n-pentane) 正十二烷(n-dodecane) 异己烷(i-hexane)
CH3CH2CH2CH2 CH3CH2CHCH3 (CH3)2CHCH2 (CH3)3C
异戊基(iso-pentyl): (CH3)2CHCH2CH2
9
2.系统命名法命名原则
(1)选主链 :选择最长碳链作为主链称某烷 (2)编号:从靠近支链一端进行编号 (3) 在母体名称前写明取代基的名称、位次及数目 ①相同取代基合并 ②不同取代基按次序规则:优先基团后列出 甲基 <乙基 <丙基 <丁基 < 戊基 <己基 < 异戊基 < 异丁基 <异丙基 <叔丁基
燃烧热:在标准状态下,一摩尔烷烃完全燃烧 所放出的热量。单位:kJ/mol 燃烧热的差别反映了化合物内能的高低和稳定 性的大小。
32
内能越高,燃烧热越大; 内能越低,燃烧热越小。
直链烷烃比支链烷烃的燃烧热大,例如:
H
(kJ/mol)
正丁烷 2878.2
异丁烷 2869.8
33
环烷烃中,因它们的分子组成不同,但可比较 它们环中一个CH2的燃烧热环烷烃分子内能大 小和相对稳定性。
CH3CH2CH2CH3 CH3CHCH3 CH3
正丁烷 n-butane bp -0.5℃ C5H12: C6H14: 三种 五种
异丁烷 i-butane bp -11.7℃
第二章烷烃和环烷烃
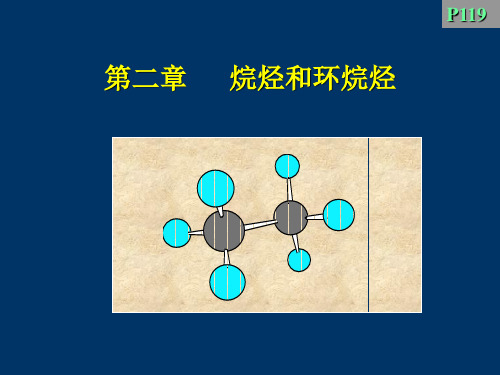
(1)乙烷的构象
H3C CH 3
当C-C键旋转时, 可产生无数个构象
有两种典型conformation:
乙烷的两种典型构象的表示方法
优势构象
交叉式 staggered
H
重叠式 eclipsed
作业:P130 /1, 6, 7 ,8; P105 / 8(3) (4) *C2-C3键旋转 阅读Section 1. Alkanes and Cycloalkanes 全文
翻译 1.1第一段,1.2.2第一段,1.2.3 第四段
CH3 CH3 CH C Br
CH3 CH3
四、环烷烃的异构现象
1. 顺反异构 cis-trans isomer (P84) 环烷烃环中C-C单键受环约束不能自由旋转,导致产生顺反异构
HH
H
CH 3
CH 3 CH 3
顺-1,2-二甲基环丙烷
CH 3 H
反-1,2-二甲基环丙烷
练习:写答出案: 1-甲基-3-乙H基环己烷的顺反异构体CH 3
伯碳(1°):一级碳原子,只与1个其他碳原子直接相连
仲碳(2°):二级碳原子,只与2个其他碳原子直接相连
叔碳(3°):三级碳原子,只与3个其他碳原子直接相连
季碳(4°):四级碳原子,只与4个其他碳原子直接相连
CH3
CH3
H3C
C CH2
3° 2°
H
伯氢(1°H):伯碳上的H
仲氢(2°H):仲碳上的H
练习:预测2-甲基丁烷在室温下进行氯代反应所得的一氯代物
Cl
答 案 : C3 C H H C2C H H 3 +C 2l 光 C3 C H C2 C H H 3
有机化学第章烷烃和环烷烃

脂环烃:碳原子之间相互连成环,其性质类似链烃 的碳氢化合物。
脂环烃
饱和脂环烃,又称环烷烃,通式:CnH2n
不饱和脂环烃
环烯烃 环炔烃
单环脂环烃:分子中只有1个碳环。 环丙烷
环丁烷
分子中含有两个或两个以上碳环结构的脂环烃称为双环或 多环脂环烃。
两个碳环共用一个碳原子的脂环烃,称为螺环烃(spiro hydrocarbon)。“螺”字表示两个碳环只共用一个碳原子,此 碳原子称为螺原子。
Alkyl group names are obtained by removing the –ane from the alkane name , and replacing it with -yl
中文名 英文名 中文名 英文名 甲烷 methane 甲基 methyl 乙烷 ethane 乙基 ethyl 丙烷 propane 丙基 propyl 丁烷 butane 丁基 butyl
2. 编号:从第一桥头(共用碳原子)开始,沿最长桥路到第二桥 头,再沿次长桥路回到第二桥头,然后编最短的桥路。(先编大 桥,再编小桥)。取代基的位置最小。
3.命名: 某基二环[n.m.p]某烷。 n.m.p---指各桥路上碳原子数。
2 1
3
7
4
6
5
8 6
4 5
7 1
2
3
1-甲基二环[4.1.0]庚烷
Homolog
同系物: 同系列中各化合物互称同系物。
同系列差:相邻两个同系物在组成上的不变差数 CH2。
烷烃中的伯、仲、叔、季碳原子。
伯碳原子:只与1个碳原子直接相连的碳原子。 (primary) 也称一级碳原子,以1° 表示。 仲碳原子:只与2 个碳原子直接相连的碳原子。 (secondary) 也称二级碳原子,以2 ° 表示。 叔碳原子:只与3 个碳原子直接相连的碳原子。 (tertiary) 也称三级碳原子,以3 ° 表示。 季碳原子:与4个 碳原子直接相连的碳原子。 (quaternary) 是四级碳原子,以4 ° 表示。
Chap02 Alkane

Chap2烷烃Alkane (Saturated hydrocarbon)内容提要(Outline)•烷烃的同系列及同分异构•烷烃的命名•烷烃的构象•烷烃的性质•烷烃的来源和用途1.2 烷烃的同系列•具有同一通式,结构和化学性质相似,物理性质则随碳原子数的增加而有规律地变化,组成上相差一个或多个CH 2的一系列化合物称为同系列(homologous series)。
•同系列中的化合物互称为同系物(homolog )。
1.3 烷烃的同分异构1.3.1 定义•具有相同的分子式,不同构造式的化合物互称同分异构体,这种现象称同分异构现象。
•构造(constitution)——分子中原子互相连接的方式和次序。
•构造异构现象是有机化学中普遍存在的异构现象的一种,这种异构是由于碳链的构造不同而形成的,故又称为碳链异构。
1.3.2 推算简单烷烃的同分异构体以CH14为例61.4 烷烃的结构1.4.1 碳原子的四面体概念•构型(Constitution):具有一定构造的分子中原子在空间的排列状况。
•Van’t Hoff and Le Bel分别提出碳四面体概念。
•凯库勒模型(又叫球-棍模型)•斯陶特模型(又叫比例模型)−++−+sp 3ssp 3-s++ 6+−+sp 3sp 3−+sp 3−−+2.2 系统命名法(IUPAC )IUPAC :I nternational U nion of P ure andA pplied C hemistry 1.2.1 直链烷烃命名同普通命名法,只是把“正”字取消。
辛烷十一烷CH 3(CH 2)6CH 3CH 3(CH 2)9CH 33 烷烃的构象•构象(Conformation):指分子中原子或原子团由于围绕单键的旋转而产生的分子中原子在空间的不同排列。
•构象异构体:分子组成相同,构造式相同,因构象不同而产生的异构体。
•构象异构体表示方法:透视式(伞形式,锯架式),纽曼投影式。
第二章 烷烃和环烷烃
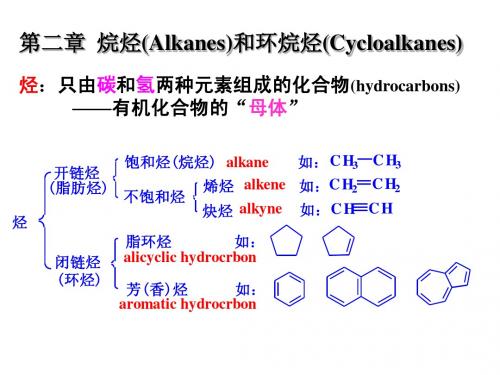
C H3C H2C H2 C H3C H2C H2C H2 C H3C HC H 2 C H3
(正)丁基 Bu 异丁基 i -Bu
C H3C HC H C H3 仲丁基 2 s-Bu C H3 C H3 C C H3 叔丁基 t-Bu
在生理状况下,机体自由基一方面不断产 生,另一方面又不断清除,活性氧处于产生与清 除平衡状态。一旦活性氧的产生和清除失去平衡 ,过多的自由基就会造成对机体的损害,从而引 起多种疾病,并可诱发癌症和导致衰老。 天然抗氧化酶系统:超氧化物歧化酶(SOD) 、 过 氧 化 氢 酶 ( CAT)、 谷 胱 甘 肽 过 氧 化 物 酶 (GSH-Px)
构象异构
(一) 烷烃的构造异构(constitutional isomerism)
戊烷有3种碳链异构体
CH3 CH3CH2CH2CH2CH3 CH3CHCH2CH3
正戊烷 异戊烷
CH3 CH3-C-CH3 CH3
新戊烷
碳原子数 异构体数 4 5 6 7 2 3 5 9
碳原子数 8 9 10 20
异构体数 18 35 75 366 319
天然抗氧剂(自由基清除剂):VE、 Vc、 2巯基乙胺、谷胱甘肽、辅酶Qn(泛醌)、-硫辛酸 等
第二节 环 烷 烃
一、脂环烃的分类和命名
(一) 分类 C3-C4
根 据 环 数 多 少 分
小环 普通环
单脂环烃
C5-C6
C7-C12
中环
C13以上 大环 多脂环烃 桥环 螺环
(二) 命名
1. 单脂环烃: 在相应的烃名前加“环”字;英文名加词头cyclo
第二章 烷烃和环烷烃
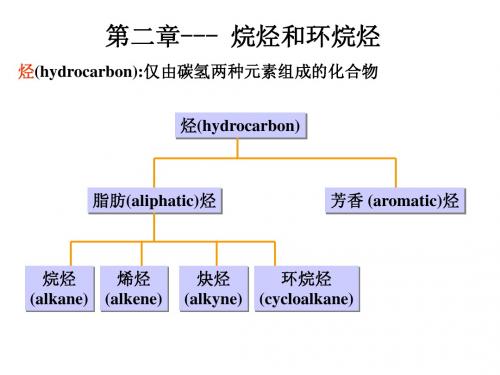
甲基
CH3CHCH3
乙基
正丙基
CH3CHCH2 CH3
正丁基 CH3
CH3C CH3
CH3 CH3C CH2 CH3
CH3CH2CHCH3
异丙基
仲丁) 主链的选择:选择一个最长的连续碳链为主链(stem chain),按 其所含碳原子数称为某烷,并以此作为母体。当分子中有几个等长 碳链可选择时,应选择含取代基较多的碳链为主链。
H H C H H H H C H H C H H H H C H H C H H C H H
烷烃的来源
•石油(petroleum) •煤(coal)
甲烷
乙烷
丙烷
•天然气(natural gas):甲烷(90%~95%)+乙烷(5%~10%)+其它低沸点烷烃
boling point (oC) < 30 30-200 200-300 300-400 >400 carbon atoms C1-C4 C4-C12 C12-C15 C15-C25 >C25 products Natural gas, methane, propane, butane, liquefied petroleum gas Petroleum ether, ligroin, naphtha, straight-run gasoline Kerosene, heater oil Gas oil, diesel fuel, lubricating oil, waxes, asphalt Residual oil, paraffin waxes, tar
CH3CH2CH2CH3
隔绝空气 CH4 + CH3CH3 + CH3CH2CH3 600oC + CH2 CHCH3 + CH2 CH2 等
第二章烷烃 (Alkanes)

CH3 CH CH3 C CH3
:
X2的活性:F2 >Cl2 >Br 2>I2
反应活性高,选择性低,过度态到达早,游离基性质较少。
反应活性低,选择性高,过度态到达迟,游离基性质较多。
5. 游离基的不重排性,同位素示踪。
CH3 CH3 CH3 C D CH3
二 构象 ( Conformation): Sawhorse Model 锯木架式: Newman Projection 投影式: 透视式 Perspective
(二) 构象变化及能量图:
构象( Conformation)
重叠 ( Eclipse)
交叉 (Stagger)
邻位交叉 Gauch 四种构象稳定性次序:
Cl
CH3
Cl2
[
D Cl + CH3 C CH3 CH3 H Cl + CH3 C D CH2
CH3 C Cl CH3 CH3 CH3 C D CH2 Cl
Cl2
CH3 CH3 D Cl H Cl = CH3 C Cl CH3 CH3 C D CH2 Cl
CH3
CH3 CH CH2 CH3
新
(neo-pentyl)
(2). IUPAC Names of Alkanes 直链: Unbranched Alkanes 支链: Branched Alkanes
a. 常见的烷基: Alkyl group
{
CH3 CH CH2 CH3 CH2 CH CH3
iso-butyl sec-butyl
对位交叉 Anti
对位交叉 > 邻位交叉 > 部分重叠 > 全重叠
(三) 影响构象稳定性的因素: 1 扭转张力 ( Torsional Strain): 2 范得华斥力 3 偶极-偶极相互作用: ( Dipole-Dipole Interaction)
Chapter.02.烷烃和环烷烃
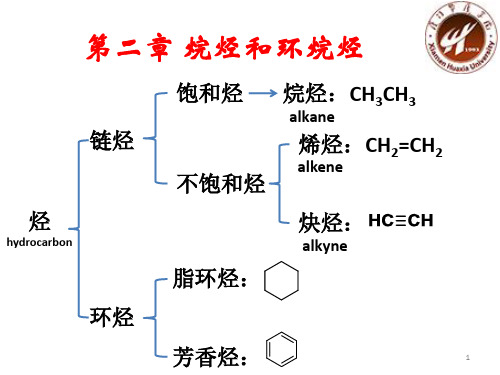
饱和烃 链烃 不饱和烃 烃
hydrocarbon
烷烃:CH3CH3
alkane alkene
烯烃:CH2=CH2 炔烃:
alkyne
脂环烃:
环烃
芳香烃:
1
2.1 烷烃(alkane)
分子中所有碳原子间彼此与碳碳单键相连,其余 价键全部与氢原子结合。 属于饱和烃,通式为:CnH2n+2
2. 基团的优先次序:首先比较键合原子的原子序数,大者优 先次序高,反之优先次序低;键合原子相同时,则顺延比 较与键合原子相连的其他原子,直至比较出次序高低为止。
原子优先次序:-OH > -CH3 原子优先次序:-CH3 <
-CH2CH3
C 6
C,H,H 6, 1, 1
键合原子: 原子序数:
O 8
C 6
常见烷基的优先次序:-C(CH3)3 > -CH(CH3)2 > -CH2CH2CH3 > -CH2CH3 > -CH3
1
2
3
4 5
6
7
8
9
4-乙基-4-叔丁基壬烷
20
系统命名法
次序规则(sequence rules):
3. 含有重键基团的优先次序:如-CH=CH2、 等,双键可视为2个单键与键合原子相联结,叁键则可视为3 个单键与键合原子相联结。
6
O, O, C
6
S, H, H
原子序数:
6,6,1
8,8,8
8,8,6
16,1,1
-SH > -OH > -NH2 > -CH2SH > -COOCH3 > -COCH3 > -CH=CH2
大学有机化学(第二版)第二章

H 3 C CH
3
H H
H H
对位交叉式
部分重叠式
邻位交叉式
全重叠式
上页
返回
(三) 直链烷烃的构象
直链烷烃的优势构象是能量最低的对位交叉 直链烷烃的优势构象是能量最低的对位交叉 在空间排布绝大多数呈锯齿形 式,在空间排布绝大多数呈锯齿形
上页
返回
六、烷烃的物理性质(自学) 烷烃的物理性质(自学) 七、烷烃的化学性质 (一)氧化反应 CnH2n+2+(3n+1)/2O2 nCO2 + (n+1)H2O
7 主链
当一个支链烷烃具有几条相同长度的碳 链可作为主链时, 链可作为主链时,则应选择具有侧链数目最 多的链或侧链具有最低位次的链作为主链。 多的链或侧链具有最低位次的链作为主链。
烷烃的位次编号: (2) 烷烃的位次编号:主链从一端向另一 端编号,位次用阿拉伯数字表示, 端编号,位次用阿拉伯数字表示,在有几种 编号可能时,应当遵循“最低系列”原则。 编号可能时,应当遵循“最低系列”原则。 最低系列:得到两种或两种以上的不同 最低系列: 编号的系列, 编号的系列,则顺次逐项比较各系列的不 同位次,最先遇到的位次最小者, 同位次,最先遇到的位次最小者,定为最 低系列” 低系列”
想一想
试指出各碳原子的类型
CH3 CH2 CH CH3 C CH2 CH3
4 5 3 8 2 7 1 6 9
CH2 CH2
键线式 ° C6、C7 — 1° C8 — 2° ° C9 — 1° °
C1 — 4° ° C2 — 3° ° C3、C4、C5 — 2° °
四、烷烃的命名
(一)普通命名法 根据分子中碳原子数目称为“某烷” 根据分子中碳原子数目称为“某烷”,碳 原子数十个以内的依次用甲 原子数十个以内的依次用甲、乙、丙、丁、 戊……癸表示,十以上的用汉字数字表示碳 癸表示, 原子数 构造异构体用“ 构造异构体用“正、异、新”表示
第二章 烷烃 (Alkane ) 第二章 烷烃 (Alkane ) 第二章 烷烃 (Alkane )

2.6 烷烃的化学性质
2.6.1 氧化反应
•燃烧: CH4 + 2O2 CO2 + 2H2O =-881kJ/mol CH3CH3 + 7O2 4CO2 + 6H2O =-1538kJ/mol •高级脂肪酸:RCH2CH2R’ + O2 RCOOH + R’COOH
条件:催化剂KMnO4,MnO2或脂肪酸锰.120℃,1.5~3MPa
第二章
(一) 烃的定义
烷烃 (Alkane )
• 分子中只含有C、H两种元素的有机化合物叫 碳氢化合物,简称烃.
(二) 烃的分类: (1)开链烃(链烃),又叫脂肪烃. 可分为:烷烃 、烯烃 、二烯烃 、炔烃等 (2)闭链烃(环烃). 又分为:脂环烃和芳香烃两类.
2.1 烷烃的通式,同系列和构造异构
(2)其它烷烃的氯代反应— 伯,仲,叔氢原子的反应活性
丙烷氯代反应:
Cl CH3CH2CH3 25℃,CCl4 CH3CH2CH2Cl + CH3CHCH3 正丙基氯43% 异丙基氯57% 设:伯氢原子活泼性为1,仲氢原子相对活泼性为x:
Cl2 光
57/43=2x/6
x=4
*异丁烷氯代反应:
CH3 CH3 CH3 CH3CH + Cl2 CH3-C-Cl + CH3-CH CH3 CH3 CH2Cl 叔丁基氯36% 异丁基氯64% •设y为叔氢原子的相对活泼性 则: 36/64 = y/9 y=5.06
注意:键线式书写烷烃的分子结构:
•为了方便,只要写出锯齿形骨架,用锯齿形线的 角 (120º )及其端点代表碳原子.不写出每个碳上所连的氢 原子.但其它原子必须写出.
2.4 烷烃的构象 2.4.1 乙烷的构象 (1) 球棒模型(一)
有机化学 第2章烷烃和环烷烃

CH3 H3C CH
3 H(叔氢)
CH3 H3C C CH3 CH3
CH3
3 (叔碳,三级碳)
4 (季碳,四级碳)
tertiary carbon
quaternary carbon
CH 1。 3
3。 CH CH3 1。
2。 CH2 C CH3 4。 1。 CH3 1。
1。 CH3
二、烷烃的构造异构和命名( Constitutional
碳链异构—由于碳链结构的不同而产生的异
构现象称为碳链异构现象,简称碳链异构。异构
体互称为碳链异构体。如:C4H10
H H C H H C H H C H H C H H H H C H H H C C H H C H H H
正丁烷
异丁烷
mp bp
-138℃ -0.5℃
-160℃ -12℃
随着分子中碳原子数目的增加,异构体的数
第二章 烷烃和环烷烃
(Alkanes and Cycloalkanes)
学习要求:
1.掌握烷烃和环烷烃的基础理论和基本知识。
2.掌握构象异构的基本概念。 烃的概念: 烃—指分子中只含C、H两种元素的化合物,又称碳 氢化合物。
烃 碳氢化合物 (hydrocarbons)
烃的分类:
饱和烃——烷烃 链烃 烯烃 不饱和烃 脂肪烃 炔烃 环烷烃 脂环烃 环烯烃 环炔烃 苯型芳香烃 芳香烃 非苯型芳香烃
较稳定。
C C H
(一)稳定性(Stability) 一般情况下烷烃化学 性质不活泼、耐酸碱、不与强氧化剂和还原剂作用。 (常用作低极性溶剂,如正己烷、正戊烷、石油醚 等) (二)卤代反应(Halogenation reation)
和含碳原子数较少的烷烃。
有机化学课件第二章烷烃与环烷烃

第二章 烷烃和环烷烃
第一节 烷烃(二、异构,命名)
CH3
甲基
CH3CH2
乙基
CH3CH2CH2
丙基
CH3CHCH3
异丙基
Methyl (Me)
Ethyl (Et)
Propyl (Pr)
Isopropyl (i-Pr)
CH3
CH3CH2CH2CH2— CH3CHCH2CH3 CH3CHCH2— CH3-C— CH3
Cl Cl
Cl
△ H = +242 kJ·mol
1
第二章 烷烃和环烷烃
第一节 烷烃(五、化学性质)
②链增长(chain-propagating step):延续自由基,形成产物.
Cl· + CH4 —> CH3· + HCl CH3· + Cl2 —>CH3Cl + Cl· △H= +4 kJ· mol-1 △H=-108kJ·mol H= -10kJ· mol-1
CH3 CH3CH2CH2CH2CH3 CH3CHCH2CH3 CH3
mp(℃) -129.8 -159.9
CH3-C-CH3 CH3
-16.8
烷烃的构象 (conformation)
●由于单键的旋转产生的分子在空间的不同排列方 式叫做构象。 构型相对稳定,构象瞬息万变。
例:乙烷的构象(CH3-CH3)
在链增长阶段, 当一氯甲烷达到一定浓度时, 氯原子 除了同甲烷作用外,也可与一氯甲烷作用,结果生成 二氯甲烷。以同样方式,可生成氯仿及四氯化碳。
Cl· + CH3Cl —> CH2Cl· + HCl CH2Cl· + Cl2 —> CH2Cl2 + Cl· Cl· + CH2Cl2 —> CHCl2· + HCl CHCl2· + Cl2 —> CHCl3 + Cl· Cl· + CHCl3 —> CCl3· + HCl CCl3· + Cl2 —> CCl4 + Cl·
Chapter 02 饱和烃(烷烃和环烷烃)

1,7-二甲基螺[4.5]葵烷
CH3
2.3 烷烃和环烷烃的结构
2.3.1 碳的SP3杂化和σ键的形成 基态时 C:1S2 2S2 2Px1 2Py1 2Pz0
英文名
结构
methyl
ethyl
H2 C
propyl
H2 C
Iso-propyl
CH3
butyl
Iso-butyl
H2 C CH3 CH
CH3
CH3
C H2
CH3
CH
CH3
CH2(CH2)2CH3
CH3
中文名 英文名 结构
仲丁基 Sec-butyl
CH3
叔丁基 Tert-butyl
CH3 CH3
CH3
单 环 (上 ) 环 炔 烃 碳环数目 双环 多环
(1) 单环环烷烃 1)按成环碳原子数目称为环某烷。
1-甲基-3-乙基环己烷 2)长链作母体,环作取代基。(以下两种情况) 3-甲基-4-环丁基庚烷
1,3-二环己基丙烷
练习:命名以下化合物
H 3C H 2C
C H 2 (C H 2 ) 4 C H 3
H
H
顺-1, 4-二甲基环己烷
反-1, 4-二甲基环己烷
(2) 双环环烷烃(分子的碳架中含有两个饱和碳环的烃) 按两个环的不同的连接方式分为联环、螺环、稠环和桥环 四种。
a)双环桥环烃命名 桥头碳原子:两环共用的碳原子。
桥:两个桥头碳原子之间的碳链或一个键。
(1 ) 桥 (2) 桥 桥头碳 桥 (3) 桥头碳
第二章 饱和烃(Saturated hydrocarbons) (烷烃alkane和环烷烃cyclic alkane )
第二章-烷烃

CH3 CH2 CH3 CH2 CH CH2 CH CH3 CH2 CH2 CH3
主链:八个碳原子,辛烷
2) 编号:从离取代基最近的一端开始,用阿拉伯数 字1,2,3...将主链碳原子编号. (使取代基的位次最小)
4
5
8
7 6
CH3 CH2
CH3 CH2 CH CH2CH CH3
3 CH2
2 CH2 1 CH3
CH3 CH3 C
CH3
i-Bu t-Bu
• 烷烃分子从形式上去掉两个氢或三个氢原子而剩下 的原子团分别称为亚基、次基。(page 20)
亚基: CH2
CHCH3
C(CH3)2
亚甲基
亚乙基
亚异丙基
CH2 CH2 1, 2-亚乙基
CH2 CH2 CH2 1, 3-亚丙基
次基:
CH
次甲基
CCH3
次乙基
(CH3)3CCH2CH3
键线式
碳干式 C C C C C C
C CCCC
C
3、碳原子和氢原子的类型
• 伯碳原子(一级碳原子, 1o)(primary): 直接与一个碳原子相连 • 仲碳原子(二级碳原子, 2o)(secondary): 直接与两个碳原子相连 • 叔碳原子(三级碳原子, 3o)(tertiary): 直接与三个碳原子相连 • 季碳原子(四级碳原子, 4o)(quaternary): 直接与四个碳原子相连
CH3
碳架异构
构造异构 位置异构
同
官能团异构(包括互变异构)
分
异
(分子式相同,而构造不同)
构
立体异构
构型异构 构象异构
顺反异构 旋光异构
(构造相同,原子在空间排布方式不同)
Chapter2 烷烃环烷烃

比较英文字母顺序时,iso(异),neo(新)参 与比较,而i-(异)、n-(正)、sec-(二 级)、tert-(三级)、cis(顺)、trans(反)、 di(二个)、tri(三个)、tetra(四个)等不参 与比较。
Shandong University at Weihai
P 39
Organic Chemistry
3-甲基-4-乙基庚烷
2,4-二甲基-4-乙基己烷
中英文命名法唯一的不同在于取代基的排序,英文 按字母顺序,中文则以顺序规则决定(先小后大)
Organic Chemistry
Shandong University at Weihai
3-甲基己烷
4,7-二甲基-3-乙基壬烷
2-甲基-3-乙基己烷
Organic Chemistry
Organic Chemistry Shandong University at Weihai
侧链数均为5。侧链的位次均为3,5,7,9,11。侧链的碳原 子数由小到大依次为:1,1,1,2,8和1,1,1,1,9,多的优先 链的长短(长的优先),侧链数目(多的优先),侧链 位次大小(小的优先),各侧链碳原子数(多的优先), 侧分支的多少(少的优先)。
Organic Chemistry Shandong University at Weihai
有两根等长的长链。两根长链均有两个侧链。侧链位次 均为4,5。侧链的碳原子数均为3,7。 蓝色长链4位无侧分支,5位有侧分支。红字长链4,5位 侧链均有侧分支。侧分支少优先。
链的长短(长的优先),侧链数目(多的优先),侧 链位次大小(小的优先),各侧链碳原子数(多的优 先),侧分支的多少(少的优先)。
Organic Chemistry Shandong University at Weihai
chapter-2 烷烃(完整)

31
思考题:丙烷有几种典型的构象并画出其典 型构象的纽曼投影式。
CH3 H H H H H
H3CH
H H
H H
交叉式
重叠式
32
画出化合物
的所有典型的构象。
最稳定
最不稳定
33
2.4 烷烃的性质
一、烷烃的物理性质
1. 存在状态
室温下,1~4个C的烷烃为气体,5~16个C的烷烃 为液体,大于16个C的烷烃为固体。 2. 熔点和沸点:随分子量的增大而升高 原因: (1)分子大,接触面积大,范德华力大;
—CH2CH3
CH2 CH2 CH2 SH
乙基
H3C CH2 CH CH3 SH
正丙基
CH3 H3C CH CH2 SH H3C
仲丙基
H3C C CH3 SH H3C
正丁基
仲丁基
CH3
CH2 CH2 CH2 CH2 SH
H3C
CH CH2 CH2 SH
异丁基
叔丁基
正戊基
异戊基
6
碳原子的四种类型:
1 H(伯氢)
原子。
F
7 6 5
CH2 CH 2
4 3 2
Cl CH2 CH3
1
15
H3C CH2 CH 2 CH CH
练习:用系统命名法命名下列烷烃
(1) 2,2-二甲基戊烷 (3)
(2)
3-甲基-4-乙基己烷 2,5,6-三甲基辛烷
(4) 2,7,9-三甲基-6-异丁基十一烷
16
2.3 烷烃的结构
一、甲烷的构型(configuration)
由于sp3杂化碳的轨道夹 角是109.5°,所以烷烃 中的碳链是锯齿形的而 不是直线。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
按环的大小
C3~C4 Common rings C5~C7
C8~C12 Large rings 按不饱和度 环烷
C13~
By the saturation CnH2n
Cycloalkanes
CnH2n-2 Cyclo olefines 环烯 CnH2n-4 Cyclo alkynes 环炔
By the number of the rings Monocyclic compounds 单环
将桥(稠)环烃变为链状化合物时需要 断裂的碳链数。如需断裂两次,则为二 环化合物,断裂三次则为三环化合物。
Some interesting bridging compounds
Cubane 立方烷 篮烷
Primane 棱烷
Diamentane 金刚烷
Sources and usages:
来源:天然气、石油(汽油 C5-11,煤油C11-15,柴油C15-18, 润滑油C16-20) 煤、液化气 煤或CO 高温高压催化剂下加氢 用途: 甲烷:燃料 生产氨和甲醇的原料
6 1 5 2 4 3 3 4 2 5 1 6
CH3 CH CH3
CH2 CH CH CH3 CH CH3 CH3 H3C
3)命名:
a. 依主链碳原子数称为某烷。
顺序规则
b. 取代基按“优先基团后列出”放在“某
烷”前面,相同基团用中文数字“二、三、 四···‖合并。
注意:阿拉伯数字与汉字或中文数字之间用
乙烷:生产乙烯及氯乙烯的原料
丙烷:燃料(液化石油气) 生产乙烯
丁烷:燃料(液化石油气) (轻汽油)
溶剂,制冷剂
1. Homologous series and Isomerism 第一节 同系列和同分异构现象
1.1 Homologous series & Homologue 同系列和同系物 1.2 Isomerism 同分异构现象 1.3 Classification of Saturated carbon atoms & hydrogen atoms 饱和碳原子和氢原子的分类
H
CH2
CH2 丙烷
CH2
H
同系物:同系列中的化合物称为同系物。相邻 同系物在组成上的差叫同系差。 烷烃的通式为CnH2n+2 ,同系差为CH2。
同系物具有相似的化学性质,但反应速率往往有
较大的差异; 物理性质一般随碳原子数的增加而呈现规律性变 化。 同系列中的第一个化合物往往具有明显的特性。
1.2 Isomerism 同分异构现象
具有相同分子式,仅由于组成分子的原子或基
团连接顺序和方式不同而引起的同分异构现象—— 构造异构
具有相同分子式,仅由于碳链结构不同而产
生的同分异构现象—— 碳链异构 碳链异构属于构造异构的一种。
碳链异构 构造异构 同分异构 立体异构 位置异构 官能团异构 互变异构
顺反异构
对映异构 构象异构
由于碳链结构的不同而产生的异构现象
正丁基
H3C CH CH2 CH3
仲丁基
叔丁基
H3C CH CH2 CH2 CH3
异丁基
异戊基
IUPAC nomenclature allowed group naming
Name Abv. Chinese naming
H 3C CH H 3C
CH 2 H 3C CH CH 3
Isopropyl
与一个碳原子相连的碳原子 — 1o碳(伯碳、一级碳)
与两个碳原子相连的碳原子 — 2o碳(仲碳、二级碳) 与三个碳原子相连的碳原子 — 3o碳(叔碳、三级碳) 与四个碳原子相连的碳原子 — 4o碳(季碳、四级碳)
H
H
C
H
Primary carbon 伯碳 Secondary carbon 仲碳 Tertiary carbon 叔碳
H
C
H
C
CH3 CH3 CH2 CH CH3
伯 仲
C CH3
叔
CH3
季
2. Nomenclature
第二节
命名
2.1 Common Nomenclature 普通命名法 2.2 Systematic Nomenclature 系统命名法
Nomenclature of Alkanes
烷烃的命名
子数称为新某烷。
CH3 CH3 C CH2 CH3
新己烷
CH3
基: 一个化合物从形式上去掉一个单价的原 子或原子团的剩余部分称之为“基” 基
Name Abv. Chinese naming 甲基 乙基
CH 3
CH 3CH 2
CH3CH2CH2
Methyl Ethyl
n-Propyl
Me Et
n-Pro
Alkanes& Cycloalkanes
第二章 烷烃和环烷烃
Content
1 Homologous series and Isomerism 第一节 同系列和同分异构现象 2 Nomenclature 第二节 命名 3 Structure 第三节 结构 4 Conformation 第四节 构象 5 Chemical properties 第五节 化学性质
H
C
H
C
H
C Quaternary carbon 季碳
与伯碳原子相连的氢原子 — 1o氢(伯氢、一级氢) 与仲碳原子相连的氢原子 — 2o氢(仲氢、二级氢) 与叔碳原子相连的氢原子 — 3o氢(叔氢、三级氢)
H
H
C
Primary hydrogen
H H
C
Secondary hydrogen
Tertiary hydrogen
如果两个多原子基团的第一个原子相同,则比较与 它相连的其他原子,比较时,按原子序数排列,先比较 最大的一个,仍相同,再顺序比较居中的、最小的。
半子线‘ - ’隔开,阿拉伯数字之间用逗号‘ , ’隔开。
顺(次)序规则:为了决定有关原子或基团排 列顺序而人为定下的规则。顺序小的写在前面 ,大基团称为优先基团,优先基团写在后面。
C C C C C C C C C C C
如何编号?
从小的基团一 端开始编号 基团谁大谁小?
基团大小的判定 (1)单原子取代基:按原子序数大小排列,原 子序数大的顺序大,原子序数小的顺序小。
烷烃常用的命名法有两种,即普通命名法和系 统命名法。
2.1 Common Nomenclature普通命名法 普通命名法又称习惯命名法,此法仅适用于直 链和含碳原子数较少的烷烃。
按分子中碳原子总数叫“某烷”。用
“正n-”“异iso-”“新neo-”等字区别同分异构体。
(i) 用天干名称甲、乙、丙……癸表示一到十的
几个名词和术语(Terminology )
碳氢化合物:只含碳和氢两种元素的化合物。
烷烃:碳氢化合物,通常指饱和的碳氢化合物。简称“烃”
饱和烃:分子中碳原子以单键相互连接成链,其余的价完全 与氢原子连接相同分子通式,组成上相差CH2或其整数倍的 一系列化合物。 同系物:同系列中各个化合物互称同系物。 同系物具有相似的化学性质,其物理性质一般随分 子量的改变而规律性变化。
eg
I > Br > Cl > S > P > F > O > N >C >D > H
B Al C Si N P O S F Cl
Ga
In
Ge
Sn
As
Sb
Se
Te
Br
I
(2)多原子取代基:先比较第一个原子
O O eg C OH
<
S O
CH3
eg
CH3 小 NH 2 大 CH CH
C (C,H,H) 大
(b.p. 36℃ ,m.p. -130℃ )
(b.p. 10℃,m.p. -17℃)
CH3
(b.p. 23℃,m.p. -160℃)
正戊烷 C6H14(5种)
异戊烷
新戊烷
随着分子中碳原子数目的增加,异构体的数目
迅速增加。如:
Constitutional isomers are derivated from the change of size of rings and length of side chains. 单环烷烃除和单烯烃互为构造异构体外,还因环 的大小和环上取代基的不同而形成多种同分异构 体。
系差: CH2为同系列的系差
构造式:代表分子中原子的种类、数目和排列次序的 式子。 结构式:除了代表分子中原子的种类、数目和排列次 序的之外,还包括了空间及原子、电子、构
型、构象等信息的式子。
同分异构:分子式相同而结构不同的现象。 同分异构体:两个或两个以上分子式相同而结构不同 的物质互称同分异构体。
碳,十 以上则用中文小写数字,依总碳原子
数称为正某烷
CH3(CH2)5CH3 正庚烷
CH3(CH2)9CH3 正十一烷
CH3 (ii) 只有 CH CH 3
端链(异丙基)的依总
碳原子数称为异某烷。
CH3
CH3 CH CH2 CH3 异戊烷
CH3 (iii) 只有 CH3 C CH3
端链(叔丁基)的依总碳原
烃
碳氢化合物 (hydrocarbons)
Classification: 烃的分类:
烃
饱和烃——烷烃 链烃 烯烃 不饱和烃 脂肪烃 炔烃 环烷烃 脂环烃 环烯烃 环炔烃 苯型芳香烃 芳香烃 非苯型芳香烃
环烷烃分类:
By the size of the ring
Small rings Medium rings
正丙基
Alkyl Groups烷基(烃基):
